碳原子数至少为多少的烷烃具有同分异构体
烷烃(同系物和同分异构体)
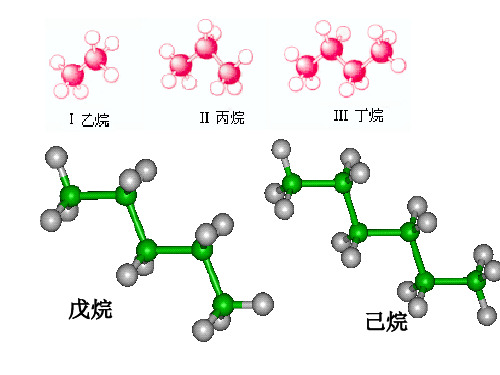
烷烃复 习一: 什么叫烷烃? 链状、单键、饱和
烷烃的通式是?其完全燃烧生成的水和二氧化碳 之比为多少? C2H2n+2 (n≥1) 已知10ml的某气态烷烃在50mlO2中充分燃烧,得到 液态水和体积为35ml的混合气体(所有气体都在同温同 压下测定),则该烃可能是什么?
烷烃的表示方法
有机物的几种表示方法
烷烃的化学性质
(1)烷烃的氧化反应 烷烃完全燃烧的通式: CnH2n+2+(3n+1)/2O2 → nCO2+(n+1)H2O
通常情况下,烷烃与高锰酸钾等强氧化剂不发 生反应,不能与强酸和强碱溶液反应。
(2)烷烃的取代反应
其它烷烃与甲烷一样,一定条件下能发生取
代反应。因为可以被取代的氢原子多,所以
H
C
H
C H
H
对称氢原子的概念
我们先看看最简单的甲烷分子… 我们知道甲烷的四个氢原 子是对称的。 如果将甲烷的四个氢原子 用甲基取代,结果会…?
由此可以得到两个规律…
对称氢原子确定的规律
同一碳原子上的氢原子完全对称 。 与同一碳原子相连的甲基上的氢原
子完全对称。
与同一碳原子相连的相同基团对应位置上的
烷烃组成和结构的表示方法
结构简式怎么写?------p23(有机化学)
1.将结构式中的C—H省略,其他的共价键一律不省略.C—C 可省也可不省.但其它如双键,叁键一律不能省. 实际上写结构简式的最简单处理方法就是省略C—H,
其它一概不变!
2.连在同一个C上的相同基团有时也可以合并,并带上括号. 3.同一条链上连续的相同的基团也可以合并,并带上括号
4、主链少三个碳原子
C C ∣ ∣ C -C - C - C ∣ ∣ C C
烷烃的命名

烷烃的命名第一篇:烷烃的命名烷烃的命名1.习惯命名法(普通命名法)碳原子总数小于或等于10时,用天干——甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示;碳原子总数大于10时,用中文数字——十一、十二等表示;同时为了区分同分异构体,在名称前加一些词头表示,如“正”、“异”、“新”。
2.系统命名法(1)命名方法:①选主链,称某烷;②编号位,定支链;③取代基,写在前,标位置,短线连;④不同基,简到繁,相同基,合并算。
(2)五个原则:①最长原则:应选最长的碳链做主链;②最近原则:应从离支链最近一端对主链碳原子编号;③最多原则:若存在多条等长主链时,应选择含支链较多的碳链做主链;④最小原则:若相同的支链距主链两端等长时,应以支链位号之和为最小原则,对主链碳原子编号;⑤最简原则:若不同的支链距主链两端等长时,应以靠近简单支链的一端对主链碳原子编号。
(3)五个必须:①取代基的位号必须用阿拉伯数字“2,3,4…”表示;②相同取代基的个数,必须用中文数字“二,三,四…”表示;③位号2,3,4等相邻时,必须用逗号“,”表示(不能用顿号“、”);④名称中凡阿拉伯数字与汉字相邻时,必须用短线“-”隔开;⑤若有多种取代基,不管其位号大小如何,都必须把简单的写在前面,复杂的写在后面。
第二篇:《烷烃的命名》说课教案各位老师:大家好!我说课的内容是人教版选修5《有机化学基础》第一章第三节《有机化合物的命名》第一课时,下面我将从教材分析、学生分析、教学设计、教学过程等几个方面对本课进行说明。
不当之处,恳请各位老师批评指正!一、教学内容分析1、教材中的内容本堂课的内容为人教版选修5《有机化学基础》第一章第三节《有机化合物的命名》第一课时,本课时具体教学内容主要包括有机化合物的习惯命名法与系统命名法,重点介绍烷烃的系统命名法。
2、分析该内容的重要性该部分内容是简单有机化合物的命名,是进行其它有机化合物命名的基础,很多有机知识点都必须以此为基础。
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)1种)一、CH4同分异构体(共1、甲烷二、C同分异构体(共1种)2H61、乙烷同分异构体(共1种)三、C3H81、丙烷四、C同分异构体(共2种)4H101、丁烷2、2—甲基丙烷五、C同分异构体(共3种)5H121、戊烷2、2—甲基丁烷3、2 , 2—二甲基丙烷六、C同分异构体(共5种)6H141、己烷2、2—甲基戊烷3、3—甲基戊烷4、2 , 2—二甲基丁烷5、2 , 3—二甲基丁烷同分异构体(共9种)七、C7H161、庚烷2、2—甲基己烷3、3—甲基己烷4、3—乙基戊烷5、2 , 2—二甲基戊烷6、2 , 3—二甲基戊烷7、2 , 4—二甲基戊烷8、3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷同分异构体(共18种)八、C8H181、辛烷2、2—甲基庚烷3、3—甲基庚烷4、4—甲基庚烷5、3—乙基己烷6、2 , 2—二甲基己烷7、2 , 3—二甲基己烷8、2 , 4—二甲基己烷9、2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C同分异构体(共35种)9H201、壬烷2、2—甲基辛烷3、3—甲基辛烷4、4—甲基辛烷5、3—乙基庚烷6、4—乙基庚烷7、2 , 2—二甲基庚烷8、2 , 3—二甲基庚烷9、2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷同分异构体(共75种)十、C10H221、癸烷2、2—甲基壬烷3、3—甲基壬烷4、4—甲基壬烷5、5—甲基壬烷6、3—乙基辛烷7、4—乙基辛烷8、2 , 2—二甲基辛烷9、2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烷烃同分异构体数目口诀

烷烃同分异构体数目口诀烷烃是指沿着碳碳键链为C基组成的烃类分子,烷烃同分异构体指在具有相同碳链结构,相同碳链重量的情况下,由于键的分布方式不同,而表现出不同的化学性质,物理性质的同分异构体的总和就是烷烃同分异构体数目。
那么我们如何来计算烷烃同分异构体数目呢?“ 十 - 八” 口诀可以提供我们一个有用的参考,此口诀概括计算方法为:1. 如果烷烃的碳链上有 n 个碳原子,就有 n! 共n× ( n−1 ) × ( n−2 )×...×3×2×1 种构型2. 单路重复:程序从最后一个碳原子开始,将它沿着 clockwise方向折叠,折叠一次等于1个异构体,直到碳链回到原来的顺序,就产生一个环型构型3. 双螺旋重复:若有位靠近碳链起点 -ω和终点α上靠近的碳被折叠,继续从终点α开始,逆时针折叠碳链若干格,直到α与ω重合(落在同一位置),这种折叠产生的异构体等于碳链长度减一。
因此,计算烷烃同分异构体数目的口诀“ 十 - 八” 就用上述的方法便可以计算出。
例如,要计算 C6H12 的烷烃同分异构体数目,n=6,因此有6!= 6×5×4×3×2×1 =720 个烷烃同分异构体。
此外,同分异构体数量也可以使用“Hypothetical Geometric Isomers Formulae” 公式来计算,它将单路重复和双螺旋重复因子分开,当一个有多个构型时,分裂开组成的n组元素之和,即为同分异构体的总数 .当考虑环烷烃的时候,可以假设环状烷烃有两个 end--groups 和一个中心碳,以及其他碳中的基,因此可以转换为 n--alkane 的形式计算,例如 C6H12 -- Cyclohexane,则所得烷烃同分异构体数目为 n--alkane 中的 6!,即 720 个。
综上所述,烷烃同分异构体数目可以使用“ 十 - 八” 口诀或 HypotheticalGeometric Isomers Formulae 公式来计算,本文介绍了烷烃同分异构体数目的定义和计算方法,希望对你有所帮助。
同分异构体

同分异构1概念:化合物具有相同的分子式,但结构不同的现象称为同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
在中学阶段,引起同分异构的原因主要有三种:碳架异构、位置异构和官能团异构。
识别两者是否是同分异构体,首先要查碳原子数,判别分子式是否相同,然后再看结构式。
在分子式相同的情况下,若结构不同,则两者必为同分异构体。
2 烃的异构2.1 烷烃的异构(碳架的异构)熟记C 1-C 6的碳链异构: CH 4、C 2H 6、C 3H 8 无异构体;C 4H 10 2种、C 5H 12 3种、C 6H 14 5种。
2.2 烯炔的异构(碳架的异构和双键或叁键官能团的位置异构)如丁烯C 4H 8有两碳链形成叁种异构体:2.3 苯同系物的异构(侧链碳架异构及侧链位置的异构) 如C 9H 12有7种异构体:3 烃的一元取代物的异构(取代等效氢法)卤代烃、醇、醛、羧酸、胺都可看着烃的一元取代物。
确定它们异构体可用取代等效氢法。
等效氢概念有机物分子中位置等同的氢叫等效氢,分子中等效氢原子有如下情况:①分子中同一个碳原子上连接的氢原子等效。
②同一个碳原子上所连接的甲基上的氢原子等效。
如新戊烷(可以看作四个甲基取代了甲烷分子中的四个氢原子而得),其四个甲基等效,各甲基上的氢原子完全等效,也就是说新戊烷分子中的12个H 原子是等效的。
③分子中处于镜面对称位置(相当于平面镜成像时,物与像的关系)上的氢原子是等效的。
如 分子中的18个H 原子是等效的。
取代等效氢法要领 利用等效氢原子关系,可以很容易判断出有机物的一元取代物异构体数目。
其方法是先写出烃(碳架)的异构体,观察分子中互不等效的氢原子有多少种,则一元取代物的结构就有多少种。
C 3H 7X 一种碳链,共有 2 种异构体 C 4H 9X 二种碳链,共有 4 种异构体C5H11X叁种碳链,共有 8 种异构体这里的一元取代基X,可以是原子,如卤原子,也可以是原子团,如-OH、-NH2、-CHO、-COOH、HCOO-等。
烃基同分异构体数

烃基同分异构体数摘要:一、烷烃同分异构体数1.碳原子数小于等于10的烷烃同分异构体数2.碳原子数大于10的烷烃同分异构体数二、烯烃同分异构体数1.碳原子数小于等于10的烯烃同分异构体数2.碳原子数大于10的烯烃同分异构体数三、炔烃同分异构体数1.碳原子数小于等于10的炔烃同分异构体数2.碳原子数大于10的炔烃同分异构体数四、烃基同分异构体的应用1.化学反应中的同分异构体2.生物分子中的同分异构体正文:烃基同分异构体数是指分子式相同但结构不同的有机化合物的数量。
在有机化学中,同分异构体是一种常见的现象,它影响着化合物的性质、反应活性和生物活性等。
一、烷烃同分异构体数烷烃是一类仅含有碳-碳单键的饱和烃。
根据碳原子数的不同,烷烃的同分异构体数也有所差异。
当碳原子数小于等于10时,烷烃的同分异构体数为1,即所有分子式相同的烷烃都只有一种结构。
当碳原子数大于10时,烷烃的同分异构体数开始增加,例如,C11H24的烷烃同分异构体数已经超过了100。
二、烯烃同分异构体数烯烃是一类含有碳-碳双键的不饱和烃。
与烷烃类似,烯烃的同分异构体数也随着碳原子数的增加而增加。
当碳原子数小于等于10时,烯烃的同分异构体数为1,即所有分子式相同的烯烃都只有一种结构。
当碳原子数大于10时,烯烃的同分异构体数开始增加,例如,C11H20的烯烃同分异构体数已经超过了100。
三、炔烃同分异构体数炔烃是一类含有碳-碳三键的不饱和烃。
与烷烃和烯烃类似,炔烃的同分异构体数也随着碳原子数的增加而增加。
当碳原子数小于等于10时,炔烃的同分异构体数为1,即所有分子式相同的炔烃都只有一种结构。
当碳原子数大于10时,炔烃的同分异构体数开始增加,例如,C11H16的炔烃同分异构体数已经超过了100。
四、烃基同分异构体的应用烃基同分异构体在化学反应中扮演着重要角色。
例如,在烷基化反应中,不同的烷基同分异构体会产生不同的反应活性和立体化学特征。
此外,在生物分子中,同分异构体也起着关键作用。
烷烃所有同分异构体的计算机求解
烷烃所有同分异构体的计算机求解摘要:本文提出了烷烃同分异构体在计算机中的两种表示方法,并用来求解输出指定碳原子个数烷烃的所有同分异构体的分子构造问题。
正文:在种类繁多的有机化合物中,烃是最简单的一种。
它的特点是只含有碳和氢两种元素。
而烷烃又是烃中构造最简单的。
它的分子中碳原子都是饱和4价的,碳原子之间只以单键相互连接,其余的价则完全与氢原子相连。
在计算机表示中只需表示出其碳链即可。
在多碳原子的烷烃中由于分子中碳链构造的不同,同一种烷烃会存在多种同分异构体。
例如丁烷有两种分子构造:C|C-C-C-CC-C-C当碳原子数较少时,其同分异构体数量也较少,凭直观还易于写出其所有的同分异构体;但当碳原子数增加时,其同分异构体数将迅速增加(见表一)从表中可看出表明并没有求烷烃同分异构体数的通式,表一的结果是30年代有人用数学上的图论的方法推算出来的。
但这种方法并不能给出某种烷烃具体的同分异构体结构式。
如果手工求算要寻找大量的碳原子组合方式,最困难的一点是判断求出的同分异构体与已有的是否重复。
用计算机来求解关键也一样,下面分别从算法、数据结构和编程实现三方面来讨论。
一、算法用计算机解决这个问题实际上模拟了人在解决这个问题时的方法。
先写出一个最简单碳链——只有两个碳原子的碳链:1 43 C—C62 5然后可在这个基础上进一步扩展。
具体方法为向这个碳原子加入新的碳原子。
现在可供扩展碳原子的位置有六个,可逐一试放。
放在一个位置后,与已得到的构造进行比较,如果重复则只算一种;如果构造不同,则把这种新的构造储存下来。
在本例中显然六个位置放置后都只算同一种。
对于四个碳原子的情况,是根据三个碳原子的结果再推算的。
在三个碳原子的结构基础上对新形成的八个空位来试放第四个碳原子,判断重复性,可得两个同分异构体。
五个碳原子的情况又是由四个碳原子的两个同分异构体再扩展而来。
按这样的算法,实际上计算N个碳原子的烷烃时都要从三个碳原子的情况一步步推过来。
2006年高考第一轮复习化学:烷烃同分异构体

第十二章烃一、烷烃同分异构体知识梳理●网络构建●自学感悟1.甲烷的分子结构和性质(1)1.甲烷的分子式是CH4,电子式是,结构式是,结构简式是CH4,甲烷的空间构型为正四面体结构,其中碳原子位于正四面体的中心,四个氢原子分别位于正四面体的四个顶点。
碳原子的四个价键之间的夹角都相等,四个碳氢键的键长也都相等。
甲烷分子是由极性键构成的非极性分子(填“极性”或“非极性”)。
(2)把1体积CH4和4体积Cl2组成混合气体充入大试管中,将此试管倒立在盛Na2SiO3溶液的水槽中,放在光亮处。
片刻后发现试管中气体颜色变浅,试管中的液面上升,试管壁上有黄色液滴出现,水槽中还观察到白色胶体状沉淀。
2.烷烃同分异构体(1)下列各物质中,互为同系物的是④,互为同素异形体的是①,互为同位素的是②,属于同一种物质的是③⑤,互为同分异构体的是⑥。
①金刚石和石墨 ②35Cl 和37Cl③④(CH 3)2CH 2与C (CH 3)4⑤液氯和氯气⑥2-甲基戊烷和2,3-二甲基丁烷(2)分子式为C 6H 14烷烃的同分异构体有5种。
分子式为C 8H 18烷烃的一种同分异构体只能生成1种一氯代物,该烷烃的结构简式是,名称是2,2,3,3-四甲基丁烷。
思考讨论1.为什么甲烷是正四面体而非正方形平面结构?中学化学中常见的正四面体结构的物质(或粒子)有哪些?提示: 如果CH 4是正四面体结构,其一、二、三、四氯代物均只有一种,如若为正方形平面结构,其一、三、四氯代物均只有一种,却应有两种二氯代物:。
事实上二氯甲烷没有同分异构体,这便可以证明CH 4是正四面体结构而非正方形平面结构。
具有正四面体结构的物质有金刚石、晶体硅、碳化硅、二氧化硅、白磷、CH 4、CCl 4、SiF 4、NH +4、SO -24等,其中只有白磷(P 4)为空心正四面体。
2.置换反应与取代反应有何区别?提示:置换反应是一种单质置换出另一种单质的无机氧化还原反应,其模式为A+BC −→−AC+B (或BA+C );取代反应是有机物分子中的某些原子或原子团被其他原子或原子团所代替的有机反应,其模式一般为AD −→−A —D+B —C (或C —B ),二者从属不同,概念相异。
苏教版高中化学必修2校本课程学习指导纲要(教师版)

苏教版高中化学必修2校本课程学习指导纲要专题1 微观结构与物质的多样性课程标准内容1、知道元素、核素的涵义。
2、了解原子核外电子的排布。
3、能结合有关数据和实验事实认识元素周期律,了解原子结构与元素性质的关系。
4、能描述元素周期表的结构,知道金属、非金属在周期表中的位置及其性质的递变规律。
5、认识化学键的涵义,知道离子键和共价键的形成。
6、了解有机化合物中碳的成键特征。
7、举例说明有机化合物的同分异构现象。
第一单元核外电子排布与周期律一、教学目标二、教学内容第二单元 微粒之间的相互作用力 一、教学目标二、教学内容第三单元从微观结构看物质的多样性一、教学目标二、教学内容三、本专题教学方法建议1、本专题学习内容层次性强,学习原子结构认识元素性质与原子结构的关系,找到元素周期律,在学习元素周期律后,让学生分析元素周期表,认识位置,结构,性质之间的关系,最后学习元素周期表的意义。
2、本专题注意控制学习的深广度,对物质结构的学习是为《物质结构与性质》选修模块打基础,通过分析一些典型事例,帮助学生掌握一些粗浅的常识和规律性知识。
3、本专题重视化学用语的学习,在本专题要使用原子结构示意图、电子式、结构式。
4、本专题充分发挥模型的作用,在教学中要灵活运用各种模型如比例模型、球棍模型、晶体结构模型,注意发展学生的空间想象能力。
5、本专题学习运用实验、查阅资料等多种手段能力获取信息,运用比较、分类、归纳、概括等方法对信息进行加工,培养问题意识和探究意识,提高逻辑思维能力。
四、本专题教学评价1.重视学生过程性学习评价,包括课堂学习的自主性、与人合作交流态度、作业完成情况。
作业要掌握数量和质量,要精选习题,主要以教材中习题和作业本习题为主。
2.在学生探究实验中要注重活动表现评价,对学生的参与意识、合作精神、实验操作技能、探究能力、表达交流能力进行评价。
3.专题检测试题难度要合理,基础题达到70%以上,年级平均分达到75分,鼓励学生学习化学的积极性。
烷烃试题

参考答案1.解析:A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为C2H6,一定是乙烷。
答案:B2.解析:烷烃的组成通式为C n H2n+2,故C项不符合。
答案:C3.解析:A项,二者互为同位素;B项,二者互为同系物;C项,二者不是同系物;D项,二者互为同分异构体。
答案:B4.解析:由于同系物在组成上相差一个或若干个“CH2”原子团,因此在相对分子质量上相差14的整数倍,只有A符合。
答案:A5.解析:A项,因二者均为烷烃,都符合通式C n H2n+2;B项,它们与其他烷烃互为同系物;C项,化学性质相似,但物理性质不同;D项,碳原子数小于或等于4的烷烃常温下是气态。
答案:A6.解析:同分异构体的分子式相同,结构不同,所以组成元素、相对分子质量都相同,但物理、化学性质则可能不同。
答案:B7.解析:选项A的一氯代物有两种同分异构体;B项的一氯代物也有两种同分异构体;C项的一氯代物只有一种,D项的一氯代物有四种同分异构体。
答案:C8.解析:不同碳原子数的烷烃,其沸点随碳原子数的增多而逐渐升高,故丙烷的沸点高于-89 ℃,低于-0.5 ℃,C正确。
答案:C9.解析:乙烷的分子式为C2H6,1 mol Cl2只能取代烷烃中的1 mol H 原子,故1 mol乙烷最多与6 mol Cl2发生取代反应。
答案:D10.解析:A项错误,三个碳原子不可能处于同一直线上;B项错误,F原子最外层有7个电子;C项正确,该反应为取代反应;D项错误,与H2加成产物为CF2H—CFH—CF3。
答案:C二、非选择题11.解析:(1)M=2 g/mol×43=86 g/mol,所以14n+2=86,n=6,即该烷烃的分子式为C6H14。
(2)由C n H2n+2,n=5,得2n+2=12,该烷烃的分子式为C5H12。
八个碳的烷烃二元取代物同分异构体

八个碳的烷烃二元取代物同分异构体八个碳的烷烃(八碳烷烃)具有分子式C8H18,是一类有机化合物。
由于碳原子的位置和键的不同排列方式,八碳烷烃可以存在多个同分异构体。
下面将介绍八碳烷烃的二元取代物同分异构体。
1. 2,2-二甲基戊烷(2,2-Dimethylpentane):这是八碳烷烃的一种同分异构体,其中两个甲基基团分别连接在碳原子的2号位置上。
由于甲基基团的取代位置不同,2,2-二甲基戊烷与其他同分异构体有明显的区别。
2. 2,3-二甲基戊烷(2,3-Dimethylpentane):这是八碳烷烃的另一种同分异构体,其中两个甲基基团分别连接在碳原子的2号和3号位置上。
与2,2-二甲基戊烷相比,2,3-二甲基戊烷在分子结构上有所不同。
3. 2,4-二甲基戊烷(2,4-Dimethylpentane):这是八碳烷烃的又一种同分异构体,其中两个甲基基团分别连接在碳原子的2号和4号位置上。
与前两种同分异构体相比,2,4-二甲基戊烷的分子结构也有所不同。
4. 2,5-二甲基戊烷(2,5-Dimethylpentane):这是八碳烷烃的另一种同分异构体,其中两个甲基基团分别连接在碳原子的2号和5号位置上。
与前面提到的同分异构体相比,2,5-二甲基戊烷的分子结构有所差异。
5. 3,3-二甲基戊烷(3,3-Dimethylpentane):这是八碳烷烃的一种同分异构体,其中两个甲基基团分别连接在碳原子的3号位置上。
与前面的同分异构体相比,3,3-二甲基戊烷在结构上有所不同。
6. 3,4-二甲基戊烷(3,4-Dimethylpentane):这是八碳烷烃的又一种同分异构体,其中两个甲基基团分别连接在碳原子的3号和4号位置上。
与前面提到的同分异构体相比,3,4-二甲基戊烷的分子结构也有所不同。
7. 3,5-二甲基戊烷(3,5-Dimethylpentane):这是八碳烷烃的另一种同分异构体,其中两个甲基基团分别连接在碳原子的3号和5号位置上。
人教版化学必修2最简单的有机化合物-甲烷练习题100题(含解析答案)7

人教版化学必修2最简单的有机化合物-甲烷练习题100题(含解析答案)学校:___________姓名:___________班级:___________考号:___________一、单选题1.设N A为阿伏伽德罗常数的值。
下列说法正确的是A.在7.8gNa2O2固体中,含有阴、阳离子的总数为0.3N AB.光照下,将16gCH4和71gCl2组成的混合气体充分反应,生成CH3Cl分子数为N A C.若发生水解的Fe3+为1mol,此时生成的氢氧化铁胶粒数为N AD.100g质量分数为46%的乙醇水溶液中,所含氢原子总数为6N A2.公元前一世纪,我国已使用天然气,天然气的主要成分为甲烷。
下列关于甲烷的叙述错误的是A.通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应B.甲烷和乙烯因碳原子数不同,所以互为同系物C.甲烷跟氯气反应每生成1molCHCl3则消耗3molCl2D.因为二氯甲烷没有同分异构体,所以甲烷为正四面体结构3.下列说法正确的是A.CH4、CCl4和CH3C1都是正四面体结构B.四氯化碳是一种常见的有机溶剂,密度比水小C.甲烷与氯气的取代反应,生成的产物中CH3C1最多D.标准状况下,2.24L一氯甲烷含有的分子数为6.02×10224.一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为99.2 g,当其缓慢经过无水CaCl2时,CaCl2增重50.4g。
原混合气体中CO的质量为()A.13.2 g B.22.4g C.24.4g D.26.4g5.下列关于甲烷与Cl2的取代反应所得产物的说法正确的是( )A.都是有机物B.都不溶于水C.有一种气态物质,其余均是液体D.除一种外均是四面体结构6.下列有关甲烷的说法中,不正确的是A.1mol甲烷中含有4mol C—H共价健B.CH4、CCl4和CH3Cl都是正四面体结构C.光照条件下甲烷能与溴蒸气发生取代反应D.通常情况下,甲烷跟强酸、强碱、强氧化剂不反应7.下列说法正确的是A.按系统命名法,的名称为2-甲基-3,5-二乙基己烷B.用Na2C03溶液能区分CH3COOH、CH3CH2OH、苯和硝基苯四种物质C.2-甲基丁醇的结构简式:OHD.CCl4分子的比例模型:8.在催化剂作用下,200mL的某烷烃与某炔烃的混合气体与氢气发生加成反应,最多需要100mL的氢气(同温同压),则混和气体中烷烃与炔烃的物质的量之比为( ) A.1∶1B.1∶2C.1∶3D.3∶19.下列分子式只能表示一种物质的是()A.C3H7Cl B.C4H8C.CH2Cl2D.C2H6O10.一定条件下,能与甲烷反应的物质是()A.水B.溴水C.氧气D.酸性高锰酸钾溶液11.以下关于甲烷的说法中,错误的是()A.甲烷是最简单的有机化合物B.甲烷分子具有正四面体结构C.甲烷分子中的4个C—H键完全相同D.甲烷分子中具有非极性键12.下列有关化学用语表示正确的是()A.中子数为20的氯原子:2017Cl B.N2的电子式:N NC.CH4分子的比例模型:D.硫离子结构示意图:13.下列反应属于取代反应的是( )A.CH4+2O2CO2+2H2OB.NaOH+HCl===NaCl+H2OC.CH2===CH2+H2CH3—CH3D.CH3CH2—Br+H2O CH3CH2—OH+HBr14.下列有关化学用语的表述正确的是()A.次氯酸的电子式为:B.丙烷分子的球棍模型为:BrC.质子数为35、中子数为45的溴原子:8045D.—Cl与Cl-两种微粒,含有相同的电子数15.按1:4比例在试管中收集甲烷和氯气的混合气体,用橡皮塞塞紧,光照一段时间后,倒扣于水中,拔开试管塞,在实验的过程中不可能观察到的现象是( )A.试管中气体黄绿色变浅B.试管中出现大量的白烟C.试管壁上有油状液滴出现D.试管内液面上升16.下列有关A、B、C、D四种固体样品的性质中,最可能是有机物的是( )A.A B.B C.C D.D17.下列烷烃中,常温下呈气态的是()A.已烷B.丁烷C.庚烷D.十二烷18.同分异构现象是造成有机物种类繁多的重要原因之一。
第3课时怎样书写同分异构体的结构简式

CH3
②
③
• (3)转换技巧 • 练5. 已知丙烷的二氯代物有四种异构体, 则其六氯代物的异构体数目为( ) • A 两种 B 三种 C 四种 D五种 • 答案:C
• 练6. 已知二氯苯有三种同分异构体,则四 氯苯有同分异构体 • A.1种 B.2种 C.3种 D.4种 • 答案:C
三、不饱和烃同分异构体书写规则:
二、同位素、同素异形体、同系物、同分异构体比较
比较 概念 同位素 定义 分子式或化学符号 结构 性质
质子数相同, 电子排布相同, 原子符号表示不同。 物理性质不同, 中子数不同的 质子数相同中 2 3 如1 化学性质相同 H 、 H 、 1 1 1H 原子 子数不同 元素符号表示相同, 同 种 元 素 组 成 分 子 式 可 不 同 。 如 单质的组成或 物理性质不同, 的不同单质 石 墨 和 金 刚 石, O 2 结构不同 化学性质相同 和 O3 结构相似,分 子组成相差若 干个CH2原子 团的有机物 分子式相同, 结构不同的化 合物 不同 相似
主链由长到短
CH3CH2CHCH2CH3
位置由心到边
CH3CCH2CH3
CH3 CH3 CH3 CH3CHCHCH3
CH3
CH3CHCH2CH2CH3
排 布 由 对 到 间
CH3
练2.写出C7H16的所有同分异构体的 结构简式
思路和分析:书写碳原子数6个以上的烷烃的同分异 构体,难在写不完全,按下列方式来写可杜绝遗漏现象: (1)写出最长的碳链(用碳架表示)C—C—C—C—C—C—C (2)拿下1个碳原子作为支链并变换连接的位置:
傅全安
一、烷烃同分异构体书写规则:
①写出最长的碳链 ②将最长碳链上的碳原子依次减少,将减下的碳原子 (一个或多个)连在主链上,并依次改变它的位置和连接方
烷烃的命名

烷烃的命名烷烃常用的命名法有普通命名法和系统命名法两种。
1. 普通命名法(习惯命名法)一般只适用于简单、含碳较少的烷烃,基本原则是:(1)根据分子中碳原子的数目称“某烷”。
碳原子数在十以内时,用天干字甲、乙、丙、丁、戊、已、庚、辛、壬、癸表示;碳原子数在十个以上时,则以十一、十二、十三、……表示。
例如:(2)为了区别异构体,直链烷烃称“正”某烷;在链端第二个碳原子上连有一个甲基且无其它支链的烷烃,称“异”某烷;在链端第二个碳原子上连有两个甲基且无其它支链的烷烃,称“新”某烷。
例如:戊烷的三种异构体,分别称为正戊烷、异戊烷、新戊烷。
2.烷基的命名烷烃分子中去掉一个氢原子形成的一价基团叫烷基。
烷基的名称由相应的烷烃命名。
常见烷基如下:CH3— CH3CH2— CH3CH2CH2—(CH3)2CH— CH3CH2CH2CH2—甲基乙基丙基异丙基丁基(CH3)3C—(CH3)2CHCH2—CH3CH2CH(CH3)—(CH3)3CCH2—(CH3)2CHCH2CH2—叔丁基异丁基仲丁基新戊基异戊基烷基通式为C n H2n+1,通常用R-表示,所以烷烃也可用RH表示。
对于结构比较复杂的烷烃,应使用系统命名法。
3.系统命名法直链烷烃的系统命名法与普通命名法相同,只是把“正”字取消。
对于结构复杂的烷烃,则按以下原则命名。
(1)在分子中选择一个最长的碳链作主链,根据主链所含的碳原子数叫做某烷。
主链以外的其它烷基看做主链上的取代基,同一分子中若有两条以上等长的主链时,则应选取分支最多的碳链作主链。
例如:正确的选择是2,不是1(2)由距离支链最近的一端开始,将主链上的碳原子用阿拉伯数字编号。
将支链的位置和名称写在母体名称的前面,阿拉伯数字和汉字之间必须加一半字线隔开。
例如:3-甲基丁烷(3)如果含有几个相同的取代基时,要把它们合并起来。
取代基的数目用二、三、四……表示,写在取代基的前面,其位次必须逐个注明,位次的数字之间要用逗号隔开。
烷烃同分异构体分子结构有几种规律

烷烃同分异构体分子结构有几种规律示例文章篇一:《烷烃同分异构体分子结构的规律》嗨,小伙伴们!今天咱们来聊聊烷烃同分异构体分子结构的规律。
这听起来可能有点复杂,但是只要跟着我一步一步来,就会发现超级有趣呢。
我先来说说什么是烷烃吧。
烷烃就像是一群小积木搭成的东西,它是由碳和氢组成的。
碳就像一个个小节点,氢就像围绕在节点周围的小伙伴。
比如说甲烷,它就是一个碳原子周围带着四个氢原子,就像一个中心有个小碳球,周围四个小氢球围着它转,特别简单。
那同分异构体是什么呢?这就好比是同样的小积木,能搭出不同的形状。
就像咱们用同样的乐高积木,可以搭出房子,也可以搭出汽车一样。
对于烷烃来说,同分异构体就是它们有着相同的分子式,但是分子结构不一样。
那烷烃同分异构体分子结构有啥规律呢?首先,咱们从最简单的开始看。
当烷烃的碳原子数比较少的时候,规律还比较好发现。
就拿丙烷来说,它只有三个碳原子,那它的结构就只有一种。
就像一个小队伍,只有三个人,排列的方式就那么一种,很简单直接。
这时候我就想啊,是不是碳原子少的时候就不会有太多花样呢?可是当碳原子数增加到四个,也就是丁烷的时候,情况就变得有趣起来了。
丁烷有两种同分异构体呢。
一种是正丁烷,四个碳原子像小火车一样,一个接一个地排着队,氢原子就规规矩矩地在两边陪着。
还有一种是异丁烷,它的结构就像一个三叉路口,中间有个碳原子,周围连着三个碳原子,氢原子也各就各位。
这就好像同样是四个人,一会儿排成一条直线走,一会儿又变成一个有中心点的形状。
我当时就惊讶得瞪大了眼睛,原来多了一个碳原子就有这么大的变化呀。
再看戊烷,它有五个碳原子。
这时候它的同分异构体就有三种了。
一种是正戊烷,就像一列更长的小火车,五个碳原子整齐地排着。
第二种是异戊烷,就像在正丁烷的结构基础上,有个碳原子从队伍里伸出了一只“小胳膊”,变成了有个小分支的结构。
第三种新戊烷就更奇特了,它像一个中心碳原子带着四个小伙伴,就像一个小明星被四个保镖围着一样,特别对称。
化学必修二—烷烃
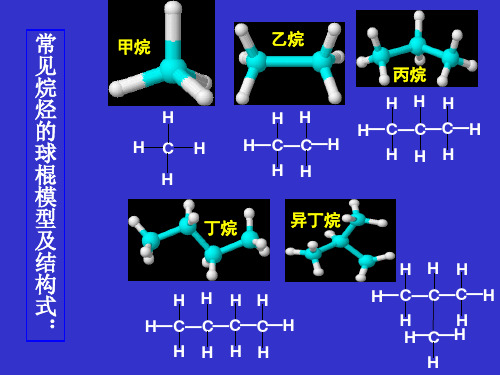
正己烷
异己烷
新己烷
正: 直链烷烃
异
CH3CHCH3
新
CH3 CH3CCH2CH3
2)系统命名法(IUPAC命名法) )系统命名法( 命名法) 命名法 a. 选最长碳链作主链,支链作取代基。遇多个等长碳链,则 选最长碳链作主链,支链作取代基。遇多个等长碳链, 取代基多的为主链。 取代基多的为主链。
2-甲基 -5-(1,1-二甲基丙基)癸烷 甲基 ( , 二甲基丙基 二甲基丙基) e. 名称的排列顺序 中文名称按基团顺序规则,较小的基团列在前; 中文名称按基团顺序规则,较小的基团列在前;英文名称 按基团首字母的字顺先后列出。 按基团首字母的字顺先后列出。
CH2CH2HC3 CH3CH2CH2CHCHCH2CH2CH2CH3 CHCH3 CH3
顺序大的基团称较优基团。 顺序大的基团称较优基团。
支链上连有取代基, d. 支链上连有取代基,则从和主链相连的碳原子开始将支链 碳原子依次编号,并将取代基位号、 碳原子依次编号,并将取代基位号、名称连同支链名写在 括号内。 括号内。
1 2 3 4 5
1'
6
2'
7
3'
8
9
10
CH3CHCH2CH2CHCH2CH2CH2CH2CH3 CH3 H3C C CH2 CH3 CH3
5-丙基 异丙基壬烷 丙基-4-异丙基壬烷 丙基 4-isopropyl-5-propylnonane [注意 注意] 注意 1)相同取代基数目用汉文数字二、三 ...表示; )相同取代基数目用汉文数字二、 表示; 表示 2)取代基位号用阿拉伯数字表示; )取代基位号用阿拉伯数字表示; 3)阿拉伯数字与汉字之间必须用短横线分开; )阿拉伯数字与汉字之间必须用短横线分开; 4)阿拉伯数字之间必须用逗号分开。 )阿拉伯数字之间必须用逗号分开。
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)一、CH4同分异构体(共1种)1、甲烷二、C2H6同分异构体(共1种)1、乙烷三、C3H8同分异构体(共1种)1、丙烷四、C4H10同分异构体(共2种)1、丁烷2、2—甲基丙烷五、C5H12同分异构体(共3种)1、戊烷2、2—甲基丁烷3、2 , 2—二甲基丙烷六、C6H14同分异构体(共5种)1、己烷2、2—甲基戊烷3、3—甲基戊烷4、2 , 2—二甲基丁烷5、2 , 3—二甲基丁烷七、C7H16同分异构体(共9种)1、庚烷2、2—甲基己烷3、3—甲基己烷4、3—乙基戊烷5、2 , 2—二甲基戊烷6、2 , 3—二甲基戊烷7、2 , 4—二甲基戊烷8、3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷八、C8H18同分异构体(共18种)1、辛烷2、2—甲基庚烷3、3—甲基庚烷4、4—甲基庚烷5、3—乙基己烷6、2 , 2—二甲基己烷7、2 , 3—二甲基己烷8、2 , 4—二甲基己烷9、2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C9H20同分异构体(共35种)1、壬烷2、2—甲基辛烷3、3—甲基辛烷4、4—甲基辛烷5、3—乙基庚烷6、4—乙基庚烷7、2 , 2—二甲基庚烷8、2 , 3—二甲基庚烷9、2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷十、C10H22同分异构体(共75种)1、癸烷2、2—甲基壬烷3、3—甲基壬烷4、4—甲基壬烷5、5—甲基壬烷6、3—乙基辛烷7、4—乙基辛烷8、2 , 2—二甲基辛烷9、2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烃的同分异构体数目的确定方法

烃的同分异构体数目的确定方法1、等效氢法烃的一取代物数目的确定,实质上是看处于不同位置的氢原子数目。
可用“等效氢法”判断。
判断“等效氢”的三条原则是:①同一碳原子上的氢原子是等效的;如甲烷中的4个氢原子等同。
②同一碳原子上所连的甲基是等效的;如新戊烷中的4个甲基上的12个氢原子等同。
③处于对称位置上的氢原子是等效的;如乙烷中的6个氢原子等同,2,2,3,3—四甲基丁烷上的24个氢原子等同,苯环上的6个氢原子等同。
在确定同分异构体之前,要先找出对称面,判断等效氢,从而确定同分异构体数目。
例1:下列有机物的一氯取代物其同分异构体的数目相等的是( )例2:含碳原子个数为10或小于10的烷烃中,其一卤代烷烃不存在同分异构体的烷烃共有( )A. 2种B. 3种C. 4种D. 5种2、轴线移动法对于多个苯环并在一起的稠环芳烃,要确定两者是否为同分异构体,则可画一根轴线,再通过平移或翻转来判断是否互为同分异构体。
例3:萘分子的结构式可以表示为,两者是等同的。
苯并[a]芘是强致癌物质(存在于烟囱灰、煤焦油、燃烧烟草的烟雾和内燃机的尾气中)。
它的分子由五个苯环并合而成,其结构式可表示为(Ⅰ)或(Ⅱ)式,这两者也是等同的。
现有结构式(A)~(D),其中(1) 跟(Ⅰ)、(Ⅱ)式等同的结构式是____________;(2) 跟(Ⅰ)、(Ⅱ)式是同分异构体的是___________。
3.定一移二法对于二元取代物的同分异构体的判断,可固定一个取代基位置,再移动另一取代基位置以确定同分异构体数目。
例4:若萘分子中有两个氢原子分别被溴原子取代后所形成的化合物的数目有( )A.5B. 7C. 8D. 10四、排列组合法例5:若萘分子中有两个氢原子分别被溴原子取代后所形成的化合物的数目有( D )A. 5B. 7C. 8D. 10例6:有三种不同的基团,分别为-X、―Y、―Z,若同时分别取代苯环上的三个氢原子,能生成的同分异构体数目是A. 10B. 8C. 6D. 4例7:分子结构中含有两个-CH3、一个-CH2-、一个基、一个-OH,且属于酚类的同分异构体有6种,其结构简式为:_____、_____、_____、_____、_____、_____。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碳原子数目越多,同分异构体越多
碳原
子数 1 2 3 4 5 6 7 8 9 10
同分
异体 数
1
1
1
2
3
5
9 18 35 75
碳原
子数 11 12 …. 15
20
40
同分
• 在有机化合物大家族里,有一类物质是仅由 碳和氢两种元素组成的,我们把这类有机化 合物总称为烃。烃也叫做碳氢化合物。
• 甲烷是组成最简单的烃
CH3Cl、CH3COOH、CH3CH2OH是否都属于烃?
.. ..
.
H..
H
CH4 H C.. H H-C-H
CH4
2
H
H
甲 分子式
电子式
结构式
结构简式
烷
练习
请写出C6H14的同分异构体。
CH3-CH2-CH2-CH2-CH2-CH3
CH3-CH2-CH-CH2CH3 CH3
CH3-CH-CH2-CH2CH3 CH3
CH3 CH3-C-CH2-CH3
CH3
CH3 CH3-CH-CH-CH3
CH3
写出分子式为C5H11Cl的所有同分异 构体的结构简式。
CH3
CH3 CH CH CH3 CH3 CH3
翻:
CH3 CH2 CH CH3构体的写法
一般采用“减链法”,可概括为“两注意,四句话
两注意: ①选择最长的碳链为主链;②找出中心对称线
四句话: 主链由长到短,支链由整到散,位置由心到边, 排布由邻到间.
分
子 表 示 式
知识支持: 用短线“-”表示原子所 形成的共价键进而表示 物质结构的式子称为结 构式。省略了部分短线
思考 甲烷的空间
结构是否为平面 结构呢?动手实 验
的结构式称为结构简式
结构式仅来表示分子中原子的连接顺序,不能表示分子中原 子在空间的分布
实验数据: 甲烷分子中有四个C-H键,且键长(1.09×10-10m) 键能(413KJ/mol)、键角(109028,)都相等。
有机化合物的结构特点
快乐是一天, 不快乐也是一天, 我们何不天天快乐!
一般甲烷高温分解,长链烷烃高温裂解、裂化。
习惯命名法
(1).碳原子数在1~10之间,用甲、乙、丙、丁、戊、
己、庚、辛、壬、癸. (2).碳原子数大于10时,用实际碳原子数表示.
(3).为了区别碳原子数相同的同分异构体,又将它 们分别称为“正”、“异”、“新”.
C2H6 乙烷
C5H12 戊烷
C9H20 壬烷
这种结合使每个碳原子的化合价都已充分利用,达 到 饱和
•定义:碳原子之间以碳碳单键相结合 成链状,碳原子剩余的价键全部被氢 原子所饱和的烃,叫烷烃。又称饱和 链烃
写出上图物质的分子式,结构式,结构简式,总结烷 烃的分子通式
通式:
CnH2n+2(n≥1)
性质: 与甲烷的化学性质相似
化学性质(与CH4相似)
试写出戊烷的同分异构体
正戊烷
异戊烷
CH3-CH2-CH2-CH2-CH3 CH3-CH-CH2-CH3 CH3
新戊烷 CH3 CH3-C-CH3 CH3
对于复杂结构的处理:拉、转、翻
拉:
CH3 CH2 CH2
CH2 CH3
CH3 CH2 CH2 CH2 CH3
转:
CH3
CH3 CH CH CH3
C4H10 丁烷
CH3CH2CH2CH3
名称 熔点
沸点
CH3CHCH3 相对密度 CH3
正丁烷 -138.4
-0.5
0.5788
异丁烷 -159.6 -11.7
0.557
1、同分异构现象 同分异构体
三个相同:分子组成相同、分子量相同、
理解:
分子式相同
二个不同:结构不同、性质不同
思考 甲烷、乙烷、丙烷有同分异构体吗?碳原 子数至少为多少的烷烃具有同分异构体?
异体 数
159
355 ….
4347
366319 62491178805931
有机物的组成元素只有几种,为什么能 衍生出几千万种有机化合物?
.
. C.
.
.
. C
:
:C :
.C :.
• 原子之间共价键相连 • 碳原子之间可以连成链状或环状 • 碳原子与碳原子之间可以单键、双键或叁键 • 分子式相同时,可以出现多种结构
共价键参数
键长: 键长越短,化学键越稳定
键角: 决定物质的空间结构
键能: 键能越大,化学键越稳定
归纳甲烷分子的结构特点:
分子结构示意图
碳与氢形成四个共价键,以C原子为中心, 四个氢位于四个顶点的正四面体立体结构
思考 甲烷的四种取代物空间结构如何?
观察下面的分子与甲烷有什么样的相同点?
结构特征: (1)碳、碳之间由 单键 相连接; (2)碳、碳之间结合成 链状 ; (3)碳原子的剩余价键被 氢原子 结合
(1)氧化反应
CnH 2n 2 3n 1O2 点燃 nCO2 (n 1)H 2O 2
均不能使KMnO4褪色,不与强酸,强碱反应。 (2)取代反应
在光照条件下进行,产物更复杂。
例如: CH 3CH 3 Cl 2 光照 会产生9种产物。
它的一氯代物和五氯代物有什么关系 3.烷烃的受热分解 由于其它烷烃的碳原子多,所以其它烷烃分解比甲烷复杂。
C12H26 十二烷
分析下列两个分子是否为烷烃,写 出它们的分子式,结构式及结构简 式 ,分析在组成和结构上有何异同?
[CH3CH2CH2CH3]
[CH3CH(CH3 )CH3] 或
CH3CHCH3 CH
1、同分异构现象 同分异构体
化合物具有相同的分子式,但具有不同 结构式的现象叫同分异构现象。 具有同分异构现象的化合物互称同分异构体。
