第二章 烷基化反应
羰基化合物的α-烷基化和催化烷基化反应
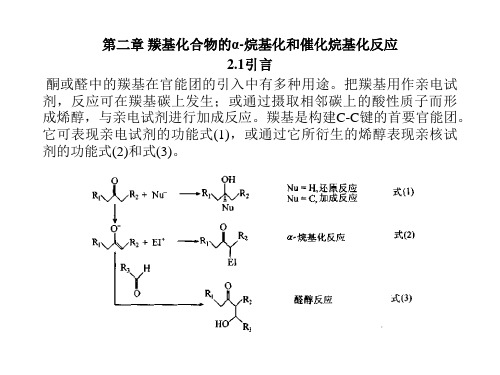
2.4 配位型的环内手性传递 配位型的手性烯醇体系,金属离子在固定原有的手性和烯醇部分之 间的立体化学关系至关重要。 2.4.1β-羟基酸 在烯醇化过程中这些底物可以形成E烯醇或者Z烯醇,对这两种烯醇 体系的任何一种而言,配位作用在确定烯醇对映面的选择中都可能 是决定性的。如图2.12所示,由于Re面进攻Z-或E-烯酵,结果都形 成了主要的组分。
从一些易得的环氧基硅烷基醚开始,合成α,α—二取代α—氨基酸衍 生物:
具有张力的氨基醇衍生的酮酯或酰胺与格氏试剂反应,制备对映体 纯叔-α -羟基酸 :
2.6 双内酰亚胺体系 甘氨酸和其它氨基酸经过二酮哌嗪,进行O—甲基化得到六元杂环产 物,水解以后以高对映体过量获得了α-甲基氨基酸。
2.7 用于羰基化合物的α-烷基化的手性辅剂一览表
三乙基铝化合物可从氢化铝和乙烯很经济地以工业规模制备,因此 这类化合物成功的烷基化反应肯定会开辟一个活跃的新研究领域。
一些新配体:
2.10 ZnR2对酮的催化不对称加成: 叔醇不对称中心的对映选择性形成 许多生物活性的天然产物含有季碳原子,通过碳亲核试剂对酮的加 成来不对称合成叔醇近来越来越受到关注(也参见2.5节)。 DAIB(142)催化二苯基锌对酮的对映选择性加成:
樟脑磺酰胺-钛醇盐衍生物催化二甲基锌和二乙基锌对潜手性酮的对 映选择性加成:
2.11 不对称氰醇化反应 光学活性的磺肟145和Ti(OPri)4生成手性钛试剂催化三甲基甲硅烷基 氰化物对醛的不对称加成。
假定的反应机理:
139(X=CN)催化三甲基甲硅烷基氰化物与醛的反应。手性的二氰 基络合物在原位生成,不对称氰硅烷化给出的e.e.值达到75%。
在同环桥键羟基氨基二茂铁(—)—130存在下,11种芳族和脂族醛与 Et2Zn进行烷基化反应。生成的醇具有67%一97%的e.e.值。这种 二茂铁催化剂成功地用于使芳族醛和直链或支链脂族醛的烷基化, 产生的仲醇e.e.值高达97%。即使用β—支链的脂族醛,得到的光 学产率也比用131所报道的要高。
烷基化反应

缺点:价格较贵,腐蚀性强。
应用:工业上用于制备十二烷基苯。
磷酸或多磷酸:无水磷酸(H3PO4)凝固点42.4 ℃,是烯 烃烷基化的良好催化剂。通常使用85~89%的含水磷酸。 多磷酸是各种磷酸多聚物的混合物,对许多类型的有机物 是良好的溶剂。
OH OH HO H3PO 4
+(CH3)3COH
HO
H2O C(CH3)3 +
§7.1 概述
一、定义 有机物分子中的碳、氮、氧等原子上引入烃基 的反应。 广义上讲,包括引入烷基、烯基、炔基、芳基、 羧甲基(-CH2COOH)、羟甲基(-CH2OH)、氯甲 基(-CH2Cl)等。 二、烃化剂 发生取代反应的:卤烷、醇类和酯类 发生加成反应的:不饱和烃和环氧化合物 发生脱水缩合反应的:醛类和酮类
卤代烃的烷基化反应
(1)烷基相同时,不同的卤素形成的卤代烷烃的反应活性 顺序为RI >RBr>RCl 。 (2)卤代烷烃中卤素相同时,不同的烷基则反应活性顺序 为:
CH2X > R3CX > R2CHX > RCH2X > CH3X
(3)不能用卤代芳烃如氯苯、溴苯代替卤代烷进行烷基化 反应,因为连接在芳环上的卤素反应活性较低,不能进行 烷基化反应。
D、只有乙烯作烷基化剂时,生成乙苯,碳原子数3以上的烯
烃,生成支链芳烃(如异丙苯的制备)。
CH3 CH
70%
+
CH3
CH CH2
AlCl3
CH3 CH2CH2CH3
30 %
(2)质子酸:硫酸、氢氟酸和磷酸。
活性次序是:HF>H2SO4>H3PO4 硫酸是以烯烃、醇、醛和酮为烷基化剂广泛使用的催化剂, 为了避免磺化、氧化、酯化、脱水等副反应,必须选择合适 的浓度。 例如,异丁烯,用85~90%的硫酸催化制备烷基苯,除了 发生烷基化反应外,还发生酯化反应;使用80%的硫酸则不 发生烷基化反应,而发生酯化反应和烷基化产物的聚合反应。
烷基化反应的简介PPT课件

★ 2.烷基化试剂 ★ 3.催化剂
★ 4. 芳环上C-烷化反应特点 5.C-烷基化方法
第4页/共35页
★ 1.C-烷基化反应历程
催化剂路易大多是斯酸、质子酸或酸性氧化物,催化剂的作用是使烷
基化剂转变成活泼的亲电质点 —— 碳正离子。烷基正离子进攻芳环发生亲
电取代反应。
H3C CH2 Cl
非离子表面活性剂
CH2CH2CN N CH2CH2CN
第22页/共35页
★ 2.N-烷化反应类型
(3)缩合——还原型: 所用N-烷化剂为醛和酮类。
O
R C H + H NH2
OH - H-OH
R CH NH2
〔H〕
R CH NH
R CH2 NH2
O
R C R` + H NH2
烷基化反应是指向有机化合物分子中的碳、氮,氧等原子上引入烃基增 长碳链(包括烷基、烯基、炔基、芳基等)的反应,其中以引入烷基最为重 要。 3.可发生烷基化反应的有机物:芳烃、活泼亚甲基化合物、胺类等。 4.烷基化试剂种类:醇、烯烃、硫酸二甲酯、卤代烷、环氧化物、醛、酮等。
第1页/共35页
二、烷基化反应的类型
一、烷基化反应的简介
1.研究作用: 可以合成塑料、医药、溶剂、合成洗涤剂、药物、染料、香料、催化剂、
表面活性剂等功能性产品。如通过C—烷基化反应可制得阴离子表面活性剂; 通过O-烷基化可制得聚乙二醇型非离子表面活性剂;通过N-烷基化合成
的季铵盐是重要的阳离子表面活性剂、相转移催化剂、杀菌剂等。 2.定义:
是有大量铝盐废液生成,有时由于副反应而不适于活泼芳烃(如:酚、 胺类)的烷基化反应。 (2)质子酸
烷基化反应

CH2
+ HCl
六、用醇对芳环的C-烷基化
• 醇类是反应能力较弱的烷基化剂,它 们只适用于活泼芳族化合物(例如苯胺、 苯酚和萘等)的C-烷基化。 • 常用的烷基化催化剂有路易斯酸和质子 酸等。 • 1.用醇对芳胺的C-烷基化
NH2
C4H9OH H2O ZnCl2催化 210℃, 0.8MPa
NHC4H9
CH3 C O + 2 OH CH3 CH3
H 催化 脱水缩合
HO
C CH3
OH + H2O
(双酚A)
8.3 N-烷基化
• 定义:氨、脂肪族或芳香族胺类氨基上的氢原 子被烷基取代,或者通过直接加成而在氮原子 上引入烷基的反应叫N-烷基化反应。 • 这是制取各种脂肪族和芳香族伯、仲、叔胺的 主要方法,其反应通式如下:
OH OH (CH3)2CHOH +
磷酸催化 二甲苯溶剂回流
OH OH + H2O C(CH3)3
七、用醛类对芳环的C-烷基化
• 1、醛对酚类的C-烷基化 • 甲醛与过量苯酚在无机酸催化作用下反应, 可制得4,4'-二羟基二苯甲烷(双酚F):
H C H O+ OH
H
H HO C H OH + H2O
4、用醛或酮的N-烷基化
• 氨或胺类化合物和许多醛或酮可发生还 原性烷基化,即伴随有还原反应的烷基 化反应,其化学反应通式如下:
H R C O H + NH3
H2O
R C NH
亚胺
还原剂
RCH2NH2
伯胺
R R
/
R C O + NH3
H2O
R
/
C
亚胺
(精品课件)烷基化反应

4 烷基化反应定义:一般而言,有机分子中的氢原子(包括某些官能团上的,如羟基和氨基等)被烷基取代,可称为烷基化反应。
意义:在药物分子中引入烷基可增加其脂溶性,或形成新的官能团赋予药物以特殊性能。
如丁卡因药效为普鲁卡因的10倍。
本章内容:醇、酚的氧烷化,胺的氮烷化,活泼亚甲基及芳烃的碳烷化等反应。
4.1 氧原子上的烷基化反应在氧原子上烷基化是获得醚,尤其是不对称醚的通用方法。
4.1.1 以卤代烃为烷基化试剂醇、酚的钠盐或醇、酚在碱(钠、氢氧化钠以及氢氧化钾等)的存在下与卤代烷生成醚的反应称为Williamson反应,是合成不对称醚的最常用方法。
(1) 反应机理Williamson反应是典型的SN2反应。
此外,醇、酚与卤代烷的反应也可按SN1机理进行。
(2) 影响因素底物的影响:①伯卤代烷一般为SN2机理;叔卤代烷一般为SN1机理;而仲卤代烷可SN1也可SN2。
②由于芳环的吸电子作用,使得酚的活性一般弱于醇。
③底物的空间位阻对反应速率影响较大。
溶剂的影响:极性溶剂可促进反应。
SN2反应一般在碱性条件下进行;而SN1反应一般在酸性或近中性(可为弱碱性)条件下进行。
(3) 反应示例①苯海拉明的合成反应机理:双分子亲核取代(SN2)。
②糖环6-伯羟基的保护在极性溶剂中,Ph3CCl可形成非常稳定的碳正离子Ph3C+,此步为控制步骤,该碳正离子形成后迅速与伯羟基结合,生成醚。
反应机理:碳正离子历程(SN1)。
③卤代烃为芳卤的情况:对硝基苯乙醚(非那西丁中间体)的合成反应机理:加成-消除机理。
反应活性:I<Br<Cl<F;芳环上一定要有吸电子基。
4.1.2 以芳磺酸酯为烷基化试剂氧原子的吸电子作用使得芳磺酸酯成为很好的离去基团,当与其相连的碳原子受到醇的进攻时,芳磺酸基很容易离去。
常见的芳磺酸酯包括苯磺酸酯、对甲苯磺酸酯、对硝基苯磺酸酯、对卤苯磺酸酯以及对三氟甲基苯磺酸酯等。
反应示例:鲨肝醇的合成(SN2反应)。
烷基化反应

化学反应
01 定义
03 相关资料
目录
02 简介
烷基化反应(Alkylation reaction)指向有机物分子中的碳、氮、氧等原子中引入烷基(-R)的反应,简称 烷基化。常用的烷基化剂有烯烃、卤代烷烃、硫酸烷酯和醇等。烷基化是有机合成的重要反应之一。例如苯与卤 代烷烃反应,可在苯环上引入烷基。
相关资料
77年,由法国化学家傅列德尔(Friedel)和美国化学家克拉夫茨(Crafts)两人发现 的。当在苯和氯甲烷中,加入无水三氯化铝便发生强烈的反应,放出氯化氢气体,并从反应混合物中分离出甲苯, 这种苯烷基化成为甲苯是最简单的一例。利用这类烷基化反应可以合成一系列烷基取代芳烃,在实验室和工业上 的用途十分广泛。
谢谢观看
通过烷基化,可形成新的碳碳、碳杂等共价键,从而延长了有机化合物分子骨架,改变了被烷基化物的化学 结构,赋予了其新的性能,制造出许多具有特定用途的有机化学品。有些是专用精细化学品,如非离子表面活性 剂壬基酚聚氧乙烯醚、邻苯二甲酸酯类增塑剂、相转移催化剂季铵盐类等。
烷基化试剂又称为烷化剂、烃化剂许,多烃的衍生物可作烷化剂。 ①卤烷:氯甲烷、碘甲烷、氯乙烷、溴乙烷、氯乙酸和氯化苄等。 ②醇类:甲醇、乙醇、正丁醇、十二碳醇等。 ③酯类:硫酸二甲酯、硫酸二乙酯、磷酸i甲酯、磷酸三乙酯、对甲基苯磺酸甲酯和乙酯等。 ④不饱和烃:乙烯、丙烯、高碳a烯烃、丙烯腈、丙烯酸甲酯和乙炔等。 ⑤环氧化合物:环氧乙烷、环氧丙烷等。 ⑥醛或酮类:甲醛、乙醛、丁醛、苯甲醛、丙酮和环己酮等。 卤烷、醇类和酯类是取代反应的烷化剂,不饱和烃和环氧化物是加成反应的烷化剂。醛类、酮类是脱水缩合 反应的烷化剂。
定义
有机化合物分子中连在碳、氧和氮上的氢原子被烷基所取代的反应 。
烷基化反应的简介

07
烷基化反应研究前沿与挑战
研究现状概述
烷基化反应类型
目前已知的烷基化反应主要包括 Friedel-Crafts 烷基化、烯烃的烷 基化、芳烃的烷基化等,每种类 型都有其特定的反应条件和机理 。
催化剂研究
催化剂在烷基化反应中起着至关 重要的作用,目前研究主要集中 在寻找高效、环保的催化剂,如 固体酸催化剂、离子液体催化剂 等。
02 03
烯烃烷基化反应数据处理
通过测定反应前后烯烃和卤代烃的含量变化来计算反应的 转化率和选择性;通过气相色谱等手段对产物进行分离和 定量分析。
羧酸烷基化反应数据处理
通过测定反应前后羧酸和卤代烃的含量变化来计算反应的 转化率和选择性;通过红外光谱、核磁共振等手段对产物 进行结构鉴定。同时,还可以通过对比实验数据,优化反 应条件,提高反应的效率和产物的纯度。
05
烷基化反应在有机合成中的应用
药物合成中的应用
1 2 3
合成药物活性成分
通过烷基化反应,可以合成具有特定药理活性的 药物分子,如抗癌药物、抗病毒药物等。
改善药物性质
烷基化反应可用于改善药物的溶解性、稳定性以 及生物利用度等性质,从而提高药物的疗效和安 全性。
药物代谢研究
烷基化反应在药物代谢研究中也有重要应用,可 以通过模拟体内代谢过程,研究药物在体内的转 化和代谢途径。
天然产物合成中的应用
合成复杂天然产物
通过烷基化反应,可以合成具有复杂结构的天然产物,如萜类、 生物碱等,这些天然产物往往具有重要的生物活性。
天然产物结构修饰
烷基化反应可用于对天然产物的结构进行修饰,从而改变其生物活 性和药理作用,为药物设计和开发提供新的思路。
合成天然产物类似物
烷基化反应ppt课件

2.1.3 用醇作烷化剂的C-烷化反应
反应历程
质 子 化 + +
R O H + H
R O H 2
解 离 +
R + H O 2
实例
(1)芳胺的C-烷化
N H 2
+ C H O H ,H O 4 9 2 Z n C l 2 2 1 0 C ,0 . 8 M P a
o
N H C H 4 9
异 构 化 Z n C l 2 o 2 4 0 C ,2 . 2 M P a
A r H 慢 离 子 对 烷 基 正 离 子
• 回顾
在Lewis酸催化作用下,芳烃及其衍生物与烯 烃、卤烷、酰卤、酸酐等活性组分反应形成新的 C-C键的反应,叫做傅氏反应。 引入烷基的反应叫做傅氏烷基化反应; 引入酰基的反应叫做傅氏酰基化反应。
反应的影响因素 (1)烷基化试剂的活性
1 R 1 R
O
O
(5)烯烃和炔烃:CH2=CH2, CH3CH=CH2, R-CH=CH2, CH2=CHCN, CH2=CHCOOCH3, CH≡CH; (6)羰基化合物:HCHO, CH3CHO, C3H7CHO, Ph-CHO, CH3COCH3, O
2.1 C-烃化
有机化合物分子中碳原子上的氢被烃 基所取代的反应叫做C-烃化反应。 F-C烷基化反应: R R 烃化剂:烯烃; 卤烷; H O H N 2 R 醇、醛、酮。 反应历程:酸催化的亲电取代反应。
A l C l 3
C C l
二 氯 二 苯 甲 烷
+ 2 H C l
2.1.2 H = C H + H 2
C H C H 2 3
5_烷基化反应(二)

LOGO
二,芳环上的O-烷基化反应 芳环上的 烷基化反应
(2)用酯的 烷基化 用酯的O-烷基化 用酯的 硫酸酯和磺酸酯均是活性较高的良好烷化剂. 硫酸酯和磺酸酯均是活性较高的良好烷化剂.硫酸二 甲酯应用最为广泛. 甲酯应用最为广泛. 优点:高沸点,因而可在高温,常压下进行反应; 优点:高沸点,因而可在高温,常压下进行反应; 缺点: 缺点:价格较高 应用:产量小, 应用:产量小,价值高的产品
LOGO
三,相转移烷基化反应 3.相转移催化剂 相转移催化剂
(2)聚醚类相转移催化剂 实现阳离子的相转移, 聚醚类相转移催化剂----实现阳离子的相转移 聚醚类相转移催化剂 实现阳离子的相转移, 适用于液-固或液 液的相转移催化过程. 固或液-液的相转移催化过程 适用于液 固或液 液的相转移催化过程. (3)三相催化剂 是最新发展起来的一种不溶于一 三相催化剂---是最新发展起来的一种不溶于一 三相催化剂 般溶剂的固体相转移催化剂,适用于液-液两相反 般溶剂的固体相转移催化剂,适用于液 液两相反 应. 4.相转移催化反应的应用 相转移催化反应的应用 相转移催化剂的应用范围很广,目前已成功 相转移催化剂的应用范围很广, 地应用于催化卤化,烷化,酰化,羧基化,酯化, 地应用于催化卤化,烷化,酰化,羧基化,酯化, 醚化,缩合,加成,氧化,还原等多种反应. 醚化,缩合,加成,氧化,还原等多种反应.
LOGO
一,N-烷基化反应 烷基化反应
2.应用 应用
工业上用于制备脂肪族和芳香族伯胺,仲胺, 工业上用于制备脂肪族和芳香族伯胺,仲胺, 叔胺,产物是制造医药, 叔胺,产物是制造医药,表面活性剂及纺织印染助 剂时的重要中间体. 剂时的重要中间体.氨基是合成染料分子中重要的 助色基团,烷基的引入可加深染料颜色,所以N-烷 助色基团,烷基的引入可加深染料颜色,所以 烷 基化反应在染料工业上有着极为重要的意义. 基化反应在染料工业上有着极为重要的意义.
有机化学基础知识点整理烷基化反应与烷化反应机制

有机化学基础知识点整理烷基化反应与烷化反应机制【有机化学基础知识点整理】烷基化反应与烷化反应机制烷基化反应是有机化学中一类重要的反应,主要涉及底物中的氢原子被烷基基团取代的过程。
烷化反应机制则是指在此类反应中所形成的反应中间体和过渡态的详细变化过程。
本文将整理烷基化反应的几个基础知识点,并探讨其中常见的烷化反应机制。
一、烷基化反应的基本概念烷基化反应是有机化学中最为常见和广泛应用的一类反应,其中最常见的就是烷基磺酸盐的合成。
其原理是通过引入一个“烷基基团”,将底物中的氢原子取代。
烷基化反应可以形成新的碳-碳键或碳-氧键,产生新的有机化合物。
二、烷基化反应的分类烷基化反应根据反应过程的类型和反应底物的不同,可以分为以下几类:1.质子接受型烷基化反应:底物中的质子被烷基离子或烷基金属试剂取代。
2.质子捐赠型烷基化反应:底物中的烷基基团将质子给予另一分子,形成新的碳-碳键。
3.亲电取代型烷基化反应:底物中的亲电试剂与烷基基团发生亲电取代反应。
4.自由基烷基化反应:底物中的烷基离子与自由基试剂发生反应,形成新的碳-碳键。
三、常见的烷化反应机制1.质子接受型烷基化反应机制:在质子接受型烷基化反应中,底物中的质子被烷基离子或烷基金属试剂取代。
这类反应通常采用强碱作为反应试剂,如氢氧化钠(NaOH)。
反应机理如下:底物 + 烷基离子/烷基金属试剂→ 产物 + 相应的离子/金属盐该反应机制属于亲核取代反应,质子首先被碱中的氢氧根离子去质子化,然后进一步与烷基离子或金属离子发生亲核取代反应,最终形成新的碳-碳键。
2.自由基烷基化反应机制:在自由基烷基化反应中,底物中的烷基离子与自由基试剂发生反应,形成新的碳-碳键。
这类反应通常通过热、光或自由基引发剂来产生自由基,如过氧化氢(H2O2)或过氧化苯甲酰(Benzoyl peroxide)。
反应机理如下:底物 + 自由基试剂→ 产物该反应机制属于自由基取代反应,首先由自由基引发剂产生自由基,然后自由基与底物反应,形成新的碳-碳键。
有机合成,烷基化反应ppt课件

O
(5)烯烃和炔烃:CH2=CH2, CH3CH=CH2, R-CH=CH2, CH2=CHCN, CH2=CHCOOCH3, CH≡CH; (6)羰基化合物:HCHO, CH3CHO, C3H7CHO, Ph-CHO, CH3COCH3, O
C-烃化 N-烃化 O-烃化
10.2 C-烷基化反应
作用:将烷化试剂转化为R+ 种类:质子酸、Lewis酸、酸性氧化物、 烷基铝
a.活性顺序:AlCl3>FeCl3> SnCl4> BF3> ZnCl2 HF> H2SO4 >H3PO4 根据RX的种类,芳烃的结构,选择催化剂用量 如PhCH2X,ZnCl2少量,CH3X,AlCl3用量多5~10%.
烃化剂:
(1)卤烷:CH3Cl, CH3I, C2H5Cl, C2H5Br, ClCH2COOH, Ph-CH2Cl; (2)酯类:(RO)2SO2, PhSO2OR, CH3-Ph-SO2OR, (RO)3PO; (3)醇类和醚类:CH3OH, C2H5OH, n-C4H9OH, C12H25OH, CH3OCH3, C2H5OC2H5; CH (4)环氧化合物: H2C ,CH H C HC ; 2 2 3
CH 3Cl/AlCl3 CH 3
0℃ △
CH 3Cl/AlCl3 CH 3
重排
CH 3
100 ℃
H 3C
CH 3
eg
C H C H O H 2 2 K O H △1 4 0 ℃ C H = C H 2
+
H C l / A l C l O C 3 3
6 ℃
A l C l 3 CC H C O O H H
第二节烷基化反应的基本原理

第二节 烷基化反应的基本原理
以烯烃、醇、醛、和酮为烷化剂时,广泛应用硫酸 作催化剂。在硫酸作催化剂时,必须特别注意选择适宜 的硫酸浓度。因为当硫酸浓度选择不当时,可能会发生 芳烃的磺化,烷化剂的聚合、酯化、脱水和氧化等副反 应。如对于丙烯要用 90% 以上的硫酸,乙烯要用 98% 硫 酸,即便如此,这种浓度的硫酸也足以引起苯和烷基苯 的磺化反应,因此苯用乙烯进行乙基化时不能采用硫酸 作催化剂。
第二节 烷基化反应的基本原理
(3)用醇烷基化的反应历程 当以质子酸作催化剂 时,醇先被质子化,然后解离为烷基正离子和水:
如用无水AlCl3为催化剂,则因醇烷基化生成的水会 分解三氯化铝,所以需用与醇等物质量之比的三氯化铝:
烷基化反应的活泼质点是按下面途径生成的:
第二节 烷基化反应的基本原理
(4)用醛、酮烷基化的反应历程 催化剂常用质子 酸。醛、酮首先被质子化得到活泼亲电质点,与芳烃加 成得产物醇;其产物醇再按醇烷基化的反应历程与芳烃 反应,得到二芳基甲烷类产物:
磷酸是较缓和的催化剂,无水磷酸(H3PO4)在高 温时能脱水变在焦磷酸。
第二节 烷基化反应的基本原理
工业上使用的磷酸催化剂多是将磷酸沉积在硅藻土、 硅胶或沸石载体上的固体磷酸催化剂,常用于烯烃的气 相催化烷基化。由于磷酸的价格比三氯化铝、硫酸贵得 多,因此限制了它的广泛应用。 阳离子交换树脂也可作为烷基化反应催化剂,其中 最重要的是苯乙烯-二烯乙苯共聚物的磺化物。它是烯烃、 卤烷或醇进行苯酚烷基化反应的有效催化剂。优点是副 反应少,通常不与任何反应物或产物形成络合物,所以 反应后可用简单的过滤即可回收阳离子交换树脂,循环 使用。缺点是使用温度不高,芳烃类有机物能使阳离子 交换树脂发生溶胀,且树脂催化活性失效后不易再生。
烷基化反应PPT培训课件

OH CH3I/NaH/THF
CH3 trans
50℃, 1 h
OCH3
CH3 trans (100%)
多卤代物的醚化
CHCl3 +
3 CH3ONa
CCl4
+
4 CH3ONa
分子内醚化,制备环氧
OH Br
NaOH
CH(OCH3)3 C(OCH3)4
O
2.磺酸酯为烃化剂
CH2OH CHOH CH2OH
OR
OH + ROH
EtOOCN=NCOOEt PPh3
ArOH +Ph3PN NCOOEt
COOEt
ROH
EtOOCNHNHCOOEt
+ Ph3P O R ArO-
ArOR + Ph3PO
第二节 氮原子上的烷基化反应
一.氨及脂肪胺的N-烷基化反应
(一)氨及胺和卤代烃的反应
RX + NH3
RNH3+X-
1(1)4选)择任一部分有并权按对合承同包条方件根和据价情C格况H执及O行考和核交标货准;进行奖M励e和2处S罚O。4/NaOH
1.面对抱怨要有正确的态度
CHO
(5)第三方出具的2014年度及2015年度财务审计报告,2015年7月-2015年12月期间任意3个月的依法缴纳税收及社会保障资金证明
, (不1)能实提施供或的监应督提货供物相的关运主输管、部现门场出移具动的O、证安H明装材和料调;试;
RNH2 + R'OP+PPh3
DMF
RR'NH + PPh3PO
R'R''NH2 + ROP+PPh3
第二章_烷基化反应

R2NH R3N
R2NH +
跟卤代烃的反应是主要方法之一, 缺点:易得到混合胺
1.伯氨的常用制备方法
(1):氨水和卤代烃的反应
O OH Br 70% NH2 NH3(70mol) O OH
用大大过量的氨水,抑制进一步反应, 该方法在工业中应用广泛
NO2 Cl O2N NH3/AcONH4 170 oC, 6h O2N NO2 NH2
CCl4/AlCl3 10-30 oC,3 h Cl Cl O H2O 80ຫໍສະໝຸດ O OH 95% CH2CH2CN
冠状动脉扩张药派克西林中间体
O OH C6H6/AlCl3 25 C, 4 h
o
冠状动脉扩张药普尼拉明中间体
MeO MeO CN AlCl3 MeO MeO
镇痛药延胡索乙素中间体
1.反应机理 :C+ 离子对芳环的亲电进攻
差向异构
OH CH3 cis CH3I/NaH/THF 50℃, 1 h OCH3 CH3 cis (100%)
OH CH3 trans
CH3I/NaH/THF 50℃, 1 h
OCH3 CH3 trans (100%)
多卤代物的醚化
CHCl3 + 3 CH3ONa CH(OCH3)3
CCl4
+
多卤代烃,甲醛,环氧乙烷
二.格氏试剂的C-烷基化 格氏试剂
OMe
Case:
NHBoc OH
PhCH2Br
NHBoc O
H N O O
二、酚的O-烷基化
1.卤代烃为烃化剂
CONH2 OH EtBr/NaOH 80~100℃, 19.6 x 10exp4 Pa CONH2 OEt
第二章 农药合成单元反应-2

活泼亚甲基反应物中Z、Z'是:
CHO , COR , COOR , CN, NO2 , COOH ,
(二)Knoevengel反应(克脑文那盖尔反应) Knoevengel反应(克脑文那盖尔反应) 反应
(一般-CH2-连两个吸电子基团),如:丙二酸、丙 二酸酯、氰乙酸酯、硝基烷烃等。 催化剂:NH3、RNH2、吡啶,哌啶 醛易发生此反应,其中以芳基醛的反应最为 重要。
CHO
+
CH2(COOEt)2
呱啶
CH
C(COOEt)2
O N CHO
+
COCH3 Et3N N CH C COOEt
CH3CCH2COOEt
(三)Claisen缩合 Claisen缩合 羧酸酯与R'CH2COR"型含活泼甲基或亚甲基的羧 酸化合物缩合生成β-羰基化合物的反应称Claisen缩 合。该反应有一分子醇脱去。
(二)Knoevengel反应(克脑文那盖尔反应) Knoevengel反应(克脑文那盖尔反应) 反应
COOH CHO
+
哌啶
COOH CH C COOH
C H2 COOH
H eat
CH
CH
COOH
+
C O2
+
H2 O
(二)Knoevengel反应(克脑文那盖尔反应) Knoevengel反应(克脑文那盖尔反应) 反应
N CHMe
H2/Raney Ni
NHCH2CH3
五、缩合反应 Condensation Reaction
(一)羟醛缩合(aldal condensation) 羟醛缩合( ) 含 α-H原子的醛或酮在催化剂作用下,生成β-羟 基醛、酮的反应称羟醛缩合,也叫醇醛缩合; 该反应通常在碱(氢氧化钠、醇钠)催化下进行, 有时也在酸(硫酸、对甲苯磺酸)催化下进行。
