共轭效应与超共轭效应的定义及特点
共轭效应介绍.

2、P-π共轭
如氯乙烯,当氯原子的p轨道的对称轴与
键中的p轨道对称轴平行时,电子发生离域。
3、超共轭(σ-π共轭)
超共轭效应是由一个烷基的C-
H键的σ键电子与相邻的半满 或全空的p轨道互相重叠而产 生的一种共轭现象。
效应(推电子),但两者均较弱,因此既不能 进行阴离子聚合,也不能进行阳离子聚合,只 能进行自由基聚合。如氯乙烯、氟乙烯、四氟 乙烯均只能按自由基聚合机理进行。
13
凡共轭体系上的取代基能降低体系的π电
子云密度,则这些基团有吸电子共轭效应, 用-C表示,如-COOH,-CHO,-COR;凡共 轭体系上的取代基能增高共轭体系的π电子云 密度,则这些基团有给电子共轭效应,用+C 表示,如-NH2,-OH,-R。
电子离域
如1,3-丁二烯,四个π电子不是
两两分别固定在两个双键碳原子之 间,而是扩展到了四个碳原子之间, 象这种现象称为电子离域。它体现 了分子内原子之间的相互影响。
二、分类:
共轭效应大致分为三类: 1、π-π共轭 2、P- π共轭
3、超共轭(σ-π共轭)
1、π-π共轭
非饱和键(双键或三键)与单键交替分 布,形成π键的P轨道在同一平面上相互重 叠而成共轭体系,称之为π-π共轭
如:1,3-丁二烯, CH2=CH-CH=CH2中,可以 看作两个孤立的双键重合在 一起,π电子的运动范围不 再局限在两个碳原子之间, 而是扩充到四个碳原子之间。
共轭效应的结果
ⁿ ⑴键长相对缩短,电子云重叠得越多,电子云密度 越大,两个原子结合得就越牢固,键长也就越短,单双 键产生了平均化
共轭效应与超共轭效应的定义及特点

1. 共轭效应与超共轭效应的定义及特点共轭效应不饱和的化合物中,有三个或三个以上互相平行的p轨道形成大n键,这种体系称为共轭体系•共轭体系中,n电子云扩展到整个体系的现象称为电子离域或离域键共轭效应:电子离域,能量降低,分子趋于稳定,键长平均化等现象称为共轭效应,也叫做C效应共轭效应的结构特点:共轭体系的特征是各6键在同一平面内,参加共轭的P轨道轴互相平行,且垂直于(T键在的平面,相邻P轨道间从侧面重叠发生键离域•共轭效应与诱导效应相比还有一个特点是沿共轭体系传递不受距离的限制•超共轭效应烷基上C原子与极小的氢原子结合,由于电子云的屏蔽效力很小,所以这些电子比较容易与邻近的n电子(或p电子)发生电子的离域作用,这种涉及到6轨道的离域作用的效应叫超共轭效应•超共轭体系,比共轭体系作用弱,稳定性差,共轭能小•2. 共轭效应共轭的类型2.1.1 n-n共轭通过形成n键的p轨道间相互重叠而导致n电子离域作用称为n-n共轭.参加共轭的原子数目等于离域的电子总数,又称为等电子共轭•我们可以简单地概括为双键,单键相间的共轭就是n-n共轭.例如:共轭体系的分子骨架称做共轭链2.1.2 p- n共轭体系通过未成键的p轨道(包括全满,半满及全空轨道)与形成n键的p轨道的重叠而导致的电子离域作用,称为p- n共轭.包括富电子,足电子,缺电子三种p- n共轭类型.我们也可以简单地理解为:双键相连的原子上的p轨道与n键的p轨道形成的共轭即为p- n共轭.例如:共轭方向及强弱判断共轭效应的方向及强弱直接影响物质的性质和稳定性,因此共轭方向及强弱的判断也就有着非常重要的作用.能够给出电子的称给电子共轭,用符号+C表示.相反,能接受电子的称吸电子共轭,用符号-C表示.卤素,羟基,氨基,碳负离子等与双键直接相连时,X. O. N .C等原子的孤对电子对与n键共轭.由于是由一个原子向共轭体系提供两个电子,相当于使n电子密度增大,所以有给出电子的能力,称为+C效应.一般富电子p- n共轭都属于给电子共轭.例如:中的都是+C效应.当参与共轭的O. N只提供一个电子,而本身电负性大于C原子,所以有使共轭体系电子向O. N转移的能力,因此有-C效应.电负性大于C的原子参与的等电子共轭是吸电子共轭.例如:都是-C效应.大多数共轭效应是由碳的2p轨道与其他原子的p轨道重叠所产生的,当某原子参与共轭的p轨道的形状大小,能量与碳的2p轨道越接近时,轨道重叠越,离域越易,共轭作用越强•即共轭效应的强弱与参与共轭的原子轨道的主量子数有关.n=2时有强的共轭,n>2有弱的共轭,n越大共轭越弱.另外,元素的电负性越小,越容易给出电子,有较强的+C效应.相反,元素的电负性越大,越容易吸引电子,有较强的-C效应.因此共轭效应也有周期性变化.同一类元素随n值增大,共轭减弱;同一周期n值相同,随原子序数增大,电负性增大,给电子共轭效应减弱吸电子共轭主要有电负性决定,电负性越大,吸电子共轭越强.3. 超共轭效应超共轭效应视其电子电子转移作用分为o- n . -p . (- a几种,以o- n最为常见.c- n超共轭丙烯分子中的甲基可绕C—C o键旋转,旋转到某一角度时,甲基中的C-Hc键与C=C的n键在同一平面内C-H -键轴与n键p轨道近似平行,形成l n共轭体系,称为o- n超共轭体系.在研究有机反应时有着重要的应用,在学习不对称烯烃的HX加成反应时,我们以C正离子形成的稳定性来解释马尔科夫尼科夫规则,若应用bn超共轭效应,则不仅说明甲基是推电子的,同时加深了对这一经验规则的深入理解.再如,不饱和烯烃的a-H的特殊活泼性也可以用& n超共轭效应来理解.丙烯的甲基比丙烷的甲H易被取代,丙烷中甲基的H不易被取代.基活泼的多,在液氨中丙烯中甲基的o-p超共轭当烷基与正离子或游离基相连时,C-H上电子云可以离域到空的p空轨道或有单个电子的p轨道上,使正电荷和单电子得到分散,从而体系趋于稳定,称做o-p超共轭体系.简单的说就是C-H的(键轨道与p轨道形成的共轭体系称做^p超共轭体系.如乙基碳正离子即为o-p超共轭体系.参加o-p超共轭的C-H数目越多,正电荷越容易分散,C正离子就越稳定.应用超共轭效应的应用也很广泛,可以应用于对碳正离子稳定性的解释,碳游离基稳定性的解释,甲苯是邻对位定位基的解释,羰基活性的解释等。
共轭效应

离域现象H2C=CH2,π键的两个π电子的运动范围局限在两个碳原子之间,这叫做定域运动。
共轭效应CH2=CH-CH=CH2中,可以看作两个孤立的双键重合在一起,π电子的运动范围不再局限在两个碳原子之间,而是扩充到四个碳原子之间,这叫做离域现象。
共轭效应这种分子叫共轭分子。
共轭分子中任何一个原子受到外界试剂的作用,其它部分可以马上受到影响。
这种电子通过共轭体系的传递方式,叫做共轭效应。
特点沿共轭体系传递不受距离的限制。
共轭效应,由于形成共轭π键而引起的分子性质的改变叫做共轭效应。
共轭效应主要表现在两个方面。
电子效应的一种。
组成共轭体系的原子处于同一平面,共轭体系的p电子,不只局限于两个原子之间运动,而是发生离域作用,使共轭体系的分子产生一系列特征,如分子内能低、稳定性高、键长趋于平均化,以及在外电场影响下共轭分子链发生极性交替现象和引起分子其他某些性质的变化,这些变化通常称为共轭效应。
共共轭效应轭效应是指在共轭体系中电子离域的一种效应是有机化学中一种重要的电子效应.它能使分子中电子云密度的分布发生改变(共平面化),内能减少,键长趋于平均化,折射率升高,整个分子更趋稳定。
编辑本段基本介绍“共轭效应是稳定的”是有机化学的最最基本原理之一.但是,自30年代起,键长平均化,4N+2芳香性理论,苯共轭效应环D6h构架的起因,分子的构象和共轭效应的因果关系,π-电子离域的结构效应等已经受到了广泛的质疑.其中,最引人注目的是Vollhardt等合成了中心苯环具有环己三烯几何特征的亚苯类化合物,Stanger等合成了键长平均化,但长度在0.143~0.148nm的苯并类衍生物.最近(1999年),Stanger又获得了在苯环中具有单键键长的苯并类化合物.在理论计算领域,争论主要表现在计算方法上,集中在如何将作用能分解成π和σ两部分.随着论战的发展,作用能分解法在有机化学中的应用不断地发展和完善,Hückel理论在有机化学中的绝对权威也受到了挑战.为此,简要地介绍了能量分解法的发展史,对Kollma法的合理性提出了质疑.此外特别介绍了我们新的能量分解法,及在共轭效应和芳香性的研究中的新观点和新的思维模式。
电子效应

CH2 CH CH CH2 4个 C 原子都是 sp2 杂化,
C-Cσ键: sp2–sp2 交盖, C-Hσ键: sp2–1s 交盖,
所有的原子共平面。 键角:120°。
1,3–丁二烯的
结构示意图
定域键
离域键
第5页
p 轨道
1,3–丁二烯的分子轨道
第6页
(1)共轭体系的分类
① π,π-共轭
第11页
(3) 推电子和吸电子共轭效应
推电子共轭效应(+C) :
若有p电子朝着双键方向移动,则为推电子+C.
X CCCC
吸电子共轭效应(-C):
推电子共轭效应用+C表示
电负性强的元素吸引电子,使共轭体系的电子云 向该元素偏移,呈吸电子共轭效应.
CCCO
吸电子共轭效应用-C表示
第12页
小结
A.共轭效应产生的条件:
第26页
(4)共振式的应用
比较物质的稳定性 预测反应的进行(产物有几种可能)
第27页
(1)共振论的基本概念
共振论是鲍林(L.Pauling)于20世纪30年代提出。
共振论认为:不能用经典结构式圆满表示其结构 的分子,其真实结构是由多种可能的经典极限式叠 加(共振杂化)而成的。
必须明确指出:真正的杂化体是一个单一的物质,决
不是几个极限式的混合物。
真实分子的能量比每一个共振极限式的能量都要低。 如共振杂化体由几个等同的经典结构式组成,则真实分 子的能量往往特别低,分子也就越稳定。
δ+
δ-
CH2 CH2 CH2
Cl
3
2
1
δ+δ-
Y--- C
C---H
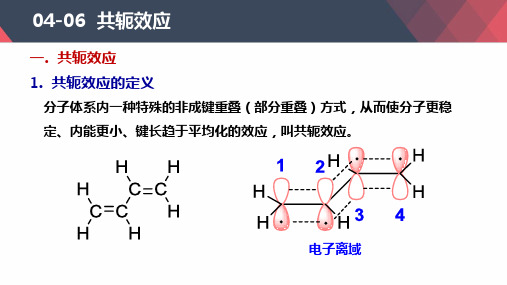
共轭效应
4
04-06 共轭效应
三. 共轭效应在有机化学中的应用
判断或解释有机反应活性中间体的稳定性
碳正离子、碳负离子、自由基、不同取代的烯烃
例如:比较下列烯烃的稳定性
>
12个σ-π 超共轭 9个σ-π 超共轭
>
6个σ-π 超共轭Βιβλιοθήκη 504-06 共轭效应
例如:比较下列碳正离子的稳定性
>
p-π共轭
>
σ-p超共轭 6个C-H
04-06 共轭效应
二. 超共轭效应
1. 含义及分类
含义:一种特殊的共轭(-、-p) -超共轭效应: 键与C-H 键共轭产生的电子离域效应。
-p超共轭效应:C-H 键与p轨道共轭产生的电子离域效应。
-超共轭效应
-p超共轭效应
04-06 共轭效应
2. 产生的原因 原因:H原子体积小,C—H键电子云的形状及大小与碳原子的p轨 道相差不大,且近似平行,易与邻位的或p电子发生相互作用,形 成-、-p共轭体系。 3. 超共轭效应的特征 超共轭效应比共轭效应弱得多; 在超共轭效应中, 键一般是给电子的, C-H键越多超共轭效应越大。 -CH3 > -CH2R > - CHR2 > -CR3
>
σ-p超共轭 3个C-H
>
无共轭
σ-p超共轭 9个C-H
6
04-06 共轭效应
一. 共轭效应
1. 共轭效应的定义
分子体系内一种特殊的非成键重叠(部分重叠)方式,从而使分子更稳
定、内能更小、键长趋于平均化的效应,叫共轭效应。
电子离域
04-06 共轭效应
2. 共轭效应的分类 π- π p- π
有机化学电子效应

六、电子效应
1共轭效应:单双键交替出现的体系称为共轭体系。
在共轭体系中,由于原子间的相互影响而使体系内的π电子(或P电子)分布发生变化的一种电子效应称为共轭效应。
凡共轭体系上的取代基能降低体系的π电子密度,则这些基团有吸电子的共轭效应,用-C表示。
凡共轭体系上的取代基能增高共轭体系的π电子云密度,则这些基团有给电子的共轭效应,用+C表示。
共轭效应只能在共轭体系中传递,但无论共轭体系有多大,共轭效应能贯穿于整个共轭体系中。
2场效应:取代基在空间可以产生一个电场,对另一头的反应中心有影响,这种空间的静电作用称为场效应,
3诱导效应:因分子中原子或基团的极性(电负性)不同而引起成键电子云沿着原子链向某一方向移动的效应称为诱导效应。
诱导效应的电子云是沿着原子链传递的,其作用随着距离的增长迅速下降,一般只考虑三根键的影响。
诱导效应一般以氢为比较标准,如果取代基的吸电子能力比氢强,则称其具有吸电子诱导作用,用-I表示。
如果取代基的给电子能力比氢强,则称其具有给电子诱导效应,用+I表示。
4超共轭效应:当C-H σ键与π键(或P轨道)处于共轭位置时,也会产生电子的离域现象,这种C-H键σ-电子的离域现象叫做超共轭效应。
在超共轭体系中电子转移的趋向可用弧形箭头表示:超共轭效应的大小,与p轨道或π轨道相邻碳上的C-H键多少有关,C-H键愈多,超共轭效应愈大。
3-2 卤代反应选择性——共轭效应和超共轭效应
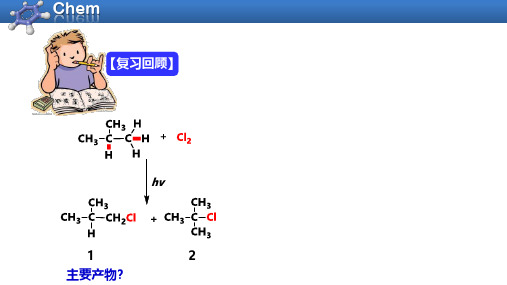
【复习回顾】12主要产物?内容:学习目标:区域选择性和化学选择性学会用超共轭效应和共轭效应来判断自由基稳定性反应活性-选择性原理烷基自由基的稳定性3区域选择性(regioselectivity )和化学选择性(chemoselectivity )1)区域选择性——优先对同一化合物中某个位置的相同化学键发生化学反应1期望值90%10%实验值64%36%期望值75%25%实验值43% 57%2)化学选择性——在一定反应条件下,优先对底物分子中某一化学键起化学反应烯丙基氢苄基基氢N-溴代琥珀酰亚胺(NBS)(1 -溴代四氢吡咯2,5-二酮)(1-bromopyrrolidine-2 ,5-dione)NBS自由基溴代反应机理1. 链引发2. 链增长3)氢原子的相对反应活性设伯氢的反应活性为1,仲氢的反应活性为X,叔氢的反应活性为Y,烯丙基氢(苄基氢)Z:57﹕2X=43﹕6X=436﹕Y=64﹕9Y=5.0680﹕2Z=20﹕3Z=6相对反应活性1o H﹕2o H﹕3o H﹕烯丙基氢(苄基)=1﹕4﹕5.06﹕6烷烃卤代反应中各种氢原子的反应活性顺序为:烯丙基氢(包括苄基氢)>3o H>2o H>1o H>CH47不同碳氢键的键能反应活性中间体的稳定性为什么烷烃卤代反应的氢原子反应活性是烯丙基氢(包括苄基氢)>3o H>2o H>1o H>CH 4?2烷基自由基的稳定性烯丙基氢CH 2=CHCH 2—H 苄基氢PhCH 2—H 1o H CH 3CH 2CH 2—H 2o H (CH 3)2CH —H 3o H (CH 3)3C —H BDE=423 kJ/mol BDE=413 kJ/mol BDE=404 kJ/mol 1)不同C-H 的解离能BDE=376 kJ/mol CH 3—H BDE=439.5 KJ/mol烯丙基自由基苄基自由基BDE=372 kJ/mol2)超共轭效应(hyperconjugation)定义:C -H 键的σ电子的离域效应Robert S. Mulliken (1896-1986)美国化学家1966年获奖Further Reading :Mulliken, R. S. J. Chem. Phys. 1939, 7, 339.大学化学. 2017, 32 (1), 84.σ-π超共轭特点:a)只存在C-H σ键♦强度:直接连接的C-H 键越多,超共轭效应越大 表示:Further Reading :钟成. 化学教育,2018, 39(12): 19.b) 给电子效应无键共振3)共轭效应(conjugation)——C效应定义:在共轭体系内由于原子的相互影响使体系内的π电子或p 轨道电子发生分布发生变化的一种电子效应π-π共轭丙烯醛C=C双键C=O双键3)共轭效应(conjugation)——C效应定义:在共轭体系内由于原子的相互影响使体系内的π电子或p轨道电子发生分布发生变化的一种电子效应π-π共轭p-π共轭乙烯基甲醚3)共轭效应(conjugation)——C效应定义:在共轭体系内由于原子的相互影响使体系内的π电子或p轨道电子发生分布发生变化的一种电子效应烯丙基自由基烯丙基碳正离子p-π共轭p-π共轭特点:a)通过π电子或p轨道孤对电子传递b)长程的c)贯穿整个共轭体系 表示:用弯箭头表示电子的离域价键理论共轭(conjugation)共振(resonance)电子离域电子离域π-π共轭和p-π共轭π-π共轭和p-π共轭都可写出共振式应用范围有局限应用范围比共轭广共轭效应分类甲氧基给电子共轭效应羰基吸电子共轭效应a)吸电子的共轭效应为-C. 如:-N O 2,-C N, -C OOH, -C HO,-C OR, -C O O R ,-C O N HR ,b) 给电子的共轭效应为+C.如:-N H 2(R),-N HCOR,-O H,-O R, -O COR. X 2(卤素)共轭效应强度a) 同周期原子(-C )-=O > -=N R > -=C H 2b )同主族原子(+C )-F> -Cl > -Br > -I(+C )-N R 2>-O R>-Fc)相同原子带更多电正性有更强的-C ,带更多电负性有更强的+C-C=N R>-C=N R+(-C )--O >-O R>-O R+(+C )-O R>-S R诱导效应vs 共轭效应和超共轭效应电子效应种类诱导效应共轭效应超共轭效应产生原因电负性离域效应离域效应适应范围所有分子共轭体系C-H键和共轭键相邻体系电子传递σ键π键σ键传递程度三键内长程短程电子效应给电子和吸电子给电子和吸电子给电子相对强弱弱强中等共轭效应和超共轭效应的相对强弱π-π共轭p-π共轭σ-π超共轭σ-p超共轭4)烷基自由基的稳定性sp3杂化sp2杂化o1o碳自由基甲基自由基更稳定诱导效应碳自由基sp 2杂化sp 3杂化超共轭效应σ-p 超共轭σ-p超共轭5)烯丙基和苄基自由基的稳定性共振式烯丙基自由基苄基自由基26p-π共轭···σ-p 超共轭共轭效应乙烯基自由基3反应活性-选择性原理(The reactivity-Selectivity Principle)溴代反应的选择性为什么比氯代反应高?卤素反应活性:F 2>Cl 2>Br 2>I 21)反应活性-选择性原理: 进攻试剂越活泼,反应的选择性越差Mayr H. , Ofial A. R. Angew. Chem. Int. Ed. 2006, 45, 1844•X + CH 3-H •CH 3+ H-XF Cl Br I568.2431.8366.1298.3-128.9+7.5+73.2+141H (kJ/mol)Ea (kJ/mol)+4.2+16.7+75.3> +141439.3439.3439.3439.3反应过程能量甲烷自由基卤代反应能量变化中间体能量增加能量减少过渡态反应过程能量甲烷自由基卤代反应能量变化中间体过渡态♦活化能E a :发生化学反应所需最低能量(反应物能量与过渡态能量之差))中间体:发生化学反应的中间产物,一般为碳正离子、碳负离子、自由基等2)如何看能量线图 过渡态:发生化学反应经过的能量最高中间状态,过渡态旧键未完全断裂,新键未完全形成反应过程能量甲烷自由基卤代反应能量变化中间体过渡态E a 1=16.7 KJ/molE a 2=8.3KJ/mol反应物阻力大阻力小反应过程甲烷自由基卤代反应能量变化中间体过渡态反应物E a 1=16.7 KJ/molE a 2=8.3KJ/mol能量♦活化能E a :发生化学反应所需最低能量(反应物能量与过渡态能量之差)) 中间体:发生化学反应的中间产物,一般为碳正离子、碳负离子、自由基等2)如何看能量线图❶过渡态:发生化学反应经过的能量最高中间状态,过渡态旧键未完全断裂,新键未完全形成❹反应热∆H :化学反应中吸收或放出的热量(反应物与产物能量之差)反应过程甲烷自由基卤代反应能量变化中间体过渡态反应物E a 1=16.7 KJ/molE a 2=8.3KJ/mol△H=-110kJ/mol△H=-101kJ/mol产物能量能量接近的有关物种结构也相似,过渡态的结构与相隔最近的稳定物种结构类似。
超共轭效应名词解释

超共轭效应名词解释
嘿,你知道超共轭效应吗?这玩意儿可神奇啦!就好像一群小伙伴
手拉手一起发挥作用一样。
比如说,在有机化学里呀,超共轭效应就像是一场无声的协作。
拿
烯烃来说吧,那碳氢键和碳碳双键之间,就存在着这种奇妙的超共轭
效应呢!你想想看,这不就像是一群小伙伴相互配合,让整个体系变
得更加稳定嘛!
再比如烷烃里,碳氢键和碳碳单键之间也有这种效应在起作用。
它
可不是那种轰轰烈烈的大变化,而是悄然地在背后助力,让整个分子
的性质都有所不同哦!
“哎呀,这超共轭效应到底是怎么一回事呀?”你可能会这么问。
嘿嘿,简单来说,它就是电子的一种微妙转移和共享。
就好比大家一起
做一件事,每个人都出一点力,最后事情就变得更容易完成啦!
在化学反应中,超共轭效应的影响可不小呢!它能改变反应的速率、选择性等等。
就好像是给化学反应这辆车加了一把力,让它跑得更快
或者跑得更稳。
想象一下,如果没有超共轭效应,那有机化学的世界会变得多么不
一样呀!很多反应可能就不会那么顺利地进行,很多化合物的性质也
会大相径庭。
所以呀,超共轭效应真的是超级重要的呢!它就像一个隐藏在化学世界里的小魔法,默默地发挥着它的作用。
你现在是不是对超共轭效应有了更清楚的认识啦?反正我是觉得它超级有趣又超级重要的!。
《有机化学》理论知识要点归纳

《有机化学》理论知识要点归纳一.有关“吸电子基和给(推)电子基”问题从极性、诱导效应、共轭效应等方面考虑,一般情况下,电子云密度大的为给电子基,极性大的为吸电子基。
例如碳碳双键、苯基等为给电子基,卤素原子、-CN 、硝基等为吸电子基。
取代基如果是像-NO 2(-SO 3H 、-COOH 、-CHO )这样的,就是与碳相连的元素的原子比氧的电负性弱(就是该元素原子得电子的能力没有氧强的时候,该元素原子的电负性比氧弱)而且还连有氧的时候,就是吸电子基,因为氧把那些元素原子的电子云向氧的一方吸引,使得那些元素把苯环上的电子向它们吸引,导致苯环的电子密度降低,因为苯上的取代反应都是自由基反应,自由基有单电子,苯环的电子密度降低自然使苯不容易放出氢自由基(就是氢原子),使得苯环钝化。
卤素具有吸电子的诱导效应,从而降低碳正离子的稳定性。
这一效应在苯环上各个住置受到进攻时都有体现,但在卤素的邻、对位受到进攻时更为显著。
二.有机反应试剂的分类1.自由基试剂:自由基:由共价键均裂所产生的带有独电子的中性基团。
自由基试剂:能产生自由基的试剂是自由基试剂。
例如:CH 4CH 3 Cl+ HClh νCl 2(氯自由基)2Cl 光或热R O O R2 RO常见的自由基试剂:X 2、过氧化物(R -O -O -R )、偶氮化物(R -N =N -R )等,高温、光照等条件也可引发自由基反应。
因自由基带有未共用电子,所以性质活泼,可引发自由基型反应。
2.亲电试剂在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对,并与之共有形成化学键,这种试剂称做亲电试剂。
亲电试剂是缺电子的试剂。
例如:RCH 2Cl + AlCl 3R +CH 2AlCl 4-亲电试剂常见的亲电试剂有:①正离子,如H +,C +,Cl +、Br +、I +,NO 2+等;②可接收孤对电子的分子,如如AlCl 3、FeCl 3、ZnCl 2、SnCl 4、SbCl 3、BF 3等Lewis 酸;③羰基碳原子等。
超共轭效应场效应空间效应

场效应和诱导效应
它们通常难以区分,往往同时存在而且作用方向 一致,实际上场效应是诱导效应的一种表现形式, 所以也把场效应和诱导效应总称为极性效应。但在 某些场合场效应与诱导效应的方向相反,从而显示 出场效应的明显作用。
例如:邻氯苯基丙炔酸的酸性比氯在间位或对位的小。
C C COOH Cl
C C COOH
(Isopropyl)
(CH3)3C-
(t-Butyl)
1.0
SN2 反应
0.28
0.03
乙氧基从背后进攻
4.2× 10-5
R越大,位阻越大
13
卤代烷在乙醇解的SN2反应中,随着R体积的大小不同, 对乙氧基从背面进攻的难易,由于空间阻碍不同而反应 速度各异。
[例2] SN1反应 P51表2-15
R
RC X R 109° 28'
sp3-四面体
R
120°
C +X RR
sp2-平面三角型
SN1反应 形成正碳离子的 一步 键角的变化
缓解了基团的 拥挤程度
来自于离去基团背后的张力-B-张力 (back strain)
14
张力对反应活性的影响
当胺同质子酸作用时,其碱性强度顺序为:
R3N > R2NH > RNH2 > NH3
看出。
叔丁苯 异丙苯 乙苯 甲苯
μ(D) 0.70
0.65
0.58
0.38
1
进行苯环上的硝化反应和卤代反应时,得到的结果却 恰恰相反。
溴化 硝化
CH3 CH3CH2 340 290 14.8 14.3
(CH3)2CH180 12.9
(CH3)3C110 10.8
共轭效应_超共轭效应

3.4.1.1共轭效应、超共轭效应影响有机化合物结构及反应性的因素⏹立体效应⏹电子效应◆诱导效应◆共轭效应◆超共轭效应◆……-70.5 kcal/mole -54.1 kcal/mole -60.8 kcal/mole 一些事实一些事实“共轭效应”通常:C -C 154.0 pmC =C 134.0 pm共轭效应的含义:共轭分子体系的一种特殊的非成键重叠(部分重叠)方式,从而使分子更稳定、内能更小、键长趋于平均化的效应。
电子离域分类:1. 按非成键重叠电子云的类型:π-πp-π2. 按共轭体系所含电子情况:等电子共轭多电子共轭缺电子共轭传递:沿共轭链减弱程度小共轭效应的强度吸电子共轭效应能降低共轭体系的π密度的基团具有“吸电子共轭效应”—NO2, —CN, —COOH, —CHO, —COR等可降低体系的π电子云密度的取代基同一周期:电负性同一族:主量子数同周期:=O > =NR > =CR 2同族:=O > =S 能降低共轭体系的 密度的基团具有“吸电子共轭效应”吸电子共轭效应给电子共轭效应能增高共轭体系的π密度的基团具有“给电子共轭效应”—NH2, —NHCOR, —OH, —OR, —OCOR等可增高体系的π电子云密度的取代基同一周期:电负性同一族:主量子数-NR 2> -OR > -F 给电子共轭效应-O -> -OR能增高共轭体系的 密度的基团具有“给电子共轭效应”共轭体系的特性1. 几何特性:共平面性(参与共轭的原子处于同一平面)键长的平均化2. 电子特性:影响分子偶极矩极化度高3. 能量特性:体系能量降低4. 化学特性超共轭效应⏹含义:一种特殊的共轭(σ-π、σ-p)C-H σ键的电子和一个邻近的半满或全空的非键p轨道、全满的π轨道之间的相互作用,该相互作用能够使整个体系变得更稳定。
⏹原因:H原子体积小,C—H键电子云的形状及大小与碳原子的p轨道相差不大,且近似平行,易与邻位的π或p电子发生相互作用,形成σ-π、σ-p共轭体系。
共轭效应

共轭效应共轭效应(conjugated effect) ,又称离域效应,是指共轭体系中由于原子间的相互影响而使体系内的π电子(或p电子)分布发生变化的一种电子效应。
凡共轭体系上的取代基能降低体系的π电子云密度,则这些基团有吸电子共轭效应,用-C表示,如-COOH,-CHO,-COR;凡共轭体系上的取代基能增高共轭体系的π电子云密度,则这些基团有给电子共轭效应,用+C表示,如-NH2,-OH,-R。
1离域现象共轭效应H2C=CH2,π键的两个π电子的运动范围局限在两个碳原子之间,这叫做定域运动。
CH2=CH-CH=CH2中,可以看作两个孤立的双键重合在一起,π电子的运动范围不再局限在两个碳原子之间,而是扩充到四个碳原子之间,这叫做离域现象。
如图,这种分子叫共轭分子。
共轭分子中任何一个原子受到外界试剂的作用,其它部分可以马上受到影响。
这种电子通过共轭体系的传递方式,叫做共轭效应。
2特点沿共轭体系传递不受距离的限制。
共轭效应,由于形成共轭π键而引起的分子性质的改变叫做共轭效应。
共轭效应主要表现在两个方面。
①共轭能:形成共轭π键的结果使体系的能量降低,分子稳定。
例如CH2=CH—CH=CH2共轭分子,由于π键与π键的相互作用,使分子的总能量降低了,也就是说, CH2=CH—CH=CH2分子的能量比两个不共轭的CH2=CH2分子的能量总和要低。
所低的数值叫做共轭能。
②键长:从电子云的观点来看,在给定的原子间,电子云重叠得越多,电子云密度越大,两个原子结合得就越牢固,键长也就越短,共轭π键的生成使得电子云的分布趋向平均化,导致共轭分子中单键的键长缩短,双键的键长加长。
共轭效应共轭效应是电子效应的一种。
组成共轭体系的原子处于同一平面,共轭体系的p电子,不只局限于两个原子之间运动,而是发生离域作用,使共轭体系的分子产生一系列特征,如分子内能低、稳定性高、键长趋于平均化,以及在外电场影响下共轭分子链发生极性交替现象和引起分子其他某些性质的变化,这些变化通常称为共轭效应。
高等有机化学相关基本理论

整个电荷的转移和价态的变化;
O
O
C l C H 2 C O H H 3 C C H 2C O H
-I,酸性增加
+I,酸性降低
(2)诱导效应沿键链迅速减小,其影响一般在三个 原子内起作用;
(3)传递方向具有单一性。
不同取代基的吸电子能力:
NR3>_NO2>_CN>_COOH>_COOR>_C=O> _F>_Cl>_Br>_I > _OCH3>_OH>_C6H5>_CH=CH2>_H
SN2反应,乙氧基从 背面进攻 R基团越大,位阻越大
4. 对反应产物的影响
• 共轭效应中的空间因素亦能影响自由基反应及 其产物。如邻异丙基甲苯的自由基氧化生成邻异 丙基苯甲酸,而不是生成邻甲基苯甲酸,这是一 个合成邻异丙基苯甲酸的好方法:
O
O-0.5
R COH
RC
+ H+
而醇羟基中无共轭效应,其酸性极弱
O-0.5
胺的碱性降低
NH2
O R CNH2
2. 加成方向
δ +δ C H 3C H C H 2 + H + X -
X C H 3 C + H 2 C H 3 X - C H 3 C H C H 3
甲基的+C 和+I效应,烯键末端具有亲核性, 反应为亲电加成反应。
+++
C C Cl
+
CH3
Cl
供电诱导效应(+I): 电负 性比氢小的原子与碳相
连引起的诱导效应
CH3
+
MgBr
R3C H I=0 标准
超共轭

只要是两个不饱和键通过一个单键相连,就可以形成π-π共轭体系。
单键仅仅一个,可以旋转,使两个π键平行,形成大π键的离域。
例如:CH2=CH-CH=CH2 (双键和双键形成的π-π共轭体系)CH2=CH-CH=O 碳碳双键和碳氧双键形成的π-π共轭体系CH2=CH-C≡N碳碳双键和碳氮三键形成的π-π共轭体系共轭效应:电子离域,能量降低,分子趋于稳定,键长平均化。
如果与π键相连的某一原子,具有一个与π键相平行的p轨道(包括全满,半满及全空轨道),形成p-π共轭。
例如:CH2=CH-O-CH3; O 有平行的p轨道eCH2=CH-N-CH3; N 有p轨道eCH2=CH-Cl Cl有p轨道e超共轭效应是由σ(C sp3-H1s)键参与的共轭效应,其中的C必须是sp3杂化。
分为σ-π超共轭和σ-p超共轭:σ-π超共轭:CH3C≡CCH3形成6个σ-π超共轭CH2=CH-CH3形成3个σ-π超共轭σ-p超共轭:(CH3)3C+形成9个σ-p超共轭CH3CH2+ 形成3个σ-p超共轭超共轭体系,比共轭体系作用弱,稳定性差,共轭能小. 由于重叠很少,才叫做”超共轭“,这里的“超”是指很小,很少,一点点的意思当然,在分子中形成的超共轭键数量越多,那么分子越稳定,因为重合的越多,键越不容易被打断。
一个基团是给电子+C还是吸电子–C?有人总结了一个简单的办法:对于一个基团-RX, 如果R的电负性大于X, 那么就是给电子的,如:C的电负性大于H,所以烷基-CH3给电子O的电负性大于C 、H,所以-OH、烷氧基-OCH3都是给电子的;硝基-NO2、-COOH、羰基、-CHO、酯基、氰根,因为N<O, C<O,所以都是吸电子基团。
共轭效应

C C F
C C Cl C C Br C C I
同族元素:电负性越大的电子,+C 效应越小
C C NR2 > C C OH > C C F
与杂原子相连的正碳离子p- π共轭结构:
氧上未共有电子对所 占 p 轨道 与中心碳原子上的空的 p轨道 侧面交盖,得到p- π共轭
CH3 O
CH2
CH3O
CH2
B对醌、循环式极化
在对子吸收光谱的分析后,在芳香族化合 物中,有循环式和对醌两种共轭极化式。
N O Me O
N OMe
O
Me2 N
N
O
Me2 N
N
O
多联苯系列直来联苯系列
...
...
间位和邻位多苯系列
...
...
C、并苯式极化
• 直链多并苯系列与直多并苯系列由对醌式共轭 极化产生的 • 并苯式极化是指各苯环的对醌式极化可以通过 侧并的苯环而传递,不限与直并的苯环。
类似地,羰基正离子:
R C O
R C
O
2.2.3 应用实例
a.苯酚分子中氧原子上的孤对电子与 苯环上的π电子形成 p- π共轭。 结果: 使羟基的邻、对位的碳原子 带有部分的负电荷。
δ
OH
δ δ
O R C OH
O R C O+ H
C C C Y
(I)
C C X
(II)
π电子转移用弧形 箭头表示
Y为吸电子基团时-吸电子共轭效应 (-C), X为供电子基团时-供电子共轭效应 (+C).
b动态:暂时的,被动的受外界因素的影响
-
+
CH2
CH
CH
第三章 烯烃2

气相 500-600℃
CH2BrCH=CH2
500-600℃
2Br
Br + CH3CH=CH2
CH2CH=CH2 + HBr
CH2CH=CH2 + Br2
CH2BrCH=CH2 + Br
注意
1* 低温、液相发生加成,而高温、气相发生取代。
2* 有些不对称烯烃反应时,经常得到混合物。 CH3CH2CH2CH=CH2 Cl2 高温
+
Nu
-
Nu C C E
fast
反应分两步进行:
第一步,亲电试剂对双键进攻形成碳正离子 。 第二步,亲核试剂与碳正离子中间体结合, 形成加成产物。
控制整个反应速率的第一步反应由亲电试剂 进攻而引起,故称为亲电加成反应。
1、加HX
R—CH = CH2 + HX
R—CH CH3
X
不对称烯烃与不对称试剂加成时,带负电的部 分总是加到含H较少的双键碳原子上。这个经
CH3CH2CHClCH=CH2 + CH3CH2CH=CHCH2Cl
CH3CH2CHCH=CH2
CH3CH2CH=CHCH2
CH3CH2CH
CH
CH2
2. NBS法(烯丙位的溴化) 反应式
O
Br
(C6H5COO)2
O
+
NBr O
CCl4 , ∆
+
NH O
NBS
N-溴代丁二酰亚胺
作业 P70: 3.(2, 3, 4, 6, 9)
2、加 X2
反应式:
C C
+ X2
C C X X
(CH3)2CHCH=CHCH3 + Br2 (CH3)2CHCHBrCHBrCH3
共轭效应与超共轭效应的定义及特点

1.共轭效应与超共轭效应的定义及特点共轭效应不饱和的化合物中,有三个或三个以上互相平行的p轨道形成大π键,这种体系称为共轭体系.共轭体系中,π电子云扩展到整个体系的现象称为电子离域或离域键.共轭效应:电子离域,能量降低,分子趋于稳定,键长平均化等现象称为共轭效应,也叫做C效应共轭效应的结构特点:共轭体系的特征是各σ键在同一平面内,参加共轭的p轨道轴互相平行,且垂直于σ键在的平面,相邻p轨道间从侧面重叠发生键离域.共轭效应与诱导效应相比还有一个特点是沿共轭体系传递不受距离的限制.超共轭效应烷基上C原子与极小的氢原子结合,由于电子云的屏蔽效力很小,所以这些电子比较容易与邻近的π电子(或p电子)发生电子的离域作用,这种涉及到σ轨道的离域作用的效应叫超共轭效应.超共轭体系,比共轭体系作用弱,稳定性差,共轭能小.2.共轭效应共轭的类型2.1.1 π-π共轭通过形成π键的p轨道间相互重叠而导致π电子离域作用称为π-π共轭.参加共轭的原子数目等于离域的电子总数,又称为等电子共轭.我们可以简单地概括为双键,单键相间的共轭就是π-π共轭.例如:共轭体系的分子骨架称做共轭链.2.1.2 p-π共轭体系通过未成键的p轨道(包括全满,半满及全空轨道)与形成π键的p轨道的重叠而导致的电子离域作用,称为p-π共轭.包括富电子,足电子,缺电子三种p-π共轭类型.我们也可以简单地理解为:双键相连的原子上的p轨道与π键的p轨道形成的共轭即为p-π共轭.例如:共轭方向及强弱判断共轭效应的方向及强弱直接影响物质的性质和稳定性,因此共轭方向及强弱的判断也就有着非常重要的作用.能够给出电子的称给电子共轭,用符号+C表示.相反,能接受电子的称吸电子共轭,用符号-C表示.卤素,羟基,氨基,碳负离子等与双键直接相连时,X. O. N .C等原子的孤对电子对与π键共轭.由于是由一个原子向共轭体系提供两个电子,相当于使π电子密度增大,所以有给出电子的能力,称为+C效应.一般富电子p-π共轭都属于给电子共轭.例如:中的都是+C效应.当参与共轭的O. N 只提供一个电子,而本身电负性大于C原子,所以有使共轭体系电子向O. N 转移的能力,因此有-C效应.电负性大于C的原子参与的等电子共轭是吸电子共轭.例如:都是-C效应.大多数共轭效应是由碳的2p轨道与其他原子的p轨道重叠所产生的,当某原子参与共轭的p轨道的形状大小,能量与碳的2p轨道越接近时,轨道重叠越,离域越易,共轭作用越强.即共轭效应的强弱与参与共轭的原子轨道的主量子数有关.n=2时有强的共轭,n>2有弱的共轭,n越大共轭越弱.另外,元素的电负性越小,越容易给出电子,有较强的+C效应.相反,元素的电负性越大,越容易吸引电子,有较强的-C效应.因此共轭效应也有周期性变化.同一类元素随n值增大,共轭减弱;同一周期n值相同,随原子序数增大,电负性增大,给电子共轭效应减弱;吸电子共轭主要有电负性决定,电负性越大,吸电子共轭越强.3. 超共轭效应超共轭效应视其电子电子转移作用分为σ-π.σ-p .σ-σ几种,以σ-π最为常见.σ-π超共轭丙烯分子中的甲基可绕C—Cσ键旋转,旋转到某一角度时,甲基中的C-Hσ键与C=C的π键在同一平面内,C-Hσ键轴与π键p轨道近似平行,形成σ-π共轭体系,称为σ-π超共轭体系.在研究有机反应时有着重要的应用,在学习不对称烯烃的HX加成反应时,我们以C正离子形成的稳定性来解释马尔科夫尼科夫规则,若应用σ-π超共轭效应,则不仅说明甲基是推电子的,同时加深了对这一经验规则的深入理解.再如,不饱和烯烃的a-H的特殊活泼性也可以用σ-π超共轭效应来理解.丙烯的甲基比丙烷的甲基活泼的多,在液氨中丙烯中甲基的H易被取代,丙烷中甲基的H不易被取代.σ-p超共轭当烷基与正离子或游离基相连时,C-H上电子云可以离域到空的p空轨道或有单个电子的p轨道上,使正电荷和单电子得到分散,从而体系趋于稳定,称做σ-p超共轭体系.简单的说就是C-H的σ键轨道与p轨道形成的共轭体系称做σ-p超共轭体系.如乙基碳正离子即为σ-p超共轭体系.参加σ-p超共轭的C-H数目越多,正电荷越容易分散,C正离子就越稳定.应用超共轭效应的应用也很广泛,可以应用于对碳正离子稳定性的解释,碳游离基稳定性的解释,甲苯是邻对位定位基的解释,羰基活性的解释等.。
有机化学课后习题答案第二章

2章思考题2.1 分析共轭效应和超共轭效应的异同点,重点阐述σ-π和p-π共轭。
2.2 请举例说明同分异构体中各种异构体的定义及其异同点。
2.3解释甲烷氯化反应中观察到的现象:(1)(1)甲烷和氯气的混合物于室温下在黑暗中可以长期保存而不起反应。
(2)(2)将氯气先用光照射,然后迅速在黑暗中与甲烷混合,可以得到氯化产物。
(3)(3)将氯气用光照射后在黑暗中放一段时期,再与甲烷混合,不发生氯化反应。
(4)(4)将甲烷先用光照射后,在黑暗中与氯气混合,不发生氯化反应。
(5)(5)甲烷和氯气在光照下起反应时,每吸收一个光子产生许多氯化甲烷分子。
2.4 3-氯-1,2-二溴丙烷是一种杀根瘤线虫的农药,试问用什么原料,怎样合成?2.5 写出烯烃C5H10的所有同分异构体,命名之,并指出哪些有顺反异构体。
2.6 找出下列化合物的对称中心.(1)乙烷的交叉式构象(2)丁烷的反交叉式构象(3)反-1,4-二甲基环已烷(椅式构象)(4)写出1,2,3,4,5,6-六氯环已烷有对称中心的异构体的构象式(椅式)。
2.7 一个化合物的氯仿溶液的旋光度为+10o, 如果把溶液稀释一倍, 其旋光度是多少? 如化合物的旋光度为-350o, 溶液稀释一倍后旋光度是多少?2.8 乙烯、丙烯、异丁烯在酸催化下与水加成,生成的活性中间体分别为、、,其稳定性>>, 所以反应速度是>>。
解答2.1 答:在离域体系中,键长趋于平均化,体系能量降低而使分子稳定性增加。
共轭体所表现出来的这种效应叫共轭效应。
共轭体系分为π-π共轭体系和p-π共轭体系。
超共轭效应是当C—H键与相邻的π键处于能重叠位置时,C—H键的轨道与π轨道也有一定程度的重叠,发生电子的离域现象,此时,键向π键提供电子,使体系稳定性提高。
它分为-p 和-π超共轭。
超共轭效应比共轭效应小。
2.3 答:(1)无引发剂自由基产生(2)光照射,产生Cl·,氯自由基非常活泼与甲烷立即反应。
有机化学理论知识要点归纳

《有机化学》理论知识要点归纳一.有关“吸电子基和给(推)电子基”问题从极性、诱导效应、共轭效应等方面考虑,一般情况下,电子云密度大的为给电子基,极性大的为吸电子基。
例如碳碳双键、苯基等为给电子基,卤素原子、-CN 、硝基等为吸电子基。
取代基如果是像-NO 2(-SO 3H 、-COOH 、-CHO )这样的,就是与碳相连的元素的原子比氧的电负性弱(就是该元素原子得电子的能力没有氧强的时候,该元素原子的电负性比氧弱)而且还连有氧的时候,就是吸电子基,因为氧把那些元素原子的电子云向氧的一方吸引,使得那些元素把苯环上的电子向它们吸引,导致苯环的电子密度降低,因为苯上的取代反应都是自由基反应,自由基有单电子,苯环的电子密度降低自然使苯不容易放出氢自由基(就是氢原子),使得苯环钝化。
卤素具有吸电子的诱导效应,从而降低碳正离子的稳定性。
这一效应在苯环上各个住置受到进攻时都有体现,但在卤素的邻、对位受到进攻时更为显著。
二.有机反应试剂的分类1.自由基试剂:自由基:由共价键均裂所产生的带有独电子的中性基团。
自由基试剂:能产生自由基的试剂是自由基试剂。
例如:CH 4CH 3 Cl+ HClh νCl 2(氯自由基)2Cl 光或热R O O R2 RO常见的自由基试剂:X 2、过氧化物(R -O -O -R )、偶氮化物(R -N =N -R )等,高温、光照等条件也可引发自由基反应。
因自由基带有未共用电子,所以性质活泼,可引发自由基型反应。
2.亲电试剂在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对,并与之共有形成化学键,这种试剂称做亲电试剂。
亲电试剂是缺电子的试剂。
例如:RCH 2Cl + AlCl 3R+CH 2AlCl 4-亲电试剂常见的亲电试剂有:①正离子,如H +,C +,Cl +、Br +、I +,NO 2+等;②可接收孤对电子的分子,如如AlCl 3、FeCl 3、ZnCl 2、SnCl 4、SbCl 3、BF 3等Lewis 酸; ③羰基碳原子等。
共轭效应

0.133
0.154
H
H
??:nm
双键与乙烯相比,变长了;单键与乙烷相比,变短了。总的说 来,是键长趋于平均化了。
10
氢化热
孤立和共轭体系的氢化热:
C H 2 C HC H 2 C HC H 2+ 2H 2 C H 3 C H C HC HC H 2+ 2H 2 所 以 1 , 3 - 戊 二 烯 的 共 轭 能 是 2 8 K J / m o l
分子中,每个碳原子都以sp2轨 道相互重叠或与氢原子的1s轨 道重叠,形成三个C-Cσ键和六 个C-Hσ键。这些σ键都处在同 一个平面上,它们之间的夹角 都接近120°,此外每个碳原子 还剩下一个来参加杂化的与这 个平面垂直的p轨道。四个p轨 道的对称轴互相平行侧面互相 重叠,形成了包含四个碳原子 的四个电子的共轭体系。 更多…..
8
1,3-丁二烯特点
ⁿ ⑴碳碳单键键长相对缩短,单双键产生了平均化 ⁿ 随构造式CH2=CH-CH=CH2,但单双键的键长已相当
接近,同样体现在环状共轭体系中。如,苯环C-C键 长是完全相等的。 ⑵化合物的能量显著降低,稳定性明显增加。决定内 能大小方法之一就是测量氢化热,氢化热越低,分子 内能越低。
C 5 H 1 2 C 5 H 1 2
H = -2 5 4K J /m o l H = -2 2 6K J /m o l
从能量图可以看出,共轭 二烯烃比孤立二烯烃能量 低了254-226=28KJ/mol 这部分低出来的能量叫共轭 能或离域能。1,3-丁二烯 的共轭能为15kJ/mol。
共轭效应
(conjugative effect )
1
共轭效应的产生 共轭效应的类型
2
共轭效应的产生
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.共轭效应与超共轭效应的定义及特点
1.1 共轭效应
不饱和的化合物中,有三个或三个以上互相平行的p轨道形成大π键,这种体系称为共轭体系.共轭体系中,π电子云扩展到整个体系的现象称为电子离域或离域键.
共轭效应:电子离域,能量降低,分子趋于稳定,键长平均化等现象称为共轭效应,也叫做C效应
共轭效应的结构特点:共轭体系的特征是各σ键在同一平面内,参加共轭的p轨道轴互相平行,且垂直于σ键在的平面,相邻p轨道间从侧面重叠发生键离域.共轭效应与诱导效应相比还有一个特点是沿共轭体系传递不受距离的限制.
1.2 超共轭效应
烷基上C原子与极小的氢原子结合,由于电子云的屏蔽效力很小,所以这些电子比较容易与邻近的π电子(或p电子)发生电子的离域作用,这种涉及到
σ轨道的离域作用的效应叫超共轭效应.超共轭体系,比共轭体系作用弱,稳定性差,共轭能小.
2.共轭效应
2.1 共轭的类型
2.1.1 π-π共轭
通过形成π键的p轨道间相互重叠而导致π电子离域作用称为π-π共轭.参加共轭的原子数目等于离域的电子总数,又称为等电子共轭.我们可以简单地概括为双键,单键相间的共轭就是π-π共轭.例如: 共轭体系的分子骨架称做共轭链.
2.1.2 p-π共轭体系
通过未成键的p轨道(包括全满,半满及全空轨道)与形成π键的p轨道的重叠而导致的电子离域作用,称为p-π共轭.包括富电子,足电子,缺电子三种p-π共轭类型.我们也可以简单地理解为:双键相连的原子上的p轨道与π键的p轨道形成的共轭即为p-π共轭.例如:
2.2 共轭方向及强弱判断
共轭效应的方向及强弱直接影响物质的性质和稳定性,因此共轭方向及强弱的判断也就有着非常重要的作用.
能够给出电子的称给电子共轭,用符号+C表示.相反,能接受电子的称吸电子共轭,用符号-C表示.
卤素,羟基,氨基,碳负离子等与双键直接相连时,X. O. N .C等原子的孤对电子对与π键共轭.由于是由一个原子向共轭体系提供两个电子,相当于使π电子密度增大,所以有给出电子的能力,称为+C效应.一般富电子p-π共轭都属于给电子共轭.例如:
中的都是+C效应.
当参与共轭的O. N 只提供一个电子,而本身电负性大于C原子,所以有使共轭体系电子向O. N 转移的能力,因此有-C效应.电负性大于C的原子参与的等电子共轭是吸电子共轭.例如:
都是-C效应.
大多数共轭效应是由碳的2p轨道与其他原子的p轨道重叠所产生的,当某原子参与共轭的p轨道的形状大小,能量与碳的2p轨道越接近时,轨道重叠越,离域越易,共轭作用越强.即共轭效应的强弱与参与共轭的原子轨道的主量子数有关.n=2时有强的共轭,n>2有弱的共轭,n越大共轭越弱.另外,元素的电负性越小,越容
易给出电子,有较强的+C效应.相反,元素的电负性越大,越容易吸引电子,有较强的-C效应.因此共轭效应也有周期性变化.
同一类元素随n值增大,共轭减弱;同一周期n值相同,随原子序数增大,电负性增大,给电子共轭效应减弱;吸电子共轭主要有电负性决定,电负性越大,吸电子共轭越强.
3. 超共轭效应
超共轭效应视其电子电子转移作用分为σ-π.σ-p .σ-σ几种,以σ-π最为常见.
3.1 σ-π超共轭
丙烯分子中的甲基可绕C—Cσ键旋转,旋转到某一角度时,甲基中的C-Hσ键与C=C的π键在同一平面内,C-Hσ键轴与π键p轨道近似平行,形成σ-π共轭体系,称为σ-π超共轭体系.
在研究有机反应时有着重要的应用,在学习不对称烯烃的HX加成反应时,我们以C正离子形成的稳定性来解释马尔科夫尼科夫规则,若应用σ-π超共轭效应,则不仅说明甲基是推电子的,同时加深了对这一经验规则的深入理解.再如,不饱和烯烃的a-H的特殊活泼性也可以用σ-π超共轭效应来理解.丙烯的甲基比丙烷的甲基活泼的多,在液氨中丙烯中甲基的H易被取代,丙烷中甲基的H不易被取代.
3.2 σ-p超共轭
当烷基与正离子或游离基相连时,C-H上电子云可以离域到空的p空轨道或有单个电子的p轨道上,使正电荷和单电子得到分散,从而体系趋于稳定,称做σ-p超共轭体系.简单的说就是C-H的σ键轨道与p轨道形成的共轭体系称做σ-p超共轭体系.如乙基碳正离子即为σ-p超共轭体系.
参加σ-p超共轭的C-H数目越多,正电荷越容易分散,C正离子就越稳定.
3.3 应用
超共轭效应的应用也很广泛,可以应用于对碳正离子稳定性的解释,碳游离基稳定性的解释,甲苯是邻对位定位基的解释,羰基活性的解释等.。
