果胶的提取作业指导书
实验五十五果胶的提取
实验五十五 果胶的提取一、目的要求1. 了解果胶的性质和提取原理。
2. 掌握果胶的提取工艺。
3. 了解果胶在食品工业中的用途。
二、仪器药品圆底烧瓶、漏斗、吸滤瓶等0.3%盐酸溶液、1%氨水、95%乙醇、柑橘皮、活性炭等 三、实验原理果胶广泛存在于各类水果和蔬菜中。
例如苹果中的含量为0.7~1.5%,蔬菜南瓜中的果胶含量最多,达到7~17%。
其用途是用作酸性食品的胶凝剂、增稠剂等。
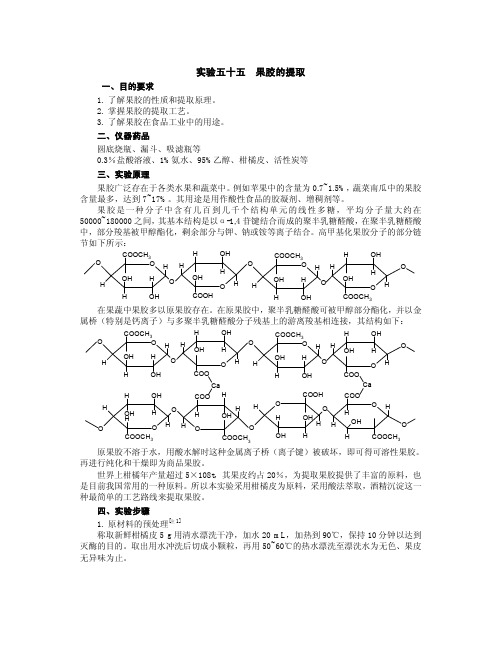
果胶是一种分子中含有几百到几千个结构单元的线性多糖,平均分子量大约在50000~180000之间,其基本结构是以α-1,4苷键结合而成的聚半乳糖醛酸,在聚半乳糖醛酸中,部分羧基被甲醇酯化,剩余部分与钾、钠或铵等离子结合。
高甲基化果胶分子的部分链节如下所示:HH OOH HCOOCH 3H OHOHH OOH HCOOCH 3H OO HOHOHOH H HCOOHO HOHOH OHH HCOOCH 3在果蔬中果胶多以原果胶存在。
在原果胶中,聚半乳糖醛酸可被甲醇部分酯化,并以金属桥(特别是钙离子)与多聚半乳糖醛酸分子残基上的游离羧基相连接,其结构如下:HH OOH H COOCH 3H OH OOHH OOH HCOOCH 3H OHOOHOOH HOHH HCOOHO OHHOH H HCOO H HOOH HCOOCH 3HH OH O HHOOHH OO COOHOH HH OH HCOOCOOCH 3HOHOHOHH HCOOOH COOCH 3CaCa原果胶不溶于水,用酸水解时这种金属离子桥(离子键)被破坏,即可得可溶性果胶。
再进行纯化和干燥即为商品果胶。
世界上柑橘年产量超过5×108t ,其果皮约占20%,为提取果胶提供了丰富的原料,也是目前我国常用的一种原料。
所以本实验采用柑橘皮为原料,采用酸法萃取,酒精沉淀这一种最简单的工艺路线来提取果胶。
四、实验步骤1. 原材料的预处理[注1]称取新鲜柑橘皮5 g 用清水漂洗干净,加水20 mL ,加热到90℃,保持10分钟以达到灭酶的目的。
果胶实验方案

果胶实验⽅案果胶提取1⽅法1.1原料制备称取10克冬青,切碎,放⼊烧杯中。
在烧杯中加⼊蒸馏⽔,⽤⽔浴锅加热到90度,加热10分钟,以除去果胶酶。
过滤,将滤液⽤蒸馏⽔多次洗涤,直到滤出液变得澄清,以出去⾊素。
1.2果胶提取把滤渣放⼊烧杯中,加⼊盐酸,调节PH⾄2,放到⽔浴锅中,100度加热1.5⼩时。
过滤,得到的溶液就是果胶溶液,向其中加⼊等量的稍多的⽆⽔⼄醇。
即可得到湿果胶2果胶提取的单因素实验,2.1 提取温度对果胶提取率的影响,在PH 2,加热时间1.5⼩时,料液⽐1:10的条件下。
设置50℃60℃80℃100℃120℃做⼀组实验。
2.2PH对果胶提取率的影响在温度100℃加热时间1.5⼩时,料液⽐1:10的条件下。
设置PH 1 2 3 4 5做⼀组实验2.3 提取时间对果胶提取率的影响在温度100℃PH 2 ,料液⽐1:10的条件下。
设置加热时间50min 60min 80min 100min 120min做⼀组实验。
2.4料液⽐对果胶提取率的影响在温度100℃加热时间1.5⼩时,PH为2的条件下。
设置料液⽐为1:6 1:8 1;10 1;12 1;14做⼀组实验。
3 实验⽬的在单因素的基础上找出每个因素下的最优条件,为正交实验做准备。
4.果胶的⼲燥(四种⽅法)1.果胶⼲燥⼤多采⽤喷雾⼲燥,即⽤压⼒式喷雾⼲燥,将浓缩液在进料温度150~160℃,出料温度220~230℃的条件下⼲燥,连续化操作中可不断得到粉末状产品。
2.将湿果胶转移于100 mL烧杯中,加⼊30 mL⽆⽔⼄醇洗涤湿果胶,再⽤尼龙布过滤、挤压。
将脱⽔的果胶放⼊表⾯⽫中摊开,在60~70 ℃烘⼲。
将烘⼲的果胶磨碎过筛,制得⼲果胶。
3.冷冻⼲燥。
将湿果胶冷冻,然后在较⾼真空下将溶液蒸发⽽⼲燥的⽅法。
4.⽤布⽒漏⽃过滤得到果胶沉淀,把果胶移动于烧杯中⽤95%⼄醇洗涤吸过滤。
搓碎放于表⾯⽫中在⼲燥器中过夜,⽤研钵研磨得到果胶粉,计算产率5果胶的纯度检验1.重量法2.咔唑⽐⾊法测定果胶含量(1)原理果胶经⽔解,其产物半乳糖醛酸可在强酸环境下与咔唑试剂产⽣缩合反应,⽣成紫红⾊化合物,其呈⾊深浅与半乳糖醛酸含量成正⽐,由此可在530nm波长下⽐⾊测定。
实验6 植物废弃物中提取果胶

实验6 植物废弃物中提取果胶一、实验目的①掌握从甜菜渣、桔皮等植物废弃物中提取果胶的原理和方法。
②了解果胶的主要性质和用途。
二、实验原理1. 主要性质和用途果胶(pectin )属多糖类植物胶,以原果胶的形式存在于高等植物的叶、茎、根等的细胞壁内,与细胞彼此粘合在一起,由水溶性果胶和纤维素结合而形成不溶于水的成分。
未成熟水果因果实细胞壁中有原果胶存在,因此组织坚实。
随着果实不断生长成熟,原果胶在酶的作用下分解为(水溶性)果胶酸和纤维素。
果胶酸再在酶的作用下继续分解为低分子半乳糖醛酸和α—半乳糖醛酸。
原果胶含量逐渐减少,因而果皮不断变薄变软。
原果胶在水和酸中加热,可分解为水溶性果胶酸。
果胶在果实及叶中的含量较多。
在橙属水果的果皮和苹果渣、甜菜渣中都含有质量分数20%~50%的果胶。
各种果实、果皮中的原果胶,通常以部分甲基化了多缩半乳糖醛酸的钙盐或镁盐形式存在,经稀盐酸水解,可以得到水溶性果胶,即多缩半乳糖醛酸的甲酯。
果胶的基本化学组成是半乳糖醛酸,基本结构是D —吡喃半乳糖醛酸以α-1,4-糖苷连接的长链,通常以部分甲酯化状态存在,其结构式为果胶水解时,产生果胶酸和甲醇等,其反应式为果胶是高分子聚合物,可以从植物组织中分离提取出来,其相对分子质量在5万~30万之间为淡黄色或白色的粉末状固体,味微酸,能溶于20倍水中生成粘稠状液体,不溶于酒精及一般的有机溶剂,若先用酒精、甘油或糖浆等浸润,则极易溶于水中。
果胶在酸性条件下稳定,但遇强酸、强碱易分解,在室温下可与)(4229710661265105332366041果胶酸O H C O H C O H C COOH CH OH CH O H O H C ++++=+强碱作用生成果胶酸盐。
果胶具有良好的胶凝化和乳化作用,在食品工业、医药工业和轻工业中有广泛的用途,他可以用于制备低浓度果酱、果胶及胶状食物,作结冻剂;用作果汁饮料、乳品、巧克力、速冻饮粉和糖果等食品中的添加剂;也可用作冷饮食品的稳定剂。
从植物中提取果胶操作方法

从植物中提取果胶操作方法
提取果胶的方法主要有以下几个步骤:
1. 选择合适的植物材料:一般可以选择富含果胶的植物,如苹果、柚子、柠檬、草莓等。
新鲜的植物材料可以提供更好的果胶提取效果。
2. 准备植物材料:将植物材料洗净,并去除果皮和籽等部分。
将果肉切成小块或搅碎,以便更好地释放果胶。
3. 浸泡植物材料:将搅碎后的植物材料放入足够的水中浸泡。
一般来说,水的浓度越高,果胶的提取效果越好。
可以根据需要调整浸泡时间和水的浓度,通常需要浸泡几个小时到一整夜。
4. 煮沸植物材料:将浸泡后的植物材料连同浸泡水一起加热至沸腾,然后继续煮沸几分钟。
这样可以促进果胶的释放和溶解。
5. 过滤植物材料:将煮沸后的植物材料过滤掉,只留下果胶溶液。
可以使用细网过滤器或纱布来过滤固体颗粒,以获得清澈的果胶溶液。
6. 浓缩果胶溶液:将过滤后的果胶溶液倒入浅平底容器中,然后将其置于通风良好的环境中待其自然脱水。
可以将容器放在阳光下或使用加热设备进行脱水。
脱水过程中,果胶溶液会逐渐变浓,直到形成固体的果胶。
7. 干燥果胶:可以将浓缩后的果胶放在通风良好的地方晾干,也可以使用烘干机等设备加速干燥过程。
待果胶完全干燥后,即可得到提取好的果胶。
需要注意的是,果胶提取的具体操作方法可能会因不同的植物材料和实验条件而有所变化,可以根据具体情况进行调整。
此外,果胶的提取可以使用化学试剂进行加工处理,但这需要更专业的实验设备和知识,且不适合家庭条件下进行。
果胶的提取

果胶的提取原料处理:原料新鲜、洗涤,挤干备用。
提取:加入0.15%盐酸溶液调pH2-3,加热到85℃~95℃,保持1~1.5h,不断搅拌。
分离:一般用布袋式螺旋挤压机,挤压分离。
脱色:加入活性炭1.5%~2%、60℃~80℃下保温20min,然后压滤浓缩:真空浓缩到,真空度13.33kPa以上,温度控制在45℃~50℃,果胶含量提高6%~9%。
沉淀:压滤洗涤:先将果胶浓缩后再用95%酒精沉淀。
烘干、粉碎包装:在60℃以下进行干燥,过60~80目筛香精油的提取蒸馏法:通过原料浸润、分层上料、蒸馏分离、提纯等步骤。
提取的香精油应过滤,装于能密封的有色瓶中,贮放在阴凉处,以防止香精油的挥发损失或氧化变质。
如:大蒜油玫瑰油浸提法:先将原料破碎,再用有机溶剂在密封容器中进行浸渍,在较低的温度条件下进行,以免浸出的香精油挥发损失。
简单易行但生产效率低。
压榨法:新鲜的柑橘类果皮以白色皮层朝上晾晒1天,使果皮水分减少到15%~18%,破碎至3mm大小压榨。
每100kg上述湿度的干皮,可得0.6~1.2kg纯净的香精油。
酸枣红色素提取工艺流程:酸枣皮连续浸润过滤调提取液PH 沉淀过滤洗涤干燥粉碎过筛成品注意事项:提取溶剂:酸枣皮中色素不溶于酸和醇,微溶于热水,易溶于碱类。
选用5%的碳酸钠和2%的氢氧化钠作为提取溶剂。
pH:溶液随pH的增大色素提取率明显提高,提取酸枣红色素的最佳pH为7~8。
热稳定性:在100℃内加热有利于色素的显色,但在煮沸的情况下再持续加热,会使颜色变浅辣椒红色素提取的操作要点1.粉碎、提取。
将粉碎后的干红辣椒投入提取罐中,用95%乙醇连续提取至红辣椒无红色,可得到辣椒油树脂。
2.蒸馏、萃取。
用水蒸汽蒸馏(辣椒油)树脂、蒸馏去残余的醇类,同时可部分蒸除辣味。
并用乙酸乙酯萃取收集含有辣椒油树脂。
3.碱水处理。
取一定量的辣椒油树脂,加入20%氢氧化钠溶液,料液比为1:4.5,搅拌处理4h,控制温度为70℃。
果胶的提取及果冻制作实验指导书

果胶的提取及果冻制作实验指导书一、实验目的通过实验,进一步加深对果胶特性的理解,掌握果胶的一般提取方法和技术,了解果胶的应用。
二、实验原理果胶是高分子糖类化合物,是一种植物性天然交替物质,广泛地存在于苹果、山楂和柑桔类等的果实及其它植物体内。
果胶在植物体中,以原果胶、果胶和果胶酸二种形式存在。
原果胶用稀酸处理或与果胶酶作用时可转变为可溶性果胶。
可溶性果胶的基本结构是多聚半乳糖醛酸,其中部分羟基被甲醇脂化为甲氧基。
一般植物中的果胶甲基含量,约占全部多聚半乳糖醛酸结构(包括被脂化的羟基)的7~14%,甲氧基含量高于7%的果胶,称为高甲氧基果胶,即普通果胶。
普通果胶中甲氧基含量越多,胶冻能力越大。
甲氧基含量低于7%的果胶,称为低甲氧基果胶,几乎无胶凝力但有多价金属离子如Ca2+、Mg2+、Al3+等存在时可生成凝胶,多价离子起到果胶分子交联剂的作用。
果胶为白色淡黄褐色粉末,溶于水成粘稠状液体,对石蕊试纸呈酸性。
果胶与适量的糖和有机酸一起煮,可形成柔软而有弹性的胶冻。
基于此特性,所以果胶在食品工业中具有用来制造果酱、果冻、巧克力、糖果等食品,也可用作冷饮食品、冰淇淋、雪糕等的稳定剂。
在医药上果胶可作为肠出血的止血剂,低甲氧基果胶能与金属离子形成不溶于水的化合物,因而果胶又是铅、汞、钴等金属中毒的良好解毒剂。
三、实验材料、试剂和仪器干桔皮;0.1NHCl;95%C2H5OH;白糖;柠檬酸;500mL烧杯2只;10mL1只;表面皿6cm 1块;干燥器、抽滤瓶1只;布氏漏斗1 只;龙头布袋一只;电炉;滤纸φ=7.0cm;研钵、量筒100mL1只;10mL1只。
四、实验内容(一)果胶提取称取干桔皮15克,用水洗净,稍软,剪碎,置于600mL烧杯中加水150~200mL 煮沸10分钟(去除糖类、色素、苦味等)弃去水,用冷水反复漂洗残渣,挤干后称重,置500mL 烧杯中,加残渣3倍量0.1NHCl煮沸10分钟,趁热用尼龙细布袋(布袋用水浸湿挤干),挤压布袋使滤渣挤干,弃去滤渣,把布袋洗净后将滤液再滤一次,把滤液浓缩至50mL,冷却,滤液中加95%乙醇至混合液中乙醇浓度达60%止,用玻璃棒搅匀,得到胶体溶液。
果胶提取实验报告

果胶提取实验报告一、实验目的本实验旨在探究从水果中提取果胶的方法,并对提取的果胶进行质量评估和分析。
二、实验原理果胶是一种多糖物质,广泛存在于植物的细胞壁中。
其主要成分是半乳糖醛酸聚合物,具有胶凝、增稠等特性。
利用酸水解的方法可以使果胶从植物组织中释放出来,然后通过沉淀、过滤、干燥等步骤获得果胶成品。
三、实验材料与仪器1、实验材料新鲜水果(如柑橘、苹果等)无水乙醇盐酸氢氧化钠活性炭2、实验仪器电子天平恒温水浴锅真空抽滤机干燥箱玻璃棒烧杯容量瓶四、实验步骤1、原料预处理选取新鲜、无腐烂的水果,洗净、去皮、去核,将果肉切成小块备用。
2、酸水解称取一定量的水果小块放入烧杯中,加入适量的蒸馏水,再加入一定浓度的盐酸,使料液比达到 1:X(X 根据具体实验条件确定)。
将烧杯置于恒温水浴锅中,在一定温度下加热搅拌进行酸水解,反应时间为 Y 小时(Y 根据具体实验条件确定)。
3、过滤水解完成后,用真空抽滤机对料液进行过滤,收集滤液。
4、脱色向滤液中加入适量的活性炭,搅拌均匀,在一定温度下保温一段时间进行脱色处理。
5、沉淀向脱色后的滤液中缓慢加入氢氧化钠溶液,调节 pH 值至 Z(Z 根据具体实验条件确定),使果胶沉淀。
6、过滤与洗涤再次用真空抽滤机对沉淀进行过滤,收集果胶沉淀。
用蒸馏水对沉淀进行多次洗涤,以去除杂质。
7、干燥将洗涤后的果胶沉淀放入干燥箱中,在一定温度下干燥至恒重,得到果胶成品。
五、实验结果与分析1、产率计算根据提取得到的果胶成品质量和原料质量,计算果胶的产率。
果胶产率(%)=(提取得到的果胶质量/原料质量)× 1002、质量评估外观:观察提取得到的果胶成品的颜色、状态等外观特征。
纯度:通过化学分析方法(如滴定法等)测定果胶的纯度。
3、结果分析比较不同水果原料对果胶产率和质量的影响。
分析酸水解条件(如盐酸浓度、温度、时间等)对果胶提取效果的影响。
探讨脱色处理和沉淀条件对果胶质量的改善作用。
实验C 果胶提取
实验四果胶的提取和应用一、目的要求1、了解果胶的性质和提取原理;2、掌握果胶的提取工艺;3、了解果胶在食品工业中的用途。
二、实验原理果胶广泛存在于水果和蔬菜中。
例如苹果(以湿品计)中含量为0.7%-1.5%,蔬菜中则以南瓜中含量最多,含7%-17%。
其主要用途是用作酸性食品的胶凝剂。
目前果酱、果子冻、桔子果冻仍然是世界上果胶的主要产品。
但随着果胶在了业上作为胶凝剂、增调剂以及保护胶体等用途的发展,用以制果酱的果胶的百分数必然减少。
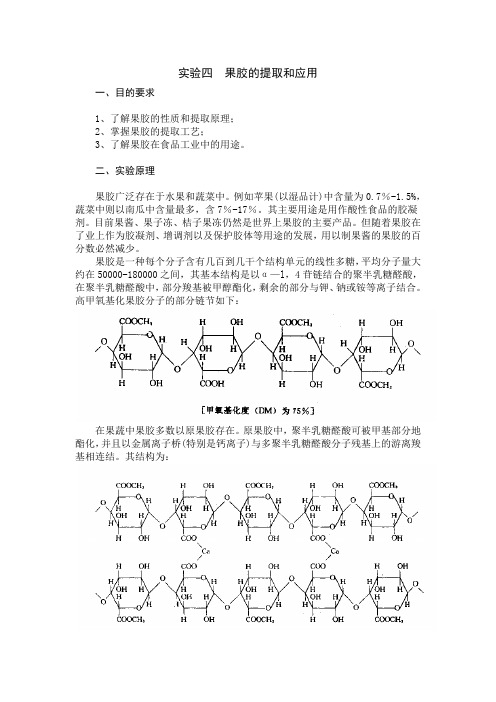
果胶是一种每个分子含有几百到几干个结构单元的线性多糖,平均分子量大约在50000-180000之间,其基本结构是以α—l,4苷链结合的聚半乳糖醛酸,在聚半乳糖醛酸中,部分羧基被甲醇酯化,剩余的部分与钾、钠或铵等离子结合。
高甲氧基化果胶分子的部分链节如下:在果蔬中果胶多数以原果胶存在。
原果胶中,聚半乳糖醛酸可被甲基部分地酯化,并且以金属离子桥(特别是钙离子)与多聚半乳糖醛酸分子残基上的游离羧基相连结。
其结构为:原果胶不溶于水,用酸水解时这种金属离子桥(离子键)被破坏,即得到可溶性果胶。
再进行纯化和干燥即为商品果胶。
甲氧基化的半乳糖醛酸残基数与半乳糖醛酸残基总数的比值称为甲氧基比度或酯化度。
果胶的胶凝强度的大小是果胶的重要质量标准之一。
影响胶凝强度的主要因素是果胶的分子量及酯化度。
酯化度增大.胶凝强度增大,同时胶凝速度也加快。
理论上完全酯化的聚半乳糖醛酸的甲氧基含量是16.32%,这时酯化度为100%,但实际上能得到的甲氧基含量最高值是12%--14%。
一般规定甲氧基含量大于7%的为高甲氧基果胶,小于和等于7%的为低甲氧基果胶。
从天然原料中提取的果胶最高酯比度为75%,食品工化中常用高甲氧基果胶来制果冻、果酱和糖果等.以及在汁液类食品中作增稠剂、乳化剂等,更高酯化度的果胶可通过用甲醇甲氧基化来获得。
若在酸性和碱性条件下加热果胶,会使甲酯水解。
苷链断裂.变成低酯化度或低分子量的果胶,从而降低果胶的胶凝强度和速度。
果胶提取

四、实验步骤 1、原料预处理:称取新鲜柑橘皮20g(或干样8g), 用清水洗净后,放入250mL烧杯中,加水120mL, 加热至90℃保持5-10min,使酶失活。用水冲洗后 切成3~5mm的颗粒,用50℃左右的热水漂洗,直 至水为无色、果皮无异味为止(每次漂洗必须把 果皮用尼龙布挤干,在进行下一次的漂洗)。 2、酸水解提取:将预处理过的果皮粒放入烧杯中, 加约60mL 0.25% HCL溶液,以浸没果皮为宜,调 pH至2.0~2.5,加热至90℃煮45min,趁热用100目 尼龙布或四层纱布过滤。
3、脱色:在滤液中加入0.5~1.0%的活性炭,于80℃加热 20min,进行脱色和除异味,趁热抽滤(如抽滤困难可加 入2%~4%的硅藻土作为助滤剂)。如果柑橘皮漂洗干净 萃取液为清澈透明则不用脱色 。 4、沉淀:待提取液冷却后,用稀氨水调pH至3~4。在不断 搅拌下加入95%乙醇溶液,加入乙醇的量约为原体积的1.3 倍,使酒精浓度达到50%~65%。 5、过滤、洗涤、烘干:用尼龙布过滤(滤液可用蒸馏法回 收酒精),收集果胶,并用95%乙醇洗涤果胶2~3次,再 于60~70℃干燥果胶,即为果胶产品。
在果蔬中尤其是未成熟的水果和皮中果胶多数以在果蔬中尤其是未成熟的水果和皮中果胶多数以原果胶存在原果胶通过金属离子桥比如原果胶存在原果胶通过金属离子桥比如ca2ca2与多聚半乳糖醛酸中的游离羧基相结合
实验 果胶的提取 一、实验目的:掌握实果胶提取的原理及方法。 二、原理: 果胶广泛存在于水果和蔬菜中,如苹果中含量为0.71.5%(以湿品计),在蔬菜中以南瓜含量最多(达7%17%)。果胶的基本结构是以α-1,4苷键连接的聚半乳糖醛 酸,其中部分羧基被甲酯化,其余的羧基与钾、钠、铵离 子结合成盐。 在果蔬中,尤其是未成熟的水果和皮中,果胶多数以 原果胶存在,原果胶通过金属离子桥(比如Ca2+)与多聚 半乳糖醛酸中的游离羧基相结合。原果胶不溶于水,故用 酸水解,生成可溶性的果胶,再进行提取、脱色、沉淀、 干燥,即为商品果胶。从柑橘皮中提取的果胶是高酯化度 的果胶(酯化度在70%以上)。在食品工业中常利用果胶制 作果酱、果冻和糖果,在汁液类食品中作增稠剂、乳化剂。
果胶的提取

6.将水浴40min的原液倒入布氏漏斗中进行抽滤。
7.滤液冷却后,加入氨水调节pH3~4,并加入95%酒精。
8.静置后看到絮状物出现(静置20min)。
9.用尼龙布过滤,在滤布上有湿果胶出现。
10.将湿果胶置于烧杯中用30ml无水乙醇洗涤并抽滤。
仪器、设备、材料等:
烧杯、水浴锅、纱布、剪刀、抽滤瓶、布氏漏斗、天平、玻璃棒、表面皿、烘箱、尼龙布、量筒、新鲜柑橘皮。
湿果胶质量g(连表面皿)
37.2
表面皿质量g
33.4
干果胶质量g(连表面皿)
33.2
干果胶质量g
0.2
11.将果胶置于天平上称取湿果胶和表面皿重为37.2g,果胶烘干后称得重为33.4g,表面皿重33.2g。故干果胶质量为0.2g。
12.将烘干后的果胶再溶入水中,以检测其复溶性。
现象描述:
柑橘皮放入水中加热,溶液呈淡黄色。搅拌一段时间后烧杯中液体表面出现白色泡沫。抽滤醇析静置后看到烧杯中有絮状物出现。用尼龙布过滤,在滤布上有果胶出现。湿果胶为无色透明的胶状物质,烘干后为呈白色。再将烘干后的果胶再溶入水中,大部分溶解,其复溶性良好。
果胶的提取
日期
000000
地点
000000
实验班组
0000
成员
Байду номын сангаас工艺步骤
果胶的提取
柑橘皮质量
20g
温度℃
热水浴
工艺时间
000
操作描述:
1.称取原料20g置于烧杯中,并预处理。
2.将烧杯置于水浴中进行加热。
3.温度达到90℃,颜色变至黄色,保持10min,用热水进行漂洗12次至无色。
用苹果皮提取果胶

用苹果皮提取果胶
(一)工艺流程
原料→粉碎→热水洗→水解萃取→过滤→沉淀→果胶→热水洗→酸化后溶解→加乙醇沉淀→果胶→洗涤→千燥→成品
(二)操作要点说明
(1)原料粉碎与洗涤:将苹果皮破碎后,用孔径为2~3毫米的筛子筛分,然后用60℃的热水清洗,以除去杂质,再洒上乙醇,晾干。
(2)水解萃取:将晒干后的原料加水(一般水为原料质量的15倍),用盐酸将水溶液的pH值调至1.6~6.3,加热至75℃,恒温1小时,保持18小时,使原料胶水解为果胶,溶于溶液内,然后过滤,得透明的溶液。
滤渣再加入原料质量5倍的盐酸溶液(pH值与第一次水解相同),在95℃的温度下保温15分钟,然后压榨取汁液,将两液合并在一起,进行过滤。
(3)沉淀:在水解滤液中加入原料质量40%的三氯化二铝,使温度保持在40℃,一边搅拌,一边加入2摩尔/升氢氧化钠溶液,调整pH至4,使果胶铝沉淀下来。
(4)水洗与酸化后溶解:把沉淀的果胶铝用70~80℃的热水清洗数次,除去水溶性杂质,再用稀盐酸将果胶铝溶解。
(5)再沉淀:向溶液中加入乙醇溶液,重新将果胶沉淀出来,过滤后回收乙醇,用乙醇将沉淀物清洗数次。
(6)干燥:在70℃的温度下进行真空干燥,约干燥8小
时,即可得到果胶成品。
纯果胶通常是浅黄色或褐色,为高甲氧基果胶。
水果中果胶物质的提取和测定

水果中果胶物质的提取和测定一、实验目的1、温水基本操作,如PH计的使用、抽滤,分光光度计的使用,标准曲线的绘制2、初步了解和掌握食品中某些成分的提取技术、分离技术以及测定方法,为灵活运用食品化学的研究方法奠定基础。
二、实验原理本实验采用钙离子螯合剂和果胶酶提取水果中的总果胶物质,然后用分光光度法测定总果胶物质,先用乙醇处理样品,使果胶沉淀,再用乙醇溶液洗涤沉淀,除去可溶性糖类、脂肪、色素等物质,从残渣中提得果胶物质。
采用NaOH溶液将果胶物质皂化,生成果胶酸钠,再经乙酸酸化使之生成果胶酸,再加入果胶酶使之水解。
分光光度法测定是以果胶分子的基本结构单位——半乳糖醛酸和咔唑的反应为基础的。
果胶经水解生成半乳糖醛酸,在强酸中与咔唑发生缩合反应,生成紫红色化合物,其呈色强度与半乳糖醛酸含量成正比,测定的结果可用脱水半乳糖醛酸(AUA)。
三、实验步骤1、果胶物质的提取将10g新鲜橘皮和125ml95%乙醇一起捣碎,抽滤后保留沉淀,用50ml75%乙醇洗涤沉淀两次,将沉淀转移到250ml烧杯中,加入100ml 1%EDTA溶液,用1mol/LNaOH将PH调节至11.5,保持30min后,再用醋酸溶液将果胶溶液酸化到PH5.0,然后加入10ml果胶酶提取液,搅拌0.5h后,定容至250ml,用脱脂棉过滤,弃去沉淀和前20ml滤液,吸取部分滤液稀释10倍,作为测定果胶含量的样品。
2、半乳糖醛酸的比色测定在20Ⅹ200mm试管中准确加入12ml浓硫酸,用冰浴将试管及内容物冷却到3℃,吸入1.00ml待测溶液,每毫升溶液中含5~40μg果胶物质。
将试管中的内容物振荡均匀后,在冰浴中冷却至5℃以下,然后将试管在100℃水浴中加热10min,冷却至20℃,吸入1.00ml0.15%咔唑试剂,充分混匀,在室温下放置25min,在520nm波长下测定溶液的吸光度,从加入咔唑试剂到测定溶液吸光度的时间和温度在各次测定中应保持一致。
果胶的提取

综合实验七超声波溶剂法从柑橘皮中提取果胶一、实验目的1.理解果胶的提取工艺原理、操作方法及其影响的因素;2.了解超声波作用机理及其在化学化工中的应用;3..掌握萃取、过滤、减压蒸馏和沉淀等工艺原理和实验操作技能。
二、实验原理本实验以柑桔皮为原料,采用酸液提取、减压蒸馏浓缩、乙醇沉淀等工艺提取果胶。
果胶是一种高分子聚合物,存在于植物组织内,一般以原果胶、果胶酯酸和果胶酸3中形式存在于各种植物的果实、果皮以及根、茎叶的组织中。
果胶为白色、浅黄色到黄色的粉末,有非常好的特殊水果香味,无固定熔点和透明度,不溶于乙醇、甲醇等有机溶剂中,粉末果胶溶于20倍水中形成黏稠状透明胶体,胶体的等电点pH值为3.5。
果胶的主要成分为多聚D-半乳糖醛酸,各醛酸单位间经α―1,4糖苷键联结,具体结构式如图1所示。
另外还有中性多糖,多聚D-半乳糖和多聚L-阿拉伯糖。
实际上,果胶是这些多糖的混合物,平均分子量在5000-18000之间。
OOH图1. 果胶的结构式果胶在柑桔皮中含量极高,约占干质的20%~30%。
在生产果胶时,原料经酸、碱或果胶酶处理,在一定条件下分解,形成可溶性果胶,然后在果胶液中加入乙醇或多加金属盐类,使果胶沉淀析出,经漂洗、干燥、精制而形成产品。
目前常用的果胶提取方法有3种:酸提取法,离子交换法和微生物法。
其中,酸提取法包括酸液提取、减压蒸馏浓缩和沉淀析出等工艺步骤。
沉淀析出有乙醇沉淀法和盐沉淀法等两种,盐沉淀法有铁盐盐析法和铁铝混合盐析法。
乙醇沉淀和用铁铝盐沉淀都各有优缺点,乙醇沉淀法生产工艺简单,所的果胶纯度高,色泽好,产率高(20%-30%,以干质计),但乙醇耗量大;盐沉淀法成本低,工艺简单,但产率低(7%左右),且铝盐沉淀颗粒小,难分离,高价铁盐颜色较深,需做脱色处理。
在这3种提取方法中,酸提取法使用最多,其主要过程为:将原料进行预处理后,用稀盐酸水解,水浴恒温并不断搅拌,将柑桔皮中的果胶溶出;然后过滤,将滤液减压蒸馏浓缩,再用乙醇或铁铝盐进行沉淀,以析出果胶。
提取果胶的实验报告

提取果胶的实验报告提取果胶的实验报告引言:果胶是一种常见的植物胶质,广泛存在于植物的细胞壁中。
它具有多种生理功能,如增加植物细胞的稳定性、保持水分、增加抗病能力等。
本实验旨在通过提取果胶的方法,了解果胶的性质和应用。
实验材料:1. 水果:柠檬、苹果、橙子2. 酒精3. 盐4. 研钵、研杵5. 滤纸6. 烧杯7. 玻璃棒8. 温度计实验步骤:1. 将柠檬、苹果、橙子分别切成小块,放入研钵中。
2. 用研杵将水果块捣碎,使果汁充分释放。
3. 将果汁倒入烧杯中,加入适量的酒精。
4. 用玻璃棒搅拌均匀,使果胶与酒精充分混合。
5. 将混合液放置一段时间,待果胶沉淀。
6. 将果胶沉淀用滤纸过滤,得到纯净的果胶。
实验结果:通过实验,我们成功提取到了柠檬、苹果、橙子中的果胶。
果胶呈现出白色或微黄色的颗粒状沉淀物。
不同水果中的果胶颗粒大小和形状略有差异。
讨论:果胶是一种多糖类物质,主要由葡萄糖、半乳糖和甘露糖等单糖组成。
它具有较高的黏性和胶凝性,可用于食品工业、医药工业等领域。
果胶在食品中常用于增加稠度、改善质感和口感。
在医药领域,果胶具有良好的药物缓释性能,可用于制备胶囊和药片。
在实验过程中,我们选择了柠檬、苹果和橙子作为提取果胶的材料。
这三种水果中富含果胶,且易于提取。
酒精是一种常用的溶剂,可有效提取果胶。
通过与果汁混合,酒精能够与果胶发生作用,使果胶从溶液中沉淀出来。
通过过滤,我们得到了纯净的果胶。
实验中的一些因素可能会影响果胶的提取效果。
首先,水果的种类和成熟度会影响果胶的含量和质量。
不同水果中果胶的含量和性质可能存在差异。
其次,酒精的浓度和用量也会对果胶的提取产生影响。
合适的酒精浓度和用量能够提高果胶的提取率。
最后,提取时间的长短也会对果胶的提取效果产生影响。
适当延长提取时间可以增加果胶的产量。
结论:通过本实验,我们成功提取到了柠檬、苹果、橙子中的果胶,并初步了解了果胶的性质和应用。
果胶是一种重要的植物胶质,具有广泛的应用前景。
2实验 果胶的提取

2实验从柑桔皮中提取液体果胶2008-09-24 信息来源:食品伙伴网视力保护色:【大中小】【打印本页】【关闭窗口】利用含果胶丰富的果实或残次落果、果皮种子残渣等作原料,而具工业化生产价值。
一般采用柑桔皮、苹果榨汁后的废渣等。
成为商品果胶有两种形态,一是上面提到的粉末果胶,一是液体果胶。
商品果胶按其酯化度分为两大类型,即高甲氧基果胶和低甲氧基果胶,其酯化度大于50%,甲氧基大于7%的为高甲氧基果胶。
如果甲氧基含量小于7%其酯化度低于50%为低甲氧基果胶。
这主要与原材料有关。
1、原料预处理:如用柑桔皮,为了保存原料,应对原料作处理,应迅速加热至95℃保持5-7分钟。
热处理的目的是钝化果胶酶以免果胶分解,使收得率降低,然后把原料进行干制,制成半成品进行保存。
2、浸泡:把干皮浸水,初步除去芳香物质、糖分、苦味物质及色素等。
3、漂洗:上面浸水主要使果皮吸水变软,通过以多量水漂洗尽量去除糖类,色素等各种非胶体物质,以保证果胶的品质。
4、沥干粉碎:可用绞肉机破碎成3-5毫米大小粒度,目的是让果胶能充分提取出来。
5、提胶:应用酸提胶法,是依据原果胶在稀酸及加热下水解成可溶性果胶理论而进行的,提胶时溶液pH值、温度、时间及酸的种类对果胶质量及数量影响极大。
可用1%稀盐酸四倍于原料加入原料中,并加热到90℃左右,溶液呈微沸状态,保持1小时左右,并不断搅拌,直到水解完毕为止。
6、过滤:过滤除渣得稀胶状果胶液。
7、脱色:目的是充分除去色素、苦味和异味。
多用活性炭进行脱色。
8、浓缩:要生产液态果胶必须把稀果胶液进行浓缩,以除去多量水分,生产上应用减压真空浓缩,采用双效蒸发罐,真空度为660毫米水银柱,沸腾温度为45-50℃,浓缩比为4:1或5:1。
最后用碳酸钠(Na2CO3)中和,提高pH值到3.5。
9、装罐,封罐:乘热装罐,密封。
10、杀菌:因果胶液呈酸性,杀菌温度应用巴氏杀菌法,即70℃30分钟足够。
11、冷却:冷却后得液态果胶制品。
提取果胶操作方法

提取果胶操作方法
1. 准备果胶原料:果胶原料可以是青梅、山楂、苹果、柚子、草莓等含有大量果胶的水果或果皮。
2. 洗净果实:将选好的果实洗净,去除果实表面的杂质和不干净的部分。
3. 切碎果实:将洗净的果实切成小块或泥状,以便后续提取果胶时更易操作。
4. 加入水煮沸:将切碎的果实加入适量清水,煮沸后改用小火慢炖,直到果实变软烂。
5. 过滤果渣:将果泥用棉布或过滤纸过滤,将果渣和果胶分离开来。
6. 沉淀分离:将过滤后的液体放置一段时间,让果胶慢慢沉淀到底部。
7. 提取果胶:将沉淀的果胶取出,用热水清洗,去除余渣和杂质。
最后将果胶晾干即可。
注意事项:
1. 操作时要注意安全,避免烫伤或火灾等事故发生。
2. 选择新鲜、干净的水果或果皮,以获得更高质量的果胶。
3. 操作时要保持卫生,避免细菌污染果胶。
4. 切碎的果实大小和形状不要过大或不均匀,以便后续操作。
实验三-从果皮中提取果胶

从果皮中提取果胶一、实验目的1、学习从从果皮中提取果胶的基本原理和方法, 了解果胶的一般性质。
2、掌握提取有机物的原理和方法。
3、进一步熟悉萃取、蒸馏、升华等基本操作。
二、实验原理果胶是一种高分子聚合物,存在于植物组织内,一般以原果胶、果胶酯酸和果胶酸3种形式存在于各种植物的果实、果皮以及根、茎、叶的组织之中。
果胶为白色、浅黄色到黄色的粉末,有非常好的特殊水果香味,无异味,无固定熔点和溶解度,不溶于乙醇、甲醇等有机溶剂中。
粉末果胶溶于20倍水中形成粘稠状透明胶体,胶体的等电点pH值为3.5。
果胶的主要成分为多聚D—半乳糖醛酸,各醛酸单位间经a—1,4糖甙键联结,具体结构式如图1。
图1 果胶的结构式在植物体中,果胶一般以不溶于水的原果胶形式存在。
在果实成熟过程中,原果胶在果胶酶的作用下逐渐分解为可溶性果胶,最后分解成不溶于水的果胶酸。
在生产果胶时,原料经酸、碱或果胶酶处理,在一定条件下分解,形成可溶性果胶,然后在果胶液中加入乙醇或多价金属盐类,使果胶沉淀析出,经漂洗、干燥、精制而形成产品。
三、主要仪器和药品仪器:恒温水浴锅、真空干燥箱、布氏漏斗、抽滤瓶、玻棒、纱布、表面皿、精密pH试纸、烧杯、电子天平、小刀、小剪刀、真空泵、。
药品:干柑桔皮、稀盐酸、95%乙醇(分析纯)等。
四、实验内容1、柑桔皮的预处理称取干柑桔皮20g,将其浸泡在温水中(60~70℃)约30min,使其充分吸水软化,并除掉可溶性糖、有机酸、苦味和色素等;把柑桔皮沥干浸入沸水5min进行灭酶,防止果胶分解;然后用小剪刀将柑皮剪成2~3mm的颗粒;再将剪碎后的柑桔皮置于流水中漂洗,进一步除去色素、苦味和糖分等,漂洗至沥液近无色为止,最后甩干。
2、酸提取根据果胶在稀酸下加热可以变成水溶性果胶的原理,把已处理好的柑桔皮放入水中,控制温度,用稀盐酸调整pH值进行提取,过滤得果胶提取液。
3、脱色将提取液装入250ml的烧杯中,加入脱色剂活性炭;适当加热并搅拌20min,然后过滤除掉脱色剂。
果胶提取-实验方案

纤维素酶协同树脂法HCl提取塔罗科血橙果胶实验方法:一、灭酶制样将洗净的血橙皮放入沸水中煮制5min,沥干后置烘箱中70℃烘干,粉碎备用。
单因子实验二、果胶的提取方法:称取血橙皮1.5g于光滑纸袋,转入提取瓶中,加45ml提取液(在料液比为1:30),加纤维素酶(10U/ml)于45℃水浴中酶解45min,加入3%(料)离子交换树脂,用HCl调节pH为2,在微波功率为250W,加热2.5min,冷却,于离心机中4000R/min,离心10min的条件下离心,取上层清液,加入等体积的食用乙醇,搅拌均匀,静置30min,用真空泵抽滤,于烘箱中50℃烘干,称量,计算果胶产率。
三、脱脂条件1、提取pH对果胶产率的影响称取血橙皮1.5g于光滑纸袋,转入提取瓶中,加45ml提取液(在料液比为1:30),加纤维素酶(10U/ml)于45℃水浴中酶解45min,加入3%(料)离子交换树脂,用HCl调节pH梯度为0.5、1、1.5、2、2.5、3、3.5、4,在微波功率为250W,加热2.5min,冷却,于离心机中4000R/min,离心10min的条件下离心,取上层清液,加入等体积的食用乙醇,搅拌均匀,静置30min,用真空泵抽滤,于烘箱中50℃烘干,称量,计算果胶产率。
2、微波功率对果胶产率的影响在料液比为20ml/g的溶液中,加入0.25g离子交换树脂,调pH值为最佳状态(上一步得出的最佳pH),设置不同梯度的微波功率100——400W之间,加热7min,冷却,在4000R/min,离心时间为12min的条件下离心,取上层清液,加入等体积的乙醇,搅拌均匀,静置30min,用真空泵抽滤,烘干,称量,计算果胶产率。
找出最佳微波功率。
3、微波时间对果胶产率的影响在料液比为20ml/g的溶液中,加入0.25g离子交换树脂,调pH值为最佳状态(上一步得出的最佳pH),调节微波功率为最佳状态(上步得出的最佳功率),设置微波时间梯度为1——12min,冷却,在4000R/min,离心时间为12min的条件下离心,取上层清液,加入等体积的乙醇,搅拌均匀,静置30min,用真空泵抽滤,烘干,称量,计算果胶产率。
实验6植物废弃物中提取果胶

实验6植物废弃物中提取果胶实验6 植物废弃物中提取果胶一、实验目的①掌握从甜菜渣、桔皮等植物废弃物中提取果胶的原理和方法。
②了解果胶的主要性质和用途。
二、实验原理1. 主要性质和用途果胶(pectin )属多糖类植物胶,以原果胶的形式存在于高等植物的叶、茎、根等的细胞壁内,与细胞彼此粘合在一起,由水溶性果胶和纤维素结合而形成不溶于水的成分。
未成熟水果因果实细胞壁中有原果胶存在,因此组织坚实。
随着果实不断生长成熟,原果胶在酶的作用下分解为(水溶性)果胶酸和纤维素。
果胶酸再在酶的作用下继续分解为低分子半乳糖醛酸和α—半乳糖醛酸。
原果胶含量逐渐减少,因而果皮不断变薄变软。
原果胶在水和酸中加热,可分解为水溶性果胶酸。
果胶在果实及叶中的含量较多。
在橙属水果的果皮和苹果渣、甜菜渣中都含有质量分数20%~50%的果胶。
各种果实、果皮中的原果胶,通常以部分甲基化了多缩半乳糖醛酸的钙盐或镁盐形式存在,经稀盐酸水解,可以得到水溶性果胶,即多缩半乳糖醛酸的甲酯。
果胶的基本化学组成是半乳糖醛酸,基本结构是D —吡喃半乳糖醛酸以α-1,4-糖苷连接的长链,通常以部分甲酯化状态存在,其结构式为果胶水解时,产生果胶酸和甲醇等,其反应式为果胶是高分子聚合物,可以从植物组织中分离提取出来,其相对分子质量在5万~30万之间为淡黄色或白色的粉末状固体,味微酸,能溶于20倍水中生成粘稠状液体,不溶于酒精及一般的有机溶剂,若先用酒精、甘油或糖浆等浸润,则极易溶于水中。
果胶在酸性条件下稳定,但遇强酸、强碱易分解,在室温下可与)(4229710661265105332366041果胶酸O H C O H C O H C COOH CH OH CH O H O H C ++++=+强碱作用生成果胶酸盐。
果胶具有良好的胶凝化和乳化作用,在食品工业、医药工业和轻工业中有广泛的用途,他可以用于制备低浓度果酱、果胶及胶状食物,作结冻剂;用作果汁饮料、乳品、巧克力、速冻饮粉和糖果等食品中的添加剂;也可用作冷饮食品的稳定剂。
实验一果胶的提取

实验一果胶的提取
实验记录:
8:37 称取橘皮21.5g,洗净后加入250ml的烧杯中,并加水120ml;8:41 开始加热(水浴加热);
8:55 水开始沸腾;
9:01 烧杯中水温达到87℃;
9:02 开始保温(88℃);
9:14 用清水清洗橘皮并切粒;
9:20 用50℃左右的热水漂洗橘皮直到洗液为无色;
9:36 将洗净的橘皮加入0.2mol/L的HCl至浸没橘皮;
9:40 将溶液PH调节至2.0~2.5,所用的为6mol/L的氨水;
9:55 将v调节好的PH溶液加热(水浴加热),时间为40min;10:35 将恒温水浴加热后的溶液趁热过滤,收集滤液;
11:00 抽滤完毕;
11:05 待滤液冷却后,用6mol/L的氨水条件PH为3.0~4.0;
11:07 加入95%的乙醇溶液,果胶开始析出;
11:08 静置20min;
14:48 开始过滤,收集白色絮状固体;
14:52 将湿果胶加入无水乙醇;
15:11 将滤渣转移到表面皿中,在60~70℃条件下烘干。
烘干后,称其质量为1.1372g,并取一定量的果胶于烧杯中加入一定量的水,在70℃的恒温水浴中溶解,34min后果胶全部溶解。
实验数据处理:
实验结果分析与讨论:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
果胶的提取作业指导书
一、目的要求
1.学习从柑橘皮中提取果胶的方法。
2.进一步了解果胶质的有关知识。
二、实验原理
果胶物质广泛存在于植物中,主要分布于细胞壁之间的中胶层,尤其以果蔬中含量为多。
不同的果蔬含果胶物质的量不同,山楂约为6.6%,柑橘约为0.7~1.5%,南瓜含量较多,约为7%~17%。
在果蔬中,尤其是在未成熟的水果和果皮中,果胶多数以原果胶存在,原果胶不溶于水,用酸水解,生成可溶性果胶,再进行脱色、沉淀、干燥即得商品果胶。
从柑橘皮中提取的果胶是高酯化度的果胶,在食品工业中常用来制作果酱、果冻等食品。
三、实验器材
烘箱、恒温水浴锅、布氏漏斗、抽滤瓶、玻棒、尼龙布、表面皿、精密pH 试纸、(100mL、250mL)烧杯、电子天平、小刀、真空泵、柑橘皮(新鲜)。
四、实验试剂
1.95%乙醇、无水乙醇。
2.0.2 mol/L盐酸溶液:18mL HCl溶于1000mL蒸馏水中。
3.6 mol/L氨水:向100mL市售氨水(25-28%)中加入19mL水。
五、操作步骤
1.称取新鲜柑橘皮20g(干品为8g),用清水洗净后,放入250 mL烧杯中,加120 mL水,加热至90℃保温5~10 min,使酶失活。
用水冲洗后切成3~5 mm 大小的颗粒,用50℃左右的热水漂洗,直至水为无色,果皮无异味为止。
每次漂洗都要把果皮用尼龙布挤干,再进行下一次漂洗。
2.将处理过的果皮粒放入烧杯中,加入0.2 mol/L的盐酸以浸没果皮为度,调溶液的pH 2.0~2.5之间。
加热至90℃,在恒温水浴中保温40 min,保温期间要不断地搅动,趁热用垫有尼龙布(100目)的布氏漏斗抽滤,收集滤液。
3.滤液冷却后,用6mol/L氨水调至pH 3~4,在不断搅拌下缓缓地加入95%乙醇溶液,加入乙醇的量为原滤液体积的1.5倍(使其中酒精的质量分数达50%~60%)。
酒精加入过程中即可看到絮状果胶物质析出,静置20min后,用尼龙布(100目)过滤制得湿果胶。
4.将湿果胶转移于100mL烧杯中,加入30mL无水乙醇洗涤湿果胶,再用尼龙布过滤、挤压。
将脱水的果胶放入表面皿中摊开,在60~70℃烘干。
将烘干的果胶磨碎过筛,制得干果胶。
六、注意事项
1.脱色中如抽滤困难可加入2%~4%的硅藻土作助滤剂。
2.湿果胶用无水乙醇洗涤,可进行2次。
3.滤液可用分馏法回收酒精。
七、问题与思考
1.从橘皮中提取果胶时,为什么要加热使酶失活?
2.沉淀果胶除用乙醇外,还可用什么试剂?
3.在工业上,可用什么果蔬原料提取果胶?。
