柠檬酸柠檬酸钠缓冲液配制
柠檬酸柠檬酸钠缓冲液配制

柠檬酸柠檬酸钠缓冲液配制
柠檬酸柠檬酸钠缓冲液配制
柠檬酸钠缓冲液(0.1 mol/L) ﻫpH 0.1 mol/L柠檬酸(毫升)0.1mol/L柠檬酸钠(毫升)
ﻫ 3.4 16.0 4.0
3.6 14.9 5.1 ﻫ柠檬酸C6H8O7.H2O:分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7.2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
ﻫ
一水柠檬酸ﻫﻫ又名一水枸椽酸ﻫ学名: 2-羟基丙烷三羧酸,2-羟基-1,2,3-三羧酸
性状:无色结晶或白色晶状粉末
ﻫ普通特性:潮湿空气中易潮解,干燥空气中易风化,比1.542g/cm3,熔点70-75°C
ﻫ分子式: C6H8O7.H2 O ﻫ
分子量: 210.14
ﻫ主要用途:ﻫ
主要用于食品、饮料行业,并在医药、化工、洗涤等行业有广泛用途,在食品领域主要用作酸味剂和调味剂。
ﻫ
包装及贮存: 25公斤/50磅牛皮纸复合袋包装,或指定包装,干燥、密闭、阴暗处贮存。
1 / 1。
柠檬酸柠檬酸钠缓冲液的配制方法

柠檬酸柠檬酸钠缓冲液的配制方法
柠檬酸柠檬酸钠缓冲液是一种常用的生化试剂,用于调节生物体系的pH值,使其保持稳定。
它是由柠檬酸和柠檬酸钠组成的缓冲液,具有良好的缓冲效果和化学稳定性。
下面介绍一下柠檬酸柠檬酸钠缓冲液的配制方法。
1. 配制柠檬酸溶液
将柠檬酸粉末加入蒸馏水中,用磁力搅拌器将其充分搅拌至柠檬酸完全溶解。
按照需要配制的浓度,将柠檬酸的质量溶于蒸馏水中,同时用万能比重计调整溶液的比重,以制得所需的柠檬酸溶液。
取一定量的柠檬酸溶液和柠檬酸钠溶液,按照不同的比例混合,在室温下充分混合搅拌,以制得所需浓度的柠檬酸柠檬酸钠缓冲液。
一般情况下,pH值在7.0-7.4之间的缓冲液比例为1:9或1:10。
注意事项:
1. 配制柠檬酸柠檬酸钠缓冲液时,要保持实验室清洁,使用干净的玻璃仪器和器皿。
2. 柠檬酸柠檬酸钠缓冲液的配制应按比例准确称量并充分搅拌混合,避免出现误差。
3. 在配制柠檬酸柠檬酸钠缓冲液的过程中,要注意pH值的监测,确保所配制的缓冲液pH值符合要求。
4. 配制好的柠檬酸柠檬酸钠缓冲液应储存在干燥的、避光的地方,避免受潮和日光照射。
常用缓冲溶液的配制
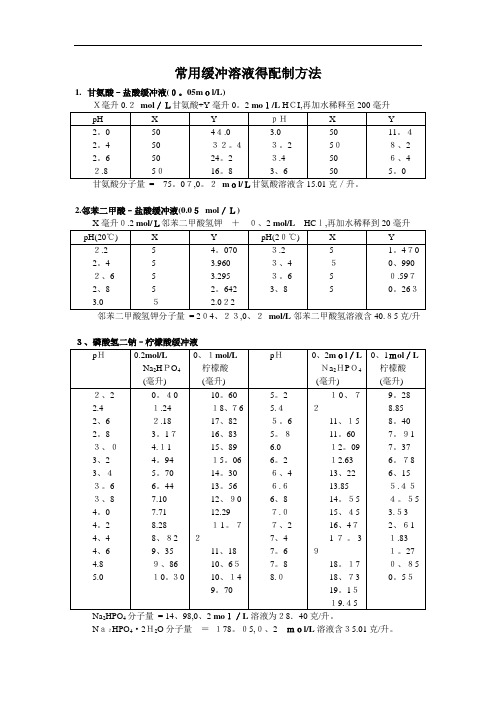
常用缓冲溶液得配制方法1.甘氨酸–盐酸缓冲液(0。
05mol/L)X毫升0.2mol/L甘氨酸+Y毫升0。
2 mol/L HCI,再加水稀释至200毫升2.邻苯二甲酸–盐酸缓冲液(0.05mol/L)邻苯二甲酸氢钾分子量= 204、23,0、2mol/L邻苯二甲酸氢溶液含40.85克/升3、磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14、98,0、2 mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量=178。
05,0、2mol/L溶液含35.01克/升。
C4H 2O 7·H 2O 分子量 = 210。
14,0。
1 m ol/L 溶液为21.01克/升。
① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存、5.柠檬酸–柠檬酸钠缓冲液(0.1 mo l/L)柠檬酸C 6H 8O7·H 2O:分子量210。
14,0.1 mol /L溶液为21.01克/升。
柠檬酸钠Na 3 C 6H5O 7·2H2O:分子量294、12,0.1 mol/L 溶液为29。
41克/毫升、Na2Ac·3H2O分子量= 136、09,0、2 mol/L溶液为27.22克/升。
7、磷酸盐缓冲液242Na2HPO4·12H2O分子量= 358。
22,0.2 mol/L溶液为71.64克/升。
Na2HPO4·2H2O分子量=156。
03,0.2mol/L溶液为31.21克/升。
Na2HPO4·2H2O分子量= 178.05,1/15M溶液为11.876克/升。
KH2PO4分子量= 136.09,1/15M溶液为9.078克/升、8.磷酸二氢钾–氢氧化钠缓冲液(0。
05M)X毫升0.2MK2PO10.Tris–盐酸缓冲液(0.05M,25℃)50毫升0。
1M三羟甲基氨基甲烷(Tris)溶液与X毫升0.1N盐酸混匀后,加水稀释至100毫三羟甲基氨基甲烷(Tris)HOCH2CH2OHCHOCH2NH2分子量=121、14;0.1M溶液为12.114克/升、Tris溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
各种缓冲液的配制方法-
各种缓冲液的配制方法之袁州冬雪创作Na2HPO4-柠檬酸钠缓冲液(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得. 醋酸-醋酸钠缓冲液(pH3.7) 取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变成纯绿色,再加水稀释至1000ml,即得.醋酸-醋酸钠缓冲液(pH3.8) 取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得.醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得. 醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得. 醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得.用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等.若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL.将称好的醋酸钠和量好的冰醋酸加入1000mL水中溶解、搅拌平均即可.当然若想配制其它的浓度,也可照公式计算即可,通常缓冲溶液不克不及配的太稀,否则缓冲才能要下降,太浓的话又华侈试剂.0.2mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时的苯二甲酸氢钾20.44g溶于水中,稀释至500ml.磷酸盐缓冲液(PBS)配制方法0.01M PBSPBS (135 mM NaCl, 2.7 mM KCl, 1.5 mM KH2PO4, and 8 mM K2HPO4,pH 7.2)称 NaCl, KCl, KH2PO4(or Na2HPO4)和 K2HPO4,溶于800 ml 蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1 L.保管于4℃冰箱中即可.需要注意的是,通常所说的浓度0.01 M指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.母液的配制:Na2HPO4:称取 Na2HPO4-12H2O,溶于 1000ml 水NaH2PO4:称取 NaH2PO4-2H2O,溶于1000ml 水各种浓度PB(pH=7.4)的配制:先配 PB (pH=7.4,100ml):取19ml 0.2mol/L的 NaH2PO4,81ml 0.2mol/L 的 Na2HPO4, 即可.然后只需将 PB (pH=7.4)按相应比例适当稀释即可,如:PB(PH=7.4):取 500ml PB,加水稀释至 1000ml 即可. PB (PH=7.4):取50ml PB,加水稀释至 1000ml 即可.PB (PH=7.4):取100ml 0.2 M PB,加水稀释至 1000ml 即可.若需要 NaCl的话,加入 NaCl 至0.9%(g/100ml)即可.另:其它各种另 PH值的 PB(100ml)配方:pH NaH2PO4(ml) Na2HPO4(ml)5.8 92 85.9 90 106.1 85 156.8 51 496.9 45 557.0 38 627.1 33 677.2 28 727.3 23 777.4 19ml 81ml7.5 16 847.6 13 877.9 7 93磷酸盐缓冲液(PBS)配制方法称取8g NaCl、 KCl、 Na2HPO4和 KH2PO4,溶于800ml蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1L即可.在15lbf/in2(1034×105Pa)高压下蒸气灭菌(至少20分钟),保管存于室温或4℃冰箱中.需要注意的是,通常所说的浓度指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.如果是用于免疫组化的话,则需要在配置的时候分别加入100 u/ml青霉素和链霉素之后再调PH、定容、灭菌消毒.PH 7.6 7.4 7.2 7.0 H2O 1000 1000 1000 1000NaCl 8.5 8.5 8.5 8.5 Na2HPO4 2.2 2.2 2.2 2.2根据经历来看,新鲜配置的PBS搅匀后其PH值约在7.2-7.4之间,可是在温度的影响下,尤其在夏天,其电离常数发生了改变,在颠末昼夜的时间后,PH值会分明改变(我亲自测过偏酸).所以做实验的同学可要注意了,PH值能够会影响实验成果,甚至能够导致阴性.所以务必记得这个时候和天气,要加强实验条件节制问题.每次使用前最好用试纸测一下过夜了的PBS,如果发生偏酸或偏碱,注意重新换新液. PBS缓冲液称取NaCl 8g,KCl ,Na2HPO4?12H2O , KH2PO4 ,溶于900ml 双蒸水中,用盐酸调pH值至7.4,加水定容至1L,常温保管备用.PBST缓冲液取300μl Tween-20 加入PBS 100ml中,混匀后即刻使用.现用现配.如果是把所有固体加大十倍,配置为稀释液,工作时候十倍稀释,那末,在刚配好稀释液时,PH在6.5左右,分明偏酸.不克不及用盐酸调.虽然可以用氢氧化钠颗粒调,但是有更方便的方法.十倍稀释以后,PH自动升高到所需要的值.不需要其它任何处理.这个可以先取少量试一试,配好之后再测一次~2. 向烧杯中加入约800 ml的去离子水,充分搅拌溶解.3. 滴加浓盐酸将pH值调节至8.0,然后加入去离子水将溶液定容至1 L.4. 高温高压灭菌后,室温保管.注意:上述PBS Buffer中无二价阳离子,如需要,可在配方中补偿1 mM CaCl2和0.5 mM MgCl2.0.05mol/L PBS(磷酸缓冲液Phosphate Buffer Solution,PBS)的配制:甲液:0.05mol/L Na2HPO4溶液:称取磷酸氢二钠,加蒸馏水至1000ml ;乙液:0.05mol/L KH2P04溶液: 称取磷酸二氢钾, ,加蒸馏水至1000m1.将甲乙液分装在棕色瓶内,于4℃冰箱中保管,用时甲、乙两液各按分歧比例混合,即可得所需pH的缓冲液,见下表: pH 甲液ml 乙液mI5.29 2.5 97.55.59 5.0 95.05.91 10.0 90.06.24 20.0 80.06.47 30.0 70.06.64 40.0 60.06.81 50.0 50.06.98 60.0 40.07.17 70.0 30.07.38 80.0 20.07.73 90.0 10.08.04 95.0 5.0你要配制pH=6.8的PBS,可用甲、乙液各50ml混合即可.硼砂易失去结晶水,必须在带塞得瓶中保管;硼砂溶液也可以用半中和的硼酸溶液代替0.02mol/LKCl溶液:溶7.455g氯化钾于水中,稀释至500ml0.02mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时额苯二甲酸氢钾20.44g溶于水中,稀释至500ml0.2mol/L磷酸二氢钾溶液:溶13.616g磷酸二氢钾于水中,稀释至500ml。
常用缓冲溶液的配制和PH计校正溶液配置方法
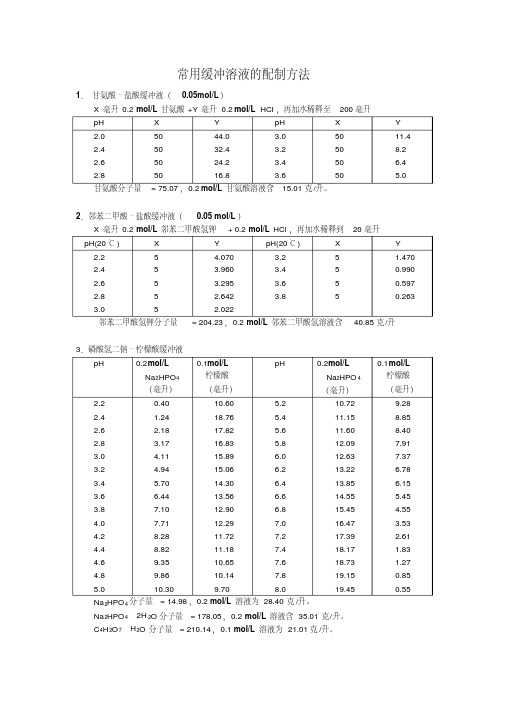
13.硼砂 - 氢氧化钠缓冲液( 0.05M 硼酸根)
X 毫升 0.05M 硼砂 +Y 毫升 0.2NNaOH 加水稀释至 200 毫升
pH
X
Y
pH
X
Y
9.3
50
6.0
9.8
50
34.0
9.4
50
11.0
10.0
50
43.0
9.6
50
23.0
10.1
50
46.0
硼砂 Na2B4O7·10H 2O,分子量 =381.43;0.05M 溶液为 19.07 克 /升。
Na2HPO 4·2H 2O 分子量 = 156.03, 0.2 mol/L 溶液为 31.21 克 /升。 (2)磷酸氢二钠 – 磷酸二氢钾缓冲液( 1/15 mol/L )
pH mol/L/15Na 2HPO 4 mol/L//15KH 2 PO4 pH mol/L//15Na 2HPO4 mol/L//15KH 2PO4
8.6
7.2
100
16.7
8.8
7.4
100
15.3
9.0
7.6
100
13.4
9.2
7.8
100
11.47
9.4
8.0
100
9.39
9.6
8.2
100
7.21
巴比妥钠盐分子量 =206.18;0.04M 溶液为 8.25 克 /升
升)
100
5.21
100
3.82
100
2.52
100
1.65
100
1.13
10.57
9
Na2CO 2·10H 2O 分子量 =286.2;0.1M 溶液为 28.62 克/ 升。 N2HCO 3分子量 =84.0;0.1M 溶液为 8.40 克 /升。
常用缓冲溶液的配制

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(L)甘氨酸分子量= ,mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(mol/L)邻苯二甲酸氢钾分子量= ,mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= ,mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= ,mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= ,mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液( mol/L )柠檬酸C 6H 8O 7·H 2O :分子量, mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C 6H 5O 7·2H 2O:分子量, mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液( mol/L )Na 2Ac·3H 2O 分子量 = , mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液()Na 2HPO4·2H 2O 分子量 = , mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = , mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = , mol/L 溶液为31.21克/升。
(2)磷酸氢二钠–磷酸二氢钾缓冲液(1/15 mol/L )18℃1M 溶液为12.114克/升。
Tris 溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
11.硼酸–硼砂缓冲液(0.2M 硼酸根)硼砂Na 2B 4O 7·H 2O,分子量=;0.05M 溶液(=0.2M 硼酸根)含19.07克/升。
柠檬酸柠檬酸钠缓冲液的配制方法

柠檬酸柠檬酸钠缓冲液的配制方法
柠檬酸柠檬酸钠缓冲液的配制方法
柠檬酸柠檬酸钠缓冲液是一种常用的生化试剂,用于调节生物体系的pH值,使其保持稳定。
它是由柠檬酸和柠檬酸钠组成的缓冲液,具有良好的缓冲效果和化学稳定性。
下面介绍一下柠檬酸柠檬酸钠缓冲液的配制方法。
1. 配制柠檬酸溶液
将柠檬酸粉末加入蒸馏水中,用磁力搅拌器将其充分搅拌至柠檬酸完全溶解。
按照需要配制的浓度,将柠檬酸的质量溶于蒸馏水中,同时用万能比重计调整溶液的比重,以制得所需的柠檬酸溶液。
取一定量的柠檬酸溶液和柠檬酸钠溶液,按照不同的比例混合,在室温下充分混合搅拌,以制得所需浓度的柠檬酸柠檬酸钠缓冲液。
一般情况下,pH值在7.0-7.4之间的缓冲液比例为1:9或1:10。
注意事项:
1. 配制柠檬酸柠檬酸钠缓冲液时,要保持实验室清洁,使用干净的玻璃仪器和器皿。
2. 柠檬酸柠檬酸钠缓冲液的配制应按比例准确称量并充分搅拌混合,避免出现误差。
3. 在配制柠檬酸柠檬酸钠缓冲液的过程中,要注意pH值的监测,确保所配制的缓冲液pH值符合要求。
4. 配制好的柠檬酸柠檬酸钠缓冲液应储存在干燥的、避光的地方,避免受潮和日光照射。
常用缓冲溶液的配置方法
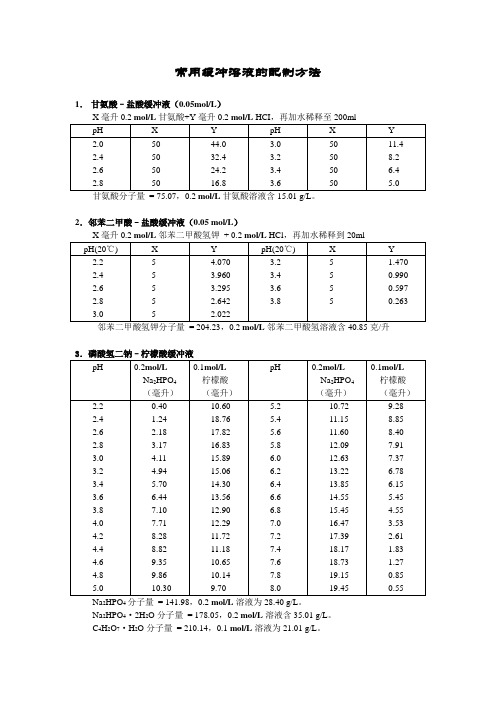
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液24Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01 g/L。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01 g/L。
① 使用时可以每升中加入1g 酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
6872柠檬酸钠Na 3 C 6H 5O7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41 g/L 。
227.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2 mol/L )Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量= 358.22,0.2 mol/L溶液为71.64克/升。
Na2HPO4·2H2O分子量= 156.03,0.2 mol/L溶液为31.21克/升。
Na2HPO4·2H2O分子量= 178.05,1/15M溶液为11.876克/升。
KH2PO4分子量= 136.09,1/15M溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05 mol/L)巴比妥钠盐分子量=206.18;0.04M 溶液为8.25克/升10.Tris –盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100吸收二氧化碳,使用时注意将瓶盖严。
11.硼酸–硼砂缓冲液(0.2M 硼酸根)硼砂Na 2B 4O 7·H 2O,分子量=381.43;0.05M 溶液(=0.2M 硼酸根)含19.07克/升。
各种缓冲液的配制方法
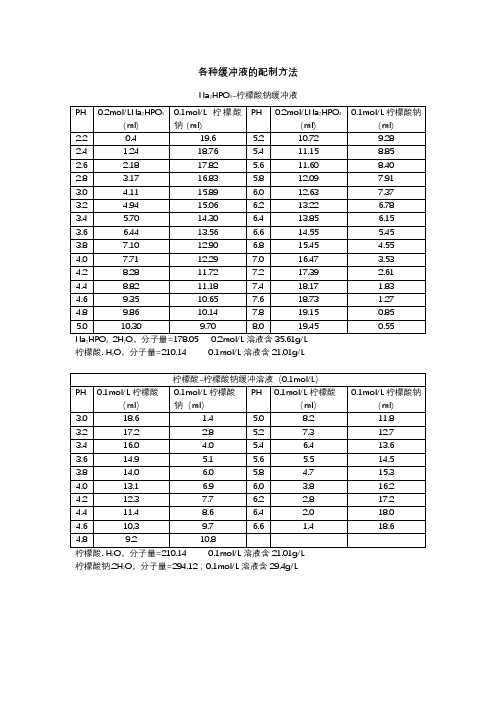
各种缓冲液的配制方法Na2HPO4-柠檬酸钠缓冲液Na2HPO4。
2H2O,分子量=178.05 0.2mol/L溶液含35.61g/L 柠檬酸. H2O,分子量=210.14 0.1mol/L溶液含21.01g/L2柠檬酸钠.2H2O,分子量=294.12;0.1mol/L溶液含29.4g/L2(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得。
醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL。
各种缓冲液的配制方法_

各种缓冲液的配制方法Na2HPO4-柠檬酸钠缓冲液24。
2柠檬酸. H2O,分子量=210.14 0.1mol/L溶液含21.01g/L2柠檬酸钠. 2H2O,分子量=294.12;0.1mol/L溶液含29.4 g/LNaAC.3 H2O,分子量=136.09 0.2mol/L溶液含27.22g/L(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得。
醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL。
各种缓冲液的配制方法-
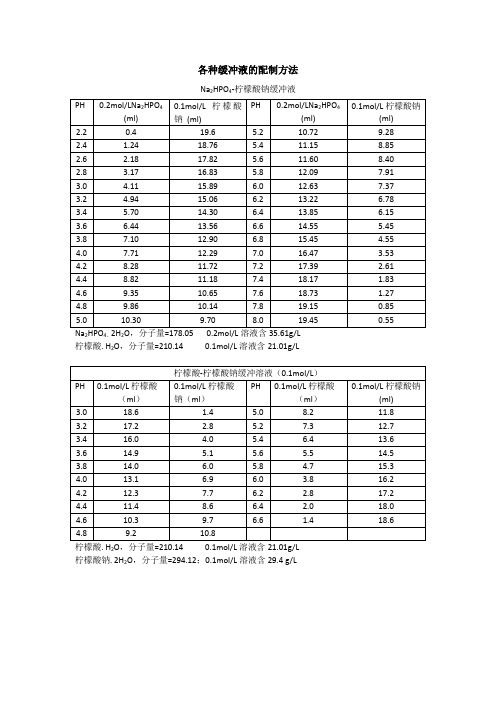
各种缓冲液的配制方法Na2HPO4-柠檬酸钠缓冲液24。
2柠檬酸. H2O,分子量=210.14 0.1mol/L溶液含21.01g/L2柠檬酸钠. 2H2O,分子量=294.12;0.1mol/L溶液含29.4 g/L2(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得。
醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL。
将称好的醋酸钠和量好的冰醋酸加入1000mL水中溶解、搅拌均匀即可。
各种缓冲液的配制方法-

各种缓冲液的配制方法之杨若古兰创作Na2HPO4-柠檬酸钠缓冲液(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水浓缩至250ml,即得. 醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝唆使液1ml 及冰醋酸60~80ml,至溶液从蓝色改变成纯绿色,再加水浓缩至1000ml,即得.醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水浓缩至1000ml,即得.醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水浓缩至1000ml,即得. 醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水浓缩至100ml,即得. 醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水浓缩至500ml,即得.用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等.若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL.将称好的醋酸钠和量好的冰醋酸加入1000mL水中溶解、搅拌均匀即可.当然若想配制其它的浓度,也可照公式计算即可,通常缓冲溶液不克不及配的太稀,否则缓冲能力要降低,太浓的话又浪费试剂.0.2mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时的苯二甲酸氢钾20.44g溶于水中,浓缩至500ml.磷酸盐缓冲液(PBS)配制方法0.01M PBSPBS (135 mM NaCl, 2.7 mM KCl, 1.5 mM KH2PO4, and 8 mM K2HPO4,pH 7.2)称NaCl,KCl,KH2PO4(or Na2HPO4)和K2HPO4,溶于800 ml 蒸馏水中,用HCl调节溶液的pH值至7.4,最初加蒸馏水定容至1 L.保管于4℃冰箱中即可.须要留意的是,通常所说的浓度0.01 M指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.母液的配制:Na2HPO4:称取Na2HPO4-12H2O,溶于1000ml 水NaH2PO4:称取NaH2PO4-2H2O,溶于1000ml 水各种浓度PB(pH=7.4)的配制:先配PB (pH=7.4,100ml):取19ml 0.2mol/L的NaH2PO4,81ml 0.2mol/L 的Na2HPO4, 即可.然后只需将PB (pH=7.4)按响应比例适当浓缩即可,如:PB(PH=7.4):取500ml PB,加水浓缩至1000ml 即可. PB (PH=7.4):取50ml PB,加水浓缩至1000ml 即可. PB (PH=7.4):取100ml 0.2 M PB,加水浓缩至1000ml 即可.若须要NaCl的话,加入NaCl 至0.9%(g/100ml)即可.另:其它各种另PH值的PB(100ml)配方:pH NaH2PO4(ml)Na2HPO4(ml)5.8 92 85.9 90 106.1 85 15 6.8 51 496.9 45 557.0 38 627.1 33 677.2 28 727.3 23 777.4 19ml 81ml 7.5 16 847.6 13 877.9 7 93磷酸盐缓冲液(PBS)配制方法称取8g NaCl、KCl、Na2HPO4和KH2PO4,溶于800ml蒸馏水中,用HCl调节溶液的pH值至7.4,最初加蒸馏水定容至1L即可.在15lbf/in2(1034×105Pa)高压下蒸气灭菌(至多20分钟),保管存于室温或4℃冰箱中.须要留意的是,通常所说的浓度指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.如果是用于免疫组化的话,则须要在配置的时候分别加入100 u/ml青霉素和链霉素以后再调PH、定容、灭菌消毒.PH 7.6 7.4 7.2 7.0H2O 1000 1000 1000 1000NaCl 8.5 8.5 8.5 8.5Na2HPO4 2.2 2.2 2.2 2.2根据经验来看,新颖配置的PBS搅匀后其PH值约在7.2-7.4之间,可是在温度的影响下,特别在炎天,其电离常数发生了改变,在经过日夜的时间后,PH值会明显改变(我亲自测过偏酸).所以做实验的同学可要留意了,PH值可能会影响实验结果,甚至可能导致阴性.所以务必记得这个时候和天气,要加强实验条件控制成绩.每次使用前最好用试纸测一下过夜了的PBS,如果发生偏酸或偏碱,留意从头换新液. PBS缓冲液称取NaCl 8g,KCl ,Na2HPO4?12H2O , KH2PO4 ,溶于900ml双蒸水中,用盐酸调pH值至7.4,加水定容至1L,常温保管备用.PBST缓冲液取300μl Tween-20 加入PBS 100ml中,混匀后即刻使用.现用现配.如果是把所有固体加大十倍,配置为浓缩液,工作时候十倍浓缩,那么,在刚配好浓缩液时,PH在6.5摆布,明显偏酸.不克不及用盐酸调.虽然可以用氢氧化钠颗粒调,但是有更方便的方法.十倍浓缩当前,PH主动升高到所须要的值.不须要其它任何处理.这个可以先取少量试一试,配好以后再测一次~2. 向烧杯中加入约800 ml的去离子水,充分搅拌溶解.3. 滴加浓盐酸将pH值调节至8.0,然后加入去离子水将溶液定容至1 L.4. 高温高压灭菌后,室温保管.留意:上述PBS Buffer中无二价阳离子,如须要,可在配方中弥补1 mM CaCl2和0.5 mM MgCl2.0.05mol/L PBS(磷酸缓冲液Phosphate Buffer Solution,PBS)的配制:甲液:0.05mol/L Na2HPO4溶液:称取磷酸氢二钠,加蒸馏水至1000ml ;乙液:0.05mol/L KH2P04溶液: 称取磷酸二氢钾, ,加蒸馏水至1000m1.将甲乙液分装在棕色瓶内,于4℃冰箱中保管,用时甲、乙两液各按分歧比例混合,即可得所需pH的缓冲液,见下表: pH 甲液ml 乙液mI5.29 2.5 97.55.59 5.0 95.05.91 10.0 90.06.24 20.0 80.06.47 30.0 70.06.64 40.0 60.06.81 50.0 50.06.98 60.0 40.07.17 70.0 30.07.38 80.0 20.07.73 90.0 10.08.04 95.0 5.0你要配制pH=6.8的PBS,可用甲、乙液各50ml混合即可.硼砂易失去结晶水,必须在带塞得瓶中保管;硼砂溶液也能够用半中和的硼酸溶液代替0.02mol/LKCl溶液:溶7.455g氯化钾于水中,浓缩至500ml0.02mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时额苯二甲酸氢钾20.44g溶于水中,浓缩至500ml0.2mol/L磷酸二氢钾溶液:溶13.616g磷酸二氢钾于水中,浓缩至500ml。
各种缓冲液的配制方法
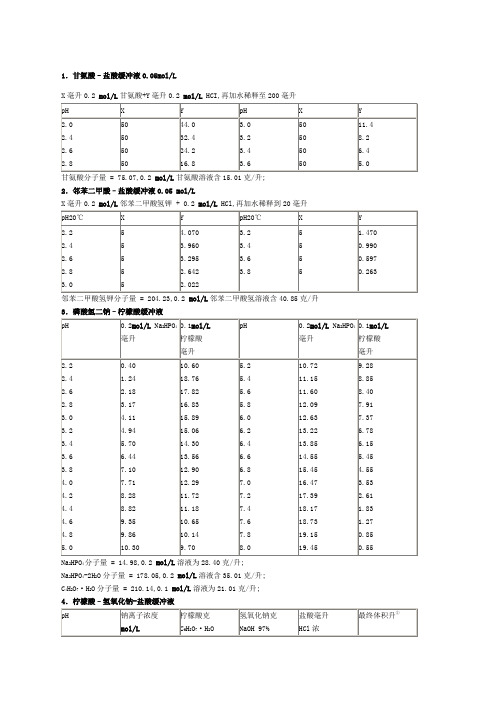
1.甘氨酸–盐酸缓冲液0.05mol/LX毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升甘氨酸分子量 = 75.07,0.2 mol/L甘氨酸溶液含15.01克/升;2.邻苯二甲酸–盐酸缓冲液0.05 mol/LX毫升0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量 = 14.98,0.2 mol/L溶液为28.40克/升;Na2HPO4-2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升;C4H2O7·H2O分子量 = 210.14,0.1 mol/L溶液为21.01克/升;4.柠檬酸–氢氧化钠-盐酸缓冲液① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存; ②5.柠檬酸–柠檬酸钠缓冲液0.1 mol/L柠檬酸C 6H 8O 7·H 2O :分子量210.14,0.1 mol/L 溶液为21.01克/升;柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升; 6.乙酸–乙酸钠缓冲液0.2 mol/LNa 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升; 7.磷酸盐缓冲液1磷酸氢二钠–磷酸二氢钠缓冲液0.2Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升; Na 2HPO 4·2H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升; Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升; 2磷酸氢二钠–磷酸二氢钾缓冲液1/15 mol/LNa 2HPO 4·2H 2O 分子量 = 178.05,1/15M 溶液为11.876克/升; KH 2PO 4分子量= 136.09,1/15M 溶液为9.078克/升; 8.磷酸二氢钾–氢氧化钠缓冲液0.05MX 毫升0.2M K 2PO 4 + Y 毫升0.2N NaOH 加水稀释至29毫升9.巴比妥钠-盐酸缓冲液18℃巴比妥钠盐分子量=206.18;0.04M溶液为8.25克/升10.Tris–盐酸缓冲液0.05M,25℃50毫升0.1M三羟甲基氨基甲烷Tris溶液与X毫升0.1N盐酸混匀后,加水稀释至100毫升;三羟甲基氨基甲烷TrisHOCH2 CH2OHCHOCH2 NH2分子量=121.14;0. 1M溶液为12.114克/升;Tris溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严; 11.硼酸–硼砂缓冲液0.2M硼酸根硼砂Na2B4O7·H2O,分子量=381.43;0.05M溶液=0.2M硼酸根含19.07克/升;硼酸H2BO3,分子量=61.84,0.2M溶液为12.37克/升;硼砂易失去结晶水,必须在带塞的瓶中保存;11.硼酸-硼砂缓冲液0.2M硼酸根硼砂Na2B4O7·10H2O,分子量=381.43;0.05M溶液=0.2M硼酸根含19.07克/升;硼酸H2BO3,分子量=61.84, 0.2M溶液为12.37克/升;硼砂易失去结晶水,必须在带塞的瓶中保存;12.甘氨酸–氢氧化钠缓冲液0.05MX毫升0.2M甘氨酸+Y毫升0.2NnaOH加水稀释至200毫升甘氨酸分子量=75.07;0.2M 溶液含15.01克/升; 13.硼砂-氢氧化钠缓冲液0.05M硼酸根X 毫升0.05M 硼砂+Y 毫升0.2NNaOH 加水稀释至200毫升 硼砂Na 2B 4O 7·10H 2O,分子量=381.43;0.05M 溶液为19.07克/升; 14.碳酸钠-碳酸氢钠缓冲液0.1M Ca 2+、Mg 2+存在时不得使用Na 2CO 2·10H 2O 分子量=286.2;0.1M 溶液为28.62克/升; N 2HCO 3分子量=84.0;0.1M 溶液为8.40克/升; 15.“PBS”缓冲液。
常用缓冲溶液的配制方法
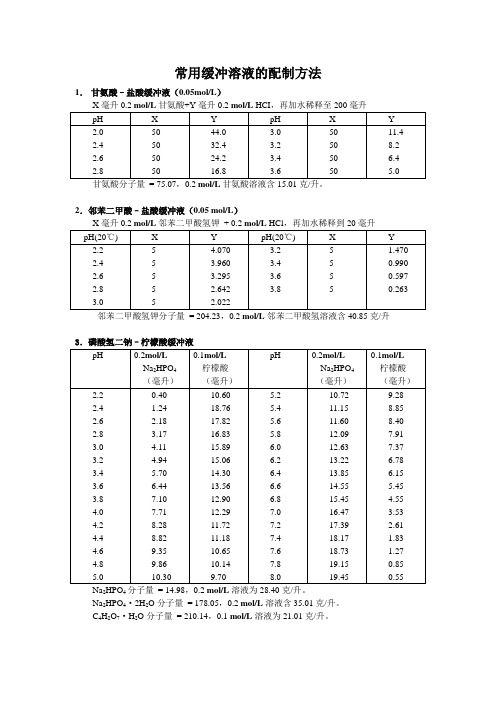
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)甘氨酸分子量= 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量= 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液液或浓盐酸调节,冰箱保存。
柠檬酸C 6H 8O 7·H 2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
Na 2HPO 4·2H 2O 分子量 = 178.05,1/15M 溶液为11.876克/升。
KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )9.巴比妥钠-盐酸缓冲液(18℃)巴比妥钠盐分子量=206.18;0.04M 溶液为8.25克/升10.T ris–盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100毫升。
PH3-10缓冲溶液配制方法

P H3-10缓冲溶液的配制方法Na2HPO4分子量= ,mol/L溶液为克/升。
Na2HPO4·2H2O分子量= ,mol/L溶液含克/升。
C4H2O7·H2O分子量= ,mol/L溶液为克/升。
①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
3.甘氨酸–盐酸缓冲液(L)4.邻苯二甲酸–盐酸缓冲液(mol/L)邻苯二甲酸氢钾分子量= ,mol/L邻苯二甲酸氢溶液含克/升6872柠檬酸钠Na3 C6H5O7·2H2O:分子量,mol/L溶液为克/升。
柠檬酸C6H8O7·H2O:柠檬酸钠Na3 C6H5O7·2H2O:H2O: 100 ml227.磷酸盐缓冲液Na 2HPO 4·2H 2O 分子量 = , mol/L 溶液为克/升。
Na 2HPO 4·12H 2O 分子量 =, mol/L 溶液为克/升。
Na 2HPO 4·2H 2O 分子量 = , mol/L 溶液为克/升。
11.硼酸–硼砂缓冲液(硼酸根)硼砂Na 2B 4O 7·H 2O,分子量=;溶液(=硼酸根)含克/升。
硼酸H 2BO 3,分子量=,溶液为克/升。
硼砂易失去结晶水,必须在带塞的瓶中保存。
11.硼酸-硼砂缓冲液(硼酸根)硼砂Na 2B 4O 7·10H 2O,分子量=;溶液(=硼酸根)含克/升。
硼酸H 2BO 3,分子量=, 溶液为克/升。
硼砂 易失去结晶水,必须在带塞的瓶中保存。
12.甘氨酸–氢氧化钠缓冲液()甘氨酸分子量=;溶液含克/升。
13.硼砂-氢氧化钠缓冲液(硼酸根) 247214.碳酸钠-碳酸氢钠缓冲液()2+2+Na 2CO 2·10H 2O 分子量=;溶液为克/升。
N 2HCO 3分子量=;溶液为克/升。
15.“PBS”缓冲液。
各种缓冲液的配制方法-

各种缓冲液的配制方法之迟辟智美创作Na2HPO4-柠檬酸钠缓冲液(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得. 醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml 及冰醋酸60~80ml,至溶液从蓝色转酿成纯绿色,再加水稀释至1000ml,即得.醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得.醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得. 醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得. 醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得.用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等.若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL.将称好的醋酸钠和量好的冰醋酸加入1000mL水中溶解、搅拌均匀即可.固然若想配制其它的浓度,也可照公式计算即可,通常缓冲溶液不能配的太稀,否则缓冲能力要下降,太浓的话又浪费试剂.0.2mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时的苯二甲酸氢钾20.44g溶于水中,稀释至500ml.磷酸盐缓冲液(PBS)配制方法0.01M PBSPBS (135 mM NaCl, 2.7 mM KCl, 1.5 mM KH2PO4, and 8 mM K2HPO4,pH 7.2)称NaCl,KCl,KH2PO4(or Na2HPO4)和K2HPO4,溶于800 ml 蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1 L.保管于4℃冰箱中即可.需要注意的是,通常所说的浓度0.01 M指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.母液的配制:Na2HPO4:称取Na2HPO4-12H2O,溶于1000ml 水NaH2PO4:称取NaH2PO4-2H2O,溶于1000ml 水各种浓度PB(pH=7.4)的配制:先配PB (pH=7.4,100ml):取19ml 0.2mol/L的NaH2PO4,81ml 0.2mol/L 的Na2HPO4, 即可.然后只需将PB (pH=7.4)按相应比例适当稀释即可,如:PB(PH=7.4):取500ml PB,加水稀释至1000ml 即可. PB (PH=7.4):取50ml PB,加水稀释至1000ml 即可. PB (PH=7.4):取100ml 0.2 M PB,加水稀释至1000ml 即可.若需要NaCl的话,加入NaCl 至0.9%(g/100ml)即可.另:其它各种另PH值的PB(100ml)配方:pH NaH2PO4(ml)Na2HPO4(ml)5.8 92 85.9 90 106.1 85 156.8 51 496.9 45 557.0 38 627.1 33 677.2 28 727.3 23 777.4 19ml 81ml7.5 16 847.6 13 877.9 7 93磷酸盐缓冲液(PBS)配制方法称取8g NaCl、KCl、Na2HPO4和KH2PO4,溶于800ml蒸馏水中,用HCl调节溶液的pH值至7.4,最后加蒸馏水定容至1L即可.在15lbf/in2(1034×105Pa)高压下蒸气灭菌(至少20分钟),保管存于室温或4℃冰箱中.需要注意的是,通常所说的浓度指的是缓冲溶液中所有的磷酸根浓度,而非Na 离子或K 离子的浓度,Na 离子和K 离子只是用来调节渗透压的.如果是用于免疫组化的话,则需要在配置的时候分别加入100 u/ml青霉素和链霉素之后再调PH、定容、灭菌消毒.PH 7.6 7.4 7.2 7.0H2O 1000 1000 1000 1000NaCl 8.5 8.5 8.5 8.5Na2HPO4 2.2 2.2 2.2 2.2根据经验来看,新鲜配置的PBS搅匀后其PH值约在7.2-7.4之间,可是在温度的影响下,尤其在夏天,其电离常数发生了改变,在经过昼夜的时间后,PH值会明显改变(我亲自测过偏酸).所以做实验的同学可要注意了,PH值可能会影响实验结果,甚至可能招致阴性.所以务必记得这个时候和天气,要加强实验条件控制问题.每次使用前最好用试纸测一下过夜了的PBS,如果发生偏酸或偏碱,注意重新换新液. PBS缓冲液称取NaCl 8g,KCl ,Na2HPO4?12H2O , KH2PO4 ,溶于900ml双蒸水中,用盐酸调pH值至7.4,加水定容至1L,常温保管备用.PBST缓冲液取300μl Tween-20 加入PBS 100ml中,混匀后即刻使用.现用现配.如果是把所有固体加年夜十倍,配置为浓缩液,工作时候十倍稀释,那么,在刚配好浓缩液时,PH在6.5左右,明显偏酸.不能用盐酸调.虽然可以用氢氧化钠颗粒调,可是有更方便的方法.十倍稀释以后,PH自动升高到所需要的值.不需要其它任何处置.这个可以先取少量试一试,配好之后再测一次~2. 向烧杯中加入约800 ml的去离子水,充沛搅拌溶解.3. 滴加浓盐酸将pH值调节至8.0,然后加入去离子水将溶液定容至1 L.4. 高温高压灭菌后,室温保管.注意:上述PBS Buffer中无二价阳离子,如需要,可在配方中弥补1 mM CaCl2和0.5 mM MgCl2.0.05mol/L PBS(磷酸缓冲液Phosphate Buffer Solution,PBS)的配制:甲液:0.05mol/L Na2HPO4溶液:称取磷酸氢二钠,加蒸馏水至1000ml ;乙液:0.05mol/L KH2P04溶液: 称取磷酸二氢钾, ,加蒸馏水至1000m1.将甲乙液分装在棕色瓶内,于4℃冰箱中保管,用时甲、乙两液各按分歧比例混合,即可得所需pH的缓冲液,见下表: pH 甲液ml 乙液mI5.29 2.5 97.55.59 5.0 95.05.91 10.0 90.06.24 20.0 80.06.47 30.0 70.06.64 40.0 60.06.81 50.0 50.06.98 60.0 40.07.17 70.0 30.07.38 80.0 20.07.73 90.0 10.08.04 95.0 5.0你要配制pH=6.8的PBS,可用甲、乙液各50ml混合即可.硼砂易失去结晶水,必需在带塞得瓶中保管;硼砂溶液也可以用半中和的硼酸溶液取代0.02mol/LKCl溶液:溶7.455g氯化钾于水中,稀释至500ml0.02mol/L苯二甲酸氢钾溶液:称取在硫酸干燥器中干燥过24小时额苯二甲酸氢钾20.44g溶于水中,稀释至500ml0.2mol/L磷酸二氢钾溶液:溶13.616g磷酸二氢钾于水中,稀释至500ml。
(最全)常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液(pH3.7):取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8.0):取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0。
三羟甲基氨基甲烷缓冲液(pH8.1):取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9.0):取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7.4):取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH 值至7.4,滤过。
巴比妥缓冲液(pH8.6):取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7.8):取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g 加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml。
甲酸钠缓冲液(pH3.3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30。
邻苯二甲酸盐缓冲液(pH5.6):取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
