二水物湿法磷酸工艺计算
二水-半水法生产湿法磷酸的技术改造探讨

二水-半水法生产湿法磷酸的技术改造探讨摘要过磷酸钙生产过程中,可采取加大磷酸浓度及减小磷石膏中P2O5含量等生产方式,这样能显著减小浓缩能耗并改善磷石膏质量的效果。
针对这一点,本文重点描述了本厂把二水法生产磷酸工艺变成二水-半水法的相关问题,如:操作步骤、新增设备、工艺指标、技术参数等等。
通过技术调整之后,磷酸ω(P2O5)由22%上升为35%,磷石膏中ω(P2O5)由1.5%减小为0.2%以下,磷石膏中的ω (H2O结晶)由14%~l6%变为4%~8%,一年内可实现节省1.5万t煤,创造的效益达1786万元。
关键词湿法磷酸;二水法改二水一半水法;工艺技术当前,湿法萃取磷酸超过90%则选择二水法流程。
产品磷酸ω(P2O5)为20%~24%;副产二水石膏,其ω(H2O结晶)14%~16%、ω(P205)为0.8%~1.5%。
广东湛化股份有限公司是全国最大的过磷酸钙(磷肥)生产企业,副产的石膏都用在生产硫酸。
使用这类工艺二水石膏烘干为半水之后再实施配料操作,对分解、煅烧生产出来的硫酸,其石膏中的ω(P205)需在1%。
如果选择二水一半水工艺发挥出来的优势更加显著,不仅副产的石膏能达到制硫酸要求,同时生产的磷酸ω(P205)也从20%~24%变为33%~39%,使得料浆浓缩的蒸汽消耗显著减小,石膏中ω(P205)则减小到0.2%以下,石膏中ω(P2O5)回收率上升1.3%,磷利用率超过99%,且石膏烘干的煤耗可降低35%的消耗。
具体分析结果如下:1 二水一半水法湿法磷酸工艺流程先进行分解反应,主要材料为磷矿浆、硫酸、滤洗液,主要反应场所在第l 反应槽完成,前后反应时间持续在1.5h~2h,磷矿浆与硫酸的加入量在投料总量中的比例达80%。
一次反应液进入第2反应槽中,并在第2反应槽中添加适量的磷矿浆与硫酸,这样可以保证分解反应更加全面,前后反应时间持续在1.5h~2h,磷矿浆与硫酸的加入量在投料总量中占20%,温度大小8O℃~93℃。
“湿法二水—半水法制磷酸”工艺流程

二水石膏转化采用硫酸、磷酸混合反应的方式进行。
上步离心分离得到的固相物料(磷石膏)进入二级串联的一级转化槽,在外加的 硫酸和适量回用的磷酸存在下,反应转化为半水物硫酸钙。反应中产生的少量含氟气 体(G-2),经微负压系统送入上步工序设置的含氟反应尾气洗涤系统,采用文丘里洗涤
酸。反应方程式为:
CqF(PQ)3+ 5H2SQ+2H2Q==3fPQ+ 5CaSQ4.-2H2Q+HFT
为避免反应生成的硫酸钙在磷矿颗粒表面形成膜层,阻碍反应继续进行,反应过 程是分成两步进行:第一步是磷矿溶解在磷酸中生成磷酸一钙;第二步是硫酸与磷酸 一钙反应生成磷酸和硫酸钙,反应方程式为:
CaF(PQ)3+ 7H3PQ+2H2。== 5Ca(H2PQ)2+HFT
半水石水料浆离暂存,
-8磷酸装置生产工艺流程图
0
成品
热磷酸储罐暂存,
然后分别去饲
*废气
菇废气
一级(1#)
回用磷
二级(2#)
回用磷
G-4
半水物洗涤过
车间滤
气液-
过滤用水
*过滤尾气
洗涤、冲洗
1论—
洗涤
*过滤
滤机
车间滤
2饲料级磷酸氢钙(DCP装置工艺流程
工艺流程介绍
采用“硫酸湿法磷酸法”工艺,主要包括净化脱硫、净化脱氟、中和离心烘干 和母液中和沉淀处理4个工段,工艺流程简述如下:
(G-3)送入闪蒸尾气洗涤塔。采用循环水对闪蒸尾气喷淋洗涤净化,净化后的气体由
水环式真空泵抽出后排放。水环式真空泵采用一次水作为补充水,排放的废液送入车 间滤布洗涤水槽,作为滤布冲洗水用。
1.5万吨磷酸毕业设计15ktaP2O5二水湿法磷酸系统工艺设计

1.5万吨磷酸毕业设计15ktaP2O5二水湿法磷酸系统工艺设计毕业论文目录设计任务书 (Ⅳ)开题报告 (Ⅵ)1 综述 (1)1.1我国磷酸工业现状 (1)1.2磷酸工业生产类型 (2)2 湿法磷酸生产的基本原理 (3)2.1湿法磷酸生产的化学反应 (3)2.1.1 化学反应 (3)2.1.2 磷矿中杂质的影响 (3)2.2硫酸钙晶型和生产方法分类 (4)2.2.1 硫酸钙的晶型 (4)2.2.2 湿法磷酸生产方法 (4)2.3硫酸钙在CaSO4-H3PO4-H2O与CaSO4-H3PO4-H2SO4-H2O体系的相平衡及转化动力学.5 2.3.1硫酸钙的结晶形态 (5)2.3.2硫酸钙在CaSO4-H3PO4-H2O三元体系的相平衡 (6)2.3.3硫酸钙在CaSO4-H3PO4-H2SO4-H2O四元体系的相平衡 (7)2.3.4 CaSO4-H3PO4-H2O体系转化动力学 (8)2.4磷矿在磷酸硫酸混合溶液中的浸取和分解过程 (10)2.5 硫酸钙的结晶 (10)2.6 生产工艺条件 (10)2.7 生产工艺流程 (12)3 湿法磷酸物料衡算 (14)3.1 全系统平衡 (14)3.1.1 进料 (15)3.1.2 出料 (15)3.1.3 逸出废气 (15)3.1.4 机械损失 (16)3.1.5 磷石膏 (16)3.2 对酸解系统作平衡 (16)3.2.1 进料 (16)3.2.2 出料 (17)3.3 对过滤部分作平衡 (17)3.3.1 进料 (17)3.3.2 出料 (17)3.4 对二次洗涤作平衡 (18)3.4.1 进料 (18)3.4.2 出料 (18)3.5 对一次洗涤作平衡 (18)3.5.1 进料 (18)3.5.1 出料 (18)3.6 P2O5平衡 (19)3.7 总物料平衡表及物料平衡图 (19)4 湿法磷酸热量衡算 (21)4.1反应热的计算 (21)4.2稀释热的计算 (24)4.3 热量衡算 (24)4.3.1 输入热量 (24)4.3.2 输出热量 (25)5 主要设备的工艺计算 (27)5.1酸解槽 (27)5.1.1 已知条件 (27)5.1.2 酸解槽的基本计算 (27)5.1.3 酸解槽的主要几何尺寸计算 (28)5.1.4 搅拌器的计算 (30)5.2盘式过滤机 (31)6 三废与治理 (38)6.1尾气回收 (38)6.2废水处理和稀酸的利用 (38)7 主要设备的技术特征 (39)致谢辞 (40)参考文献 (41)附录学院化学与材料工程系毕业设计(论文)任务书学院化学与材料工程系毕业设计(论文)开题报告1 综述1.1 我国磷酸工业现状我国是一个拥有13亿人口的大国,但人均耕地面积不足2亩,仅为世界人均耕地面积的二分之一;加上耕地逐年减少,人口逐年增加,而随着人民生活水平的提高,粮食消费又不断上升。
湿法磷酸工艺计算及其物料衡算

湿法磷酸工艺计算及其物料衡算湿法磷酸工艺是一种用于生产磷酸的常见方法。
在这个工艺中,磷矿石通过酸洗和煮沸的方式转化为磷酸。
在进行湿法磷酸工艺计算和物料衡算时,需要考虑磷矿石的成分、反应物料的摩尔比、反应效率以及产物的纯度等因素。
首先,进行湿法磷酸工艺计算时需要确定磷酸的目标产量。
根据目标产量,可以计算所需的磷矿石量。
磷矿石一般含有磷酸盐矿物,例如正磷酸钙 (Ca3(PO4)2)。
通过分析磷矿石样本,可以确定其磷酸钙的含量,从而计算所需的磷矿石量。
其次,确定所需的反应物料摩尔比。
湿法磷酸工艺中,通常使用磷酸 (H3PO4) 和硫酸 (H2SO4) 作为反应剂。
反应的化学方程式为:Ca3(PO4)2 + 3H2SO4 + 4H2O → 2H3PO4 + 3CaSO4·2H2O根据化学方程式,可以确定反应物料的摩尔比。
在计算过程中,需要考虑反应剂的纯度和反应的效率,以确保反应的正常进行和产物的纯度。
最后,进行物料衡算时,需要考虑反应剂的消耗和产物的生成。
根据反应物料摩尔比和产物的纯度,可以计算出实际所需的反应剂量和产物量。
在实际操作中,还需要考虑反应剂的循环利用和废液的处理等因素,以保证工艺的可持续发展和环境友好。
总之,湿法磷酸工艺计算和物料衡算是确定生产磷酸所需的磷矿石量、反应剂摩尔比和产物量的关键步骤。
通过合理的计算和衡算,可以确保工艺的高效运行和产物的高纯度,满足生产要求并提高工艺的经济性和可持续性。
湿法磷酸工艺是一种重要的磷酸生产工艺,广泛应用于农业、化学工业等领域。
在湿法磷酸工艺中,磷矿石经过一系列反应和处理过程,最终转化为磷酸产品。
在进行湿法磷酸工艺计算和物料衡算时,需要考虑多种因素,如反应剂摩尔比、反应效率、产物纯度等。
本文将深入探讨湿法磷酸工艺计算和物料衡算的相关内容。
首先,进行湿法磷酸工艺计算时需要确定磷酸的目标产量。
根据生产需求和市场需求,确定所需的磷酸产量。
然后,根据磷酸的化学反应方程式和磷矿石的成分,计算所需的磷矿石量。
年产26000吨P2O5湿法磷酸工艺设计_毕业设计

淮海工学院专业设计报告书题目: 26000吨/年P2O5湿法磷酸厂工艺设计系(院):化学工程学院专业:化学工程与工艺设计任务书班级:姓名:学号:一、设计题目: 26000吨/年P2O5湿法磷酸厂工艺设计。
二、设计条件:1、原料磷矿的主要成分(%):P2O5:33.95;F:4.58;CaO:47.25;Fe2O3:1.47;Al2O3:1.63;A·I:2.38;CO2:2.68;SiO2:2.28;MgO:0.42、硫酸用量:为理论用量的104%3、硫酸浓度:含H2SO492%4、转化率:98.2%5、洗涤效率:98.7%6、料浆液固比:2.87、成品稀磷酸浓度:含P2O531%8、氟逸出率(%):二水法: 1.43 半水法:45。
9、机械损失(P2O5): 4 % 。
10、水份蒸发量(以100kg磷矿为基准): 16.75 kg;如采用真空冷却,则冷却器中的蒸发水量占80%。
11、滤饼含液量(以干磷石膏为准;%):过滤后滤饼:69.48;一次洗涤后滤饼:45.26;二次洗涤后滤饼:20.37;三次洗涤后滤饼:10.3412、洗液浓度(P205)%:一次洗液:22.6;二次洗液:7.7;三次洗液:3.413、返回淡磷酸的温度(℃):6414、萃取槽排出料浆的温度(℃):7615、萃取槽排出废气的温度(℃):5516、料浆循环比:6517、磷灰石分解率(%)98.818、萃取槽排出废气的相对湿度:0.9419、料浆在萃取槽中的停留时间: 6.5 小时。
20、料浆的密度(kg/m3):147021、夏季最高月平均温度(℃):3022、不考虑萃取槽中的热量损失;23、喷嘴风压:废气温度为60℃时取5000-6000Pa,废气温度为55℃±时取1300-2800Pa。
24、过滤机漏气量:1.35m3/m2·min(按过滤机总面积计算)。
25、原料硫酸温度:20℃;26、过滤常数:qe =0.94m3/m2;K过滤=5.25;K一洗=3.42。
磷酸工艺

磷酸工艺知识讲解第一讲二水湿法磷酸工艺原理一、湿法磷酸生产化学反应原理1、反应方程式:Ca5(PO4)3F + 5H2SO4+ 5n•H2O = 5CaSO4•nH2O + 3H3PO4+ HF↑磷矿石硫酸磷石膏(副产品) 磷酸(产品) 尾气其中,未定变量n有三种值,分别为0、1/2、2,则对应的副产品也分为三种,分别为无水物、半水物与二水物。
同时对应的生产方法也分别叫:无水法、半水法与二水法。
在实际的国内乃至国际工业生产中,二水法磷酸的生产工艺占80%以上。
2、二水法磷酸工艺原理:当n=2时,1中的方程式为:Ca5(PO4)3F + 5H2SO4 + 10H2O = 5CaSO4•2H2O + 3H3PO4+ HF↑3、硫酸分解中磷矿分两步完成①磷矿首先被磷酸分解:Ca5(PO4)3F+7H3PO4=5Ca(H2PO4)2+HF② Ca(H2PO4)2与硫酸反应生成磷酸:5Ca(H2PO4)2 + 5H2SO4 + 10H2O = 5CaSO4•2H2O + 10 H3PO4由上可知,磷矿在反应槽中首先与槽内的磷酸反应,所以工艺上应将硫酸加入点放在磷矿加入点的后面位置。
4、什么叫二水湿法磷酸工艺?磷酸的工业生产方法分为热法生产与湿法生产两类。
从广义上讲,凡是用酸分解磷矿制成的磷酸,称为湿法磷酸,通常用硫酸分解磷矿,所以上述用硫酸分解磷矿,且副产品是二水物的磷酸生产工艺称为二水湿法磷酸工艺。
5、二水法工艺技术主要特点:(与半水法或其它方法相比较)①流程简单、操作稳妥可靠;②装置建厂数量最多,且单系列生产规模最大,居各种工艺之首;③对磷矿适应性强,特别对我国磷矿品位低,杂质含量高的情况尤为适用;④在较低的酸温和较低的酸浓度下操作,使得衬胶设备和不锈钢设备使用寿命延长;⑤二水石膏过滤不受过滤机类型限制,转台式、翻盘式及带式均可使用;⑥工业化磷酸装置P2O5收率一般在94%——96%之间。
二、湿法磷酸生产的原料湿法磷酸生产的主要原料是磷矿与硫酸。
“湿法二水—半水法制磷酸”工艺流程.docx

1 磷酸装置工艺流程1.1工艺流程介绍采用“湿法二水—半水法制磷酸”工艺,主要包括原料处理工段、磷酸生产和两水磷石膏转化3个工段,工艺流程简述如下:1、原料处理磷矿石经鄂式破碎机破碎至粒度达到3~13mm后,由裙边胶带输送机、圆盘喂料机送至碎矿贮斗经计量后喂入球磨机内,与工艺水混合,研磨成含水约22%的磷矿浆。
出磨矿浆经滚筒筛去除粗粒子后在矿浆池暂存,然后由矿浆泵送入磷酸装置作为原料用;粗粒子返回碎矿贮斗循环使用。
部分磷矿浆去饲钙装置用于脱硫用。
鄂式破碎机上方设置集气罩,粉尘收集后送袋式收尘器除尘,除尘后的废气(G1-1)经1#排气筒(H=15m)排放。
2、磷酸生产①反应部分来自原料工段的磷矿浆由矿浆泵送到两级串联二水萃取反应槽的一级反应槽中,在进入反应槽前磷矿浆计量其流量和密度,以维持磷矿浆加料量的恒定。
来自硫酸装置的93%的浓硫酸(不足部分外购)计量后,送到二级串联二水萃取反应槽的一级反应槽中,同时加入下步回用的含磷酸的过滤酸、洗涤酸。
各类物料在反应槽中进行化学反应,硫酸分解磷矿石生成二水合结晶硫酸钙(CaSO4·2H2O)和稀磷酸。
反应方程式为:Ca5F(PO4)3 + 5 H2SO4 + 2H2O == 3H3PO4 + 5 CaSO4.·2H2O + HF↑为避免反应生成的硫酸钙在磷矿颗粒表面形成膜层,阻碍反应继续进行,反应过程是分成两步进行:第一步是磷矿溶解在磷酸中生成磷酸一钙;第二步是硫酸与磷酸一钙反应生成磷酸和硫酸钙,反应方程式为:Ca5F(PO4)3 + 7 H3PO4 + 2H2O == 5 Ca(H2PO4)2 + HF↑5Ca(H2PO4)2 + 5 H2SO4 + 2H2O == 10 H3PO4 + 5 CaSO4.·2H2O 反应过程中生成的含氟气体(G1-2),经微负压系统送入反应尾气洗涤系统采用文丘里洗涤器(采用水作为洗涤溶液)净化处理。
“湿法二水 半水法制磷酸”工艺流程

1 磷酸装置工艺流程1.1工艺流程介绍采用“湿法二水—半水法制磷酸”工艺,主要包括原料处理工段、磷酸生产和两水磷石膏转化3个工段,工艺流程简述如下:1、原料处理磷矿石经鄂式破碎机破碎至粒度达到3~13mm后,由裙边胶带输送机、圆盘喂料机送至碎矿贮斗经计量后喂入球磨机内,与工艺水混合,研磨成含水约22%的磷矿浆。
出磨矿浆经滚筒筛去除粗粒子后在矿浆池暂存,然后由矿浆泵送入磷酸装置作为原料用;粗粒子返回碎矿贮斗循环使用。
部分磷矿浆去饲钙装置用于脱硫用。
鄂式破碎机上方设置集气罩,粉尘收集后送袋式收尘器除尘,除尘后的废气(G1-1)经1#排气筒(H=15m)排放。
2、磷酸生产①反应部分来自原料工段的磷矿浆由矿浆泵送到两级串联二水萃取反应槽的一级反应槽中,在进入反应槽前磷矿浆计量其流量和密度,以维持磷矿浆加料量的恒定。
来自硫酸装置的93%的浓硫酸(不足部分外购)计量后,送到二级串联二水萃取反应槽的一级反应槽中,同时加入下步回用的含磷酸的过滤酸、洗涤酸。
各类物料在反应槽中进行化学反应,硫酸分解磷矿石生成二水合结晶硫酸钙(CaSO4·2H2O)和稀磷酸。
反应方程式为:Ca5F(PO4)3 + 5 H2SO4 + 2H2O == 3H3PO4 + 5 CaSO4.·2H2O + HF↑为避免反应生成的硫酸钙在磷矿颗粒表面形成膜层,阻碍反应继续进行,反应过程是分成两步进行:第一步是磷矿溶解在磷酸中生成磷酸一钙;第二步是硫酸与磷酸一钙反应生成磷酸和硫酸钙,反应方程式为:Ca5F(PO4)3 + 7 H3PO4 + 2H2O == 5 Ca(H2PO4)2 + HF↑5Ca(H2PO4)2 + 5 H2SO4 + 2H2O == 10 H3PO4 + 5 CaSO4.·2H2O反应过程中生成的含氟气体(G1-2),经微负压系统送入反应尾气洗涤系统采用文丘里洗涤器(采用水作为洗涤溶液)净化处理。
半水_二水湿法磷酸工艺设计方法和工业实践

第13卷 第3期1997年云南工业大学学报Journal of Yunnan Polytechnic University Vol.13 No.31997①收稿日期:1996-08-27半水—二水湿法磷酸工艺设计方法和工业实践①廖学品 牛存镇(化工轻工工程学院,云南工业大学,昆明,650051)摘要 本文简要介绍了半水—二水湿法磷酸的工艺流程及工艺条件,并以每小时酸产量8750千克为例进行了该工艺的物料衡算、热量衡算、主要设备的工艺设计计算.关键词:半水—二水物,湿法磷酸,工艺设计前 言 近年来,随着农业对含磷肥料的需求,湿法磷酸有了较大的发展.磷酸是生产高浓度磷复肥的重要原料,磷铵、重钙等主要依赖于磷酸工业的发展.磷酸的生产方法分为热法与湿法,热法磷酸由于其能耗高、价格贵而主要用于磷酸盐的生产,而湿法磷酸目前主要用于生产高浓度复合肥料,随着湿法磷酸净化技术的不断发展,经净化后的湿法磷酸也可用于生产磷酸盐.湿法磷酸的生产广泛采用二水物流程,它具有操作控制容易、对设备材质要求较低和对磷矿适应性强等特点,因而得到广泛采用.但二水物法制得的产品酸浓度较低,通常为22%~28%P 2O 5,需将其浓缩到40%~50%P 2O 5后才能用于磷铵和重钙等高浓度复合肥料的生产,因此需增加一套浓缩装置,能耗高;另外P 2O 5的收率较低,即使在最好条件下也很少超过96%,因为要维持水平衡,要想洗涤石膏滤饼达到完全回收可溶性P 2O 5是不可能的.为提高P 2O 5回收率和磷酸浓度,近年来开发出了半水—二水流程法,其产品酸浓度可达45%P 2O 5以上,这种产品酸可以不经浓缩而直接用于生产磷铵及重钙等磷肥产品,并且P 2O 5的回收率可达99%,比二水物流程节能10%左右,得到的磷石膏质量较好,易于综合利用.但该种流程对磷矿的质量有较高要求,腐蚀性较大,技术要求较高.但因其工艺流程的先进合理,应成为湿法磷酸的又一主要生产方法.目前,云南省红河州磷肥厂从国外引进技术,按该工艺流程生产浓度为45%P 2O 5的磷酸.本文对每小时酸产量8750kg (100%P 2O 5)半水—二水物湿法磷酸装置进行工艺设计,系统地介绍了该工艺流程和工艺条件,进行了物料衡算、热量衡算、主要设备的工艺设计计算,所采用的基础数据大部分来自工业生产中的实际数据.1 半水—二水物湿法磷酸工艺流程简述 该工艺流程包括萃取系统、半水物过滤系统、转化系统、二水物过滤系统、氟回收系统.本工艺设计不包括氟回收系统的工艺设计.111 萃取系统图1 萃取系统工艺流程简图萃取系统工艺流程简图如图1.合格的磷矿粉(100%地小于116mm )在1#萃取槽中与循环料浆中的磷酸硫酸反应,萃取料浆从1#萃取槽溢流至2#萃取槽,再溢流至3#萃取槽,3#萃取槽中部份料浆用循环泵送至闪蒸冷却器进行真空冷却,以保持半水萃取系统料浆98~103℃的温度.闪蒸冷却器的料浆通过闪蒸冷却器的液封槽后一部分到1#萃取槽,其料浆流量应严格控制保证1#萃取槽的磷矿石中总CaO 只有40%析出,另一部分溢流返回到3#萃取槽中,3#萃取槽中液相游离硫酸根应控制在210%左右.闪蒸冷却器蒸发气体经除沫器后抽至氟回收系统.3#萃取槽中部分反应料浆由半水过滤给料泵送至半水真空过滤机过滤后得成品磷酸.因反应温度较高,一般均设置消泡剂系统.图2 半水过滤系统工艺流程简图主要工艺条件:1#萃取槽温度:98~103℃;2#萃取槽温度:98~102℃;3#萃取槽温度:98~103℃;闪蒸冷却器液封槽温度:91~100℃.3#萃取槽中SO 42-含量:1185%~2114%w/w ;3#萃取槽固体含量:2911%~31%w/w ;3#萃取槽中液相P 2O 5浓度:≥45%w/w.112 半水过滤系统半水过滤系统工艺流程如图2.由可进行流量控制的半水过滤给料泵把3#萃取槽的半水料浆送到半水过滤机(带式),在半水过滤机上磷酸与半水石膏得以分离.在过滤过程中有多级滤液排出,第一级滤液是少量的混浊酸,这部分浊酸放至回磷酸槽,第二级滤液是45%的成品酸进入成品酸槽,然后用成品酸泵送至贮槽.在过滤出成品酸后,半水滤饼受到三次逆流洗涤,经半水过滤机过滤后的半水石膏同滤布冲洗水一起通过半水石膏溜槽进入转化系统进行转化.主要工艺条件:91第3期廖学品,牛存镇:半水—二水湿法磷酸工艺设计方法和工业实践半水过滤机真空箱真空度:64kPa 以上; 滤饼中游离P 2O 5:≤15%;半水过滤机热水温度:45℃左右;滤饼温度:55℃左右;装置冲洗水温度:80℃;半水过滤机正常带速:7~1015m/min. 半水滤饼含水量:≤30%;1.3 转化系统转化系统工艺流程图如图3.图3 转化系统工艺流程简图图4 二水过滤系统工艺流程简图 从半水真空过滤机排出的半水滤饼通过半水石膏溜槽进入第一转化槽.经计量的硫酸给入第一转化槽,第一转化槽料浆溢流至第二转化槽.在转化系统半水物转化为二水物,“晶格”中P 2O 5进入溶液中,为加速半水物转化为二水物,将活性SiO 2加入到第一转化槽,二水料浆泵至二水过滤机进行液固分离.主要工艺条件:第一转化槽料浆温度:60~70℃;转化槽中SO 42-含量:3%~8%SO 42-;第二转化槽料浆温度:60~70℃;转化槽中固体含量:3911%~41%(w/w ).转化槽中P 2O 5浓度:6%~12%P 2O 5;114 二水物过滤系统二水过滤系统流程图如图4.二水过滤系统给料泵把转化槽中的二水料浆送至二水过滤机,在二水过滤机上二水石膏和稀磷酸得以分离.在过滤机中有三级滤液排出,第一、第二级滤液流至半水滤布/滤饼洗涤槽,一部分由半水滤饼洗涤泵送至半水过滤机进行最终滤饼洗涤,另一部分由半水滤布洗涤泵送至半水过滤机进行滤布洗涤,其洗涤液最终排入转化槽,滤饼进行两次逆流洗涤.主要工艺条件:二水过滤机真空箱真空度:64kPa 以上;二水过滤机正常带速:3~6m/min.二水滤饼含水量:≤24%;2 物料及热量衡算211 物料衡算(1)衡算条件:规模:8750(100%P 2O 5)/h 磷酸,实物产品磷酸浓度45%P 2O 5,折合02云南工业大学学报第13卷实物酸产量1944414kg/h.磷矿的化学组成:P 2O 5SiO 2Al 2O 3Fe 2O 3CaOMgO Na 2OK 2O CO 2S F CCl -灼失311816121110411124416601250123212621250115217015890ppm 0135 硫酸浓度:96%,用量为理论用量的105%,转化率为:P 2O 5:99%;Fe 2O 3:65%;Al 2O 3:80%;MgO :100%.洗涤率:9815%; 水分蒸发量:20kg 水/100kg 磷矿;料浆液固比:半水物7:3,二水物6:4;氟分配:气相:60%;液相:20%;机械损失:115%;固相:12%;损失:8%.滤饼含湿量:半水物二水物半水物过滤后含湿量:45%二水物过滤后含湿量:40%半水物一洗后含湿量:40%二水物一洗后含湿量:30%半水物二洗后含湿量:35%二水物二洗后含湿量:24%半水物三洗后含湿量:30% (2)衡算结果:(单位kg/h )(见下页图5)212 热量衡算(只对萃取系统作热量衡算)(1)基础数据矿粉比热:01770kJ/kg.k硫酸(96%,25℃)比热:114546kJ/kg.k 返回淡磷酸(38187%P 2O 5,94℃)比热:217563kJ/kg.k 磷矿的化学反应热:64418kJ/kg 磷矿萃取槽共3个搅拌器,功率:75kW磷酸稀释热:100%的磷酸稀释至62%的磷酸(45%P 2O 5)的稀释热为153181kJ/kgH 3PO 4.淡磷酸与硫酸混合稀释热:38187%P 2O 5的磷酸稀释至30117%P 2O 5的磷酸的稀释热为27175kJ/kgH 3PO 4.萃取料浆比热(100℃):2.357kJ/kg.K.(2)衡算结果输 入输 出项 目kJ/h ×106%项 目kJ/h ×106%矿粉带入热0155151122酸解料浆带出热291678666136硫酸带入热0184641189CO 2气体带出热010********回磷酸带入热201974446190SiF 4气体带出热010*********化学反应热181473541131水份蒸发带出热131068429122磷酸稀释热1185774115热损失1187834122回磷酸稀释热1120522169搅拌器作功01811183合 计4417187100100合 计441718710010012第3期廖学品,牛存镇:半水—二水湿法磷酸工艺设计方法和工业实践22云南工业大学学报第13卷图5 物料衡算结果简图(右图)3 主要设备工艺计算 基础数据:半水料浆密度:1720kg/m3;二水料浆密度:1400kg/m3;回浆倍数:3;萃取时间:1号萃取槽015h,2号萃取槽015h,3号萃取2h;转化时间:1号转化槽2h,2号转化槽2h;萃取槽及转化槽的装填系数:018;萃取槽的D/H=114转化槽的D/H=1真空带式过滤机过滤强度:1000~3000kg磷石膏(干)/m2.h.(1)1号萃取槽有效容积:146142m3;总容积:183103m3;直径D:618841m;高H:419172m;(2) 2号萃取槽同1号萃取槽.(3) 3号萃取槽同1号萃取槽.(4) 1号转化槽.有效容积:156194m3;总容积:196118m3;直径D:612978m;高H:612978m; (5)2号转化槽同1号转化槽.(6)半水真空带代过滤机.过滤强度:1000kg 磷石膏(干)/m 21h ;过滤面积:43194m 2,取为50m 2;(7)二水真空带式过滤机过滤强度:2000kg 磷石膏(干)/m 2.h ;过滤面积:21197m 2,取为25m 2.4 结束语 本文系统地介绍了半水—二水湿法磷酸的工艺流程和工艺条件,进行了物料衡算、热量衡算、主要设备的工艺设计计算,其计算结果与实际生产情况吻合得很好.本文采用的计算方法和得到的计算结果合理、可靠,对半水—二水湿法磷酸的工业生产具有非常重要的指导意义.参 考 文 献1 吴佩芝.湿法磷酸.化学工业出版社,1987,72 (法)皮埃尔.贝凯.陈明磊,张国信,华青(译).磷矿和磷酸.化学工业出版社,1988.123 化学工业部化肥司,中国磷肥工业协会.磷酸磷铵的生产工艺.成都:成都科技大学出版社,1991,74 冷元琦.化肥企业能平衡.化学工业出版社,1989,65 米蒂素依-托阿特素化学公司.M T -50半水—二水磷酸工艺.磷酸盐工业,1990,1(37)The Method &Industry Practice of T echnological Designof H alf -hydrate -Dihydrate Wet Phosphoric AcidLiao Xuepin Niu cunzheng(School of Chemical and Light Industrial Engineering ,YPU ,Kunming ,China ,650051)Abstract This paper introduced the technological process and technological conditions of half -hydrate -dihydrate wet phosphoric acid ,and for the example of output 8750kg/h (100%P 2O 5),carried out the calculation of mass balance ,the calculation of heat balance ,as well as the technological design calculation of main equipments.K ey w ords :Half -hydrate -dihydrate ,Wet phosphoric acid ,Technological design32第3期廖学品,牛存镇:半水—二水湿法磷酸工艺设计方法和工业实践。
二水物法和二水化法

二水物法和二水化法1、湿法磷酸3种工艺路线的生产原理湿法磷酸生产主要是用硫酸分解磷矿,然后将生成的磷酸与硫酸钙分离。
其主要反应式为:CasF(POA)s + 5H,SO4 + mHO--5CaSO-m/5HO + HF + 3H,P040反应分两步进行:第一步,磷矿溶解在磷酸(由后续工序返回一部分)中生成磷酸一钙;第二步,硫酸与磷酸一钙反应生成磷酸和硫酸钙。
CasF(PO4)+ 7HP04 5Ca(HPO4)2 + HF;(2)5Ca(HPO4)2 + 5H:SO4 + mH:O--5CaSO-m/5HO + 10H,PO40(3)在磷酸水溶液中硫酸钙可以3种水合晶型存在,即:无水物(CaS04)、半水物(CaSO4-1/2H,0)和二水物(CaS04-2H:0)。
硫酸钙水合结晶形态受反应过程的温度和POs浓度的影响,也受溶液中剩余硫酸浓度和杂质的影响。
在CaSO4-H,PO4-H0三元体系的相平衡中(见图1),硫酸钙水合物有2种稳定晶型:无水物、二水物。
硫酸钙结晶转化的顺序:第一种为半水物一无水物一二水物;第二种为半水物一二水物一无水物;第三种为二水物一半水物一无水物。
半水物为介稳定态,相对稳定的半水物只有在Ca0过剩时才形成;在硫酸稍过剩条件下才能促进半水物结晶的成长,获得粗大的结晶。
所以为了获得半水物粗大的结晶必须在不同单元操作下进行。
不管是无水物法、半水物法还是二水物法,都是为了获得粗大的结晶和高的磷酸浓度,使得料浆的过滤速率加快。
无水物法结晶太细,过滤困难;半水物法和二水物法能获得粗大的结晶。
半水物法是在介稳定态操作,难度大,但能获得较高的磷酸浓度;二水物法在稳定态操作,难度小,wPos较半水物法低15个百分点。
精典理论二水硫酸钙结晶区的磷酸w(P:os)为28%~32%、温度为70~80℃,但实际控制上需根据磷矿杂质、萃取结晶情况在一定区间进行调整,在这样条件下的磷酸生产称为二水物工艺,它一直是工业上使用最普遍的工艺。
湿法磷酸生产工艺

湿法磷酸生产工艺技术1. 产品性质、规格及用途:湿法磷酸生产技术采用湿法二水物流程,主要产品为44—46%P2O5的磷酸,副产品为12—18%H2SiF6的氟硅酸。
磷酸为五价磷的含氧酸,有正磷酸、偏磷酸、焦磷酸三种,通常所说的磷酸指正磷酸(H3PO4)。
纯磷酸在常温下呈透明的单斜晶体,比重为1.88g/ml,熔点为42.4℃,含P2O5 72.4%。
一般商品磷酸是含有75%或85%H3PO4的液体,溶液的冰点分别为-20℃及21℃,低于此温度时将析出半水物结晶,磷酸对皮肤有腐蚀性,能吸收空气中的水份,为中强酸。
磷酸的用途很广。
湿法磷酸主要用于生产肥料,如磷酸一铵、磷酸二铵、重过磷酸钙、沉淀磷肥、过磷酸、液体肥料等。
其次用于工业磷酸盐的生产,如磷酸一钙、磷酸二钙、磷酸三钙、磷酸一钠、磷酸二钠、磷酸三钠等。
副产品氟硅酸的无水物是无色气体,不稳定,易分解为四氟化硅和氟化氢。
氟硅酸水溶液呈无色,具有强酸性,有腐蚀性,能腐蚀玻璃。
氟硅酸有消毒性能,主要用于生产氟硅酸盐和冰晶石,并用于电镀、啤酒消毒、木材防腐等。
2、生产原理湿法磷酸生产技术采用湿法二水物流程,单槽单浆、表面冷却、干法排渣、强制循环真空蒸发浓缩生产工艺。
2.1磷矿与硫酸反应1 反应原理磷矿的主要成分为氟磷酸钙Ca5F(PO4)3,另外还含有铁盐、镁盐、铝盐、钠盐、钾盐、碳酸盐、活性二氧化硅、酸不溶物等物质。
⑴磷矿与硫酸在反应槽内主要发生下列反应:Ca5F(PO4)3+5H2SO4+溶液5CaSO4 ·2H2 O+3H3PO4+HF+溶液生成的氢氟酸进一步与活性二氧化硅反应,得到氟硅酸:6HF+SiO2H2SiF6+2H2O当活性SiO2过量存在时,将继续发生下列反应:H2SiF6+SiO23SiF4+2H2OH2SiF6不稳定,受热易发生分解:H2SiF62HF+SiF4因此反应槽排出的尾气中含有HF和SiF4气体。
⑵磷矿中含有的碳酸盐与硫酸反应,产生二氧化碳气体,在反应槽液面上形成泡沫:CaCO3·MgCO3+2H2SO4CaSO4·2H2O+MgSO4+2CO2↑泡沫的产生会影响反应过滤正常运行,应设法消除。
“湿法二水—半水法制磷酸”工艺流程

1 磷酸装置工艺流程工艺流程介绍采用“湿法二水—半水法制磷酸”工艺,主要包括原料处理工段、磷酸生产和两水磷石膏转化 3 个工段,工艺流程简述如下:1、原料处理磷矿石经鄂式破碎机破碎至粒度达到 3~13mm后,由裙边胶带输送机、圆盘喂料机送至碎矿贮斗经计量后喂入球磨机内,与工艺水混合,研磨成含水约 22%的磷矿浆。
出磨矿浆经滚筒筛去除粗粒子后在矿浆池暂存,然后由矿浆泵送入磷酸装置作为原料用;粗粒子返回碎矿贮斗循环使用。
部分磷矿浆去饲钙装置用于脱硫用。
鄂式破碎机上方设置集气罩,粉尘收集后送袋式收尘器除尘,除尘后的废气 (G1-1) 经1#排气筒( H=15m)排放。
2、磷酸生产①反应部分来自原料工段的磷矿浆由矿浆泵送到两级串联二水萃取反应槽的一级反应槽中,在进入反应槽前磷矿浆计量其流量和密度,以维持磷矿浆加料量的恒定。
来自硫酸装置的 93%的浓硫酸 (不足部分外购) 计量后,送到二级串联二水萃取反应槽的一级反应槽中,同时加入下步回用的含磷酸的过滤酸、洗涤酸。
各类物料在反应槽中进行化学反应,硫酸分解磷矿石生成二水合结晶硫酸钙( CaSO4· 2H2O)和稀磷酸。
反应方程式为:Ca5F(PO4) 3 + 5 H 2SO4 + 2H 2O == 3H3PO4 + 5 CaSO4.·2H2O + HF↑为避免反应生成的硫酸钙在磷矿颗粒表面形成膜层,阻碍反应继续进行,反应过程是分成两步进行:第一步是磷矿溶解在磷酸中生成磷酸一钙;第二步是硫酸与磷酸一钙反应生成磷酸和硫酸钙,反应方程式为:Ca5F(PO4) 3 + 7 H 3PO4 + 2H 2O == 5 Ca(H 2PO4) 2 + HF↑5Ca(H2PO4) 2 + 5 H 2SO4 + 2H 2O == 10 H3PO4 + 5 CaSO4. ·2H2O反应过程中生成的含氟气体( G1-2),经微负压系统送入反应尾气洗涤系统采用文丘里洗涤器(采用水作为洗涤溶液) 净化处理。
湿法磷酸生产饲料级磷酸氢钙

调整过滤负荷和过滤机转速来实现。对洗涤率影响很大。 3、防止边壁效应。
石膏开裂造成洗水短路。 4、提高洗水温度。(70~80℃) 5、利用添加剂。 6、调节洗水分布器位置和选择合适的滤布。
2、磷酸氢钙中和
经过脱氟净化后的磷酸用石灰乳进行中和,反应如下: 2H3PO4+Ca(OH)2=Ca(H2PO4)2·H20+H2O H3PO4+Ca(OH)2=CaHPO4·2H2O ①、缓慢向磷酸中加入石灰乳 ②、控制适宜的中和温度:温度低于20℃,磷酸氢钙沉淀析出
细小晶体;温度升高到40-60 ℃时,结晶增大;超过60 ℃时, 磷酸氢钙的结晶形状和大小骤变,出现形状不规则的微细结 晶。因此中和反应温度以50 ℃左右为宜。 ③、控制适宜的PH值:当溶液PH值小于4.8时,磷酸的第一个 氢当出离溶;子液当P被溶H中液值和P等H,于值反4升.应8至时主6,.要0磷时生酸,成氢磷磷钙酸酸(的二C第氢a二钙HP个(O氢C4.a2离(HH子22OP完)O全4开)被2始)中析; 和,磷酸氢钙完全析出,当溶液PH值大于6.0时,磷酸的第 三个氢离子开始被中和,主要形成有无定型磷酸三钙。
②、矿份细度
磷矿的分解速度与矿表面积成正比,酸解反 应对磷浆的细度有一定的要求,因此提高矿 细度,增加比表面积,从而加快酸解速度, 提高矿的分解率;但过细的会增加动力消耗, 太细也有不利之处,矿浆中的一些酸不溶物 作为泥质颗粒会堵塞过滤孔道,导致过滤强 度和洗涤率的降低,同时反应槽加矿区由于 反应剧烈造成局部过饱和现象
工艺指标
中和后PH值: 5.8-6.5; 反应前的温度:36-40℃; 中和终点温度: 40-50℃;
二水物湿法磷酸工艺计算
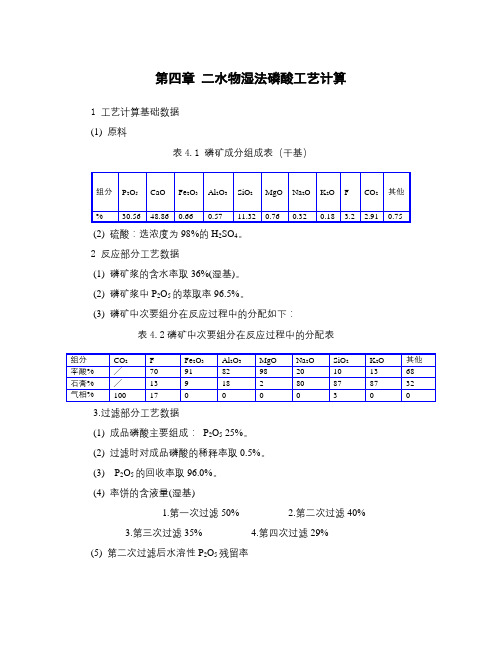
第四章二水物湿法磷酸工艺计算1 工艺计算基础数据(1) 原料表4.1 磷矿成分组成表(干基)(2) 硫酸:选浓度为98%的H2SO4。
2 反应部分工艺数据(1) 磷矿浆的含水率取36%(湿基)。
(2) 磷矿浆中P2O5的萃取率96.5%。
(3) 磷矿中次要组分在反应过程中的分配如下:表4.2磷矿中次要组分在反应过程中的分配表3.过滤部分工艺数据(1) 成品磷酸主要组成:P2O5 25%。
(2) 过滤时对成品磷酸的稀释率取0.5%。
(3) P2O5的回收率取96.0%。
(4) 率饼的含液量(湿基)1.第一次过滤50%2.第二次过滤40%3.第三次过滤35%4.第四次过滤29%(5) 第二次过滤后水溶性P2O5残留率R 1=氧化二磷洗涤前率饼中水溶性五五氧化二磷洗涤后率饼中水溶性 =0.3(6) 第三次洗涤后水溶性P 2O 5残留率R 2=氧化二磷洗涤前率饼中水溶性五五氧化二磷洗涤后率饼中水溶性 =0.15(7) 第四次过滤后水溶液中P 2O 5浓度为1.13%4 计算过程及结果 以1000Kg 磷矿(干基)为准: 1)磷矿用量:1000kg(干基) 磷矿浆量:5.1562%)361(1000=-kg已知成品磷酸为80万t/a ,折成小时磷矿消耗量为:干基量4201022.5300100.995/(130.56%96%)t h ⨯⨯=⨯⨯ 矿浆量100.995157.805/(136%)t h =- 2)硫酸用量(1) 假定磷矿中的MgO 全部以MgCO 3形式存在,多余的CO 2则以CaCO 3形式存在,矿中的F 及P 2O 5分别以Ca 5F(PO 4)3及CaF 2形式存在。
MgCO 3与H 2SO 4反应生成MgSO 4,而MgSO 4在磷酸溶液中呈离子状态,故计算成品磷酸中游离硫酸时将MgSO 4计入,而计算硫酸消耗时不再列入。
假定成品磷酸中不含Ca 2+。
(2)计算1000Kg 磷酸矿中各种Ca 的量。
磷酸生产工艺

(2)矿份细度
磷矿的分解速度与矿表面积成正比,提高矿粉细度,可 以加快反应速度;但矿粉过细会增加动力消耗,局部硫酸 钙浓度瞬间增高,造成硫酸钙局部过饱和影响结晶。
(3)搅拌强度
一定的搅拌强度可使物料充分接触,保证传质传热均匀, 使局部环境稳定,但过强的搅拌会使已有的结晶相互碰撞 导致破碎。
(4)回浆量
液相SO3含量过低不利于反应的充分进行,同时硫酸 钙的形成速度也会降低; SO3含量过高时,硫酸钙形成 速度过快,浓度过高会导致析出大量细小结晶。因此,在 调节过程中,应注意控制硫酸的加入量以及加入速度,过 浓过快斗不利于结晶的形成、长大。
保证液相中一定量的SO3浓度可以降低磷酸根的取代 作用;一定的SO3浓度还影响磷酸的生产成本。
由相平衡图可以看出,在一定的反应环境下, P2O5浓 度影响结晶种类和形式。
当矿中MgO及R2O3含量增加时,滤液密度应降低以防止 磷酸盐的大量形成。
(8)料将含固量
保证料浆固含量可以提高搅拌效果,同时合理控制生 产负荷。
固含量过低导致生产负荷降低,装置能力无法提高; 含量过高时,搅拌过程中离子间碰撞加剧,剪切力增大, 容易使结晶变小,不利于输送和过滤。
二水-半水物平衡曲线
二水-无水物平衡曲线
Ⅰ 半水→无水→二水
磷酸浓度P2O5%
CaSO4·nH2O对应的P2O5-T平衡曲线
温度℃
110 100
90 80 70 60 50 40 30 20 10
0
0
Ⅲ Ⅱ
Ⅰ
5 10 15 20 25 30 35 40 45 50
P2O5%
反应控制条件
(1)停留时间τ
当原矿中Mg、R2O3含量高时,过高的固含量会加大结 晶取代作用,导致磷损失。
日产333T P2O5二水法湿法酸物热计算(磷酸、磷铵、重钙技术与设计手册P217-224)天蓝公司

日产333T P2O5二水法湿法酸物热计算(磷酸、磷铵、重钙技术与设计手册P217-224)天蓝公司。
一、工艺计算基础数据:1、原料:马边精磷矿的化学组成(干基)组成:P2O5CaO Fe2O3A12O3MgO SiO2K2O Na2O CO2 F 酸溶物SO3 含量%:31.39 39.95(偏低)0.88 1.30 0.6(低)8.91 0.054 0.73 4.40 3.11 8.57?0.11(查设计手册资料P142)矿浆含水≤35% 温度40℃硫酸98% 温度40℃2、成品磷酸22-28%取25%3、料浆液固比:2:14、氟的分配:气相5%、固相25%、液相70%5、滤饼含液量(湿基),过滤后41%、一洗后30%、二洗后28%、三洗后23%二、物料计算:以1000kg P2O5磷酸为计算基准:1、计算:磷矿成分核查E=31.39%+8.91%+0.11%+4.40%+1.30%+39.95%+0.88%+0.6%+0.054%+0.73%+0.58%×3.11%=90.12% 磷矿成份分析<97%,检查分析成份是否有错或遗漏。
分成份可靠有问题。
2、反应槽液相磷酸密度ρL杂质系数I=(0.7×0.88+0.5× 1.3+0.6×0.6-1.2× 3.11+0.8×0.73+0.029)/31.39=-0.04756温度系数F=(0.38+0.8×25%)×(85-25)=34.8ρL=1000+【820+670×(-0.04756) 】×25%+718×(25%)2.58-34.8=1207.1kg/m33 、未反应P2O5损失L O一般为0.3—0.5%取0.4%L=5.54×10-5×(39.95/31.39)×25%×1207×100%=2.13%水溶性P2O5损失0.5—1.0%取0.75%4、反应收率:Rd=1-0.4%-2.13%=97.47%过滤收率:Rt=1-0.75%=99.25%总P2O5收率Rt=97.47%+99.25%-1=96.72%5、硫酸比耗量:MSA=1.745×39.95%-0.718×31.39%(1-96.72%)-1.225×0.11%+0.015×31.39%/25%=0.70722kgH2S04/kg干矿(偏低?)6、石膏值:G=3.07×(39.95%-0.002×96.72%×31.39%/25%)+8.91%-0.53×3.11%=1.2916kg/kg干矿7、矿浆量:1000/(96.72%×31.39×65%)=5067.328kg干矿:1000/(96.72%×31.39%)=3293.76 kg含P2O53293.76×31.39%=1033.91kgF :3293.76×3.11%=102.436kgH2O:5067.328kg-3293.76=1773.568kg8、硫酸量:0.70722×3293.76/98%=2376.95kg其中H2S04:2329.41kg、H2O:47.54kg硫酸过量3~5% 取4%,则1.04×2376.95=2472.0 kg/吨P2O5。
二水法湿法磷酸生产中提高磷收率的探讨

2005年7月第20巷第4期磷肥与夏肥Phosphate8LCompoundFertilizerJuly2005V01.20NO.4二水法湿法磷酸生产中提高磷收率的探讨邓金玉(安徽六国化工股份有限公司,安徽铜陵244023)[关键词]湿法磷酸;磷收率[摘要]安徽六国化工股份有限公司现有两套磷酸装置,磷回收率仅为91%左右,达不到设计(大于93%)要求。
介绍公司通过提高转化率、洗涤率来提高系统磷收率所采取的系列措施,使磷收率提高到94.5%以上,全年可节约矿粉约3000t,年成本降低18万元。
[中图分类号]TQ126.3+5[文献标识码]A[文章编号]1007—6220(2005)04-0034—03ApproachtoincreaseP205recoveryinproductionofWPAbydihydrateprocessDENGJin—yu(AnhuiLiuguoChemicalCo.,厶d。
Tongling,Anhui244023,China)Keywords:wet—processphosphoricacid;phosphorusrecoveryrateAbstract:Thereare2phosphoricacidfacilitiesinLiuguoChemicalCo.,Ltd.,withphosphorusrecoveryrateof91%andlowerthanthedesignedindex(morethan93%).Thecountermeasuresforimprovingphosphorusrecoveryrate(raisingconvertingrateandwashingrate)areadoptedandtheindexhasincreasedtoover94.5%,savingphosphatepowderof3000tonsorloweringcOStof180thousandRMBY11an.磷收率是二水法湿法磷酸生产中一项主要的经济技术指标,它的高低直接影响磷矿的消耗。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章二水物湿法磷酸工艺计算1 工艺计算基础数据(1) 原料表4.1 磷矿成分组成表(干基)(2) 硫酸:选浓度为98%的H2SO4。
2 反应部分工艺数据(1) 磷矿浆的含水率取36%(湿基)。
(2) 磷矿浆中P2O5的萃取率96.5%。
(3) 磷矿中次要组分在反应过程中的分配如下:表4.2磷矿中次要组分在反应过程中的分配表3.过滤部分工艺数据(1) 成品磷酸主要组成:P2O5 25%。
(2) 过滤时对成品磷酸的稀释率取0.5%。
(3) P2O5的回收率取96.0%。
(4) 率饼的含液量(湿基)1.第一次过滤50%2.第二次过滤40%3.第三次过滤35%4.第四次过滤29%(5) 第二次过滤后水溶性P2O5残留率R 1=氧化二磷洗涤前率饼中水溶性五五氧化二磷洗涤后率饼中水溶性 =0.3(6) 第三次洗涤后水溶性P 2O 5残留率R 2=氧化二磷洗涤前率饼中水溶性五五氧化二磷洗涤后率饼中水溶性 =0.15(7) 第四次过滤后水溶液中P 2O 5浓度为1.13%4 计算过程及结果 以1000Kg 磷矿(干基)为准: 1)磷矿用量:1000kg(干基) 磷矿浆量:5.1562%)361(1000=-kg已知成品磷酸为80万t/a ,折成小时磷矿消耗量为:干基量4201022.5300100.995/(130.56%96%)t h ⨯⨯=⨯⨯ 矿浆量100.995157.805/(136%)t h =- 2)硫酸用量(1) 假定磷矿中的MgO 全部以MgCO 3形式存在,多余的CO 2则以CaCO 3形式存在,矿中的F 及P 2O 5分别以Ca 5F(PO 4)3及CaF 2形式存在。
MgCO 3与H 2SO 4反应生成MgSO 4,而MgSO 4在磷酸溶液中呈离子状态,故计算成品磷酸中游离硫酸时将MgSO 4计入,而计算硫酸消耗时不再列入。
假定成品磷酸中不含Ca 2+。
(2)计算1000Kg 磷酸矿中各种Ca 的量。
Ca 5F(PO 4)3的量:1000⨯103⨯30.56%⨯1421⨯32=1434.742mol 2CaF 的量:(31100010 3.2%1434.74219⨯⨯⨯-)⨯0.5=124.735 mol 3MgCO 的量:311000100.76%188.53940.31⨯⨯⨯= mol 3CaCO 的量:31100010 2.91%188.53944⨯⨯⨯-=472.825 mol(3) 各种钙盐消耗硫酸量:Ca5F(PO4)3的消耗量1434.74296.5%5981000⨯⨯⨯=678.418kg2CaF的消耗量:124.7359812.2241000⨯=kg3CaCO消耗量:472.8259846.3371000⨯=kg(4)成品酸中的游离硫量1100032.2%96.5% 2.9%96.5%33.01125%⨯⨯⨯⨯⨯=kg(5)消耗硫酸总计678.41812.22446.33733.011769.99+++=kg 折算成98%的H2SO4为:1769.99785.70498%⨯=kg折算成SO3的量为:1769.9980628.56398⨯⨯=kg3)成品磷酸组成:(1)成品磷酸中个组分量P2O5=100030.56%96.5%294.904⨯⨯=kgSO3=11100032.2%96.5% 2.9%96.5%8026.94825%98⨯⨯⨯⨯⨯⨯⨯=kgFe2O3=10000.66%91% 6.006⨯⨯=kg Al2O3 =10000.57%82% 4.674⨯⨯=kg SiO2=100011.32%10%11.32⨯⨯=kg K2O=10000.18%13%0.234⨯⨯=kg Na2O=10000.32%20%0.64⨯⨯=kg MgO=10000.76%98%7.448⨯⨯=kg F=1000 3.2%70%22.4⨯⨯=kg其他=10000.75%68% 5.1⨯⨯= kg (2)总磷酸量:294.9041179.61625%= kg(3)成品磷酸中水的计算在磷酸中的水可以分为自由水和结合水两种,结合水的计算采用阴阳离子平衡方法。
非金属和其他氧化物:52O P SO 3 SiF 4 F 等。
金属及其他氧化物:Fe 2O 3 Al 2O 3 MgO Na 2O K 2O 等。
判断F 与Si 是否平衡,首先判断磷酸中F 与Si 是否平衡,如果是Si 过量,则酸中F 以SiF 62-的形式存在,多余的Si 以SiO 2的形式存在,如果是F 过量,则酸中Si 全部以 SiF 62-的形式存在,多余的F 以F -形式存在。
FSiO M :M 2=11.3260.10.16022.419=<0.1667 说明F 过量。
阴离子组 物质的量:P 2O 5 =1294.904612.461142⨯⨯=kmol SO 3=1226.94820.67480⨯⨯⨯= kmolSiO 2=111.3220.37760.1⨯⨯= kmolF=11.321[22.4(619)]10.04960.119-⨯⨯⨯⨯= kmol小计:13.561 kmol 阳离子组物质的量:Fe 2O 3=16.00660.231159⨯⨯= kmolAl 2O 3=14.67460.273102⨯⨯= kmol MgO=17.44820.37040.31⨯⨯= kmol Na 2O 、K 2O 及其他物质的量均用Na 2O 的值代替1(0.640.234 5.1)20.19362++⨯⨯= kmol小计:1.067 kmol结合水量:113.5611.06718112.4462-⨯⨯=()kg由于在计算干物质时以氧原子代替SiF 62-、F -等形式等量的氧为:SiO 2→SiF 6→O116(11.32142.1) 3.01460.1142.1⨯⨯⨯=kgF→O 11(22.411.32619)160.39160.1192-⨯⨯⨯⨯⨯=⨯kg小计 :3.405 kg总干物质的量:294.904+26.948+6.006+4.674+11.32+0.64+0.234+7.448+22.4+5.1+112.446-3.405=488.715 kg自由水量:1179.6-488.715=690.885 kg(4)成品磷酸组成:表4.3成品磷酸组成表以上合计 100.766 调整-0.766,总计100 4 磷石膏组成(1)磷石膏的组成量(kg )CaO =100048.86%488.6⨯=P 2O 5=()100030.56%196.5%10.696⨯⨯-=SO 3=()1678.41812.22446.33780601.61598++⨯⨯= Fe 2O 3=10000.66%90%0.594⨯⨯= Al 2O 3=10000.57%18% 1.206⨯⨯= SiO 2=100011.32%87%98.484⨯⨯= Na 2O=10000.32%80% 1.84⨯⨯= MgO=10000.76%2%0.152⨯⨯= K 2O=10000.18%87% 1.566⨯⨯= F=10003.2%13% 4.160⨯⨯=其他=10000.75%32% 2.4⨯⨯= 结晶水()1678.41812.22446.337182270.76798++⨯⨯⨯= (2)干物质中扣除与F 相当的氧的物质的量为:F→O 14.16161.751192⨯⨯=⨯kg(3)干物质总两量为:488.6+10.696+601.615+0.594+1.026+98.484+0.152+1.84 +1.566+4.16+2.4+270.767-1.751=1480.149 kg(4)磷石膏的组成表4.5磷石膏的组成表以上合计100.1,调整-0.1,总计1005 反应料浆量反应后磷酸料浆中固体含量即干物质总量为1480.149 kg 已知料浆含固量为33%所以料浆量:1480.1494485.333%= kg6.反应过程中排出气体的量,排出气体含CO 2、HF 、SiF 4和H 2O 。
各组分的量分别为: CO 2:1000 2.91%29.1⨯= kgSiF 4:1100011.32%3%104 5.87760.1⨯⨯⨯⨯= kg HF :11[1000 3.2%17%100011.32%2%4]201.2061960.1⨯⨯⨯-⨯⨯⨯⨯⨯=()() kg反应槽排出的水与闪蒸冷却蒸发水的计算,假定其总和为S=164.35 kg7.回磷酸量及其组成: (1) 对反应槽进行物料衡算,则有回磷酸量+磷矿浆量+硫酸量=磷酸料浆量+反应过程中排出的气体量+闪蒸冷却水量+反应槽蒸发水量回磷酸=4485.3+(29.1+5.877+1.206)-1562.5-785.704+S=2173.279+170.34=2343.619 kg(2) 对反应槽进行P 2O 5平衡1[(4485.31480.149)(25%0.5%)100030.56%96.5%]20.115%2343.619-⨯+-⨯⨯⨯=(3) 假定回磷酸是由成品磷酸稀释而成,故回磷酸组成(%)如下:表4.6 回磷酸组成表8 热平衡计算数据 (1) 物料温度:磷矿浆 40℃ 磷酸料浆温度 78℃ 回磷酸 62℃98% H 2SO 4 40℃磷酸料浆闪蒸冷却温差2.7℃萃取槽尾气65℃(2) 大气参数:环境温度 15℃ 相对湿度 78% 大气压 91.9KPa(3) 比热容干磷矿粉比热容:0.92 KJ/(kg ·℃) 矿浆比热容:0.9264% 4.184(164%) 2.095/()KJ kg ⨯+⨯-=℃98%硫酸比热容:239.61714.3870.98 6.1540.98 1.86010(4020) 1.466/()p C KJ kg -=-⨯+⨯+⨯⨯-=℃磷酸料浆比热容:24.184 4.97825.5%0.38825.5% 2.940/()p C KJ kg =-⨯+⨯=℃回磷酸比热容:24.184 4.97820.115%0.38820.115% 3.198/()p C KJ kg =-⨯+⨯=℃ (4) 生成热 (25℃ KJ/mol )Ca 5F(PO 4)3(s)-6813.8 Fe 2O 3(s) -824.80H 2O (l) -286.03FePO 4(s)-1297.0CaSO 4.2H 2O (s) -2022.47 Al 2O 3(s) -1676.80MgCO 3(s) -1113.68 AlPO 4(s) -1735.0 MgSO 4(s) -1278.88CaCO 3(s)-1207.68 HF (g) -271.30 CO 2(g) 393.77 CaF 2(s)-1215.40 SiF 4(g) -1549.10 SiO 2(s)-909.66H 2SiF 6(g)-2332.88 H 2SO 4(l)(100%)-909.8759 显热热量平衡计算的温度基准25℃,单位KJ(1) 磷矿浆 2.0951562.5(4025)49101.563KJ ⨯⨯-=(2) 98%硫酸 1.466769.99(4025)16932.080KJ ⨯⨯-= (3) 回磷酸 3.1982343.619(6225)277345.206KJ ⨯⨯-= (4) 搅拌产生热量:搅拌桨装机功率850kW18503600=30298.530100.995KJ ⨯⨯10 热损失计算反应槽和过滤热量损失为5%(49101.56316932.080277345.20630298.530)0.0518683.869KJ +++⨯= 11硫酸的稀释热假如在反应过程中加入反应器的浓硫酸先稀释到料浆液相的硫酸根浓度,然后再与磷矿反应。
