新人教版化学选修4第四章第三节《电解池》
合集下载
4.3《电解池》课件(新人教版选修4)

阳极
阴极
氧
氢
气
气
实例
电极反应
浓度 PH 复原 值
Na2SO4
阴极(H+ Na+) :4H ++ 4e- = 2H2 ↑ 阳极(OH- SO42-): 4OH-- 4e- = 2H2O+O2 ↑ 变大
通电 2H2O == 2H2 ↑+O2 ↑
不加 变 H2O
第二组:电解H2SO4
阳极
阴极
氧
氢
气
气
实例
NaOH 阳极(OH- ): 4OH-- 4e- = 2H2O+O2↑
通电
变大
变 大
2H2O == 2H2 ↑+O2 ↑
复原
加 H2O
第三组:电解NaCl
阳极
阴极
氯
氢
气
气
实例
电极反应
浓度 PH 值
阴极(Na+ H+):2H ++ 2e- = H2 ↑ NaCl 阳极(Cl- OH-): 2Cl-- 2e- = Cl 2 ↑
2NaOH +Cl2↑+H2 ↑
电镀应用于铜的电解精练
粗铜板
硫酸铜溶液
纯铜板
电极反应式
电解精练铜原理
阴极(纯铜): Cu2+ + 2e- = Cu (还原反应)
阳极(粗铜): Cu - 2e- = Cu2+ (氧化反应)
杂质:Zn - 2e- = Zn2+ Ni-2e- = Ni2+
阳极泥: 相对不活泼的金属以单质的形式沉积在
金属越不活泼,对应阳离子氧化性越强,越容易得电子。
人教化学选修4第四章第3节 电解池(共28张PPT)

AgNO3
二、电解原理的应用
应用一:氯碱工业即电解饱和食盐水
阳极:2Cl- 阴极:2H+ +
2e-= Cl2如↑ 何检验两极产物? 2e- = H2↑
总反应:
电解
2NaCl + 2H2O==
CC
存在问题: 2NaOH + H2↑+ Cl22↑
H2+ Cl2=2HCl爆炸 氯气溶于水与水反应 氯气与NaOH反应产物不纯更纯
AgNO3溶液
当阳极金属与电解质溶液中的金属 阳离子相同,则为电镀
例:在50mL 0.2mol/L的硫酸铜溶液中插入两个
电极,通电电解(不考虑水分蒸发),则:
⑴若两极均为铜片,试说明电解过程中溶液
溶质浓度将怎样变化 不变
。
⑵若阳极为纯锌,阴极为铜片,阳极反应式
是 Zn -2e-=Zn2+
⑶如果两极均为铜片且不考虑H+在阴极上放电,
3、构成电解池的条件: ① 直流电源;
② 阴、阳电极
③ 电解质溶液或熔融电解质; ④ 形成闭合回路。
⑤非自发进行的氧化还原反应
原电池与电解池的比较
比较内容
原电池
电解池
装置举例 铜锌原电池
电解氯化铜
电极名称 正极、负极
阴极、阳极
电极反应 负极氧化反应 正极还原反应
能量转变 将化学能转变成电能
阳极氧化反应 阴极还原反应
实质:电解水
溶液pH变化: 增大 溶液复原方法:加入H2O
1、复习提问:
电极名称_阴__极____ C
反应类型_还__原____
C 电极名称__阳__极___
反应类型__氧__化___
电极反应_Cu_2+ _+_2e_- _= C_u 实验现象_红_色__固__体_
二、电解原理的应用
应用一:氯碱工业即电解饱和食盐水
阳极:2Cl- 阴极:2H+ +
2e-= Cl2如↑ 何检验两极产物? 2e- = H2↑
总反应:
电解
2NaCl + 2H2O==
CC
存在问题: 2NaOH + H2↑+ Cl22↑
H2+ Cl2=2HCl爆炸 氯气溶于水与水反应 氯气与NaOH反应产物不纯更纯
AgNO3溶液
当阳极金属与电解质溶液中的金属 阳离子相同,则为电镀
例:在50mL 0.2mol/L的硫酸铜溶液中插入两个
电极,通电电解(不考虑水分蒸发),则:
⑴若两极均为铜片,试说明电解过程中溶液
溶质浓度将怎样变化 不变
。
⑵若阳极为纯锌,阴极为铜片,阳极反应式
是 Zn -2e-=Zn2+
⑶如果两极均为铜片且不考虑H+在阴极上放电,
3、构成电解池的条件: ① 直流电源;
② 阴、阳电极
③ 电解质溶液或熔融电解质; ④ 形成闭合回路。
⑤非自发进行的氧化还原反应
原电池与电解池的比较
比较内容
原电池
电解池
装置举例 铜锌原电池
电解氯化铜
电极名称 正极、负极
阴极、阳极
电极反应 负极氧化反应 正极还原反应
能量转变 将化学能转变成电能
阳极氧化反应 阴极还原反应
实质:电解水
溶液pH变化: 增大 溶液复原方法:加入H2O
1、复习提问:
电极名称_阴__极____ C
反应类型_还__原____
C 电极名称__阳__极___
反应类型__氧__化___
电极反应_Cu_2+ _+_2e_- _= C_u 实验现象_红_色__固__体_
人教版高中化学选修4第四章第三节 电解池 课件(共19张PPT)

电极反应类型 阴极:还原反应 阳极:氧化反应
发生电解的条件:1、电源
2、电解质溶液 3、两个电极 4、形成闭合回路
电解池:把电能转变为化学能的装置。
电解池 分析电解反应的一般思路
分析电极材料
阳极为惰性电极时
明确溶液中存在哪些离子
阴阳两极附近各有哪些离子
根据阳极氧化,阴极还原分析得出产物
电解池
利用电解原理,如何 实现在铁件上镀一层铜?
Cu
Fe
CuCl2
电解池
作业
根据本节课所学内容分析用惰性电极电 解的电解质溶液是NaCl溶液该如何反应?
如果是熔融NaCl呢?
方向如何?
电解池
实验探究
有红色物质析出。 无气泡产生。
有气泡产生,该 气体可使润湿的淀粉 碘化钾试纸变蓝。
Cu
Cl2
Cu2+ + 2e- = Cu
2Cl- - 2e- = Cl2↑
还原反应
氧化反应
总反应
CuCl2 电解 Cu + Cl2↑
电解池
探究真相:
1、通电前,CuCl2溶液中存在哪些离子,如何运 动? 2、通电后,CuCl2溶液中的离子如何运动? 3、在阴阳两极,离子会发生什么变化?(从得 失电子,发生氧化还原反应的的角度分析)
【阴极】阳离子得电子能力 Ag+ >Hg2+ >Fe3+ >Cu2+ >H+> Pb2+> Fe2+ >Zn2+> Al3+> Mg2+> Na+> Ca2+> K+ 【阳极】阴离子失电子能力
发生电解的条件:1、电源
2、电解质溶液 3、两个电极 4、形成闭合回路
电解池:把电能转变为化学能的装置。
电解池 分析电解反应的一般思路
分析电极材料
阳极为惰性电极时
明确溶液中存在哪些离子
阴阳两极附近各有哪些离子
根据阳极氧化,阴极还原分析得出产物
电解池
利用电解原理,如何 实现在铁件上镀一层铜?
Cu
Fe
CuCl2
电解池
作业
根据本节课所学内容分析用惰性电极电 解的电解质溶液是NaCl溶液该如何反应?
如果是熔融NaCl呢?
方向如何?
电解池
实验探究
有红色物质析出。 无气泡产生。
有气泡产生,该 气体可使润湿的淀粉 碘化钾试纸变蓝。
Cu
Cl2
Cu2+ + 2e- = Cu
2Cl- - 2e- = Cl2↑
还原反应
氧化反应
总反应
CuCl2 电解 Cu + Cl2↑
电解池
探究真相:
1、通电前,CuCl2溶液中存在哪些离子,如何运 动? 2、通电后,CuCl2溶液中的离子如何运动? 3、在阴阳两极,离子会发生什么变化?(从得 失电子,发生氧化还原反应的的角度分析)
【阴极】阳离子得电子能力 Ag+ >Hg2+ >Fe3+ >Cu2+ >H+> Pb2+> Fe2+ >Zn2+> Al3+> Mg2+> Na+> Ca2+> K+ 【阳极】阴离子失电子能力
人教版选修四高中化学4-3-电解池(共36张PPT)

⑵ 电解无氧酸溶液(氢氟酸除外)、不活泼金属的 无氧酸盐溶液时,实质上是电解质本身被电解。 如电解盐酸、CuCl2溶液等时
电解盐酸 阳极: 2Cl -- 2e-=Cl2↑
阴极:
2H+
+2e-=
通电
H2
↑
总反应:2HCl
Cl2↑ + H2↑
电解后溶液中溶质的质量分数减小,
若要恢复原来的组成和浓度,需加入一 定量的溶质(加入一定量的HCl气体、
阴极 : 2Cu2+ +4e-=2Cu
总反应: 2CuSO4 +2H2O 通电 2Cu+O2↑ +2H2SO4
电解后原溶液中溶质的质量分数减小,
若要恢复原来的组成和浓度,需加入一定 C或
C或
量金属氧化物。
Pt
Pt
人教版选修四高中化学4-3-电解池(共 36张PP T)
溶液
人教版选修四高中化学4-3-电解池(共 36张PP T)
电解一段时间后, 判断溶液的质量分数将如何变化? 溶液的PH值将如何变化? 加入什么物质可以使电解质溶液恢复到电解前?
人教版选修四高中化学4-3-电解池(共 36张PP T)
人教版选修四高中化学4-3-电解池(共 36张PP T)
二、电解规律的讨论:(用惰性电极电解时)
(1)电解含氧酸、强碱溶液、活泼金属的含氧酸盐 溶液时,实质上是电解水。如电解H2SO4、HNO3 NaOH、Na2SO4等溶液时其电极反应式为:
阳极 : 4OH--4e-=2H2O +O2↑
阴极: 4H+ +4e-=2H2 ↑
总反应:2H2O 通电 O2↑ +2H2↑
C或
人教版化学选修四第四章第三节电解池 课件 ( 共28张PPT)

第三节 电解池 一、电解原理 (一)【实验】电解CuCl2溶液 阳极
现象:
+-
阴极 碳棒上覆盖了一层红色物质。
阳极 生成有刺激性气味的气体, 该气体能使湿润的淀粉 碘化钾试纸变蓝。
碳棒
说明:阴极有Cu生成,阳极有Cl2生成。
阴极 CuCl2溶液
思考:为什么CuCl2溶液在通电时会生成Cu和Cl2的呢? (1)通电前水中存在那些离子?
AlCl3
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
阳:阴: 阳:阴: 阳:阴: 阳:阴: 阳:阴: 阳:阴:
2.电解电解质型 3.放O2生酸型: 4.放H2生碱型:
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
二、电解原理的应用
1、电镀铜
电镀:应用电解原理在某些金属表面镀上一薄层其它 金属或合金的方法。
课件 ( 共28张PPT)
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
阳极反应:2Cl--2e- = Cl2↑(氧化反应) 阴极反应:2H+ + 2e-=H2↑(还原反应)
总反应离子方程式: 2Cl- + 2H2O 电解 2OH- + H2↑ + Cl2↑
总反应:
电解
2NaCl + 2H2O
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
3、电解饱和食盐水------氯碱工业
(1)电解饱和食盐水的实验
思考: (1)写出电极反应式和电解的总 反应式。
(2)电解池的两极各产生什么现 象?若在两极附近均滴加酚酞试液, 会有什么现象? (3)分析产生这种现象的原因。
现象:
+-
阴极 碳棒上覆盖了一层红色物质。
阳极 生成有刺激性气味的气体, 该气体能使湿润的淀粉 碘化钾试纸变蓝。
碳棒
说明:阴极有Cu生成,阳极有Cl2生成。
阴极 CuCl2溶液
思考:为什么CuCl2溶液在通电时会生成Cu和Cl2的呢? (1)通电前水中存在那些离子?
AlCl3
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
阳:阴: 阳:阴: 阳:阴: 阳:阴: 阳:阴: 阳:阴:
2.电解电解质型 3.放O2生酸型: 4.放H2生碱型:
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
二、电解原理的应用
1、电镀铜
电镀:应用电解原理在某些金属表面镀上一薄层其它 金属或合金的方法。
课件 ( 共28张PPT)
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
阳极反应:2Cl--2e- = Cl2↑(氧化反应) 阴极反应:2H+ + 2e-=H2↑(还原反应)
总反应离子方程式: 2Cl- + 2H2O 电解 2OH- + H2↑ + Cl2↑
总反应:
电解
2NaCl + 2H2O
人教版化学选修四第四章第三节电解 池
课件 ( 共28张PPT)
3、电解饱和食盐水------氯碱工业
(1)电解饱和食盐水的实验
思考: (1)写出电极反应式和电解的总 反应式。
(2)电解池的两极各产生什么现 象?若在两极附近均滴加酚酞试液, 会有什么现象? (3)分析产生这种现象的原因。
人教版高二化学选修4教学课件:第四章4.3 电解池(共50张PPT)

第2课时 电解原理的 2 应用
• 1. 氯碱工业
• (1)概念 • 用电解饱和食盐水的方法来制取Cl2、NaOH、H2,并
以它们为原料生产一系列化工产品的工业,称为氯碱工业。
• 1. 氯碱工业
• (2)原理
• ①通电前,NaCl溶液中含有的离子是___________。
• 通电时,移向阴极的离子是______,移向Na阳+极C的l− 离H+子O是H−
Fe2+>Zn2+>H+(水)>
•
Al3+、Mg2+、Na+、Ca2+、K+
• 2. 电解产物的判断 • (3)电极产物的判断
离子 S2− 产物 S
SO32− SO42−
I− Br− Cl− OH−
I2
Br2 Cl2 O2
离子 Ag+ Hg2+ Fe3+ Cu2+ H+ 产物 Ag Hg Fe2+ Cu H2
借助于电流,反应进行是 不自发的氧化还原反应。
• 2. 构成条件
直流电源 两个电极 电解质溶液(或熔融电解质) 闭合回路
阴极
阳极
• 3. 工作原理
e-
e-
二、电解原理
• 1. 电解
• 使(直流)电流通过电解质溶液(或熔融电解质)而在阴、 阳两极引起氧化还原反应的过程叫做电解。
电离与电解的比较
合金的方法。 • (2)电解槽构成 • 阴极——待镀金属 • 阳极——镀层金属 • 电镀液——含有镀层金属离子 • (3)特点 • ①阳极参与电极反应 • ②电镀液浓度保持不变
• 3. 电解精炼铜
• (1)电解槽构成 • 阳极:粗铜 (含Zn、Fe、Ni、Au、Ag等杂质) • 阴极:纯铜 • 电解液:CuSO4溶液
人教化学选修4第四章第3节 电解池(共19张PPT)

巩固提高
活动探究1,了解离子放电顺序
拓展
活动探究2,完善放电顺序
巩固提高
突出重点 易化难点
实验探究,易 化难点,实现 三维目标。
五、教学过程
教材 方法
1.创设情境,引入课题
借用初中电解水的实验装置, 给出电解池、电解、电极的定义。
学情
教学 过程
板书
五、教学过程
教材 方法
2.学习电解原理
1.注意装置的如何变化? 2.碳棒上有何变化?
阳极:与电源正极相连的电极。(发生氧化反应)
3、电解CuCl2溶液:
电解
电解总反应:CuCl2 == Cu+Cl2↑
CuCl2 =Cu2++2Cl-
阳极:2Cl--2e-=Cl2↑(氧化反应)
阴极:Cu2++2e-=Cu(还原反应)
4、构成电解池的条件:
①直流电源;②电极 ③电解质溶液或熔融电解质;
电解
总反应:2CuSO4+2H2O====2Cu+ 2H2S + O2↑ (3)电解H2SO4溶液: 阳极:4OH- - 4e- = 2H2O + O2↑ 阴极:4H+ + 电4解e- = 2H2↑
电源负极→电解池阴极→电解液中的阳离子(被还原总)反应:2H2O === 2H2↑ + O2↑
电解池中阴离子(被氧化)→电解池阳极→电源正极
板书
二、教学目标
教材
方法
学情 教学 过程
❖《普通高中化学课程标准》的叙述和分析
具体内容
体验化学能与电 能相互转化的探 究过程,了解电 解池的工作原理。
活动建议 行为
动词
探究电能和 化学能的相互 转化。
高中化学人教版选修四 4-3 电解池 课件(19张)
人教版选修4 · 化学反应原理
第四章 第三节
电化学基础 电解池
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
戴维著名的电解水实验:
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
第三节 电解池
一 电解原理 阅读课本实验4-2 电解氯化铜溶液 (1)用什么做电极材料? (2)电源正负极相连接的看到的现象? (3)产物的检验方法?
电解池,阴阳极;阳极氧化,阴极还原。
阳极:活泼金属或阴离子- ne- = 氧化产物 阴极: 阳离子+ ne- = 还原产物 总电解反应式:阴阳极反应式相加所得的式子 (考虑电子守恒)
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
4、分析电解反应的一般思路(惰性电极电解时)
明确溶液中存在哪些离子
HCl溶液
电解
实质: 电解了HCl本身
2H++2Cl- == H2 ↑ +Cl2 ↑
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
电解NaOH溶液 阳极:4OH- - 4e- = 2H2O + O2 ↑ 阴极:4H+ + 4e- = 2H2 ↑
电解
NaOH溶液
总反应: 2H2O = = 2H2 ↑+ O2 ↑
CuSO4溶液
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
小结:
一、电解原理
1、电解 2、电解池 3、电解池形成条件
电子的流向?
离子移动的方向?
电极反应式? 阳极氧化,阴极还原
第四章 第三节
电化学基础 电解池
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
戴维著名的电解水实验:
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
第三节 电解池
一 电解原理 阅读课本实验4-2 电解氯化铜溶液 (1)用什么做电极材料? (2)电源正负极相连接的看到的现象? (3)产物的检验方法?
电解池,阴阳极;阳极氧化,阴极还原。
阳极:活泼金属或阴离子- ne- = 氧化产物 阴极: 阳离子+ ne- = 还原产物 总电解反应式:阴阳极反应式相加所得的式子 (考虑电子守恒)
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
4、分析电解反应的一般思路(惰性电极电解时)
明确溶液中存在哪些离子
HCl溶液
电解
实质: 电解了HCl本身
2H++2Cl- == H2 ↑ +Cl2 ↑
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
电解NaOH溶液 阳极:4OH- - 4e- = 2H2O + O2 ↑ 阴极:4H+ + 4e- = 2H2 ↑
电解
NaOH溶液
总反应: 2H2O = = 2H2 ↑+ O2 ↑
CuSO4溶液
引入 新课
实验 探究
原理 分析
巩固 练习
小结 作业
小结:
一、电解原理
1、电解 2、电解池 3、电解池形成条件
电子的流向?
离子移动的方向?
电极反应式? 阳极氧化,阴极还原
人教化学选修4第四章第3节 电解池(共19张PPT)
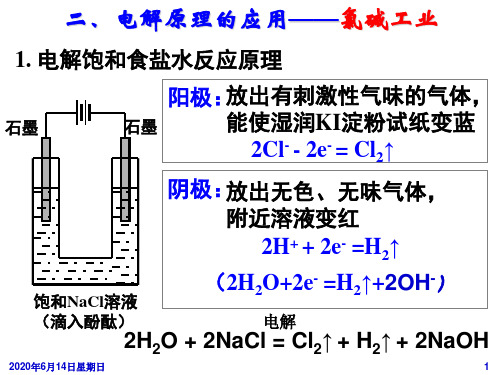
Cl2
H2
(2)电解饱和食盐水
2的Cl离-+子2方H2程O式=电=是解==2;OH淡-盐+水H2↑+Cl2N↑a+ (3)电解时用盐酸控
溶液A
制阳极区溶液的pH
氯 H减在 衡 酸C少气的移2l~O氯与作动,3气水用原,增在反_理用_大水应解_化H_中:释学_C_的C盐l平_的l_溶2+浓;解H度,2可O有使精利制平于饱衡和氯逆H气水向C的(移含l+溢少动出,。
2020年6月14日星期日
10
二、电解原理的应用——电解精炼铜
2020年6月14日星期日
11
二、电解原理的应用——电冶金
电解是最强有力的氧化还原手段,用于 冶炼Na、Ca、Mg、Al这样活泼的金属
钠的冶炼 (熔融NaCl作电解质)
阳极:2Cl--2e-=Cl2↑ 阴极:2Na++2e-=2Na 总反应: 2NaCl(熔融)通==电=2Na+Cl2↑
Cu
以粗铜为阳极,以纯铜
Zn Fe
纯铜 Cu
为阴极, 以CuSO4溶液 为电解液进行电解。
Ni Ag
Au
②电解后CuSO4浓度的变化 CuSO4浓度减小
CuSO4溶液
阳极: Zn -2e-=Zn2+ Fe-2e-=Fe2+
Ni -2e-=Ni2+ Cu-2e-=Cu2+
阴极: Cu2+ +2e-=Cu
2020年6月14日星期日
NaCl
量NaOH) 19
阴极:
4Al 3+ + 12 e- =4Al 阳极:
C
Fe
6O 2- -12e - =3O2↑ 总反应: 2Al2O3(熔融)通==电=4Al+3O2↑
人教版化学选修四第四章第三节《电解池 金属的电化腐蚀与防护》课件

例 4.CuI 是一种不溶于水的白色固体,可以由反应:2Cu2++4I- ===2CuI↓+I2 得到。现以石墨为阴极,以 Cu 为阳极电解 KI 溶液, 通电前向电解液中加入少量酚酞和淀粉溶液。回答下列问题: (1)阳极区的现象__铜 __电 __极__逐__渐__溶__解__,__有__白__色__沉__淀__产__生__,_。溶液变为蓝色 (2)阳极电极反应式___2_C_u_+ __4_I_-_-__4_e_-_=_=_=_2_C_u_I_↓__+__I_2 ___。
主干知识梳理
(2)工作原理(以电解CuCl2溶液为例)
电极 名称
电极 材料
电极 反应
反应 类型
阴极(接电源负极)
石__墨__
C__u_2_+_+__2_e_-_=_=__=_C_u_ 还__原__反__应____
阳极(接电源正极)
__石__墨__
_2__C_l_-_-__2_e_-_=_=_=__C_l_2↑_ 碳
例2.电解原理在化学工业中有广泛应用。下图表示两个串联 的电解池。图中B装置中盛有1 L 2 mol·L-1Na2SO4溶液,A装 置中盛有1 L 2 mol·L-1AgNO3溶液。通电后,铂片上有气体 生成。
(1)电源X极为__负______极。 (2)B池中阳极电极反应式为___C_u_-_2_e_-_=_=_=_C_u_2_+_________,
(1)冶炼钠 2NaCl(熔融)=电==解==2Na+Cl2↑ 电极反应:
阳极: 2Cl--2e-===Cl2↑ ,阴极:2Na++2e-===2Na 。 (2)冶炼铝 2Al2O3(熔融)=电==解==4Al+3O2↑ 电极反应: 阳极:6O2--12e-===3O2↑ ,阴极:4Al3++12e-===4Al。
主干知识梳理
(2)工作原理(以电解CuCl2溶液为例)
电极 名称
电极 材料
电极 反应
反应 类型
阴极(接电源负极)
石__墨__
C__u_2_+_+__2_e_-_=_=__=_C_u_ 还__原__反__应____
阳极(接电源正极)
__石__墨__
_2__C_l_-_-__2_e_-_=_=_=__C_l_2↑_ 碳
例2.电解原理在化学工业中有广泛应用。下图表示两个串联 的电解池。图中B装置中盛有1 L 2 mol·L-1Na2SO4溶液,A装 置中盛有1 L 2 mol·L-1AgNO3溶液。通电后,铂片上有气体 生成。
(1)电源X极为__负______极。 (2)B池中阳极电极反应式为___C_u_-_2_e_-_=_=_=_C_u_2_+_________,
(1)冶炼钠 2NaCl(熔融)=电==解==2Na+Cl2↑ 电极反应:
阳极: 2Cl--2e-===Cl2↑ ,阴极:2Na++2e-===2Na 。 (2)冶炼铝 2Al2O3(熔融)=电==解==4Al+3O2↑ 电极反应: 阳极:6O2--12e-===3O2↑ ,阴极:4Al3++12e-===4Al。
人教版高中化学选修四课件4.3电解池课件

电子流向
构成条件
原电池
电解池
化学能转化为电能
电能转化为化学能
反应自发
反应不自发
相对活泼的金属 作为负极 相对不活泼的金属 或石墨作为正极
阴离子向负极迁移, 阳离子向正极迁移
连接电源的正极, 作为阳极
连接电源的负极, 作为阴极
阴离子向阳极迁移, 阳离子向阴极迁移
负极→正极
负极→阴极,阳 极→正极
两个电极、电解质溶液形成闭合回路。 电解池有外电源,原电池无需外电源。
后体积变化可以忽略),电极上析出银的质量大
约是: A、27mg C、108mg
B、54mg B D、216mg
例2、下图所示装置中, 甲,乙、丙三个烧杯依 次分别盛放100g5.00% 的NaOH溶液、足量的 CuSO4溶液和100g10% 的K2SO4溶液,电极均为石墨电极。 (1)接通电源,经过一段时间后,测得丙中
电离和电解的比较
电
离电
解
条件 在水溶液或融化状 在水溶液或融化
态下,不需通电。 状态下通电。
过程 电解质电离成为 阴、阳离子定向移动,
自由移动的离子。在两极上得失电子成 为分子或原子。
特点 只产生自由移
动的离子。
产生氧化还原反应, 有新物质生成。
联系 电离是电解的先决 必须有电解质的
条件和物质基础。 电离作前提。
在电镀工业的废水中常含有剧毒物质,如氰化 物、重金属离子等, 减少电镀污染的途径: (1)电镀废水经过处理,回收其中有用成分,把有 毒有害物质的浓度降低到符合工业废水的排放标准. (2)改进电镀工艺,尽量使用污染少的原料.如采用无 氰电镀等
3、电解饱和氯化钠溶液
氯碱工业:离子交换膜法制烧碱
构成条件
原电池
电解池
化学能转化为电能
电能转化为化学能
反应自发
反应不自发
相对活泼的金属 作为负极 相对不活泼的金属 或石墨作为正极
阴离子向负极迁移, 阳离子向正极迁移
连接电源的正极, 作为阳极
连接电源的负极, 作为阴极
阴离子向阳极迁移, 阳离子向阴极迁移
负极→正极
负极→阴极,阳 极→正极
两个电极、电解质溶液形成闭合回路。 电解池有外电源,原电池无需外电源。
后体积变化可以忽略),电极上析出银的质量大
约是: A、27mg C、108mg
B、54mg B D、216mg
例2、下图所示装置中, 甲,乙、丙三个烧杯依 次分别盛放100g5.00% 的NaOH溶液、足量的 CuSO4溶液和100g10% 的K2SO4溶液,电极均为石墨电极。 (1)接通电源,经过一段时间后,测得丙中
电离和电解的比较
电
离电
解
条件 在水溶液或融化状 在水溶液或融化
态下,不需通电。 状态下通电。
过程 电解质电离成为 阴、阳离子定向移动,
自由移动的离子。在两极上得失电子成 为分子或原子。
特点 只产生自由移
动的离子。
产生氧化还原反应, 有新物质生成。
联系 电离是电解的先决 必须有电解质的
条件和物质基础。 电离作前提。
在电镀工业的废水中常含有剧毒物质,如氰化 物、重金属离子等, 减少电镀污染的途径: (1)电镀废水经过处理,回收其中有用成分,把有 毒有害物质的浓度降低到符合工业废水的排放标准. (2)改进电镀工艺,尽量使用污染少的原料.如采用无 氰电镀等
3、电解饱和氯化钠溶液
氯碱工业:离子交换膜法制烧碱
人教版高中化学选修4第四章第三节 电解池 课件 .(共12张PPT)

阴极放电顺序:
无论是惰性电极还是活性电极做阴极,阴极都不参与电极反应,发 生反应的是溶液中的阳离子。阳离子在阴极上放电顺序是:Ag+ > Fe3+ > Cu2+ > H+(酸) > Pb2+ > Sn2+ > Fe2+ > Zn2+ > H+(水) > Al3+ > Mg2+ > Na+ > Ca2+ > K+。
【小 结】
电解池电源、电极、电极反应关系
与电源正极相连
阴离子移向 阳离子移向
阳极 阴极
发生氧化反应 发生还原反应
与电源负极相连
三、电极反应式、电解方程式的书写
①分析、比较,得出阴、阳电极的放电物质。
②写出阴、阳电极反应式。 ③使得失电子数相等,用阴、阳电极反应式相加得电解方 程式。
【分析电解反应的一般思路】
(2)阴极和阳极材料:
惰性电极:石墨(C)、金(Au)、铂(Pt)等,不论做阴极还是做阳极, 电极本身都不反应。
活性电极:除石墨(C)、金(Au)、铂(Pt)以外的金属,如Fe、Cu、 Ag等。做阳极时,电极本身被氧化溶解;做阴极时,电极本身不反 应。
4.电解池电极反应规律(阳极氧化阴极还原)
(1)阳极:失去电子,发生氧化反应。 ①若为活性电极,电极本身失电子溶解。 ②若为惰性电极,电解质溶液中阴离子“争”失电子。
减小 增大 不变 增大 增大 增大 减小
H2O
HCl CuCl2 HCl CuO
练习1. 用铂电极电解下表中各组物质的水溶液,电解一段时间以后, 甲、乙两池中溶液的pH值均减小,而在①和④两极,电极产物的 物质的量之比为1:2的是( D )
无论是惰性电极还是活性电极做阴极,阴极都不参与电极反应,发 生反应的是溶液中的阳离子。阳离子在阴极上放电顺序是:Ag+ > Fe3+ > Cu2+ > H+(酸) > Pb2+ > Sn2+ > Fe2+ > Zn2+ > H+(水) > Al3+ > Mg2+ > Na+ > Ca2+ > K+。
【小 结】
电解池电源、电极、电极反应关系
与电源正极相连
阴离子移向 阳离子移向
阳极 阴极
发生氧化反应 发生还原反应
与电源负极相连
三、电极反应式、电解方程式的书写
①分析、比较,得出阴、阳电极的放电物质。
②写出阴、阳电极反应式。 ③使得失电子数相等,用阴、阳电极反应式相加得电解方 程式。
【分析电解反应的一般思路】
(2)阴极和阳极材料:
惰性电极:石墨(C)、金(Au)、铂(Pt)等,不论做阴极还是做阳极, 电极本身都不反应。
活性电极:除石墨(C)、金(Au)、铂(Pt)以外的金属,如Fe、Cu、 Ag等。做阳极时,电极本身被氧化溶解;做阴极时,电极本身不反 应。
4.电解池电极反应规律(阳极氧化阴极还原)
(1)阳极:失去电子,发生氧化反应。 ①若为活性电极,电极本身失电子溶解。 ②若为惰性电极,电解质溶液中阴离子“争”失电子。
减小 增大 不变 增大 增大 增大 减小
H2O
HCl CuCl2 HCl CuO
练习1. 用铂电极电解下表中各组物质的水溶液,电解一段时间以后, 甲、乙两池中溶液的pH值均减小,而在①和④两极,电极产物的 物质的量之比为1:2的是( D )
人教版高中化学选修4第四章第三节 电解池 课件(共18张PPT)

• 8、普通的教师告诉学生做什么,称职的教师向学生解释怎么做,出色的教师示范给学生,最优秀的教师激励学生。下午1时17分4 3秒下午1时17分13:17:4321.11.16
结论
惰性电极电解时,离子的放电顺序主要与离子 得失电子的能力,即氧化性、还原性强弱有关。
实 电解NaCl溶液,观察现象。实验结束后,向 验 装置中滴加酚酞溶液,观察现象,解释原因。
学 回顾课前微视频,以电解盐酸为例,画出实验装 情 反 置图,标出电极名称、电流方向、电极反应式、
馈 反应类型及总反应方程式。
C
阳极
C
阴极
2Cl-- 2e-= Cl2↑
氧化ห้องสมุดไป่ตู้应
HCl 溶液
2H+ + 2e- = H2↑
还原反应
总反应式:2HCl 电解 H2↑ + Cl2↑
人教版
第三节 电解池
电解:使电流通过电解质溶液而在阴、阳两极引起 氧化还原反应的过程。
Fe
Cu
CuSO4溶液
☆ 作业:
1、分析比较原电池和电解池的异同。 2、请利用今天所学知识,设计一套实验装置实 现铜与稀硫酸反应生成氢气。 3、练习册(本课时)。
请写出电极反应式、
C
C
总反应的离子方程式。
NaCl溶液
阳极
C
阴极
C
2Cl-- 2e-= Cl2↑
氧化反应
2H+ + 2e- = H2↑
还原反应
NaCl 溶液
总反应式:2H2O +2Cl - 电解 H2↑ + Cl2↑+2OH -
电解 NaCl溶液时,若将惰性电极更换为 问 题 活性电极(如Fe),是否会影响离子在
结论
惰性电极电解时,离子的放电顺序主要与离子 得失电子的能力,即氧化性、还原性强弱有关。
实 电解NaCl溶液,观察现象。实验结束后,向 验 装置中滴加酚酞溶液,观察现象,解释原因。
学 回顾课前微视频,以电解盐酸为例,画出实验装 情 反 置图,标出电极名称、电流方向、电极反应式、
馈 反应类型及总反应方程式。
C
阳极
C
阴极
2Cl-- 2e-= Cl2↑
氧化ห้องสมุดไป่ตู้应
HCl 溶液
2H+ + 2e- = H2↑
还原反应
总反应式:2HCl 电解 H2↑ + Cl2↑
人教版
第三节 电解池
电解:使电流通过电解质溶液而在阴、阳两极引起 氧化还原反应的过程。
Fe
Cu
CuSO4溶液
☆ 作业:
1、分析比较原电池和电解池的异同。 2、请利用今天所学知识,设计一套实验装置实 现铜与稀硫酸反应生成氢气。 3、练习册(本课时)。
请写出电极反应式、
C
C
总反应的离子方程式。
NaCl溶液
阳极
C
阴极
C
2Cl-- 2e-= Cl2↑
氧化反应
2H+ + 2e- = H2↑
还原反应
NaCl 溶液
总反应式:2H2O +2Cl - 电解 H2↑ + Cl2↑+2OH -
电解 NaCl溶液时,若将惰性电极更换为 问 题 活性电极(如Fe),是否会影响离子在
人教化学选修4第四章第3节 电解池 课件 (共26张PPT)

阴极:2Na+ +2e- = 2Na
阳极
阴极
阳极:2Cl- -2e- = Cl2↑
氯
钠
气
熔融NaCl
总反应: 2NaCl 电解 2Na+Cl2 ↑
15
二、电解原理的应用
1、氯碱工业:通过电解饱和食盐水以制造烧碱、 氯气和氢气的工业。
阳极 阴极
总反应:
2NaCl+2H2O 通电 2NaOH +Cl2↑+H2 ↑
阳极:
Zn Zn-2e- = Zn2+ F阳e极泥F: 相e -对2e不- =活泼Fe的2+金 NC属解iu以槽单底NC质,形iu的成--22形阳ee--式极==沉泥CN积ui在22++ 电 Ag 阳极泥 Au
阴极: Cu2+ + 2e- = Cu
-+
纯铜
粗铜
CuSO4溶液
电解精炼铜
电解精炼铜原理:
②阳极是惰性电极(Pt、Au、石墨等) 时:溶液中阴离子的放电顺序是:
S 2->I ->Br ->Cl ->OH – >NO3 ->SO42-(等含氧酸根离子)>F-
9
阴离子放电顺序口诀:
硫碘溴氯氢氧根 含氧酸根氟离子
8.阴极上的放电(得电子)顺序:
阴极无论是惰性电极还是活性电极都不参 与电极反应,发生反应的是溶液中的阳离 子。阳离子在阴极上放电顺序是:
(4)“自发”进行的氧化还原反应
2
〖复习回顾〗
想一想:原电池的电极如何判断?
1.根据组成原电池的两极材料判断 (较活泼金属:负极 较不活泼金属:正极) 2.根据电子流动方向判断 (电子流出:负极 电子流入:正极) 3.根据电流方向判断 (流入:负极 流出:正极) 4.根据离子移动的方向判断 (离子移动方向:正正负负 本质:异性相吸) 5.根据原电池两极发生的反应来判断 (记忆方法:横极撇极定反应)
人教化学选修4第四章第三节电解池(共18张PPT)

Cu
Cu2+
e- oooo
oooo oooo oooo oooo
Cl Cl
Cl2
电子从负极流向阴极,经溶液离 子导电,再从阳极流回正极
2020年6月13日星期六
6、离子放电顺序
(1)阳极:还原性强的离子先失电子
金属>S2->I->Br->Cl->OH-> NO3->SO42->F-
(2)阴极:氧化性强的离子先得电子
第三节 电解池
电解的应用
2020年6月13日星期六
2020年6月13日星期六
CuCl2溶液
C
观察 现象 并设 计方 案进 行验 证。
探究实验பைடு நூலகம்
2020年6月13日星期六
+
-
C
C
电极1
-- CuCl2溶液
电极2
CuCl2溶液
C
我要试一试
练习:书写刚才实验中的电极反应式
阳极:2Cl- _ 2e- = Cl2 ↑ (氧化反应)
(弱电解质的须保持分子形式)
2020年6月13日星期六
练习:
PH=a的某电解质溶液中,插入两支惰性电极 通直流电一段时间后,溶液的PH>a,则该
电解质可能是( A )
A.NaOH
B.H2SO4
C.AgNO3
D.Na2SO4
2020年6月13日星期六
练 习:下图所示装置中,a、b都是惰性电极,通
电一段时间后,b极附近溶液呈红色。下列说法
正确的是
( AC )
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的PH值逐渐减小 D.CuSO4溶液的PH值不变
•X Y •
高中化学人教版选修4第四章第三节-电解池

关叙述正确的是 B
A.P是电源的正极 B.F极上产生的反应为:4OH- - 4e-=2H2O+O2↑ C.电解时,甲、乙、丙三池中,除E、F两极外, 其余电极均参加了反应 D.通电后,甲池的PH减小,而乙、丙两池溶液的 PH不变
3.用铂电极电解下表中各组物质的水溶液,
电解一段时间以后,甲、乙两池中溶液的 pH值均减小,而在①和④两极,电极产物 的物质的量之比为1︰2的是
电解
2NaCl+2H2O
2NaOH+H2 ↑ + Cl2 ↑
3.放出氢气生成碱型:
如电解NaCl、KCl、MgCl2溶液等。 阳极 (C): 2Cl -- 2e-=Cl2↑ 阴极 (C): 2H+ +2e-= H2 ↑ 总反应: 2NaCl+2H2O=电解=2NaOH+ Cl2↑ + H2↑
电解后原溶液中溶质的质量分数减小,若要恢
(4)分析电解质溶液的变化情况:氯化铜溶液浓度降低
小结:
1.放电: 阴离子失去电子而阳离子得到电子的过程叫放电。
2.放电顺序: 阳极: ①活性材料作电极时:
金属在阳极失电子被氧化成阳离子进人溶液,阴
离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴
离子的放电顺序(由易到难)是:
第三节 电解池
你知道吗?
工业上分别以氯化钠和氧化铝为原料生产金 属钠和金属铝。你知道工业生产中是如何实现 此过程的吗?
阳极
阴极
氯
气
钠
熔融NaCl
电解熔融氯化钠
一、电解原理(以电解氯化钠为例)
实验:用惰性(石墨)电极电解熔融的氯化钠
现象:
阳极:有气泡,有
A.P是电源的正极 B.F极上产生的反应为:4OH- - 4e-=2H2O+O2↑ C.电解时,甲、乙、丙三池中,除E、F两极外, 其余电极均参加了反应 D.通电后,甲池的PH减小,而乙、丙两池溶液的 PH不变
3.用铂电极电解下表中各组物质的水溶液,
电解一段时间以后,甲、乙两池中溶液的 pH值均减小,而在①和④两极,电极产物 的物质的量之比为1︰2的是
电解
2NaCl+2H2O
2NaOH+H2 ↑ + Cl2 ↑
3.放出氢气生成碱型:
如电解NaCl、KCl、MgCl2溶液等。 阳极 (C): 2Cl -- 2e-=Cl2↑ 阴极 (C): 2H+ +2e-= H2 ↑ 总反应: 2NaCl+2H2O=电解=2NaOH+ Cl2↑ + H2↑
电解后原溶液中溶质的质量分数减小,若要恢
(4)分析电解质溶液的变化情况:氯化铜溶液浓度降低
小结:
1.放电: 阴离子失去电子而阳离子得到电子的过程叫放电。
2.放电顺序: 阳极: ①活性材料作电极时:
金属在阳极失电子被氧化成阳离子进人溶液,阴
离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴
离子的放电顺序(由易到难)是:
第三节 电解池
你知道吗?
工业上分别以氯化钠和氧化铝为原料生产金 属钠和金属铝。你知道工业生产中是如何实现 此过程的吗?
阳极
阴极
氯
气
钠
熔融NaCl
电解熔融氯化钠
一、电解原理(以电解氯化钠为例)
实验:用惰性(石墨)电极电解熔融的氯化钠
现象:
阳极:有气泡,有
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
〖复习回顾〗
问一问:原电池的 电极如何判断?
正极 较不活泼金属 较活泼金属 或非金属 电子流出 电子流入 氧化反应 还原反应 负极
Zn
e-
e- Cu
CuCl2溶液
原电池:将化学能转变为电能的装置。
〖复习回顾〗
G
写一写:原电池的 电极反应式?
Zn
Cu
负极: Zn – 2e- = Zn2+ 正极: Cu2+ + 2e- = Cu CuCl2溶液 电池总反应: Zn+Cu2+ = Zn2++Cu
注:当离子浓度相差较大时,放电顺序要发生变化
阳极: ①活性材料作电极时:金属在阳极失 电子被氧化成阳离子进人溶液,阴离子不容 易在电极上放电。 ②用惰性电极(Pt、Au、石墨、钛等)时:溶 液中阴离子的放电顺序是:
S 2->SO32->I ->Br ->Cl ->OH ->NO3 >SO42-(等含氧酸根离子)>F2014/9/30 16
【思考11】电解氯化铜溶液时,溶液中Cu2+和Cl-放
电基本完毕后,电解过程是否也就停止了呢?
溶液中Cu2+和Cl—放电完毕后,原溶液变为纯 水,此时,在纯水中存在H+和OH—, H+在阴极放 电,OH-在阳极放电,实际上是电解水的过程,所 以:
阴极:4H+ + 4e— = 2H2 ↑
阳极:4OH— -4e— =2H2O + O2 ↑ 总反应:2H2O = 2H2↑ + O2 ↑ 【思考12】在电解氯化铜溶液的装置中,若把电解 质换成氯化钠,其结果又如何呢?写出电极反应。
CuCl2溶液
【思考3】在电解过程中,电子、离子 是如何形成闭合回路的?
电子的流向: 电子从外加电 源的负极流出,流到电解 e- 阴极 池的阴极,再从阳极流回 电源正极。(注意:电子 C 只在外电路定向移动,不 能从溶液中移动) 离子定向移动的方向: 阳离子向阴极移动, 阴离子向阳极移动。
e- 阳极 C
阳极 C
【思考6】电解后氯化铜的浓度如何变化? 变小 【思考7】若要使电解质溶液复原,怎么办? 加CuCl2溶液 【思考8】什么叫放电?
阴离子失去电子而阳离子得到电子的过程叫放电。
【思考9】为什么Cu2+、Cl-放电,而不是 H+和OH-?
阴离子放电:与阴离子的还原性的相对强弱有关 阳离子放电:与阳离子的氧化性的相对强弱有关
阳离子移向阴极放电, 阴离子移向阳极放电
6、电极反应式的书写: (以电解CuCl2 为例)
e- 阴极
e-
C 阴极:Cu2++2e-=Cu 还原反应 阳极:2Cl- -2e- =Cl2 ↑ 氧化反应 电解 总反应式: CuCl2 Cu+Cl2 ↑ 通式: CuCl2溶液 阴极:氧化剂+ne- = 还原产物 阳极:还原剂-ne- = 氧化产物 总电解反应式:阴阳极反应式相加所得的式子 (考虑电子守恒)
CuCl2溶液 CuCl2溶液 惰性电极(铂、金、石墨): ——仅仅导电,不参与反应 活性电极(除铂、金外的金属): ——既可以导电、又可以参与电极反应
【思考2】形成电解池的条件是什么?
4、形成电解池的条件
e- ⑴与电源相连的两个电极 阴极 C
e- 阳极 C
⑵电解质溶液或熔化的 电解质 ⑶形成闭合回路
2
结论: CuCl2溶液在电流的作用下发生了 化学变化,分解生成了Cu和Cl2
实验分析:
电解氯化铜溶液微观模拟
第三节
电解池
一、电解原理 使电流通过电解质溶液而在阴、 1、电解: 阳两极引起氧化还原反应的过程。
注意:①电流必须是直流而不是交流。
②熔融态的电解质也能被电解。 2、电解池(电解槽): 把电能转化为化学能的装置
电解
(1)溶液中所含阳离子:H+、Na+, 放电顺序:H+ > Na+ 阴 极:2H+ + 2e— = H2 ↑
(2)溶液中所含阴离子:OH—、Cl—, 放电顺序:Cl— > OH— 阳 极:2Cl— -2e— = Cl2 ↑
电解
【思考1】电解池的两极是怎样确定的?
3、两个电极及电极反应
⑴、两个电极的确定及电极反应
e- 阴极 C
e-
阳极 C
CuCl2溶液 阴极:与电源负极相连——电子流进——还原反应 阳极:与电源正极相连——电子流出——氧化反应
⑵、两个电极的类型: 惰性电极与活性电极
阴极 C 阳极 C 阴极 Cu 阳极 Cu
【思考10】阴阳离子的放电顺序是什么?
7、离子放电顺序: 阴极 : 无论是惰性电极还是活性电极都不参与电极反
应,发生反应的是溶液中的阳离子。阳离子在阴极 上放电顺序(即得e-)是:
Ag+>Hg2+>Fe3+>Cu2+>H+(指酸电离) >Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na +>Ca2+>K+
人教版选修4 · 化学反应原理
第四章
电化学基础
第三节
电解池
2014/9/30
1
〖复习回顾〗
想一想:构成原电 池的条件是什么?
⑴两个活性不同的电极 ⑵电解质溶液(一般与活泼性强 的电极能发生氧化还原反应) ⑶形成闭合回路 (4)自发进行的氧化还原反应
Zn
e-
e- Cu
CuCl2溶液
原电池:将化学能转变为电能的装置。
CuCl2溶液
【思考4】电解质溶液导电的实质是什么?
5、电解质溶液导电的实质
对电解质溶液(或熔融态电解质)通电时,电 子从电源的负极沿导线流入电解池的阴极,电 解质的阳离子移向阴极得电子发生还原反应; 电解质的阴离子移向阳极失去电子(有的是组 成阳极的金属原子失去电子)发生氧化反应, 电子从电解池的阳极流出,并沿导线流回电源 的正极。这样,电流就依靠电解质溶液(或熔 融态电解质)里阴、阳离子的定向移动而通过 溶液(或熔融态电解质),所以电解质溶液 (或熔融态电解质)的导电过程,就是电解质 溶液(或熔融态电解质)的电解过程。 【思考5】如何书写电极反应方程式和总方程式?
联想*质疑
CCBiblioteka 如果把两根石墨棒作电极插入 CuCl2 溶液中,外接直流电源, CuCl2溶液 这还是原电池装置吗?
一、电解原理(以电解氯化铜为例) 实验4-2:用惰性(石墨)电极电解氯化铜溶液 现象: 阴极 阴极:碳棒上有一层红色 阳极 的物质析出 ——铜 氯 有气泡,气体有刺 铜 阳极: 气 CuCl 溶液 激性气味,并能使 湿润的 KI-淀 粉试纸变蓝 ——Cl2
