金属腐蚀与防护课后习题答案
金属的腐蚀与防护(讲义)含答案

金属的腐蚀与防护(讲义)一、知识点睛1.金属的腐蚀(1)定义金属表面与周围物质发生_________或因________作用而遭到破坏的过程。
(2)实质金属失去电子被_________的过程,其过程可表示为:M-n e-M n+。
2.金属腐蚀类型(1)化学腐蚀金属跟接触到的物质(如O2、Cl2、SO2等)直接发生_______而引起的腐蚀。
(2)电化学腐蚀①定义两种金属_________且又同时暴露在______空气里或与_____________接触时,由于形成________而发生的腐蚀。
②实质被腐蚀金属成为原电池的______而被溶解。
③分类:a.吸氧腐蚀(以铜板上的铁铆钉为例)通常情况下水膜呈____性或___性,正极上____参加反应。
负极:_____________;正极________________;总反应:__________________________。
b.析氢腐蚀(以铜板上的铁铆钉为例)特殊情况下水膜呈___性,正极上___参加反应。
负极:____________;正极:____________;总反应:__________________________。
注:①纯金属只会发生化学腐蚀,不会发生电化学腐蚀;不纯的金属可能发生化学腐蚀,也可能发生电化学腐蚀,腐蚀类型取决于是否接触到电解质溶液。
②在金属腐蚀中,以电化学腐蚀为主,而电化学腐蚀中又以吸氧腐蚀为主。
3.金属腐蚀的影响因素(1)金属本性①金属越活泼,越易____电子而被腐蚀;②两极材料的活动性差别越大,较活泼金属被腐蚀的速率越______。
(2)介质①金属在潮湿的空气或电解质溶液中,容易腐蚀;②强电解质>弱电解质>非电解质。
(3)环境温度温度越高,金属腐蚀速率越____。
(4)金属腐蚀快慢的一般规律(同一种金属的腐蚀)电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极4.金属的防护(1)本质:阻止金属发生_________反应。
高中化学(新人教版)选择性必修一课后习题:金属的腐蚀与防护(课后习题)【含答案及解析】

金属的腐蚀与防护课后篇素养形成必备知识基础练1.下列与金属腐蚀有关的说法不正确的是()A.钢铁在潮湿空气中生锈属于电化学腐蚀B.电化学腐蚀一般可分为吸氧腐蚀和析氢腐蚀C.金属腐蚀的本质是金属原子失去电子被氧化D.铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应项,铝具有很强的抗腐蚀能力,是因为铝易被空气中的氧气氧化生成一层致密的氧化物保护膜,使内部金属不被腐蚀。
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。
观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。
以下有关解释合理的是()A.生铁片中的碳是原电池的负极,发生还原反应B.雨水酸性较强,生铁片仅发生析氢腐蚀C.墨水回升时,碳极反应式为O2+2H2O+4e-4OH-D.具支试管中溶液pH逐渐减小解析发生原电池反应时,生铁片中的碳是原电池的正极,A错误;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面上升,B错误;导管内液面上升时,铁片发生吸氧腐蚀,碳为正极,正极电极反应式为O2+2H2O+4e-4OH-,C正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管内溶液pH均增大,D错误。
3.为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法错误的是()A.正极的电极反应式为O2+2H2O+4e-4OH-B.将石墨电极改成Mg电极,难以观察到铁锈生成C.若向自来水中加入少量NaCl(s),可较快地看到铁锈D.分别向铁、石墨电极附近吹入O2,前者铁锈出现得快,失电子被氧化成Fe2+;在正极氧气得电子发生还原反应生成OH-,故向石墨电极附近吹入O2的腐蚀速率比向铁电极附近吹入O2的腐蚀速率大;向自来水中加入NaCl(s),可使电解质溶液的导电能力增加,增大腐蚀速率;若将石墨电极换成Mg电极,则负极为Mg,Fe被保护,难以看到铁生锈。
4.一定条件下,碳钢腐蚀与溶液pH的关系如下:下列说法不正确的是()A.在pH<4的溶液中,碳钢主要发生析氢腐蚀B.在pH>6的溶液中,碳钢主要发生吸氧腐蚀C.在pH>14的溶液中,碳钢腐蚀的正极反应为O2+4H++4e- 2H2OD.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减小解析C项,在pH>14的溶液中,碳钢腐蚀的正极反应为O2+2H2O+4e- 4OH-。
金属腐蚀与防护课后习题及实验答案

金属腐蚀与防护课后习题及实验答案课后习题1.什么是金属腐蚀?请简要说明。
金属腐蚀是指金属在与外界环境接触的过程中,由于化学或电化学作用导致金属表面逐渐失去其原有的金属性质的一种现象。
金属腐蚀主要由电子传递过程和离子传递过程构成。
2.列举几种常见的金属腐蚀类型。
•电化学腐蚀•化学腐蚀•氧化腐蚀3.金属腐蚀的影响主要体现在哪些方面?金属腐蚀的主要影响包括: - 金属材料的破坏和失效 - 资源浪费 - 生态环境污染4.请列举几种常见的金属腐蚀防护方法。
•表面涂覆防护•电化学防护•材料选择防护5.什么是阴极保护?它是如何实现的?阴极保护是一种主动防护措施,通过在金属表面引入外部电流,使金属表面成为阴极,从而抑制金属腐蚀的一种方法。
实现阴极保护的关键是保证外部电流的输入和金属结构的良好接触。
常见的阴极保护方法包括外加电流阴极保护和阳极保护。
实验答案实验一:金属腐蚀观察实验目的:观察不同金属在某种腐蚀剂作用下的腐蚀现象。
实验步骤: 1. 准备实验器材和试剂,包括不同金属样品、腐蚀剂。
2. 将不同金属样品分别放入不同的容器中。
3. 向不同容器中添加适量的腐蚀剂。
4. 观察金属样品在腐蚀剂中的变化,记录下观察结果。
实验结果:观察不同金属样品在腐蚀剂中的变化,记录下观察结果。
金属样品腐蚀剂腐蚀现象铁盐酸表面产生气泡铝硝酸表面逐渐变薄铜硫酸表面出现绿色物质实验结论:根据实验结果可以得出以下结论: - 铁在盐酸中会发生气泡,产生氢气。
- 铝在硝酸中会逐渐被腐蚀,表面变薄。
- 铜在硫酸中会生成绿色物质,表明发生了腐蚀反应。
实验二:金属腐蚀防护实验目的:通过表面涂覆防护来延缓金属腐蚀的过程。
实验步骤: 1. 准备实验器材和试剂,包括金属样品、防护涂层材料。
2. 将金属样品分别涂覆上防护涂层材料。
3. 将涂好防护涂层的金属样品放入腐蚀介质中。
4. 观察金属样品在腐蚀介质中的变化,记录下观察结果。
实验结果:观察涂有防护涂层的金属样品在腐蚀介质中的变化,记录下观察结果。
第17练 电解原理及其应用 金属腐蚀与防护(解析版)
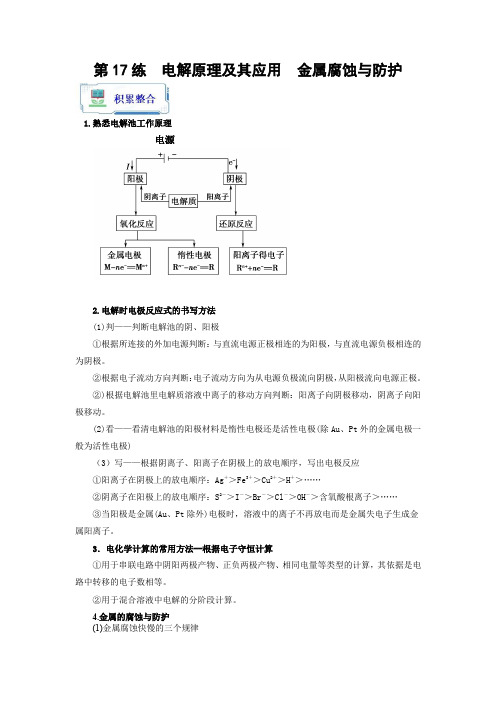
第17练电解原理及其应用金属腐蚀与防护1.熟悉电解池工作原理电源2.电解时电极反应式的书写方法(1)判——判断电解池的阴、阳极①根据所连接的外加电源判断:与直流电源正极相连的为阳极,与直流电源负极相连的为阴极。
②根据电子流动方向判断:电子流动方向为从电源负极流向阴极,从阳极流向电源正极。
②)根据电解池里电解质溶液中离子的移动方向判断:阳离子向阴极移动,阴离子向阳极移动。
(2)看——看清电解池的阳极材料是惰性电极还是活性电极(除Au、Pt外的金属电极一般为活性电极)(3)写——根据阴离子、阳离子在阴极上的放电顺序,写出电极反应①阳离子在阴极上的放电顺序:Ag+>Fe3+>Cu2+>H+>……②阴离子在阳极上的放电顺序:S2->I->Br->Cl->OH->含氧酸根离子>……③当阳极是金属(Au、Pt除外)电极时,溶液中的离子不再放电而是金属失电子生成金属阳离子。
3.电化学计算的常用方法--根据电子守恒计算①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相等。
②用于混合溶液中电解的分阶段计算。
4.金属的腐蚀与防护(1)金属腐蚀快慢的三个规律①金属腐蚀类型的差异电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀。
①电解质溶液的影响a.对同一金属来说,腐蚀的快慢(浓度相同):强电解质溶液>弱电解质溶液>非电解质溶液。
b.对同一种电解质溶液来说,电解质浓度越大,腐蚀越快。
①活泼性不同的两金属,活泼性差别越大,腐蚀越快。
(2)两种腐蚀与三种保护①两种腐蚀:析氢腐蚀、吸氧腐蚀(关键在于电解液的pH)。
①三种保护:电镀保护、牺牲阳极的阴极保护法、外加电流的阴极保护法。
1.(2023·湖北·校联考模拟预测)科研团队开创了海水原位直接电解制氢的全新技术(如图所KOH侧的水蒸气压力差使海水自发蒸发,并示)。
高中化学选择性必修1 第四章 第三节 金属的腐蚀与防护同步练习含详解答案

金属的腐蚀同步练习(答题时间:40分钟)一、选择题1. 下列有关金属腐蚀的说法中正确的是( )A. 金属腐蚀指不纯金属与接触到的电解质溶液进行化学反应而损耗的过程B. 电化学腐蚀指在外加电流的作用下不纯金属发生化学反应而损耗的过程C. 钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈D. 金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生2. 下列各种镀有金属保护层的铁板,镀层破损后在相同的环境中,铁板最易被腐蚀的是( )A. 镀锌铁(白铁)B. 镀锡铁(马口铁)C. 镀铜铁D. 镀银铁*3. 如图为模拟铁生锈的实验。
铁粉中均匀混有少量炭粉,撒入内壁已分别用氯化钠溶液和稀醋酸润湿过的甲、乙两个具支试管中,打开止水夹片刻后,下列有关该实验的说法合理的是( )甲 乙A. 甲装置导管口有气泡,乙装置导管内出现一段液柱B. 甲装置中发生的电化学腐蚀主要是析氢腐蚀C. 乙装置中发生的电化学腐蚀主要是吸氧腐蚀D. 乙装置导管口有气泡冒出4. 下列关于金属腐蚀的说法正确的是A. 金属在潮湿空气中腐蚀的实质是M +n H 2O =M (OH )n +2n H 2↑ B. 金属的化学腐蚀的实质是M -n e -=M n +,电子直接转移给氧化剂C. 金属的化学腐蚀必须在酸性条件下进行D. 在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀下列说法不正确...的是A. 对比②③,可以判定Zn保护了FeB. 对比①②,K3[Fe(CN)6]可能将Fe氧化C. 验证Zn保护Fe时不能用①的方法D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼二、非选择题6. 如图所示,水槽中试管内有一枚铁钉,放置数天后观察:(1)铁钉在逐渐生锈,则铁钉的腐蚀属于________腐蚀(填“化学”或“电化学”)。
(2)若试管内液面上升,则原溶液呈__________性,发生________腐蚀,电极反应式分别为负极:______________;正极:__________________。
金属腐蚀与防护课后习题及实验答案

3、大阴极小阳极会加速腐蚀速率4、腐蚀极化图说明其应用。
腐蚀极化图是一种电位—电流图,它是把表征腐蚀电池特征的阴、阳极极化曲线画在同一张图上构成的。
腐蚀极化图的应用(1)极化图用于分析腐蚀速度的影响因素(a)腐蚀速度与腐蚀电池初始电位差的关系:腐蚀电池的初始电位差(EO,C- EO,A ),是腐蚀的原动力(b)极化性能对腐蚀速度的影响:若腐蚀电池的欧姆电阻很小,则极化性能对腐蚀电流有很大的影响(c)溶液中含氧且及络合剂对腐蚀速度的影响;(例铜在含氧酸及氰化物中腐蚀极化图)(d)其他影响腐蚀速度的因素,如阴、阳极面积比和溶液电阻等。
(2)腐蚀速度控制因素:阳极控制、阴极控制、混合控制和欧姆控制。
1化学腐蚀的概念、及特点答案:化学腐蚀:介质与金属直接发生化学反应而引起的变质或损坏现象称为金属的化学腐蚀。
是一种纯氧化-还原反应过程,即腐蚀介质中的氧化剂直接与金属表面上的原子相互作用而形成腐蚀产物。
在腐蚀过程中,电子的传递是在介质与金属之间直接进行的,没有腐蚀电流产生,反应速度受多项化学反应动力学控制。
归纳化学腐蚀的特点1.在不电离、不导电的介质环境下2.反应中没有电流产生,直接完成氧化还原反应3.腐蚀速度与程度与外界电位变化无关11、举例说明有哪些可能的阴极去极化剂?当有几种阴极去极化剂同时存在时,如何判断哪一种发生还原的可能性最大?自然界中最常见的阴极去极化反应是什么?答案:(1)氢离子还原反应或析氢反应(电极反应式);(2)溶液中溶解氧的还原反应;(3)溶液中高价离子的还原反应;(4)溶液中贵金属离子的还原反应。
判断:(⊿G)T,P= nF⊿E(⊿G)T,P= nF(EC - EA)其中:EC 为氧化剂电位; EA为还原剂电位。
因此,⊿E越负,反应可能性越最大;有些情况下可利用氧化剂的平衡电极电位EC来粗略判断阴极去极化反应的可能性大小。
最常见的阴极去极化反应:析氢反应和吸氧反应12、何谓腐蚀极化图?说明其应用。
金属腐蚀与防护课后题答案

1.材料腐蚀的定义:腐蚀是材料受环境介质的化学、电化学和物理作用产生的损坏或变质现象。
腐蚀包括化学、电化学与机械因素或生物因素的共同作用。
2.腐蚀的特点:自发性/铁腐蚀变成以水和氧化铁为主的腐蚀产物,这些腐蚀产物在结构或形态上和自然界天然存在的铁矿石类似,或者说处于同一能量等级自发性只代表反应倾向,不等于实际反应速度普遍性/ 元素周期表中约有三、四十种金属元素,除了金和铂金可能以纯金属单体形式天然存在之外,其它金属都以它们的化合物(氧化物、硫化物)形式存在隐蔽性/ 应力腐蚀断裂管道:表面光亮如新,几乎不存在均匀腐蚀迹象,金相显微镜下,可观察到管道内部布满细微裂纹3.按材料腐蚀形态如何分类:全面腐蚀<均匀和不均匀腐蚀> 局部腐蚀{ 点蚀(孔蚀、)缝隙腐蚀及丝状腐蚀、电偶腐蚀(接触腐蚀)晶间腐蚀}选择性腐蚀4.按材料腐蚀机理如何分类:化学腐蚀、电化学腐蚀、物理溶解腐蚀5.按材料腐蚀环境如何分类:自然环境腐蚀、工业环境腐蚀、生物环境腐蚀1、名词解释物理腐蚀:是指金属由于单纯的物理溶解作用而引起的破坏电化学腐蚀:就是金属和电解质组成两个电极,组成腐蚀原电池。
电极电位:金属-溶液界面上建立了双电层,使得金属与溶液间产生电位差,这种电位差称为电极电位(绝对电极电位)非平衡电极电位:(在生产实际中,与金属接触的溶液大部分不是金属自身离子的溶液)当电极反应不处于平衡状态,电极系统的电位称为非平衡电位。
平衡电极电位:水合金属离子能够回到金属中去,水合-金属化过程速率相等且又可逆,这时的电极电位。
标准电极电位:金属在25℃浸于自身离子活度为1mol/L的溶液中,分压为1×105Pa时的平衡电极电位极化:电流流过电极表面,电极就会失去平衡,并引起电位的变化去极化:能降低电极极化的因素称为去极化因素过电位:是电极的电位差值,为一个电极反应偏离平衡时的电极电位与这个电极反应的平衡电位的差值。
活化极化:设电极反应的阻力主要来自电子转移步骤,液相传质容易进行,这种电极反应称为受活化极化控制的电极反应。
第3节金属的腐蚀与防护

第三节金属的腐蚀与防护课后·训练提升基础巩固1.铁锅表面覆盖有下列物质时,锈蚀最快的是()。
A.水B.食盐水C.食用油D.酒精答案:B解析:当形成电化学腐蚀,且铁作原电池的负极材料时,表面覆盖的溶液导电性越强,锈蚀越快。
食用油和酒精不能导电,不能形成原电池反应,而水的导电性没有食盐水强,所以锈蚀最快的是食盐水,故选B。
2.下列叙述不正确的是()。
A.锌与稀硫酸反应制取氢气,加入少量的硫酸铜能增大反应速率B.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀C.钢铁表面常易被锈蚀生成Fe2O3·n H2OD.钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应答案:B解析:锌与CuSO4发生置换反应后,铜附着在锌的表面上,浸泡在稀硫酸中形成锌铜原电池,负极锌被氧化而加速反应,A项正确;镀锌的铁构成原电池时锌为负极,铁为正极,铁被保护,镀锡的铁构成原电池时铁作负极,锡作正极,加速了铁的腐蚀,B项不正确;钢铁的锈蚀主要是吸氧腐蚀,负极(Fe)反应为Fe-2e-Fe2+,正极(C)反应为2H2O+O2+4e-4OH-,形成Fe(OH)2,在空气中4Fe(OH)2+O2+2H2O4Fe(OH)3,久置后2Fe(OH)3Fe2O3+3H2O,所以铁锈的成分是Fe2O3·n H2O,C项正确;钢铁在发生析氢腐蚀和吸氧腐蚀时,负极反应相同,都是Fe-2e-Fe2+,但正极反应不同,分别是析出氢气和吸收氧气,D项正确。
3.下列说法中,不正确的是()。
A.钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀B.钢铁表面水膜的酸性较强,发生析氢腐蚀C.将锌板换成铜板对钢闸门保护效果更好D.钢闸门作为阴极而受到保护答案:C解析:当钢铁表面的水膜酸性很弱或显中性时,铁在负极放电,氧气在正极上放电,发生的是钢铁的吸氧腐蚀,A项正确;当钢铁表面的水膜酸性较强时,铁在负极放电,水膜中的氢离子在正极放电生成氢气,发生的是析氢腐蚀,B项正确;在原电池中,正极被保护,当将锌板换成铜板后,铜作正极被保护,钢闸门作负极被腐蚀,起不到对钢闸门的保护作用,C项错误;在电解池中,阴极被保护,故要保护钢闸门,就要使钢闸门作电解池的阴极,D项正确。
高中化学 金属的腐蚀与防护(解析版)

课时34 金属的腐蚀与防护1.关于金属腐蚀的叙述中,正确的是( )A .金属被腐蚀的本质是M +n H 2O===M(OH)n +n 2H 2↑ B .马口铁(镀锡铁)镀层破损后被腐蚀时,首先是镀层被氧化C .金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀D .常温下,置于空气中的金属主要发生化学腐蚀【答案】C【解析】金属腐蚀的本质主要是金属原子失电子被氧化,腐蚀的内因是金属的化学性质比较活泼,外因是金属与空气、水和其他腐蚀性的物质相接触,腐蚀主要有化学腐蚀和电化学腐蚀。
A 中金属腐蚀的本质应包括化学腐蚀和电化学腐蚀,为M -n e -===M n +;B 选项中Sn 、Fe 构成电化学腐蚀,主要是Fe -2e -===Fe 2+,铁先被腐蚀。
常温下,空气中的金属主要发生电化学腐蚀中的吸氧腐蚀,难以和非金属氧化剂(Cl 2、S)等反应,发生化学腐蚀。
2.下列叙述中正确的是( )A .原电池的负极发生还原反应B .电化学腐蚀的实质是金属单质失去电子形成阳离子,而电子直接转移给氧化剂C .金属在中性环境中主要发生析氢腐蚀D .钢铁在潮湿环境中锈蚀时,开始生成Fe(OH)2,而后逐渐变成Fe(OH)3和Fe 2O 3·xH 2O【答案】D【解析】不论是吸氧腐蚀还是析氢腐蚀,都是先生成Fe(OH)2,再逐渐转变成Fe(OH)3和Fe 2O 3·xH 2O 。
3.以下防腐措施中,属于电化学保护法的是( )A .用氧化剂使金属表面生成致密稳定的氧化物保护膜B .在金属中加入一些铬或者镍制成合金C .在轮船的船壳水线以下部分,装上一锌锭D .在金属表面喷漆【答案】C【解析】在轮船的船壳水线以下部分,装上锌能形成铁锌原电池,锌为负极,被腐蚀,铁被保护。
4.铜制品上的铝质铆钉,在潮湿空气中易发生腐蚀的主要原因可描述为( )A .形成原电池,铝作负极B.形成原电池,铜作负极C.形成原电池时,电流由铝经导线流向铜D.铝质铆钉发生了化学腐蚀【答案】A【解析】金属铝发生的是电化学腐蚀,铝比铜活泼,故金属铝是负极,电流的流动方向与电子的流动方向恰好相反,应是由铜经导线流向铝。
人教版高中化学选修1 第三章 第二节 金属的腐蚀和防护练习含答案

第二节金属的腐蚀和防护1.为什么钢铁在潮湿的环境中比在干燥的环境中更容易生锈?提示:不纯的金属或合金,在潮湿的空气中形成微小原电池而发生电化学腐蚀,主要发生吸氧腐蚀,加快了反应速率。
►综合拓展一、化学腐蚀和电化学腐蚀的比较二、吸氧腐蚀与析氢腐蚀的比较(以钢铁腐蚀为例)►尝试应用1.钢铁在很弱的酸性或中性条件下发生电化学腐蚀时,正极的反应式为(C)A.Fe-2e-===Fe2+B.2H++2e-===H2↑C.2H2O+O2+4e-===4OH-D.Fe-3e-===Fe3+解析:考查金属的电化学腐蚀的实质。
钢铁中含有多种杂质,在考虑钢铁的电化学腐蚀时,为了简化问题,主要讨论碳杂质问题,也就是以Fe为负极,C为正极的原电池反应。
在中性条件或弱酸性条件下发生的是吸氧腐蚀,原电池的正极为C,发生还原反应,即得电子反应,故A、D两项应排除,在B、C两项中,B项是析氢腐蚀的电极反应式,所以C项符合题意。
金属的防护2.镀锌铁与镀锡铁的镀层破损后,哪个更耐腐蚀?提示:镀锌铁更耐腐蚀,因为发生电化学腐蚀时,锌比铁活泼,因此适合作原电池的负极,失去电子被氧化,从而保护了铁。
而锡不如铁活泼,当镀锡铁镀层破损后,铁做负极,失去电子被氧化。
►综合拓展三、金属的防护1.保持金属表面清洁干燥。
2.金属表面涂抹油漆等保护层。
3.改变金属内部结构,如制成合金。
4.通过化学方法使其表面形成保护层,如电镀、形成氧化膜等。
5.电化学防护法——牺牲阳极的阴极保护法。
电化学防护法应用原电池原理,让被保护金属作为正极,另找一种活动性较强的金属作为负极。
例如在锅炉内壁、船舶外壳装上若干锌块,就可保护钢铁设备。
发生的电极反应:负极:2Zn-4e-===2Zn2+;正极:O2+2H2O+4e-===4OH-。
锌块不断被腐蚀,可定期拆换,使铁得到保护。
►尝试应用2.下列做法不能起防锈作用的是(A)A.保留铁制品上的铁锈B.在铁制品表面镀锌C.在金属机械上涂油D.在车、船的表面刷油漆解析:铁锈是比较疏松的氧化膜,容易保存一些水分,形成电解质溶液加速铁的腐蚀,不能起到防锈的作用。
金属防护与腐蚀习题解答

因不知icorr ,所以忽略a ,可用E0,a 估算 Ecorr ,即E0,a =Ecorr
EFe=E0Fe
0.029 Ecorr EFe E Fe lg106 2 0.44 (0.087) 0.527(V )
0
铜电极和氢电极(PH2=2atm)浸在Cu2+ 活度为1且pH=1的CuSO4溶液中 组成电池,25°C,求该电池的电动势,并判断电池的极性。
低碳刚在pH=1的无氧水溶液中,腐蚀电位 为-0.72V(相对饱和Cu/CuSO4电极)。对于同 样钢的氢过电位(单位为V)遵循下列关系:η =0.7+0.1lgi,式中i的单位为A· -2。假定所有 cm 钢表面近似作为阴极,计算腐蚀速度(g/m2· h)。
解: 已知pH=1, Ecorr = -0.72V(相对饱和Cu/Cu2+) 饱和Cu/Cu2+的E = + 0.32V 故Ecorr= -0.72 + 0.32 = -0.4 V(SHE) E 0,C = EH+/H2 = -0.059 pH=-0.0591=-0.059(V) ηC= Ecorr- E 0,C = -0.4 - (-0.059) = -0.341 (V) 根据η=0.7 + 0.1 lgi 可求出lgicorr
4
(icorr单位:µA•cm-2)
A Vt 3.27 10 icorr n 56 3 3.27 10 100 2 7.87 1.16(m m a 1 )
3
或Vt 8.76
1.04 8.76 7.87 1.16(m m a 1 )
V
aCd 2
KspCd (OH )2 a 2OH
2 1014 2 7 2 (1 10 )
(完整版)金属腐蚀与防护课后习题答案

腐蚀与防护试题1化学腐蚀的概念、及特点答案:化学腐蚀:介质与金属直接发生化学反应而引起的变质或损坏现象称为金属的化学腐蚀。
是一种纯氧化-还原反应过程,即腐蚀介质中的氧化剂直接与金属表面上的原子相互作用而形成腐蚀产物。
在腐蚀过程中,电子的传递是在介质与金属之间直接进行的,没有腐蚀电流产生,反应速度受多项化学反应动力学控制。
归纳化学腐蚀的特点在不电离、不导电的介质环境下反应中没有电流产生,直接完成氧化还原反应腐蚀速度与程度与外界电位变化无关2、金属氧化膜具有保护作用条件,举例说明哪些金属氧化膜有保护作用,那些没有保护作用,为什么?答案:氧化膜保护作用条件:①氧化膜致密完整程度;②氧化膜本身化学与物理稳定性质;③氧化膜与基体结合能力;④氧化膜有足够的强度氧化膜完整性的必要条件:PB原理:生成的氧化物的体积大于消耗掉的金属的体积,是形成致密氧化膜的前提。
PB原理的数学表示:反应的金属体积:V M = m/ρ m-摩尔质量氧化物的体积: V MO = m'/ ρ '用ϕ = V MO/ V M = m' ρ /( m ρ ' )当ϕ > 1 金属氧化膜具备完整性条件部分金属的ϕ值氧化物ϕ氧化物ϕ氧化物ϕMoO3 3.4 WO3 3.4 V2O5 3.2Nb2O5 2.7 Sb2O5 2.4 Bi2O5 2.3Cr2O3 2.0 TiO2 1.9 MnO 1.8FeO 1.8 Cu2O 1.7 ZnO 1.6Ag2O 1.6 NiO 1.5 PbO2 1.4SnO2 1.3 Al2O3 1.3 CdO 1.2MgO 1.0 CaO 0.7MoO3 WO3 V2O5这三种氧化物在高温下易挥发,在常温下由于ϕ值太大会使体积膨胀,当超过金属膜的本身强度、塑性时,会发生氧化膜鼓泡、破裂、剥离、脱落。
Cr2O3 TiO2 MnO FeO Cu2O ZnO Ag2O NiO PbO2 SnO2 Al2O3 这些氧化物在一定温度范围内稳定存在,ϕ值适中。
金属腐蚀与防护课后习题答案培训资料

金属腐蚀与防护课后习题答案腐蚀与防护试题1化学腐蚀的概念、及特点答案:化学腐蚀:介质与金属直接发生化学反应而引起的变质或损坏现象称为金属的化学腐蚀。
是一种纯氧化-还原反应过程,即腐蚀介质中的氧化剂直接与金属表面上的原子相互作用而形成腐蚀产物。
在腐蚀过程中,电子的传递是在介质与金属之间直接进行的,没有腐蚀电流产生,反应速度受多项化学反应动力学控制。
归纳化学腐蚀的特点在不电离、不导电的介质环境下反应中没有电流产生,直接完成氧化还原反应腐蚀速度与程度与外界电位变化无关2、金属氧化膜具有保护作用条件,举例说明哪些金属氧化膜有保护作用,那些没有保护作用,为什么?答案:氧化膜保护作用条件:①氧化膜致密完整程度;②氧化膜本身化学与物理稳定性质;③氧化膜与基体结合能力;④氧化膜有足够的强度氧化膜完整性的必要条件:PB原理:生成的氧化物的体积大于消耗掉的金属的体积,是形成致密氧化膜的前提。
PB原理的数学表示:反应的金属体积:V M = m/ρ m-摩尔质量氧化物的体积: V MO = m'/ ρ '用ϕ = V MO/ V M = m' ρ /( m ρ ' )当ϕ > 1 金属氧化膜具备完整性条件部分金属的ϕ值氧化物ϕ氧化物ϕ氧化物ϕMoO3 3.4 WO3 3.4 V2O5 3.2Nb2O5 2.7 Sb2O5 2.4 Bi2O5 2.3Cr2O3 2.0 TiO2 1.9 MnO 1.8FeO 1.8 Cu2O 1.7 ZnO 1.6Ag2O 1.6 NiO 1.5 PbO2 1.4SnO2 1.3 Al2O3 1.3 CdO 1.2MgO 1.0 CaO 0.7MoO3 WO3 V2O5这三种氧化物在高温下易挥发,在常温下由于ϕ值太大会使体积膨胀,当超过金属膜的本身强度、塑性时,会发生氧化膜鼓泡、破裂、剥离、脱落。
Cr2O3 TiO2 MnO FeO Cu2O ZnO Ag2O NiO PbO2 SnO2 Al2O3 这些氧化物在一定温度范围内稳定存在,ϕ值适中。
金属腐蚀与防护课后习题 陈颖敏 李志勇编

阳极极化: -E(mV,对SCE) i(A/cm2)
360 47 350 57 72
406
404
3
第四章(P62)
9. 已知ECu2+/Cu=+0.34V(25oC),在溶液中,为什么铜可能发生耗 氧腐蚀,并不会发生析氢腐蚀?
解:因为EH+/H2= -0.059pH = -0.413(V) EO2/OH- =1.229 - 0.059 pH =+0.814(V )
(pH=7) (pH=7)
0.202 0.7 lg i 0.1
icorr 9.551010 A cm2 9.551010
A cm
2
Vt 3.27 103
3
A icorr n
56 9.5510 4 3.27 10 2 7.87 1.11105 m m a 1
解:已知E0Cu=+0.337V, aCu=1 0.059 ECu 0.337 lg1 0.337(V ) 2
已知PH2=2atm, pH=1(aH=10-1)
EH E
0 H
0.059lg
aH
PH 2
101 EH 0 0.059lg 0.0295 2
E电=+0.337-(-0.029)=+0.3665(V) 铜电极为正极,氢电极为负极。43;/Cu < E0 O2/H2O = +1.229 (V) Cu可能发生腐蚀。
金属腐蚀与防护课后习题答案 (1)

腐蚀与防护试题1化学腐蚀的概念、及特点答案:化学腐蚀:介质与金属直接发生化学反应而引起的变质或损坏现象称为金属的化学腐蚀。
是一种纯氧化-还原反应过程,即腐蚀介质中的氧化剂直接与金属表面上的原子相互作用而形成腐蚀产物。
在腐蚀过程中,电子的传递是在介质与金属之间直接进行的,没有腐蚀电流产生,反应速度受多项化学反应动力学控制。
归纳化学腐蚀的特点在不电离、不导电的介质环境下反应中没有电流产生,直接完成氧化还原反应腐蚀速度与程度与外界电位变化无关2、金属氧化膜具有保护作用条件,举例说明哪些金属氧化膜有保护作用,那些没有保护作用,为什么?答案:氧化膜保护作用条件:①氧化膜致密完整程度;②氧化膜本身化学与物理稳定性质;③氧化膜与基体结合能力;④氧化膜有足够的强度氧化膜完整性的必要条件:PB原理:生成的氧化物的体积大于消耗掉的金属的体积,是形成致密氧化膜的前提。
PB原理的数学表示:反应的金属体积:V M = m/? m-摩尔质量氧化物的体积: V MO = m'/ ? '用? = V MO/ V M = m' ? /( m ? ' )当? > 1 金属氧化膜具备完整性条件部分金属的?值氧化物?氧化物?氧化物?MoO3 WO3 V2O5Nb2O5 Sb2O5 Bi2O5Cr2O3 TiO2 MnOFeO Cu2O ZnOAg2O NiO PbO2SnO2 Al2O3 CdOMgO CaOMoO3 WO3 V2O5这三种氧化物在高温下易挥发,在常温下由于?值太大会使体积膨胀,当超过金属膜的本身强度、塑性时,会发生氧化膜鼓泡、破裂、剥离、脱落。
Cr2O3 TiO2 MnO FeO Cu2O ZnO Ag2O NiO PbO2 SnO2 Al2O3 这些氧化物在一定温度范围内稳定存在,?值适中。
这些金属的氧化膜致密、稳定,有较好的保护作用。
MgO CaO ?值较小,氧化膜不致密,不起保护作用。
(完整版)材料腐蚀与防护工程课后习题答案

五、忠考题1•秦见教材P4-5.2. 化学腐蚀包括金属在千燥气体(我高温%体)作用下的馬蚀和金属在非电解质溶液中的傳蚀•其反应过程的历栈特点是金属表面的原子与敦化制直揍发生直化还原反应而形成腐蚀产物,电子在金属和氧化刑之间直揍传递,无腐蚀电流产生。
电化学腐蚀是金属表而与电終质溶液发生电化学反应而弓起的砍坏•例如钢铁在土煨中的局蚀。
电化学局蚀的希点是腐蚀及应过桂中至少有一个阳极反应和阴极反应,在反宜过程中发生电荷转移,伴有电流产生。
金属在实际工程中出现的腐蚀大多數均为电化学腐蚀,金属点电化学和应力及微生扬共同作用下还会发生应力以蚀和微生扬腐蚀。
联系:二者均发生氧化还原反应。
3. 参见教材P11-12.第2章野—、滇空题1. 氢2•阳.阴3.紮密双电层结构樓型、扩敷双电展结的樓型、斯转恩双电孱樸型4•显若、较小5.电子、电极反应6.仅有一个电极反应、零、平衡电位二、判断题1. x2. x3. x4. x5. V6. V7. J三、名词解释腐蚀原电池:局蚀体系中形成的粗路原电池,祖:腐蚀金属麦它的一个电极。
氧浓差电池:由金屬与敦含叢不同的腐蚀外施相扶統时形成的浓差电池电极电位;电极及应早致农金属和溶液的界面上形成双电展,双电鸟两侧的电伎差,即为电极电位,又称为处•对电极电位。
平衡电位:当金属浸在同种金爲禹子的濬液中发生唯一的一种电极反应,且当电极反应达到动态平衡时,印金属的溶解速度等于金属离子的況积速度,将这种电位称为平衡电位戏可逆电位.腐蚀电位:材料在给定摘蚀依系*的电极电位。
非平衡电位:一个电极上同时发生两个或两个以上的电极反应,当动态平衡时,电极上不能出现粉质交换与电荷交换均达到平衡的悄况,此时的电极电位称非平衡电位。
极化:由于电极上有净电流通过,电极电位显著僞离了未通电时的开略电位(平虧电位或非平衡的稳态电位),这种现象通帑称为极化.过电位:某一极化电流下而叛生的电极电位E僞离于原电极平衡电位Ee的曼化值的址对值,称作该电极反应的过电位。
高中化学《金属的化学腐蚀与防护》练习题(附答案解析)

高中化学《金属的化学腐蚀与防护》练习题(附答案解析)学校:___________姓名 ___________班级 ___________一单选题1.铁钉和碳棒用导线连接后,浸入0.01 mol·L-1 NaCl溶液中,可能发生的是()①碳棒上有氢气析出②碳棒附近产生OH- ③碳棒上有氧气析出④铁钉被氧化A.①③B.①④C.②③D.②④2.下列有关金属的腐蚀与防护的说法中,不正确的是()A.在铁管外壁上镀锌可防止其被腐蚀 B.金属被腐蚀的本质是金属发生了氧化反应C.温度越高,金属腐蚀速率越快 D.将钢闸门与直流电源的正极相连可防止其被腐蚀3.下列关于钢铁锈蚀的叙述中,错误的是()A.酸雨能使钢铁更容易发生电化学腐蚀B.钢铁在潮湿的地窑中较易发生析氢腐蚀C.铁锈的主要成分是Fe2O3·nH2OD.钢铁锈蚀时,铁原子失去电子成为Fe3+,而后生成Fe(OH)3,再部分脱水成为氧化铁的水合物4.下列关于自行车金属部件的防腐措施中,错误的是()A.为车架,挡泥板车座弹簧烤上一层漆B.为链条涂上机油,为轴承涂上凡士林C.对车圈,辐条进行电镀处理D.把自行车存放在高温潮湿的地方5.2021年在四川广汉三星堆新发现大量青铜器,下列有关说法错误的是()A.铜是人类使用最早的金属之一B.青铜比纯铜具有更高的硬度和更强的抗腐蚀性能C.出土的青铜器深埋于地下生锈是因为发生了析氢腐蚀D.青铜是铜锡铅等的合金,常见的铜合金还有黄铜和白铜6.下列关于钢铁腐蚀的叙述不正确...的是()A.钢铁在潮湿的空气中易腐蚀B.钢铁腐蚀的主要原因是化学腐蚀C.腐蚀使钢铁色泽外形等发生变化D.一般情况下,温度对钢铁的化学腐蚀影响较明显7.下列措施不能有效防止钢铁腐蚀的是()A.在钢铁中加入铬B.把钢铁零件放在机油中保存C .在较小钢铁制品的表面包裹塑料D .在大型铁壳船表面喷涂油漆并铆上铜块8.结合学习生活经历,判断下列叙述不正确的是( )A .电热水器用镁棒防止金属内胆腐蚀,原理是牺牲阳极的阴极保护法B .将单液原电池设计成双液原电池是为了减少化学能转化为热能而造成损失C .测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度D .铅蓄电池使用一段时间后,电解质溶液的酸性减弱,导电能力下降9.下列对于电化学说法正确的是( )A .为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭B .电解精炼铜时,阳极泥中常含有金属金 银 锌等C .可充电电池放电时,化学能转变为电能D .利用电解池原理对金属进行腐蚀防护的方法叫牺牲阳极的阴极保护法10.化学与生产 生活 科技和环境等联系密切,下列说法错误的是( )A .襄阳大头菜含有氨基酸 维生素 纤维素等高分子有机物,均可被人体吸收利用B .襄阳汉江边的临汉门是木质,包上铁皮订上铜钉可防火攻但是会加快铁皮的腐蚀C .锅炉水垢中含有4CaSO ,可先用23Na CO 溶液处理,后用酸除去D .较低温度更有利于合成氨反应得到较大的平衡转化率11.下列事实可以用电化学理论解释的是( )A .白磷固体在空气中易自燃B .实验室中镁不需要保存在煤油中C .实验室配制CuCl 2溶液时常加入适量盐酸D .电工规范上,铜 铝电线不能直接绞接在一起12.利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间。
金属腐蚀与防护课后习题答案(精选)

第二章2. 某腐蚀体系的参数为:E 0a = -0.4V ,E 0c = 0.8V ,E cor = -0.2V 。
当R = 0时,I cor = 10mA ,该腐蚀电池属于什么控制类型?如果欧姆电阻R = 90Ω,那么I 'cor =? 腐蚀电池又属于什么控制类型?解:由题可知:当R=0时有: I cor =(Eoc-Eoa)/ (Pc+Pa )Pc+Pa=(Eoc-Eoa)/ I cor =(0.8+0.4)/10×210-=120ΩPc=(Eoc-Ec)/ I cor =(0.8+0.2)/10×310-=100Ω则有 Pa=120-100=20Ω因为Pc>>Pa ,所以该电池属于阳极极化控制。
当欧姆电阻R=90Ω时有:'Icor=(Eoc-Eoa)/(Pc+Pa+R)=(0.8+0.4)/(120+90)=5.71mA因为R 与Pc 接近,所以该腐蚀电池为欧姆电阻和阳极极化共同控制。
第四章5. 一个活化极化控制腐蚀体系,阴极反应和阳极反应的交换电流密度为0c i 、0a i ;Tafel斜率为b c 、b a ;腐蚀电位满足条件E ea <<E cor <<E ec 。
设加入阴极性缓蚀剂,使阴极反应受到抑制,阴极反应交换电流密度改变为)(0'c i 。
假定其他参数都不改变,此时腐蚀电位负移到E 'cor ,腐蚀电流密度下降到i 'cor 。
(1) 作加入缓蚀剂前后腐蚀体系的极化曲线图。
(2) 用图解法求腐蚀电流密度的变化r = i 'cor / i cor 和腐蚀电位的变化∆E = E 'cor – E cor 。
解:极化曲线如右图;由(1)的极化曲线利用图解法求解得:在△ABC 中,1.2直线段位两平行线,则有:ADCD bc DBCD ba ====αβtan ,tanba ,bc 分别为未加入缓蚀剂时阳极反应和加入缓蚀剂后阴极反应的Tafel 斜率:根据AB babc bc DB AB BDCD ADCD DC CDAB DBAD DB AB ABDB DB 11)(,)(--+=+=+==即由图可知有:10001)(lg|)|lg |'|(lg ,)'(lg|)|lg |'|(lg --=--==--=cc c c corcor cor cor i i i i AB i i i i DB,','lg'lg,)|||'|(lg)()'(lg111BD BDCD CD E E i i babc bc i i i i BDCD ADCD BD CDi i cor cor cc corcor c c corcor ⨯==-+=∴⨯+=--- 又0'lg'lg'cc cc cor cor i i bcba babc i i bcba bc ba E E E +=⨯+⨯=-=∆∴第四章6. 一个阳极反应受活化极化控制、阴极反应受浓度极化控制的腐蚀体系,阴极反应的极限扩散电流密度为i d ,腐蚀电位为E cor 。
金属腐蚀与防护课后习题 陈颖敏 李志勇编

解:
A V 3.7310 icorr n 56 4 3.7310 100 2 1.04( g m 2 h 1 )
4
(icorr单位:µA•cm-2)
A Vt 3.27 10 icorr n 56 3 3.27 10 100 2 7.87 1.16(m m a 1 )
解:阳极反应 : Fe
0
2
Fe2+ + 2e (25℃)
0.059 EFe2 / Fe E Fe / Fe lg106 2 0.44 (0.177) 0.617(V )
阴极反应: 2H+ + 2e EH+/H2 = - 0.059pH = - 0.413(V)
H2 (pH=7)
24 365 Vt 1000 V 0.1 8.76 8.76 8.9 V 0.098(m m a 1 )
可见, Vt在0.05~0.5 mm/a , 由表1-3知,Cu 的耐蚀性良好。
第二章(P31)
11. 已知铜在含氧酸中和无氧酸中的电极反应及其标准电极电位:
0.059 lg a Fe2 2 0.059 0.44 lg 0.164 2 0.463(V )
因为,EO2/OH- = + 0.815 (V) EO2/OH- > EFe2+/Fe E电 = + 0.815 - (-0.463) = +1.278(V) > 0 故发生耗氧腐蚀。
13.铜电极和氢电极(PH2=2atm)浸在Cu2+ 活度为1且pH=1的 CuSO4溶液中组成电池,25°C,求该电池的电动势,并判断电池的极 性。
i(A/cm2) 470 54 480 66 406 0 490 78 410 2.2 500 89 420 5.6 510 104 430 14 520 119 440 24 450 34 460 44
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
腐蚀与防护试题1化学腐蚀的概念、及特点答案:化学腐蚀:介质与金属直接发生化学反应而引起的变质或损坏现象称为金属的化学腐蚀。
是一种纯氧化-还原反应过程,即腐蚀介质中的氧化剂直接与金属表面上的原子相互作用而形成腐蚀产物。
在腐蚀过程中,电子的传递是在介质与金属之间直接进行的,没有腐蚀电流产生,反应速度受多项化学反应动力学控制。
归纳化学腐蚀的特点在不电离、不导电的介质环境下反应中没有电流产生,直接完成氧化还原反应腐蚀速度与程度与外界电位变化无关2、金属氧化膜具有保护作用条件,举例说明哪些金属氧化膜有保护作用,那些没有保护作用,为什么?答案:氧化膜保护作用条件:①氧化膜致密完整程度;②氧化膜本身化学与物理稳定性质;③氧化膜与基体结合能力;④氧化膜有足够的强度氧化膜完整性的必要条件:PB原理:生成的氧化物的体积大于消耗掉的金属的体积,是形成致密氧化膜的前提。
PB原理的数学表示:反应的金属体积:V M = m/ρ m-摩尔质量氧化物的体积: V MO = m'/ ρ '用ϕ = V MO/ V M = m' ρ /( m ρ ' )当ϕ > 1 金属氧化膜具备完整性条件部分金属的ϕ值氧化物ϕ氧化物ϕ氧化物ϕMoO3 3.4 WO3 3.4 V2O5 3.2Nb2O5 2.7 Sb2O5 2.4 Bi2O5 2.3Cr2O3 2.0 TiO2 1.9 MnO 1.8FeO 1.8 Cu2O 1.7 ZnO 1.6Ag2O 1.6 NiO 1.5 PbO2 1.4SnO2 1.3 Al2O3 1.3 CdO 1.2MgO 1.0 CaO 0.7MoO3 WO3 V2O5这三种氧化物在高温下易挥发,在常温下由于ϕ值太大会使体积膨胀,当超过金属膜的本身强度、塑性时,会发生氧化膜鼓泡、破裂、剥离、脱落。
Cr2O3 TiO2 MnO FeO Cu2O ZnO Ag2O NiO PbO2 SnO2 Al2O3 这些氧化物在一定温度范围内稳定存在,ϕ值适中。
这些金属的氧化膜致密、稳定,有较好的保护作用。
MgO CaO ϕ值较小,氧化膜不致密,不起保护作用。
3、电化学腐蚀的概念,与化学腐蚀的区别答案:电化学腐蚀:金属与介质发生电化学反应而引起的变质与损坏。
与化学腐蚀比较:①是“湿”腐蚀②氧化还原发生在不同部位③有电流产生④与环境电位密切相关⑤有次生产物4、解释现象:试验1:铜块与锌块相互接触,放入稀盐酸介质中,在铜块一侧有氢气产生,而锌块逐渐溶解。
试验2:将铜块与锌块不相互接触,而在体系外用导线连接,若在导线间连接电流表。
铜块一侧有氢气产生,而锌块逐渐溶解,电流表针发生转动。
试验3:将锌块置于稀盐酸介质中,可见锌块不断溶解,氢气不断产生。
答案:在电动序上,锌比铜易失去电子,电子通过导线或与铜接触面进入铜块,在铜表面将电子传递给氢离子而形成氢气。
同时锌离子进入溶液。
Zn → Zn 2++2e 阳极 2H ++2e(Cu) →H 2↑ 阴极锌块自身在盐酸介质之中的溶解问题的解释:微观动态腐蚀电池。
结论:将两种不同电极电位的金属相互接触(或用导线连接)放入同一种电解质溶液中。
现象:电位较正的一端产生气泡,较负的一端会逐渐溶解。
5、解释现象:试验:3%NaCl 水溶液1滴至光亮的铁片上,加少量铁氰化钾(K 3Fe(CN)6)和酚酞试剂,然后把铁片置于磁场中。
现象:在液滴上逐渐产生蓝红相间的斑点,接着液滴中心变蓝,边缘便成粉红,液滴缓慢旋转。
答案:解释现象:在液滴上,初期溶解氧一旦被还原,大气中的氧优先溶于液滴边缘,使液滴中心相对贫氧,使整个液滴产生氧浓差。
结果:液滴中心较负成为阳极, 发生:Fe →2e = Fe 2+反应。
Fe 2+ 与K 3Fe(CN)6作用,形成蓝色。
液滴边缘部位较正,成为阴极, 发生:O 2+H 2O +4e →4OH -反应。
OH -与酚酞作用,形成粉红色。
又由于液滴中心的Fe 2+ 向边缘扩散, OH -向中心扩散,使在铁片内部的电子流向液滴边缘而形成磁场,在外磁场的相互作用下,使液滴发生旋转。
6、举例说明氧浓差腐蚀答案:例:金属在土壤中(与土接触点为贫氧,为负极,金属腐蚀;与空气接触点为富氧,为正极,金属不腐蚀。
)船的吃水线附近(水下为贫氧区,为负极,金属腐蚀;水上为富氧区,金属不腐蚀。
搅拌杆与液面接触处(同上)。
7、解释现象:试验:一根铜丝一端置于0.1mol/LCuSO 4溶液中,另一端置于1mol/LCuSO 4溶液中。
发现,铜丝置于0.1mol/LCuSO 4溶液中的一端发生腐蚀(不断溶解)。
答案:解释:由于两种浓度的盐通过铜丝组成了同一体系:高浓度一端铜离子有沉积的趋势,低浓度的一端铜有溶解的趋势,则,低浓度一端溶解给出的电子沿铜片流向另一端(高浓度一端),以满足沉积铜所需要的电子。
只所以发生电子流动,是因为在两端盐浓差使铜丝两端产生电位差。
8、解释现象:试验:一根铁丝一端置于高温溶液中,另一端置于低温溶液中。
发现,铁丝置于高温溶液中的一端发生腐蚀(不断溶解)。
答案:解释:高温部位金属活性强,易脱离金属表面而氧化,低温区或性弱。
这样形成高温区的金属氧化,产生的电子由铁丝流向低温一端,是低温一端的金属离子沉积。
各种热交换器、燃烧器等已发生温差腐蚀9、绘出Fe —H 2O 的E —pH 图,指出保护区、腐蚀区、钝化区和过钝化区。
并举例说明该图的应用。
答案:金属的E—pH图的应用预计一定条件下的金属腐蚀行为反应金属自发腐蚀热力学倾向指明金属实施保护的可能性与方向总结E—pH图的规律:上腐蚀、下稳定、两边(左右)腐蚀、中间钝化。
常见金属在中性介质中都比较稳定。
应用举例:如图1,当环境条件在红点处时,通过调整酸度可使其进入钝化区;实行阴极保护可使其进入保护区。
10、理论电位—pH图的局限性?答案:一些局限性:1.由于金属的理论电位—pH图是一种以热力学为基础的电化学平衡图,因此它只能预示金属腐蚀倾向的大小,而不能预测腐蚀速度的大小。
2.图中的各条平衡线,是以金属与其离子之间或溶液中的离子与含有该离子的腐蚀产物之间建立的平衡为条件的,但在实际腐蚀情况下,可能偏离这个平衡条件。
3.电位—pH图只考虑了OH-这种阴离子对平衡的影响。
但在实际腐蚀环境中,往往存在Cl-、SO42-、P032-等阴离子,它们可能因发生一些附加反应而使问题复杂化。
4.理论电位—pH图中的钝化区并不能反映出各种金属氧化物、氢氧化物等究竟具有多大的保护性能。
5.绘制理论电位—pH图时,往往把金属表面附近液层的成分和PH大小等同于整体的数值。
实际腐蚀体系中,金属表面附近和局部区域内的pH值与整体溶液的pH值其数值往往并不相同。
因此,应用电位—pH图时,必须针对具体情况,进行具体分析,过分夸大或贬低电位—pH图的作用都是不对的。
11、举例说明有哪些可能的阴极去极化剂?当有几种阴极去极化剂同时存在时,如何判断哪一种发生还原的可能性最大?自然界中最常见的阴极去极化反应是什么?答案:(1)氢离子还原反应或析氢反应(电极反应式);(2)溶液中溶解氧的还原反应;(3)溶液中高价离子的还原反应;(4)溶液中贵金属离子的还原反应。
判断:(⊿G)T,P= nF⊿E(⊿G)T,P= nF(EC - EA)其中:EC 为氧化剂电位; EA为还原剂电位。
因此,⊿E越负,反应可能性越最大;有些情况下可利用氧化剂的平衡电极电位EC来粗略判断阴极去极化反应的可能性大小。
最常见的阴极去极化反应:析氢反应和吸氧反应12、何谓腐蚀极化图?说明其应用。
答案:一腐蚀电池,开路时,测得阴、阳极的电位分别为E0,C和E0,A。
然后用可变电阻把二电极连接起来,依次使电阻R值由大变小,电流则由零逐渐变大,相应地测出各电流强度下的电极电位,绘出阴、阳极电位与电流强度的关系图,就是腐蚀极化图。
因此,腐蚀极化图是一种电位—电流图,它是把表征腐蚀电池特征的阴、阳极极化曲线画在同一张图上构成的。
腐蚀极化图的应用(1)极化图用于分析腐蚀速度的影响因素(a)腐蚀速度与腐蚀电池初始电位差的关系:腐蚀电池的初始电位差(EO,C- EO,A ),是腐蚀的原动力;(例氧化性酸对铁的腐蚀;不同金属平衡电位对腐蚀电流的影响)(b)极化性能对腐蚀速度的影响:若腐蚀电池的欧姆电阻很小,则极化性能对腐蚀电流有很大的影响;(例钢在非氧化酸中的腐蚀极化图)(c)溶液中含氧且及络合剂对腐蚀速度的影响;(例铜在含氧酸及氰化物中腐蚀极化图)(d)其他影响腐蚀速度的因素,如阴、阳极面积比和溶液电阻等。
(2)腐蚀速度控制因素:阳极控制、阴极控制、混合控制和欧姆控制。
13、试用腐蚀极化图说明电化学腐蚀的几种控制因素以及控制程度的计算方法。
答案:×100%×100%14、混合电位理论的基本假说是什么?答案:混合电位理论包含两项基本假说:(1)任何电化学反应都能分成两个或两个以上的氧化分反应和还原分反应。
(2)电化学反应过程中不可能有净电荷积累。
根据混合电位理论,腐蚀电位是由同时发生的两个电极过程,即金属的氧化和腐蚀剂的还原过程共同决定的,是腐蚀体系的混合电位。
因此,根据腐蚀极化图很容易确定腐蚀电位并解释各种因素对腐蚀电位的影响。
而根据腐蚀电位的变化却不能准确判断腐蚀速度的大小或变化。
必须测定相应的极化曲线,根据腐蚀极化图或动力学方程式才能确定腐蚀速度,研究腐蚀动力学过程和机理。
15、何谓差异效应?产生负差异效应的原因是什么?(1)答案:差异效应现象和定义图中开关又断开的情况下,锌试样处于自腐蚀状态,锌上的析氢速度为V0。
然后接通开关,使锌试样与同溶液中的电位正的金属铂连通,锌上的析氢速度为V1,则(2)差异效应的腐蚀极化图解释(3)负差异效应,及其形成原因16、为什么说防腐就是防水?(可从极化与去极化角度解释)答案:在一般情况下,具备腐蚀电池条件后,腐蚀初始速度较大,但很快变慢,直至很小。
此现象称为极化现象。
但当环境有水存在时,会发生:氢去极化腐蚀:氢离子还原为氢气。
酸性介质中: 2H ++2e → H 2反应步骤如下: H + H 2 O → H + + H 2 OH + +M (e )→ MHMH +MH → H 2 +2M或 MH + H + +M (e )→ H 2 +2M碱性介质中:H 2O +M (OH -)→ OH -+M(H 2O )M(H 2O ) → M ( H )+ OH- M ( H )+ M ( H )→ H 2 +2M氢离子小,得电子后变相,使反应不断进行,去极化能力强。
氧去极化腐蚀氧分子在阴极上的还原反应(生成H 2O 、OH -)的电化学腐蚀称为氧去极化腐蚀。
由于氧分子的非离子化,氧分子在溶液中的溶解度较小(常压下最高浓度约为10-4mol/L ),所以,氧向金属表面的输送过程如下:①通过空气-溶液界面融入溶液,②以对流或扩散方式通过溶液的主要厚度层,③以扩散方式通过金属表面的溶液静止层而到达金属表面。
