现代物理方法在有机化学中的应用
现代物理方法在有机化学中的应用

由紫外光谱的λmax数值得到的信息:
①在200~400nm区间无吸收峰,可断定分子中无共轭 双键。
②在200~400nm区间有吸收峰,则可能有苯环、共轭 双键、碳氧双键等结构。
③在260~300nm区间内有强吸收峰,表示有3~5个共轭 双键,如果化合物有颜色,则含5个以上双键。
红外光谱的作用:确定化合物中官能团的存在,确定 两个化合物是否相同。
助色基:本身在紫外或可见光区不显吸收,当它们连 在双键或共轭体系上时,使吸收向长波方向位移,颜色 加深。如:—OH、—NH2、—Cl等。
红移现象:由于取代基或溶剂的影响使最大吸收峰向 长波方向移动的现象称为红移现象。 蓝移现象:由于取代基或溶剂的影响使最大吸收峰向 短波方向移动的现象称为蓝移现象。
电子的跃迁 :
σ*
E
π*
CO
n
π
σ
2 紫外光谱图的组成
横坐标表示吸收光的波长λ,纵坐标表示吸收强度。
丙酮的紫外光谱
光的吸收强度,可以用吸光度A、透射比或透光率T、 吸收率1-T、摩尔吸收系数κ中的任何一个来表示。 文献中的紫外光谱数据,是吸光度极大处的波长λmax和 它的摩尔吸收系数κ。
OH O HO
吗啡碱
NCH3
1 电磁波
电磁波是电磁场的一种运动形态,这种运动以光速C 在空间行进。具有波粒二象性。
波动性:可用波长λ、频率ν或波数σ来描述。
ν=
C λ
= Cσ
微粒性:可用光量子的能量来描述。
E = hν
普朗克常数h = 6.626×10-34 J·s。
波长不同的电磁波性质不同,根据电磁波的波长划分 为几个不同的区域。
溶剂的影响,π→π*跃迁,溶剂极性增加,吸收红移。 n→π*跃迁,溶剂极性增加,吸收蓝移。
一苏州大学 化学考研 提纲

一、原子结构与元素周期律共济网(1) 氢原子光谱33623 037(2) 核外电子运动状态的描述和四个量子数共济(3) 核外电子排布和元素周期律021-(4) 元素性质的周期性共济二、分子结构200092(1) 离子键和晶格能同济(2) 价键理论200092(3) 杂化轨道理论研(4) 价层电子对互斥理论3362 3039(5) 离域大p键理论济(6) 分子轨道理论同济(7) 分子间作用力48号三、晶体结构正门(1) 离子晶体类型和半径比规则336260 37(2) 离子极化作用48号四、酸碱平衡网络督察(1) 酸碱质子理论和酸碱电子理论(2) 水的电离和K w(3) 弱酸的电离和弱碱的电离(4) 两性物质的电离(5) 缓冲溶液五、沉淀平衡(1) 溶度积原理和溶度积常数(2) 沉淀平衡的移动六、氧化还原反应(1) 氧化数(2) 氧化还原反应的配平(3) 原电池(4) 标准电极电势及其应用(5) 能斯特方程(6) 元素电势图和φ-pH图(7) 电解七、氢和希有气体八、卤素(1) 卤素单质(2) 卤化氢和氢卤酸(3) 多卤化物、卤素互化物和拟卤素(4) 卤素含氧酸九、氧族元素(1) 氧族元素单质(2) 过氧化氢和过氧化物(3) 硫和硒及其化合物十、氮族元素(1) 氮及其化合物(2) 磷及其化合物(3) 砷、锑和铋及其化合物十一、碳族元素(1) 碳及其化合物(2) 硅及其化合物(3) 锡和铅及其化合物十二、硼族元素(1) 硼及其化合物(2) 铝及其化合物(3) 镓、铟和铊简介十三、碱金属和碱土金属(1) 碱金属化合物(2) 碱土金属化合物十四、配位化合物(1) 配位化合物概念、组成和命名(2) 配合物价键理论和晶体场理论(3) 配合物异构现象(4) 配位平衡十五、铜和锌族元素(1) 铜族元素及其化合物(2) 锌族元素及其化合物十六、过渡金属(1) 第一过渡金属及其化合物(2) 第二过和第三过渡金属简介《物理化学》部分的内容范围第一章气体理想气体状态方程,van der Waals方程,virial方程,对比状态和对比状态原理第二章热力学第一定律1 基本概念:系统与环境,系统的性质,热力学平衡态,状态函数,状态方程,过程和途径,热和功2 热力学第0定律3 热力学第一定律与内能4 准静态过程与可逆过程5 焓,等压热容,等容热容6 热力学第一定律对理想气体的应用理想气体的热力学能和焓,理想气体的Cp与Cv之差,绝热过程和过程方程,卡诺循环7 焦耳-汤姆逊效应,实际气体的△H和△U8 热化学等压热效应与等容热效应,反应进度,标准摩尔焓变,Hess定律,标准摩尔生成焓,标准摩尔离子生成焓,标准摩尔燃烧焓,反应焓变与温度的关系,绝热反应-非等温反应,热容-能量均分原理第三章热力学第二定律1 自发变化,不可逆性2 热力学第二定律3卡诺定理4 熵的定义5 克劳修斯不等式与熵增加原理6 熵变的计算7 热力学第二定律的本质和熵的统计意义,玻兹曼公式8 亥姆霍兹自由能和吉布斯自由能, 亥姆霍兹自由能和吉布斯自由能判据9 DG的计算10 热力学函数间的关系基本公式,特性函数,麦克斯韦关系式及应用,吉布斯-亥姆霍兹方程式,吉布斯自由能与温度、压力的关系112 热力学第三定律与规定熵第四章溶液1 溶液组成的表示法2 偏摩尔量,定义,加合公式,吉布斯-杜亥姆公式3 化学势定义,在相平衡中的应用,化学势与温度、压力的关系4 气体混合物中各组分的化学势, 逸度,逸度因子5 拉乌尔定律,亨利定律6 理想液态混合物,理想液态混合物中任一组分的化学势,理想液态混合物的通性,7 理想稀溶液中任一组分的化学势8 稀溶液的依数性蒸气压下降,凝固点降低,沸点升高,渗透压9 活度和活度因子10 分配定律-溶质在两互不相溶液相中的分配第五章相平衡1 多相体系平衡的一般条件2 相律, 相,组分数,自由度,相律3 单组分体系的相平衡单组分体系的两相平衡,克拉贝龙方程式,克拉贝龙-克劳修斯方程,外压与蒸气压的关系,水的相图,超临界状态4 二组分体系的相图及其应用理想的完全互溶双液系,杠杆规则,蒸馏、精馏的基本原理,非理想的完全互溶双液系,部分互溶的双液系,不互溶的双液系,简单的低共熔二元相图,形成化合物的体系,液固相都完全互溶的相图,固态部分互溶的相图第六章化学平衡1 化学反应的平衡条件与反应进度的关系2 化学反应的平衡常数和等温方程式, 气相反应的平衡常数, 溶液中反应的平衡常数3 平衡常数表示式4 复相化学平衡5 标准生成吉布斯自由能标准状态下反应的吉布斯自由能变化值,标准摩尔生成吉布斯自由能6 温度、压力及惰性气体对化学平衡的影响7 同时化学平衡8 反应的耦合第七章统计热力学基础1 统计系统的分类,统计热力学的基本假定2 玻兹曼分布,定位系统的最概然分布,非定位系统的最概然分布,3 配分函数, 配分函数与热力学函数的关系,配分函数的分离4.各配分函数求法及其对热力学函数的贡献原子核配分函数,电子配分函数,平动配分函数,单原子理想气体的热力学函数,转动配分函数,振动配分函数, 分子的全配分函数第八章电解质溶液1 法拉第定律2 离子电迁移率和迁移数3 电解质溶液的电导, 摩尔电导率,浓度对摩尔电导率的影响,离子独立移动定律,离子淌度,电导的应用4.离子强度,电解质的平均活度和平均活度系数第九章可逆电池的电动势及其应用1 可逆电池,可逆电极,电极反应,电动势的测定,电池的书写方法2 可逆电池的热力学,Nernst 方程,标准电动势求电池反应的平衡常数3 界面电势,接触电势,液体接界电势4 标准电极电势, 标准氢电极,参比电极,电池电动势的计算5 电动势测定的应用电解质的平均活度因子,难溶盐的活度积,溶液PH值的测定,电势—pH图及应用第十章电解与极化1 分解电压2 极化作用浓差极化,电化学极化,极化曲线,氢超电势,塔菲尔公式3 电解时电极上的竞争反应金属的析出与氢的超电势,金属离子的分离,电解过程的应用第十一章化学动力学基础(一)1 基本概念反应速率及其表示法,基元反应,反应级数与反应分子数,反应机理,质量作用定律,反应速率常数2 具有简单级数的反应一级反应,二级反应,三级反应,n级反应,反应级数的测定方法3 几种典型的复杂反应对峙反应,平行反应,连续反应,链反应4 温度对反应速率的影响阿累尼乌斯经验式,反应速率与温度关系的几种类型,活化能5 链反应, 稳态近似,链反应历程第十二章化学动力学基础(二)1 速率理论,基本假设,基本观点,活化能,表观活化能,概率因子2 过渡态理论基本观点,势能面,活化络合物3 光化学反应,初级过程和次级过程,光化学基本定律,量子产率,光化学反应动力学4 催化反应动力学,基本概念,基本特征,酶催化反应,自催化反应第十三章表面物理化学1 表面张力及表面Gibbs自由能,表面张力与溶液浓度的关系2 弯曲表面下的附加压力和蒸汽压,Young-Laplace公式,Kelvin公式3 溶液的表面吸附——Gibbs吸附公式4 液-液界面的铺展,单分子表面膜5 液固界面, 粘湿过程,浸湿过程,铺展过程,接触角与润湿方程6 固体的表面吸附, Langmuir吸附理论,BET吸附公式,7 气-固表面催化反应速率第十四章胶体分散体系和大分子溶液1 胶体及其基本特征2 溶胶的动力性质, 布朗运动,扩散和渗透压4 溶胶的光学性质,丁铎尔现象5 溶胶的电学性质, 电动现象,电泳、电渗6 大分子溶液,大分子化合物的平均分子量,唐南平衡《结构化学》部分的内容范围一、量子力学基础和原子结构(1)量子力学基本原理:波粒二象性、海森堡测不准原理、波函数、力学量的算符、薛定谔方程、态叠加原理等。
第八章 现代物理实验方法在有机化学中的应用练习及答案

第八章现代物理实验方法在有机化学中的应用1.指出下列化合物能量最低的电子跃迁的类型。
答案:⑴. π-π* ⑵.n-σ*⑶.n-π* ⑷. n-σ* ⑸. п-п*2.按紫外吸收波长长短的顺序,排列下列各组化合物。
⑴.⑵.CH3-CH=CH-CH=CH2 CH2=CH-CH=CH2 CH2=CH2(3).CH3I CH3Br CH3Cl⑷.⑸. 反-1,2-二苯乙烯顺-1,2-二苯乙烯答案:⑴以环己酮为基准,添加共轭双键及增加助色基都使UV吸收产生红移。
⑵以乙烯为基准,添加共轭双键及增加助色基都使UV吸收产生红移。
CH3-CH=CH-CH=CH2>CH2=CH-CH=CH2>CH2=CH2⑶杂原子的原子半径增大,化合物的电离能降低,吸收带波长红移。
n ® s*CH3I>CH3Br>CH3Cl⑷以苯环为基准,硝基苯增加p-p共轭,氯苯增加p-p共轭,UV吸收红移。
⑸反式异构体的共轭程度比顺式异构体更大。
反-1,2-二苯乙烯>顺-1,2-二苯乙烯3.指出哪些化合物可在近紫外区产生吸收带.(1) (2)CH3CH2OCH(CH3)2(3) CH3CH2C≡CH(4) (5) CH2=C=O (6).CH2=CH-CH=CH-CH3答案:可在近紫外区产生吸收带的化合物是⑷,⑸,⑹。
4、图8-32和图8-33分别是乙酸乙酯和1-己烯的红外光谱图,试识别各图的主要吸收峰:答案:图8-32己酸乙酯的IR图的主要吸收峰是:①.2870-2960cm-1为-CH3,>CH2的V C-H碳氢键伸缩振动。
②.1730cm-1为V C=O羰基伸缩振动。
③.1380cm-1是-CH3的C-H弯曲振动。
④.1025cm-1,1050CM-1为V C-O-C 伸缩振动。
图8-33,1-己烯的IR图主要吸收峰是①.=C-H伸缩振动。
②.-CH3,>CH2中C-H伸缩振动。
③.伸缩振动,④.C-H不对称弯曲振动。
Quantum Mechanics in Organic Chemistry

Quantum Mechanics in Organic Chemistry 量子力学在有机化学中的应用量子力学是现代物理学中的基础理论之一,它不仅对物理学有着深刻的影响,而且在化学领域中也有着广泛应用。
有机化学是研究有机物质构成、属性和反应的学科,而有机化学家们广泛应用量子力学的理论和方法来研究有机化学中的各种问题。
在本文中,我们将重点介绍量子力学在有机化学中的应用。
1. 分子结构和性质的计算量子力学可以用来计算分子结构和性质,包括分子的几何结构、电荷分布和电子结合能等。
有机化学家们用量子力学计算方法来研究各种分子结构和性质,这些计算可以帮助我们了解分子中化学键的形成、化学反应中的能量变化以及分子的光谱性质等。
2. 化学键的理论在有机化学中,物质的结构和性质与元素之间的化学键密切相关。
化学键是指原子之间相互结合的强力,量子力学可以精确地计算和预测化学键的性质。
因此,有机化学家们可以使用一些量子化学方法来研究化学键的理论和性质。
例如,Mulliken键级理论和价键理论等。
3. 反应机理的研究有机化学反应机理的研究是有机化学家的一个重要研究领域。
量子力学可以帮助有机化学家们理解有机反应中的分子间相互作用和转移过程。
通过计算反应势能面和反应的动力学参数,有机化学家们可以预测反应速率常数和选择性,这对于合理设计和优化化学合成路线至关重要。
4. 光学性质的计算有机化合物的光学性质是研究它们光谱性质的重要因素。
有机化合物的电子能级结构对光学性质有着极其重要的影响。
量子力学可以精确地计算分子中每个电子的能量、振动模式和光谱特性等。
因此,使用量子化学方法计算有机化合物的光学性质是有机化学家们的一个重要研究领域。
5. 学术界和工业界中的应用量子力学在理论和实践中都有着广泛的应用。
在学术界,有机化学家们研究有机化学中的各种问题,探索新的反应、材料和设计新的化学反应路线。
在工业界,有机化学家们可以利用量子力学的理论,快速而准确地预测化学反应过程,在工业应用中得到广泛的应用。
08 w现代物理实验方法在有机化学中的 应用

吗啡碱结构的测定,从1805年开始研究,直至1952 年才完全阐明,历时147年。
OH O HO
吗啡碱
NCH3
三、电磁波的一般概念
1. 频率与波长 电磁波:速率相同3×1010cm/s 波长与频率的关系为: γ = c /λ 频率(γ ,HZ),波长(λ ,cm) 1 cm=10 mm,1mm=103μm,1μm =103 nm λ=300nm的光,频率?(1HZ=1S-1)
分 物理方法
析
现代物理方法:主要指吸收电磁波谱
一.常见有机波谱
常 见 有 机 波 谱
电磁波谱与有机光谱的对应关系 波长不同的电磁波性质不同,根据电磁波的波长划分为 几个不同的区域。
电磁波谱
二、有机四大谱及其特点
有机四大谱:紫外吸收光谱(UR)、红外吸收光谱(IR)、 核磁共振谱(NMR)、质谱(MR)
CH 2800-300cm-1
一般的紫外光谱仪:测定近紫外和可见光区域
一、紫外光谱的产生
有机物分子吸收紫外光,核外价电子发生能级跃迁,从 而产生紫外吸收光谱。 价电子跃迁常伴有分子转动和振动能级的跃迁
二、电子跃迁
价电子有三种类型: σ 电子、 π 电子、n电子(孤对电子)
C=O: n σ
Hπ
σ*
跃迁类型:
π*
σ
σ *,π *
E
n—>σ*跃迁
等杂原子上的n电子,发生n—σ*跃迁需要的能量比σ— >σ* 跃迁小,有的也在远紫外区有吸收。
n—π*跃迁 、
C≡N:等杂原子形成重键,其上的n电子吸收能量发生n— >π*跃迁,其能量较低,发生在近紫外区。
π—>π*跃迁。 C=C,C=O、C=C-C=C、C=C-C=C-C=O等π 电子吸收能
现代分析技术及其在化学分析中的应用

现代分析技术及其在化学分析中的应用在当今信息化时代,数据分析技术已经越来越成为人类活动的重要组成部分。
在众多领域中,化学分析是其中一个非常重要的方面。
化学分析是指通过识别物质的化学和物理特性来确定其成分和结构的方法。
在化学分析中,现代分析技术发挥着越来越重要的作用。
本文将探讨现代分析技术及其在化学分析中的应用。
一、光谱分析光谱分析是一种基于物质吸收或发射特定波长的光的技术。
这个技术广泛应用于化学、物理、生物、地质等领域。
在化学中,光谱分析被用来确定物质的分子结构,通过测量不同波长的光线吸收光线的程度来确定物质的成分。
常用的光谱分析技术有红外光谱、紫外-可见光谱、拉曼光谱等。
例如,红外光谱被广泛应用于药品、化妆品等行业,从而保证这些产品符合质量标准。
二、质谱分析质谱分析是一种通过对化合物中分子的不同离子来确定物质成分的技术。
它采用质谱仪将物质分离成分子或原子的荷电离子并分离,然后以质量-电荷比的方式进行分析。
质谱分析在药品、农药、击剂、食品等行业都有重要的应用。
例如,它可以用来检测水中的污染物或某种特定药物残留。
三、薄层色谱法薄层色谱法可以使用非常小的样品量来分离化学物质,并使用标准化工具和技术来识别这些物质。
这种技术可以用于食品安全、环境污染、制药等方面。
例如,在药品制造中,薄层色谱法可以确定不同的药物成分,从而确保制造了正确的药物量。
四、原子吸收光谱原子吸收光谱分析是一种用于测量物质中元素含量的技术。
原子吸收光谱法通过让光通过含有特定元素的物质,并测量该元素吸收光的程度来确定其含量。
这种技术广泛应用于石油、有机化合物等领域。
例如,它可以在石油勘探中确定地下沉积物中的金属含量。
五、液相色谱法液相色谱技术是一种分离化学混合物的方法,广泛应用于制药、环保、农业等行业。
液相色谱法可以将混合物分解成其组成部分并进行检测。
例如,在农业上,它可以在无需将大量实验室样本带回实验室,并且可以马上得到结果的情况下确定营养成分和其他分析数据。
有机化学现代物理实验方法的应用

当分子吸收一个具有一定能量的光子时,分子就由较低的能级E1 跃迁到较高的能级E2,被吸收光子的能量必须与分子跃迁前后的能 级差恰好相等,否则不能被吸收,它们是量子化的。
Δ E分子= E2- E1 = E光子 = hν
上述分子中这三种能级,以转动能级差最小(约在0、05-10-4 ev)分子的振动能差约在1-0、05ev之间,分子外层电子跃迁的能 级差约为20-1ev。
⑴转动光谱 在转动光谱中,分子所吸收的光能只引起分子转动能级的变
化,即使分子从较低的转动能级激发到较高的转动能级。 转动光谱是由彼此分开的谱线所组成的。 由于分子转动能级之间的能量差很小,所以转动光谱位于电
磁波谱中长波部分,即在远红外线及微波区域内。 根据简单分子的转动光谱可以测定,键长和键角。
⑵振动光谱 在振动光谱中分子所吸收的光能引起振动能级的变化。分子
中振动能级之间能量要比同一振动能级中转动能级之间能量差 大100倍左右。振动能级的变化常常伴随转动能级的变化,所 以,振动光谱是由一些谱带组成的,它们大多在红外区域内, 因此,叫红外光谱。
⑶电子光谱
在电子光谱中分子所吸收的光能使电子激发到较高的电子 能级,使电子能级发生变化所需的能量约为使振动能级发生 变化所需能量的10-100倍。
H3C CH2 CH2+ + H2C CH2 m/e43
R'2C
C
CH2 R
CH R'
OH +
C
H2C
R
H+
H2C
H2C
H2C
H2C
C
CH2 H
《有机化学》三基要求

《有机化学》三基要求课程编码:190142107,190142108课程性质:学科专业必修课程教学对象:化学专业本科学生学时学分:136学时 8学分编写单位:化学系编写人:董玉环审定人:刘立华编写时间:2006年11月前言有机化学是化学专业本科生一门重要的基础理论必修课程,课程教学的目的是使学生系统地掌握有机化学的基本理论和有机化合物的结构、性质、制备、应用、反应历程等基础知识,初步具备能运用有机化学知识的从业能力,提升其分析问题、解决问题的综合能力。
学生不仅了解化学变化的普遍规律,而且对化学变化的规律性,能从理论上有更深刻、更本质的认识。
培养学生树立科学的自然观,掌握正确的方法论,使学生了解有机化学的一般研究方法。
课程教学的基本要求,掌握各章节的基础知识、基本理论、基本技能,掌握物质的基本理化性质、变化规律,明确其特点,掌握适用范围及应用的技巧。
第一章绪论基础知识:1、有机化学和有机化合物的涵义。
2、有机化学的产生和发展。
3、有机化合物的特性。
4、研究有机化合物的一般方法。
5、有机化合物的分类和官能团。
基本理论:1、共价键理论(价键理论和分子轨道理论)。
2、共价键的键参数。
3、共价键的断裂与有机反应类型。
4、有机化合物中的电子效应—诱导效应。
基本技能:1、了解有机化学的涵义,有机化学的发展史。
2、了解有机化学的研究的对象及其在现代化建设中的重要作用。
3、用共价键理论的要点及共价键的键长、键角、键能、元素的电负性和键的极性等知识,解决有机化学中的一些实际问题。
4、了解有机化合物的特性。
5、根据共价键的不同断裂方式对有机反应进行分类。
6、掌握有机化合物中的电子效应—诱导效应,并能应用在有机化学理论和有机化合物的性质上。
7、根据不同的分类方法对有机化合物进行分类。
第二章烷烃基础知识:1、烃的通式、同系列、同系物、同系差。
2、伯、仲、叔、季碳原子,伯、仲、叔氢原子。
3、烷烃的同分异构现象。
4、烷烃的命名(普通命名和系统命名法)。
有机化学第五版第八章课后答案(李景宁编)

第八章现代物理实验方法在有机化学中的应用& 析(2> CH S—CH—CH—CH=CH2 > CH】YHYHYH* > CH T—€H a(3) CH3I > CH3Br > CH3C1NO2(5)反-1,2-二苯乙烯>顺一1,2-二苯乙烯3-解:可在近紫外区产生吸收带的是(4八(5)、(6)。
4.解:乙酸乙酯=2980^2850 cm^1为甲基、亚甲基C-H伸缩振动产生的吸收峰:1 742 cm—L为C=O伸缩振动产生的吸收峰匕1 374 cm"1为甲基C」H弯曲振动产生的吸收Mh]240 cm^和1047 cnT】为C—O- C伸缩振动产生的吸收峰。
1—己烯【3070 cm"1为=C—H伸缩振动产生的吸收峰*2960-2866 cm"1为甲基、亚甲基C—H伸缩振动产生的吸收峰*1S41 cmT为碳碳双键伸缩振动产生的吸收峰鼻1460 cm-1和1370 cm"】为C—H弯曲振动产生的吸收峰;910 cm-1为RCH—CH3式烯绘C-H面外弯曲振动产生的吸收峰,乩(1)舸者c—C和C—Q的伸箔振动峰与后者的C—C和-一OH的伸缩振动峰有很大憧别I (2)=C-H面外弯曲振动中,反式和孤式产生的峰有但别丿<3)前者具有共無结构,C—O伸缩振动吸收峰较启者的波数低'<4)积累二烯烽申C—C—C伸端抿动吸收峰与孤立二烯烂的C = C伸縮振动吸收蜂宥饨别,C5)前妾的C—C—C [申缩振动与后者的E—C—N的伸缩振动产生的吸收峰有区别.6.糠t不堰和度U=8+l-0.5Xe = 6>4t可能有苯环.3300 和2110沁一1的吸收峰说明有Y—H t3 0S0 cm-] J 600 cm'1J 5()0 cm^1吸收峰说明有笨环?75€ cm'1和&91 m 1 吸收峰说明苯环上是单履代.再结合题中所已知的化学性质’可推得该化合物E的结构足:C^CHH S C\ b/H11.解:(1) CHjCHzCH^CH,&V&(2) c —cH /b ^CHja入>5.abba(3) CH S CH,OCH 2CH 5&A&a b b a (4) QH 5CH ?CH ,CH , a b ・c d&>&>&>&(5) CUCHCHzCl九〉A a b(6) CICH,CH 2CH,Br a b c(7) CHsCHO仇>&(8) C HjCOOCH^CH,矗>&>&12.解「在室温下,环己烷的两种构象转换很快,6个4键质子和6个€键质子处于平均的环境中, 所以其:H NMR 中质子只有一个峰;当温度降至一100弋时,环己烷两种构象转换速度很慢,所 以在】H NMR 谱图中,a 键质于和e 键质子各有一个单峰,即西个峰.13.解'不饱和度U=9+l-0・5X12 = 4.说明可能冇苯!H NMR 谱中古约为 7.0 的信号以及 IR 谱 3030 cm"1 J602 cnT' J 500 cm^1 J 462 cm'】 这些吸收谱带都说明有■苯环存在.根据不饱和度,除苯环外,分子中剩余的部分只能是烷基. 由】H NMR 谱可推得•可能得烷基为一CH :和-CH 2CH S e 再由IR 谱知,780 cnT*和680 cm"1 处有较强的吸收•这是间二取代苯的特征谱带.因此该化合物的结构为,8.解$ (1)两个$(2)四个M3)四个;(4)两个$(5》四个)(6)—个$(7)三个.(8〉五个。
补充现代物理分析方法_有机化学及实验

第七章 现代物理分析方法前面已经提到, 确定一个化合物的结构, 可以用化学方法, 例如测定有无某些官能团; 降解成简单化合物; 转变成衍生物; 用一个明确无疑的路线加以合成等来实现。
用化学方法测定有机化合物结构是一项非常繁复、费时, 有时甚至是很难完成的工作, 例如: 胆固醇结构的确定花了三、四十年, 这项工作在当时被认为一项非常杰出的工作。
但后来发现, 确定的结构式还是错的, 这是因为在用化学方法测定结构式的过程中, 往往发生结构重排或某些出乎意料的反应,容易得到错误的结论。
近三、四十年来,物理学与化学的结合,产生了一些现代物理测试方法,这些方法已经基本上取代了化学分析方法。
运用这些方法, 可以用微量样品(几微克),在较短时间内, 正确地测定有机化合物的结构。
有机化合物结构的常规测定有IR 、UV 、NMR 、MS 。
7.1紫外光谱7.1.1 紫外—可见光谱的形成原理7.1.1.1 电子跃迁与紫外—可见光谱的形成紫外光谱测定有机化合物中双键结构的一种重要方法,分子吸收能量后,电子能从成键轨道跃迁到反键轨道,从不同成键轨道(ζ,π,n)跃迁到反键轨道时,分子吸收的光能不同,n *及共轭烯的*吸收的能量在200nm 以上,落在近紫外区(200-400nm 为近紫外区),其它形式的跃迁都在200nm 以下。
7.1.1.2 紫外—可见光谱测定中的定量关系:Lambert —Beer 定律化合物吸收能量过程中遵循下列关系(比耳一朗的特定律)。
A 为吸光度,I 0入射光强度,I 为透射光强度。
ε为摩尔消光系数,b 为光线通过的溶液厚度(dm),C 为浓度(mol/L)。
溶液对吸收有影响,因此,文献在报道紫外光谱数据时都应标明溶剂。
一个特定化合物在指定溶剂中,吸收的波长和消光系数是相同的。
7.1.1.3 紫外—可见光谱图紫外光谱图采用波长λ为横坐标,A 为纵坐标,在不同波长下,化合物的吸光度构成一条连续曲线A10.5200 250 300 λ/ nm能够吸收可见光或近紫外光(200-800nm)的孤立官能团叫发色团,一般为:CCCNONNC有些官能团在200nm 以上没有吸收带,但是,它们与发色团连接在一起时使吸收带向长波方向移动(能量降低),并使吸收的程度增加,这种官能团叫助色团,通常有—OH ,—NH 2,bc II A ε==0lg—X等。
研究有机化学的一般方法
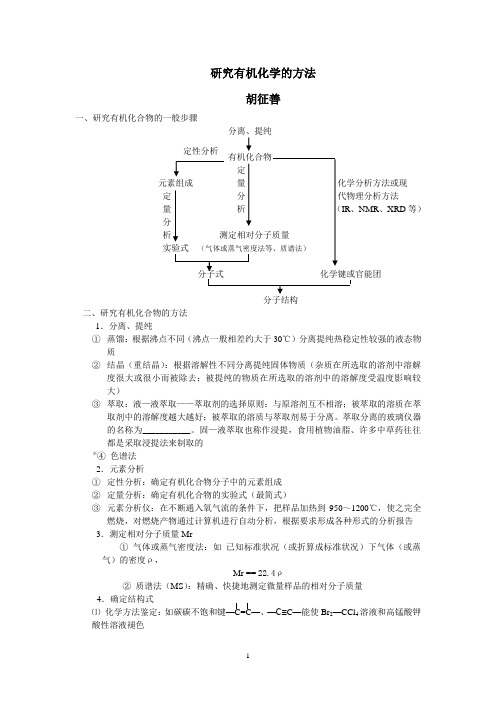
研究有机化学的方法胡征善一、研究有机化合物的一般步骤 分离、提纯定 元素组成 量定 分量 析 IR 、NMR 、XRD 等)分 析分子结构二、研究有机化合物的方法1.分离、提纯① 蒸馏:根据沸点不同(沸点一般相差约大于30℃)分离提纯热稳定性较强的液态物质② 结晶(重结晶):根据溶解性不同分离提纯固体物质(杂质在所选取的溶剂中溶解度很大或很小而被除去;被提纯的物质在所选取的溶剂中的溶解度受温度影响较大)③ 萃取:液—液萃取——萃取剂的选择原则:与原溶剂互不相溶;被萃取的溶质在萃取剂中的溶解度越大越好;被萃取的溶质与萃取剂易于分离。
萃取分离的玻璃仪器的名称为___________。
固—液萃取也称作浸提,食用植物油脂、许多中草药往往都是采取浸提法来制取的※④ 色谱法2.元素分析① 定性分析:确定有机化合物分子中的元素组成② 定量分析:确定有机化合物的实验式(最简式)③ 元素分析仪:在不断通入氧气流的条件下,把样品加热到950~1200℃,使之完全燃烧,对燃烧产物通过计算机进行自动分析,根据要求形成各种形式的分析报告3.测定相对分子质量Mr① 气体或蒸气密度法:如 已知标准状况(或折算成标准状况)下气体(或蒸气)的密度ρ,Mr == 22.4ρ② 质谱法(MS ):精确、快捷地测定微量样品的相对分子质量4.确定结构式⑴ 化学方法鉴定:如碳碳不饱和键—C=C —、—C≡C —能使Br 2—CCl 4溶液和高锰酸钾酸性溶液褪色⑵现代物理方法(波谱分析)——具有微量、快速、高效、精确等特点①红外光谱(IR):确定分子中的各种化学键和官能团②核磁共振氢谱(1H—NMR):确定分子中不同化学环境氢原子的种数及其数目之比※③X射线衍射(XRD):分析和确定固体有机分子特别是复杂的生物大分子的结构(键长、键角、三维结构等的测定)※④紫外光谱(UV):确定有机分子中有无共轭双键(即单双键交替出现)三、小结1、了解有机化合物的分类方法(按碳骨架分类和按官能团分类);能知道有机化合物中常见官能团的名称与结构2、明确碳原子及其有机化合物的结构特点,知道表示有机化合物组成与结构的各种式子;明确有机化合物中普遍存在的同分异构现象(本节需要知道的同分异构体有碳链异构、位置异构和官能团异构),掌握一些简单有机化合物同分异构体的确定与书写3、知道烃基的概念,掌握几种重要的烃基;掌握烷烃、烯烃、苯及其同系物等几类有机化合物尤其是烷烃的命名原则,在系统命名法中要求“一式一名”,“名”“式”相符4、知道研究有机化合物的一般步骤;掌握几种常见分离提纯有机化合物的方法;初步了解现代物理分析(波谱分析)方法,了解各种波谱信号在分析研究有机化合物中的作用典例分析【例1】烷烃分子可看成由—CH3、—CH2—、—CH、——等结构构成。
现代物理有机化学

现代物理有机化学物理有机化学是一门研究物质的结构、性质及其反应动力学的科学。
它理解和解释了物质的结构、性质及其反应的形式和机制。
物理有机化学是由有机化学和物理化学相结合形成的一门新的科学,它为化学家和其他学者提供了新的视角来研究有机物质。
物理有机化学在有机化学实验室中发挥着重要作用。
一般来说,它涉及对有机分子及其复杂结构进行研究,例如研究分子的构态和活动,以及它们之间的相互作用。
物理有机化学可以为有机化学实验提供理论基础和技术支持,它可以帮助分析有机反应的机制和评估反应结果,以及更好地了解活性中心的运作原理。
此外,物理有机化学在有机材料的制备和表征中也发挥着重要作用。
现代物理有机化学科学研究的基础是经典物理有机化学知识,例如化学力学、内键化学、极性化学和共价化学。
在现代物理有机化学中,量子化学是关键,因为它可以帮助化学家们更好地理解和更准确地描述有机反应的机理和结果。
有机物的结构及其反应将结合量子化学的概念,充分利用它的模拟和计算技术,帮助人们认识到未知的有机物质或反应,以及研究有机反应条件及其影响因素。
另一个重要方面是有机反应动力学,它是一门研究物质反应特性和反应动力学的科学。
有机反应动力学是有机反应机理研究中一个重要的方面,它可以研究各种有机反应的速率,分析和推测反应动力学参数,以及模拟和预测有机反应的轨迹。
在现代物理有机化学研究中,实验室实践也发挥着重要作用。
通过实验室实践,可以更加深入的研究有机物质的结构、化学反应机理、反应动力学参数等。
此外,实验室实践也可以验证理论假设,并为有机材料的开发提供有效的方法。
目前,现代物理有机化学在分子生物学、有机分析化学、无机生物化学以及量子材料等领域有着广泛的应用。
例如,在分子生物学中,物理有机化学可用于研究基因转录和蛋白质合成过程,特别是可以更好地理解和描述分子的活性中心。
在有机分析化学中,它可以帮助分析有机物质的结构和反应机理,探索有机物质的化学合成方法,从而推动有机化学实验的高效进行。
《现代物理有机化学》笔记第六章立体化学

《现代物理有机化学》笔记第六章立体化学一、教学内容本节课的教学内容选自《现代物理有机化学》笔记的第六章,主要讲述立体化学的相关知识。
本章内容主要包括立体化学的基本概念、立体异构体的类型、立体化学的测定方法以及立体化学在有机合成中的应用。
具体内容包括:1. 立体化学的基本概念:手性、手性碳、非手性碳、绝对构型、相对构型等。
2. 立体异构体的类型:顺反异构体、对映异构体、非对映异构体等。
3. 立体化学的测定方法:旋光法、圆二色法、核磁共振等。
4. 立体化学在有机合成中的应用:立体选择性反应、立体固定化催化剂等。
二、教学目标1. 使学生了解立体化学的基本概念,理解手性碳和非手性碳的区别,掌握绝对构型和相对构型的表示方法。
2. 使学生掌握立体异构体的类型,能识别顺反异构体、对映异构体和非对映异构体。
3. 使学生了解立体化学的测定方法,理解旋光法、圆二色法和核磁共振的原理及应用。
4. 使学生了解立体化学在有机合成中的应用,能运用立体化学的知识解释立体选择性反应和立体固定化催化剂的原理。
三、教学难点与重点1. 教学难点:立体异构体的类型及识别,立体化学的测定方法及应用。
2. 教学重点:立体化学的基本概念,绝对构型和相对构型的表示方法。
四、教具与学具准备1. 教具:黑板、粉笔、多媒体教学设备。
2. 学具:笔记本、彩笔、剪刀、胶水。
五、教学过程1. 实践情景引入:通过展示一些具有不同立体结构的有机分子,引导学生思考为什么有机分子会有不同的结构。
2. 讲解基本概念:讲解手性、手性碳、非手性碳、绝对构型、相对构型的定义及表示方法。
3. 分析立体异构体:分析顺反异构体、对映异构体和非对映异构体的特点,引导学生通过观察分子结构来识别不同类型的立体异构体。
4. 讲解测定方法:讲解旋光法、圆二色法和核磁共振的原理及应用,引导学生理解这些方法在立体化学研究中的重要性。
5. 应用实例解析:分析一些具有立体选择性反应的有机合成实例,讲解立体固定化催化剂的原理及应用。
现代物理有机化学

现代物理有机化学现代物理有机化学是一门对实际应用非常重要的学科,它结合了物理学和有机化学,为科学家们提供了一系列关于一些重要分子的研究方法。
它致力于研究分子的结构、性质和反应特性。
从原子分子的结构、气体的分子运动、求解量子力学方程的算法,到表面化学、光解反应等,现代物理有机化学涉及非常广泛的领域。
现代物理有机化学较其他专业更加综合,它包括:1)计算化学:通过数值计算解决化学问题;2)理论化学:通过推导出的方程系统来研究原子分子的性质;3)实验物理有机化学:对分子的构型和性质进行实验测量;4)发展新的有机合成方法:发展合成反应的机理和来源,构建新的催化剂,使合成可控化、效率更高等。
现代物理有机化学可以帮助科学家们了解分子的结构和性质,探索合成反应的机理,研究新型催化剂,掌握反应条件,并改进反应条件,从而满足合成反应的应用需求。
它被广泛用于生物技术、制药、材料、环境、农业等方面的开发,其中生物技术、制药和材料技术是现代物理有机化学最主要的应用领域。
生物技术方面,现代物理有机化学可以用来研究和分析小分子和大分子的结构,并通过研究和调控分子的结构来让基因表达更为有效;在制药方面,它可以帮助探索新药物结构,从而提高新药的安全性和药效;在材料方面,现代物理有机化学可以帮助我们通过改变分子的结构,制备出具有理想性能的材料,给人们的日常生活带来更多的便利。
此外,现代物理有机化学还可以用于研究新型能源和环境污染防治技术,帮助开发出更加可持续的能源和更有效的环境防护技术。
它在农业方面也有所作为,可以改进现有农药的副作用,并开发出新型农药,使其安全、高效。
总之,现代物理有机化学是一门贯穿物理学和有机化学的交叉学科,它在实验、理论、计算上都有着丰富的内涵,承担着重要的应用任务,亟需广大科学家们的传承和发展。
- 1 -。
Ch.8 现代物理实验方法

第八章现代物理实验方法在有机化学中的应用测定有机物的结构,是研究未知有机物和鉴定有机物的重要环节。
过去,测定有机物的结构,主要依靠化学方法,化学方法要消耗较多的样品,而且费时费力。
近几十年来,化学方法测定有机物结构已被现代物理方法取代,化学方法了退居辅助地位。
物理方法的优点是样品用量少、快速、准确。
目前广泛用于测定有机分子结构的物理方法是波谱法。
紫外-可见光谱UV-V i s红外光谱IR核磁共振谱NMR质谱MS第一节关于光光是电磁波,具有波动性和粒子性。
一、光的波动性ν与λ成反比关系。
二、光的粒子性表现在光具有能量。
一个光子的能量:E正比于ν反比于λ一摩尔光子的能量:三、电磁波的区域划分四、比耳-朗伯特定律A为吸光度,A的大小反映出样品(溶液)对特定波长的光的吸收程度。
E和ε不随溶液的厚度及浓度的变化而变化,但随单色光波长的不同而变化。
E和ε反映分子中某种价电子吸收某种波长的光发生跃迁的几率。
每一种化合物对特定波长的光的吸收,其E或ε值是特定的,所以消光系数是化合物的特征常数,是鉴定化合物的重要依据。
第二节UV-V i s光谱一、价电子原子中的价电子是填充在一定的原子轨道(s、p、d、f等)。
分子处于基态时,σ电子填充在成键的σ分子轨道中;π电子填充在成键的π分子轨道中;n 电子填充在原子轨道(s或P或SP3轨道)中。
如果用能量合适的光照射分子,分子中的价电子就会吸收光能,从成键的σ轨道或成键的π轨道或原子轨道跃迁到反键的σ*轨道或反键的π*轨道上。
分子中σ轨道、σ*轨道、π轨道、π*轨道、n 电子的轨道的能级相对高低如下图所示:有机分子中的价电子有6种可能的跃迁,这6种跃迁的能级差,其大小顺序为:一个有机分子究竟有可能发生哪几种跃迁,要看该分子含有些价电子,或者说,要看含有哪些分子轨道。
例如烷烃分子,其价电子只有σ电子,其分子轨道只有σ轨道和σ*轨道,所以,烷烃分子吸收能量合适的光,只能发生σ→σ*这种跃迁。
有机化学(organic chemistry)

有机化学(organic chemistry)教学大纲(适用于化学专业)说明有机化学课程是高等学校化学类各专业教学计划中一门必修的基础课程,它是为培养满足化工行业对工程技术人才的需要而设置的。
通过对本课程的学习,可以使学生对本大纲范围内的有机化学内容有比较系统和比较全面的了解,掌握有机化学的基本理论、基本知识和基本技能,了解本学科范围内重大的科学技术新成就,培养学生具有分析和解决有机化学一般问题的初步能力,为学习后续课程和培养造就高级化学化工技术人才打好一定基础。
本课程总学时为122学时,4学分。
学时具体分配如下:有机化学教学大纲一、课程教学目标有机化学课程是高等学校化学类各专业教学计划中一门必修的基础课程,它是为培养满足化工、制药、环保等行业对工程技术人才的需要而设置的。
通过对本课程的学习,可以使学生对本大纲范围内的有机化学内容有比较系统和比较全面的了解,掌握有机化学的基本理论、基本知识和基本技能,了解本学科范围内重大的科学技术新成就,培养学生具有分析和解决有机化学一般问题的初步能力,为学习后续课程和培养造就高级化学化工技术人才打好一定基础。
二、教学内容及基本要求第一章绪论教学目的1.掌握有机化合物和有机化学的一般概念;2.理解有机结构基本理论到现代化学键理论的发展、有机化合物的特点;3.了解研究有机化合物的一般步骤,掌握有机化合物的分类和官能团。
教学内容1.有机化学的产生和发展2.有机化合物的特性3.有机化合物中的共价键4.共价键的断裂方式5.有机化合物构造式的表示方法6.有机化学中的酸碱概念7.有机化合物的分类8.研究有机化合物的一般程序和方法第二章烷烃教学目的1.掌握系统命名法;2.掌握甲烷的四面体构型,能够用杂化轨道理论说明烷烃的结构和σ键的特点;3.掌握烷烃的卤代反应及其历程;4.理解卤代反应的相对活性与烷基自由基的稳定性。
教学内容1.烷烃的通式、同系列和同分异构现象;2.烷烃的命名;烷烃的分子结构;烷烃的物理性质;3.烷烃的化学性质。
第八章现代物理实验方法在有机化学中的应用

图8-11:一挥发性的无色液体,经元素分析结果C占91.4%,H 占8.7%,它的红外光谱如图所示,确定这个化合物的结构。
• ΔE = h h=planck常数 6.626*10—34J/S • ΔE是获得的能量
• 紫外光的波长较短(一般指100—200nm)。能量 较高,当它照射到分子上时,会引起分子中价电 子能级的跃迁。
• 红外光的波长较长(一般指2.5—25μm),能量稍 低,它只能引起分子中成键原子的振动和转动能 级跃迁。 • 核磁共振谱的能量更低(一般指60—250MHz,波 长约105cm)它产生的是原子核自旋能级的跃迁。
第四节
一、基本知识
1.氢的自旋量 子数(m s)
核磁共振谱
当ms= + 时,如果取其方向与外磁场方向平行,为 低能级(低能态)。 当ms=时,如果取其方向与外磁场方向相反,为高 能级(高能态)。
ΔE = r
H0
2. 核磁共振
若质子受到一定频率的电磁波辐射,辐射所提供 的能量恰好等于质子两种取向的能量差(ΔE)时, 质子就吸收电磁辐射的能量,从低能级跃迁到高能级 ,这种现象即称为核磁共振。
3. 产生吸收峰的条件 : 只有偶极矩大小或方向有一定改变的振动 才能吸收红外光而发生振动能级跃迁。
4.红外光谱与有机分子结构的关系: ①C—H 伸缩振动,在波数2850—3000cm—1间将出现 吸收峰。
②O—H 伸缩振动,在波数2500—3650cm—1间将出现 吸收峰。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8-10 二甲基环丙烷有三各异构体,分别给出 2,3 和 4 个核磁共振信号,试画出这三个异构 体的构型式。 8-11 按化学位移δ值的大小,将下列每个化合物的核磁共振信号排列成序列。
(5)
CH 2
C
O
(6)
CH 2
CH
CH
CH
CH3
8-4 图 8-1(见教材,下同)和图 8-2 分别是乙酸乙酯和 1-己烯的红外光谱(IR)图,试识 别各图的主要吸收峰。 8-5 指出如何应用红外光谱来区分下列各对异构体:
O (1) CH3 H (2) C6H5 O (3) CH3 和 H C C H CH CH C H C6H5 和 H C6H5 C C H O C6H5 和 CH3 C C CH2OH
(4)
C C6H5 C C6H5 CH3 CN
和 C6H5 和 C6H5
CH2
(5)
C
N CH CH2
8-6 化合物 E,分子式为 C8H6,可使 Br2-CCl4 溶液退色,用硝酸银氨溶液处理,有白色沉淀 生成,E 的红外光谱如图 8-3 所示,E 的结构是什么? 8-7 试解释下列现象: 乙醇以及乙二醇四氯化碳浓溶液的红外光谱在 3350cm-1 处都有一个宽 的 O-H 吸收带。当用四氯化碳解释这两种醇溶液时,乙二醇光谱的这个吸收带不变,而乙 醇光谱的这个带被在 3600cm-1 一个尖峰所代替。 8-8 下列每个化合物将有几个核磁共振信号?
(3) A 的 NMR 图在δ值2.2和δ值1.4处有共振信号,强度比为 3:1,A 的结构如何? (4) 在 A 的质谱中,发现基峰是 m/z 67,这个峰是由什么离子造成的?如何解释它 的丰度? 8-18 均三甲苯的 NMR 图δ值2.35(9Η)单峰:δ值6.70(3Η)单峰,在液态 SO2 中,用 HF 合 SbF5 处理均三甲苯,在 NMR 图上看到的都是单峰,δ值2.8(6Η) ,δ值2.9(3Η) ,δ值4.6 (2Η) ,δ值7.7(2Η) 。这个谱是由什么化合物产生的?标明它们的吸收峰。 8-19 1,2,3,4−四甲基−3,4−二氯环丁烯()的 NMR 图在δ值1.5和δ值2.6各有一个单峰,当把 ()溶解在 SbF5 和二氧化硫的混合物中时,溶液的 NMR 图开始呈现三个单峰,δ值2.05 (3Η) ,δ值2.20(3Η) ,δ值2.65(6Η) ,但几分钟以后,出现一个新的谱,只在δ值3.68处有 一单峰。 推测中间产物和最终产物的结构,并用反应式表示上述变化。 8-20 某化合物的分子式为 C7H8O,其 13C{1H}谱中各峰的δ值分别为140.8、128.2、127.2、 126.8和64.5,而这些峰在偏共振去偶谱中分别表现为单峰、二重峰、二重峰、二重峰和三重 峰。其1H NMR 谱有三个单峰,δ值分别为7.3(5Η) 、4.6(2Η)和2.4(1Η) 。试确定该化合 物的结构式。 8-21 一化合物的分子式为 C5H10O,其红外光谱在 1700cm-1 处有强吸收,1H NMR 谱在δ值 为9−10处无吸收峰。从质谱知,其基峰 m/z 为 57,但无 m/z 为 43 和 71 的峰,试确定该化 合物的结构式。 8-22 戊酮有三个异构体,A 的分子离子峰的 m/z 为 86,并在 m/z 为 71,43 处各有一个强 峰,但在 m/z 为 58 处没有峰;B 在 m/z 为 86、57 处各有一个强峰,但没有 m/z 为 43、71 处的强峰;C 有一个 m/z 为 58 处的强峰。试推出这三个戊酮的构造式。 8-23 一中性化合物 C7H13O2Br 的 IR 谱在 2850~2950cm-1 有一些吸收峰,但在 3000cm-1 以 上无吸收峰,另一强吸收峰在 1740 cm-1 处。1H NMR 谱在δ为1.0(三重峰,3Η) ,1.3(二重 峰,6Η) ,2.1(多重峰,2Η) ,4.2(三重峰,1Η)和4.6(多重峰,1Η)有信号,碳谱在δ 为168处有一个特殊的共振信号。试推测该化合物可能的结构,并给出各谱峰的归属。
CH 3 (1) CH3CH2CH2CH3 (2) H (3) (5) (7) CH 3CH 2OCH 2CH 3 Cl2CHCH 2Cl CH 3CHO (4) (6) (8) C C CH 3 H
C 6H 5CH 2CH 2CH 3 ClCH 2CH 2CH 2Br CH 3 C O O CH 2CH3
第八章
习题
现代物理实验方法在有机化学中的应用
8-1 指出下列化合物能量最低的电子跃迁的类型。
(1) (3) (5)
CH 3CH 2CH
CH 2
(2) (4)
CH 3CH 2CHCH 3 OH
CH 3CH 2CCH 3 O CH 2 CH CH O
CH 3CH 2OCH2CH 3
8-2 按紫外吸收波长长短的循序,排列下列各组化合物
8-12 在室温下,环己烷的核磁共振谱只有一个信号,但在-100℃时分裂成两个峰。试解释 环己烷在这两种不同温度下的 NMR 图。 8-13 化合物 A,分子式为 C9H12,图 8-4 和图 8-5 分别是它的核磁共振谱和红外光谱,写出 A 的结构。 8-14 推测具有下列分子式及核磁共振谱(见图 8-6)的化合物的构造式,并标出各助峰的相 对面积。 8-15 从以下数据推测化合物的结构。 试验式:C3H6O NMR:δ1.2(6Η)单峰,δ2.2(3Η)单峰,δ2.6(2Η)单峰,δ4.0(1Η)单峰; IR:在 1700cm-1 处有吸收带。 8-16 用 1molCH3CH2CH3 和 2mlCl2 进行自由基氯化反应时,生成氯化混合物,小心分馏得 到四种二氯丙烷 A、B、C、D。从这四种异构体的核磁共振谱的数据,推测 A、B、C、D 的结构。 化合物 A: (bp 69 ℃)δ值2.4(6Η)单峰; 化合物 B: (bp 88 ℃)δ值1.2(3Η)三单峰,1.9(2Η)多重峰,5.8(1Η)三重峰; 化合物 C: (bp 96 ℃)δ值1.4(3Η)二重峰,3.8(2Η)二重峰,4.3(1Η)多重峰; 化合物 D: (bp 120 ℃)δ值2.2(2Η)五重峰,3.7(4Η)三重峰。 8−17 化合物Α,分子式为 C5H8,催化氢化后,生成顺-1,2-二甲基环丙烷。 (1) 写出 A 的可能结构。 (2) 已知 A 在 890cm-1 处没有红外吸收,A 的可能结构又是什么?
(1) CH 3CH 2CH 2CH 3 (2) CH 3CH O (3) (5) CH 3CH CH 2 (4) 反-2-丁烯 CH 2
1,2-二溴丙烷 O
(6) CH 2BrCl
(7)
CH 3 C
OCH(CH 3)2
(8)
2-氯丁烷
8-9 写出具有下列分子式但仅有一个核磁共振信号的化合物结构式:
O O O
(1)
CH3
(2) (3)
CH2
CH CH
CH2
CH3
CH2
CH CH
CH2
CH2
CH2
CH3Cl
CH3I Cl
CH3Br NO2
(4)
(5) 顺 -1, 2-二苯乙烯和反 -1, 2-二苯乙烯
8-3 指出哪些化合物可在近紫外区产生吸收带:
(1) CH 3CH 2CHCH 3 CH 3 (3) CH 3CH 2C CH (4) O CH 3CCH 2CH 3 (2) CH 3CH 2OCH(CH 3)2
