木炭活性炭石墨的物理性质和用途物理性质
课题1 金刚石、石墨和C60教案

课题1 金刚石、石墨和C 60第1课时 碳的单质情景导入“碳氏三兄弟”一天碳氏家族的三个兄弟在表功,老大说:“我是天然矿物质中最硬的,我能破石开山”;老二说:“我是天然矿物质中最软的,我很滑,能导电,但我过后留有痕迹”;老三说:“我在当前社会上具有广泛应用高科技材料”。
合作探究探究点一 碳的单质提出问题 金刚石、石墨、C60都是有碳元素组成的单质,为什么它们的物理性质有很大的差异? 交流讨论 阅读教材归纳总结。
归纳总结1.碳的几种单质:金刚石 、石墨和C 60课堂讨论 (1)金刚石和石墨是同一种物质吗?由石墨制造金刚石是物理变化还是化学变化?(2)一种元素只能组成一种单质吗?这些碳单质的性质和用途为什么不同?知识拓展(1)一种元素可以组成不同种单质。
例如:金刚石、石墨和C60都是由碳元素组成的不同单质;白磷、红磷都是由磷元素组成的不同单质;氧气和臭氧都是由氧元素组成的不同单质;同种元素可以组成不同单质。
因此,我们不能说“由同种元素组成的物质叫单质”。
(2)石墨在一定条件下可以转化为金刚石,该变化属于化学变化。
探究点一无定形碳提出问题无定形碳是碳的单质吗?它是一种物质还是一类物质呢?交流讨论阅读教材归纳总结。
归纳总结木炭、焦炭、活性炭和炭黑主要是由石墨的微小晶体和少量杂质构成的。
因为它们没有固定的几何形状,所以叫无定形碳,⑴木炭具有吸附能性,可以吸附气体、色素,可用来作冰箱的去味剂。
(2)活性炭的吸附能力比木炭强,可以用在防毒面具中吸收毒气、制糖工业中脱色制白糖、处理水等。
(3)焦炭用于冶金工业,作还原剂。
(4)炭黑用于制造油墨、油漆、鞋油、橡胶工业的填充剂等。
知识拓展1.木炭、活性炭的吸附性是物理性质,木炭、活性炭的脱色吸附是物理变化。
2.“碳”和“炭”的区别:“碳”是元素的名称,是核电荷数为6的一类原子的总称。
比如碳元素、碳单质、含碳化合物、一氧化碳等。
而“炭”指的是具体物质,它表示由碳元素组成的某种单质——木炭、活性炭、焦炭、炭黑等。
人教版化学-九年级上册-第六单元 课题1 金刚石、石墨和C60

第六单元碳和碳的氧化物课题1 金刚石、石墨和C60教案【教学课型】新授◆课程目标导航:【教学课题】课题1 金刚石、石墨和C60【教学目标】1、知识与技能:(1)了解金刚石、石墨、木炭、活性炭的主要物理性质和用途。
(2)知道碳单质的化学性质。
(3)知道C60的分子结构及其发展前景。
2、过程与方法:(1)会对展示或演示的资料分析、归纳(2)培养学生实验设计的能力。
3、情感态度与价值观:(1)树立物质的性质决定用途的观点。
(2)以发展的观点看待碳的单质。
【教学重点】金刚石、石墨、木炭的物理性质和用途。
【教学难点】(1)金刚石和石墨物性差异很大的原因。
(2)碳跟某些氧化物的反应。
【教学准备】教师用具:玻璃片、玻璃刀、6B铅笔、干电池、石墨电极、投影仪、电视媒体、防毒面具、导线、灯泡。
学生用具:玻璃片、铅笔刀、铅笔一只、干电池、导线3根、小灯泡、蜡烛一根、火柴、活性炭、红墨水、烧杯、药匙、注射器(50mL)、棉花。
◆课前预习1.(1)观看教材图6-1金刚石的结构和用途,结合教材内容回答下列问题:①纯净的金刚石是色、形状的固体。
②金刚石的结构图中,若每一个小球代表一个碳原子,请你观察金刚石中每一个碳原子最多与个碳原子相连。
③图片上金刚石的用途分别是和。
其中,金刚石用在玻璃刀刀头上是利用了金刚石的性质。
(2).观察教材图6-2石墨的结构和用途,结合教材内容回答下列问题:①石墨是一种色的,状固体。
②石墨的结构图中,若每一个小球代表一个碳原子。
那么,石墨中每一个碳原子最多与碳原子相连,并且碳原子是排列的。
③说出图中石墨的用途分别是和。
其中做铅笔芯是利用了石墨很,且在纸上划过后会留有色痕迹的性质。
做电极是利用了石墨的性。
2.焦炭、活性炭、木炭和炭黑是碳单质吗?(1)由于它们主要是的微小晶体和少量构成的。
故它们是,而不是单质。
(2)在书写这四种物质的名称时,要写(填“碳”或“炭”)这一个字。
(3)在这四种物质中,和,具有的结构。
高中化学 活性炭和木炭的结构和用途

浅灰色多孔固体,质地坚硬
作燃料,作冶金工业还原剂
烟煤隔绝空气条件下加强热制得
无定形碳的物理性质、主要用途及制法
物理性质
用途
制法
木炭
灰黑色多孔固体
制黑火药。制活性炭,制炭笔,吸附色素
木材隔绝空气加强热
活性炭
黑色粉Байду номын сангаас或颗粒状固体
净化多种气体和液体,制作防毒面具,使溶液脱色
木炭在高温下用水蒸气处理
炭黑
黑色粉末状固体
制造油墨、油漆、鞋油、颜料、墨汁及橡胶制品的填料
含碳物质不完全燃烧
活性炭和木炭的结构和用途
定义:
木炭、活性炭、炭黑、焦炭是由石墨的微小晶体和少址杂质构成的,均属混合物。没有固定的几何外形,所以称为无定形碳。
木炭、活性炭的吸附作用:
木炭、活性炭因具有疏松多孔的结构,表面积很大,所以吸附能力很强,吸附时被吸附物(有色液体、有毒气体等)吸附在其表面(细孔管道内),这个过程是物理变化。木炭、活性炭的吸附性属于物理性质。活性炭是木炭经过水蒸气高温处理得到的,它具有很大的表面积,因此活性炭的吸附能力比木炭强。
碳单质的性质与用途

1.金刚石、石墨、活性炭、焦炭、炭黑、C60的性质与用途碳的单质有金刚石、石墨、木炭、焦炭、活性炭等等,从晶体形态考虑,碳有两种同素异形体——石墨和金刚石。
平常所说的无定形碳如木炭、活性炭、焦炭、炭黑等实际上也具有石墨的晶体结构,并不是真正的另一种晶体类型。
直到8O 年代中期,人类发现了富勒烯(Fullerene),科学家进一步研究确认富勒烯是碳元素存在的第三种晶体形态,至此人类对碳的认识提高了一个新层次。
美国科学家Curl和Smalley教授及英国科学家Kroto教授为此荣获1996年诺贝尔化学奖。
金刚石:金刚石为无色透明固体,硬度10莫氏,熔点3550℃,沸点4827℃,密度3.51g/cm3,是天然存在的最硬的物质。
在温室下对所有化学试剂都显惰性,在氧气中燃烧温度为777℃,燃烧热为395.40KJ/mol。
透明的金刚石可以作宝石或钻石。
黑色和不透明的金刚石在工业上用以制钻头和切割金属、玻璃或矿石的工具。
金刚石粉是优良的研磨材料,可以制砂轮[1]。
石墨:石墨为灰黑色不透明固体,硬度1莫氏,熔点3652℃,沸点4827℃,密度2.2g/cm3,是电和热的良导体。
化学性质比金刚石稍活泼,在氧气中燃烧温度687℃,燃烧热为393.50KJ/mol。
石墨能被强氧化剂如浓HNO、NaCIO4和KMnO4等氧化为石墨氧化物。
石墨在工业上被大量地用于制造电极、坩埚、某些化工设备及高温热电偶,也可以作原子反应堆中的中子减速剂。
石墨粉可以作润滑剂、颜料和铅笔芯。
石墨能与许多金属生成碳化物,如青铜色的C8K[1]。
无定形碳:无定形碳大都为黑色不透明固体,物理性质各不相同。
化学性质比金刚石和石墨都稍活泼。
在高温下,除与O2及金属氧化物反应外,还与硫反应。
与某些金属反应,可得到碳化物。
(1)木炭一般是由木材、纤维在隔绝空气的条件下加热制得,主要用于冶金、吸附剂、黑色火药原料。
(2)焦炭若是由煤干馏得到的,其成分和机械性能不一;若是由沥青或天然气的蒸馏残渣碳化得到的产物成分一致。
碳和碳的氧化物

证明CO2能和氢氧化钠溶液反应
2NaOH + CO2 = Na2CO3 + H2O 实验原理:检验生成物中有碳酸钠
根据二氧化碳和氢氧化钠溶液反应后 装置内压强减小,大气压作用下观察 到的现象,要用水做对比实验(控制 变量)
CO的还原性
先通CO赶走玻璃 管内的空气后加热。
CO + CuO
△
Cu + CO2
碳和碳的氧化物
——复习篇
请同学们回忆一下,自己到目前为止知 道哪些含碳元素的物质,请说出他们的 名称,越多越好。
金刚石、石墨、C60、木炭、活性炭、一氧化碳、 二氧化碳、石灰石、碳酸钠、碳酸等。
木炭、活性炭 混合物 含 碳 元 素 的 物 质 纯净物 石灰石或大理石
金刚石、石墨、C60 单质(C): 氧化物:CO、CO2
6、将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中, 观察到前者变浑浊,后者无明显现象。CO2和NaOH是 否发生了化学反应? ①小明设计了甲、乙两个实验来 验证C02与NaOH发生了化学反应, 如右图所示。实验现象为: 甲软塑料瓶变瘪,乙“瓶吞鸡蛋”。 小虎同学认为上述实验是可行的。其共同原理 是 。 小雯同学提出质疑,她认为上述实验还不足以说明CO2 和NaOH发生了反应。其理由是 。 小明同学针对小雯的质疑又补充了一个对照实验,这 个实验是 。 ②小虎向甲实验后变瘪塑料瓶的溶液中加入 , 观察到 现象,从而证明CO2与NaOH已 经发生了反应。
反应中CO得氧,具有还原性,发生氧化反 应 ;CuO失氧,具有氧化性,发生还原反应。
CO2的氧化性
C + CO2
高温
2CO
设计碳和二 氧化碳反应 思路引导: 的实验装置, 设计实验装置时 并证明产物 要根据反应物的 为一氧化碳 状态,反应条件, 和实验目的
金刚石、石墨和C60

(4)你还能列举其他类似的化学反应吗?
答案:3C+2Fe2O3
4Fe+3CO2↑
CuO+H2
Cu+H2O
4 还原反应:__含__氧__化__合__物__里__的__氧__被__夺__去__的__反__应____。
二、碳的化学气中燃烧的实验时,需要先将木炭在酒精灯 上烧到红热,然后慢慢伸到集气瓶内;再向瓶内倒入少量澄 清石灰水振荡,石灰水变浑浊,说明生成物是__二__氧__化__碳___; 这一实验说明木炭在点燃的条件下具有___可__燃__性___,化学方 程式为___C_+_O_2______C_O_2 _______。 (2)冬天用煤火炉取暖,若通风不畅会发生煤气中毒,这是因 为当氧气不充足时,碳不充分燃烧就会生成__一__氧__化__碳____, 造成煤气中毒,化学方程式为__2_C_+_O_2______2_C_O________。
3 思考并交流以下问题。
(1)铅笔芯中含铅吗?它的主要成分是什么?用石墨作电极 反映了石墨的什么性质? (2)生锈的铁锁孔里加点铅笔芯就容易打开,为什么?
二、碳的化学性质
1 常温下,碳的化学性质__不__活__泼__(_或__比___较__稳__定__)__, 碳受日光照射或与空气、水分接触,都不容易起变 化。
答案:由于这二者的碳原子排列方式不同,决定了物 理性质差别很大。物质的结构、性质和用途 之间联系紧密,物质的结构决定着性质,性质 在很大程度上决定了物质的用途,反过来,用 途能反映出物质的性质。
3 木炭与氧化铜反应的化学方程式: _C_+_2_C_u_O_2______C_u_+_C_O_2_↑____;焦炭还原氧化铁的化 学方程式:_3_C_+_2_F_e_2_O_3 _____4_F_e_+_3_C_O_2_↑__,碳还原二 氧化碳的化学方程式:__C_O_2_+_C______2_C_O_____,这些 反应说明碳具有__还__原__性____。
碳的几种单质

碳的几种单质知识要点:了解金刚石、石墨、木炭等单质的物理性质和用途。
知识详解:以单质形式存在的碳有金刚石、石墨,还有无定形碳,如木炭、活性炭、焦炭和炭黑等。
1、金刚石、石墨的物理性质和用途金刚石和石墨是两种具有不同物理性质的单质,但当它们分别在氧气中燃烧时,只能生成CO2,说明金刚石和石墨都是由碳元素组成的。
金刚石、石墨都是由碳元素组成的单质,但它们的物理性质有很大差别。
这是因为金刚石、石墨中碳原子的排列方式不同。
2、木炭、焦炭、活性炭、炭黑等通常称为无定形碳,它们主要是由石墨的微小晶体和少量杂质构成的。
木炭是多孔性固体,表面积很大,因此有吸附性,能吸附气体或染料等微小颗粒,常用它来吸附一些食品和工业产品里的色素,也可以用它吸附有臭味的物质。
活性炭表面积比木炭更大,活性炭的吸附能力比木炭还强,防毒面具里就是用它来吸附毒气的。
“碳”和“炭”的区别和联系:“碳”指的是碳元素,它是核电荷数为6的同—类原子总称,不具体指某种物质。
“炭”指的是具体物质,如木炭、活性炭、焦炭、炭黑,这些物质都是碳元素形成的单质。
[典型例题剖析][例1]下列关于石墨的性质和用途的说法中,不正确的是()A、熔点高,有滑腻感,可用于制润滑剂B、质软,在纸上划过留痕迹,可用于制铅笔芯C、有良好的导电性,可用于制干电池的电极D、耐高温,可用于制作刻划玻璃的工具分析:物质的用途与性质是紧密联系的。
由于石墨有滑腻感,可减小物质间的摩擦力,可作润滑剂,又由于耐高温可做耐高温的润滑剂。
做电池,必须要求要有良好的导电性。
玻璃较硬,刻划玻璃的工具必须是硬度很大的物质。
答案:D[例2]下列叙述中,正确的是()A、由碳元素的单质组成的物质一定是纯净物B、金刚石和石墨具有相同的元素组成C、石墨转变为金刚石不属于化学变化D、C60是一种碳元素的单质分析:由碳元素组成的单质有石墨、金刚石和C60。
若将它们混合在一起,则该物质只含碳元素的单质,但属于混合物。
化学人教版(2024版)九年级上册6.1 碳单质的多样性 教学教案 教学设计01

第六单元碳和碳的氧化物课题1 碳单质的多样性第1课时碳的单质1.核心素养(1)了解金刚石和石墨的物理性质和主要作用。
(2)知道不同的元素可以组成不同的物质,同一种元素也可以组成不同的物质。
(3)以碳的单质为载体,引导学生形成观念:①物质的性质在很大程度上决定了物质的用途;②科学发展是无止境的。
2.教学重点金刚石、石墨、木炭和活性炭的物理性质和用途。
3.教学难点物质的结构与性质、性质与用途的关系。
4.教学建议【建议1】有关物质的结构与性质、性质与用途的关系。
(1)观察下列图片,总结物质的结构与性质的关系。
(2)石墨为什么能作干电池的电极?石墨为什么可制铅笔芯?用金刚石制玻璃刀利用了它的什么性质?(3)通过对问题(2)的理解,请你总结一下物质的性质和用途的关系。
(4)你知道为什么食品包装用氮气作保护气,金属铜能作导线,H2O和H2O2的组成元素相同而性质却不同吗?【建议2】比较木炭和活性炭吸附性的强弱。
教师演示木炭吸附性实验,同时做一个活性炭吸附性的对比实验:取两个50 mL的烧杯,各加入20 mL蒸馏水,然后各滴入2滴红墨水,分别放入相同质量的木炭和活性炭,比较溶液中红色褪去所需的时间,进而确定两者吸附性的强弱。
教学过程一、情景导入【师讲解】物质是由元素组成的。
例如氧气是由氧元素组成的,氢气是由氢元素组成的,水是由氢、氧两种元素组成的。
不同的元素组成不同的物质。
那么,有没有同一种元素组成不同种物质的例子呢?【师问】氧元素能组成哪些单质?【师问】磷元素能组成哪些单质?【师问】由此说明什么?【师讲解】碳元素能不能组成不同的单质呢?研究表明:金刚石、石墨和C60都是由碳元素组成的单质。
今天,我们就来学习金刚石、石墨和C60。
二、合作探究探究点①碳的单质(1)金刚石【提出问题】通过前面的学习,我们知道不同的元素可以组成不同的物质,如氧气是由氧元素组成的,氢气是由氢元素组成的,那么,同种元素可以组成不同的物质吗?【归纳总结】同种元素可以组成不同的物质,如氧气和臭氧(O3)都是由氧元素组成的,红磷和白磷都是由磷元素组成的。
活性炭的特性,作用原理及其应用[1]
![活性炭的特性,作用原理及其应用[1]](https://img.taocdn.com/s3/m/2f3269c4aa00b52acec7ca04.png)
活性炭的特性,作用原理及其应用活性炭介绍活性炭是以优质椰子壳、核桃壳、杏壳、桃壳为原料,经系列生产工艺精制而成,外观呈黑色颗粒状。
优点是孔隙结构发达,比表面积大,吸附性能强,库层阻力小,化学性能稳定,易再生。
适用于高纯度的生活饮用水、工业用水和废水处理的深度净化脱氯、脱色、除臭和黄金提炼等方面。
活性炭是一种多孔性的含炭物质, 它具有高度发达的孔隙构造, 是一种极优良的吸附剂,每克活性炭的吸附面积更相当于八个网球埸之多. 而其吸附作用是藉由物理性吸附力与化学性吸附力达成. 其組成物质除了炭元素外,尚含有少量的氢、氮、氧及灰份,其結构则为炭形成六环物堆积而成。
由于六环炭的不规则排列,造成了活性炭多微孔体积及高表面积的特性。
活性炭可由许多种含炭物质制成,这些物质包括木材、锯屑、煤、焦炭、泥煤、木质素、果核、硬果壳、蔗糖浆粕、骨、褐煤、石油残渣等。
其中煤及椰子壳已成为制造活性炭最常用的原炓。
活性炭的制造基本上分为两过程,第一过程包括脱水及炭化,将原料加热,在170至600℃的温度下干燥,並使原有的有机物大約80%炭化。
第二过程是使炭化物活化,这是经由用活化剂如水蒸汽与炭反应来完成的,在吸热反应中主要产生由CO及H2组成的混合气体,用以燃烧加热炭化物至适当的溫度(800至1000℃),以烧除其中所有可分解的物质,由此产生发达的微孔結构及巨大的比表面积,因而具有很强的吸附能力。
活性炭的孔隙按孔径的大小可分為三类。
大孔:半径1000 - 1000000 A。
过渡孔:半径20 - 1000 A。
微孔:半径- 20 A。
由不同原料制成的活性炭具有不同大小的孔径。
由椰壳制的活性炭具有最小的孔隙半径。
木质活性炭一般具有最大的孔隙半径,它们用於吸附较大的分子,並且几乎专用于液相中。
在都市給水处理领域中使用的第一种类型之粒状活性炭即是用木材制成的,称为木炭。
煤质活性炭的孔隙大小介於两者之间。
在煤质活性炭中,褐煤活性炭比无烟煤活性炭具有较多的过渡孔隙及较大的平均孔径,因此能有效地除去水中大分子有机物。
2022年中考化学总复习第一部分考点知识梳理 模块一身边的化学物质 专题二 碳和碳的化合物

专题二碳和碳的化合物1.了解金刚石和石墨的物理性质和主要用途。
2.知道木炭和活性炭具有吸附性。
3.知道不同元素可以组成不同的物质,同种元素也可以组成不同的物质。
4.知道碳单质的化学性质——稳定性、可燃性、还原性。
5.了解实验室中制取二氧化碳的反应原理。
6.探究实验室制取二氧化碳的装置,并利用设计的装置制取二氧化碳。
7.知道二氧化碳、一氧化碳的物理性质和化学性质。
8.了解二氧化碳、一氧化碳在生活和生产中的用途。
9.了解自然界中的氧循环和碳循环。
10.知道温室效应,了解防止温室效应进一步增强应采取的措施。
名师考点精讲考点1 碳单质的性质及碳、氧循环[5年5考]1.碳单质的物理性质和用途金刚石、石墨、C 60是常见的碳单质,它们虽然都是由 碳元素 组成的,但属于三种不同的物质;由于构成它们的 碳原子的排列方式 不同,因此它们的物理性质存在很大差异。
(1)金刚石、石墨、C 60的物理性质和用途:(2)木炭、活性炭的性质及用途:①木炭具有疏松多孔的结构,因此它具有较强的吸附能力,可用于吸附色素和异味。
②活性炭的吸附作用比木炭强,常应用于水的净化、防毒面具里的滤毒罐、制糖工业、冰箱除味剂等。
(1)石墨在一定条件下可转化成金刚石,属于化学变化。
(2)活性炭的吸附性是物理性质。
2.碳的化学性质和用途充分燃烧:C+O2CO2不充分燃烧:2C+O22CO说明:相同反应物在不同条件下反应产物可能不同现象:黑色固体逐渐变为红色,澄清石灰水变浑浊,反应的化学方程式:C+2CuO与CO2反应:C+CO22CO1.对“同种元素不一定只组成一种单质”的说法理解不透彻。
如碳元素可组成金刚石、石墨和C60等单质,所以只含一种元素的物质不一定是单质,也可能是几种单质组成的混合物。
2.金刚石、石墨、C60等都是由碳元素组成的单质,构成它们的碳原子的最外层电子数相同(都是4),因此,不同碳单质的化学性质相同。
3.碳、氧循环(1)人和动植物的呼吸、化石燃料的燃烧等均能产生二氧化碳;而绿色植物的光合作用却吸收二氧化碳,放出氧气。
第7讲碳单质

第七讲碳的单质基础知识过关题一一、碳的单质:金刚石、石墨、C60、无定形碳(木炭、活性炭、焦炭、炭黑)。
1.金刚石的物理性质及用途物理性质:用途:2.石墨的物理性质及用途物理性质:用途:(1) (2) (3) (4)3. 金刚石、石墨都是碳的单质,在物理性质上存在巨大差异的原因:小结①一种元素可以形成多种不同的单质。
由此可知,由同种元素组成的纯净物叫单质。
②多种单质可能由同一种元素组成,如红磷和白磷。
4. C60:5.无定形碳:木炭、焦炭、活性炭、炭黑也是碳的单质,它们通常称为无定形碳。
(1) 木炭:(2) 活性炭:吸附作用:气体或液体里的某些物质被吸附到固体表面的作用。
能大量吸附气体和小微粒。
具有吸附性的原因:(3) 焦炭:(4) 炭黑:【基础夯实】1.自然界里存在的碳单质有______和______。
在天然物质里硬度最大的是________,它可以做________ 等。
________是最软的矿物之一,可用于制作 _____ _等。
2.金刚石和石墨在氧气里燃烧后,生成的产物都是____,说明它们都是由____元素组成的____。
但它们的物理性质却有很大的____,这是由于它们的晶体中____而造成的。
3.下列物质中,不属于碳单质的一组物质是()A.金刚石和石墨B.木炭和焦炭 C.活性炭和炭黑D.一氧化碳和二氧化碳4.下列说法正确的是()A.一种元素只能形成一种单质 B.一种元素可能形成几种单质C.同种元素组成的不同种单质性质相同D.由碳元素形成的单质都是黑色的5.木炭可用来脱色、除臭味,这是利用了它的()A.可燃烧B.稳定性C.还原性D.吸附性6.木炭具有很强的吸附性,这是因为()A.木炭比木材轻B木炭不溶于水C.木炭具有疏松多孔的结构D木炭不易跟其它物质发生化学反应7、低碳生活,从我做起。
下列做法不符合低碳生活理念的是()A 拒绝使用一次性木筷B 出门随手关灯C 废旧书籍做焚烧处理D 草稿纸双面使用8.金刚石和石墨都是由____元素组成的__,但是它们的物理性质差异很大,这是因为它们的晶体结构中____而引起的。
常见物质性质归纳
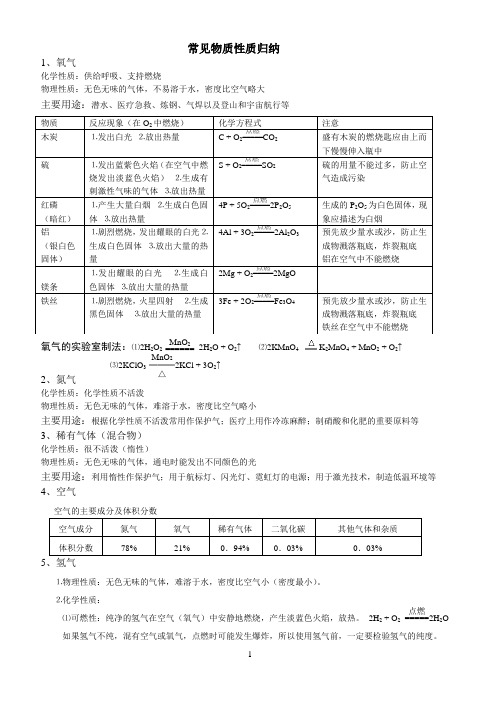
常见物质性质归纳1、氧气化学性质:供给呼吸、支持燃烧物理性质:无色无味的气体,不易溶于水,密度比空气略大主要用途:潜水、医疗急救、炼钢、气焊以及登山和宇宙航行等氧气的实验室制法:⑴2H 2O 2 MnO 2====== 2H 2O + O 2↑ ⑵2KMnO 4K 2MnO 4 + MnO 2 + O 2↑⑶2KClO 3 MnO 2═══△2KCl + 3O 2↑2、氮气化学性质:化学性质不活泼物理性质:无色无味的气体,难溶于水,密度比空气略小主要用途:根据化学性质不活泼常用作保护气;医疗上用作冷冻麻醉;制硝酸和化肥的重要原料等 3、稀有气体(混合物)化学性质:很不活泼(惰性)物理性质:无色无味的气体,通电时能发出不同颜色的光主要用途:利用惰性作保护气;用于航标灯、闪光灯、霓虹灯的电源;用于激光技术,制造低温环境等 4、空气空气的主要成分及体积分数5⒈物理性质:无色无味的气体,难溶于水,密度比空气小(密度最小)。
⒉化学性质:⑴可燃性:纯净的氢气在空气(氧气)中安静地燃烧,产生淡蓝色火焰,放热。
2H 2 + O 2 点燃=====2H 2O 如果氢气不纯,混有空气或氧气,点燃时可能发生爆炸,所以使用氢气前,一定要检验氢气的纯度。
⑵还原性(氢气还原CuO)实验现象:黑色粉末变红色;试管口有水珠生成H2 + CuO Cu + H2O⒊氢气的用途:充灌探空气球;作高能燃料;冶炼金属。
6、碳的单质⒉木炭、活性炭⑴木炭:有吸附作用,用于吸附一些食品和工业产品里的色素,吸附有异味的物质。
⑵活性炭:有较强的吸附作用,用于防毒面具、冰箱的除臭剂。
7、碳⒈常温下,碳的化学性质不活泼(碳原子最外层有4 个电子)应用:解释古代字画为什么经历几千年而不变色?档案资料为什么要求用碳素墨水书写?⒉碳的可燃性(相同的反应物,因反应物的量不同,生成物不同)充分燃烧 C + O2点燃===== CO2放热不充分燃烧2C + O2点燃===== 2CO⒊碳的还原性⑴C + 2CuO 2Cu + CO2↑现象:黑色粉末变红色,澄清的石灰水变浑浊。
石墨的物理性质

石墨的物理性质
石墨是一种天然矿物,具有独特的物理性质。
本文将探讨石墨的物理性质,包
括其晶体结构、导电性、热导性等方面。
1. 晶体结构
石墨的晶体结构属于六方晶系,通常以由碳原子构成的平行六边形的层状结构
存在。
每一层的碳原子之间通过σ键和π键相互连接,形成类似于蜂窝的结构。
这种层状结构使得石墨在一个平面上具有很高的强度和硬度。
2. 导电性
石墨具有较好的导电性,这主要是由于其层状结构中的π键的存在。
π键的存
在使得电子在层与层之间可以自由移动,从而导致石墨具有良好的导电性能。
因此,石墨常被用作导电材料,例如在电池制造中的应用。
3. 热导性
石墨也具有优异的热导性能。
与导电性类似,石墨的热导性能也与其层状结构
中的π键有关。
热能可以通过层与层之间自由传递,使石墨可以迅速传导热量。
因此,石墨广泛用于高温热导材料的制备。
4. 其他性质
除了上述物理性质外,石墨还具有一些其他特殊的性质。
例如,石墨具有良好
的润滑性能,常常被用作润滑剂。
此外,石墨还具有较高的化学稳定性,不易与许多化学物质发生反应。
综上所述,石墨作为一种独特的材料,具有优异的物理性质,包括其特殊的晶
体结构、优良的导电性和热导性等特点,使得其在许多领域都有重要的应用价值。
人教版初三化学(上)第六单元 碳和碳的氧化物 复习总结(含答案解析)

第六单元复习__________________________________________________________________________________ __________________________________________________________________________________1.了解金刚石、石墨、活性炭、木炭的性质和用途。
2.探究实验室中制取CO2的装置,并制取CO2。
3.掌握二氧化碳的性质及一氧化碳的性质。
一、碳的几种单质金刚石无色透明,正八面体形状的固体,是天然最硬的物质。
1.常温下,碳的化学性质不活泼,但在高温或点燃条件下,碳的活性大大增强。
2.可燃性:碳在氧气中充分燃烧:C + O2点燃 CO2碳在氧气中不充分燃烧:2C + O2点燃 2CO3.还原性:木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑用于装饰品钻石,切割玻璃、钻探机的钻头。
石墨深灰色,有金属光泽,不透明细鳞片状固体,质软,有良好的导电性、润滑性常用于做电极,铅笔芯、石墨炸弹等活性碳吸附性常用木炭与活性炭做吸附剂。
金刚石和石墨的物理性质有很大差异的原因是:碳原子的排列不同。
CO和CO2的化学性质有很大差异的原因是:分子的构成不同。
无定形碳:由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑等.活性炭、木炭具有强烈的吸附性,焦炭用于冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。
二、单质碳的化学性质单质碳的物理性质各异,而各种单质碳的化学性质却完全相同!1.常温下的稳定性强2.可燃性:完全燃烧(氧气充足),生成CO2: C+O点燃CO2不完全燃烧(氧气不充足),生成CO:2C+O点燃2CO3.还原性:C+2CuO 高温2Cu+CO2↑(置换反应)应用:冶金工业三、二氧化碳的制法1.实验室制取气体的思路:(原理、装置、检验)(1)发生装置:由反应物状态及反应条件决定:反应物是固体,需加热,制气体时则用高锰酸钾制O2的发生装置。
2021秋人教版初中化学《金刚石、石墨和C60》同步学案(解析版)

课题6.1 金刚石、石墨和C601.了解金刚石、石墨、木炭、活性炭的主要物理性质和用途,认识C60的分子结构;2.掌握碳单质的化学性质;3.认识结构、性质和用途之间的关系,能用发展的观点看待碳单质。
1.了解金刚石、石墨、活性炭、木炭的性质和用途;2.掌握碳单质的化学性质;一、碳的单质【独具慧眼】下列各组物质中哪几组是由同种元素组成的不同单质?(填序号)。
①H2O和H2O2 ②二氧化碳和干冰③红磷和白磷④H2和N2⑤O2和O3⑥CO2和CO【答案】③⑤研究表明,碳元素也可以组成不同的单质,透明的金刚石、浅灰色的石墨和足球状的C60都是由碳元素组成的单质。
1.金刚石(1)金刚石的结构(2)金刚石的物理性质和用途【练一练】天然存在的最硬的物质是()A.金刚石 B.石墨 C.石头 D.黄金【答案】A2.石墨(1)石墨的结构石墨的碳原子呈层状结构。
(2)石墨的物理性质和用途(3)木炭、活性炭、炭黑、焦炭在日常生活和工农业生产中,我们常用到木炭、活性炭、炭黑、焦炭等,它们的主要成分也是碳单质,它们的结构也与石墨类似。
木炭具有疏松多孔的结构,表面积很大,具有较强的吸附性。
活性炭的吸附作用比木炭还要强,它的用途主要有:①装在防毒面具里的滤毒罐中来吸附毒气;②制糖工业也需要活性炭来脱色来制白糖;③做冰箱中的除异味剂;④饮用水的深度净化。
【练一练】高铁动车与电路连接的是石墨电刷,它没有体现出石墨具有的性质是()A.导电性B.还原性 C.滑腻感D.稳定性【答案】B【练一练】下列有关物质性质与用途的说法,错误的是()A.石墨有滑腻感,可用来作电极B.石墨很软,可用来制铅笔芯C.活性炭有吸附性,可用来吸附异味D.金刚石的硬度大,可用来切割玻璃【答案】A【练一练】如图为金刚石、石墨、C60结构示意图,下列说法正确的是()A.金刚石、石墨属于单质,C60属于化合物B.它们都是由碳元素组成的,属于同一种物质C.这三种物质中碳原子的排列方式不同D.石墨在一定条件下转化为金刚石属于物理变化【答案】C3. C60C60的分子结构【想一想】从C60的分子式和结构图中你能得到哪些信息?①C60是一种分子;②每个C60的分子是由60个碳原子构成。
活性炭的特性,作用原理及其应用

活性炭的特性,作用原理及其应用活性炭介绍活性炭是以优质椰子壳、核桃壳、杏壳、桃壳为原料,经系列生产工艺精制而成,外观呈黑色颗粒状。
优点是孔隙结构发达,比表面积大,吸附性能强,库层阻力小,化学性能稳定,易再生。
适用于高纯度的生活饮用水、工业用水和废水处理的深度净化脱氯、脱色、除臭和黄金提炼等方面。
活性炭是一种多孔性的含炭物质, 它具有高度发达的孔隙构造, 是一种极优良的吸附剂, 每克活性炭的吸附面积更相当于八个网球埸之多. 而其吸附作用是藉由物理性吸附力与化学性吸附力达成. 其組成物质除了炭元素外,尚含有少量的氢、氮、氧及灰份,其結构则为炭形成六环物堆积而成。
由于六环炭的不规则排列,造成了活性炭多微孔体积及高表面积的特性。
活性炭可由许多种含炭物质制成,这些物质包括木材、锯屑、煤、焦炭、泥煤、木质素、果核、硬果壳、蔗糖浆粕、骨、褐煤、石油残渣等。
其中煤及椰子壳已成为制造活性炭最常用的原炓。
活性炭的制造基本上分为两过程,第一过程包括脱水及炭化,将原料加热,在170至600℃的温度下干燥,並使原有的有机物大約80%炭化。
第二过程是使炭化物活化,这是经由用活化剂如水蒸汽与炭反应来完成的,在吸热反应中主要产生由CO及H2组成的混合气体,用以燃烧加热炭化物至适当的溫度(800至1000℃),以烧除其中所有可分解的物质,由此产生发达的微孔結构及巨大的比表面积,因而具有很强的吸附能力。
活性炭的孔隙按孔径的大小可分為三类。
大孔:半径1000 - 1000000 A。
过渡孔:半径20 - 1000 A。
微孔:半径- 20 A。
由不同原料制成的活性炭具有不同大小的孔径。
由椰壳制的活性炭具有最小的孔隙半径。
木质活性炭一般具有最大的孔隙半径,它们用於吸附较大的分子,並且几乎专用于液相中。
在都市給水处理领域中使用的第一种类型之粒状活性炭即是用木材制成的,称为木炭。
煤质活性炭的孔隙大小介於两者之间。
在煤质活性炭中,褐煤活性炭比无烟煤活性炭具有较多的过渡孔隙及较大的平均孔径,因此能有效地除去水中大分子有机物。
《碳和碳的氧化物》知识点

《碳和碳的氧化物》知识点一、知识考查点考点1碳单质的性质与用途碳单质包括金刚石、石墨、无定形碳(木炭、活性炭、焦炭、炭黑)、C60、碳纳米管、石墨烯等,学习或复习时按“名称――结构性质用途”这条线来掌握这部分知识。
1.碳单质的物理性质与用途。
金刚石的正八面体结构坚硬性作玻璃刻刀、机器钻头、装饰品等;石墨的细鳞片状结构质软、导电性、滑腻性、耐高温铅笔芯、电极、润滑剂、坩埚;木炭和活性炭的疏松多孔的结构吸附性吸附食品色素、除臭、防毒面具、冰箱除味剂等;C60分子(又称足球烯)的球状结构稳定性超导体等;碳纳米管的多孔结构储氢等。
2.碳单质的化学性质与用途。
碳单质物理性质各异,但化学性质类似,都具有可燃性作燃料,家庭取暖、做饭等;具有还原性冶炼金属,如冶炼金属铜、铁等;常温下稳定性制作字画、书写档案等。
考点2二氧化碳制取的探究气体制取设计思路一般为发生装置(先组装装置并检验装置的气密性)→净化装置→干燥装置→收集装置→验证气体性质装置→尾气处理装置(对有毒气体用溶液吸收或燃烧掉)等。
实验室里制取二氧化碳是根据反应物的状态(大理石为固体、稀盐酸为液体)和反应条件(常温)发生装置(与用过氧化氢溶液制取氧气类似),二氧化碳的密度比空气大且易溶于水收集装置(用向上排气法,不用排水法)。
工业上常用煅烧石灰石可制得副产品二氧化碳气体(CaCO3CaO + CO2↑)。
另外,从实验室制取二氧化碳可得到碳酸盐的检验方法:用试管取样品少许,滴加稀盐酸,并将产生的气体通入到澄清石灰水,若澄清石灰水变浑浊,证明是二氧化碳气体,原样品含有碳酸盐。
考点3二氧化碳与一氧化碳的比较一般的,物质的结构决定其性质。
CO2的结构式为O=C=O,分子形状为直线形的,属于非极性分子,表现出在于其它物质起反应时容易失氧,具有氧化性,发生还原反应。
而CO的结构式为O=C,分子形状为直线形的,属于极性分子,表现出在于其它物质起反应时容易得氧,具有还原性,发生氧化反应.1.二氧化碳的性质及其用途:不支持燃烧且密度比空气大灭火,干冰制冷剂或人工降雨,与某些物质反应化工产品的原料或植物光合作用,石灰水吸收空气中二氧化碳石灰浆抹墙等。
2020年中考化学知识点之碳单质性质和用途

2020年中考化学知识点之碳单质性质和用途
碳单质性质和用途
1. 金刚石、石墨和C60都是碳元素的单质,但由于碳原子的排列方式不同,决定了它们的物理性质存在了很大的差异。
(1)金刚石:立体网状结构物理性质:自然界中最硬的物质。
用途:玻璃刀、钻头、饰品
(2)石墨:平面结构物理性质:有滑腻感,导电性。
用途:铅笔芯、电极材料、润滑剂
(3)C60:一个分子由六十个碳原子组成的碳单质,是足球状。
相对分子质量
2.无定形碳
(1)木炭:具有疏松多孔结构,决定了它有吸附能力,可做燃料火药、活性炭、吸附剂。
(2)活性炭:(吸附剂净化空气净化甲醛)。
(3)炭黑:用途:染料,墨汁,油漆
(4)焦炭:用途燃料,冶金工业还原剂。
炭:表示碳元素组成的某种单质。
碳是元素名称。
第六单元碳和碳的氧化物课题1金刚石石墨和C6020232024九年级上化学人教知识必备典例解析课后作

第六单元 碳和碳的氧化物(教用)课题1 金刚石、石墨和C 60一、知识必备 知识点1 单质碳的性质与用途1. 金刚石、石墨的物理性质和用途化学式 颜色 形状 硬度 导电性 导热性 润滑性 熔点 用途 金刚石C无色透明 正八面体 最硬无 无 无 高 划玻璃、切割金属、钻探机钻头、制装饰品等 石墨 深灰色、有金属光泽、不透明 细鳞片状 最软之一 优良 良好 良好 电极、铅笔芯、润滑剂等 注:金刚石是天然存在的最硬的物质;在一定条件下,将石墨转化为金刚石的变化是化学变化。
2. 木炭、活性炭、焦炭和炭黑的性质与用途颜色、状态 制法 用途 木炭灰黑色的多孔性固体 木材隔绝空气加强热 燃料、黑火药、制活性炭、冶炼金属 活性炭 灰黑色多孔颗粒状固体 木炭在高温下用水蒸气处理净化多种气体和液体、作防毒面具 焦炭浅灰色多孔性固体 烟煤隔绝空气加强热 冶炼金属 炭黑 极细的黑色粉末 含碳物质不完全燃烧 墨、油墨、油漆、鞋油、燃料等,作橡胶制品的填料 注:木炭、活性炭具有吸附性(物理性质),活性炭的吸附性更强。
3. C 60:C 60分子是一种由60个碳原子构成的分子,它形似足球,这种足球结构的碳分子很稳定。
4. 金刚石、石墨、C 60性质不同的原因:碳原子的排列方式不同。
知识点2 碳的化学性质1. 稳定性:在常温下,碳的化学性质不活泼。
2. 可燃性:C+O 2CO 2(充分燃烧) 2C+O 22CO (不充分燃烧)碳在氧气中燃烧的现象:燃烧剧烈,发出白光;放热;生成能使澄清石灰水变浑浊的气体。
3. 还原性:C+2CuO 2Cu+CO 2↑ 2Fe 2O 3+3C 4Fe+3CO 2↑ 单质碳的还原性可用于冶金工业。
4. 木炭还原氧化铜的实验(见右图)【实验操作】① 把刚烘干的木炭粉末和氧化铜粉末混合均匀,小心地铺放进试管;② 将试管固定在铁架台上。
试管口装有通入澄清石灰水的导管;③ 集中加热;④ 过几分钟后,先撤出导气管,待试管冷却后再把试管里的粉末倒在纸上。
8课题1__金刚石、石墨和C60 课时1

作业
1.制作炭黑(教材P108页)
2.请你调查:一般对于写档案的墨 水有什么要求,为什么?(预习—碳的 化学性质)
我的梦 中国梦
学会对比 寻找差距 放飞思维 实现梦想
C60
C60除了在材料科学、超导体等方面的应用
在以下几个方面具有广泛的应用前景 还
①气体的贮存 ②有感觉功能的传感器 ③增强金属的强度 ④新型催化剂 ⑤光学应 用 ⑥对癌细胞的杀伤效应
碳的其它几种单质
C20
C60 C70
C40
C540
纳米碳管
纳米碳管有着不可思议的强度与韧性, 重量却极轻,导电性极强,兼有金属 和半导体的性能 ;把纳米管组合起来, 比同体积的钢强度高100倍,重量却只 有1/6。
层状结 石墨的碳原子呈平面层状结 构
构,层与层之间作用力小,所 以质软、有滑腻感,能导电。
金刚石和石墨的物理性质差异很大原因? 碳原子排列方式不同
决定
反映
物质的结构
物质的性质
决定
反映
物质的用途
铅笔含“铅”吗?
猜猜看:为什么叫铅笔?
铅笔小知识
在古代的希腊和罗马,人们用铅条或铅块来写 字。因为铅较软能够在纸上划出清晰的黑色,所 以就有了“铅笔”这个名字。但铅有毒且密度大, 后来就不再用它写字了。 铅笔上的“B”是英文“Black”的第一个字母, 在铅笔中表示“软”;“H”是英文“Hard”的第 一个字母,在铅笔中表示“硬”。铅笔为什么有 软和硬和差别呢?这是因为石墨太软,光用石墨 做笔芯,既易断也易磨损,因此,生产上常在石 墨粉末中掺进一些粘土 粉末以增加硬度。粘土掺 得越多,铅笔就越硬;粘土掺得越少,铅笔就越 软。 想一想,“6B”、“6H”与“HB”三种类型的 铅笔,哪种铅笔最硬?哪种铅笔最软?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
活性炭具有吸附能力
练习
练习2
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
2.金刚石、石墨、 C60都是由_碳__元__素_ 组成的单质。但是,它们的性质却 存在巨大的差异(例如金刚石是天 然存在的最硬的物质,而石墨却很 软),这是因为它们原___子__排__列__方__式_ 不同。
• 一、金刚石
• 二、结构
• 三、物理性质 和用途
物理性质 对应的主要用途
① 无 色 透 明 、 ①装饰品——钻 正八面体形状 石 的固体
②天然存在最 ②划玻璃、钻
硬的物质
头等
金刚石的主要用途
金刚石的主要用途
• 一、金刚石
• 二、结构
• 三、物理性质 和用途
三 石墨
石墨
• 一、石墨
• 二、结构
• 三、物理性质 和用途
例如:活性炭用于制造防毒面具, 白糖脱色,冰箱除异味等。
防毒面具
• 一、石墨 • 二、结构 • 三、物理性质
和用途 • 四、木炭、活
性炭
防毒面具
比较金刚石、石墨的结构:
金刚石结构
石墨结构
正八面体结构
金刚石的碳原子在空间 构成连续的,坚固的骨 架的结构,所以坚硬。
层状结构
石墨的碳原子呈平面 层状结构,层与层之间 作用力小,所以质软。 有滑感。
总目录
课题1 金刚石、石墨和C60
• 一、问题 • 二、金刚石 • 三、石墨 • 四、C60 • 五、小结 • 六、练习
? 一 问题
问题
•一、问题
•二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
同一种元素能不能组 成不同的单质呢?
几种不同的单质
几种单质
几种不同的单质:同一类原子,排列方式不同, 所形成的单质不同。 例如:金刚石、石墨、 C60都是由 碳元素组成,却形态各异!根本原 因就在于它们的原子排列方式不同
。(O2 , O3分子的构成不同)
性质有何不同?
?
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
金刚石、石墨、 C60都是由碳元 素组成的单质,那它们的性质用 途又有哪些不同呢?
记
因为碳原子的排列方 式不同,所以金刚石和石 墨的物理性质有很大差异
结构决定性质
四 C60
• 一、C60 • 二、结构
C60
C60结构
• 一、C60 • 二、结构
C60的结构
每一个C60分子都是由60个碳原子构成。
“碳”:碳元素,属于化学用语。在书写元素名称 和碳的单质及碳的化合物等用到。
“炭”:不是化学用语,无定形炭是人工制造的碳单质, 都含有少量杂质为表示区别,常写:木炭, 活性 炭,焦炭,炭黑等。
• 四、木炭、活 性炭
石墨的结构
石墨的结构(细鳞片状)
• 一、石墨
• 二、结构
• 三、物理性质 和用途
• 四、木炭、活 性炭
石墨的物理性质和用途 石墨的物理性质和用途
• 一、石墨
• 二、结构
• 三、物理性质 和用途
• 四、木炭、活 性炭
物理性质
对应的主要用途
①深灰色、有金属
光 泽 、 不 透 明 、 细 ①制造铅笔芯,
阅读课本104-106页,填写课本 121页表格一的碳的单质部分
钻石恒久远 一颗永流传!
二 金刚石
金刚石
• 一、金刚石 • 二、结构 • 三、物理性质
和用途
金刚石的结构
• 一、金刚石 • 二、结构 • 三、物理性质
和用途
金刚石的结构 (正八面体形状)
金刚石的物理性质和用途 金刚石的物理性质和用途
五 小结
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
小结
同一种元素也可以组成不同 的物质。金刚石、石墨和C60 等都是由碳元素组成的单质。
金刚石是天然存在的最硬的 物质 木炭和活性炭具有吸附性
结构决定 性质决定 用途
六 练习
练习
1.这个实验说明了活性炭的什么性质
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
和用途 • 四、木炭、活
性炭
石墨润滑 生锈的铁锁
木炭活性炭
木炭、活性炭
• 一、石墨
• 二、结构
• 三、物理性质 和用途
• 四、木炭、活 性炭
木炭,活性炭主要由_石__墨___构 成,具有_疏__松__多__孔_的结构,因 此 它 具 有 _吸__附__ 能 力 , 可 用 于 _吸_附__除__杂_____。
3.下列物质中最硬的单质是( C )
A.木炭 B. C60 C.金刚石 D.二氧化碳
练习3
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
练习
4.1999年,美国使用了一种“石墨 炸弹”,奇袭获胜。这种炸弹爆炸 后释放出大量的纤维状石墨,覆盖 在发电厂的设备上,造成设备短路 而停电。请解释这是什么原因。 答:这是因为石墨具有优良的导电 性能。
足球烯(C60)
金刚石、石墨、 C60都是由碳元素组成的单质
原因
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
金刚石 石墨
同一类原子,排列方式不同,所形成的单质不同。
? 为什么
为什么?
•一、问题 •二、金刚石 •三、石墨 •四、C60 •五、小结 •六、练习
同一种元素可以组成不同的单质
鳞片状固体
做润滑剂
②很软,有滑腻感
③优良的导电性 ②石墨电极
铅笔芯
制造铅笔芯
• 一、石墨 • 二、结构 • 三、物理性质
和用途 • 四、木炭、活
性炭
石墨和粘土混合制成铅笔芯
电极
• 一、石墨 • 二、结构 • 三、物理性质
和用途 • 四、木炭、活
性炭
石墨电极
电极
• 一、石墨 • 二、结构 • 三、物理性质
5.作业
课后习题1,2(1,2,3小题),5 题
木炭能吸附红墨水吗?
加热后的 木炭
现象: 红色逐渐褪去 分析: 木炭具有疏松多孔的结构,表面积很
大,具有较强的吸附性,能将红墨水 吸附在木炭多孔性结构中。
