苯酚
苯酚ppt课件

苯酚在其他领域的应用
塑料工业
苯酚可以与其他物质合成许多塑料,如酚醛树脂 、聚酚等。
橡胶工业
苯酚可以与其他物质合成橡胶,如丁苯橡胶、丁 腈橡胶等。
油漆和染料工业
苯酚可以与其他物质合成油漆和染料,如酸性染 料、酸性媒介染料等。
05 苯酚的发展前景与展望
苯酚的市场需求和发展趋势
苯酚市场需求持续增长
随着化工、医药、农药等行业的快速发展,苯酚作为重要的中间 体,市场需求量不断攀升。
油等。
合成药物
苯酚是许多药物和合成药物的原料 ,如阿司匹林、布洛芬等。
消毒剂
苯酚具有杀菌作用,可用于医疗器 械、手术工具、伤口等的消毒。
苯酚在农药领域的应用
杀虫剂
苯酚可以与其他物质合成杀虫剂 ,用于防治农业害虫。
除草剂
苯酚可以与其他物质合成除草剂 ,用于清除农田杂草。
杀菌剂
苯酚可以与其他物质合成杀菌剂 ,用于防治植物病害。
合成原料
苯酚可用于合成许多有机化合 物,如酚醛树脂、染料等。
化工原料
苯酚可用于制造其他化学品, 如苯胺、苯甲酸等。
02 苯酚的生产方法
苯酚的合成方法
苯酚的合成方法有多种,其中最常用 的是苯酚的直接氧化法。该方法以苯 为原料,在催化剂的作用下,通过空 气氧化生成苯酚。
此外,还有苯酚的生物合成法,利用 微生物或酶催化苯氧化生成苯酚。
苯酚ppt课件
目录
CONTENTS
• 苯酚的简介 • 苯酚的生产方法 • 苯酚的危害与防护 • 苯酚的应用领域 • 苯酚的发展前景与展望
01 苯酚的简介
苯酚的物理性质
沸点:181.7℃
熔点:40.3℃
01
02
苯酚是什么

苯酚是什么苯酚是一种广泛应用的有机化合物,也被称为羟基苯或碳酸基酚。
它是由苯环上的一个氢原子被一个羟基取代而形成的。
苯酚是无色结晶固体,有特殊的芳香味道。
在本文中,我们将探讨苯酚的化学性质、用途以及对环境和健康可能产生的影响。
首先,苯酚的化学性质使其具有广泛的用途。
由于它具有强大的抗菌性能,所以在制造消毒剂和杀真菌剂时被广泛应用。
此外,苯酚也被用作生物化学试剂,如DNA和RNA的提取和纯化过程中的溶剂。
此外,苯酚还用于制造塑料、染料、杀虫剂等各种产品。
然而,尽管苯酚有许多有用的用途,但它也对环境和人类的健康产生潜在的危害。
苯酚是一种可能有毒的物质,吸入或接触大量苯酚可能会对人体产生严重的危害。
长期接触高剂量的苯酚可能导致中毒症状,包括头痛、恶心、呕吐、中枢神经系统抑制等。
此外,苯酚还可以对水生生物产生毒性影响,污染水体中的苯酚可能导致生态系统的破坏。
对于苯酚的环境排放和处理也是一个重要的问题。
苯酚的排放往往来自于工业废水和废弃物处理厂等源头,这些排放物质可能对环境和水资源造成污染。
为了减少苯酚的排放,需要加强工业企业的管理和监督,实施严格的环境保护措施。
此外,苯酚的处理也是一个挑战,因为苯酚在水中的溶解度较高,容易被传播和扩散。
为了减少苯酚对环境和人类健康的潜在危害,许多国家和地区都制定了相关的法规和标准。
这些法规要求企业减少苯酚的排放,采取有效的治理措施,并对苯酚的使用进行限制。
此外,相关的监测和检测方法也得到了广泛的研究和应用,以保证人们生活和工作环境中的苯酚浓度处于安全水平。
总结起来,苯酚是一种有机化合物,具有广泛的应用。
它具有杀菌功能,可用于制造消毒剂和杀真菌剂等产品。
然而,长期接触高剂量的苯酚可能对人体和环境产生危害。
因此,加强苯酚的管理和监控,减少苯酚的排放,对于保护人类健康和环境具有重要意义。
同时,还需要进一步研究苯酚的毒性机制和治理技术,以期找到更好的解决方案。
苯酚的化学性质

苯酚的化学性质苯酚,又称为羟基苯,是一种有机化合物,化学式为C6H6O。
它是一种无色结晶体,具有特殊的芳香味道。
苯酚是一种重要的化学原料,在医药、染料、农药等领域有着广泛的应用。
本文将着重探讨苯酚的化学性质。
首先,苯酚具有醇的特点,因为它含有羟基(-OH)官能团。
这使得苯酚具有一些与醇类相似的性质。
例如,苯酚能够和酸反应生成酯。
酯是一种有机化合物,由酸和醇反应生成。
苯酚与酸反应时,羟基中的氧原子与酸中的氧原子结合,形成酯的酯基。
这种反应在一些有机合成中具有重要的应用。
其次,苯酚还具有酚类化合物的一些特性。
酚是一类含有苯环的含氧有机化合物。
苯酚与其他酚类化合物一样,具有氧化性。
这是因为苯酚分子中的羟基中含有活泼的氢原子,它很容易被氧气夺走,从而发生氧化反应。
当苯酚暴露在空气中时,会慢慢变黄,并逐渐氧化产生酚醛或酚酮等化合物。
此外,苯酚还可以通过氧化反应制备一些重要的化学品,如苯酚氧化合成醛基苯酚。
此外,苯酚还具有一些典型的酸碱反应。
酸碱中的酸性指的是物质在溶液中释放出H+离子,而碱性则指物质能够从溶液中接收H+离子。
苯酚在水中呈现弱酸性,它能够与碱发生反应,形成盐和水。
例如,苯酚与氢氧化钠反应时,会生成钠苯酚和水。
除此之外,苯酚还具有亲电取代反应的性质。
亲电取代是一种常见的有机反应类型,指的是通过亲电试剂的进攻来取代分子中的某个原子或基团。
亲电试剂是一种亲电子的物质,它具有空的轨道,可以吸引外层电子并参与化学反应。
苯酚与亲电试剂反应时,通常会发生芳香取代反应。
这种反应是一种重要的有机合成反应,能够合成出许多有用的化合物。
总结起来,苯酚的化学性质非常丰富多样。
它既可以发生与醇类相似的反应,也可以表现出酚类的特性。
此外,苯酚还具有酸碱反应和亲电取代反应的性质。
这些性质赋予了苯酚广泛的应用领域和重要的作用。
对于深入了解苯酚的化学性质,可以为其后续的应用研究提供一定的指导。
苯酚的性质

苯酚的性质苯酚是一种碱式有机化合物,其化学式为C6H5OH,是一种低分子量碱性有机化合物,分子量约为94.11,为弱酸。
苯酚无色液体,具有独特的气味,通常为无色液体或淡黄色晶体。
苯酚酸性强,可与碱和弱碱反应,且可溶于水、有机溶剂、氧化剂和碱性溶剂中。
一、苯酚的性质1、溶解性苯酚在水、二甲醚、乙醇、乙醚、苯、醚和其它易溶有机溶剂中可溶解,但溶解度较低,可能因其物质间的疏水作用而变为坚硬的晶体。
2、稳定性苯酚的热稳定性较好,可在100℃下烘干后保持其外观不变,然而在空气中容易发生氧化反应,特别是在温度较高时,由于它与氧发生氧化反应,更容易发生氧化反应。
3、pH值苯酚的pH值为4.7,稍高于中性,它是一种弱酸,可以发生酸碱反应,可与碱和弱碱反应生成盐和水。
二、苯酚的用途合成颜料和溶剂苯酚可用于合成颜料,常用于染料、香料、香料和医药行业中的色料等。
催化剂苯酚可作为催化剂,可用于进行多种反应,例如油水反应、聚合反应和氧化反应等。
清洗剂苯酚也可用作清洗剂,因其具有高性能、无毒、高通用性和环保性等特点,广泛用于电子材料、机械工程、电子和工厂等行业的清洗应用。
三、苯酚的安全性苯酚虽然具有许多优异的性质,但其对人体有一定的负面影响。
高浓度苯酚会刺激眼睛和皮肤,如果处理不当,还可能导致中毒。
因此,使用苯酚时应加以认真的防护措施,并确保正确的使用方法,以避免不必要的伤害和损害。
总之,苯酚是一种独特的有机物质,具有良好的性能,可用于许多化学反应和应用,但也有可能引起机体不良反应。
因此,使用苯酚时,应注意安全防护措施,并确保科学正确的使用方法,以保证苯酚的安全性。
苯酚

苯酚苯酚(C6H6O,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。
常温下为一种无色晶体。
有毒。
有腐蚀性,常温下微溶于水易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶,其溶液沾到皮肤上用酒精洗涤。
暴露在空气中呈粉红色。
苯酚是一种常见的化学品,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料。
【中文名称】苯酚;石炭酸【英文名称】phenol【结构或分子式】所有C原子均以sp2杂化轨道形成σ键,O原子均以sp3杂化轨道形成σ键。
【相对分子量或原子量】94.11【密度】1.071【熔点(℃)】42~43【沸点(℃)】182【折射率】1.5425(41)【毒性LD50(mg/kg)】大鼠经口530。
【性状】无色或白色晶体,有特殊气味。
【溶解情况】溶于乙醇、乙醚、氯仿、甘油、二硫化碳等。
【用途】用于制染料合成树脂、塑料、合成纤维和农药、水杨酸等。
作外科消毒剂消毒能力大小的标准(石炭酸系数)。
【制备或来源】由煤焦油经分馏,由苯磺酸经碱熔。
由氯苯经水解,由异丙苯经氧化重排。
【其他】加热至65℃时能溶于水(在室温下,在水中的溶解度是9.3g,当温度高于65℃时能与水混溶),有毒,具有腐蚀性如不慎滴落到皮肤上应马上用酒精(乙醇)清洗,在空气中易被氧化而变粉红色。
在民间有土方用石炭酸来治皮肤顽疾,以毒攻毒,如用来治脚底起泡。
三维结构一种重要的苯系中间体[1]。
又称石炭酸。
低熔点(43℃)白色晶体,在空气中放置及光照下变红,有臭味,沸点181.84℃。
对人有毒,要注意防止触及皮肤。
工业上主要由异丙苯制得。
苯酚产量大,1984年,世界总生产能力约为5兆吨。
苯酚用途广泛。
第一次世界大战前,苯酚的唯一来源是从煤焦油中提取。
绝大部分是通过合成方法得到。
有磺化法、氯苯法、异丙苯法等方法。
分子结构:苯环上的C原子以sp2杂化轨道成键,O原子以sp3杂化轨道成键。
苯酚主要用于制造酚醛树脂,双酚A及己内酰胺。
苯酚
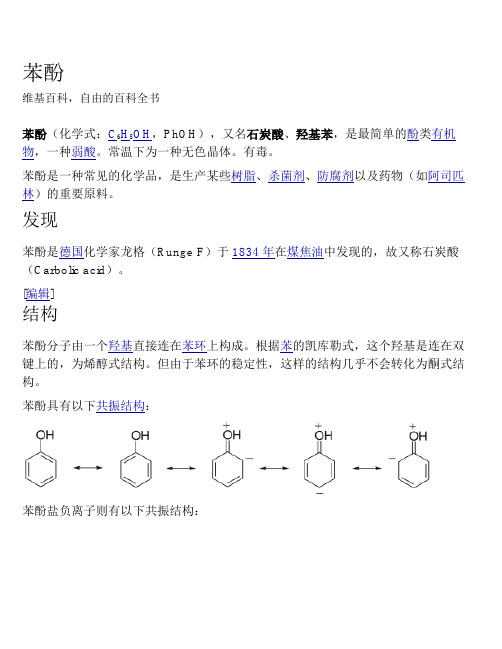
苯酚维基百科,自由的百科全书苯酚(化学式:C6H5OH,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。
常温下为一种无色晶体。
有毒。
苯酚是一种常见的化学品,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料。
发现苯酚是德国化学家龙格(Runge F)于1834年在煤焦油中发现的,故又称石炭酸(Carbolic acid)。
[编辑]结构苯酚分子由一个羟基直接连在苯环上构成。
根据苯的凯库勒式,这个羟基是连在双键上的,为烯醇式结构。
但由于苯环的稳定性,这样的结构几乎不会转化为酮式结构。
苯酚具有以下共振结构:苯酚盐负离子则有以下共振结构:酚羟基的氧原子采用sp2杂化,提供1对孤电子与苯环的6个碳原子共同形成离域键。
大Π键加强了烯醇的酸性,羟基的推电子效应又加强了O-H键的极性,因此苯酚中羟基的氢可以电离出来。
[编辑]物理性质苯酚熔点为40.5℃,沸点为181.7℃,常温下为一种无色或白色的晶体,有特殊气味。
苯酚密度比水大,微溶于冷水,可在水中形成白色混浊;但易溶于65℃以上的热水。
易溶于醇、醚等有机溶剂。
[编辑]化学性质酸碱反应苯酚是一种弱酸,能与碱反应:苯酚pKa=10,酸性介于碳酸两级电离之间,因此苯酚不能与NaHCO3等弱碱反应:此反应现象:二氧化碳通入后,溶液中出现白色混浊。
显色反应苯酚遇三氯化铁溶液显紫色,原因是苯酚根离子与Fe3+形成了有颜色的络合物。
(紫色)取代反应■苯环上的亲电取代:苯酚由于结构中有苯环,可以在环上发生类似苯的亲电取代反应,如硝化、卤代等:对比苯的相应反应可以发现,苯酚环上的取代比苯容易得多。
这是因为羟基有给电子效应,使苯环电子云密度增加。
值得注意的是,苯酚的亲电取代总是发生在羟基的邻位和对位。
这是羟基等给电子基团的共性。
■酚羟基上的取代:酚羟基上的氢原子可以被含碳基团取代,生成醚或酯。
氧化还原反应苯酚在空气中久置会变为粉红色,是因为生成了苯醌:苯酚的氧化产物一般是对苯醌。
苯酚的性质和应用

苯酚的性质和应用苯酚,又称为羟基苯,是一种有机化合物,化学式为C6H6O。
它是一种无色或微黄色的固体晶体,具有特殊的芳香味道。
苯酚可以溶于水、乙醇和醚等常见溶剂,具有一定的挥发性。
下面我将详细介绍苯酚的性质和应用。
首先,让我们来了解一下苯酚的性质。
苯酚是一种酚化合物,具有独特的化学性质。
它可以与酸反应生成对应的酚盐,例如与盐酸反应生成盐酸苯酚。
此外,苯酚还可以与酚醛类化合物发生缩合反应,形成呈深红色的产物。
这种缩合反应在有机合成中有重要的应用价值。
苯酚还具有一定的物理性质。
它的熔点为40°C,沸点为181°C,密度为1.07 g/cm³。
苯酚具有较强的刺激性气味和腐蚀性,对皮肤和黏膜有刺激作用,应避免直接接触。
接下来,我们来探讨一下苯酚的应用。
由于苯酚具有一系列特殊的化学性质,因此在很多领域都有广泛的应用。
首先,苯酚被广泛应用于医药领域。
作为一种消毒剂,苯酚可以杀灭细菌和病毒,常用于外科手术器械的消毒和灭菌。
此外,苯酚还具有一定的麻醉作用,在一些外科手术中被用作局部麻醉剂。
此外,苯酚还可以用于制备一些药物原料,制成消炎止痛的药物。
其次,苯酚在化工工业中也有重要的应用。
由于苯酚具有较强的溶解性和稳定性,它常被用作溶剂和中间体。
苯酚可以用于制备各种化工产品,如合成树脂、合成橡胶和合成香料等。
此外,苯酚还可以用于电镀工业,作为硫酸电镀液中的还原剂,用于电镀金属表面。
在有机合成中,苯酚可以通过苯酚酸化反应制备羧酸,这一反应广泛应用于有机合成的领域。
此外,苯酚还可用于染料工业。
苯酚可以与胺类化合物发生偶氮反应,生成偶氮染料。
这些染料具有鲜艳的颜色和良好的耐光性,广泛应用于纺织和印刷工业。
最后,苯酚还可以用于农业。
苯酚具有一定的杀菌作用,可以用于农作物的防治。
此外,苯酚还可以用作杀虫剂,帮助农民保护农作物。
综上所述,苯酚是一种具有特殊性质和广泛应用的化合物。
它在医药、化工、染料和农业等领域都扮演着重要的角色。
苯酚的结构特点与

在一定条件下,苯酚可以被还原 成苯胺或其它还原产物。
聚合反应
聚合方式
苯酚可以自身发生聚合生成高分子化合物,也可以与其它单 体进行共聚。
应用领域
苯酚的聚合产物在塑料、涂料、胶粘剂等领域有广泛应用。
04 苯酚的制备和工业用途
制备方法
苯酚的制备方法主要有异丙苯氧化法、苯酚丙酮 法、苯直接羟基化法和生物发酵法等。其中,异 丙苯氧化法是最常用的方法,通过异丙苯的氧化 和酸性水解得到苯酚。
酸性比较
苯酚的酸性比醇强,但比碳酸弱,因此可以与碳酸氢钠反应生成苯酚钠和碳酸氢钠。
亲电取代反应
卤代反应
苯酚可以与卤素发生亲电取代反应,生成邻位或对位的卤代苯酚。
硝化反应
在浓硫酸和浓硝酸的条件下,苯酚可以发生硝化反应生成硝基苯酚。
氧化和还原反应
氧化反应
苯酚容易被氧化,在空气中容易 被氧化成粉红色或红色的醌类物 质。
对于废弃的苯酚,应按照相关规定进行妥善处理,避免对环境造成污染。
05 苯酚在生物体内的代谢和 作用
在生物体内的代谢过程
01
02
03
苯酚通过肠道吸收进入 血液,通过循环系统分
布到全身各组织。
在肝脏中,苯酚经过羟 化酶的作用转化为苯醌 ,再进一步代谢为苯酸 和乙酰辅酶A等物质。
苯酸和乙酰辅酶A等物质 可参与三羧酸循环和脂 肪酸合成等代谢过程。
苯酚与其他化合物之间的相互作用可 能产生协同或拮抗作用,影响生物体 的健康状况。
苯酚可以与某些药物发生相互作用, 影响药物的吸收和疗效。
THANKS FOR WATCHING
感谢您的观看
02
苯酚还可用于制造农药、医药、染料、香料等领域,用途广泛。
苯酚化学结构式

苯酚化学结构式
苯酚,化学式C6H5OH,是一种简单的芳香酚化合物,也被称为羟基苯或苯羟基。
它是一种无色至白色的结晶固体,具有特殊的酚味。
苯酚是一种重要的有机化合物,具有多种用途和应用。
苯酚的化学结构可由苯环和一个羟基组成。
苯环是一个六元环,由六个碳原子组成,每个碳原子上连接一个氢原子。
其中一个碳原子上连接一个羟基(-OH),形成苯酚的结构。
这种结构使得苯酚具有一系列独特的化学性质和反应特点。
苯酚是一种弱酸性物质,可以和碱反应生成盐类。
它还可以发生酯化反应、烷基化反应等多种反应。
在氧化条件下,苯酚可以被氧化成苯醌或二苯酮等产物。
此外,苯酚还可以通过芳香氧化反应制备酚醛树脂,具有良好的胶黏性和耐磨性,被广泛用于涂料、粘合剂等领域。
苯酚在医药领域也有重要应用。
它是一种常用的外用抗菌药物,可以用于治疗皮肤病、烧伤等疾病。
此外,苯酚还是一种重要的化学中间体,可以用于合成染料、香精、橡胶助剂等化合物,对化工、医药、农药等行业都具有重要意义。
值得一提的是,苯酚是一种有毒物质,长期接触或吸入高浓度的苯酚蒸气会对人体造成危害,甚至引起中毒。
因此在使用苯酚时,必须严格按照安全操作规程进行操作,避免接触或吸入过量的苯酚。
苯酚作为一种重要的有机化合物,具有广泛的用途和应用。
它的化学结构简单,但却具有丰富的化学性质和反应特点,对化工、医药、农药等领域都具有重要意义。
然而,由于其毒性,使用苯酚时必须谨慎小心,确保安全操作,以免对人体造成危害。
希望随着科学技术的进步,人们能够更好地利用苯酚这种化合物,为社会发展做出更大的贡献。
苯酚的性质

苯酚的性质
苯酚,又称羟基苯,化学式C6H5OH,是一种常见的有机化合物。
它具有许多
独特的性质,使其在工业和实验室中具有广泛的应用。
以下将探讨苯酚的性质。
1. 物理性质
•外观:苯酚呈白色结晶固体,在室温下呈固体状态。
•气味:苯酚具有特殊的酚类气味,有时会被认为是药物或清洁剂的气味。
•密度:苯酚的密度约为1.07 g/cm³。
•熔点和沸点:苯酚的熔点为43°C,沸点为182°C。
2. 化学性质
•酸碱性:苯酚是一种弱酸,具有一定的酸性,可以与碱反应生成盐。
•溶解性:苯酚易溶于乙醇、乙醚等有机溶剂,但在水中的溶解度较小。
•氧化性:苯酚能够被氧化剂氧气氧化成对苯醌。
•与金属反应:苯酚与一些金属反应生成相应的酚盐。
3. 化合性质
•酯化反应:苯酚可以和酰氯反应生成酯类化合物。
•硝化反应:苯酚可以被硝碱硝化生成硝基苯酚。
•磺化反应:苯酚可以被磺酰氯磺化为苯酚磺酸酯。
4. 应用
苯酚由于其独特的性质,具有许多重要的应用领域,包括但不限于:•化妆品和个人护理产品的配方中作为防腐剂或抗氧化剂。
•化工领域中作为合成其他有机化合物的重要原料。
•医药领域用于生产某些药物,如抗生素等。
综上所述,苯酚是一种具有多种性质和广泛应用的有机化合物,在各个领域都
拥有重要地位。
其物理性质和化学性质的研究对于深入了解和应用苯酚具有重要意义。
苯酚反应总结

苯酚反应总结概述苯酚,也被称为羟基苯,是一种常见的有机化合物,化学式为C6H6O。
它具有无色结晶或液体状,有特殊的酚味。
苯酚可通过多种反应进行化学变化,本文将对苯酚的几种常见反应进行总结和讨论。
1. 烷基化反应苯酚经烷基化反应可以得到烷基苯醚化合物。
这种反应可以使用氯代烷基和苯酚在酸性条件下进行,生成对应的烷基苯醚。
反应的机理是先生成一个间位碳正离子,然后苯酚氧化剂为碳正离子进行亲电攻击,生成烷基苯醚。
C6H6O + R-Cl -> C6H5OR + HCl2. 氧化反应苯酚可通过氧化反应转化为苯酚醛、苯酚酮等化合物。
常见的氧化剂包括过氧化氢、高锰酸钾等。
氧化反应中,苯酚的羟基被氧化成羰基。
例如,苯酚通过氧化反应可以得到苯酚醛:C6H6O + KMnO4 (l) -> C6H5CHO + MnO2 (s) + KOH3. 酯化反应苯酚可以与酸酐反应生成酯。
酯化反应通常需要在酸性催化剂的存在下进行。
例如,苯酚和乙酸酐反应可以得到乙酸苯酯:C6H6O + CH3COOC2H5 -> C6H5COOC2H5 + H2O4. 亲电取代反应苯酚可以通过亲电取代反应引入各种官能团,例如卤素、氨基等。
例如,苯酚和溴化亚铁反应可以得到溴苯:C6H6O + FeBr3 -> C6H5Br + FeO + HBr结论苯酚是一种广泛应用的有机化合物,其可以通过多种反应得到多种与之相关的化合物。
烷基化反应、氧化反应、酯化反应和亲电取代反应是苯酚的主要反应类型。
这些反应不仅为化学合成提供了方法,也为苯酚的进一步应用提供了基础。
需要注意的是,这里只列举了苯酚的几种常见反应,实际上还存在其他类型的反应,如取代反应、缩合反应等。
对于不同的反应,我们需要选择适当的反应条件和催化剂。
希望本文总结的内容能对读者对苯酚的化学性质和应用有所了解,并能在实际应用中发挥指导作用。
参考文献:1.陈景秋, 张忠国, 张岳明. 有机化学实验[M]. 高等教育出版社, 2000.2.Morrison R T.. Organic chemistry[M]. 2004.3.Carey F A, Giuliano R M. Organic Chemistry[M]. McGraw-Hill, 2017.。
苯 酚

例3.A和B两种物质的分子式都是C7H8O,它们都能跟金属钠反应放出H2。A不与NaOH溶液反应,而B能与NaOH溶液反应。B能使适量溴水褪色,并产生白色沉淀,A不能。B的一溴代物有两种结构。试推断A和B的结构,并说明它们各属于哪一类有机物。
解析:本题重点考查酚和醇的结构及性质的区别。由于A、B都能与金属钠反应放出氢气,且这两种物质分子中都只含一个氧原子,所以它们结构中都有羟基,即它们为醇或酚;A不与NaOH溶液反应,说明A为醇,结构简式可写成C7H7OH。B能与NaOH溶液反应,B为酚。分子中一定含苯环,分子式可写成CH3C6H4OH;A不能使溴水褪色,说明分子中不能有不饱和链烃基,再从组成分析它应含有苯环,即A是一种芳香醇——苯甲醇C6H5CH2OH。B能使溴水褪色,并生成白色沉淀,进一步证明它是酚类。甲基苯酚CH3C6H4OH,甲基苯酚有邻、间、对三种同分异构体。但只有对甲苯酚的一溴代物含有两种结构:
答案:5种
其中苯甲醇、苯甲醚不属于苯酚同系物。
例5.已知酸性强弱顺序为H2CO3>C6H5OH>HCO ,下列化学方程式正确的是( )
分析:从试题所给的信息可知:H2CO3、C6H5OH、HCO ,均是弱酸,它们都可以部分电离出H+离子。
其电离式:
6C6H5OH+Fe3+→ +6H+,此为特征反应,可以检验苯酚,反之检验Fe3+。
4.加成反应
苯酚中含有苯环,在一定条件下可以和H2发生加成反应。
5.氧化反应:①易被空气中的氧气氧化而显粉红色。
②苯酚可以使酸性高锰酸钾溶液发生氧化还原反应而褪色。
例2.试用一种试剂区别苯、苯酚溶液、己烯和CCl4,说明依据。
苯酚

苯酚苯酚(C6H6O,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。
常温下为一种无色晶体。
有毒。
有腐蚀性,常温下微溶于水,易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶,其溶液沾到皮肤上用酒精洗涤。
暴露在空气中呈粉红色。
中文名:苯酚外文名:p henol 别名:石炭酸分子式:C6H6O 相对分子质量:94.11化学品类别:有机物--苯的衍生物管制类型:不管制储存:密封保存理化性质物理性质外观与性状:白色结晶,有特殊气味。
熔点(℃):40.6相对密度(水=1):1.07沸点(℃):181.9相对蒸气密度(空气=1):3.24折射率1.5418闪点79.5℃分子式:C6H6O化学式:C6H5OH,PhOH分子量:94.11饱和蒸气压(kPa):0.13(40.1℃)燃烧热(kJ/mol):3050.6临界温度(℃):419.2临界压力(MPa):6.13辛醇/水分配系数的对数值:1.46闪点(℃):79爆炸上限%(V/V):8.6引燃温度(℃):715爆炸下限%(V/V):1.7溶解性:可混溶于、醚、氯仿、甘油、二硫化碳、凡土林、挥发油、强碱水溶液。
室温时稍溶于水,与大约8%水混合可液化,65℃以上能与水混溶,几乎不溶于石油醚。
化学性质可吸收空气中水分并液化。
有特殊臭味,极稀的溶液有甜味。
腐蚀性极强。
化学反应能力强。
与醛、酮反应生成酚醛树脂、双酚A,与醋酐;水杨酸反应生成醋酸苯酯、水杨酸酯。
还可进行卤代、加氢、氧化、烷基化、羧基化、酯化、醚化等反应。
[2]苯酚在通常温度下是固体,与钠不难顺利发生反应,如果采用加热熔化苯酚,再加入金属钠的方法进行实验,苯酚易被氧化,在加热时苯酚颜色发生变化而影响实验效果。
本人在教学中采取下面的方法实验,操作简单,取得了满意的实验效果。
在一支试管中加入2-3毫升无水乙醚,取黄豆粒大小的一块金属钠,用滤纸吸干表面的煤油,放入乙醚中,可以看到钠不与乙醚发生反应。
苯酚高中知识点

苯酚高中知识点苯酚是一种常见的有机化合物,化学式为C6H5OH,也叫作羟基苯。
它是一种有毒的颜色无色、有刺激性味道的晶体,可以在水中和许多有机溶剂中溶解。
苯酚在工业界和医学界有着广泛的应用,同时也是高中化学学习中的重要知识点。
一、苯酚的物理性质苯酚是一种具有极性的分子,它具有较强的氢键作用力,因此其熔点和沸点都比较高。
在标准状态下,苯酚的熔点为43℃,沸点为181℃。
苯酚的密度为1.07 g/cm3,易溶于水,而在有机溶剂中的溶解度则随着分子量的增大而增大。
二、苯酚的化学性质苯酚是一种亲电性较强的化合物,它可以和许多具有亲电性的物质发生反应。
例如,苯酚可以和卤素反应,生成卤代苯酚,同时还会伴随着氢气的放出。
苯酚还可以和酸反应,生成苯酚钠,同时也会放出氢气。
苯酚变色试剂也是化学实验中常用的试剂,它可以和苯酚发生颜色反应,从而用于检测苯酚的存在。
另外,苯酚的稳定性较低,容易被氧化,因此在保存和使用时需要注意防止暴露在空气中。
三、苯酚的制备方法苯酚的制备方法有多种,其中最常见的是通过苯的氧化反应来制备苯酚。
这个反应需要使用到一定的催化剂和氧化剂,反应条件和反应物的比例对反应产物的生成也会有影响。
以过氧化氢和苯为反应物,用钼酸铵做催化剂,可以得到苯酚。
反应的化学方程式如下:C6H6 + H2O2 → C6H5OH + H2O四、苯酚的应用由于苯酚具有抗菌、消毒、止痛等功效,因此在医学领域中有着广泛的应用。
例如,苯酚可以作为局麻药的添加剂,用于减少局部刺痛感;同时也可以作为外科手术前的皮肤消毒剂等。
除此之外,苯酚在工业界中也有着重要的应用,例如可以作为制造某些化学品的原料,或者用来制造防止污染的防腐剂等。
总的来说,苯酚是一种非常重要的有机化合物,在高中化学学习中也是一个重要的知识点。
通过深入了解苯酚的物理性质、化学性质、制备方法以及应用,可以帮助我们更好地理解化学反应和化学原理的工作原理。
苯酚的结构与性质

定期检查身体
长期接触苯酚的工作人员应定期进 行身体检查,发现异常及时就医。
储存注意事项
苯酚应储存于阴凉、通风良好的地 方,远离火源和热源,避免阳光直 射。
THANKS FOR WATCHING
感谢您的观看
对环境的危害
01
02
03
水体污染
苯酚泄露至水体中可导致 水生生物中毒死亡,破坏 水体生态平衡。
土壤污染
苯酚渗入土壤后难以降解, 对土壤结构、肥力产生不 良影响。
大气污染
苯酚挥发至大气中可形成 有害气体,影响大气环境 质量。
安全措施与储存
佩戴防护用品
在接触苯酚时,应佩戴化学防护 眼镜、化学防护服、化学防护手
05 苯酚的危害与安全措施
对人体的危害
急性毒性
致癌性
苯酚具有强烈的刺激性,接触后可引 起皮肤、眼睛、呼吸道刺激症状,严 重者可发生化学性肺炎、肺水肿。
苯酚在动物实验中已被证实具有致癌 作用,长期接触苯酚可能增加患癌症 的风险。
慢性毒性
长期低浓度接触苯酚可能导致皮肤、 肝、肾等器官的损害,如皮肤色素沉 着、肝肾功能异常等。
味道
苯酚是有毒的,不能用于食品添加剂 ,因此没有味道。
溶解性
溶解性
苯酚易溶于有机溶剂如乙醇、乙醚等,也能溶于热水。在水中溶解度较小,仅 能溶于4.3%的水。
溶解度参数
苯酚的溶解度参数约为12.7 (J/cm^3)^0.5,表明其具有一定的极性。
03 苯酚的化学性质
酸性
酚羟基的酸性
苯酚是一种弱酸,其酸性主要来源于酚羟基。酚羟基的酸性比 醇羟基强,因为酚羟基中的氧原子与苯环形成了p-π共轭,使得 氧原子上的电子密度降低,增强了氧原子对氢离子的吸引力。
苯酚-MSDS

苯酚-MSDS概述苯酚,化学式C6H6O,是一种无色结晶固体。
它具有香味并可溶于水。
苯酚常用作杀菌剂、溶剂和防腐剂。
本文档将提供苯酚的MSDS(材料安全数据表)。
物理性质- 外观:无色结晶固体- 沸点:182 °C- 熔点:41 °C- 密度:1.07 g/cm³- 溶解性:可溶于水健康和安全信息苯酚具有一定的毒性,接触或吸入过量可能对人体造成危害。
以下是一些关于苯酚的健康和安全信息:吸入苯酚的蒸气或粉尘可能对呼吸系统产生刺激作用。
如果吸入过量,可能导致头痛、头晕和恶心。
确保在通风良好的环境下使用苯酚。
接触接触苯酚可能对皮肤和眼睛产生刺激作用。
应尽量避免接触苯酚,如不慎接触,立即用大量清水冲洗受影响区域并寻求医疗援助。
食入苯酚具有毒性,食入苯酚可能导致中毒。
如果误食苯酚,应立即漱口并寻求医疗援助。
灭火措施苯酚可燃,遇到明火时可能发生燃烧。
如果发生火灾,应采取以下措施:- 使用干粉灭火剂、二氧化碳或泡沫灭火器进行灭火。
- 避免使用水直接灭火,以避免有害气体和化学反应的发生。
废弃物处理苯酚被认为是危险废物。
在处理过程中,应遵循当地法规,并采取适当的措施进行废弃物处理。
请注意,本文档提供的信息仅供参考,根据特定需求和场景,可能需要进一步的安全和健康措施。
在使用苯酚或处理苯酚时,请始终遵循当地法规,并向相关专业人士寻求建议和指导。
> 注意:本文档根据最新的可靠信息编写,但不能保证其准确性和完整性。
请在使用苯酚之前,务必查阅最新的MSDS和相关文件,并与可信赖的数据源核实上述提供的信息。
参考。
苯酚的课件

苯酚的熔点为100.4℃,沸点为181.7℃。 苯酚具有弱酸性,可以与碱反应生成盐。
苯酚的化学性质
苯酚可以与甲醛、乙酸等物质发生缩 聚反应,生成酚醛树脂和酚酯树脂等 高分子化合物。
苯酚可以与羧酸发生酯化反应,生成 酯类物质。
苯酚可以与金属钠、钾等活泼金属发 生置换反应,生成苯酚盐。
苯酚可以与氯化铁等强氧化剂发生氧 化反应,生成醌类物质。
苯酚的防治
政府应加强对涉及苯酚行业的 监管力度,严格控制苯酚的排
放标准。
替代品研发
鼓励和支持企业研发苯酚的替 代品,减少生产和使用过程中
的苯酚排放。
公众教育
提高公众对苯酚危害的认识, 倡导绿色环保的生活方式。
应急处理
建立苯酚污染应急处理机制, 及时处理突发事故,减轻对环
苯酚可用于合成植物生长调节剂,如 赤霉素等。
合成除草剂
苯酚可用于合成选择性除草剂,如草 甘膦等。
苯酚在其他领域的应用
高分子材料
苯酚可用于合成酚醛树脂 、环氧树脂等高分子材料 ,广泛应用于建筑、汽车 、电子等领域。
染料
苯酚可用于合成染料,如 酸性染料、直接染料等。
化学工业
苯酚可用于合成多种有机 化合物,如醚类、酯类等 ,广泛应用于化学工业。
两种方法相比较,异丙苯法具有工艺成熟、原料易得、产品质量好等优点,因此是目前国内外生产苯酚的主要方法。而苯酐 加氢法则由于原料来源受限、工艺流程长、能耗高等缺点,较少采用。
苯酚的生产原料
苯酚的生产原料主要包括苯、丙烯、邻苯二甲酸酐和氢气等 。其中,苯是最主要的原料之一,丙烯则是用来合成异丙苯 的原料。邻苯二甲酸酐与氢气反应生成苯酚和丙酮,也是生 产苯酚的一种方法。
的风险。
苯酚的化学性质

在农药领域的应用
除草剂
苯酚可以作为除草剂的合成原料,如草甘膦等。
杀虫剂
苯酚可以用于制作杀虫剂,如有机磷农药等。
杀菌剂
苯酚可以用于制作杀菌苯酚可以与其他物质反应合成酚醛树脂等合成树脂,用于制造塑料、涂料等。
合成纤维
苯酚可以与其他物质反应合成纤维,如尼龙等。
大气污染
03
苯酚挥发到大气中可参与光化学反应,加剧空气污染。
苯酚的防护措施
01
02
03
04
穿戴防护服
在接触苯酚时应穿戴化学防护 服、化学防护眼镜和化学防护
手套。
保持通风
在操作苯酚时,应保持良好通 风,降低空气中苯酚浓度。
使用个人防护用品
应使用个人防护用品,如化学 防护眼镜、化学防护口罩和化
学防护手套等。
苯胺和亚硝酸反应生成重氮盐, 重氮盐再与水反应生成苯酚。
该方法需要使用重氮化试剂和还 原剂,操作较为复杂,但可以获
得高纯度的苯酚。
04
苯酚的应用
在医药领域的应用
抗菌剂
苯酚是常用的抗菌剂,可用于手术器械、注射器 等医疗器械的消毒。
药物合成
苯酚是许多药物合成的中间体,如阿司匹林、布 洛芬等。
防腐剂
苯酚可用于制作防腐剂,如苯酚钠盐,用于食品、 药品等的防腐。
呼吸道刺激
吸入苯酚蒸汽可能导致呼吸道 刺激症状,如咳嗽、呼吸困难 和喉咙疼痛。
消化系统损害
误食苯酚可能导致口腔、咽喉、食 管和胃的腐蚀性损害,引起口腔溃
疡、吞咽困难和胃出血等症状。
苯酚对环境的危害
水体污染
01
苯酚排放到水体中可导致水生生物受到毒害,破坏水生态平衡。
土壤污染
化学苯酚的知识点总结

化学苯酚的知识点总结
1. 化学性质:
苯酚是一种易氧化的有机化合物,当暴露在空气中时会逐渐氧化成苯醛和苯甲酸。
它在酸性溶液中可以被氧化成喹啉醌,这也是制备染料和颜料的重要步骤之一。
2. 物理性质:
苯酚是一种无色至白色的结晶性固体,有特殊的酚味。
它在水中微溶,在乙醇、乙醚等有机溶剂中溶解度较大。
苯酚可以形成由氢键连接的分子聚合体,这使得它在溶液中有着较高的凝聚性。
3. 合成方法:
苯酚可以从苯乙烯或苯的氧化反应中得到。
一种常用的合成方法是将苯烯与过氧化氢一起在氧化铜催化剂的条件下反应,得到苯酚。
苯酚也可以通过碳酸盐的加成反应得到,这是一种重要的工业合成方法。
4. 应用:
苯酚在医药和化工行业有着广泛的应用。
它是一种重要的消毒剂,能够杀灭细菌和真菌。
苯酚也被用作防腐剂,能够延长一些产品的保质期。
在有机合成中,苯酚也是一种重要的中间体,可以用于合成染料和香料等化合物。
总的来说,苯酚作为一种重要的有机化合物,在工业和科学研究领域有着广泛的应用。
它的独特性质使得它成为一种不可或缺的化工原料,对于推动化学工业的发展起着重要的作用。
苯酚

苯酚苯酚苯酚(C6H6O,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。
常温下为一种无色晶体。
有毒。
有腐蚀性,常温下微溶于水,易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶,其溶液沾到皮肤上用酒精洗涤。
暴露在空气中呈粉红色。
基本介绍苯酚是一种常见的化学品,是生产某些树脂、杀菌剂、防腐剂以及药物的重要原料。
是一种电解质。
【中文名称】苯酚;石炭酸【英文名称】phenol【分子式】 C6H6O分子量:94.11所有C原子均以sp2杂化轨道形成σ键,O原子以sp2杂化轨道形成σ键,剩余p轨道与苯环的大π键进行共轭。
现代量子理论和现代测试技术表明:苯分子高度对称,12个原子处于同一平面内。
六元环是等边的;6个碳碳键完全相同,键长比普通单键短,比普通双键长。
【相对分子量或原子量】94.11 【密度】1.071 【熔点(℃)】42~43【沸点(℃)】182 【折射率】1.5425(41)【毒性LD50(mg/kg)】大鼠经口530。
【性状】无色或白色晶体,有特殊气味。
【溶解情况】溶于乙醇、乙醚、氯仿、甘油、二硫化碳等。
易溶于有机溶液,常温下微溶于水,当温度高于70℃时,能跟水以任意比例互溶。
物理性质性状无色针状结晶或白色结晶熔块。
瓶口的苯酚显粉红色,原因是被空气中的氧气氧化。
有特殊的臭味和燃烧味,极稀的溶液具有甜味。
熔点43℃沸点181.7℃凝固点41℃相对密度 1.0576 折射率 1.54178 闪点79.5℃溶解性在水中溶解性不大,但当温度高于70°C时,则能与水混容。
易溶于乙醇、乙醚、氯仿、甘油、二硫化碳、凡士林、挥发油、固定油、强碱水溶液。
几乎不溶于石油醚。
储存管理要求储存于阴凉、通风的库房。
远离火种、热源。
避免光照。
库温不超过30℃,相对湿度不超过70%。
包装密封。
应与氧化剂、酸类、碱类、食用化学品分开存放,切忌混储。
配备相应品种和数量的消防器材。
储区应备有合适的材料收容泄漏物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、物质的理化常数
CA
国标编号: 61067
108-95-2
S:
中文名称: 苯酚
英文名称: phenol;carbolic acid
别名: 酚;石炭酸
分子
分子式: C6H6O;C6H5OH
94.11
量:
熔点: 40.6℃ 沸点:181.9℃
密度: 相对密度(水=1)1.07;
蒸汽压: 79℃
溶解性: 可混溶于乙醇、醚、氯仿、甘油
稳定性: 稳定
外观与性
白色结晶,有特殊气味
状:
危险标记: 14(有毒品)
用作生产酚醛树脂、卡普隆和己二酸的原料,也用于
用途:
塑料和医药工业
2.对环境的影响:
一、健康危害
侵入途径:吸入、食入、经皮吸收。
健康危害:苯酚对皮肤、粘膜有强烈的腐蚀作用,可抑制中枢神经或损害肝、肾功能。
急性中毒:吸入高浓度蒸气可致头痛、头晕、乏力、视物模糊、肺水肿等。
误服引起消化道灼伤,出现烧灼痛,呼出气带酚味,呕吐物或大便可带血液,有胃肠穿孔的可能,可出现休克、肺水肿、肝或肾损害,出现急性肾功能衰竭,可死于呼吸衰竭。
眼接触可致灼伤。
可经灼伤皮肤吸收经一定潜伏期后引起急性肾功能衰竭。
慢性中毒:可引起头痛、头晕、咳嗽、食欲减退、恶心、呕吐,严重者引起蛋白尿。
可致皮炎。
二、毒理学资料及环境行为
毒性:属高毒类。
急性毒性:LD50317mg/kg(大鼠经口);850mg/kg(兔经皮);LC50316mg/m3(大鼠吸入);人经口
1000mg/kg,致死剂量。
刺激性:家兔经眼:20mg(24小时),中度刺激。
家兔经皮:500mg(24小时),中度刺激。
亚急性和慢性毒性:动物长期吸入酚蒸气(115.2-230.4mg/m3)可引起呼吸困难、肺损害、体重减轻和瘫痪。
致突变性:DNA抑制:人Hela细胞1mmol/L。
姊妹染色单体交换:人淋巴细胞5μmol/L。
生殖毒性:大鼠经口最低中毒剂量(TDL0):1200mg/kg(孕6-15天),引起胚胎毒性。
致癌性:小鼠经皮最低中毒剂量(TDL0):16g/kg,40周(间歇),致癌,皮肤肿瘤。
污染来源:苯酚用于生产或制造炸药、肥料、焦炭、照明气、灯黑、涂料、除涂剂、橡胶、石棉品、木材防腐剂、合成树脂、纺织物、药品、药物制剂、香水、酚醛塑料和其它塑料,以及聚合物的中间体。
也可在石油、制革、造纸、肥皂、玩具、墨水、农药、香料、染料等行业中使用。
在医药上用作消毒剂、杀虫剂、止痒剂等。
在实验室中用作溶剂、试剂。
酚类化合物在微生物和光解的作用下,在环境中分解较快。
研究结果表明,在夏季4小时之内酚的浓度可以从125ppb下降到10ppb以下,而这种酚的降解速度随着河水中微生物数量的增加而增加,在冬季最冷的天气里,酚的降解速率则很弱。
另外,酚的降解速率与水中溶解氧量成正比,酚的生物富集程度很低。
苯酚对人体任何组织都有显著腐蚀作用。
如接触眼,能引起角膜严重损害,甚至失明。
接触皮肤后,不引起疼痛,但在暴露部位最初呈现白色,如不迅速冲洗清除,能引起严重灼伤或全身性中毒。
苯酚为细腻原浆毒物,能使蛋白质发生变质和沉淀,故对各种细胞有直接损害。
因此,任何暴露途径都可能产生全身性影响。
通常酚中毒主要由皮肤吸收所引起,其腐蚀性随液体的pH值、溶解性及分解度和温度等条件而异。
危险特性:遇明火、高热或与氧化剂接触有引起燃烧爆炸的危险。
燃烧(分解)产物:一氧化碳、二氧化碳。
3.现场应急监测方法:
快速检测管法;便携式气相色谱法《突发性环境污染事故应急监测与处理处置技术》万本太主编
直接进水样气相色谱法
气体速测管(德国德尔格公司产品)
4.实验室监测方法:
5.环境标准:
6.应急处理处置方法:
一、泄漏应急处理
隔离泄漏污染区,限制出入。
切断火源。
建议应急处理人员戴自给式呼吸器,穿防毒服。
小量泄漏:用干石灰、苏打灰覆盖。
大量泄漏:收集回收或运至废物处理场所处置。
⑴水体被污染的情况主要有:水体沿岸上游污染源的事故排放;陆地事故(如交通运输过程中的翻车事故)发生后经土壤流入水体,也有槽罐直接翻入路边水体的情况。
可按以下方法处理:
①查明水体沿岸排放废水的污染源,阻止其继续向水体排污。
②如果是液体苯酚的槽车发生交通事故,应设法堵住裂缝,或迅速筑一道土堤拦住液流;如果是在平地,应围绕泄漏地区筑隔离堤;如果泄漏发生在斜坡上,则可沿污染物流动路线,在斜坡的下方筑拦液堤。
在某些情况下,在液体流动的下方迅速挖一个坑也可以达到阻载泄漏的污染物的同样效果。
③在拦液堤或拦液坑内收集到的液体须尽快移到安全密封的容器内操作时采取必要的安全保护措施。
④已进入水体中的液体或固体苯酚处理较困难,通常采用适当措施将被污染水体与其它水体隔离之手段,如可在较小的河流上筑坝将其拦住,将被污染的水抽排到其它水体或污水处理厂。
⑵土壤污染的主要情况有各种高浓度废水(包括液体苯酚)直接污染土壤,固体苯酚由于事故倾洒在土壤中。
①固体苯酚污染土壤的处理方法较为简单,使用简单工具将其收集至容器中,视情况决定是否要将表层土剥离作焚烧处理。
②液体苯酚污染土壤时,应迅速设法制止其流动,包括筑堤、挖坑等措施,以防止污染面扩大或进一步污染水体。
③最为广泛应用的方法是使用机械清除被污染土壤并在安全区进行处置,如焚烧。
④如环境不允许大量挖掘和清除土壤时,可使用物理、化学和生物方法消除污染。
如对地表乾封闭处理;地下水位高的地方采用注水法使水位上升,收集从地表溢出的水;让土壤保持休闲或通过翻耕以促进苯酚蒸发的自然降解法等等。
二、防护措施
呼吸系统防护:可能接触其粉尘时,佩戴自吸过滤式防尘口罩。
紧急事态抢救或撤离时,应该佩戴
自给式呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿透气型防毒服。
手防护:戴防化学品手套。
其它:工作现场禁止吸烟、进食和饮水。
工作毕,淋浴更衣。
单独存放被毒物污染的衣服,洗后备用。
保持良好的卫生习惯。
三、急救措施
皮肤接触:立即脱去被污染的衣着,用甘油、聚乙烯乙二醇或聚乙烯乙二醇和酒精混合液(7:3)抹洗,然后用水彻底清洗。
或用大量流动清水冲洗,至少15分钟。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:立即给饮植物油15-30mL。
催吐。
就医。
灭火方法:消防人员须佩戴防毒面具、穿全身消防服。
灭火剂:水、抗溶性泡沫、干粉、二氧化碳。
