化学知识结构框图(超详细)
化学知识结构框图(超详细)
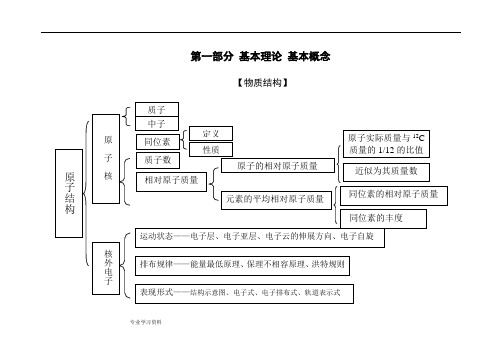
. 专业学习资料 .第一部分 基本理论 基本概念【物质结构】. 专业学习资料.晶体结构. 专业学习资料.晶体熔沸点比较表. 专业学习资料.【元素周期律】. 专业学习资料.【化学反应速率与化学平衡】. 专业学习资料.. 专业学习资料.. 专业学习资料... . .. . ... 专业学习资料 .【胶体】【电解质溶液】.. 专业学习资料.. 专业学习资料.【氧化还原反应电化学】. 专业学习资料.【各种化学反应的关系】. 专业学习资料..专业学习资料.【化学反应规律】. 专业学习资料.. 专业学习资料.. 专业学习资料 .【物质的量】nVV n m =→nm M =Vn C =nN N A =M=a 1%·M 1+ a 2%·M 2+…(a%为体积分数). 专业学习资料..第二部分 元素及其化合物【元素化合物概述】【非金属元素】. 专业学习资料.【卤族元素】. 专业学习资料.PbS. 专业学习资料.. 专业学习资料... . .. . ... 专业学习资料 .【金属元素】.. . .. . ..【铝及其化合物】. 专业学习资料.. 专业学习资料.. 专业学习资料.【化工生产】. 专业学习资料.第三部分 有机物【有机物导学】[有机物推断]浓H2SO4加热苯的硝化醇分子内、间脱水酯化光照——烷基卤代[官能团特征反应]聚酯反应类型与官能团的关系官能团(或物质)的特征反应[各类有机物之间的相互关系]2 =CH 2CH 3 —CH 3 CH CH CH 2 O HCH 3 CH 3 C H 2 C lCH 2 CH 2 Cl CH C HO CHClCH 2-CH NH 2n2HOCH 2 CH 2OHCH 3 C OOHCH 3 C OO CH 2 CH 3第四部分 化学实验导学[物质的分离和提纯][物质的检验][常见气体的实验室制法]第五部分 化学计算。
初中化学1至12单元知识框架图(全)(打印)

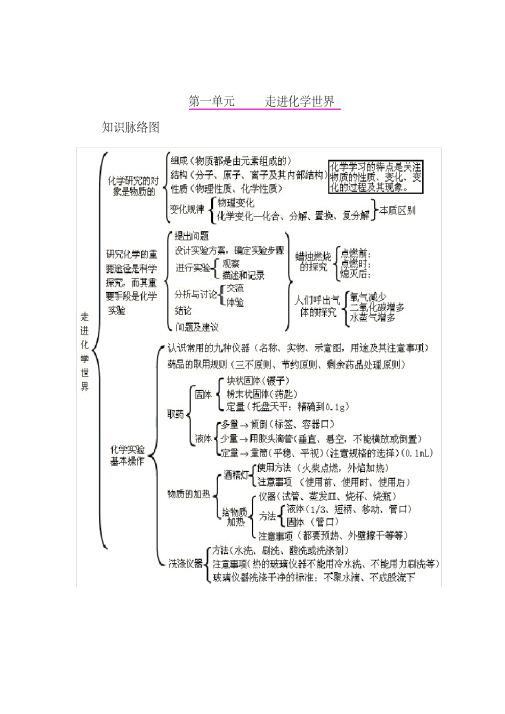
第一单元 走进化学世界f 育法(水洗、刷洗、酸洗或洗涤剂)洗涤仪器彳注意事项(热的玻璃仪器不能用冷水i 总 不能用力刷洗等〉I 玻璃仪器洗涤干净的标准:不聚水辖U 不成股流下1锅炉爆炸、轮胎爆炸是物理变化,可燃性物质导致的爆炸是化学变化,如氢气爆炸,烟花爆炸等。
2、 催化剂能加快和减慢反应速率,其质量和化学性质反应前后不变,物理性质,如形状、状态可能改 变 3、 由一种元素组成的物质可能为单质,也可能为混合物。
如氧气02和臭氧03两种单质混合得到混合物,也只由氧(O )元素组成。
金刚石C 和石墨C 的混合物,只由碳(C )元素组成等。
只有说由一种元素 组成的纯净物,才能说一定是单质。
冰水混合物是纯净物,冰是水的固态,还是水。
优学研究的对象是物质的 组成(物质都是由元素组成的〉结构(分子、原子、离子及其商部结构) 〈性质(物理性质、化学隍质)变化规律r 物理变化[化学变化一k 合、分摒、置换、复分解}本质区别走 进 化 学 世 界硏究化学的重 要途径是科学 探究,而其重 要r提出间題设计实验有案.确定貓歩骤 迸行实验・ 分析与讨论* 结论I 间题及建议r 观察1摊述和记录交赢 体■验J 占嵌时.、、体的探究峙二氧化碳增多 水蒸气增多/认识常用的九种仪器(名称、实物、示宜图,用途及其注言事项〉 药品的取用规则(三不原则、节约J®则、剩余葯品处理原则)取药&化学实验J基耳操作%. 「块状固您(辍子)固体・粉耒状固悴(药匙)L 定量(托盘天平:精确到0*1或「多壘-倾倒(:标签,容器口)襪体{少壘T 用胶头滴管〔垂宜、悬空,不能横放或倒置) ' L 定堇一壘筒(平稳、平视)(注意规格的选择)(0. ImL )「使用右法〔火柴点燃,外焰加热〉 I 注意車项〔使用前、使用时、使用后〉 「仪器■(试管、葵发皿、烧杯、烧瓶) 、吐J 液体茨短柄、移动、管口) 万京1固体(管口)I 注意事项(都要预热、外壁擦干等等)广酒周丁 物I 质的加热J4、原子是化学变化中的最小粒子。
化学知识结构框图(超详细)!
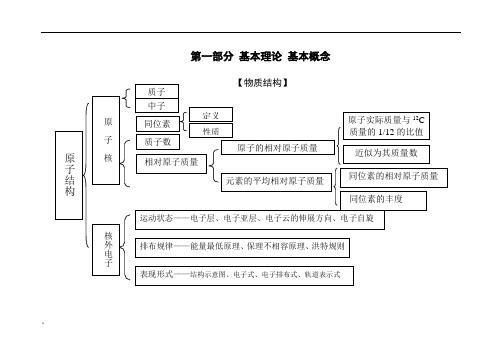
第一部分 基本理论 基本概念晶体结构晶体熔沸点比较表【元素周期律】【化学反应速率与化学平衡】..【胶体】【电解质溶液】【氧化还原反应电化学】【各种化学反应的关系】【化学反应规律】【物质的量】nVV n m =→nm M =Vn C =nN N A =M=a 1%·M 1+ a 2%·M 2+…(a%为体积分数)第二部分元素及其化合物【元素化合物概述】【非金属元素】【卤族元素】PbS....【金属元素】【铝及其化合物】【化工生产】第三部分 有机物 【有机物导学】[有机物推断]浓H 2SO 4加热 苯的硝化 醇分子内、间脱水 酯 化 稀H 2SO 4加热 酯的水解 糖类水解 NaOH 水溶液加热 酯的水解 卤代烃的水解 NaOH 醇溶液加热—卤代烃消去 Cu 、加热—醇的氧化 脱水 醇的消去、羟基间脱水 羧基间脱水 羟基与羧基间脱链酯 环酯 光照——烷基卤代 [官能团特征反应] 聚酯反应类型与官能团的关系官能团(或物质)的特征反应[各类有机物之间的相互关系]2 =CH 2CH 3 —CH 3CH CH CH 2 O HCH 3 CH 3 C H 2 C lCH 2 CH 2 Cl CH C HO CHClCH 2-CH NH 2n22HOCH 2 CH 2OHCH 3 C OOHCH 3 C OO CH 2 CH 3第四部分 化学实验导学[物质的分离和提纯][物质的检验][常见气体的实验室制法]第五部分 化学计算。
(完整)高中化学知识结构图
决 定
外 电 子
表 律 的排
结
周布
构
期周
离 子
性期 性
晶
体
横:周期 元素种类
起止序号
n=1
2
1~2
n=2
8
短周期
3~10
元素性质
n=3
8
11~18
周
原
n=4
18
19~36
n=5
18 长周期
37~54
期 表 位
子 结 构
n=6
32
55~86
置
n=7
21 不完全周期 87~111
纵:族
主族:ⅠA~ⅦA
副族:ⅢB~ⅦB、ⅠB ⅡB
原子晶体 石墨(混合晶体)
金属晶体 大多数盐
强 碱 离子晶体 碱性氧化物 部分过氧化物
物理性质 宏观
化学性质 纯净物
单质 化合物
非金属 稀有气体
组成
分类
性质
物质 分 子
变化
原 子 微观
离 子
无机物 氢化物
氧化物
有机物
金属氢化物
酸性
非金属氢化物
碱性
成盐氧化物
两性
特殊
不成盐氧化物
含氧酸、无氧酸
酸
强酸、弱酸
电离度平衡的移动
质离 ) 水的电离平衡 H2O H++OH-
水的离子积 KW=1×10-14(25℃) 溶液的酸碱性:PH=-log[H+]
装置
离子反应
实质
发生条件 表示方式-离子方程式
盐类的水解
常见类型
非氧化还原
复分解反应 水解反应 络合反应
类型 规律(酸碱性性判断) 影响因素
初中化学各单元知识点框架图

初中化学各单元知识点框架图work Information Technology Company.2020YEAR初中化学各单元知识点框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料第九单元溶液第十单元 酸、碱、盐(一)化学用语1电离方程式:-++=24422SO H SO H ;-++=OH Na NaOH ;-++=24334232)(SO Al SO Al2物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO 3;食盐的主要成分NaCl ;纯碱、口碱Na 2CO 3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾CuSO 4·5H 2O ;碳酸钠晶体Na 2CO 3·10H 2O ;氨水NH 3·H 2O 。
(二)金属活动性 1金属活动性顺序:K >Ca >Na >Mg >Al >Zn >Fe >Sn >Pb(H)Cu >Hg >Ag >Pt >Au 2金属活动性顺序的意义:在金属活动顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失去电子而变成离子,它的活动性就越强。
3金属活动性顺序的应用:⑴排在氢前的金属能置换出酸里的氢(元素)。
⑵排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
(三)酸、碱、盐的溶解性1常见盐与碱的溶解性钾(盐)、钠(盐)铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2八个常见的沉淀物氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁 3四微溶物Ca(OH)2(石灰水注明:澄清“的原因)CaSO 4(实验室制二氧化碳时不用稀硫酸的原因)Ag 2SO 4(鉴别-24SO 和-Cl 时,不用硝酸银的原因)MgCO 3(碳酸根离子不能用于在溶液中除去镁离子的原因)4三个不存在的物质氢氧化银、碳酸铝、碳酸铁(四)复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO 3、NaNO 3、AgNO 3、BaSO 4不能做复分解反应的反应物。
初中化学各单元知识框架图(全)

小屯一中化学复习计划第一单元走进化学世界1、锅炉爆炸、轮胎爆炸是物理变化,可燃性物质导致的爆炸是化学变化,如氢气爆炸,烟花爆炸等。
2、催化剂能加快和减慢反应速率,其质量和化学性质反应前后不变,物理性质,如形状、状态可能改变3、由一种元素组成的物质可能为单质,也可能为混合物。
如氧气O2和臭氧O3两种单质混合得到混合物,也只由氧(O)元素组成。
金刚石C和石墨C的混合物,只由碳(C)元素组成等。
只有说由一种元素组成的纯净物,才能说一定是单质。
冰水混合物是纯净物,冰是水的固态,还是水。
4、原子是化学变化中的最小粒子。
但不能说原子一定就比分子小。
原子是化学变化中的最小粒子,在化学变化中不可再分。
但是某些物理变化中是可再分(核裂变)的第二单元我们周围的空气测氧气含量实验失败原因:红磷量不足,装置漏气,未等到装置冷却就打开弹簧夹不是所有的燃烧都需氧气参与。
如氢气在氯气中能燃烧。
着火点是物质的固有属性,不能说降低物质的着火点,只能说把温度升高到物质的着火点。
燃烧需三个条件都具备,灭火只要破坏任一条件。
第三单元自然界的水沉淀有静置沉淀和吸附沉淀。
吸附沉淀是指加明矾生成胶体吸附大颗粒固体杂质,获得比静置沉淀更快的沉淀。
过滤是在沉淀后,把不溶于水的沉淀和水分离的操作。
若单独提到吸附,则是指加活性炭吸附色素和气体。
蒸馏后得到的水净化程度最高,为蒸馏水,是纯净物。
蒸馏操作可以使硬水软化第四单元物质构成的奥秘原子团的记忆找诀窍:如碳酸根CO3,就是二氧化碳CO2多1个O。
硫酸根SO4,是三氧化硫SO3多1个O。
硝酸根NO3,是二氧化氮NO2多1个O。
铵根NH4,是氨气NH3多1个O.第五单元化学方程式1、如点燃A克氧气和B克氢气的混合气体,生成水的质量是小于或等于(A+B)克。
氧气和氢气要么恰好按质量比完全反应,都不剩余,则生成水质量等于(A+B)克。
要么,氢气过量剩余或者氧气过量剩余,有一种没有全部反应,则生成水质量小于(A+B)克。
化学知识结构框图(超详细)!

化学知识结构框图(超详细)!第一部分基本理论基本概念质子和中子是构成原子核的基本粒子。
物质结构指的是物质的构成方式,包括原子的相对原子质量、原同位素、质子数等概念。
原子的相对原子质量可以近似看作其质量数,同位素的相对原子质量和丰度也是物质结构的重要概念。
原子的结构包括核和核外电子。
电子排布规律包括能量最低原理、保里不相容原理和洪特规则,可以用结构示意图、电子式、电子排布式和轨道表示式等形式表现。
化学键是化合物形成的基础。
极性共价键和非极性共价键是常见的两种共价键类型。
离子键和金属键也是化合物中常见的键类型。
晶体结构包括分子晶体、离子晶体、原子晶体和金属晶体。
元素周期律是元素周期性变化的规律。
周期表的结构包括短周期、周期长周期和不完全周期。
元素周期律可以用来预测元素的性质,如农药、半导体、合金、催化剂、光电管等应用。
化学反应速率是指化学反应中物质消失或生成的速度。
它可以用平均速率来表示,受内因、温度等多种因素影响。
化反应中,元素守恒和电荷守恒都得到满足,但能量高的物质生成能量低的物质的作用更大,因此反应发生。
化学反应是化学变化的过程,可以分为不同类型的反应。
其中,分解反应是一种将一种物质分解成两种或更多种物质的反应,化合反应是两种或更多种物质结合成一种物质的反应,氧化还原反应是指物质的氧化产生电子,还原则是指物质的还原接受电子。
离子反应是指离子之间的反应,包括置换反应和复分解反应。
在化学反应中,有一些规律需要遵守。
电荷守恒规律指的是反应前后电荷总量不变,元素守恒规律指的是反应前后元素总量不变,溶解度规律指的是溶解度较大的物质生成溶解度较小的物质,强弱规律指的是能量高的物质生成能量低的物质。
在实际应用中,需要根据具体情况确定哪种规律影响更大,以此决定反应的发生。
氧化还原反应是一种特殊的化学反应,涉及到还原剂和氧化剂的作用。
还原剂具有还原性,可以引起氧化反应,被氧化的物质叫做还原剂。
氧化剂具有氧化性,可以引起还原反应,被还原的物质叫做氧化剂。
(完整)高中化学知识结构图

或 4OH-—4e H2O+O2↑
金属电极做阳极,电极本身被氧化 M-n氧e→化 Mn+
第三部分:元素化合物转化关系
Na2S C2H5ONa
Na2O
NaOH
NaCl
Na
Na2O2
Na2CO3
NaCl
CH3COONa
NaHCO3
N2 Mg3N2
CO2 MgO
H2O Mg(OH)2
X2 MgX2
煅烧
O2 Mg
Ⅷ族
0族
比较
类型
构成晶体微粒
形成晶体作用力
熔沸点
硬度
物 理
导电性
性 质
传热性
延展性
溶解性
典型实例
离子晶体 阴、阳离子
离子键 较高
硬而脆 不良 水熔溶融液.导电
不. 良 不良 易溶于极性溶剂
NaCl,KBr
原子晶体 原子 共价键 很高 大
绝缘体(半导体) 不良 不良
不溶于任何溶剂 单质:金刚石、SiC、
H2O MgO
Mg(OH)2
H2O MgCO3
△
HCl
△
Cl2
HCl NaOH H2O HCl
或
电解
CO2 OH-
HCl
MgCl2
Mg(HCO3)2
CaCl2 HCl Cl2 或 HCl
Na2CO3 HCl
CaCO3
HCl CO2
CO2+H2O
△
O2 Ca
CaO H2O
H3PO4 Ca(OH)2
CaHPO4
CaC2
Ca(OH)2
CaO
非金属:按照化合价寻找各类物质,主要有氢化物、
单质、氧化物、含氧酸、及其盐
初中化学知识点框架图

初中化学知识框架图第一单元走进化学世界第二单元我们四周的空气第三单元自然界的水第四单元物质组成的神秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属资料九、溶液十、酸碱盐一、化学用语1、电离方程式2、物质的俗称和主要成分:生石灰 CaO;熟石灰、消石灰、石灰水的主要成分 Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾 CuSO4.5H2O;碳酸钠晶体 Na2CO3.10H2O;氨水 NH3.H 2O;二、金属活动性1、金属活动性次序: K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性次序的意义:在金属活动性次序中,金属地点越靠前,金属在水溶液 ( 酸溶液或盐溶液 ) 中就越简单失电子而变为离子,它的活动性就越强。
3、金属活动性次序的应用:(1) 排在氢前的金属能置换出酸里的氢( 元素 ) 。
(2)排在前面的金属才能把排在后边的金属从它们的盐溶液中置换出来(K、Ca、Na 除外 ) 。
三、酸、碱、盐的溶解性1、常有盐与碱的溶解性:钾( 盐) 、钠( 盐) 、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾 ( 盐) 、钠 ( 盐) 、铵( 盐) 。
碱类物质溶解性:只有 ( 氢氧化 ) 钾、 ( 氢氧化 ) 钠、( 氢氧化 ) 钙、 ( 氢氧化 ) 钡溶。
2、八个常有的积淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2( 石灰水注明“澄清〞的原由) 、CaSO4( 实验室制二氧化碳时不用稀硫酸的原由 )Ag2SO4( 鉴识 SO42-和 Cl -时,不用硝酸银的原由 ) 、MgCO3( 碳酸根离子不可以用于在溶液中除掉镁离子的原由)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁四、复分解反应发生的条件反应:有气体、水或积淀生成( 即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只好与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应 (3)KNO、NaNO3、AgNO3、BaSO4不可以做复分解反应的反应物五、溶液的酸碱性与酸碱度的测定1、指示剂 --- 溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液 ( 特例:碳酸钠的水溶液显碱性)2、pH值--- 溶液的酸碱度: pH<7溶液为酸性 ( 越小酸性越强 ) ;ph=7 溶液为中性;ph>7 溶液为碱性 ( 越大碱性越强 )六、离子的查验Cl - ( 在溶液中 )---在被测溶液中参加硝酸银溶液, 假如生成不溶于硝酸的白色沉淀,那么原被测液中含氯离子。
(完整)高中化学知识结构图.doc
2n
物
物
及
云
素
响
个
2
合
个
个
实
周
物
金
期
理
质
律
性
质
表
元
元
元
核
晶
示
方
素
编素
归
素
外
体
决
制
类
结构简图
法
周
周纳
性
定
电
型
表
期
期
质
子
表
律
的
排
的
电子式
结
周
布
构
期
周
金
分
原
离
性
期
性
属
子
子
子
晶
晶
晶
晶
横:周期
元素种类
体
体
体
体
起止序号
n=1
2
短周期
1~2
n=2
8
3~10
元素性质
n=3
8
11~18
周
原
n=4
18
19~36
期
子
等于 反 方程式的系数比
化
内因(主)
反 物的 构、性
学
化
影响因素
度
反
学
学
平
反
用
速
衡
率
温度
和
的 合
外因( )
化
成
催化
氨
其他条件
光、超声
适
化
于
波、激光、放射 ⋯
条
可逆反
纯干货:初中化学各单元知识框架图(收藏)

纯干货:初中化学各单元知识框架图(收藏)第一单元:走进化学世界第二单元:我们周围的空气第三单元:自然界的水第四单元:物质构成的奥秘第五单元:化学方程式第六单元:碳和碳的氧化物第七单元:燃料及其利用第八单元:金属和金属材料第九单元:溶液第十单元:酸碱盐1化学用语1、电离方程式:2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O;3、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O。
2金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
3酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁4复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物。
(完整版)初中化学各单元知识框架图
2 、溶液 ( 多为无色 ) 浅绿色溶液 ---( 亚铁盐溶液 )FeCl2
溶液、 FeSO4 溶液黄色溶液 --- ( 铁盐溶液 )FeCl3
溶液、 Fe2(SO4)3 溶液、 Fe(NO3)3
溶液蓝色溶液 ---( 铜盐溶液 )CuCl2
溶液、 CuSO4 溶液、 Cu(NO3)2 溶液蓝绿色溶液 -CuCl2
溶质的 质量分数
不饱和溶液
饱和溶液 结晶
溶解度
十、酸 碱 盐 氧化物、酸、碱和盐的知识点可以从以下十个方面掌握: 一、化学用语 1、电离方程式
H 2 SO4 2 H SO42 ; NaOH Na OH ; Al 2 ( SO4 ) 3 2Al 3 3SO42
2、物质的俗称和主要成分生石灰 ??CaO熟石灰、消石灰、 石灰水的主要成分 ??Ca(OH)2石灰石、大理石 ??CaCO3食盐的主 要成分 ??NaCl 纯碱、口碱 ??Na2CO3烧碱、火碱、苛性钠 ??NaOH 胆矾、蓝矾 ??CuSO4.5H2O碳酸钠晶体 ??Na2CO3.10H2O氨 水 ??NH3.H2O
(2) 碱能与酸性氧化物反应生成盐和水 (3) 碱能与酸反应生成盐和水 (4) 某些碱能与某些盐反应生成新的盐和新的碱 3、盐的性质 (1) 某些盐能与较活泼的金属反应生成新的盐和金属 (2) 某些盐能与酸反应生成新的盐和新的酸 (3) 某些盐能与某些碱反应生成新的盐和新的碱 (4) 有些不同的盐之间能反应生成两种新的盐
六、溶液的酸碱性与酸碱度的测定 1、指示剂 --- 溶液的酸碱性紫色的石蕊试液遇酸性溶液变 红;遇碱性溶液变蓝 无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作 用碱性溶液不一定是碱的溶液 ( 特例:碳酸钠的水溶液显碱性 ) 2、pH值 --- 溶液的酸碱度 pH>7溶液为酸性 ( 越小酸性越 强)pH=7 溶液为中性 pH<7溶液为碱性 ( 越大碱性越强 ) 七、离子的检验 Cl-( 在溶液中 )--- 在被测溶液中加入硝酸银溶液 , 如果生成 不溶于硝酸的白色沉淀,则原被测液中含氯离子。 SO42-(在溶液中 )--- 在被测溶液中加入氯化钡 ( 或硝酸钡、 或氢氧化钡 ) 溶液,如果生成不溶于硝酸 ( 或盐酸 ) 的白色沉淀, 则原被测液中含硫酸根离子。 CO32-(1)( 固体或溶液 )--- 在被测物质中加入稀酸溶液,如 果产生能使澄清石灰水变浑浊的气体,则原被测物质中含碳酸 根离子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
. 专业学习资料 .
第一部分 基本理论 基本概念
【物质结构】
. 专业学习资料.
晶体结构
. 专业学习资料.
晶体熔沸点比较表
. 专业学习资料.
【元素周期律】
. 专业学习资料.
【化学反应速率与化学平衡】. 专业学习资料.
. 专业学习资料
.
. 专业学习资料.
.. . .. . ..
. 专业学习资料 .
【胶体】
【电解质溶液】
.
. 专业学习资料.
. 专业学习资料.
【氧化还原反应电化学】
. 专业学习资料.
【各种化学反应的关系】
. 专业学习资料.
.
专业学习资料.
【化学反应规律】
. 专业学习资料.
. 专业学习资料.
. 专业学习资料 .
【物质的量】
n
V
V n m =
→n
m M =
V
n C =
n
N N A =
M=a 1%·M 1+ a 2%·M 2+…(a%为体积分数)
. 专业学习资料.
.
第二部分 元素及其化合物
【元素化合物概述】
【非金属元素】
. 专业学习资料.
【卤族元素】
. 专业学习资料.
PbS
. 专业学习资料.
. 专业学习资料.
.. . .. . ..
. 专业学习资料 .
【金属元素】
.. . .. . ..
【铝及其化合物】
. 专业学习资料.
. 专业学习资料.
. 专业学习资料.
【化工生产
】
. 专业学习资料.
第三部分 有机物
【有机物导学】
[有机物推断]
浓H2SO4加热苯的硝化
醇分子内、间脱水酯化
光照——烷基卤代
[官能团特征反应]
聚酯
反应类型与官能团的关系
官能团(或物质)的特征反应
[各类有机物之间的相互关系]
2 =CH 2
CH 3 —
CH 3 CH CH CH 2 O H
CH 3 CH 3 C H 2 C l
CH 2 CH 2 Cl CH C HO CH
Cl
CH 2-CH NH 2
n
2
HOCH 2 CH 2OH
CH 3 C OOH
CH 3 C OO CH 2 C
H 3
第四部分 化学实验导学
[物质的分离和提纯]
[物质的检验]
[常见气体的实验室制法]
第五部分 化学计算。
