波尔的原子模型 能级 (课件)
2022-2023年人教版(2019)新教材高中物理选择性必修3 第4章第4节波尔的原子模型课件

r3=0.477nm
氢原子中电子轨道半径示意图
一、玻尔原子理论的基本假设源自2. 能量量子化假说假说:
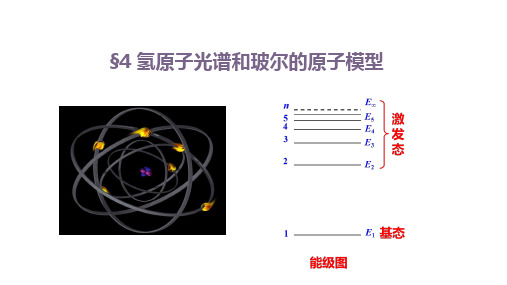
(1)电子在不同轨道上运动时,原子处于不同 的状态,具有不同的能量,即原子的能量是量子 化的,这些量子化的能量值叫作能级。 (2)原子中这些具有确定能量的稳定状态,称 为定态。能量最低的状态(n=1)叫作基态,其 他的状态(n=2,3,4……)叫作激发态。
资料
美丽的天津海河夜景
同时由于各种气体原子的能 级不同,跃迁时发射光子的能量 不同、频率不同,从而导致颜色 1不. 同,因此我们可以根据需要的 颜色选取合适的气体原子制成五 颜六色的霓虹灯
三、玻尔理论的局限性
1. 玻尔理论的成就 (1)玻尔的原子理论第一次将量子观念引 入原子领域,提出了定态和跃迁的概念。 (2)玻尔理论成功地解释了1巴. 尔末系,并 很好地解释甚至预言了氢原子的其他谱 线系。
n=∞ n=5 n=4 n=3 n=2
撞击 n=1
0 E5=-0.54eV E4=-0.85eV E3=-1.51eV E2=-3.4eV
E1=-13.6eV
二、玻尔理论对氢光谱的解释
电子从能量较低的定态轨道跃迁到能量较高 的定态轨道时,除了可以通过吸收光子获取 能量外,还可通过碰撞方式获得实物粒子的 能量。
由于实物粒子的动能可全部或部分地被 电子吸收,所以入射粒子的能量大于或等 于两能级的能量差值(E=Em-En),就可使 电子发生能级跃迁。
Em
撞击
En
能量较高的定态轨道能量记为Em 较低的定态轨道能量记为En
二、玻尔理论对氢原子光谱的解释
5.为什么不同元素的原子具有不同的特征谱线?
由于不同的原子具有不同的结构, 能级各不相同,因此辐射(或吸收) 的光子频率也不相同,所以每种原子 都有专属的原子光谱,不同元素的原 子具有不同的特征谱线。
教科版高中物理选择性必修第三册精品课件 第4章 原子结构 光谱 氢原子光谱 玻尔的原子模型 能级

内
容
索
引
01
自主预习·新知导学
02
合作探究·释疑解惑
03
课 堂 小 结
04
随 堂 练 习
自主预习·新知导学
一、光谱及光谱分析
1.光谱。
(1)定义:复色光通过分光镜后,分解为按波长顺序排列的一条单色光光带,
称为光谱。
(2)分类
①根据特征分
连续光谱:由波长连续分布的光组成的光谱。
明线光谱:由分立的光谱线组成的光谱。
特定频率的光会被太阳大气层中的某些元素的原子吸收,从而使我们观察
到的太阳光谱是吸收光谱,分析太阳的吸收光谱,可知太阳大气层的物质组
成,因此,选项C正确,A、B、D错误。
知识点二
氢原子光谱的规律
【问题引领】
(1)氢原子光谱是什么光谱?它是如何获取的?
(2)能否根据巴耳末公式计算出对应的氢光谱的最长波长?
②根据成因分
发射光谱:由发光物质所发的光直接产生的光谱。如连续光谱(炽热的固体、
液体及高压气体发光产生的光谱)和明线光谱(稀薄气体发光产生的光谱)。
吸收光谱:白光通过元素蒸气时被吸收一些特定频率的光形成的谱线,也称
暗线光谱。
(3)原子光谱:同一种原子发射光谱中的明线与吸收光谱中暗线的位置是相
同的,称为这种原子的特征光谱,也称原子光谱。
不同。
光谱分析的意义:考古学家对文物进行无损检测;科学家发现未知元素并测
出太阳大气外层的元素组成;医学上分析药物组成、进行肿瘤诊断等为治
疗提供依据;进行食品检测为健康保驾护航;分析空气质量、探测环境污染;
天文学家发现有机分子、分析宇宙起源等。
【归纳提升】
1.光谱的分类
2018-2019学年教科版高中物理选修3-5课件:2.4玻尔的原子模型 能级

【判一判】 (1)氢原子从基态跃迁到激发态时,总能量变大,电子动 能变小,势能变大。 ( ) (2)大量原子从n=5的激发态向低能态跃迁时,产生的光 谱线条数是4条。 ( ) (3)氢原子核外电子在能级1轨道和能级2轨道运行时, 轨道半径之比为1∶4,轨道能级的绝对值之比为2∶1。
()
(4)已知氢原子基态能量为-13.6eV,用能量为11eV光子 的光照射时,可使处于基态的氢原子电离。 ( )
(3)注意跃迁与电离 hν=En-Em只适用于光子和原子作用而使原子在各定态 之间跃迁的情况,对于光子和原子作用而使原子电离的 情况,则不受此条件的限制,这是因为原子一旦电离,原 子结构即被破坏,因而不再遵守有关原子结构的理论。 如基态氢原子的电离能为13.6eV,只要能量大于或等于 13.6eV的光子都能被基态的氢原子吸收而发生电离,只
供向心力,即氢原子中电子绕核运动时 由ke r上2 2 式m 可v r2知, 故 ,电E k 子n 绕1 2核m v 运n2 动k 2 的e rn 2。 半径r越大,Ek越小。
②电子与原子核间的电势能Epn 当电子的轨道半径增大时,库仑力做负功,原子的电势 能增大,反之电势能减小。 由此可见,电子在可能的轨道上绕核运动时,r增大,则 Ek减少,Ep增大,E增大;反之,r减小,则Ek增大,Ep减少,E 减少。与卫星绕地球运行相似。
【过关训练】 1.一个氢原子从n=3能级跃迁到n=2能级。该氢原子
() A.放出光子,能量增加 B.放出光子,能量减少 C.吸收光子,能量增加 D.吸收光子,能量减少
【解析】选B。根据玻尔理论,氢原子能级越高对应的 能量越大,当氢原子从较高能级向较低能级跃迁时放出 光子。
2.根据玻尔理论,下列关于氢原子的论述正确的是 ()
人教版高中物理选修35课件:第十八章 4 玻尔的原子模型

2
1
-
1 1
由于 c=λν,所以上式可写作 = ℎ1 2 - 2 。
2
。
把这个式子与前面的巴耳末公式相比较,可以看出它们的形式
是完全一样的,并且 R=-ℎ1。计算出-ℎ1的值为 1.097×107 m-1,与前面
给出的 R 的实验值符合得很好。这就是说,根据玻尔理论,不但可以
推导出表示氢原子光谱的规律性的公式,而且还可以从理论上来计
不同频率的光
D.大量处于 n=4 能级的氢原子向低能级跃迁时,可能发出 3 种
不同频率的可见光
解析:紫外线的频率比可见光的高,因此紫外线光子的能量应大
于 3.11 eV,而处于 n=3 能级的氢原子其电离能仅为 1.51 eV,小于
3.11 eV,所以处于 n=3 能级的氢原子可以吸收任意频率的紫外线,并
跃迁到能级 k 时吸收紫光的频率为 ν2,已知普朗克常量为 h,若氢原子
从能级 k 跃迁到能级 m,则(
)
A.吸收光子的能量为 hν1+hν2
B.辐射光子的能量为 hν1+hν2
C.吸收光子的能量为 hν2-hν1
D.辐射光子的能量为 hν2-hν1
解析:氢原子从能级 m 跃迁到能级 n 时,辐射红光,则 hν1=Em-En;
E3=-1.51 eV,
……
4.氢原子的能级图
氢原子的能级图如图所示。
5.对氢原子光谱的巴耳末系的解释及推测
按照玻尔原子理论,氢原子的电子从能量较高的轨道 n 跃迁到
能量较低的轨道 2 时,辐射出的光子能量应为 hν=En-E2。根据氢原
1
En=2 ,可得
1
1
1
18.4《玻尔的原子模型》 课件

n=1
-13.6 eV
1
巴尔末公式:
1 R( 22
1 n2
) n
3,4,
5,
L
R=1.10 107m1
Hα
Hβ
Hγ
Hδ
H
n=1 n=2 n=3 n=4
n=5 n=6
1
1 R( 22
1 n2
)
n 3,4, 5, L
R=1.10 107m1
1. 从高能级向低能级跃迁 发射光子:以光子形式辐射出去(原子发光现象)。
5. 一群处于基态的氢原子吸收某种单色光的光子后,
只能发出频率为 ν1、ν2、 ν3 的三种光子,且 ν1 > ν2 >
ν3 ,则 ( AC )
A. 被氢原子吸收的光子的能量为 hν1 B. 被氢原子吸收的光子的能量为 hν2
C. ν1 = ν2+ ν3 D. 被氢原子吸收的光子的能量为 hν1+ hν2+ hν3
玻尔理论成功的解释并预言了氢原子辐射的电磁波的问题, 但是也有它的局限性
在解决核外电子的运动时 成功引入了量子化的观念
同时又应用了“粒子、轨 道”等经典概念和有关牛 顿力学规律
量子化条件的引进没 有适当的理论解释
氦原子光谱
除了氢原子光谱外,在解决其 他问题上遇到了很大的困难
? α汤原粒氢姆子子光孙稳发散定谱思关现射性实想 键实电事验怎验子实: :样必 用修须 电观察与实验所获得的事实否否否彻子改定 定定底云玻放概尔弃念模原汤 卢 式经取瓜子姆 结瑟型典代模不孙 构福?经概型可的 模的典念割西 型核 的轨出出道现建建 建建立科学模型提出科学假说现矛概矛立立立盾念盾
2. 根据玻尔理论,某原子的电子从能量为 E 的轨道跃迁 到能量为 Eʹ 的轨道,辐射出波长为 λ 的光,以 h 表示普
波尔的原子模型(课堂PPT)

E1
轨道半径: rn n2r1 (n=1,2,3……)
式中r1 =0.53×10-10m 、E1=-13.6ev
频率条件 hEmEn
4 3 21
轨道假设
1
43 2
定态假设
E4 E3 E2
E1
43 2
跃迁假设
E4 E3 E2
1
E1
9
Hδ
n=1 n=2 n=3 n=4 n=5 n=6
(巴尔末系)
Hγ
Hβ
Hα
1R(212n12) n3,4,5,...
巴 耳 末 公 式R=1.10107m1 里 德 伯 常 量
根据:E=hv,λ=c/v
又Eδ =1.89eV= 3.03 ×10-19J 所以, λ δ=hc/ Eδ = 6.63×10-34 ×3.0 ×10-8 / 3.03 ×10-19J
A、原子要发出一系列频率的光子
B、原子要吸收一系列频率的光子
C、原子要发出某一频率的光子
D、原子要吸收某一频率的光子
4、根据玻尔理论,氢原子中,量子数n越大,则下列说 法中正确的是( ACD) A、电子轨道半径越大 B、核外电子的速率越大 C、氢原子能级的能量越大 D、核外电子的电势能越大
5、如图所示是某原子的能级图,a、b、c 为原子跃迁所
2、根据玻尔的原子理论,原子中电子绕核运动的半径 ( D) A、可以取任意值 B、可以在某一范围内取任意值 C、可以取一系列不连续的任意值 D、是一系列不连续的特定值
3、按照玻尔理论,一个氢原子中的电子从一半径为ra 的圆轨道自发地直接跃迁到一半径为rb的圆轨道上,已 知ra>rb,则在此过程中( C )
在普朗克关于黑体辐射的量子论和爱因斯坦关于 光子概念的启发下,波尔于1913年把微观世界中物理 量取分立值的观念应用到原子系统,提出了自己的原 子结构假说。
玻尔的原子模型-能级PPT课件

2、同时,按照经典电磁理论,电子绕核运行时 辐射电磁波的频率应该等于电子绕核运行的频率, 随着运行轨道半径的不断变化,电子绕核运行的 频率要不断变化,因此原子辐射电磁波的频率也 要不断变化。这样,大量原子发光的光谱就应该 是包含一切频率的连续谱。
以上矛盾表明,从宏观现象总结出来的经典 电磁理论不适用于原子这样小的物体产生的微观 现象。为了解决这个矛盾,1913年玻尔在卢瑟福 学说的基础上,把普郎克的量子理论运用到原子 系统上,提出了玻尔理论。
2、下面关于玻尔理论的解释中,不正确的说法 是( C )
A、原子只能处于一系列不连续的状态中,每 个状态都对应一定的能量
B、原子中,虽然核外电子不断做加速运动, 但只要能量状态不改变,就会向外辐射能量
C、原子从一种定态跃迁到另一种定态时,一 定要辐射一定频率的光子
D、原子的每一个能量状态都对应一个电子轨 道,并且这些轨道是不连续的
3、根据玻尔理论,氢原子中,量子数N越大,则下列 说法中正确的是( ACD ) A、电子轨道半径越大 B、核外电子的速率越大 C、氢原子能级的能量越大 D、核外电子的电势能越大
4、根据玻尔的原子理论,原子中电子绕核运动的半 径( D ) A、可以取任意值 B、可以在某一范围内取任意值 C、可以取一系列不连续的任意值 D、是一系列不连续的特定值
15一、郑和下西洋的概况和源自用1、目的:宣扬国威;满足统治者对异域珍宝特产的需求。加强与海外诸国的联 系; 2、时间:1405年——1433年。比欧洲人开辟新航路早半个多世纪。 3、手段:和平亲善
4、路线:江苏刘家港出发,经东南亚、南亚、 西5、传亚对出外的,贸物易品最:、技远术 到达红海沿传岸入的和物非品、洲技术东海岸地区。
丝织品、瓷器、茶叶、 印花布、铁器
第二章 第4节 玻尔的原子模型 能级

第4节玻尔的原子模型__能级一、玻尔的原子结构理论(1)电子围绕原子核运动的轨道不是任意的,而是一系列分立的、特定的轨道,当电子在这些轨道上运动时,原子是稳定的,不向外辐射能量,也不吸收能量,这些状态称为定态。
(2)当原子中的电子从一定态跃迁到另一定态时,才发射或吸收一个光子,其光子的能量hν=E n-E m,其中E n、E m分别是原子的高能级和低能级。
(3)以上两点说明玻尔的原子结构模型主要是指轨道量子化和能量量子化。
[特别提醒]“跃迁”可以理解为电子从一种能量状态到另一种能量状态的瞬间过渡。
二、用玻尔的原子结构理论解释氢光谱1.玻尔的氢原子能级公式E n=E1n2(n=1,2,3,…),其中E1=-13.6 eV,称基态。
2.玻尔的氢原子中电子轨道半径公式r n=n2r1(n=1,2,3,…),其中r1=0.53×10-10 m。
3.玻尔理论对氢光谱解释按照玻尔理论,从理论上求出里德伯常量R H的值,且与实验符合得很好。
同样,玻尔理论也很好地解释甚至预言了氢原子的其他谱线系。
三、玻尔原子结构理论的意义1.玻尔理论的成功之处第一次将量子观念引入原子领域,提出了定态和跃迁的概念,成功地解释了氢原子光谱的实验规律。
2.玻尔理论的局限性不能说明谱线的强度和偏振情况;不能解释有两个以上电子的原子的复杂光谱。
1.判断:(1)玻尔的原子结构假说认为电子的轨道是量子化的。
()(2)电子吸收某种频率条件的光子时会从较低的能量态跃迁到较高的能量态。
()(3)电子能吸收任意频率的光子发生跃迁。
()(4)玻尔理论只能解释氢光谱的巴尔末系。
()答案:(1)√(2)√(3)×(4)×2.思考:卢瑟福的原子模型与玻尔的原子模型有哪些相同点和不同点?提示:(1)相同点:①原子有带正电的核,原子质量几乎全部集中在核上。
②带负电的电子在核外运转。
(2)不同点:卢瑟福模型:库仑力提供向心力,r的取值是连续的。
波尔的原子模型课件

2.能级跃迁:处于激发态的原子是不稳定的,它会自发地向较低 能级跃迁,经过一次或几次跃迁到达基态。所以一群氢原子处于量子 数为 n 的激发态时,可能辐射出的光谱线条数为:N=nn2-1=C2n.
3.光子的发射:原子由高能级向低能级跃迁时以光子的形式放出 能量,发射光子的频率由下式决定.
hν=Em-En(Em、En 是始末两个能级且 m>n) 能级差越大,放出光子的频率就越高.
A.氢原子从 n=2 跃迁到 n=1 的能级时, 辐射光的波长大于 656 nm B.用波长为 325 nm 的光照射,可使氢 原子从 n=1 跃迁到 n=2 的能级 C.一群处于 n=3 能级上的氢原子向低 能级跃迁时最多产生 3 种谱线 D.用波长为 633 nm 的光照射,不能 使氢原子从 n=2 跃迁到 n=3 的能级
特别提醒 (1)处于基态的原子是稳定的,而处于激发态的原子是不稳定的. (2)原子的能量与电子的轨道半径相对应,轨道半径大,原子的能 量大,轨道半径小,原子的能量小.
典例精析 (多选)玻尔在他提出的原子模型中所做的假设有( )
A.原子处于具有一定能量的定态中,虽然电子做加速运动,但 不向外辐射能量
2.能量量子化:与轨道量子化对应的能量不连续的现象. 电子在可能轨道上运动时,尽管是变速运动,但它并不释放能量, 原子是稳定的,这样的状态也称之为定态. 由于原子的可能状态(定态)是不连续的,具有的能量也是不连续 的,这样的能量形式称为能量量子化.
3.频率条件 原子从一种定态(设能量为 E2)跃迁到另一种定态(设能量为 E1)时, 它辐射或吸收一定频率的光子,光子的频率由这两种定态的能量差决 定,即 hν=E2-E1. 可见,电子如果从一个轨道到另一个轨道,不是以螺旋线的形式 改变半径大小的,而是从一个轨道上“跳迁”到另一个轨道上.玻尔 将这种现象称作电子的跃迁. 总而言之:根据玻尔的原子理论假设,电子只能在某些可能轨道 上运动,电子在这些轨道上运动时不辐射能量,处于定态.只有电子 从一条轨道跃迁到另一条轨道上时才辐射能量,辐射的能量是一份一 份的,等于这两个定态的能量差.这就是玻尔理论的主要内容.
鲁科版高中物理选择性必修第三册精品课件 第4章 第4节 玻尔原子模型

光子,故B错误;电子由半径大的轨道跃迁到半径小的轨道,能级降低,因而
要辐射某一频率的光子,故C正确;原子吸收光子后能量增加,能级升高,故D
错误。
规律方法
解决玻尔原子模型问题的四个关键
(1)电子绕原子核做圆周运动时,不向外辐射能量。
中E1代表氢原子的基态的能级,即电子在离核最近的可能轨道上运动时原
子的能量值,E1=-13.6 eV。n是正整数,称为量子数。量子数n越大,表示能
级越高。
(3)原子的能量包括:原子的原子核与核外电子所具有的电势能和电子运动
的动能。
3.跃迁
原子从一种定态(设能量为Em)跃迁到另一种定态(设能量为En)时,它辐射
(或吸收)一定频率的光子,光子的能量由这两种定态的能量差决定。
高能级Em
低能级En
可见,电子如果从一个轨道到另一个轨道,不是以螺旋线的形式改变半径大
小的,而是从一个轨道“跳跃”到另一个轨道上。玻尔将这种现象叫作电子
的跃迁。
典例剖析
例1 根据玻尔理论,下列关于氢原子的论述正确的是(
)
A.若氢原子由能量为En的定态向低能级跃迁时,氢原子要辐射的光子能量
(2)电子在轨道间跃迁时会吸收光子或辐射出光子。
知识归纳
1.轨道量子化
“量子化”意味着“不连续”
(1)轨道半径只能是不连续的、某些分立的数值。
(2)氢原子中电子轨道的最小半径为r1=0.053 nm,其余轨道半径满足rn=n2r1,
式中n称为量子数,对应不同的轨道,只能取正整数。
2.能量量子化
(1)不同轨道对应不同的状态,在这些状态中,电子在可能轨道上运动时,尽
氢原子光谱和波尔的原子模型ppt课件
Na原子的发射光谱(明线)
H原子的吸收光谱(暗线)
H原子的发射光谱(明线)
吸收光谱和线状谱(发射光谱)的关系:
各种原子的吸收光谱中的每一条暗线都跟该种原子的发射光谱(线状光谱)中的
一条明线相对应。
3.光谱分析
既然每种原子都有自己的特征谱线,我们就可以利用它来鉴别物质和确定物质的组
成成分。这种方法称为光谱分析。
4.由于不同的原子具有不同的结构,能级各不
相同,因此辐射(或吸收)的光子频率也不相
同。这就是不同元素的原子具有不同的特征谱
线的原因。
六、玻尔理论的局限性
1.玻尔理论的不足之处在于保留了
经典粒子的观念,仍然把电子的运
动看作经典力学描述下的轨道运动。
2.玻尔理论成功地解释了氢原子光
谱的实验规律。但对于稍微复杂一
1
E1
激
发
态
h E n E m
基态
原子从低能级向高能级跃迁(电子从低轨道向高轨道跃迁): 吸收光子,原子能量增大
电子从低轨道向高轨道跃迁,电子克服库仑引力做
功,电势能增大,原子的能量增加,要吸收能量。
吸收光子能量:
h E n E m
原子从高能级向低能级跃迁(电子从高轨道向低轨道跃迁): 辐射光子,原子能量减小
优点:灵敏度高
样本中一种元素的含量达到10-13kg时就可
以被检测到。
利用白炽灯的光谱,能否检测出灯丝的成分?
不能,白炽灯的光谱是连续谱,不是原子
的特征谱线,因而无法检测出灯丝的成分
原子的特征光谱
二、氢原子光谱(发射光谱)的实验规律
氢原子是最简单的原子,其光谱也最简单。
n=6
n=5
人教版高中物理选择性必修三 第4章第3节氢原子光谱和玻尔的原子模型 课件

四、玻尔原子理论的基本假设
假说3:频率条件(跃迁
假说)
吸
收
基光
子
态
针对原子光谱是线状
谱提出
电子克服库仑力做功增大电
势能,
激
n
E∞
5
4
3
E
5E
4
E
原子的能量增加
跃
发
辐
电子所受库仑力做正功减小电
迁
射
势能,
原子的能量减少
光
子
3
2
E
2
态
= − (
> )
激
发
态
1
E
1
基
态
新知讲解
五、玻尔理论对氢光谱的解释
光谱研究是探索原子结构的一条重要途径。
氢气光
谱管
分光
镜
高压电
源
新知讲解
二、氢原子光谱的实验规律
许多情况下光是由原子内部电子的运动产生的,因此
光谱研究是探索原子结构的一条重要途径。
新知讲解
二、氢原子光谱的实验规律
新知讲解
二、氢原子光谱的实验规律
氢原子是最简单的原子,其光谱也最简单。
7 m−1
4
N=
5
N=
6
帕邢系(红
外线)
布喇开系
逢德
系
成功解释了
氢光谱的所
有谱线
新知讲解
五、玻尔理论对氢光谱的解释
新知讲解
五、玻尔理论对氢光谱的解释 Nhomakorabea新知讲解
五、玻尔理论对氢光谱的解释
新知讲解
五、玻尔理论对氢光谱的解释
1.从高能级向低能级跃迁
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
h E2 E1
3、氢原子在不同能级上的能量和相应的电子轨道半径为:
E1 En 2 , (n 1,2,3......) n rn n 2 r1, (n 1,2,3......) 式中,E 1 13.6ev, r1 0.531010 m
n= n=5 n=4
n=3 n=2
n= n=5 n=4 n=3 n=2
E4= -0.85ev E3= -1.5ev E2= -3.4ev
n=1
E1= -13.6ev
2、当氢原子从n=3的能级跃到n=1的能级时,能辐射出多少 种的光子,它们的频率是多少
氢原子的光谱图
可 见 光 区
特点
1.几种特定频率的光
2.光谱是分立的亮线
原子光谱
1、原子会发射电磁波(电子做变速运动) 2、电子的能量减小 3、原子发射的电磁波的频率是连续的 4、电子最终将坠毁,原子处在不稳定 状态。
一、玻尔的原子结构模型: 1、原子只能处于一系列能量不连续的状态中。在这些状态 中原子是稳定的,电子虽然做变速运动,但并不向外辐射能量, 这些状态叫做定态。电子绕原子核做圆周运动,只能处在一些 分立的轨道上,它只能在这些轨道上绕核转动而不产生电磁辐射。 2、原子从一种定态跃迁到另一定态时,吸收(或辐射)一定频率 的光子能量 h 。例如,原子从定态E2跃迁到定态E1辐射的光子 能量为 h E2 E1 3、原子的不同能量状态对应于电 子的不同运动轨道,原子的能量 状态是不连续的,电子不能在任 意半径的轨道上运动。 轨道半径r跟电子动量mv的 乘积满足下式
每一种原子都有自己特定的原子光谱,不同原子,其原子 光谱均不同
h me vr n , (n 1发射光子 吸收光子 E2
的这些轨道才是可能的。
二、氢原子的能级结构: 1、能级:原子只能处于一系列不连续的能量状态。在每个 状态中,原子的能量值是确定,各个确定的能量值叫做能级。 2、基级:原子尽可能处于最低能级,这时原子的状态叫基态, 较高能级所对应的状态叫激发态。电子从高能级跃迁到低能级 时,原子会辐射能量,而电子从低能级跃迁到高能级时, 原子要吸收能量,辐射(或吸收)能量
2.4 波尔的原子模型 能级
自学提示: 1、玻尔的原子结构理论内容
2、具体概念:定态、能级跃迁时的公式(如何 理解)
3、能级公式、半径公式(基态、激发态) 4、玻尔理论的应用范围
问题
按卢瑟福原子结构模型: 电子在原子核外绕原子核 做圆周运动,你会发现什 么问题?
n=1 n=2 n=3 n=4
重大发现:
E4= -0.85ev
E3= -1.5ev E2= -3.4ev
n=1
E1= -13.6ev
三、原子的跃迁: 1、当氢原子从n=2的能级跃到n=1的能级时, (1)原子是吸收光子还是辐射光子, (2)辐射光子的能能量、频率和波长是多少
解: E E2 E1 10.2ev
E 2.461015 H Z h c 1.22107 m
