波尔的原子模型(课堂PPT)
合集下载
波尔的原子模型ppt正式完整版

子处于量子数为 n 的激发态上时,最多可辐射出 n-1 条光 谱线.
三、玻尔模型的局限性
玻尔理论成功的解释并预言了氢原子辐射
的电磁波的问题,但是也有它的局限性.
一、玻尔原子理论的三个基本假设
C.这些氢原子总共可辐射出3种不同频率的光
2000 C. 针对原子核式结构模型提出
光子的能量必须等于能级差
2、原子从一种定态(设能量为E初)跃迁到另一种定态(设能量为E终)时,它辐射(或吸收)一定频率的光子,光子的能量由这两
布 喇 开 系
普 丰 德 系
-0.85 -1.51
-3.4
耳
级
末
图
系
基态
1
赖曼系
-13.6
二、玻尔理论对氢光谱的解释
1、向低轨道跃迁
跃迁时发射光子的能量:
hvEmEn
光子的能量必须等于能级差
处于激发态的原子是不 稳定的,可自发地经过一 次或几次跃迁达基态
发射光子
n 量子数
∞
5 4 3 2
E /eV
一个原子和一群原子 氢原子核外只有一个电子,这个电子在某个时刻只能处在某 一个可能的轨道上,在某段时间内,由某一轨道跃迁到另一 个轨道时,可能的情况只有一种,但是如果容器中盛有大量 的氢原子,这些原子的核外电子跃迁时就会有各种情况出现
了.即:一群氢原子处于量子数为 n 的激发态时,可 能辐射出的光谱条数为 N=nn2-1=C2n,而一个氢原
为什么氢光谱是线状光谱?
二、玻尔理论对氢光谱的解释
n ∞:电子脱离核束缚
存在困难:原子的稳定性
氢原子从一个电子 4、原子发光现象:原子从较高的激发态向较低的激发态或基态跃迁的过程,是辐射能量的过程,这个能量以光子的形式辐射出去,这
三、玻尔模型的局限性
玻尔理论成功的解释并预言了氢原子辐射
的电磁波的问题,但是也有它的局限性.
一、玻尔原子理论的三个基本假设
C.这些氢原子总共可辐射出3种不同频率的光
2000 C. 针对原子核式结构模型提出
光子的能量必须等于能级差
2、原子从一种定态(设能量为E初)跃迁到另一种定态(设能量为E终)时,它辐射(或吸收)一定频率的光子,光子的能量由这两
布 喇 开 系
普 丰 德 系
-0.85 -1.51
-3.4
耳
级
末
图
系
基态
1
赖曼系
-13.6
二、玻尔理论对氢光谱的解释
1、向低轨道跃迁
跃迁时发射光子的能量:
hvEmEn
光子的能量必须等于能级差
处于激发态的原子是不 稳定的,可自发地经过一 次或几次跃迁达基态
发射光子
n 量子数
∞
5 4 3 2
E /eV
一个原子和一群原子 氢原子核外只有一个电子,这个电子在某个时刻只能处在某 一个可能的轨道上,在某段时间内,由某一轨道跃迁到另一 个轨道时,可能的情况只有一种,但是如果容器中盛有大量 的氢原子,这些原子的核外电子跃迁时就会有各种情况出现
了.即:一群氢原子处于量子数为 n 的激发态时,可 能辐射出的光谱条数为 N=nn2-1=C2n,而一个氢原
为什么氢光谱是线状光谱?
二、玻尔理论对氢光谱的解释
n ∞:电子脱离核束缚
存在困难:原子的稳定性
氢原子从一个电子 4、原子发光现象:原子从较高的激发态向较低的激发态或基态跃迁的过程,是辐射能量的过程,这个能量以光子的形式辐射出去,这
人教版 物理 选修3—5 18.4 玻尔的原子模型(共24张PPT)(优质版)

三、玻尔的原子理论之定态假设:
2、定态假设:(本假设是针对原子稳定性提出的) 不同的轨道对应着不同的状态,在这些状态中,尽管电子 在做变速运动,却不辐射能量,因此这些状态是稳定的; (1)当电子在不同轨道上运动时,原子处于不同的状态中,具 有不同的能量,即原子的能量是量子化的,这些量子化的能 量值叫作能级。 (2)原子中这些具有确定能量的稳定状态,称为定态。能量 最低的状态叫作基态,其他的能量状态叫作激发态。
五、玻尔理论的成功与局限性:
1.玻尔理论的成功之处:玻尔的原子理论第一次将量子观念引入原子领域, 提出了定态和跃迁的概念,成功地解释了氢原子光谱的实验规律。轨道 量子化假设把量子观念引入原子理论,这是玻尔的原子理论之所以成功 的根本原因
2.玻尔理论的局限性:对更复杂的原子发光,玻尔理论却无法解释,它过多 地保留了经典粒子的概念。把电子运动看成是经典力学描述下的轨道运 动。
四、玻尔原子理论对氢光谱的解释:
3.解释了气体导电发光现象:
处于基态的原子受到电子的撞击,可以跃迁到激发态,处于激发态的原子是 不稳定的,会自发地向能量较低的能级跃迁,放出光子,最终回到基态。
4.解释了氢原子光谱的不连续性
原子从较高能级向低能级跃迁时放出光子的能量等于前后两能级差,由于 原子的能级是分立的,所以放出的光子的能量也是分立的,因此原子的发射 光谱只有一些分立的亮线。
大学以E.卢瑟福为首的科学集体,从此和卢瑟福建立了长期的密切关系。
1912年,玻尔考察了金属中的电子运动,并明确意识到经典理论在阐明微观现象 方面的严重缺陷,赞赏普朗克和爱因斯坦在电磁理论方面引入的量子学说,创造性地 把普朗克的量子说和卢瑟福的原子核概念结合了起来。
1913年提出了量子不连续性,成功地解释了氢原子和类氢原子的结构和性质,提 出了原子结构的玻尔模型。
玻尔的原子模型PPT教学课件

汉初,接秦之敝,诸 侯并起,民失作业而大饥 谨。凡米石五千,人相食, 死者过半。高祖乃令民得 卖子,就食蜀、汉。天下 既定,民亡盖藏,自天子 不能具醇驷 (同一颜色的四匹 马),而将相或乘牛车。
——《汉书.食货志》
经济残败、百废待兴
修养生息、轻徭薄赋
西汉初年的社会状况
西汉建立之初, 经过秦末农民战争, 经济受到严重破坏。 为了恢复元气,汉 初实行休养生息的 政策。对外与匈奴 “和亲”,对内轻 徭薄赋。
罢 1、“无为而治” 不能适应中央集权的需要。 匈奴南下侵汉;
黜 诸侯“自为法令,拟于天子”—七国之乱 2、儒学的自我调节符合中央集权的要求——
百 吸收大一统的思想。 家 3、汉的强大使其统治者不满足于“无为”,推
崇
“有为”而治。
独 尊 儒 术
罢黜百家 独尊儒术
董仲舒: 中国古代著名的思想家。 (前179——前104年)广
川人(今河北景县人)向 汉武帝提出“罢黜百家 独尊儒术”的主张,创立 新儒学。
2、董仲舒的新儒学的思想内涵
#思想来源: 以《公羊春秋》为骨干, 融合阴阳家,黄老之学 以及法家思想而形成的 新的思想体系。
#理论基础: “天人感应”学说。
#思想核心: 大一统(“新”所在)
天人感应
“天子受命于天,天下受命于天子”;“古之造文者,三画 连其中,谓之王,三画者,天地人,而连其中,通其道也, 谓之王。”
光子的发射和吸收
原子在始、 末两个能级Em和 En( Em>En )间 跃迁时发射光子 的频率可以由下 式决定:
h Em En
人们早在了解原子内部结构之前就已经观 察到了气体光谱,不过那时候无法解释为什么气 体光谱只有几条互不相连的特定谱线,玻尔理论 很好的解释了氢原子的光谱.
——《汉书.食货志》
经济残败、百废待兴
修养生息、轻徭薄赋
西汉初年的社会状况
西汉建立之初, 经过秦末农民战争, 经济受到严重破坏。 为了恢复元气,汉 初实行休养生息的 政策。对外与匈奴 “和亲”,对内轻 徭薄赋。
罢 1、“无为而治” 不能适应中央集权的需要。 匈奴南下侵汉;
黜 诸侯“自为法令,拟于天子”—七国之乱 2、儒学的自我调节符合中央集权的要求——
百 吸收大一统的思想。 家 3、汉的强大使其统治者不满足于“无为”,推
崇
“有为”而治。
独 尊 儒 术
罢黜百家 独尊儒术
董仲舒: 中国古代著名的思想家。 (前179——前104年)广
川人(今河北景县人)向 汉武帝提出“罢黜百家 独尊儒术”的主张,创立 新儒学。
2、董仲舒的新儒学的思想内涵
#思想来源: 以《公羊春秋》为骨干, 融合阴阳家,黄老之学 以及法家思想而形成的 新的思想体系。
#理论基础: “天人感应”学说。
#思想核心: 大一统(“新”所在)
天人感应
“天子受命于天,天下受命于天子”;“古之造文者,三画 连其中,谓之王,三画者,天地人,而连其中,通其道也, 谓之王。”
光子的发射和吸收
原子在始、 末两个能级Em和 En( Em>En )间 跃迁时发射光子 的频率可以由下 式决定:
h Em En
人们早在了解原子内部结构之前就已经观 察到了气体光谱,不过那时候无法解释为什么气 体光谱只有几条互不相连的特定谱线,玻尔理论 很好的解释了氢原子的光谱.
《玻尔的原子模型》课件

经典物理学认为 电子在原子中的 运动是连续的, 而玻尔的原子模 型则认为电子只 能在特定的轨道 上运动。
经典物理学认为 电子在原子中的 能量是连续的, 而玻尔的原子模 型则认为电子的 能量是量子化的。
经典物理学认为 电子在原子中的 运动是受电磁力 作用的,而玻尔 的原子模型则认 为电子在原子中 的运动是受量子 力学规律的作用。
对科学教育的影响
玻尔原子模型是量子力学的基石,对科学教育产生了深远影响。
玻尔原子模型提出了电子轨道的概念,为后来的量子力学奠定了基 础。
玻尔原子模型激发了人们对微观世界的探索兴趣,推动了科学教育的 发展。
玻尔原子模型对科学教育的影响不仅体现在物理学领域,还涉及到 化学、生物等学科。
05
对玻尔原子模型的探讨和评价
玻尔的科学成就
提出玻尔模型: 描述原子结构
和电子运动
提出量子力学: 解释微观世界
的现象
提出互补原理: 解释量子力学
中的矛盾
提出波粒二象 性:解释微观 粒子的波粒二
象性
玻尔的学术影响
提出玻尔模型,对量子力学的发展起到了关键作用 提出互补原理,对量子力学的诠释产生了深远影响 提出量子跃迁理论,为量子力学的发展奠定了基础 提出氢原子光谱理论,为量子力学的应用提供了重要依据
钾原子: 玻尔模型 能够解释 钾原子光 谱的规律 性
铷原子: 玻尔模型 能够解释 铷原子光 谱的规律 性
验证的意义和局限性
验证了玻尔原子模型的正确性
推动了量子力学的发展
局限性:无法解释某些现象, 如电子自旋等
局限性:无法解释某些实验结 果,如电子双缝干涉实验等
04
玻尔原子模型的影响和贡献
对量子力学发展的影响
chap3(II)-波尔原子模型.ppt
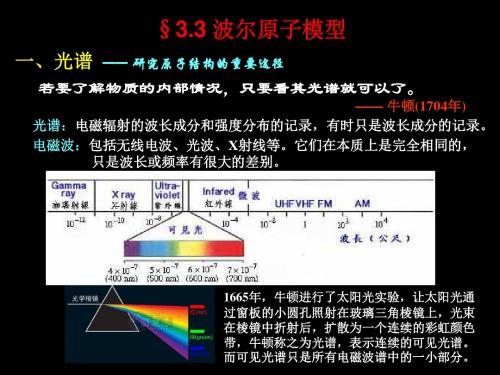
氢原子光谱的线系
~ 赖曼系(m = 1) :
1 ], n 2,3,4, RH [ 1 12 n 2 R H [ 12 12 ], n 3,4,5, 2 n
在紫外区,是1914年由赖曼发现的。
~ 巴耳末系(m = 2) : ~ 帕邢系(m = 3) :
体系的角动量是量子化的
2
2
2
r M 1 C
Ze
r2
v
m
V
Mm M m
消去,求得r
MVr1 m v r2 n
r n
2
2 2 4 π 4 π 2 0 0 rn n 2 r n n e 2 Z me 2 Z 2 2 2 Ze 1 1 原子体系的能量 E MV m v 2 2 4 π 0 r
434.010nm
486.074nm
• 波长遵守巴耳末公式的这一系列谱线称为巴耳末线系 • 波长间隔沿短波方向递减 • 谱线系的系限—谱线系中最短的波长
n
B 364.56 nm
2 ~ n 4 4 ( 1 1 ) 1 1 波数 B n2 B 22 n2
对氢原子,计算得 R H 理论 1 .097 373 1 10 7 m 1 玻尔理论的成功之四
当时实验测得
RH实验 1.096 775 8 10 7 m 1
问题:里德伯常数的理论计算结果与实验结果误差超过了万分之五,其原因何在?
۩ 考虑到核不会固定不动,上式中电子质量应理解为折合质量 mM mM 2 4
410.120nm
Ha : 红 Hb : 深绿 Hg : 青 Hd : 紫
656.210nm 486.074nm 434.010nm 410.120nm
《玻尔的原子模型》课件1(10张PPT)(鲁科版选修3-5)

gkxx精品课件
氢原子的光谱图
可 见 光 区
特点 1.几种特定频率的光 2.光谱是分立的亮线
gkxx精品课件
原子光谱
每一种原子都有自己特定的原子光谱,不同原子,其原子 光谱均不同
gkxx精品课件
gkxx精品课件
n= n=5
E h
2.461015 HZ
n=4 n=3
c 1.22107 m
n=2
E4= -0.85ev E3= -1.5
E1= -13.6ev
2、当氢原子从n=3的能级跃到n=1的能级时,能辐射出多少 种的光子,它们的频率gkx是x精多品课少件
E2
的这些轨道才是可能的gk。xx精品课件
二、氢原子的能级结构:
1、能级:原子只能处于一系列不连续的能量状态。在每个 状态中,原子的能量值是确定,各个确定的能量值叫做能级。
2、基级:原子尽可能处于最低能级,这时原子的状态叫基态, 较高能级所对应的状态叫激发态。电子从高能级跃迁到低能级 时,原子会辐射能量,而电子从低能级跃迁到高能级时, 原子要吸收能量,辐射(或吸收)能量
一、玻尔的原子结构模型:
1、原子只能处于一系列能量不连续的状态中。在这些状态 中原子是稳定的,电子虽然做变速运动,但并不向外辐射能量, 这些状态叫做定态。电子绕原子核做圆周运动,只能处在一些 分立的轨道上,它只能在这些轨道上绕核转动而不产生电磁辐射。
2、原子从一种定态跃迁到另一定态时,吸收(或辐射)一定频率
第3节 玻尔的原子模型
gkxx精品课件
问题
按卢瑟福原子结构模型: 电子在原子核外绕原子核 做圆周运动,你会发现什 么问题?
n=1
n=2
波尔的原子模型课件上课用

轰击而跃迁到激发态,在这些氢原子从激发态向 低能级跃迁的过程中( AC ) A. 总共能辐射出6种不同频率的光子 B. 总共能辐射出10种不同频率的光子 C. 辐射出波长最长的光子是从n=4跃迁到n=3 能级时放出的
D. 辐射出波长最长的光子是从n=5跃迁到n=4 能级时放出的
6、(多选)已知氢原子部分能级示意图如图所示, 则具有下列能量的光子,能被处于基态的氢原子 吸收的是( CD )
过一次或几次跃迁到达某个高能 2
E /eV
0
-0.54 -0.85 -1.51 -3.4
级激发态;此时处于激发态的原
子不稳定,继而向低能级跃迁, 1Fra bibliotek-13.6
发出光子;
由于能级是分立的,所以原子吸收光子后又放
出光子的光谱也是分立的暗线,此时为吸收光谱,
吸收光子波长等于之后放出的光子波长;
4、电子跃迁发出光谱的光谱数计算
5 4 3 2
1
E /eV
E∞ =0
E5 =-0.54 E4 =-0.85 E3=-1.51 E2=-3.4
8
取n= 时的能量为
0,其他的能级能量均为
负
En
1 n2
E1
(E1 13.6eV )
E1=-13.6
n越大,r越大,能级 的能量越大
3、原子为什么会发光?——跃迁假设
n 量子数
∞
5 4 3 2
,则照射光的频率必须是多少?
跃迁后能发出几种不同频率的光? n 量子数
E /eV
求辐射光的最大频率和最小频率?
各种光能量之间的关系?
∞
0
5
-0.54
4
-0.85
3
-1.51
D. 辐射出波长最长的光子是从n=5跃迁到n=4 能级时放出的
6、(多选)已知氢原子部分能级示意图如图所示, 则具有下列能量的光子,能被处于基态的氢原子 吸收的是( CD )
过一次或几次跃迁到达某个高能 2
E /eV
0
-0.54 -0.85 -1.51 -3.4
级激发态;此时处于激发态的原
子不稳定,继而向低能级跃迁, 1Fra bibliotek-13.6
发出光子;
由于能级是分立的,所以原子吸收光子后又放
出光子的光谱也是分立的暗线,此时为吸收光谱,
吸收光子波长等于之后放出的光子波长;
4、电子跃迁发出光谱的光谱数计算
5 4 3 2
1
E /eV
E∞ =0
E5 =-0.54 E4 =-0.85 E3=-1.51 E2=-3.4
8
取n= 时的能量为
0,其他的能级能量均为
负
En
1 n2
E1
(E1 13.6eV )
E1=-13.6
n越大,r越大,能级 的能量越大
3、原子为什么会发光?——跃迁假设
n 量子数
∞
5 4 3 2
,则照射光的频率必须是多少?
跃迁后能发出几种不同频率的光? n 量子数
E /eV
求辐射光的最大频率和最小频率?
各种光能量之间的关系?
∞
0
5
-0.54
4
-0.85
3
-1.51
人教版物理选修-玻尔的原子模型-ppt精品课件
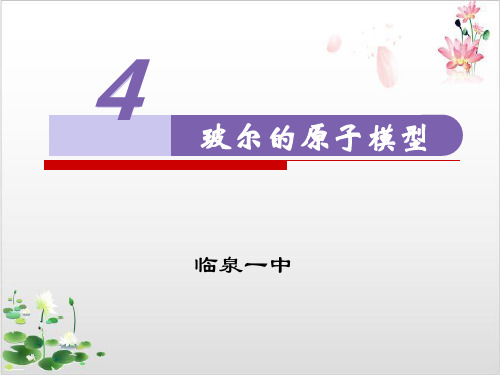
E/eV
0 -0.54 -0.85 -1.51
-3.4
1
人教版物理选修3-5 18.4 玻尔的原子模型(共28张PPT)【PPT优秀 课件】 -精美 版
赖曼系
-13.6
20
人教版物理选修3-5 18.4 玻尔的原子模型(共28张PPT)【PPT优秀 课件】 -精美 版
思考与讨论:
1. 根据氢原子能级取值量子化,如何解释 原子的光谱是分立的线状谱?
7.先用低 倍镜找 到叶肉 细胞, 然后换 用高倍 镜观察 。注意 观察叶 绿体随 着细胞 质流动 的情况 ,仔细 看看每 个细胞 中细胞 质流动 的方向 是否一 致致。
8.内质网 以类似 于“出 芽”的 形式形 成具有 膜的小 泡,小 泡离开 内质网 ,移动 到高尔 基体与 高尔基 体融合 ,成为 高尔基 体的一 部分。 高尔基 体又以 “出芽 ”方式 形成小 泡,移 动到细 胞膜与 细胞膜 融合, 成为细 胞膜的 一部分 。
hc
1 n2
2π2e4k 2me h2
1 ( 22
2π2e4k h2
2me
)
1 2π2e4k 2me ( 1 1 )
h3c
22 n2
17
人教版物理选修3-5 18.4 玻尔的原子模型(共28张PPT)【PPT优秀 课件】 -精美 版
1
1 R( 22
1 n2 )
1 2π2e4k 2me ( 1 1 )
4
原子光谱对玻尔创立原子结构具有重 要作用,然而最初玻尔没有意识到这一点.
玻尔曾这样说道: “人们总以为[光谱是]神奇的,但在 那儿不可能取得进步.这就彷佛你有蝴蝶的 翅膀,那么其色彩等等当然是非常有规律的, 但是没有人想到能从蝴蝶翅膀的颜色推出生 物学的基础”
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
E1
轨道半径: rn n2r1 (n=1,2,3……)
式中r1 =0.53×10-10m 、E1=-13.6ev
频率条件 hEmEn
4 3 21
轨道假设
1
43 2
定态假设
E4 E3 E2
E1
43 2
跃迁假设
E4 E3 E2
1
E1
9
Hδ
n=1 n=2 n=3 n=4 n=5 n=6
(巴尔末系)
Hγ
Hβ
Hα
1R(212n12) n3,4,5,...
巴 耳 末 公 式R=1.10107m1 里 德 伯 常 量
根据:E=hv,λ=c/v
又Eδ =1.89eV= 3.03 ×10-19J 所以, λ δ=hc/ Eδ = 6.63×10-34 ×3.0 ×10-8 / 3.03 ×10-19J
A、原子要发出一系列频率的光子
B、原子要吸收一系列频率的光子
C、原子要发出某一频率的光子
D、原子要吸收某一频率的光子
4、根据玻尔理论,氢原子中,量子数n越大,则下列说 法中正确的是( ACD) A、电子轨道半径越大 B、核外电子的速率越大 C、氢原子能级的能量越大 D、核外电子的电势能越大
5、如图所示是某原子的能级图,a、b、c 为原子跃迁所
2、根据玻尔的原子理论,原子中电子绕核运动的半径 ( D) A、可以取任意值 B、可以在某一范围内取任意值 C、可以取一系列不连续的任意值 D、是一系列不连续的特定值
3、按照玻尔理论,一个氢原子中的电子从一半径为ra 的圆轨道自发地直接跃迁到一半径为rb的圆轨道上,已 知ra>rb,则在此过程中( C )
在普朗克关于黑体辐射的量子论和爱因斯坦关于 光子概念的启发下,波尔于1913年把微观世界中物理 量取分立值的观念应用到原子系统,提出了自己的原 子结构假说。
一、玻尔原子理论的基本假设
1、轨道假设:原子中的电子在库仑力的作用下,绕原子核 做圆周运动,服从经典力学的规律。
但是,电子轨道半径不是任意的,只有当半径大小符合一定条件 时,这样的轨道才是可能的。即电子的轨道是量子化的。 电子在这 些轨道上绕核的转动是稳定的,不产生电磁辐射。
1
赖曼系
-13.6
大量氢原子处于n=4激发态
1、会辐射出几种频率的光?
6种
2、其中波长最短的是在哪 两个能级之间跃迁时发 出的?
波长最短,频率最大,故 在41之间跃迁时发出的
n 量子数
∞ 5 4 3 2
1
光子的能量必须等于能级差
E /eV 0 -0.54 -0.85 -1.51 -3.4
-13.6
发出的三种波长的光. 在下列该原子光谱的各选项中,谱
线从左向右的波长依次增大,则正确的是 _____C________.
三种光的频率,波长满足什么关系?
小结
一、玻尔原子理论的基本假设
1、轨道假设: 2、能级假设: 3、跃迁假设:
二、玻尔理论对氢光谱的解释
三、玻尔模型的局限性
电子云是近代对电子用统计的方法,在核外空间分布 方式的形象描绘,它的区别在于行星轨道式模型。
达标练习:
1、玻尔在他提出的原子模型中所做的假设有( ABC )
A.原子处在具有一定能量的定态中,虽然电子做变速运动, 但不向外辐射能量 B.原子的不同能量状态与电子沿不同的圆形轨道绕核运动相 对应,而电子的可能轨道的分布是不连续的 C.电子从一个轨道跃迁到另一个轨道时,辐射(或吸收)一 定频率的光子 D.电子跃迁时辐射的光子的频率等于电子绕核做圆周运动的 频率
知识拓展:
实物粒子使原子跃迁
实物粒子和原子碰撞的情况,由于实物粒子的 动能可全部或部分地为原子吸收,所以只要入射粒 子的动能大于或等于原子某两定态能量之差,也可 使原子受激发而向较高能级跃迁。
E电子 EmEn
三、玻尔模型的局限性
玻尔理论解决了原子的稳定性和辐射的频率条 件问题,但是也有它的局限性.
电离:(完全脱离原子核束缚 )
使原子电离 hvEEn
即:hv En
电离后电子剩余动能为:
Ek hvEnhv En
注意:En为负值
n 量子数
∞
5 4 3 2
E /eV
0
-0.54 -0.85 -1.51
-3.4
1
-13.6
思考:分别能量为2eV、10eV的光子照射处于n=2激发态的 氢原子,结果如何? 2eV—跃迁,10e脱 ∞
离核束缚
5
4
3
rn n2r1
2
E /eV
0
-0.54 -0.85 -1.51 -3.4
E 0
En
E1 n2
r10.05n3m1
-13.6 E113.6eV
氢原子能级图
二、玻尔理论对氢光谱的解释
氢原子中电子的可能轨道半径和相应的能量
能
量:
En
1 n2
= 6.57 ×10-7(m)
Hδ
Hγ
巴尔 末系 氢吸 收光 谱
n=1 n=2 n=3 n=4
n=5 n=6
Hβ
Hα
氢原子的能级图
n
E/eV
∞----------------- 0 eV
5 4 3
激 发
2
态
-0.54
巴
帕 邢 系
布 喇 开 系
普 丰 德 系
-0.85 -1.51
-3.4
耳
末
系
基态
在解决核外电子的运动时 成功引入了量子化的观念
同时又应用了“粒子、 轨道”等经典概念和 有关牛顿力学规律
除了氢原子光谱外,在解决其他 问题上遇到了很大的困难.
氦原子光谱
波尔理论还没有完全解 释微观粒子运动的规律。
电子是一种微观粒子,在原子如此小的空间(直径约 10⁻¹⁰m)内作高速(接近光速3×10⁸m·s⁻¹)运动,核外 电子的运动与宏观物体运动不同,没有确定的方向和轨迹 ,只能用电子云描述它在原子核外空间某处出现机会(几 率)的大小。
人教版选修3-5
第十八章 原子结构
第四节 玻尔的原子模型
1
经典理论的困难
核外电子绕核运动
辐射电磁波
电子轨道半径连续变小
原子不稳定
事实上:原子是稳定的
辐射电磁波频率连续变化
辐射电磁波频率只是 某些确定值
历史回顾
卢瑟福的核式结构模型 正确地指出了原子核的存在, 很好地解释了α散射实验。 但是,经典物理学既无法解 释原子的稳定性,又无法解 释原子光谱的分立特征。
rn n2r1
氢原子中电子轨道的最小半径
r10.05n3m
一、玻尔原子理论的基本假设
2、能级假设:当电子在不同轨道上运动时,原子处于 不同状态,具有不同能量,所以原子能量也是量子化的。
这些量子化的能量值叫能级;原子中这些具有确 定能量的稳定状态叫定态。
能量最低的状态叫基态,其他状态叫激发态。
En
1 n2
E1
氢原子在基态(第一能级)的能量:
E113 .6eV
一、玻尔原子理论的基本假设
3、跃迁假设:当电子从能量较高的定态轨道(设能量为Em)
跃迁到能量较低的定态轨道(设能量为En,m>n)时,它辐射
出一定频率的光子,光子的能量由这两种定态的能量差决定, 即
h EmEn (频率条件或辐射条件)
反之,当电子吸收光子时会从较低的能量态跃迁到较高 的能量态,吸收的光子的能量同样由两种定态的能量差决定。
