游离三碘甲状腺原氨酸(FT3)作业指导书
放免作业指导书
温度:18-25℃,测定时温度在±2℃以内;湿度:30-70%RH。
(3)仪器保养,零部件是否完整。清洁内部,检查有无异常情况(声音、湿度、指示灯)。
(4)试剂要求:
a精密度:批内≤6%,批间相对极差≤6%。
b准确度:测定质控血清,偏差≤20%。
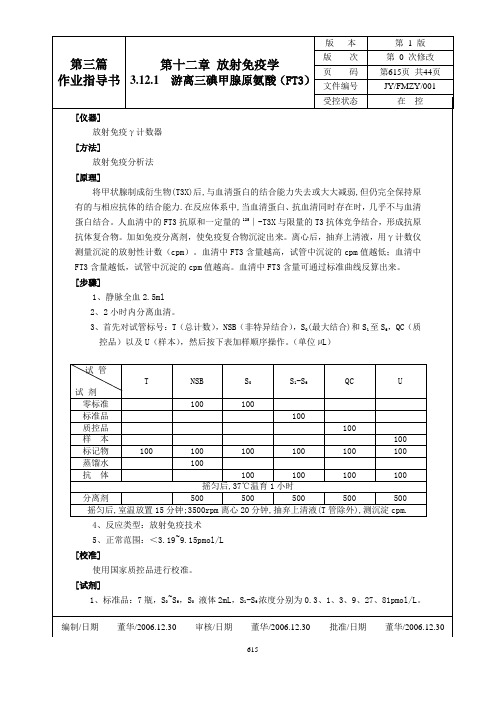
[仪器]
放射免疫γ计数器
[方法]
放射免疫分析法
[原理]
将甲状腺制成衍生物(T3X)后,与血清蛋白的结合能力失去或大大减弱,但仍完全保持原有的与相应抗体的结合能力.在反应体系中,当血清蛋白、抗血清同时存在时,几乎不与血清蛋白结合。人血清中的FT3抗原和一定量的125∣-T3X与限量的T3抗体竞争结合,形成抗原抗体复合物。加如免疫分离剂,使免疫复合物沉淀出来。离心后,抽弃上清液,用γ计数仪测量沉淀的放射性计数(cpm)。血清中FT3含量越高,试管中沉淀的cpm值越低;血清中FT3含量越低,试管中沉淀的cpm值越高。血清中FT3含量可通过标准曲线反算出来。
(7)病人准备、标本要求:
抽血时,最好空腹、不要输液。
(8)参考资料:
来源于厂家仪器、试剂使用说明书。
[仪器]
放射免疫γ计数器
[方法]
放射免疫分析法
[原理]
本项目采用竞争性放射免疫分析方法,将甲状腺激素制成衍生物(T4X)后,与血清蛋白的结合能力失去或大大减弱,但仍完全保持原有与相应抗体的结合能力。在反应体系中,当血清蛋白、抗血清同时存在时,几乎不与血清蛋白结合。人血清中的FT4抗原和一定量的125︱—T4X与限量的T4抗体竞争结合,形成抗原抗体复合物,加入免疫分离剂,使免疫复合物沉淀出来,离心后,抽弃上清液,用γ计数仪测量沉淀的放射性计数(cpm)。血清中FT4含量越高,试管中沉淀的cpm值越低;血清中FT4含量越低,试管中沉淀的cpm值越高。血清中FT4含量可通过标准曲线反算出来。
游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求爱康试剂

游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)性能指标1试剂条性能指标1.1外观和性状试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰、准确、牢固;试剂条中第7孔内组分应为棕色含固体微粒的液体或含棕色固体沉淀的透明液体;第12 孔内化学发光底物应为无色或淡绿色液体;其余皆应为无色透明液体,无悬浮物、无沉淀、无絮状物。
1.2检出限应不大于0.600pmol/L。
1.3准确度-相对偏差使用企业参考品进行测定,实测值与标示值的相对偏差应在±15.0%内。
1.4线性区间试剂盒在0.600pmol/L~50.0pmol/L区间内,其线性相关系数(r)应不小于0.9900。
1.5重复性用同一批次的试剂盒测定两份不同浓度的内控品,重复检测10次,其变异系数(CV)应不大于10.0%。
1.6批间差用3个批号试剂盒测定两份不同浓度的内控品,重复检测10次,测定结果的变异系数(CV)应不大于15.0%。
1.7分析特异性a)对浓度为200ng/mL的甲状腺激素进行测定,测定结果应不高于0.600pmol/L;b)对浓度为100ng/mL的3,3’,5’-三碘甲腺原氨酸进行测定,测定结果应不高于15.0pmol/L;c)对浓度为100ng/mL的3,3’- 二碘甲腺原氨酸进行测定,测定结果应不高于20.0pmol/L。
2校准品性能指标2.1外观校准品应为无色透明或淡黄色液体,无悬浮物、无沉淀、无絮状物。
2.2装量校准品装量偏差应在±10.0%之内。
2.3准确度游离三碘甲状腺原氨酸(FT3)校准品,测试结果偏差应在±10.0%之内。
2.4均一性对同一瓶校准品1、校准品2分别重复10次检测,对同一批次10瓶校准品1、校准品2进行检测,检测校准品1、校准品2瓶内差CV应≤10.0%,批内瓶间差CV应≤10.0%。
3质控品性能指标3.1外观质控品应为无色透明或淡黄色液体,无悬浮物、无沉淀、无絮状物。
游离三碘甲腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求yuande

游离三碘甲腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)适用范围:本产品用于体外定量测定人血清中的FT3的含量。
1.1 产品规格试剂盒规格为48人份/盒、96人份/盒。
1.2 主要组成成分表1 游离甲状腺素(FT3)测定试剂盒(化学发光免疫分析法)主要组成成分a) 酶结合物以含牛血清白蛋白的缓冲液配制的联接HRP的T3,其中含ProClin300做为防腐剂。
b) 反应抗体:以含牛血清白蛋白的缓冲液配制的T3单克隆抗体,其中含ProClin300做为防腐剂。
c) 校准品校准品主要是牛血清白蛋白的缓冲液,其中含ProClin300做为防腐剂。
校准品A~F目标浓度分别为0、1 pmol/L、3 pmol/L 、6.5 pmol/L、12 pmol/L、40pmol/L。
校准品具体浓度详见标签及试剂盒参数IC卡。
d) 发光液发光液A主要成份为鲁米诺,发光液B主要成份为过氧化脲,两者均以pH8.6的Tris-HCl缓冲液配制。
e) 包被微孔板包被有羊抗鼠白色聚苯乙烯微孔板,用铝箔袋真空包装。
f) 质控品(备选)以正常人血清为基质制备的冻干品,其中含ProClin300做为防腐剂,其靶值浓度范围QCⅠ为2.00 pmol/L~8.00 pmol/L,QCⅡ为9.00 pmol/L~24.00 pmol/L。
质控品具体浓度详见质控品参数表。
不同批号试剂盒中的相同组分不能互换。
2.1 外观a)液体组分应澄清,无沉淀或絮状物,实际装量应不小于标示装量;b)冻干组分呈白色或淡黄色疏松体,加水后应在3分钟内完全溶解;c)所有组分均无包装破损,标示清楚。
2.2 准确度使用试剂盒校准品校准后测定企业工作参考品,企业工作参考品的实测浓度与标示浓度的偏差在±15%之间。
2.3 线性用Logit-Ln数学模型拟合,在[1,40] pmol/L范围内,剂量-反应曲线相关系数(r)的绝对值应不低于0.9900。
2.4 精密度2.4.1分析内精密度:CV≤10%2.4.2分析间精密度:CV≤15%2.4.3批间精密度:CV≤15%2.5空白限试剂盒空白限应不高于1.0 pmol/L。
FT3作业指导书

进样分析,将标本按在Workplace菜单中输入的标本号顺序在样本架上排好,放入进样盘内,按START键,输入该批上机标本的起始标本号,再点START键,仪器自动开始推架检测标本。
8.参考范围
3.1-6.8 pmol/L (2.0-4.4 pg/mL)
每个实验室必须调查各自患者群体的参考范围变异性,必要时根据具体情况制订自己的参考范围。
9.分析性能
10.干扰因素
该方法不受黄疸(胆红素<37mg/dl)、溶血(血红蛋白<2g/dl)、脂血(脂质<1500mg/dl)生物素<20ng/ml等干扰。
PreciControl Universal质控液1(浅褐色瓶盖):1瓶3ml,以人血清为基质;经过防腐处理。
PreciControl Universal质控液2(褐色瓶盖):1瓶3ml,以人血清为基质;经过防腐处理。
其他所需材料:
常规实验设备
Elecsys E 170/E 411
Elecsys系统清洗液(SysClean),货号11298500
6.质量控制
用PreciControl Universal质控品1和2。质控品1和质控品2至少每24小时或每一次定标后测定一次。质控间隔期应适用于各实验室的具体要求。检测值应落在确定的范围内,如出现质控值落在范围以外,应采取校正措施。
7.计算方法
分析仪自动计算每份标本的测定浓度,单位为pmol/l或pg/ml。
接受高剂量生物素(>5mg/天)治疗的病人,至少要等最后一次摄入生物素8小时后才能采血。
游离三碘甲腺原氨酸(Free T3)标准操作规程

游离三碘甲腺原氨酸(Free T3)标准操作规程1.【实验目的】为了保证游离三碘甲腺原氨酸测定结果的准确性,以及可靠性。
2.【职责】2.1 实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.2 本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
3.【样品类型及实验前准备】3.1 样本类型:血清和血浆,稳定性: 2-8℃可稳定6天,如需存放大于6天时,请于-20℃或更低的温度下保存。
3.2 患者准备:实验前正常饮食,晨起空腹,安静状态下抽取静脉血,条件特殊情况下可非空腹抽血检测。
3.3 容器,添加剂类型:血清(包括在血清分离器管中采集的血清),血浆(EDTA三钾、肝素锂、肝素钠),使用玻璃管或塑料管分离样本。
3.4 仪器设备:雅培ARCHITECT i1000SR, 低速离心机3.5 实验试剂:3.5.1.1 ARCHITECT Free T3试剂盒(6C28)(绵羊)包被的磁性微粒子抗T3吖啶酯标记的T33.5 .1.2其他试剂:激发液、预激发液、清洗缓冲液(需另行配置)3.5.2校准品:名称:美国雅培i2000SR 游离T3校准品 LIST NO.: 6C48--01规格:CAL 1: 1.4pg/mL 1LX4mlCAL 2: 30pg/mL 1LX4ml 3.5.3质控品名称:美国雅培i1000SR 游离T3质控品 LIST NO:6C48-10水平浓度(pg/mL ) 范围(pg/mL ) 体积(ml)质控L 3.1 2.02 - 4.09 8质控M 6.0 4.20 - 7.80 8质控H 10.5 7.88 - 14.18 84.【实验原理】ARCHITECT i1000SR 游离T3是采用化学发光微粒子免疫分析(ChemiluminesentMicroparticle ImmunoAssay, CMIA)技术,两步法对待测样品中的游离三碘甲腺原氨酸(游离T3)进行定量检测。
游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求国赛

2.性能指标2.1试剂条性能指标2.1.1外观试剂盒组分齐全,内外包装均完整,标签清晰,液体试剂无渗漏,试剂条中第7孔内组分为棕色含固体微粒的液体或含棕色固体沉淀的透明液体,其余皆为透明液体,无悬浮物、无沉淀、无絮状物。
172.1.2装量孔位2液体装量不低于80μL,孔位3,4,5液体装量均不低于380μL,孔位7液体装量不低于45μL,孔位10液体装量不低于85μL,孔位12液体装量不低于130μL。
2.1.3空白限不大于0.5pg/mL。
2.1.4准确度相对偏差应在±10%以内。
2.1.5线性试剂盒在1pg/mL~30pg/mL区间内,线性相关系数的绝对值(|r|)应不低于0.9900。
2.1.6精密度2.1.6.1批内精密度用同一批次的试剂盒,质控品测定结果的变异系数(CV)应不大于10%。
2.1.6.2批间精密度在多个不同批次的试剂盒之间,质控品测定结果的变异系数(CV)应不大于15%。
2.2校准品性能指标2.2.1外观校准品CAL1与CAL2均为冻干块。
加入纯水后在10min内溶解,无沉淀或絮状物。
172.2.2校准品准确度校准品CAL2测试结果偏差应在±10%之内。
校准品CAL1为零浓度校准品除外。
2.2.3校准品均匀性校准品C A L2变异系数CV不大于10%,校准品C A L1为零浓度校准品除外。
2.3质控品性能指标2.3.1外观质控品为冻干块,加入纯水后在10min内溶解,无沉淀或絮状物。
2.3.2质控品准确度测试结果应在靶值范围之内。
2.3.3质控品均匀性变异系数CV不大于10%27。
游离三碘甲状腺原氨酸测定SOP

性。
2.测定方法竞争性结合酶免疫检验。
3. 测定原理Access Free T3 测定是一种竞争结合免疫法测定,将样本添加到含碱性磷酸酶结合物抗T3 单克隆抗体的反应管中。
在温育过程中,样本中的游离T3 与抗T3 抗体发生反应。
然后将包被着链霉亲和素和生物素化T3 相似物的微粒添加到混合物中。
抗T3 抗体上的未结合位点通过T3 相似物与微粒相结合。
在反应管内温育完成后,结合在固相上的物质将置于一个磁场内被吸住,而未结合的物质被冲洗除去。
然后,将化学发光底物 Lumi-Phos* 530添加到反应管内,然后由照度计对反应中所产生的光进行测量。
所产生光的量与样本内游离T3 的浓度成反比。
样本内分析物的量由所储存的多点校准曲线来确定。
4.性能参数无须输入操作参数,仪器根据预设的分析项目参数和试剂条码的信息自动进行分析。
标本量125 µL。
4.1 精密度:批内CV<12.5%。
4.2 分析范围:0.3 ~ 30.0 pg/ml (0.4 ~ 50.0 pmol/L ) 。
4.3 灵敏度:0.3 pg/ml。
4.4 方法的有限性及干扰因素:胆红素10mg/L、TG 18 g/L、肝素、Hb 2.5 g/L在检测允许的精密度范围内对结果没有影响。
5.原始样本系统5.1 总则:符合本室《检验标本采集手册》5.2 常规静脉采血约2ml,不抗凝,置普通试管中。
或采用含分离胶的真空采血管。
5.3 检验申请单和血标本试管标上统一且唯一的标识符。
5.4 急诊标本采集后,在检验申请单上填写标本采集时间。
5.5 标本采集后与检验申请单一起及时运送至检验科。
专人负责标本的接收并记录标本的状态,对不合格标本予以拒收。
5.6 标本拒收标准5.6.1 标本量过少。
5.6.2 检验申请单上姓名或条码与标本上姓名或条码不一致。
5.6.3 检验项目与标本类型不符,或抗凝剂不符。
5.6.4 标本送检时已放置时间过久。
5.6.5 输液时在同侧血管抽血。
游离三碘甲状腺原氨酸(FT3)校准品产品技术要求hkt
游离三碘甲状腺原氨酸(FT3)校准品
组成:
游离三碘甲状腺原氨酸(FT3)校准品S0-S5为冻干粉,校准品S0含添加0.1%生物防腐剂的牛血清,校准品S1-S5为在含0.1%生物防腐剂的牛血清中添加游离三碘甲状腺原氨酸(FT3)抗原。
注:1、校准品靶值批特异、具体浓度详见标签。
2、校准品溯源至企业工作校准品,并与已上市产品比对赋值。
适用范围:游离三碘甲状腺原氨酸(FT3)校准品与本公司游离三碘甲状腺原氨酸(FT3)测定试剂盒(磁微粒化学发光法)配套使用,用于人血清中游离三碘甲状腺原氨酸(FT3)测定系统的校准。
2.1 外观
校准品包装标签应清晰,无磨损;冻干粉呈疏松体,溶解后的液体澄清透明,无沉淀或絮状物。
2.2 溯源性
根据GB/T 21415-2008的有关规定,提供所用校准品的来源、赋值过程及测量不确定度等内容,溯源至企业工作校准品,并与已上市产品比对赋值。
2.3 准确度
检测企业工作校准品,其测量结果的相对偏差应在±10%范围内。
2.4 均匀性
2.4.1 瓶内均匀性
各浓度点(除零外),变异系数(CV)应不高于10%。
2.4.2 瓶间均匀性
各浓度点(除零外),变异系数(CV)应不高于15%。
2.5 稳定性
2.5.1 复溶稳定性
校准品复溶后,-20℃以下储存,有效期15天,在效期内赋值结果的变化趋势不显著。
2.5.2 效期稳定性
校准品原包装2℃~8℃储存,有效期12个月,在效期内赋值结果的变化趋势不显著。
FT3操作规程

4.1时间分辨荧光分析仪;
4.2微孔洗涤机;
4.3微孔振荡器;
5.操作步骤
5.1.试剂的准备
⑴洗涤液:将40ml浓缩洗液和960ml蒸馏水在干净的洗液瓶中混合,作为工作洗涤液。
⑵加入1.0ml蒸馏水于冻干铕标记小瓶中,待铕标记充分溶解(静置至少30分钟)。
⑶加入1.0ml蒸馏水于各冻干校准品小瓶中,待校准品充分溶解(静置至少30分钟)。
9.11所有的样本和本试剂盒应作为潜在的传染原看待,按传染病实验室检查规程操作。
9.12如对实验结果有疑问,应重复试验。
9.13为保证实验的准确性,处理后得到的血样应不含纤维蛋白、红细胞、血脂等,并要保证血样吸取的量的准确性,否则容易引起测量值的差异。
9.14本试剂盒应置2—8℃保存,有效期参考瓶上所贴标签。
⑷将分析缓冲液、校准品、待测样品和所需数量的微孔反应条平衡至室温(20~250C)。
⑸使用前一小时内,按照需要用量以分析缓冲液稀释铕标记(1:100)(详见操作流程图)
5.2.吸取25μl校准品和待测样品,加入反应板微孔内。
5.3.在各微孔内加入150μl已稀释的铕标记溶液,在室温(20~25℃)下慢速振动1小时。
7.临床意义
血清中约80%以上的T3由T4脱碘生成,其余直接由甲状腺合成。进入血液循环的T3大部分与结合蛋白结合,仅约0.3% T3呈游离状态。FT3被认为是循环血中甲状腺激素的活性部分。FT3浓度分析不受血液中甲状腺激素结合蛋白浓度的影响,是甲状腺功能亢进的敏感指标,并且是评价T4-替代疗法疗效的常用分析手段。
c.校准品(A、B、C、D、E、F):一套,1.0ml/瓶(冻干品)
d.浓缩洗液:一瓶,40ml
e.荧光增强液:一瓶,30ml
游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求tgkx

游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)适用范围:本试剂盒主要用于体外定量测定人血清中的游离三碘甲状腺原氨酸(FT3)含量。
1.1 规格48人份/盒,96人份/盒。
1.2 主要组成成分2.1 外观液体组分澄清,无沉淀或絮状物;其它组分无包装破损,标签外观完整、无脱落、标签标识清晰。
2.2 装量装量不少于标示值。
2.3 准确性回收率应在90.0%~110%范围内。
2.4 剂量-反应曲线线性相关系数在[2.9,28]pmol/L范围内,用log-logit数学模式拟合,剂量-反应曲线相关系数(r)的绝对值应不小于0.9900。
2.5 精密度2.5.1 重复性(C.V%)应不高于15.0%;2.5.2 批间差(C.V%)应不高于20.0%。
2.6 最低检出量应不高于2.00pmol/L。
2.7 质控血清测定值应在允许的范围之内。
2.8 特异性与浓度为320nmol/L 的T4反应,测定结果应小于2.00 pmol/L;与浓度为10nmol/L 的rT3反应,测定结果应小于2.00 pmol/L。
2.9 稳定性2.9.1 37℃放置3天,测定结果应符合上述2.1~2.7项要求。
2.9.2 成品试剂盒2~8℃存放6个月后,测定结果应符合上述2.1~2.7项要求。
2.10 校准品溯源性按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》要求,该校准品溯源至本公司内部工作校准品,通过与进口试剂盒(Siemens Healthcare Diagnostics Inc.)比对赋值。
游离T3(FT3)测定

游离T3(FT3)测定1. 原理采用夹心法原理、电化学发光法(E CL)定量检测FT3。
待测样本中的F T3与三联吡啶钌(R u(b py)32+)标记的单抗和生物素标记的单抗结合生成抗原抗体复合物。
该复合物与亲和素包被的磁珠结合,吸附于检测室(Cel l)电极表面,经氧化还原反应,三联吡啶钌与TP A作用释放光子,以光信号的强弱定量标本中检测物的含量。
2. 标本采集:2.1标本采集前病人准备:受检者应空腹。
2.2标本种类:血清或血浆。
2.3标本要求:采集血清样本,取被检者静脉血,用无菌取血针抽取病人静脉血3ml,收集干燥试管中,室温放置不超过8小时,2000转/分离心20分钟备用.采集血浆样本,用无菌取血针取被检者静脉血3m l,收集于含有ED TA 作抗凝剂的试管中,室温放置不超过8小时,2000转/分离心20分钟备用。
3. 标本储存:待测样本室温不超过8小时,4-8℃不超过72小时,-20℃可长期保存,避免反复冻融。
4. 标本运输:室温运输。
5. 标本拒收标准:细菌污染,严重溶血或脂血标本不能作测定。
6. 试剂:6.1试剂名称:游离T3试剂盒。
6.2试剂生产厂家:罗氏公司6.3包装规格:100T est/盒6.4试剂盒组成:游离T3诊断试剂。
6.5试剂储存条件及有效期:试剂盒贮存2-8℃条件,有效期见条形码。
7. 仪器设备:7.1仪器名称:罗氏全自动电化学发光免疫分析仪7.2仪器厂家:罗氏公司7.3仪器型号:c oba s e 4117.4仪器校准:本仪器校准由厂家工程师负责校准8. 操作步骤:8.1样本处理:取待测样本血清或血浆(尿液)置于样本杯中(不能有纤维蛋白,不能有气泡)。
8.2仪器准备:检查纤维杯,反应杯数量满足实验需要,废物桶和废液桶是否连接好,仪器的光路是否正常,环境温度是否符合要求,打印机的连接。
8.3试剂准备与检查:从冰箱取试剂放入仪器,检查所有试剂量是否足够,是否在有效期内。
游离三碘甲腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求beifang
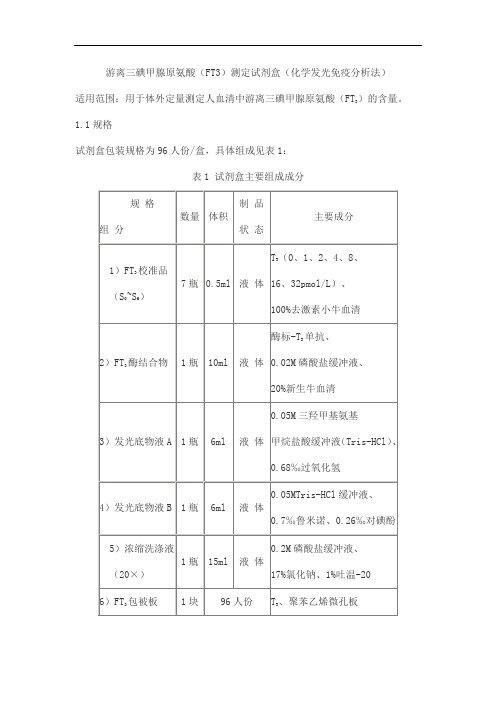
游离三碘甲腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)
)的含量。
适用范围:用于体外定量测定人血清中游离三碘甲腺原氨酸(FT
3
1.1规格
试剂盒包装规格为96人份/盒,具体组成见表1:
表1 试剂盒主要组成成分
2.1外观和物理检查
液体组分应澄清透明,无沉淀或絮状物,包被板的真空封袋应无破损漏气现象。
各组分装量不少于表1中要求。
2.2线性
用百分结合率对数(Log-Logit)数学模型拟合,在1~32pmol/L范围内,剂量-反应曲线相关系数的绝对值(|r|)应不低于0.9900。
2.3精密度
2.3.1批内精密度(CV%)应不高于15.0%。
2.3.2批间精密度(CV%)应不高于15.0%。
2.4最低检出限
试剂盒最低检出限应不高于0.5pmol/L。
2.5特异性
)结果应小于10.0pmol/L;
检测浓度为100ng/ml的甲状腺素(T
4
)结果应小于1.0pmol/L。
检测浓度为50ng/ml的反三碘甲腺原氨酸(rT
3
2.6稳定性
2.6.1 37℃放置7天后,测定结果应符合上述2.1~2.4要求。
2.6.2 2~8℃放置12个月后,测定结果应符合上述2.1~2.4要求。
总三碘甲状腺原氨酸检测作业指导书医学检验

《文件已阅声明表》《Procedure circulation form》文件名称: 总三碘甲状腺原氨酸检测作业指导书表号: KM-MP03•02•02已阅声明:本人承诺已了解此文件中的相关内容,今后的工作中将严格按照此文件执行,不随意对外传阅此文件,如有因与文件不相符的操作,责任由本人承担。
(I have understood the relevant content of the document. I will keep the document secret and be responsible to properly perform procedure)阅读人签名表姓名(NAME)职务(POSITION)签名(SIGNATURE)签名日期(DATE)文件修改记录页(Procedure amendment form)表号: KM-MP03•02•03 序号NO. 页码(Page) 内容更改说明(Description of Modifiedcontents)审批人(Approvedby )批准生效日期(Approveddate)1 换版文件信息表(Procedure information form)表号: KM-MP03•02•04文件名Title of Doc.(Doc.Code)总三碘甲状腺原氨酸检测作业指导书(KM-SOP0300•303)版本号(Edition No.) Edition 生效日期(Operativedate)2008-03-13文控部门(Doc. Control Dept.)实验室文控室回顾人签名/日期(Reviewed by : Signature/Review date) 回顾日期(Reviewdate)回顾人员签名( Signature )替代文件(Replaces) 总三碘甲状腺原氨酸检测作业指导书 (Edition存放地点(Location)/持有人(Holder)No. Location (Holder) No. Location (Holder)1 实验室文控室(陈彬)2 化学发光室(段学成)作者签名/日期(Authorsignature/date)袁意彬审批人签名/日期(Authorized by :Signature/Date)陈建波接收人签名/日期(Receiptor/Date)副本数(Copy No.) 本文件是第个文件拷贝 / 共发放 2个文件拷贝。
人游离三碘甲状腺原氨酸(Free-T3)酶联免疫分析(ELISA)

人游离三碘甲状腺原氨酸(Free-T3)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用人血清,血浆及相关液体样本中游离三碘甲状腺原氨酸(Free-T3)的含量。
试剂盒性能:1.样品线性回归与预期浓度相关系数R值为0.95以上。
2.批内与批见应分别小于9%和11%检测范围:请来电咨询保存条件及有效期:1.试剂盒保存:;2-8℃。
2.有效期:6个月注意事项:1.试剂盒从冷藏环境中取出应在室温平衡15-30分钟后方可使用,酶标包被板开封后如未用完,板条应装入密封袋中保存。
2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。
3.各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。
一次加样时间最好控制在5分钟内,如标本数量多,推荐使用排枪加样。
4.请每次测定的同时做标准曲线,最好做复孔。
如标本中待测物质含量过高(样本OD值大于标准品孔第一孔的OD值),请先用样品稀释液稀释一定倍数(n倍)后再测定,计算时请最后乘以总稀释倍数(×n×5)。
5.封板膜只限一次性使用,以避免交叉污染。
6.底物请避光保存。
7.严格按照说明书的操作进行,试验结果判定必须以酶标仪读数为准.8.所有样品,洗涤液和各种废弃物都应按传染物处理。
9.本试剂不同批号组分不得混用。
10. 如与英文说明书有异,以英文说明书为准。
实验原理:本试剂盒应用双抗体夹心法测定标本中人游离三碘甲状腺原氨酸(Free-T3)水平。
用纯化的人游离三碘甲状腺原氨酸(Free-T3)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入游离三碘甲状腺原氨酸(Free-T3),再与HRP标记的游离三碘甲状腺原氨酸(Free-T3)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的游离三碘甲状腺原氨酸(Free-T3)呈正相关。
游离三碘甲状腺原胺酸检测作业指导书医学查验

《文件已阅声明表》《Procedure circulation form》文件名称: 游离三碘甲状腺原胺酸检测作业指导书表号: KM-MP03•02•02文件修改记录页(Procedure amendment form)表号: KM-MP03•02•03文件信息表(Procedure information form)表号: KM-MP03•02•04游离三碘甲状腺原胺酸检测作业指导书(Analysis of Free T-3 by IMMULITE 2000)1. 原理(Test principle):基于类似物的竞争法化学发光免疫检测:包括免疫反映和化学反映,利用在化学反映中释放大量自由能查声激发态中间体,当其回到稳固的基态时,同时也发射出光子,利用发光信号测量仪对所发出的光量子进行定量测量。
2. 样本搜集和贮存(Specimen Collection and Storage):标本搜集(Specimen collection):类型(Type):血清(Serum);用量(Volume),仪器加样量(Sampling volume)100μL拒收标本(Specimen rejection):EDTA抗凝血,严峻脂血或污染样本应拒收。
推荐利用超速离心清除脂血(lipoprotein)样本。
溶血(hemolysis)样本提示样本在送达实验室之前处置不妥,因此检测结果将受到影响,应予以注意。
血清(serum)样本在未充分凝集前离心将致使纤维蛋白的存在。
为避免纤维蛋白对结果的影响必需确保离心处置前样本已经完全充分凝集。
对于正在同意抗凝剂医治的病人样本,需要延长凝集时刻。
源于不同生产商的血样搜集试管,由于原材料和添加剂不同,包括凝胶或物理涂层、促凝剂和/或抗凝剂,可能致使取得不同的结果。
本试剂盒没有对所有可能应用的搜集管类型进行测试。
标本贮存条件(Specimen storage conditions):2-8℃2天;-20℃2个月;十天后处置标本.3. 试剂(Reagent):美国DPC IMMULITE 2000 原装试剂。
游离三碘甲状腺原氨酸操作规程

1 检验申请单独检验项目申请:游离三碘甲状腺氨酸测定 (缩写FT3);组合检验项目申请:甲状腺功能检查组合;临床医生根据需要提出检验申请。
2 标本采集与处理2.1标本采集2.1.1常规静脉采血约2ml,不抗凝,置普通试管中。
或采用含分离胶的真空采血管。
2.1.2检验申请单和血标本试管标上统一且唯一的标识符。
2.1.3急诊标本采集后,在检验申请单上填写标本采集时间。
2.1.4标本采集后与检验申请单一起及时运送至检验科。
专人负责标本的接收并记录标本的状态,对不合格标本予以拒收。
2.1.5 下列标本为不合格标本2.1.5.1标本量不足:少于0.3ml的全血标本,或少于0.1ml的血清或血浆。
2.1.5.2对于测定和吸样有干扰的标本:如近期使用鼠源性单克隆抗体诊断后采取。
2.1.5.3无法确认标本与申请单对应关系的。
2.1.5.4其他如标识涂改、标本试管破裂等。
2.2标本保存2.2.1接收标本后在30min内将标本离心分离出血清, 避免溶血。
2.2.2标本保存时间:室温(15~25℃)下可稳定8h,普通冰箱中(2~8℃)稳定48h。
需较长时间保存应将血清存放于-20℃。
冰冻标本仅可冻融一次。
为避免标本中水分挥发使血清浓缩,对保存时间超过1d的标本均加塞密闭或覆盖湿巾。
2.2.3已完成测试的标本保持完整的识别号,置2~8℃冰箱内保存7d。
2.3标本采集的注意事项2.3.1采血前使受检者保持平静、松弛、避免剧烈活动。
2.3.2采血后应使血液充分凝固,离心后的血清中不能含有颗粒物或微量纤维蛋白;可使用选用肝素、EDTA抗凝的血液标本。
3 方法原理采用竞争结合化学发光免疫分析法,其检测原理如下:第一步:将样本-碱性磷酸酶标记的T3抗体加入反应管中,经过孵育,样本中的FT3与标记抗体结合;第二步:将链霉亲和素包被的磁珠及生物素化的T3加入反应管中,经过孵育,样本中FT3和生物素化T4竞争性的结合标记抗体,形成生物素化的T3-标记抗体复合物,前者可以通过生物与磁珠上链霉亲和素特异性结合,从而被固定在固相上,而其余未结合物质到固相上的物质则通过下一步的清洗步骤除去;第三步:将化学发光物添加到反应管内,发光底物(AMPPD)被碱性磷酸酶所分解,脱去一个磷酸基,生成一个不稳定的中间产物,该中间产物通过分子内发态返回基态时,产生化学发光,再通过光电倍增管对反应中所产生的光子数进行测量。
游离三碘甲状腺原氨酸测定标准操作规程

游离三碘甲状腺原氨酸测定标准操作规程1检验原理:采用两步法免疫检测,运用化学发光微粒子免疫检测(CMIA)技第一步,术与灵活的检测模式的结合,测定人血清和血浆中的游离(未结合)T3o将样本和T3抗体包被的顺磁微粒子混合。
样本中的T3(未结合型)与T3抗体包被的微粒子结合。
冲洗后进入第二步,加入哇咤酯标记的T3结合物。
随后将预激发液和激发液加入反应混合物中;测量化学发光反应结果,以相对发光单位(RLUs)表示。
样本中的游离T3含量和ARCHITECTi光学系统检测到的RLUs值之间成反比。
2.试剂主要组成部分:2.1试剂盒微粒子:三碘甲状腺原氨酸抗体(绵羊)包被的微粒子,储存于含有绵羊IgG 稳定剂的2-(N-吗啡咻)乙磺酸(MES)缓冲液中。
最低浓度:0.085%固体物质。
防腐剂:抗菌剂。
结合物:口丫咤酯标记的三碘甲状腺原氨酸结合物,储存于含有氯化钠(NaCI)和聚乙二醇辛基苯基酸(TritonXT00)稳定剂的柠檬酸盐缓冲液中。
最低浓度:0.33ng∕mL.防腐剂:抗菌剂。
2.2需要但未提供的试剂预激发液:预激发液含有1.32%(W/V)过氧化氢激发液:激发液含有0.35N氢氧化钠浓缩清洗缓冲液:浓缩清洗缓冲液含有磷酸盐缓冲液。
防腐剂:抗菌剂。
3.样本要求:人血清(包括采集于血清分离管中的血清)或采集于肝素、肝素锂或EDTA钾抗凝管中的血浆。
血清和血浆样本中应不含纤维蛋白、红细胞或其他颗粒物质。
2-8°C可保存6天;-10℃以下可保存6个月。
样本应避免反复冻融。
4.检验方法:仪器法(详见雅培i1000标准操作规程)1.1游离三碘甲状腺原氨酸项目通过四参数Logistic曲线拟合数据约简法(4PLC,Y加权)生成一条校准曲线6.2结果单位转换:浓度(pg∕mL)XL536=浓度(pmol∕L)7.检验方法的局限性7.1将检测结果用于诊断时,应与其他数据:如症状、其他甲状腺检查结果、临床表现等结合使用。
医学检验·检查项目:游离三碘甲状腺原氨酸(FT3)_课件模板

医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
ห้องสมุดไป่ตู้相关疾病:
腺肿、甲亢合并妊娠、老年人甲状腺功能 亢进症、甲亢性心脏病、亚临床甲状腺功 能减退症、甲状腺功能减退伴发的精神障 碍。
谢谢!
相关检查: 游离甲状腺素、血清甲状腺素、总甲状腺 素、促甲状腺激素。
医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
相关症状: 新陈代谢旺盛、碘甲亢、青春期甲亢、妊 娠期间甲亢、潮汗、心悸伴心率异常。
医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
相关疾病:
甲状腺功能异常伴发的精神障碍、单纯性 甲状腺肿、静止性淋巴细胞性甲状腺炎、 老年人甲状腺功能低下、老年甲状腺功能 减退症、甲状腺激素抵抗综合征、甲状腺 功能减退症、地方性甲状腺肿、地方性克 汀病、亚临床型克汀病、碘源性甲亢、高 碘性甲状腺肿、放射性甲状腺炎、非甲状 腺性的病态综合征、结节性甲状
医学检验·各论 游离三碘甲状腺原氨酸
(FT3) 内容课件模板
医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
别名: 血清游离三碘甲状腺原氨酸。
医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
简介:
T3是由甲状腺滤泡细胞合成及分泌的 激素。FT3约占T3的0.3%,能透过细胞膜 进入组织细胞,发挥生理效应,其浓度与 组织中的三碘甲状腺原氨酸浓度一致,也 与机体代谢状态一致,对非甲状腺疾病也 有诊断价值。临床上常用RIA法测定。
医学检验·各论:游离三碘甲状腺原氨酸(FT3) >>>
临床意义: 增高:见于甲亢、三碘甲状腺原氨酸
FT3中文说明书

定标频率:每批试剂必须用新鲜试剂(试剂经仪器注册24小时以内) 标定一次,如再次标定即根据下列要求: E170/Elecsys2010: · 一个月(同一批号试剂) · 4天(放置仪器上的同一试剂盒) Elecsys1010: · 每一试剂盒做一次 · 7天(室温20-25 度) · 3天(室温25-32 度) 各种分析仪均适用的情况: ·根据要求进行标定:如质控结果超出范围时。 质控: Elecsys通用质控品l和2以及其它合适的质控品。各浓度区域的质控至少每 24工作时、每个试剂盒或每一次定标后测定一次。质控间隔期应适用于各
定分析仪。
· Elecsys测量池清洗液(CleanCell M)货号12135027
· Elecsys系统缓冲液/测量池清洗液预热杯(PC/CC-Cup)货号03023141
概述:
· Elecsys反应杯/吸样头盒(AssayCups/AssayTips Combimagazine M)
三碘甲腺原氨酸(T3)是血清中的甲状腺激素之一,起调节代谢作用。
· Elecsys 1010反应杯(Assay Cup) 货号11706829 Elecsys 2010反应杯(Assay Cup) 货号11706802
稀释: 标本不可以稀释,因为血中的T3是以游离状态以及结合状态两种形式存在, 并处在平衡状态中。结合蛋白质浓度的变化可改变这种平衡。
正常参考值: 2.8-7.1pmol/l或1.8-4.6pg/ml(范围:第2.5百分位-第97.5百分位, n=962)。 如有必要,各实验室应自己测定一个正常值范围。
开封后,2-8 度12周; 放在E170上,5周; 放在Elecsys2010上,8周; 放在Elecsys1010上,7周(使用后放回2-8度 ;如置20-25 度,约20 小时)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
PreciControl Universal质控液1(浅褐色瓶盖):1瓶3ml,以人血清为基质;经过防腐处理。
PreciControl Universal质控液2(褐色瓶盖):1瓶3ml,以人血清为基质;经过防腐处理。
其他所需材料:
常规实验设备
Elecsys E 170/E 411
Elecsys系统清洗液(SysClean),货号11298500
Elecsys适配器(Adapterfor SysClean),货号11933159,
Elecsys反应杯(CUP),货号11706829
Elecsys加样头(TIP),货号11706802
4.仪器和校准
使用仪器:瑞士罗氏诊断公司生产Elecsys 2010/E 170/E 411全自动电化学发光免疫自动分析仪
R2:生物素化的T3(黑盖),1瓶,14ml。浓度高于5mg/l,磷酸缓冲液0.1mol/l,pH7.4,含防腐剂。
校准品:
Cal 1FT3定标液1(白盖),2瓶,1.0ml/瓶,以人血清为基质;经过防腐处理。
Cal 2FT3定标液2(黑盖),2瓶,1.0ml/瓶,以人血清为基质;经过防腐处理。
质控品:
标本、定标液和质控品在测定前应预温到室温。
3.试剂、校准品、质控品和其他所需材料
采用罗氏原装配套试剂。
试剂:
M:链霉亲和素包被的微粒(透明瓶盖),1瓶,12ml。粒子浓度0.72mg/ml,生物素结合能力:470ng生物素/mg粒子。含
防腐剂。
R1:Ru(bpy)32+标记的羊抗T3多克隆抗体(灰盖),1瓶,14ml,浓度高于75mg/l,磷酸缓冲液0.1mol/l,pH7.4,含防腐剂。
用光电倍增管进行测定。通过检测仪的定标曲线得到最后检测结果(定标曲线通过2定标点和试剂条形码提供的主曲线成)。
2.标本要求
血清:按标准常规方法采集。
血浆:肝素、EDTA-K3、枸橼酸钠、氟化钠/草酸-K抗凝均可。标本在2-8度可稳定7天,-20oC可稳定1个月,标本可
冻融1次。有沉淀的标本使用前需离心,加热灭活的标本不可使用,标本和质控品禁用叠氮钠防腐。
批量常规标本的输入,在主菜单下选择Workplace- Testslection,在Sequence No栏输入起始标本号,然后选择该标本所需做的单个项目或组合项目,点REPEAT,输入该批标本的最后一个标本号,点OK即可。
进样分析,将标本按在Workplace菜单中输入的标本号顺序在样本架上排好,放入进样盘内,按START键,输入该批上机标本的起始标本号,再点START键,仪器自动开始推架检测标本。
Elecsys E 170分析仪所需材料:
Elecsys系统缓冲液(ProCell M),货号12135019
Elecsys检测池洗液(CleanCell M),货号12135027
ElecsysPC/CC杯,货号03023141
Elecsys清洗液(ProbeWash M),货号03005712
Elecsys反应杯/加针头/废物袋(CUP/TIP),货号12102137
6.质量控制
用PreciControl Universal质控品1和2。质控品1和质控品2至少每24小时或每一次定标后测定一次。质控间隔期应适用于各实验室的具体要求。检测值应落在确定的范围内,如出现质控值落在范围以外,应采取校正措施。
7.计算方法
分析仪自动计算每份标本的测定浓度,单位为pmol/l或pg/ml。
仪器校准:每批FT3试剂盒必须用新鲜试剂和FT3Cal 1,Cal 2定标一次。另外,以下情况需要再次定标:
·)
各种分析仪均适用的情况:根据要求进行标定:如质控结果超出范围时;根据规定进行多次标定。
5.操作步骤(以E 170为例)
5.1校准操作步骤:
在Calibration—Status菜单中看定标结果,点Calibration Result键看定标结果,点Reaction Monitor键看每个定标物的反应曲线。
5.2样本检测程序:
单个样本输入,在主菜单下选择Workplace- Testslection,在Sequence No栏输入标本号,然后选择该标本所需做的单个项目或组合项目,点SAVE键,样本号自动累加。
1.分析原理
采用竞争法原理,整个过程18分钟完成。
·第1步:30μl标本与钌(Ru)标记的抗T3抗体混匀。
·第2步:加入链霉亲和素包被的微粒和生物素化的T3。后者占据标记抗体上仍然游离的结合位点,形成抗体-半抗原复合物。
形成的免疫复合物通过生物素、链酶亲和素之间的反应结合到微粒上。
·第3步:反应混和液吸到测量池中,微粒通过磁铁吸附到电极上,未结合的物质被清洗液洗去,电极加电压后产生化学发光,
Elecsys系统清洗适配器(SysCleanAdapterM),货号03027651
Elecsys E 411分析仪所需材料:
Elecsys系统缓冲液(ProCell),货号11662988
Elecsys测量池清洗液(CleanCell),货号11662970
Elecsys系统清洗液(SysWash),货号11930346
8.参考范围
3.1-6.8 pmol/L (2.0-4.4 pg/mL)
每个实验室必须调查各自患者群体的参考范围变异性,必要时根据具体情况制订自己的参考范围。
9.分析性能
10.干扰因素
该方法不受黄疸(胆红素<37mg/dl)、溶血(血红蛋白<2g/dl)、脂血(脂质<1500mg/dl)生物素<20ng/ml等干扰。
