游离三碘甲状腺原氨酸(FT3)测定试剂盒(电化学发光免疫分析法)产品技术要求lztk
血清三碘甲状腺原氨酸(T3)实验室检测

血清三碘甲状腺原氨酸【试剂名称】通用名称:血清三碘甲状腺原氨酸(T3)测定试剂盒(化学发光法)1. 用途本试剂用于定量测定人血清或血浆内三碘甲状腺原氨酸(T3)的含量。
本方法适用标本的浓度范围为0-10 ng/ml (0-15.5 nmol/l )。
该测试必须在MAGLUMI ® 1000 分析仪上进行。
2. 概述与说明- 健康人中,甲状腺每天大约分泌5-10μg 的T3。
然而,循环的T3最主要由外周脱碘作用产生,从而,每天总T3的分泌水平高达20μg (5)。
在血清中,甲状腺激素与载体蛋白结合,只有它们的游离部分是生理活性的。
- 定量测定T3在可疑甲状腺疾病中的临床意义主要在于诊断及评估甲状腺机能亢进(2,3)。
尤其在单独的T3型甲亢中, 观察到T3浓度升高,TBG 及T4水平正常。
在甲状腺外科手术切除及用I-131治疗后,T3与T4浓度可能保持一个很高的水平甚至还会升高(甲亢的复发)。
- 在大约50%与甲亢有关的自发性腺瘤病人中发现T3水平的偶尔升高。
这种升高也可出现在早期甲亢、与潜伏性甲亢有关的内分泌性眼疾、甲亢的治疗(甲状腺拮抗剂)过程中、甲状腺肿或非甲状腺肿性碘缺乏及Hashimoto 氏甲状腺炎中(代谢状态可能是正常的)。
3. 测试原理本试剂盒利用免疫发光竞争法的原理检测T3;采用抗T3单克隆抗体标记ABEI ,T3纯抗原标记FITC 。
标本,定标液,(质控液)与ABEI 标记的单抗,FITC 标记的纯抗原,包被有羊抗FITC 抗体的纳米免疫磁性微珠置37℃ 孵育形成免疫复合物,然后外加磁场沉淀,去掉上清液,用洗液循环清洗沉淀复合物1次,直接进入样品测量室,仪器自动泵入发光底物1和2,自动监测3秒钟内发出的相对光强度(RLU )。
T3浓度与RLU 成一定的比例关系,仪器自动拟合计算T3浓度。
4. 试剂4.1试剂组成4.2试剂的准备 在揭开密封纸之前,先轻轻地水平摇晃试剂盒(为了防止泡沫形成!)。
体外诊断试剂 校准品溯源报告 量值传递方案依据 GBT21415-2008ISO17511-2003 FT3测定试剂盒

游离三碘甲状腺原氨酸(FT3)测定试剂盒(免疫荧光法)校准品溯源报告1.目的制备性能稳定的工作校准品,用作游离三碘甲状腺原氨酸(FT3)测定试剂盒(免疫荧光法)的质控控制。
2.范围适用于游离三碘甲状腺原氨酸(FT3)(免疫荧光法)校准品的溯源、制备、赋值。
3.制备过程3.1材料(1)高纯度的三碘甲状腺原氨酸(FT3)抗原(纯度≥99%)。
(2)采用标准小牛血清作为基质。
3.2制备方法取适量高纯度的三碘甲状腺原氨酸(FT3)(纯度≥99%),用标准小牛血清将其稀释成约0.7、6.5、15、35、45pmol/L。
4.浓度测定、赋值过程4.1试剂参考测量程序:Biomerieux,SA生产的游离三碘甲状腺原氨酸检测试剂盒(酶联荧光法),注册证号:国械注进20162400887。
常规测量程序:***生物游离三碘甲状腺原氨酸(FT3)(免疫荧光法)测定试剂盒、干式免疫荧光分析仪;有证参考物质:中检所国家标准品150550-201203。
4.2赋值流程按下图的溯源流程对制备的工作校准品进行赋值。
物质程序实施4.2.1操作步骤4.2.1.1制造商选定测量程序(参考测量程序)的校准按《GB/T21415-2008/ISO17511:2003体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》4.2.2f 要求:制造商选定测量程序应是一个或多个现有一级或二级校准品校准的测量系统。
用参考测量程序重复测量中检所国家标准品150550-201203,对测量结果进行t 检验,验证测量值是否与参考物质的理论值存在显著差异。
在δ未知的情况下,单个平均数的显著性检验—t 检验(t-test)统计量计算公式如下:计量学溯源校准赋值国际公认参考测量程序中检所国家标准品150530-0312制造商工作校准品IVD 制造商内部参考测量程序:Biomerieux,SA 生产的游离三碘甲状腺原氨酸检测试剂盒(酶联荧光法)IVD 常设测量程序本公司产品多次测量制造商产品校准品IVD 制造商常规测量程序临床样本临床检测结果中检所或相关组织***IVD 制造商终端用户ns u x t 0-=参考测量程序校准结果如下:中检所国家标准品150550-201203(15.68pmol/L )参考测量程序测量值16.2315.2116.5614.3915.4814.9614.9114.3614.8616.5716.2615.7616.5016.8615.7715.0416.6216.2814.9315.9815.9817.1416.9517.0414.6115.3716.7616.7915.6314.6916.6717.1116.9515.8414.6017.0015.7916.3216.7115.7115.5714.66中检所国家标准品1150550-201203稀释后的理论值为15.68pmol/L ,经计算,统计量t=1.584<t (0.05,双侧)=2.326,参考测量程序检测结果与理论值差异不明显。
游离三碘甲腺原氨酸(Free T3)标准操作规程

游离三碘甲腺原氨酸(Free T3)标准操作规程1.【实验目的】为了保证游离三碘甲腺原氨酸测定结果的准确性,以及可靠性。
2.【职责】2.1 实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.2 本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
3.【样品类型及实验前准备】3.1 样本类型:血清和血浆,稳定性: 2-8℃可稳定6天,如需存放大于6天时,请于-20℃或更低的温度下保存。
3.2 患者准备:实验前正常饮食,晨起空腹,安静状态下抽取静脉血,条件特殊情况下可非空腹抽血检测。
3.3 容器,添加剂类型:血清(包括在血清分离器管中采集的血清),血浆(EDTA三钾、肝素锂、肝素钠),使用玻璃管或塑料管分离样本。
3.4 仪器设备:雅培ARCHITECT i1000SR, 低速离心机3.5 实验试剂:3.5.1.1 ARCHITECT Free T3试剂盒(6C28)(绵羊)包被的磁性微粒子抗T3吖啶酯标记的T33.5 .1.2其他试剂:激发液、预激发液、清洗缓冲液(需另行配置)3.5.2校准品:名称:美国雅培i2000SR 游离T3校准品 LIST NO.: 6C48--01规格:CAL 1: 1.4pg/mL 1LX4mlCAL 2: 30pg/mL 1LX4ml 3.5.3质控品名称:美国雅培i1000SR 游离T3质控品 LIST NO:6C48-10水平浓度(pg/mL ) 范围(pg/mL ) 体积(ml)质控L 3.1 2.02 - 4.09 8质控M 6.0 4.20 - 7.80 8质控H 10.5 7.88 - 14.18 84.【实验原理】ARCHITECT i1000SR 游离T3是采用化学发光微粒子免疫分析(ChemiluminesentMicroparticle ImmunoAssay, CMIA)技术,两步法对待测样品中的游离三碘甲腺原氨酸(游离T3)进行定量检测。
罗氏中文说明书:甲状腺球蛋白检测试剂盒(电化学发光法)说明书

【产品名称】通用名称:甲状腺球蛋白检测试剂盒(电化学发光法)英文名称:Tg II【包装规格】100测试/盒【预期用途】主要用途用于体外定量测定人血清和血浆的甲状腺球蛋白含量。
Tg的测定能辅助监控甲状腺切除术后的情况。
Elecsys和cobas e 免疫分析仪的工作原理是电化学发光免疫分析“ECLIA”。
临床应用甲状腺球蛋白是一种分子量接近660 kDa的糖蛋白。
4Tg由甲状腺细胞大量合成并释放到甲状腺滤泡腔内。
TSH、甲状腺内碘缺乏、促甲状腺激素免疫球蛋白均可刺激Tg的生成。
Tg对外周甲状腺激素T3和T4的合成起决定作用。
它含有约130种酪氨酸残基,其中一部分在TPO(甲状腺过氧化物酶)和碘化物存在时被碘化为单碘-和二碘酪氨酸(MIT和DIT)。
3随后也是在Tg和TPO的作用下,MIT和DIT偶联结合成T3和T4。
5甲状腺细胞合成Tg以及将Tg转送到滤泡的过程中,少量蛋白可进入血流。
因此无甲状腺疾病的健康个体中也能检出低浓度Tg。
Tg浓度升高在不同的甲状腺疾病中均有报道,桥本氏病、葛瑞夫兹病等。
Tg还有助于鉴别亚急性甲状腺炎和人为甲状腺毒症。
对于先天性甲状腺功能减退症Tg的检测可用于鉴别先天性甲状腺缺失和甲状腺发育不全或其它病理情况。
5,6,7Tg检测主要用于甲状腺全切或次全切术后病人的随访。
由于甲状腺是Tg的唯一已知来源,在甲状腺全切或次全切伴随放射性碘成功消融残留甲状腺组织后,血清Tg浓度将降至极低,甚至检测不到。
对于部分甲状腺切除的病人,检测到的Tg水平取决于手术后残留的甲状腺组织的多少。
若甲状腺全切术后仍可检出Tg则提示DTC残留或复发。
因此Tg明显升高常提示该疾病复发。
8,9,10,11,12,13采用高灵敏度Tg检测后,“甲状腺球蛋白阳性”病人数量增加,即使这些病人并未表现出疾病症状。
13不能认为这些病人没有疾病,应根据当前指南进行监测随访。
已有不同临界值报道用以鉴别仅需监测的病人和那些需要接受进一步诊断和治疗的复发病人。
游离T3FT3标准操作程序SOP文件

·一个月(同一批号试剂)
·4天(放置仪器上的同一试剂盒)
·根据要求进行标定:如质控结果超出范围时。
质控:
Elecsys通用质控品l和2以及其它合适的质控品。各浓度区域的质控至少每24工作时、每个试剂盒或每一次定标后测定一次。质控间隔期应适用于各实验室的具体要求。检测值应落在确定的范围内,如出现质控值落在范围以外,应采取校正措施。
ABCD医院
免疫实验室
文件编号:
ABCD-02-11
游离T3FT3
版序:ABCD
页码:第1页,共3页
用途:
用免疫学方法定量测定人血清或血浆的游离三碘甲腺原氨酸(fT3)含量。电化学发光免疫测定试剂,适用于罗氏Elecsys、2010免疫测定分析仪。
概述:
三碘甲腺原氨酸(T3)是血清中的甲状腺激素之一,起调节代谢作用。测定该激素的含量对鉴别诊断甲状腺功能是否正常、亢进或低下有重要意义。绝大多数的T3与其转运蛋白质(TBG、前白蛋白、白蛋白)结合,fT3是T3的生理活性形式。fT3测定的优点是不受其结合蛋白质浓度和结合特性变化的影响。因此不需另加测定结合参数(T-uptake,TBG)。连续的测定步骤和采用标记抗体可降低来自血清某些结合特性改变的影响,如见于用抗原做标记物的测定方法。有许多方法可用于测定fT3的水平。通过平衡透析或超滤法直接测定fT3和fT4主要作为参考方法,用于标化那些作常规诊断手段的免疫学方法。Elecsys fT3采用钌标记的抗T3抗体。
ABCD医院
免疫实验室
文件编号:
ABCD-02-11
游离T3FT3
版序:ABCD
页码:第2页,共3页
游离三碘甲状腺原氨酸(FT3)校准品产品技术要求hkt
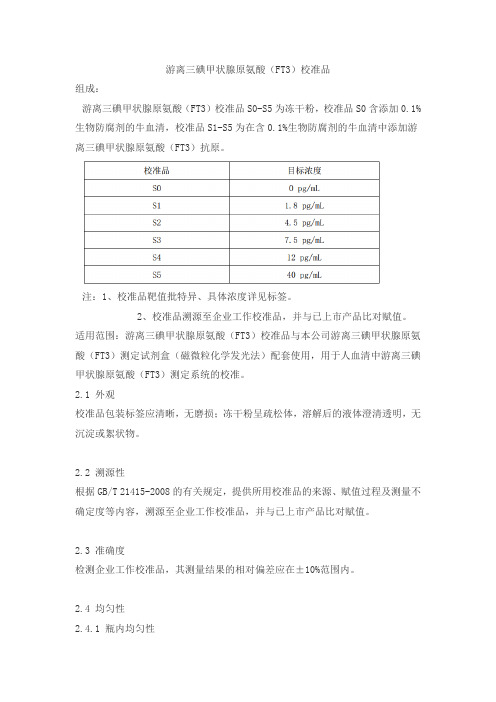
游离三碘甲状腺原氨酸(FT3)校准品
组成:
游离三碘甲状腺原氨酸(FT3)校准品S0-S5为冻干粉,校准品S0含添加0.1%生物防腐剂的牛血清,校准品S1-S5为在含0.1%生物防腐剂的牛血清中添加游离三碘甲状腺原氨酸(FT3)抗原。
注:1、校准品靶值批特异、具体浓度详见标签。
2、校准品溯源至企业工作校准品,并与已上市产品比对赋值。
适用范围:游离三碘甲状腺原氨酸(FT3)校准品与本公司游离三碘甲状腺原氨酸(FT3)测定试剂盒(磁微粒化学发光法)配套使用,用于人血清中游离三碘甲状腺原氨酸(FT3)测定系统的校准。
2.1 外观
校准品包装标签应清晰,无磨损;冻干粉呈疏松体,溶解后的液体澄清透明,无沉淀或絮状物。
2.2 溯源性
根据GB/T 21415-2008的有关规定,提供所用校准品的来源、赋值过程及测量不确定度等内容,溯源至企业工作校准品,并与已上市产品比对赋值。
2.3 准确度
检测企业工作校准品,其测量结果的相对偏差应在±10%范围内。
2.4 均匀性
2.4.1 瓶内均匀性
各浓度点(除零外),变异系数(CV)应不高于10%。
2.4.2 瓶间均匀性
各浓度点(除零外),变异系数(CV)应不高于15%。
2.5 稳定性
2.5.1 复溶稳定性
校准品复溶后,-20℃以下储存,有效期15天,在效期内赋值结果的变化趋势不显著。
2.5.2 效期稳定性
校准品原包装2℃~8℃储存,有效期12个月,在效期内赋值结果的变化趋势不显著。
FT3操作规程

4.1时间分辨荧光分析仪;
4.2微孔洗涤机;
4.3微孔振荡器;
5.操作步骤
5.1.试剂的准备
⑴洗涤液:将40ml浓缩洗液和960ml蒸馏水在干净的洗液瓶中混合,作为工作洗涤液。
⑵加入1.0ml蒸馏水于冻干铕标记小瓶中,待铕标记充分溶解(静置至少30分钟)。
⑶加入1.0ml蒸馏水于各冻干校准品小瓶中,待校准品充分溶解(静置至少30分钟)。
9.11所有的样本和本试剂盒应作为潜在的传染原看待,按传染病实验室检查规程操作。
9.12如对实验结果有疑问,应重复试验。
9.13为保证实验的准确性,处理后得到的血样应不含纤维蛋白、红细胞、血脂等,并要保证血样吸取的量的准确性,否则容易引起测量值的差异。
9.14本试剂盒应置2—8℃保存,有效期参考瓶上所贴标签。
⑷将分析缓冲液、校准品、待测样品和所需数量的微孔反应条平衡至室温(20~250C)。
⑸使用前一小时内,按照需要用量以分析缓冲液稀释铕标记(1:100)(详见操作流程图)
5.2.吸取25μl校准品和待测样品,加入反应板微孔内。
5.3.在各微孔内加入150μl已稀释的铕标记溶液,在室温(20~25℃)下慢速振动1小时。
7.临床意义
血清中约80%以上的T3由T4脱碘生成,其余直接由甲状腺合成。进入血液循环的T3大部分与结合蛋白结合,仅约0.3% T3呈游离状态。FT3被认为是循环血中甲状腺激素的活性部分。FT3浓度分析不受血液中甲状腺激素结合蛋白浓度的影响,是甲状腺功能亢进的敏感指标,并且是评价T4-替代疗法疗效的常用分析手段。
c.校准品(A、B、C、D、E、F):一套,1.0ml/瓶(冻干品)
d.浓缩洗液:一瓶,40ml
e.荧光增强液:一瓶,30ml
游离T3(FT3)测定

游离T3(FT3)测定1. 原理采用夹心法原理、电化学发光法(E CL)定量检测FT3。
待测样本中的F T3与三联吡啶钌(R u(b py)32+)标记的单抗和生物素标记的单抗结合生成抗原抗体复合物。
该复合物与亲和素包被的磁珠结合,吸附于检测室(Cel l)电极表面,经氧化还原反应,三联吡啶钌与TP A作用释放光子,以光信号的强弱定量标本中检测物的含量。
2. 标本采集:2.1标本采集前病人准备:受检者应空腹。
2.2标本种类:血清或血浆。
2.3标本要求:采集血清样本,取被检者静脉血,用无菌取血针抽取病人静脉血3ml,收集干燥试管中,室温放置不超过8小时,2000转/分离心20分钟备用.采集血浆样本,用无菌取血针取被检者静脉血3m l,收集于含有ED TA 作抗凝剂的试管中,室温放置不超过8小时,2000转/分离心20分钟备用。
3. 标本储存:待测样本室温不超过8小时,4-8℃不超过72小时,-20℃可长期保存,避免反复冻融。
4. 标本运输:室温运输。
5. 标本拒收标准:细菌污染,严重溶血或脂血标本不能作测定。
6. 试剂:6.1试剂名称:游离T3试剂盒。
6.2试剂生产厂家:罗氏公司6.3包装规格:100T est/盒6.4试剂盒组成:游离T3诊断试剂。
6.5试剂储存条件及有效期:试剂盒贮存2-8℃条件,有效期见条形码。
7. 仪器设备:7.1仪器名称:罗氏全自动电化学发光免疫分析仪7.2仪器厂家:罗氏公司7.3仪器型号:c oba s e 4117.4仪器校准:本仪器校准由厂家工程师负责校准8. 操作步骤:8.1样本处理:取待测样本血清或血浆(尿液)置于样本杯中(不能有纤维蛋白,不能有气泡)。
8.2仪器准备:检查纤维杯,反应杯数量满足实验需要,废物桶和废液桶是否连接好,仪器的光路是否正常,环境温度是否符合要求,打印机的连接。
8.3试剂准备与检查:从冰箱取试剂放入仪器,检查所有试剂量是否足够,是否在有效期内。
电化学发光法检测甲状腺素的临床分析

电化学发光法检测甲状腺素的临床分析目的分析采用电化学发光法检测甲状腺素的结果,为临床诊断甲状腺相关疾病提供参考依据。
方法方便选取2016年1月—2017年12月在该院就诊的70例甲状腺机能亢进患者作为甲亢组,选取同期在该院就诊的70例甲状腺功能减退患者作为甲减组,同时同期在该院进行健康体检的80例健康人作为对照组,对比3组游离三碘甲状腺元氨酸(FT3)、游离甲状腺素(FT4)、促甲状腺素(TSH)、总三碘甲状腺激素(TT3)、总四碘甲状腺激素(TT4)等甲状腺激素指标。
结果甲亢组患者FT3、FT4、TT3、TT4等指标均显著高于对照组以及甲减组患者(P 0.05)。
1.2 方法该次所有研究对象均采用电化学发光法检测甲状腺素,选用的检测仪器为cobas e602电化学发光仪(ROCHE公司)及其配套试剂盒。
采集3组清晨空腹外周静脉血3 mL作为血液标本,注意避免标本出现溶血、脂血,放在真空采血管(未加抗凝剂),放置于室温条件下凝固,在1 500~2 000 r/min条件下进行离心处理,分离血清,取上层清液,当天检测TT3、TT4、TSH、FT3、FT4等指标,操作过程中要求严格根据试剂盒说明书操作。
1.3 观察指标详细记录3组TT3、TT4、TSH、FT3、FT4等甲状腺素指标检测结果,并进行对比分析。
1.4 统计方法选用SPSS 13.0统计学软件处理该次所有研究数据,FT3、FT4、TT3、TT4等数据采用(x±s)表示,进行t检验,P<0.05为差异有统计学意义。
2 结果甲亢组患者FT3、FT4、TT3、TT4等指标均显著高于对照组以及甲减组患者(P<0.05),甲减组患者FT3、FT4、TT3、TT4等指标均显著低于对照组(P <0.05)。
甲亢组患者TSH水平(0.4±0.1)mIU/L显著低于对照组(1.6±1.1)mIU/L 及甲减组患者(67.4±32.4)mIU/L(t=3.421 2,t=10.658,P<0.05),甲减组患者TSH水平显著高于对照组(t=9.934,P<0.05),见表1。
三碘甲腺原氨酸(T3)测定试剂盒(酶联免疫法)产品技术要求beifang
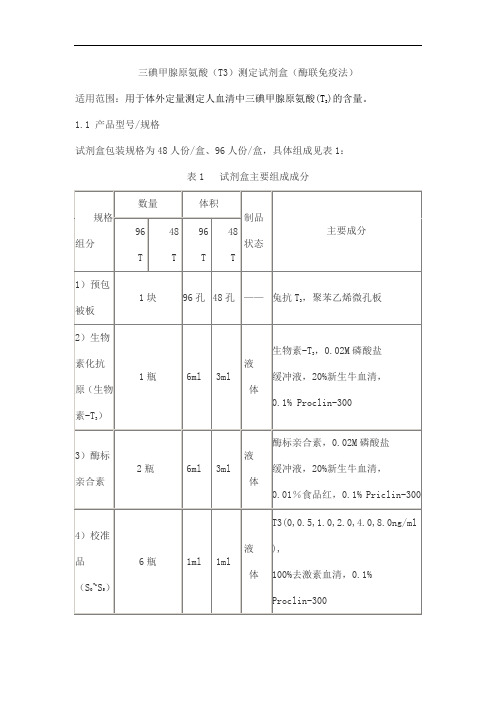
三碘甲腺原氨酸(T3)测定试剂盒(酶联免疫法))的含量。
适用范围:用于体外定量测定人血清中三碘甲腺原氨酸(T31.1 产品型号/规格试剂盒包装规格为48人份/盒、96人份/盒,具体组成见表1:表1 试剂盒主要组成成分2.1外观和物理检查试剂盒应组分齐全,内外包装均应完整,标签清晰,液体试剂无渗漏。
各组分装量不少于表1中要求。
2.2准确性试剂盒内校准品与相应浓度的国家标准品同时进行分析测定,用百分结合率对数(logit-ln)数学模型拟合,要求两条剂量-反应曲线不显著偏离平行(t检验);以国家标准品为对照品,试剂盒内校准品的实测效价与标示值效价的比应在0.900~1.100之间。
2.3线性用logit-ln数学模型拟合,在0.5~8.0ng/mL范围内,剂量-反应曲线相关系数(r)的绝对值应不低于0.9900。
2.4精密度2.4.1分析内精密度试剂盒质控品测定结果的变异系数(CV)应不大于15.0%。
2.4.2批间精密度在三个不同批次产品之间,质控品测定结果的变异系数(CV)应不大于15.0% 2.5最低检出限应不高于0.4ng/mL。
2.6质控品测定值每次检测结果均应在允许范围内。
2.7特异性)结果不高于0.5ng/mL。
检测浓度为5000ng/mL的甲状腺素(T4)结果不高于0.5ng/mL。
检测浓度为500ng/mL的反三碘甲状腺原氨酸(rT32.8稳定性2.8.1效期内稳定性试剂盒在2~8℃储存12个月,测定结果应符合上述2.1、2.2、2.3、2.4.1、2.5、2.6要求。
2.7.2热稳定性将试剂盒在37℃条件下放置7天,测定结果应符合上述2.1、2.2、2.3、2.4.1、2.5、2.6要求。
游离三碘甲状腺原氨酸测定标准操作规程

游离三碘甲状腺原氨酸测定标准操作规程1检验原理:采用两步法免疫检测,运用化学发光微粒子免疫检测(CMIA)技第一步,术与灵活的检测模式的结合,测定人血清和血浆中的游离(未结合)T3o将样本和T3抗体包被的顺磁微粒子混合。
样本中的T3(未结合型)与T3抗体包被的微粒子结合。
冲洗后进入第二步,加入哇咤酯标记的T3结合物。
随后将预激发液和激发液加入反应混合物中;测量化学发光反应结果,以相对发光单位(RLUs)表示。
样本中的游离T3含量和ARCHITECTi光学系统检测到的RLUs值之间成反比。
2.试剂主要组成部分:2.1试剂盒微粒子:三碘甲状腺原氨酸抗体(绵羊)包被的微粒子,储存于含有绵羊IgG 稳定剂的2-(N-吗啡咻)乙磺酸(MES)缓冲液中。
最低浓度:0.085%固体物质。
防腐剂:抗菌剂。
结合物:口丫咤酯标记的三碘甲状腺原氨酸结合物,储存于含有氯化钠(NaCI)和聚乙二醇辛基苯基酸(TritonXT00)稳定剂的柠檬酸盐缓冲液中。
最低浓度:0.33ng∕mL.防腐剂:抗菌剂。
2.2需要但未提供的试剂预激发液:预激发液含有1.32%(W/V)过氧化氢激发液:激发液含有0.35N氢氧化钠浓缩清洗缓冲液:浓缩清洗缓冲液含有磷酸盐缓冲液。
防腐剂:抗菌剂。
3.样本要求:人血清(包括采集于血清分离管中的血清)或采集于肝素、肝素锂或EDTA钾抗凝管中的血浆。
血清和血浆样本中应不含纤维蛋白、红细胞或其他颗粒物质。
2-8°C可保存6天;-10℃以下可保存6个月。
样本应避免反复冻融。
4.检验方法:仪器法(详见雅培i1000标准操作规程)1.1游离三碘甲状腺原氨酸项目通过四参数Logistic曲线拟合数据约简法(4PLC,Y加权)生成一条校准曲线6.2结果单位转换:浓度(pg∕mL)XL536=浓度(pmol∕L)7.检验方法的局限性7.1将检测结果用于诊断时,应与其他数据:如症状、其他甲状腺检查结果、临床表现等结合使用。
游离三碘甲状腺原氨酸(FT3)时间分辨荧光免疫分析试剂盒的研制

游 离 三 碘 甲状 腺 原 氨 酸 (free triiodothyr0nine, FT3)是 由甲状腺滤泡细胞合成及分泌 的激素 ,具有 促 进物 质 与能量 代谢 ,促 进机 体生 长 和发育 的生 物 学 活 性 ,是 甲状 腺疾 病 的重 要诊 断 指标 ,对某 些 非 甲状
W AN G Yi,H E Yongting,FENG Jianm ing ,LIU Yinhe
fClinical Laboratory of Shenzhen Sun Yat—Sen Cardiovascular Hospital,Guangdong,Shenzhen 5 1 8000)
[ABSTRACT】 Objective To develop a kit for the detection of human free triiodothyronine(FT3)in serum by time.resolved fluoroimmunoassay (TRFIA). Methods The TRFIA FT3 kit was established by
direct competitive method(solid—phase was coated with T3 complex,and competitively binded to T3 monoclonal antibody labeled DTTA—Eu with FT3).And the performance of the kit was evaluated. Results The effective working range of the kit w as 1.5-70 pm ol/L and the analytical sensitivity w as not higher than O.7 pm ol/L.The intra.assay and inter-assay coeficients of variation were not higher than 8.2% and 10.5% .respectively.The percentage of cross reactivity with T4,FT4,rT3,rT4 were<0.01%,0.11%,<0.01% and<0.01% ,respectively. The TRFIA FT3 reagents can be stored at 2℃ ~8 for one year and at 37oC for 7 days.The cutoff value for TRFIA FT3 kit in healthy subjects was 3.2 pmol/L~6.5 pmol/L,in according to 500 cases of health sample serum with this kit.The correlation coefficient of blood samples detection results(n=1 56)between home·made and CLIA kit of one wel1.known foreign brands was 0.992. Conclusion FT3 TRFIA kit was a valuable diagnostic kit f o r clinical application w ith better sensitivity,specificity,and accuracy.
FT3中文说明书

定标频率:每批试剂必须用新鲜试剂(试剂经仪器注册24小时以内) 标定一次,如再次标定即根据下列要求: E170/Elecsys2010: · 一个月(同一批号试剂) · 4天(放置仪器上的同一试剂盒) Elecsys1010: · 每一试剂盒做一次 · 7天(室温20-25 度) · 3天(室温25-32 度) 各种分析仪均适用的情况: ·根据要求进行标定:如质控结果超出范围时。 质控: Elecsys通用质控品l和2以及其它合适的质控品。各浓度区域的质控至少每 24工作时、每个试剂盒或每一次定标后测定一次。质控间隔期应适用于各
定分析仪。
· Elecsys测量池清洗液(CleanCell M)货号12135027
· Elecsys系统缓冲液/测量池清洗液预热杯(PC/CC-Cup)货号03023141
概述:
· Elecsys反应杯/吸样头盒(AssayCups/AssayTips Combimagazine M)
三碘甲腺原氨酸(T3)是血清中的甲状腺激素之一,起调节代谢作用。
· Elecsys 1010反应杯(Assay Cup) 货号11706829 Elecsys 2010反应杯(Assay Cup) 货号11706802
稀释: 标本不可以稀释,因为血中的T3是以游离状态以及结合状态两种形式存在, 并处在平衡状态中。结合蛋白质浓度的变化可改变这种平衡。
正常参考值: 2.8-7.1pmol/l或1.8-4.6pg/ml(范围:第2.5百分位-第97.5百分位, n=962)。 如有必要,各实验室应自己测定一个正常值范围。
开封后,2-8 度12周; 放在E170上,5周; 放在Elecsys2010上,8周; 放在Elecsys1010上,7周(使用后放回2-8度 ;如置20-25 度,约20 小时)。
游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发光免疫分析法)产品技术要求kangrun

游离三碘甲状腺原氨酸(FT3)测定试剂盒(化学发
光免疫分析法)
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;R1 组分应为棕色含固体微粒的液体,无板结、无絮状物。
R2 和R3 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
2.2装量
应不少于试剂瓶的标示装量值。
其中R1≥5.6mL,R2≥6.0mL,R3≥6.0mL。
2.3准确度
对具有溯源性的两个浓度水平的工作校准品进行检测,检测结果与标定浓度的相对偏差在±10%范围内。
2.4空白限
空白限应不大于0.8 pg/mL。
2.5线性
试剂盒在0.8-30 pg/mL 区间内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV 应≤ 8%。
2.7批间差
变异系数CV 应≤ 15%。
2.8特异性
浓度不低于300ng/mL 的L-T4 样本,检测结果应不高于空白限。
浓度不低于10µg/mL 的rT3 样本,检测结果应不高于空白限。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
游离三碘甲状腺原氨酸(FT3)测定试剂盒(电化学发光免疫分析法)
组成:
适用范围:本试剂盒用于体外定量测定人体血清样本中游离三碘甲状腺原氨酸(FT3)的含量。
2.1 外观
2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;
2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;
2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;
2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限
应不大于0.4pmol/L。
2.3 准确度
用FT3企业参考品进行检测,其测量结果的相对偏差应在±15%范围内。
2.4 线性
在[1.0,50.0]pmol/L范围内,线性相关系数的绝对值(|r|)应不小于0.9900。
2.5 精密度
2.5.1 分析内精密度
在试剂盒的线性范围内,浓度为(5.0±1.0pmol/L)和(30.0±6.0pmol/L)的样品检测结果的变异系数(CV)应不大于8%。
2.5.2 批间精密度
在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(5.0±1.0pmol/L)和(30.0±6.0pmol/L)的样品,检测结果的变异系数(CV)应不大于15%。
2.6 特异性
2.6.1 与甲状腺素(T4)
浓度不低于200ng/mL的T4样品,在本试剂盒测定结果应不大于0.4pmol/L;2.6.2 与3、3’、5’-三碘甲腺原氨酸(rT3)
浓度不低于200ng/mL的rT3样品,在本试剂盒测定结果应不大于0.4pmol/L。
2.6.3 与3、3’-二碘甲腺原氨酸
浓度不低于200ng/mL的T2样品,在本试剂盒测定结果应不大于0.4pmol/L。
2.7 效期末稳定性
本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.8 溯源性
依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至罗氏诊断生产的FT3定标液。
