江苏省盐城市2013届高三第二次模拟(3月化学)
中学2013届高三2月联考化学

高三理科综合测试三化学试题一、单选题:(每小题4分,共24分)7.下列说法正确的是A.糖类、油脂、蛋白质在一定条件都能发生水解反应B.苯只能发生取代反应,不能发生加成反应C.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2OD.溴乙烷与NaOH的乙醇溶液共热生成乙烯1、【答案】D2、【知识点】化学与生活3、【难度值】34、【基础试题☆】5、【优质试题□】6、【易错试题○】7、【解析】A中糖类中的单糖不能发生水解反应,错误;B中苯在一定条件下能和氢气、氯气等加成,错误;C羊毛是蛋白质含有氮元素,错误;D卤代烃在碱的醇溶液中发生消去反应,正确。
8.用N A表示阿伏加德罗数的值。
下列叙述正确的是A.25°C时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2N AB.室温下,14.0g乙烯气体中含有的碳原子数目为1.0N AC.0.1molFe在0.1molCl2中充分燃烧,转移的电子数为0.3N AD.标准状况下,22.4L乙醇中含有的氧原子数为1.0N A1、【答案】B2、【知识点】粒子数与N A阿伏伽德罗定律及推论3、【难度值】54、【基础试题☆】5、【优质试题□】6、【易错试题○】7、【解析】A.25°C时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.1N A,错误;B.室温下,14.0g乙烯气体中含有的碳原子数目为14/28×2=1.0N A,正确;C. 0.1molCl2只能得到0.2N A电子,错误;D.标准状况下,乙醇不是气体,错误;9.常温下,下列各组离子在指定溶液中一定能大量共存的是A.某澄清透明溶液中:K+、H+、Fe2+、NO3-B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO-C.含0.1mol·L-1HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42-D.含0.1mol·L-1SCN-的溶液中:Fe3+、NH4+、Cu2+、NO3-1、【答案】B2、【知识点】离子共存3、【难度值】64、【基础试题☆】5、【优质试题□】6、【易错试题○】7、【解析】A. H+、Fe2+、NO3-因发生氧化还原反应不能共存,错误;B.c(H+)<c(OH-)的溶液即碱性溶液,Na+、K+、SO42-、ClO-均能存在,正确;C. HCO3-与Al3+发生双水解反应不能共存,错误;D. SCN-与Fe3+发生络合反应不能共存,错误。
江苏省盐城中学2013届高三下学期开学考试 化学 Word版含答案.pdf

质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有
▲
。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有 ▲ 。
CaSO4除去,根据上表数据,简要说明操作步骤 ▲
、▲。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的
产率为
▲。
17.(16分)5-氨基酮戊酸盐是一种抗肿瘤药,其合成路线如下:
⑴已知A分子结构中有一个环,A不能使溴水褪色,且核磁共振氢谱图上只有一个峰,则A的结构简式为
..常温下,下列各组粒子在指定溶液中不能大量共存的是
A.pH=l的溶液中:、O4—、K+、SO42-
?B.NaHCO3溶液中:、CO32-、Br-、K+
?C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+ 、NO3- 、Cl-
?D.c( CH3COO- )=0.1 mol·L-1的溶液中:NH4+、K+、Ca2+、Br-.用NA表示阿伏加德罗常数的值。下列叙述
江苏省盐城中学高三年级综合测试
化学试题(2013.02)
命题人:卞淼 陈惠军
审题人:陈一
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Si-28 P-31 S-32 Cl-35.5
-Ca-40 Ni-59 Ca-40 I-127
选择题 (共40分)
江苏省扬州、南通、泰州、宿迁四市2013届高三3月第二次调研测试化学试题 Word版含答案

江苏省扬州、南通、泰州、宿迁四市2013届高三第二次调研测试化学2013.3注意事项考生在答题前请认真阅读本注意事项及各题答题要求1.本试卷共8页.包含选择题(第1题~第15题,共40分)、非选择题(第16题~第21题,共80分)两部分。
本次考试满分为120分,考试时间为100分钟。
考试结束后,请将答题纸交回。
2.答题前.请您务必将自己的姓名、学校、考位号、考试号等用书写黑色字迹的0.5毫米签字笔填写在答题纸上。
3.请认真核对答题纸表头规定填写或填涂的项目是否准确。
4.作答选择题必须用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,请用橡皮擦干净后.再选涂其他答案。
作答非选择题必须用书写黑色字迹的0.5毫米签字笔写在答题纸上的指定位置.在其他位置作答一律无效。
5.作答选做题时.需用2B铅笔将选做的试题号所对应的口涂黑,漏涂、错涂、多涂的答案无效。
可能用到的相对原子质量H 1 C 12 N 14 O 16 Mg 24 K 39 Ca 40 Fe 56 Cu 64 I 127选择题(共40分)单项选择题:本题包括10小题,每小题2分,共计20分。
每小题只有一个选项符合题意。
1.今年两会期间,习近平勉励江苏代表为“让生态环境越来越好”做贡献。
下列做法均正确的是①合理开发利用可燃冰②全面关停化工企业③研发易降解的生物农药④改进汽车尾气净化技术A.①②③ B.①③④ C.①②④ D.②③④2.下列有关化学用语表示正确的是A.对硝基甲苯的结构简式: B.镁离子的结构示意图:C.次氯酸的电子式:D.亚硫酸钠水解的离子方程式:3.下列有关物质的性质与应用相对应的是A.NH3极易溶于水,可用作制冷剂B.A12O3熔点高,。
可用作耐高温材料C.SO2具有氧化性,可用于漂白品红、织物等D.BaCO3能与盐酸反应,可用于治疗胃酸过多4.在指定条件下,下列各组离子可能大量共存的是A、无色澄清透明溶液中:的溶液中:B、与铝反应放出H2C、滴加酚酞显红色有溶液中:D、由水电离的5.右下图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出)。
江苏省盐城市伍佑中学2013届高三学情调研考试化学试题.pdf

C.图中所示转化反应都不是氧化还原反应
D.反应的化学方程式为NaAlO2 + CO2 + 2H2O=Al(OH)3↓ + NaHCO3
14.( ) A.转移0.1mol电子时,a电极产生1.12LH2(标准状况)
B.b电极上发生的电极反应是:
2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
为使电解质溶液恢复到原状态,需要向溶液中加入9.8 g Cu(OH)2
固体。则原CuSO4溶液的物质的量浓度为_______________,
电解过程中收集到标准状况下的气体体积为_____________。
17.(1分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以
2. 下列有关化学用语表示正确ห้องสมุดไป่ตู้是( )
A. 乙酸的结构简式: C2H4O2
B. F-的结构示意图:
C. 中子数为20 的氯原子: 2017Cl D. NH3 的电子式:
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol?L-1FeCl2溶液:H+、Na+、Cl-、NO3-B.0.1 mol?L-1的溶液:、、、NO3-
D图4所示转化反应都是氧化还原反应
16.(分)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
(1)该电池中OH-向_______极移动(填“正”或“负”)
(2)该电池负极的电极反应为_______________________________。
(3)用该电池电解(惰性电极)500 mL某CuSO4溶液,电解一段时间后,
江苏省盐城中学2013届高三第一次模拟考试化学试题.pdf

道的杂化类型有
;m=________(填数字)。
(4)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为__________g·cm-3(用NA表示阿伏加德罗
常数的数值)。
16.
(1)V2O5(2分)
(2)VOSO4(2分)
(3) V2O5 +Na2SO3+SO4===VOSO4+Na2SO4+2O 4 80 ℃(每空2分)
()①d(分)②不严密(分),产物中含+3价铁的物质与稀硫酸反应后生成Fe3+,Fe3+可与过量的Fe反应生成
Fe2+,2Fe3++Fe===3Fe2+。(2分)
5.6×10—5mo1/L (2分)
(4)H2(分)Fe+H++O===Fe3++O+H2O (2分) mol·L-1(2分)
A.溶质物质的量相等的Ba(OH)2与KAl(SO4)2·12H2O溶液混合:
Ba2++6OH-+2Al3++SO===BaSO4↓+2Al(OH)3↓
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO+CO2+2H2O===Al(OH)3↓+HCO
D.将适量CO2通入Ca(ClO) 2溶液中:2ClO-+CO2+H2O===CO+2HClO
7.NA表示阿伏加德罗常数的值,下列说法正确的是
A.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
B.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA
2.下列有关化学用语的表示,正确的是
A. NaClO的电子式为: B.CCl4分子的比例模型:
江苏省盐城市2013届高三化学12月月考

江苏省盐城中学高三年级综合测试化学试题(12月)可能用到的相对原子质量:H-1 C-12 O-16 Na-23 N-14 Si-28 Fe-56单项选择题:本题包括10小题,每小题2分,共计20分。
每小题只有一个....选项符合题意。
1.在“十二五”期间,江苏省将大力实施“清水蓝天”工程。
下列不利于...“清水蓝天”工程实施的是A.加大稀土资源的开采和出口,促进经济快速发展B.加强城市生活污水脱氮除磷处理,遏制水体富营养化C.积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用D.大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染2.下列有关化学用语表示正确的是A.CO2的电子式: B.铵根的结构式:C.乙烯的球棍模型: D.中子数为20的钙原子:3.下列各组离子在指定溶液中能大量共存的是①常温下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2一、CO32一、Na+②加入苯酚显紫色的溶液:K+、NH4+、Cl一、I一③中性溶液:Fe3+、Al3+、NO3一、SO42一④使pH试纸变蓝的溶液中:Al3+、Na+、SO42一、Cl一⑤无色溶液中:K+、Al3+、NO3一、HCO3一A.②③ B.①③ C.①D.①④⑤4.石头纸(Rich Mineral Paper)也叫石科纸,就是用磨成粉末的碳酸钙为主要原料,加上15%的聚乙烯和5%胶合剂制成的。
下列有关“石头纸”的说法错误的是A.“石头纸”不宜在高温条件下生产B.“石头纸”能耐强酸与强碱的腐蚀C.“石头纸”与普通纸相比不易燃烧D.推广使用“石头纸”能达到保护森林和环保的目的5.下列有关物质的性质、应用的说法正确的是A.氯气通入澄清石灰水中,制取漂白粉B.除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤C.自来水厂可用硫酸铁对水进行消毒杀菌D.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸6.下列有关实验装置的说法中正确的是浓氨水Cl2A .用图1装置制取干燥纯净的NH 3B .用图2装置制备Fe(OH)2并能在较长时间观察其颜色C .用图3装置可以完成“喷泉”实验D .用图4装置测量Cu 与浓硝酸反应产生气体的体积78.下列离子方程式书写正确的是A .向明矾溶液中加入过量的氢氧化钡溶液:2Al 3++3SO 42-+6OH -+3Ba 2+=2Al(OH)3↓+3BaSO 4↓B .向氢氧化亚铁中加入足量的稀硝酸: Fe(OH)2+2H +=Fe 2++2H 2O C .向碳酸氢铵溶液中加入足量的氢氧化钠溶液:NH 4++HCO 3-+2OH -=CO 32-+ NH 3·H 2O+H 2OD .向CH 2BrCOOH 中加入足量的氢氧化钠溶液并加热: CH 2BrCOOH+ OH -△CH 2BrCOO -+H 2O9.用N A 表示阿伏加德罗常数的值,下列说法中正确的是A .7.8 g 苯中含有0.3N A 个碳碳双键,0.3N A 个碳碳单键B .2 L 0.1 mol/L 的醋酸钠溶液中,醋酸根离子数为0.2N AC .5.6 g 铁与足量的稀硝酸反应,失去电子数为0.2N AD .SiO 2晶体中,有N A 个Si 就有4N A 个Si —O 键10.下图所示为海水资源综合利用的一部分。
江苏省南京市、盐城市2023届高三下学期3月第二次模拟考试 化学含答案
南京市、盐城市2023届高三年级第二次模拟考试化 学(答案在最后)可能用到的相对原子质量:H-1 O-16 S-32 Fe-56一、单项选择题:共13题,每题3分,共39分。
每题只有一个选项最符合题意。
1.“神舟飞船”接力腾飞、“太空之家”遨游苍穹、“福建号”航母下水、国产“C919”大飞机正式交付都彰显了中国力量。
下列成果所涉及的材料为金属材料的是 A.“神舟十五”号飞船使用的耐辐照光学窗材料——石英玻璃 B.“天宫”空间站使用的太阳能电池板材料——砷化镓 C.“福建号”航母使用的高强度甲板材料——合金钢D.“C919”大飞机使用的机身复合材料——碳纤维和环氧树脂2.用NaCN 溶液浸取矿粉中金的反应为()2224Au 2H O 8NaCN O 4Na Au CN 4NaOH ⎡⎤⎣⎦+++=+。
下列说法正确的是A.H 2O 的空间结构为直线形B.NaCN 中含有离子键和共价键C.1mol[Au(CN)2]-中含有2molσ键D.NaOH 的电子式为3.由SiCl 4制备高纯SiH 4的反应为4443SiCl LiAIH SiH LiCl AlCl ↑乙醚+++。
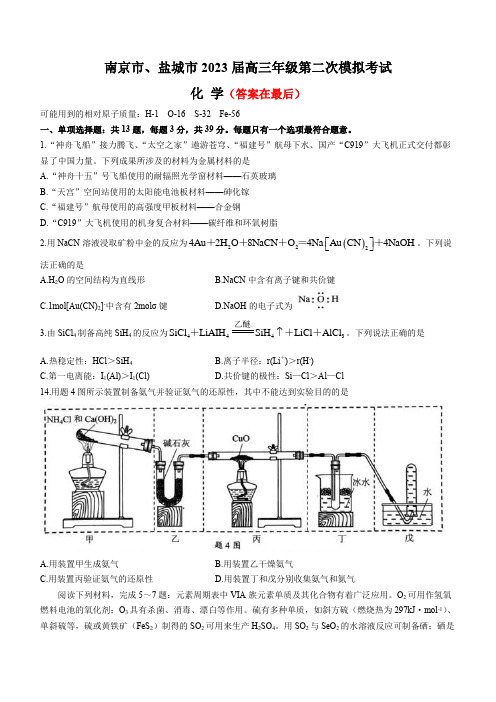
下列说法正确的是A.热稳定性:HCl >SiH 4B.离子半径:r(Li +)>r(H -) C.第一电离能:I 1(Al)>I 1(Cl)D.共价键的极性:Si —Cl >Al —Cl14.用题4图所示装置制备氨气并验证氨气的还原性,其中不能达到实验目的的是A.用装置甲生成氨气B.用装置乙干燥氨气C.用装置丙验证氨气的还原性D.用装置丁和戊分别收集氨气和氮气阅读下列材料,完成5~7题:元素周期表中VIA 族元素单质及其化合物有着广泛应用。
O 2可用作氢氧燃料电池的氧化剂;O 3具有杀菌、消毒、漂白等作用。
硫有多种单质,如斜方硫(燃烧热为297kJ ·mol -1)、单斜硫等,硫或黄铁矿(FeS 2)制得的SO 2可用来生产H 2SO 4。
江苏省盐城市高三年级第二次调研考试化学试题

CH 3-C=CH -CH 2CH 3CH 3盐城市2008/2009学年度高三年级第二次调研考试化学试题第Ⅰ卷 (选择题共48分)可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Cl-35.5一、单项选择题:(本题包括8小题,每小题3分,共24分。
每小题只有一个....选项符合题意) 1.美国化学家诺塞拉研制出一种可以将水分解成氢气和氧气的催化剂,这将使氢气生产成为可能,并使太阳能使用步入新的时代,被称为“水发电技术”。
下列有关说法正确的是 A .“水发电技术”是指水分解生成氢气和氧气,同时放出能量来发电 B .“水发电技术”的能量转换形式为:化学能→热能→电能C .若水分解产生的H 2和O 2分别通入燃料电池的两极,通H 2的极为电源正极D .“水发电技术”可实现发电过程中的零排放2.下列文字表述与对应的化学用语或名称关系正确的是A .CS 2电子式B .光气(COCl 2)结构式C .的名称 1,3-二甲基―2―丁烯D .NaH 中氢离子结构示意图3.石墨烯(graphene )是目前科技研究的热点,可看作将石墨的层状结构一层一层的剥开得到的单层碳原子。
将氢气加入到石墨烯排列的六角晶格中可得最薄的导电材料石墨烷(graphane ,如下图),下列说法中正确的是(N A 表示阿伏伽德罗常数) A .石墨烯与石墨烷互为同素异形体 B .石墨烯转变为石墨烷可看作取代反应 C .12g 石墨烯所含碳碳键数目为1.5N A D .12g 石墨烯完全转变为石墨烷需氢气11.2L4.下列有关说法不正确的是A .光导纤维的成分为二氧化硅B .被酸雨污染的农田及湖泊可洒石灰石粉末,减轻其危害C .轮船浸在水下部分可镶上一些铜锭,以防止船体表面铁的腐蚀D .天然气管道在运输天然气前需先通氮气,将空气排出,然后再输送天然气5.著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。
化学高考模拟卷-高三化学试题含答案-盐城市高三3月第二次模拟考试化学试题及答案03

盐城市2013届高三年级第二次模拟考试化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Si 28 K 39 Fe 56选择题单项选择题:本题包括10小题,每小题2分,共计20分。
每小题只有一个选项符合题意。
1.化学在资源合理开发利用和生态环境保护方面正发挥着积极作用,下列行为与可持续发展理念相违背的是A.提高车用燃气、燃油品质,减少大气污染物的排放B.调整能源结构,推广核电、水电、天然气等清洁能源的应用比例C.将造纸废水通过高压水井压到地下,节约生产成本D.探寻新的反应途径、不断提高化学反应过程的选择性,提高合成反应的原子利用率2.下列有关化学用语表示正确的是A.羧基电子式B. O2-的结构示意图C.质子数35,中子数44的溴原子D. Al(OH)3在水溶液中的电离方程式H++H2O+AlO2-\leftrightharpoons AI(OH)3\leftrightharpoonsAl3+++3OH-3.常温下,下列各组离子在指定溶液中一定能大量共存的是A.0.1mo1/L NaI溶液:K+, Na+ , MnO4- , OH-B.能溶解CaCO3的溶液:K+, NH4+, Cl -, NO3-C.0.1mo1/LNaHSO3溶液:Na +, Mg2+, SO42- , ClO-D. c(H+)/c(OH-}=1013,的溶液:K+, Fe2+, Cl-, NO3-4.以0.1000 mol·L-1 NaOH溶液滴定c mol·L-1,某弱酸HA溶液,其滴定曲线如图I所示,下列说法正确的是A.可用甲基橙作滴定指示剂B.指示剂指示的滴定终点就是反应终点C.突变范围的大小与酸的强弱及酸的浓度有关D.滴定时氢氧化钠溶液盛放在带活塞的滴定管中5.下列有关物质的性质与其应用不相对应的是A. NH3分解生成N2和H2吸热热量,液氨可用作致冷剂B.浓硫酸具有吸水性,可用作Cl2的干燥剂C: CaO2能与水缓慢释放O2,可用作供氧剂D.聚合硫酸铁[Fe x(OH)Y(SO4)z·nH2O]能水解得到Fe(OH)3胶体,可用作净水剂6:下列使用漏斗的几个实验装置中,设计正确且能达到实验目的的是A.用图2所示装置进行过滤,过滤时不断搅拌B.用图3所示装置吸收NH3制氨水C.用图4所示装置用苯萃取碘水中的碘,并把碘的苯溶液从漏斗下口放出D.用图5所示装置用石灰石与稀盐酸制取CO2气体7.下列是部分矿物资源的利用及产品流程(如图6),有关说法不平确的是A.粗铜电解精炼时,粗铜作阳极B.生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应C.黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶铁的原料D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法8.设N A表示阿伏加德罗常数的值。
2013年江苏省盐城市高二学业水平测试模拟试题(化学)含答案

2013 年江苏省学业水平测试化学模拟试题2013.2可能用到的相对原子质量:H-1C-12 N-14O-16S-32 Cl-35.5Na-23Ca-40 Fe-56Cu 64Ag-108一、单项选择题:在每题的 4 个选项中。
只有 1 个选项是切合要求的,本部分23 题,每题3 分,共 69 分)1.黑火药是我国古代的四大发明之一。
以下物质不属于黑火药成分的是A .硝酸钾B .硫黄C.木炭 D .小苏打2.石英(SiO 2)系列光纤,拥有低耗、宽带的特色,已宽泛应用于有线电视和通讯系统。
SiO 2属于A .氧化物B.酸C.碱D.盐3.以下物质不需经过化学变化就能从海水中获取的是A .烧碱B.食盐C.单质镁D.单质溴4.以下物质属于共价化合物的是A .CaCl 2B. KF C. C6H6D. C605.以下对 1mol· L—1氢氧化钠溶液的表达中,正确的选项是A .含有钠离子 1molB .含有 3mol 原子C.含有 NaOH 分子数为 6.02 ×1023D.每升氢氧化钠溶液含有 NaOH40.0g6.以下说法正确的选项是A.O2、 O3是同一种单质B.1H、2H 、3H 、 H+、 H2是氢元素形成的五种不一样粒子C.正丁烷和异丁烷互为同系物D.乙醇、乙醚互为同分异构体7.以下工业上制备物质的过程中,无氧化复原反响发生的是A .合成氨B.玻璃制造C.从铝土矿中获取铝D.由硫铁矿 (FeS2)制硫酸8.以下化学用语正确的选项是A.氯化钠的电子式:B.磷原子的构造表示图:C.乙酸的分子式:C2 H4O2D .乙炔的构造式H- C= C-H9.乙烯是重要的有机化工原料。
以下对于乙烯的相关说法中错误的选项是A .一栽种物生长调理剂B.易燃C.不可以发生加成反响D.能使溴水、酸性高锰酸钾溶液退色10.天文科学家研究证明,构成太阳的气体中存在20Ne和22Ne,以下对于20Ne和22Ne的说法正确的选项是A .20Ne 和22Ne互为同位素B.20Ne 和22Ne的电子数不一样C.20Ne 和22Ne的质量数同样D.20Ne 和22Ne的中子数同样11.宋朝有名法医学家宋慈的《洗冤集录》中有“银针验毒”的记录,“银针验毒”的原理是 4Ag+2H 2S+O2= 2 Ag2S +2H 2 O,此中 H 2S 是A .氧化剂B.复原剂C.既是氧化剂又是复原剂D.既不是氧化剂又不是复原剂12.在溶液中能大批共存的离子组是A .Na +、OH 一、HCO3-B . Ba2+、 OH 一、 C1—C.H +、 K +、 CO32-、 D .NH 4+、NO 3—、OH —13.以下对于物质性质的说法正确的选项是A .往常状况下, NO 2是无色的气体B . SO2能漂白品红等物质,说明SO2有氧化性C.氯化钙溶液和 AgNO 3溶液混淆有白色积淀产生D.加热时,铁单质与浓硝酸不发生反响14.以下反响属于吸热反响的是A .CaO+H 2O = Ca(OH) 2B . 2Na+O 2Na2O2高温C.Fe2O3 + 2Al2Fe + Al 2O3D.右图所示的反响为吸热反响15.以下实验方法错误的选项是A.用丁达尔效应鉴识葡萄糖溶液和蛋白质溶胶B.用澄清石灰水鉴识 SO2和 CO2C.用过度的 NaOH 溶液鉴识 AlCl 3溶液和 MgCl 2溶液D .用加热后称量其质量能否变化鉴识Na2CO3和 NaHCO 3固体16.以下反响的离子方程式书写正确的选项是A .硫酸与氢氧化钡溶液反响:H ++OH —=H 2O+—=3 Cu 2+—B .Cu 与浓硝酸反响: 3Cu+8H +2NO 3+2NO 3 +4H 2OC.碳酸钙与稀硝酸反响: CO32—+2H+= CO2↑+H 2OD .实验室用氢氧化钠溶液汲取剩余的Cl2: Cl2+ 2OH—=Cl —+ClO —+H 2O 17.以下相关实验装置、原理或操作正确的选项是A .分别乙醇和水B.食盐水制食盐晶体C.除掉氯气中氯化氢C.实验室制取氨气18.用 N A表示阿伏加德罗常数的值。
江苏省盐城市高考化学三模试卷

江苏省盐城市高考化学三模试卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共14分)1. (2分)物质的用途体现性质.下列有关物质的用途和性质的说法中正确的是()A . 烧碱可以中和酸性土壤﹣﹣烧碱显碱性B . 氮气可充入食品包装袋中防腐﹣﹣氮气化学性质稳定C . 洗涤剂能清洗油污﹣﹣洗涤剂能溶解油污D . 干冰可用于人工降雨﹣﹣干冰升华放出热量2. (2分) (2018高一上·宜昌期中) 用NA表示阿伏德罗常数,下列叙述正确的是()A . 标准状况下,22.4L H2O含有的分子数为 NAB . 通常状况下,NA 个CO2分子占有的体积为22.4LC . 物质的量浓度为1mol/L的MgCl2溶液中,含有Cl—个数为2NAD . 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA3. (2分) (2018高二上·腾冲期中) 某芳香烃的分子式为C10H14 ,不能使溴水褪色,但可使酸性KMnO4溶液褪色,分子结构中含有两个烷基,则此烃的结构共有()A . 6种B . 7种C . 8种D . 9种4. (2分) (2016高一上·沭阳期中) 关于萃取的实验,下列说法正确的是()A . 可以用四氯化碳把溴水中的溴萃取出来,振荡静置分层后,下层液体为无色B . 萃取分液时,从分液漏斗下口流完下层液体,及时关闭.再打开流出上层液体C . 碘易溶于酒精,微溶于水,故可以用酒精萃取碘水中的碘D . 萃取之后,一般通过分液漏斗将互不相溶的液体分离5. (2分) (2016高一下·庄浪期中) 下列说法正确的是()A . 第三周期非金属元素含氧酸的酸性从左到右依次增强B . HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱C . 元素周期律是元素原子核外电子排布周期性变化的结果D . 形成离子键的阴、阳离子间只存在静电吸引力6. (2分) (2018高二下·宜昌期末) 某温度时,使用一对石墨电极电解饱和Na2SO4溶液,当转移2 mol电子时停止电解,析出Na2SO4·10H2O晶体m g,所有数据都在相同温度下测得,下列叙述错误的是()A . 电解后溶液质量减少(m+18)gB . 原溶液中Na2SO4的质量分数为C . 若其他条件不变,将石墨替换为铜电极,则阴极析出1mol H2D . 若其他条件不变,将石墨替换为铜电极,则析出Na2SO4·10H2O晶体仍为m g7. (2分) (2018高二下·北京期末) 下列各组物质充分反应后过滤,将滤液加热、蒸干至质量不变,最终不能得到纯净物的是()A . 向漂白粉浊液中通入过量的CO2B . 向带有氧化膜的铝片中加入盐酸C . 向含有1molCa(HCO3)2的溶液中加入1molNa2O2D . 向含有1molKAl(SO4)2的溶液中加入2molBa(OH)2二、实验题 (共1题;共7分)8. (7分)(2020·江苏模拟) 矿业废水中Al3+含量的测定和处理是环境保护的重要课题。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐城市2013届高三年级第二次模拟考试化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Si 28 K 39 Fe 56选择题单项选择题:本题包括10小题,每小题2分,共计20分。
每小题只有一个选项符合题意。
1.化学在资源合理开发利用和生态环境保护方面正发挥着积极作用,下列行为与可持续发展理念相违背的是A.提高车用燃气、燃油品质,减少大气污染物的排放B.调整能源结构,推广核电、水电、天然气等清洁能源的应用比例C.将造纸废水通过高压水井压到地下,节约生产成本D.探寻新的反应途径、不断提高化学反应过程的选择性,提高合成反应的原子利用率2.下列有关化学用语表示正确的是A.羧基电子式B. O2-的结构示意图C.质子数35,中子数44的溴原子D. Al(OH)3在水溶液中的电离方程式H++H2O+AlO2-\leftrightharpoons AI(OH)3\leftrightharpoonsAl3+++3OH-3.常温下,下列各组离子在指定溶液中一定能大量共存的是A.0.1mo1/L NaI溶液:K+, Na+ , MnO4- , OH-B.能溶解CaCO3的溶液:K+, NH4+, Cl -, NO3-C.0.1mo1/LNaHSO3溶液:Na +, Mg2+, SO42- , ClO-D. c(H+)/c(OH-}=1013,的溶液:K+, Fe2+, Cl-, NO3-4.以0.1000 mol·L-1 NaOH溶液滴定c mol·L-1,某弱酸HA溶液,其滴定曲线如图I所示,下列说法正确的是A.可用甲基橙作滴定指示剂B.指示剂指示的滴定终点就是反应终点C.突变范围的大小与酸的强弱及酸的浓度有关D.滴定时氢氧化钠溶液盛放在带活塞的滴定管中5.下列有关物质的性质与其应用不相对应的是A. NH3分解生成N2和H2吸热热量,液氨可用作致冷剂B.浓硫酸具有吸水性,可用作Cl2的干燥剂C: CaO2能与水缓慢释放O2,可用作供氧剂D.聚合硫酸铁[Fe x(OH)Y(SO4)z·nH2O]能水解得到Fe(OH)3胶体,可用作净水剂6:下列使用漏斗的几个实验装置中,设计正确且能达到实验目的的是A.用图2所示装置进行过滤,过滤时不断搅拌B.用图3所示装置吸收NH3制氨水C.用图4所示装置用苯萃取碘水中的碘,并把碘的苯溶液从漏斗下口放出D.用图5所示装置用石灰石与稀盐酸制取CO2气体7.下列是部分矿物资源的利用及产品流程(如图6),有关说法不平确的是A.粗铜电解精炼时,粗铜作阳极B.生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应C.黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶铁的原料D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法8.设N A表示阿伏加德罗常数的值。
下列说法正确的是A. 45gHCH0与CH3COOH混合物含氢原子数为3N AB.常温常压下,54g重水(D20)含水分子数为3N AC.标准状况下,11.2L苯含有C-H键数目为3N AD.反应KIO3+6HI=3I2+KI+3H20,每生成1.5mol I2转移电子数为3N A9.下列表示对应化学反应的离子方程式正确的是A.足量Cl2通入FeBr2溶液中:2Br-+ Cl2 = Br2 +2Cl-B.用NaClO除去水体中CO(NH2)2产生CO2和N2:3ClO +CO(NH2)2=3Cl- +CO2\uparrow +N2\uparrow +2H2OC.过量CO2通入Na2SiO3溶液中:Si032-+CO2+H2O = H2SiO3\downarrow +CO32-D. Ca(HCO3)=溶液中加入过量NaOH溶液:Ca2+ + HCO3-+OH-= CaCO3\downarrow +H2O10.下列有关说法正确的是A. 4CuO(s)=2Cu2O(s)-+O2(g)在室温下不能自发进行,说明该反应△H<0B.生铁和纯铁同时放入海水中,纯铁更易腐蚀C,常温下,PbSO4易溶于pH=7的CH3COONH4溶液,说明((CH3COO)2Pb是弱电解质D. H2S(g)+FeO(s)\leftrightharpoons FeS(s)+H2O(g),其他条件不变时增大压强,反应速v(H2S)和H2S的平衡转化率均增大不定项选择题:本题包括5小题,每小题4分,共计20分。
每小题只有一个或两个选项符合题意。
若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分. 11. 4`-去甲基表鬼臼毒素具有抗肿瘤、抗菌、抗病毒等作用,它的结构式如图7所示,下列关于该有机物的结构和性质描述正确的是A.分子中含有2个手性碳原子B.能与FeCl3溶液发生显色反应C.能发生加成、消去、氧化及取代反应D. 1 mol该物质最多可与3 mol NaOH反应12.短周期元素X, Y, Z, W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y原子基态时最外层电子数是次外层的3倍,}z是一种储氢材料,W与Y属于同一主族。
下列叙述正确的是A.原子半径:rW >rZ>rYB.元素Y的简单气态氢化物的热稳定性比W的弱C.化合物从X2Y、ZY,、WY3中化学键的类型相同D.化合物ZWY4·7X2Y的水溶液显酸性13.下列根据实验操作和现象所得出的结论正确的是14.二甲醚是一种清洁燃料,以n(H2)/n(CO)=2通入1L的反应器中,一定条件下发生反应:2CO(g)+4H2(g)\leftrightharpoons CH3OCH3(g) +H2O(g) \triangle H,其CO的平衡转化率随温度、压强变化关系如图8所示,下列说法正确的是A.上述反应△H>0B.图中P1<P2<P3C.若在P3和316℃时,测得容器中n(H2)=n(CH3OCH3),此时v(正)<v(逆)D.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%15.己知H2CO3的酸性强于H2S,将amol·L -1 NaHS与bmol·L-1NaOH两种稀溶液等体积混合(a>0,b>0),所得溶液中微粒间的物质的量浓度关系正确的是A. a=b时:c(OH-)= c(H+)+c(HS-)B. a=2b时:c(S2-)>c(HS )>c(OH-)>c(H+)C. a=3b时:。
C(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)D. a=4b时:4c(Na+)=5c(S2-)+5c(HS-)5c(H2S)非选择题16. (12分)用石灰乳、石灰氮(CaCN2)和炼厂气(含H2S)反应,既能净化尾气,又能获得应用广泛的CS(NH2)2(硫脲),其部分工艺流程如下:(1)高温下,H2S存在下列反应:2H2S(g)\leftrightharpoons 2H2(g)+S2(g),其平衡常数表达式为K=▲。
(2)用石灰乳吸收H2S制取Ca(HS)2需要在低温下进行,其原因是▲;过滤得到的滤渣可再利用,滤渣的主要成分是▲(填化学式)。
(3)合成硫脲需长时间搅拌,并在较高温度(80℃-85℃)下进行,其目的是▲。
Ca(HS)2与CaCN2在水溶液中合成硫脉的化学方程式为▲。
(4)化合物X与硫脲互为同分异构体,X加入FeCl3溶液中,溶液显红色,X的化学式为▲。
17. (15分)托卡朋是基于2012年诺贝尔化学奖的研究成果开发的治疗帕金森氏病药物,《瑞士化学学报》公布的一种合路线如下:(1) C→D的反应类型▲。
(2)化合物F中的含氧官能团有经基、▲和▲(填官能团名称)。
(3)写出同时满足下列条件的D的一种同分异构体的结构简式▲。
①能与Br2发加成反应;②是萘,的衍生物,且取代基都在同一个苯环上;③在酸性条件下水解生成的两种产物都只有4种不同化学环境的氢.(4)实现A→B的转化中,叔丁基锂[(CH3)CLi]转化为((CH3)2C=CH2,同时有LiBr生成,则X(分子式为C15H14O3)的结构简式为▲。
(5) 是合成神经兴奋剂回苏灵的中间体,请写出以CH3CH2CH2Br和为原料(原流程图中的试剂及无机试剂任用)该化合物的合成路线流程图。
合成路线流程图示例如下:▲。
18. (12分)二硫化亚铁是Li/FeS2电池的正极活性物质,可用水热法合成。
FeSO4、Na2S2O3、S及H2O在200℃连续反应24小时,四种物质以等物质的量反应,再依次用CS2、H2O洗涤、干燥及晶化后得到。
(1)合成FeS2离子方程式为▲。
(2)用水洗涤时,如何证明S042-己除尽▲。
(3)己知1.20gFeS2在O2中完全燃烧生成Fe2O3和SO2气体放出8.52kJ热量,FeS2燃烧反应的热化学方程式为▲。
(4)取上述制得的正极材料1.1200g (假定只含FeS一种杂质),在足量的氧气流中充分加热,最后得0.8000g红棕色固体,则该正极材料中FeS2的质量分数(写出计算过程)。
▲19. (15分)过二硫酸钾(K2S2O8)是一种无色结晶,不溶于乙醇,有强氧化性,易分解。
实验室制备过二硫酸钾可通过低温电解KHSO4认溶液得到。
实验步骤如下:步骤I.称取40gKHSO4溶解90mL蒸馏水,倒入大试管,试管浸在冰水浴中(装置见图9),并冷却到5℃以下。
步骤2电解2h,每隔约半小时补一次冰步骤3.将沉淀收集在漏斗中,直接用乙醇和乙醚洗涤和过滤步骤4.干燥、称重步骤5.回收乙醚和乙醇(1)电解总反应的化学方程式为▲。
(2)电解过程中,阳极产生微量且能使湿润的KI-淀粉变蓝的有色单质气体,该气体可能是▲(填化学式)。
(3)步骤2每隔半小时要向大烧杯添加冰块,其原因是▲。
(4)步骤5回收乙醇、乙醚时采用的操作方法是▲。
(5)取得到的样品0.2500g溶于30mL水,加4gKI,塞住瓶塞,振荡,静止15min,加入1mL 冰醋酸,再用cmol·L- 1Na2S2O3溶液滴定。
(S2O82- +3I- =2SO42- +I3-; I3-\leftrightharpoons I2+I;2S2O32-+I2=2I- + S4O62-)①溶解时,加入KI后需塞住瓶塞,其目的是▲。
②本实验所用的指示剂为,▲。
③若本次滴定消耗Na2SO3溶液VmL,由本次结果计算,样品中K2S2O8的纯度为▲(用含c、V的代数式表示)。
(6)分析化学上检验Mn2+在Ag+催化下K2S2O8溶液将Mn2+氧化为紫色的MnO4-,该反应的离子方程式为▲。
