2-甲基-6-硝基苯胺的合成及表征
2-甲基-4(6)-硝基苯胺合成工艺的研究

江 苏 技 术 师 范 学 院 学 报 ( 然 科 学 版) 自
Vo .4 N . 1 . o3 1 S p, 2 0 e. 08
2 一甲基 一4 6 一硝基苯胺合成工艺 的研 究 ()
王 雅 珍
( 苏技术 师范学 院 化学化工学院, 江 江苏 常州 2 3 0 10 )
摘
要: 2一 甲基苯胺 为原料 , 冰醋 酸酰化 , 酸硝 化 , 以 经 混 再用 盐酸水解 来合 成 2一甲基 一4一硝基 苯胺 和
2 一甲基 一 一硝基苯胺为橙红色针状 晶体 ,是一种工业中应用广泛的有机染料或有机物的中间体 , 6 也 是 医药 中 间体 , 以合 成具 有 保养性 能 的药 物 ; 一甲基 一4一硝基 苯 胺 ( 品名 为红 色 基 R ) 黄色 粉 可 2 商 L为 末 状 , 一 种工 业 中应用 广泛 的有机染 料 , 是 以其为 主要 原料 , 可合 成分 散染 料 , 还 主要 有 分散 荧火 黄 I、 分 散黄 8媒染染料等 , 、 同时它也是医药中间体 。 以2 一甲基苯胺 、 乙酸酐为原料 , 经酰化 、 硝化、 再水解合成 2 一甲基 一 一 6 硝基苯胺 , 产率为 4 %t 由 6 l 。 于 乙酸酐 是 限购 产 品 , 易 购买 , 且 冰 乙酸 比乙酸 酐价 格低 , 不 并 故选 用 冰 醋 酸做 酰化 试 剂 , 上述 的合 成 对 方法进行研究并加以改进 , 混酸硝化 以惰性 的 1 一二氯 乙烷翻 , 2 做溶剂 , 硝化产物的分离采用粱毓学等[ 3 1 的 分 离方 法 , 终得 到 两种 硝 化产 物 , 最 分别 是 2一甲基 一6一硝基 苯 胺 和 2一甲基 一4一硝 基 苯胺 , 对 影 响 并 酰化 、 化 、 硝 水解 反 应产 率 的 因素进 行 了研 究 , 2一甲基 一 4一硝基 苯胺 的产率 是 2 .2 2一甲基 一6 77 %, 一硝 基 苯胺 的产 率是 4 .5 47 %。 N一 酰化反应常见的酰化剂是羧酸 、酸酐和酰氯。当 R相同时 ,酰化反应的活性次序是 : C : R OH< (C ) R O: O<R O 1 C C。用酸酐进行酰化反应是不可逆 的, 由于乙酸酐的反应活性 比较高 , 乙酸酐滴加要严格 控制温度 , 需要冰盐浴来控温 , 而且 由于价格较高 , 乙酸酐作为酰化剂的应用受到一定限制 , 使 通常乙酸 酐用 在碱 性 较弱 的芳 胺 的酰 化 和在水 介 质 中酰化 。用 羧酸 对胺 进行 酰化 反应 是 可逆 的 , 要使 反应 进 行 到 底, 必须 加入 过量 羧 酸 , 不 断 除去生 成 的水 , 并 本研 究采 用 分馏 的办 法使水 和 乙酸 分离 。合成 反应 的路线
一种荧光增强型的GSH荧光探针

一种荧光增强型的GSH荧光探针孟美荣;阴彩霞【摘要】常见的生物硫醇包括半胱氨酸(Cys)、同型半胱氨酸(Hcy)以及谷胱甘肽(GSH),它们在人体中起着十分重要的作用.使用荧光探针检测此类生物硫醇具有灵敏度高、选择性好、响应时间快等优势.由于3种硫醇具有相似的化学结构(含有活性巯基),因此给这类生物硫醇的选择性检测带来挑战,本文设计了一种荧光探针(2-甲基,6-丙烯酰基喹啉)用于区分检测GSH和Cys/Hcy.通过测试该探针的光谱性质,发现在含有该探针的水溶液中加入谷胱甘肽(GSH)后,相应的荧光光谱和紫外-可见光谱都有显著的变化,相比其他分析物,发现探针在水溶液中对GSH具有较高的选择性和灵敏度.此外,考虑到该检测过程是在水相中进行的,因此该探针在生物成像方面具备潜在的使用价值.【期刊名称】《河北大学学报(自然科学版)》【年(卷),期】2019(039)001【总页数】7页(P49-55)【关键词】荧光探针;喹啉;生物硫醇;荧光增强【作者】孟美荣;阴彩霞【作者单位】山西大学化学化工学院,山西太原030006;山西大学分子科学研究所,山西太原030006【正文语种】中文【中图分类】O316生物硫醇存在于许多蛋白质和简单小分子中,其在防御细胞氧化过程中起着重要的作用[1].内源性生物硫醇主要由小分子生物硫醇和大分子生物硫醇组成.小分子生物硫醇主要包含谷胱甘肽(GSH)、半胱氨酸(Cys)、同型半胱氨酸(Hcy)等,大分子生物硫醇则包括酶、肽、生物膜等.研究发现细胞内小分子生物硫醇中谷胱甘肽(GSH)的含量最为丰富[2-4],并且在二硫化物(氧化形式,GSSG)和巯基(还原形式,GSH)之间存在氧化还原平衡[5].谷胱甘肽(GSH)通过维持细胞生长的氧化还原稳态而在氧化应激中起关键作用[6],且其水平与众多疾病相关,包括癌症,心血管疾病和阿尔茨海默氏症等[7-10].游离谷胱甘肽与其氧化态谷胱甘肽二硫化物的物质的量比(通常为4 100∶1)通常作为一种指示相应酶活性的指示剂[11].在硫醇分析技术中,与高效液相色谱法[12-13]和电化学检测[14-15]作对比,基于荧光探针的检测是最有效的工具,并且在体内硫醇成像方面,特别是活细胞中,具有明显的优势.在探针对生物硫醇的检测中,主要利用了生物硫醇中的巯基具有强的亲核性,该反应类型通常包括磺酸酯和磺酰胺的裂解[16-17],迈克尔加成[18-19],Se-N键或S-S键的裂解.通过巯基与α,β-不饱和羰基进行迈克尔加成去辨别同型半胱氨酸(Hcy)、半胱氨酸(Cys)和谷胱甘肽(GSH)是困难的,因为3种硫醇中巯基的亲核性比较接近[20]. 据报道,1,8-萘酰亚胺-Cu(Ⅱ)组装体作为用于检测硫醇的新型增强型荧光探针,其对硫醇具有较高的选择性,但不能特异性识别硫醇[21]. 近来报道的基于ICT和PET组合使用的荧光探针也不能很好的区分识别生物硫醇. 此外,探针对生物硫醇的响应时间也是一个关键的因素[22]. 鉴于喹啉及其衍生物具有优异的水溶性和稳定的光学性质,因此它可作为许多荧光探针的荧光团[23]. 此项工作中,笔者设计了一个高选择性、高灵敏度荧光探针:2-甲基,6-丙烯酰基喹啉,该探针能特异性识别谷胱甘肽(GSH),并且在H2O溶液中光谱性质良好,在活体细胞成像中具备广阔的运用前景.1 实验部分1.1 仪器和试剂1.1.1 仪器Hitachi F-7000荧光光谱仪、Cary 50 Bio紫外-可见光谱仪、Bruker ARX 300超导核磁共振仪、圆底烧瓶、恒温磁力搅拌器、旋转蒸发仪等.1.1.2 试剂所有试剂均为分析纯. 对硝基苯胺、巴豆醛、浓盐酸(12 mol/L)、氯化亚锡、丙烯酰氯、谷胱甘肽(GSH)、半胱氨酸(Cys)、同型半胱氨酸(Hcy)、各类氨基酸(L-赖氨酸、L-亮氨酸等)、各类阴离子等)、三乙胺等均购于Sigma-Aldrich公司.1.2 一般的测量方法用甲醇制备探针的储备液,使其浓度为2×10-3 mol/L. 荧光光谱和紫外-可见光谱均在H2O中检测得到. 荧光光谱在激发狭缝/发射狭缝为2.5 nm/5 nm,激发波长280 nm条件下测得. 该探针的荧光光谱在448 nm处对GSH呈现荧光增强响应,探针对硫醇的检测限为0.13 μmol/L. 实验所用阴离子溶液均由其钠盐经去离子水制备而成,各类氨基酸(半胱氨酸、同型半胱氨酸、谷胱甘肽、L-赖氨酸、L-亮氨酸、L-异亮氨酸、γ-氨基丁酸、L-丙氨酸、甘氨酸、L-苏氨酸)的储备液均由去离子水制备得到.1.3 荧光探针的制备及表征1.3.1 化合物2的合成在50 mL圆底烧瓶中加入2.762 4 g对硝基苯胺(化合物1,2 mmol)和15 mL盐酸(6 mol/L),开启冷凝回流装置,在搅拌状况下将反应液加热到100 ℃,利用注射器缓慢将1.5 mL巴豆醛(32 mmol)加入上述反应液中,并恒温反应12 h.反应结束后将反应液冷却到室温,用50 mL蒸馏水和20 mL乙酸乙酯进行萃取,去除上层有机相溶液,用氨水(NH3·H2O)调节下层水相溶液pH至中性,此时有大量墨绿色固体析出,通过循环水真空泵进行减压抽滤,得到墨绿色固体,将固体放入真空干燥箱烘干,经称量固体重量为1.04 g,产率为37.6 %.1.3.2 化合物3的合成在50 mL圆底烧瓶中加入1 g化合物2(5 mmol)和10 mL盐酸(1 mol/L),开启搅拌装置,将反应体系加热到105 ℃,同时将4.513 g氯化亚锡(20 mmol)溶于10 mL盐酸(1 mol/L)中配成溶液加入反应体系中,恒温反应1~3 h. 反应结束后先将反应液冷却到室温,再转移至烧杯中并加入20 mL蒸馏水,用氨水(NH3·H2O)调节溶液pH,直至有橙蓝色荧光为止.然后将上述溶液用乙酸乙酯进行萃取,收集上层有机相溶液. 利用旋转蒸发仪将有机相溶液蒸干,得到黄色固体. 随后将固体产物进行分离纯化,展开剂选用V(乙酸乙酯)∶V(石油醚)= 5∶1进行过柱,收集有蓝色荧光的产物,最终得到淡黄色固体(0.54 g),产率为54%.1.3.3 探针(化合物4)的合成探针的合成路线如图1所示,将0.316 4 g化合物3(2 mmol)和15 mL二氯甲烷加入到圆底烧瓶中,再加入0.3 g三乙胺(3 mmol),最后加入0.271 53 g丙烯酰氯(3 mmol),将上述体系在冰水浴中持续搅拌12 h.反应结束后用旋转蒸发仪将反应液蒸干,得到黄色粗产物.随后将粗产物进行过柱纯化,用V(乙酸乙酯)∶V(石油醚)∶V(二氯甲烷)=1∶1∶1的展开剂进行分离,收集蓝绿色荧光产物,最终得到0.289 5 g白色固体产物,产率为91.5 %. 探针的核磁表征如图2所示,1H NMR (600 MHz, Chloroform-d):δ 8.44 (s, 1H), 8.12 (s, 1H), 8.00 (d, J = 8.4 Hz,1H), 7.94 (d, J = 9.0 Hz, 1H), 7.56 (d, J = 8.9 Hz, 1H), 6.49 (d, J = 16.8 Hz,1H), 6.34 (dd, J = 16.8, 10.2 Hz, 1H), 5.79 (d, J = 10.2 Hz, 1H), 2.72 (s, 4H);13C NMR (75 MHz, Chloroform-d):163.9,158.1,145.0,136.3,135.2,131.0,129.0,128.2,127.0,123.2,122.7,116.5,25.1.图1 探针的合成路线Fig.1 Synthetic route of probe1H NMR (600 MHz) 13C NMR (75 MHz)图2 探针在CDCl3溶液中的1H NMR (600 MHz)和13C NMR (75 MHz)Fig.2 1H NMR (600 MHz) and 13C NMR (75 MHz) of probe in CDCl32 结果与讨论2.1 探针对GSH的紫外-可见吸收光谱探针对谷胱甘肽(GSH)的紫外滴定用Cary 50 Bio紫外-可见光谱仪进行测定. 检测谷胱甘肽(GSH)的紫外-可见吸收光谱如图3所示,在2 mL含2-甲基,6-丙烯酰基喹啉(20 μmol/L)的H2O溶液中加入谷胱甘肽(GSH)溶液,随着谷胱甘肽(0~65 μmol/L)的加入,探针在230 nm处的吸收峰逐渐降低,在275 nm处的吸收峰逐渐升高,在210 nm和255 nm处出现2个等吸收点,这表明有新的物质生成.2.2 探针对GSH的荧光光谱滴定探针对谷胱甘肽(GSH)的荧光滴定实验用Hitachi F-7000荧光光谱仪进行测定. 检测谷胱甘肽(GSH)的荧光发射光谱如图4所示,图4说明探针对谷胱甘肽(GSH)有较强的荧光响应,随着谷胱甘肽(GSH)浓度(0~37 μmol/L)的增加,448 nm处的荧光不断增强,表明此探针对GSH的荧光识别具有荧光增强的效果(激发狭缝宽度/发射狭缝宽度:2.5 nm/5 nm,激发波长:280 nm).图3 在H2O溶液中,探针(20 μmol/L)在不同浓度谷胱甘肽(0~65 μmol/L)下的紫外-可见吸收光谱Fig.3 UV-Vis absorption spectra of probe(20 μmol/L) in the presence of various concentrations of GSH (0~65 μmol/L) in H2O激发狭缝宽度/发射狭缝宽度:2.5 nm/ 5 nm,激发波长:280 nm图4 在H2O 溶液中,探针(2 μmol/L)在不同浓度谷胱甘肽(0~37 μmol/L)下的荧光光谱Fig.4Fluorescence spectra of probe (2 μmol/L) in the presence of various concentrations of GSH (0~37 μmol/L) in H2O2.3 探针的选择性实验选择性是探针性能的一个重要指标. 为了探究探针的选择性,进行了紫外-可见吸收光谱干扰和荧光光谱干扰实验. 探针(20 μmol/L)对65 μmol/L谷胱甘肽(GSH)和其他干扰物(650 μmol/L)的紫外-可见吸收光谱如图5A所示.由图5A中紫外-可见吸收光谱变化曲线可知:在2 mL含有探针化合物的H2O溶液中,加入浓度为100 μmol/L的各种分析物,包括半胱氨酸、同型半胱氨酸、谷胱甘肽、L-赖氨酸、L-亮氨酸、L-异亮氨酸、γ-氨基丁酸、L-丙氨酸、甘氨酸、L-苏氨酸. 除了谷胱甘肽(GSH)外,均无明显变化. 探针(2 μmol/L)对37 μmol/L谷胱甘肽(GSH)和其他干扰物(370 μmol/L)的荧光光谱图如图5B所示. 由图5B的变化曲线可知:在激发波长为280 nm时,探针与谷胱甘肽(GSH)有较强的荧光发射. 当加入其他分析物半胱氨酸、同型半胱氨酸、谷胱甘肽、L-赖氨酸、L-亮氨酸、L-异亮氨酸、γ-氨基丁酸、L-丙氨酸、甘氨酸、L-苏氨酸)时,其在448 nm处的荧光强度无明显变化. 实验结果表明,探针对谷胱甘肽(GSH)具有较好的选择性识别.图5 a) 探针对GSH的紫外-可见吸收光谱选择性实验; b) 探针对GSH的荧光光谱选择性实验Fig.5 a) The selective experiment of probe to GSH by UV-Vis absorption spectra; b) the selective experiment of probe to GSH by Fluorescence spectra2.4 探针的动力学研究对探针与谷胱甘肽(GSH)的动力学进行了相关研究,如图6所示. 从图6可以看出,当探针(2 μmol/L)中加入37 μmol/L谷胱甘肽(GSH)时,体系荧光强度立即增强,且荧光强度在220 s后不再增加,这表明探针与谷胱甘肽(GSH)在220 s后反应完全.激发波长: 280 nm, 激发狭缝宽度/发射狭缝宽度:2.5 nm/5 nm图6 在H2O溶液中,探针(2 μmol/L)与谷胱甘肽(37 μmol/L)在448 nm处的反应时间曲线Fig.6 Reaction time profile of fluorescence spectra of probe (2 μmol/L) upon addition of GSH2.5 探针的检测限通过对荧光光谱数据进行分析可以得到检测极限. 首先将探针溶液(2 μmol/L)连续扫描10次,其中激发狭缝宽度/发射狭缝宽度为2.5 nm/5 nm,测定其在448 nm处的荧光发射强度,然后计算标准偏差σ,再通过滴定实验得到不同GSH浓度下的荧光发射光谱,将荧光发射光谱中448 nm处的荧光强度对不同浓度GSH(0~40 μmol/L)作图,线性拟合得到一条直线,如图7所示,其线性方程为Y=87.57c+154.22,线性相关系数R2=0.985. 由IUPAC定义的检出限公式(CDL= 3σ/k),得到探针对谷胱甘肽(GSH)的检出限为0.13 μmol/L.可看出此探针对GSH具有较高的灵敏度.图7 448 nm处荧光强度随GSH浓度变化关系Fig.7 Fluorescence intensity at 488 nm was plotted as a function of GSH concentration3 结论综上所述,利用市售的对硝基苯胺通过三步反应合成了一种荧光增强型的GSH探针:2-甲基,6-丙烯酰基喹啉.通过核磁共振数据对该探针的结构进行了表征,通过紫外-可见吸收光谱和荧光发射光谱等手段对探针进行了相应的光谱性能测试,发现探针对谷胱甘肽(GSH)有较高的选择性. 此外,探针可以在水相中对GSH进行光谱检测,其荧光检测限可低至0.13 μmol/L. 因此,该探针可以对癌细胞内的谷胱甘肽(GSH)浓度进行相应的检测.参考文献:【相关文献】[1] ZHANG S Y, ONG C N, SHEN H M. Critical roles of intracellular thiols and calcium in parthenolide-induced apoptosis in human colorectal cancer cells [J]. Cancer Lett, 2004, 208(2): 143-153. DOI: 10.1016/j.canlet.2003.11.028.[2] HUANG C, SINSKEY A J, LODISH H F. Oxidized redox state of glutathione in the endoplasmic reticulum [J]Science, 1992, 257(5076): 1496-1502. DOI:10.1126/science.1523409.[3] HONG R, HAN G, FERNNDEZ J M, et al. Glutathione-mediated delivery and release using monolayer protected nanoparticle carriers [J]. J Am Chem Soc, 2006, 128(4): 1078-1079. DOI: 10.1021/ja056726i.[4] HASSAN S S M, RECHNITZ G A. Determination of glutathione and glutathione reductase with a silver sulfide membrane electrode [J]. Anal Chem, 1982, 54(12): 1972-1976. DOI: 10.1021/ac00249a013.[5] KIZEK R, VACEK J, TRNKOV L, et al. Cyclic voltammetric study of the redox system of glutathione using the disulfide bond reductant tris(2-carboxyethyl)phosphine [J]. Bioelectrochemistry, 2004, 63(1-2): 19-24. DOI: 10.1016/j.bioelechem.2003.12.001.[6] RAHMAN I, MACNEE W. Regulation of redox glutathione levels and gene transcription in lung inflammation: therapeutic approaches [J]. Free Radic Biol Med, 2000, 28(9): 1405-1420. DOI: 10.1016/S0891-5849(00)00215-X.[7] CURELLO S, CECONI C, CARGNONI A, et al. Improved procedure for determining glutathione in plasma as an index of myocardial oxidative stress [J]. Clin Chem, 1987, 33(8): 1448-1449.[8] KLEINMAN W A, RICHIE JR J P. Status of glutathione and other thiols and disulfides in human plasma [J]. Biochem Pharmacol, 2000, 60(1): 19-29. DOI: 10.1016/S0006-2952(00)00293-8.[9] MACDONALD C M, DOW J, MOORE M R. A possible protective role for sulphydryl compounds in acute alcoholic liver injury [J]. Biochem Pharmacol, 1977, 26(16): 1529-1531. DOI: 10.1016/0006-2952(77)90428-2.[10] BUHL R, HOLROYD K J, MASTRANGELI A, et al. Systemic glutathione deficiency in symptom-free HIV-seropositive individuals [J]. The Lancet, 1989, 334(8675): 1294-1298. DOI: 10.1016/S0140-6736(89)91909-0.[11] DALTON T P, SHERTZER H G, PUGA A. Regulation of gene expression by reactive oxygen [J]. Annu Rev Pharmacol Toxicol, 1999, 39(1): 67-101. DOI:10.1146/annurev.pharmtox.39.1.67.[12] IVANOV A R, NAZIMOV I V, BARATOVA L. Determination of biologically active low-molecular-mass thiols in human blood: I. Fast qualitative and quantitative, gradient and isocratic reversed-phase high-performance liquid chromatography with photometric and fluorescence detection [J]. Chromatogr A, 2000, 895(1-2): 157-166. DOI: 10.1016/S0021-9673(00)00713-5.[13] AMARNATH K, AMARNATH V, AMARNATH K, et al. A specific HPLC-UV method for the determination of cysteine and related aminothiols in biological samples [J]. Talanta, 2003, 60(6): 1229-1238. DOI: 10.1016/S0039-9140(03)00232-7.[14] JIANG H, JU H. Electrochemiluminescence sensors for scavengers of hydroxyl radical based on its annihilation in CdSe quantum dots film/peroxide system [J]. Anal Chem, 2007, 79(17): 6690-6696. DOI: 10.1021/ac071061j.[15] WANG W, LI L, LIU S, et al. Determination of physiological thiols by electrochemical detection with piazselenole and its application in rat breast cancer cells 4T-1 [J]. J Am Chem Soc, 2008, 130(33): 10846-10847. DOI: 10.1021/ja802273p.[16] BOUFFARD J, KIM Y, SWAGER T M, et al. A highly selective fluorescent probe for thiol bioimaging [J]. Org Lett, 2008, 10(1): 37-40. DOI: 10.1021/ol702539v.[17] JI S, GUO H, YUAN X, et al. A highly selective OFF-ON red-emitting phosphorescent thiol probe with large stokes shift and long luminescent lifetime [J]. Org Lett, 2010, 12(12): 2876-2879. DOI: 10.1021/ol100999j.[18] SIPPEL T O. New fluorochromes for thiols: maleimide and iodoacetamide derivatives of a 3-phenylcoumarin fluorophore [J]. J Histochem Cytochem, 1981, 29(2): 314-316. DOI: 10.1177/29.2.7019305.[19] ROS-LIS J V, GARCA B, JIMÉNEZ D, et al. Squaraines as fluoro-chromogenic probes for thiol-containing compounds and their application to the detection of biorelevant thiols [J]. J Am Chem Soc, 2004, 126(13): 4064-4065. DOI: 10.1021/ja031987i.[20] ELLMAN G L. Tissue sulfhydryl groups [J]. Arch Biochem Biophys, 1959, 82(1): 70-77. DOI: 10.1016/0003-9861(59)90090-6.[21] LE M, MEANS G E. A procedure for the determination of monothiols in the presence of dithiothreitol-an improved assay for the reduction of disulfides [J]. Anal Biochem, 1995, 229(2): 264-271. DOI: 10.1006/abio.1995.1411.[22] YUAN L, LIN W, XIE Y, et al. A native-chemical-ligation-mechanism-based ratiometric fluorescent probe for aminothiols [J]. Chem Eur J, 2012, 18(45): 14520-14526. DOI:10.1002/chem.201201606.[23] HENDRICKSON K M, GEUE J P, WYNESS O, et al. Coordination and fluorescence of the intracellular Zn2+ probe [2-methyl-8-(4-toluenesulfonamido)-6-quinolyloxy] aceticacid (Zinquin A) in ternary Zn2+ complexes [J]. J Am Chem Soc, 2003, 125(13): 3889-3895. DOI: 10.1021/ja020685y.。
简述由甲苯制备2甲基5硝基苯胺的合成路线

简述由甲苯制备2甲基5硝基苯胺的合成路线1. 引言1.1 概述甲苯是一种常见的有机溶剂,具有广泛的应用领域。
它是由苯环上一个甲基取代而成,其化学结构简单直观,使得它成为许多化工合成反应中的重要中间体。
本文将介绍由甲苯制备2甲基5硝基苯胺的合成路线。
1.2 文章结构本文分为五个主要部分。
引言部分即当前所在部分,旨在对文章内容进行概述和介绍。
第二部分将介绍甲苯的性质和用途,包括其化学性质、应用领域以及制备方法概述。
第三部分将详细介绍合成路线一:甲苯氧化制备对甲酚,再经硝化制备2,4-二硝基甲苯(DNT)的过程和条件,并讨论其中存在的问题以及可能的改进方法。
第四部分将阐述合成路线二:甲苯烷基化生成二正十四烷,再经硝化反应制备2,4,6-三硝基-16-亚胺基双(十四烷基)萘(TATB)的过程和条件,并探讨其中存在的问题和改进方向。
最后,第五部分将给出对本合成路线的总结和结论。
1.3 目的本文旨在简述由甲苯制备2甲基5硝基苯胺的两种合成路线,并探讨这两种方法的优缺点及可能存在的改进方向。
通过深入了解这些合成路线,我们可以更好地理解甲苯在化工领域中的应用以及相关反应机制,为未来的研究提供有价值的参考和指导。
2. 甲苯的性质和用途:2.1 甲苯的化学性质:甲苯,化学式为C7H8,是一种无色液体。
它具有辛辣的芳香气味,并且不溶于水,可溶于大多数有机溶剂。
甲苯是一种稳定的化合物,但在高温、光照及与氧气接触时可能发生自燃。
2.2 甲苯的应用领域:甲苯在工业上广泛应用于多个方面。
首先,由于其具有良好的溶解性和挥发性,在油漆、清漆和胶黏剂制造中被广泛使用。
其次,甲苯也是许多塑料、橡胶和纤维素等材料的重要原料。
此外,由于其在化学反应中作为溶剂和试剂具有重要作用,因此也被广泛应用于医药、农药和染料工业。
2.3 甲苯制备方法概述:主要有两种常见的方法用于合成甲苯:一是通过乙烷与异丁烷催化重整得到对二甲苯再经分离获得纯净甲苯;另一种方法是通过对二甲苯的氧化反应制备。
2-甲基-4-硝基苯胺的制备方法

2-甲基-4-硝基苯胺的制备方法一、概述2-甲基-4-硝基苯胺是一种重要的有机化合物,广泛应用于染料、颜料、药物等领域。
其制备方法具有一定的技术难度,但经过不懈努力和研究,已经有了一些比较成熟的方法。
本文将介绍几种常见的2-甲基-4-硝基苯胺的制备方法,并对比它们的优缺点,为相关领域的研究人员提供参考。
二、硝基苯的氨基化反应1. 反应原理硝基苯的氨基化反应是2-甲基-4-硝基苯胺制备的关键步骤。
该反应是通过硝基苯和甲醛在氢气催化下发生缩合反应,生成对甲基苯胺,并且在硝基苯上有硝基基团。
2. 实验步骤(1)将硝基苯和甲醛溶于适量乙醇中;(2)向溶液中加入氢气催化剂;(3)在加热条件下,进行氨基化反应,得到2-甲基-4-硝基苯胺。
3. 优缺点分析优点:该方法操作简单,原料易得,反应条件温和。
缺点:反应过程中需要氢气催化剂,安全风险较高;所得产物纯度较低,需要进一步提纯。
三、硝基化反应1. 反应原理硝基化反应是将硝基磺酸铅与苯胺在硫酸存在下反应制备2-甲基-4-硝基苯胺的方法,属于亲电取代反应。
2. 实验步骤(1)将苯胺溶于硫酸中;(2)逐渐加入硝基磺酸铅,控制反应温度;(3)反应结束后,对产物进行提取和纯化,得到2-甲基-4-硝基苯胺。
3. 优缺点分析优点:反应条件温和,产率较高,适用于大规模生产。
缺点:硝基磺酸铅是一种有毒物质,操作过程中需要严格控制反应温度和压力,对实验操作人员要求较高。
四、芳香硝化法1. 反应原理芳香硝化法是将硝基硫酸与苯胺在硫酸存在下发生反应,生成硝基苯。
然后利用取代反应,将甲基基团引入到硝基苯中,制备2-甲基-4-硝基苯胺。
2. 实验步骤(1)将苯胺溶于浓硫酸中冷却至低温;(2)逐渐加入硝基硫酸,控制反应温度;(3)得到硝基苯后,再进行甲基化反应,得到2-甲基-4-硝基苯胺。
3. 优缺点分析优点:芳香硝化法可以较高产率地制备硝基苯,适用于工业化生产。
缺点:该方法操作复杂,且硝基硫酸也是一种有毒物质,需要严格控制操作条件和废弃物处理。
2-甲基-4(6)-硝基苯胺合成工艺的研究

2-甲基-4(6)-硝基苯胺合成工艺的研究
2-甲基-4(6)-硝基苯胺是一种重要的有机合成化合物,广泛应用于染料、医药和农药
等领域。
本文介绍了一种可行的2-甲基-4(6)-硝基苯胺的合成工艺。
实验材料:
2-甲基-4-硝基苯胺、硫酸、硝酸、苯酚、氢氧化钠、环己酮、蔗糖、氯化钙。
实验方法:
第一步,将2-甲基-4-硝基苯胺和苯酚按2:1的比例混合,加入环己酮中,搅拌至完
全溶解。
然后将混合物加入氢氧化钠溶液中,调节pH至8左右,再将蔗糖加入溶液中。
反应体系放置于温度为25℃的恒温槽中进行反应。
第二步,将反应物过滤,洗净出现的沉淀,过滤后沉淀再加入硫酸-硝酸混合液中进
行硝化反应。
加热至硝化反应结束,继续加热至沸腾状态下煮沸数小时,最后冷却至室温,用水洗涤沉淀,过滤干燥。
第三步,将干燥的产品加入氯化钙溶液中,过滤出溶液中的沉淀,再用醚萃取物进行
回流提取。
最后得到目标产物2-甲基-4(6)-硝基苯胺。
实验结果:
经过实验验证,得到的2-甲基-4(6)-硝基苯胺符合质量要求,并且还可以通过进一步的提纯工艺提高产品的纯度。
该方法制备2-甲基-4(6)-硝基苯胺的工艺简单、成本低,产品质量稳定,适用于大规模生产。
同时,该方法还可以通过对工艺参数的优化来进一步提高产率和纯度。
2-甲基-6-硝基苯胺的合成工艺研究[1]
![2-甲基-6-硝基苯胺的合成工艺研究[1]](https://img.taocdn.com/s3/m/5e12fcc38bd63186bcebbcdb.png)
2-甲基-6-硝基苯胺的合成工艺研究作者:祁磊, 庞思平, 孙成辉, QI Lei, PANG Si-ping, SUN Cheng-hui作者单位:祁磊,庞思平,QI Lei,PANG Si-ping(北京理工大学生命科学与技术学院,北京,100081), 孙成辉,SUN Cheng-hui(北京理工大学材料科学与工程学院,北京,100081)刊名:含能材料英文刊名:CHINESE JOURNAL OF ENERGETIC MATERIALS年,卷(期):2009,17(1)1.Narasimhulu M;Srikanth M R;Chinni K M Lanthanum(III) nitrate hexahydrate orgadolinium(III)chloride hexahydrate catalyzed one-pot synthesis of α-amino nitriles[外文期刊] 2007(1/2)2.Srikanth T R;Narasimhulu M;Suryakiran N A mild and efficient acetylation of alcohols,phenols and amines with acetic anhydride using La(NO3)3@6H2O as a catalyst under solvent-free conditions[外文期刊] 2006(38)3.朱淮武有机分子结构波谱解析 20054.刘艳红;张同来;杨利多硝基多甲基取代苯的核磁共振氢谱及质谱研究[期刊论文]-分析化学 2007(02)5.肖新亮;古风才;赵桂英实用分析化学 20006.徐寿昌有机化学 19837.北京化学试剂公司化学试剂.精细化学品产品目录 19998.A McGookin;S R Swift The nitration of the acet-toluidides[外文期刊] 19399.Norman Rabjohn Org Synth Coll IV 196310.梁毓学;高爽;陈惠麟一种简便分离2-甲基-6-硝基苯胺和2-甲基-4-硝基苯胺的方法[期刊论文]-精细化工2003(01)11.梁诚我国染颜料中间体投资热点分析[期刊论文]-四川化工与腐蚀控制 2003(04)12.梁诚我国染料中间体生产现状与发展趋势 2000(02)13.钱崇濂国外非致癌染料研究进展[期刊论文]-纺织化学品 2005(02)本文链接:/Periodical_hncl200901002.aspx。
苯胺类药物合成

典型药物的合成实例
总结
以上介绍了苯胺类药物合成的基本原理和方法,以及一些典型药物的合成实例。这些药物 在临床和实验室中都有着广泛的应用和研究价值。通过了解这些药物的合成路线和方法, 可以更好地理解其药理作用和化学结构之间的关系,为新药的研发提供参考和启示
-
请各位老师批评指正!
THESIS DEFENSE POWERPOINT
阿司匹林是一种常见的解热镇痛药,可以通过酰化反应合成。以下是阿司匹林的合成步骤
将苯酚与氯化亚砜反应:生成苯甲酰氯 将苯甲酰氯与苯胺反应:生成苯甲酰胺 将苯甲酰胺与乙酸酐反应:生成阿司匹 林
典型药物的合成实例
2. 对乙酰氨基酚(paracetamol)的合成
对乙酰氨基酚是一种常用的解热 镇痛药,可以通过甲基化反应合 成。以下是对乙酰氨基酚的合成 步骤
XXXXXXXXXX
指导老师:X药物的合成实例
4. 盐酸苯丙氨酸(phenylalanine)的合成
苯丙氨酸是一种人体必需的氨基 酸,可以通过苯乙酮的羟基化反 应合成。以下是苯丙氨酸的合成 步骤
将苯乙酮与氢氧化钠反应: 生成苯乙酸钠
将苯乙酸钠与水合肼反应: 生成苯丙氨酸
典型药物的合成实例
5. 盐酸盐酸盐酸盐酸(R)-卡托普利的合成
苯胺类药物合成的基本原理和方法
2. 硝化反应
硝化反应是将硝基化合物引入苯胺分子中的 过程。在适当的条件下,可以使用硝酸或硝 酸盐进行硝化反应,得到硝基苯胺类化合物
苯胺类药物合成的基本原理和方法
3. 磺化反应
苯胺类药物合成的基本原理和方法
磺化反应是将苯胺分子中的氢原 子被磺酸基取代的过程。可以通 过使用硫酸或磺酸酐等试剂来进 行磺化反应,得到磺基苯胺类化 合物
对硝基苯胺生产工艺

对硝基苯胺生产工艺
硝基苯胺(化学式:C6H6N2O2)是一种重要的化工原料,广
泛应用于染料、医药、农药等行业。
下面介绍一种硝基苯胺的生产工艺。
硝基苯胺的生产工艺主要包括苯胺硝化反应、硝基苯胺还原反应和后处理三个步骤。
首先是苯胺硝化反应。
反应原料为苯胺(C6H5NH2)和硝酸(HNO3),反应物质量比为1:1。
将苯胺和硝酸加入硝化反
应釜中,控制反应温度在40-60℃之间,反应时间约4-6小时。
在反应过程中需要不断搅拌,以保证反应均匀。
反应完成后,得到硝基苯胺(C6H5N2NO2)。
然后是硝基苯胺还原反应。
反应原料为硝基苯胺和亚硫酸钠(Na2SO3),反应物质量比为1:1。
将硝基苯胺和亚硫酸钠加入还原反应釜中,控制反应温度在50-70℃之间,反应时间约
2-4小时。
在反应过程中需要不断搅拌,以保证反应均匀。
反
应完成后,得到苯胺和硝基苯胺的混合物。
最后进行后处理。
将反应结束后得到的混合物进行过滤、干燥等处理,得到纯净的硝基苯胺产品。
同时,还需要对反应釜和设备进行清洗,以便下一批次的生产使用。
硝基苯胺的生产工艺需要严格控制反应条件和设备操作,确保反应过程的安全和产品质量。
同时,还需要注意废气的处理,减少对环境的污染。
以上就是一种硝基苯胺的生产工艺,每个步骤都需要严格控制反应条件和操作。
在实际生产中,还需要根据具体情况进行优化和改进,以达到更好的效果。
对硝基苯胺 生产工艺

对硝基苯胺生产工艺
硝基苯胺是一种有机化合物,化学式为C6H6N2O2,主要用
作染料中间体,也可以用于制药、农药等领域。
下面是硝基苯胺的生产工艺的简要介绍。
硝基苯胺的生产工艺可以从苯甲酸出发,经过硝化反应得到硝基苯甲酸,再经过还原反应得到硝基苯胺。
具体工艺步骤如下:
1. 原料准备:准备苯甲酸、浓硝酸、浓硫酸等原料,并按比例配制好硝化混合酸。
2. 硝化反应:将苯甲酸和硝化混合酸加入反应釜中,加热搅拌使反应进行,并控制反应温度和时间,通常反应温度为60-70℃,反应时间为6-8小时。
3. 中间体分离:将反应混合物进行冷却,同时以水作为冷冻剂,使中间体硝基苯甲酸结晶析出。
通过过滤或离心等分离技术,将硝基苯甲酸分离出来。
4. 还原反应:将硝基苯甲酸加入反应釜中,加入还原剂如亚硫酸钠,控制反应温度和时间,进行还原反应,得到硝基苯胺。
5. 精制处理:对得到的硝基苯胺进行进一步的精制处理,如洗涤、蒸馏、结晶等,以提高产品的纯度和质量。
6. 产品包装:对精制后的硝基苯胺进行包装,通常采用塑料桶、铁桶等包装形式,以便储存和运输。
需要注意的是,在整个生产工艺中,应严格控制反应条件,尤其是温度和时间,以避免发生副反应和产生不良的化学物质。
以上是对硝基苯胺生产工艺的简要介绍,具体的工艺条件和操作方法还需要根据实际情况进行调整和优化,以确保产品的质量和安全性。
2,6二甲基硝基苯的生产工艺过程

2,6二甲基硝基苯的生产工艺过程向50ml圆底烧瓶中加入4.2g(0.04mol)间二甲苯,搅拌下加入39.2g(0.40mol)98%浓硫酸及少量硫酸汞,加热,控制温度在100—105℃,搅拌1.5小时后冷至室温,得浅红色糊状物。
然后将产物在冰水浴上冷却,充分搅拌下将6g浓硫酸(98%)及3g发烟硝酸(99%)的混合物滴入圆底烧瓶中,滴加完毕,控制温度在30—35℃,继续搅拌20min,得白色糊状物,将其小心移入100ml圆底烧瓶中,冷却下加入50ml水稀释,调ph=4后水蒸气蒸馏至无油状液滴流出。
收集液由分液漏斗分出,水相用乙醚萃取2次,合并有机相,水洗1次,以碳酸氢钠调至中性,再水洗1次,经氯化钙干燥后,减压蒸馏,收集224—225℃(99.2Kpa)馏分,得淡黄色油状物4.7g,即为产品,收率78%。
另一种工艺流程:将间二甲苯投入硝化釜中,冷却至0—5℃,分批加入冷却后的混酸(56.5%硫酸、28%硝酸、15.5%水),第一次保持温度在15—17℃,在3小时内加完;第二次保持温度在17—25℃,在2小时内加完;最后滴加温度为25—30℃,在1小时内完成。
在25—30℃搅拌30min,将上层硝化物分出,用水洗至刚果红试纸显酸性为止,然后减压蒸馏得粗品,再进行蒸馏,收集78—85℃(667Pa)馏分,冷冻结晶,过滤即得2,6二甲基硝基苯,同时副产2,4二甲基硝基苯。
间二甲苯被硝化后,不仅生成2,4和2,6二甲基硝基苯,而且还生成少量的2,5二甲基硝基苯以及二硝基化合物;另外,体系内还有部分未被硝化的间二甲苯和水洗时残存的水分,组分十分复杂。
2,4和2,6二甲基硝基苯的沸点较高,二者的沸点差也较小,这就决定了如采用精馏过程只能在真空条件下进行,并应选择效率高、阻力小的高效填料作为传质元件。
西北大学化工系选用上海化工研究院开发的SW型网孔波纹填料,在直径200mm的填料塔中进行了工业规模的精馏实验。
19种苯胺类化合物

19种苯胺类化合物苯胺类化合物是一类含有苯胺基的有机化合物,它们具有各种不同的结构和性质。
以下是一些常见的苯胺类化合物:1. 苯胺(Aniline),最简单的苯胺类化合物,是一种无色至黄色液体,常用于染料和橡胶生产。
2. 二甲苯胺(Dimethylaniline),含有两个甲基基团的苯胺衍生物,常用作有机合成中间体。
3. 三甲苯胺(Trimethylaniline),含有三个甲基基团的苯胺衍生物,具有多种工业用途,如染料和颜料的生产。
4. 甲基苯胺(Methylaniline),含有一个甲基基团的苯胺衍生物,常用作染料和农药的合成原料。
5. 乙基苯胺(Ethylaniline),含有一个乙基基团的苯胺衍生物,常用于有机合成和染料工业。
6. 正丙基苯胺(n-Propylaniline),含有一个正丙基基团的苯胺衍生物,在染料和颜料工业中有应用。
7. 异丙基苯胺(Isopropylaniline),含有一个异丙基基团的苯胺衍生物,常用于染料和橡胶生产。
8. 正丁基苯胺(n-Butylaniline),含有一个正丁基基团的苯胺衍生物,在有机合成和染料工业中有一定用途。
9. 异丁基苯胺(Isobutylaniline),含有一个异丁基基团的苯胺衍生物,具有一定的工业应用价值。
10. 氯苯胺(Chloroaniline),苯胺的氯取代衍生物,常见的有邻氯苯胺、间氯苯胺和对氯苯胺。
11. 溴苯胺(Bromoaniline),苯胺的溴取代衍生物,常见的有邻溴苯胺、间溴苯胺和对溴苯胺。
12. 硝基苯胺(Nitroaniline),苯胺的硝基取代衍生物,常见的有邻硝基苯胺、间硝基苯胺和对硝基苯胺。
13. 甲基氨基苯(Methoxyaniline),苯胺的甲氧基取代衍生物,常见的有邻甲氧基苯胺、间甲氧基苯胺和对甲氧基苯胺。
14. 乙基氨基苯(Ethoxyaniline),苯胺的乙氧基取代衍生物,在染料和颜料工业中有应用。
2-甲基-4-硝基苯胺的制备方法

2-甲基-4-硝基苯胺的制备方法
2-甲基-4-硝基苯胺是一种有机化合物,可以通过多种方法制备。
以下是其中一种制备方法:
1. 制备甲基苯胺的方法
首先,将苯胺溶解在稀硫酸中,加入过量的甲醛(甲醛的浓
度为30-40%),并在冰浴中搅拌。
然后缓慢地滴加稀硫酸的
硝化混合液(由浓硫酸和浓硝酸配制而成)至反应溶液中,并继续搅拌。
反应完成后,将反应溶液转移至冷冻条件下,过滤并用冷水洗涤产物。
最后,将产物重新结晶并干燥,得到甲基苯胺。
2. 制备2-甲基-4-硝基苯胺的方法
将甲基苯胺溶解在硫酸中,并加热至80-90℃。
然后,在搅
拌下缓慢滴加稀硝酸。
反应完成后,冷却溶液并在冷冻条件下結晶生成的产物。
最后,过滤产物并用冷水洗涤,然后干燥,得到2-甲基-4-硝基苯胺。
需要注意的是,以上制备方法只是其中一种方法,实际上还有其他不同的方法可以制备2-甲基-4-硝基苯胺。
在实验中,为
了保证反应的安全性和成功率,需要严格控制反应条件和反应物的用量。
MEA2-甲基-6-乙基苯胺MSDS

河南颖泰化工有限责任公司2-甲基-6-乙基苯胺化学品安全技术说明书(MSDS)第一部分化学品及企业标识化学品中文名称:2-甲基-6-乙基苯胺化学品俗名或商品名:MEA化学品英文名:2—Methyl—6—ethylaniline企业名称:河南颖泰化工有限责任公司地址:濮阳市高新区胜利西路与濮水路交汇处邮编:457000企业传真号码:+86-(0)393-8910756企业应急电话:+86-(0)393-8913073电子邮件地址:hnythgahb@技术说明书编码:MCS-20061010-01生效日期:2006年10月10日国家应急电话:+86-(0)532-83889090第二部分成分/组成信息纯品□混合物□化学品名称:2-甲基-6-乙基苯胺有害物成分浓度 CAS No.2-甲基-6-乙基苯胺99.0-99.5% 24549-06-2第三部分危险性概述危险性类别:不属于危险品。
不属于放射性危险品。
不属于腐蚀品。
无氧化剂危险性。
侵入途径:吸入、食入、经皮吸收。
健康危害:吞下可导致中毒,皮肤接触可导致中毒。
吸入蒸汽对身体有害。
安全建议:不要与眼、皮肤接触,不要吸入该物质蒸汽。
环境危害:对海洋生物有害及长时间持续影响。
燃爆危险:本品可燃。
无爆炸危险性。
预防:远离火源,不准吸烟。
在室外和空气流通的地方使用。
避免在郊外排放。
戴防护手套、防护眼镜、防护服。
第四部分急救措施皮肤接触:立即脱去污染的衣着,用肥皂水和大量的流动清水冲洗至少15分钟。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
第五部分消防措施危险特性:遇明火、高热可燃。
受高热分解放出有毒的一氧化碳、二氧化碳有害燃烧产物:一氧化碳、二氧化碳、氧化氮。
灭火方法及灭火剂:消防人员须佩戴防毒面具、穿全身消防服,在上风向灭火。
n甲基苯胺生产工艺

n甲基苯胺生产工艺
n甲基苯胺生产工艺
n甲基苯胺生产工艺
n甲基苯胺是重要的有机合成原料之一,广泛用于染料、医药、橡胶、柔性聚氨酯泡沫等领域。
其生产工艺主要分为两种:氢气还原法和热氨法。
氢气还原法是目前主流的生产工艺,其主要原料为硝基苯和氢气,在催化剂的作用下,硝基苯被还原成n甲基苯胺。
而热氨法则是将亚硝酸钠和氨气在高温下反应生成n甲基苯胺。
两种工艺各有优缺点,选择何种工艺应根据生产需求和经济效益综合考虑。
- 1 -。
有机胺
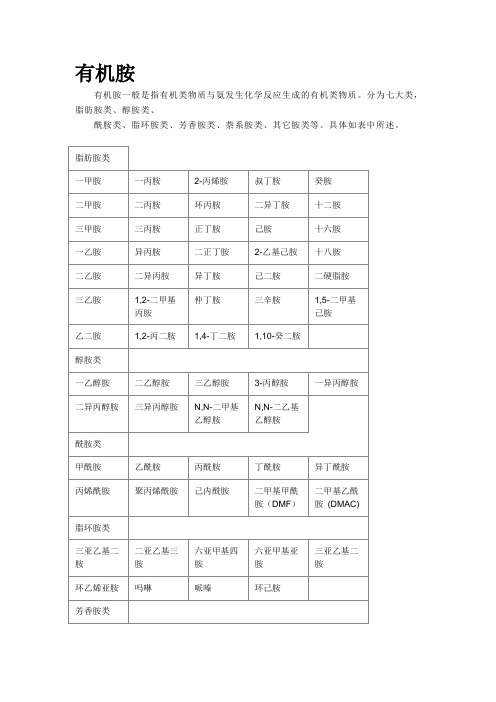
有机胺有机胺一般是指有机类物质与氨发生化学反应生成的有机类物质。
分为七大类,脂肪胺类、醇胺类、酰胺类、脂环胺类、芳香胺类、萘系胺类、其它胺类等。
具体如表中所述。
聚乙烯亚胺羟胺絮凝剂理论基础是;“聚并”理论,絮凝剂主要是带有正电(负)性的基团中和一些水中带有负(正)电性难于分离的一些粒子或者叫颗粒,降低其电势,使其处于不稳定状态,并利用其聚合性质使得这些颗粒,集中,并通过物理或者化学方法分离出来。
一般为达到这种目的而使用的药剂,称之为絮凝剂。
絮凝剂主要应用于给水各污水处理领域。
絮凝剂按照其化学成分总体可分为无机絮凝剂和有机絮凝剂两类。
其中无机絮凝剂又包括无机凝聚剂和无机高分子絮凝剂;有机絮凝剂又包括合成有机高分子絮凝剂、天然有机高分子絮凝剂和微生物絮凝剂。
[编辑本段]无机絮凝剂按其分子量的大小可分为低分子絮凝剂和高分子絮凝剂两大类。
低分子絮凝剂价格低、货源充足、但因其用量大、残渣多、效果差,故无机絮凝剂的发展已经基本上完成了低分子向高分子的转变。
现常用的无机高分子絮凝剂有聚合铝类絮凝剂、聚合铁类絮凝剂和活性硅酸类絮凝剂以及复合絮凝剂四大类。
(1)聚合铝类絮凝剂(如聚合氯化铝,硫酸铝等)聚合铝水解产生高价离子,形成各种类型的羟基多核络合物。
它们通过羰基式桥联作用,处于亚稳定状态。
而OH-与Al3+的比值[2](一般称盐基度或碱基度)对絮凝效果影响很大。
通常盐基度越高,絮凝效果越强,但过高则本身易生成难溶的氢氧化铝沉淀,导致絮凝效果降低。
研究表明,盐基度在75%-85%时最佳,此时絮凝体产生快,颗粒大而重,沉淀性能好。
聚合铝具有投药量少、沉降速度快、颗粒密实、除浊、除色效果明显等特点。
在工业水处理中得到广泛的应用[3]。
值得注意的是铝,尤其是活性铝,毒性较大,同时聚合铝制备方法不完善,致使较多水解铝的微细颗粒存在于溶液中,这在一定程度上限制了聚合铝的使用。
通过改善混凝反应条件,延长慢速混凝时间,能有效降低水中铝的含量。
硝基化合物的合成

N
N O 2
3.3 胺和肟的氧化反应示例
胺的氧化,特别是肟的氧化,是合成脂肪族硝基化合物的一个重要手段。因为肟 可以方便地由醛酮和羟胺制得。这是由醛酮合成硝基化合物的有效的方法,常用 的氧化剂有过酸、臭氧、Oxone,高锰酸钾,高硼酸钠,次氯酸。
HO N Ph
CF3CO3H
NO2 Ph
17
3.4 烯烃硝化反应示例
sieves,graphite
• 硝酸盐 Nitrate salts
AgNO3/BF3,
KNO3/H2SO4,K(Na)NO3/TMSCl/AlCl3,Cu(NO3)2/(CH3CO)2O,
NH4NO3/(CF3CO)2O, (NH4)2Ce(NO3)
• 硝酸酯 Nitrate esters
BuONO2/Nafion-H, MeONO2/BF3, Me3SiONO2, acetone
Br
Br
KNO3/H2SO4
O
O2N
O
OO
OO
2.4 HNO3/Ac2O 作为硝化试剂反应示例
硝酸和醋酐混和,生成醋酸和硝酸的混酐(CH3COONO2),是一个良 好的硝化试剂,反应条件比较温和。
C H OH N O 3
C H O
A c 2 O
N O 2
8
2.5 硝酸或硝酸铵/三氟乙酸酐作为硝化试剂反应示
硝酸和三氟乙酸酐也是一个类似的硝化试剂,硝酸也可用硝酸铵代替。
H N O 3 OC H O(C F 3 C O )2 O O 2 NOC H O
2.6 2,3,5,6-四溴-4-甲基-4-硝基-环己-2,5-二烯酮为硝化试剂反应示例
一般情况下,在芳环上有游离的氨基存在时,由于许多硝化试剂具有较强的 氧化性使得在硝化的同时,氨基也会被氧化成一系列复杂的副产物,有文献 报道2,3,5,6-四溴-4-甲基-4-硝基-环己-2,5-二烯酮是一种基本上没有氧 化性的温和的硝化试剂,可用于带有游离氨基的芳香化合物的硝化。其制备
甲磺酸伊马替尼合成路线工艺

合成路线一:以 4-甲基—3—硝基苯胺为起始原料,经过缩合、还原、环合等反应制得抗肿瘤药物甲磺酸伊马替尼。
并分别讨论了采用无水碳酸钾代替二异丙基乙胺、水合肼和普通催化剂代替铂炭催化剂以及采用异戊醇作为溶剂的优点. 最终反应总收率超过 50%,用高效液相色谱分析产品纯度在 99.5%以上。
合成路线二:用 3—乙酰吡啶 (2) 和 N,N—二甲基甲酰胺二甲缩醛 (3) 反应得 3—二甲胺基 -1-(3- 吡啶基 )-2—丙烯 -1- 酮 (4),4 与2—甲基 -5—硝基苯基胍硝酸盐 (6) 经成环、还原、由 4- 氯甲基苯甲酰氯酰化后与 N- 甲基哌嗪反应,所得伊马替尼再成盐即得甲磺酸伊马替尼,总收率约 58%。
合成路线:为研究和改进甲磺酸伊马替尼的合成工艺,以2-甲基-5-硝基苯胺为原料,先后经历加成、环合、还原、酰化等反应制备甲磺酸伊马替尼,并对其中的加成、环合、还原、酰化等反应与工艺过程进行了改进。
采用经改进的工艺制备甲磺酸伊马替尼,反应总收率为41.9%,产品纯度可达99.75%(高效液相色谱法).合成路线三:以 3-乙酰吡啶、 2-甲基-5-硝基苯胺等为原料, 经缩合、成环、氢化、酰化, 进而与甲磺酸成盐得到甲磺酸伊马替尼。
结果中间体及目标化合物经质谱、核磁共振氢谱、红外光谱等确证, 总收率 27.0%。
本路线操作简单,成本较低, 适合工业化生产。
合成路线四:改进甲磺酸伊马替尼的合成工艺。
方法以 4-[( 4-甲基哌嗪—1-基)甲基]苯甲酰氯二盐酸盐与 4-甲基—N3 -[4—( 3-吡啶基)嘧啶-2-基]-1,3 苯二胺为起始原料,进行水相缩合反应得到伊马替尼游离碱,再与甲磺酸成盐,两步反应合成新型酪氨酸酶抑制剂类抗肿瘤药物伊马替尼。
结果优化后的工艺成本低廉、后处理简便、产品纯度高、收率高,并且对环境污染小.纯度可达 99.7% ,且单一杂质< 0。
1%。
结论新工艺的总收率达 81。
5% ,可工业化生产,前景广阔.方法五:以3—硝基苯基甲基胍和3—二甲氨基— 1—( 3—吡啶基)—2—丙烯1-酮为起始原料,经关环、还原、缩合得到伊马替尼( 图1) 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ab s t r a c t :Us i n g o - n i t r o a n i l i n e a s r a w ma t e r i a l ,t h r o u g h a c e yl t a t i o n ,me t h y l a t i o n ,h y d r o l y s i s r e a c t i o n s ,t h e
2 . 甲基 一 6 一 硝基 苯胺 是 重要 的染料 中间体 和化 工 中 间体 ,主要用于有机 合成 ,是油漆 、制药 、印染 等 重要 的原材料 ,也 是混合炸 药 的重 要成分 之一【 1 J 。 国 内外 曾有 2 . 甲基 . 6 一 硝 基苯 胺合 成方 法 的报 道 , 祁 磊等 人采 用邻 甲基苯 胺 为原料 ,改进 乙酰 化和 硝化 反应 合成 2 . 甲基一 6 . 硝 基 苯胺 ,产 率 仅为 5 9 . 4 %,纯
Ke y wo r d s : 0 一 n i t r o a n i l i n e ; a c e t y l a t i o n ; me hy t l a t i o n ; h y d r o l y s i s ; 2 - me t h y 1 . 6 . n i t r o a n i l i n e
第3 5 卷第 1 期
2 0 1 4年 1 月
V o 1 . 3 5 No . 1
J a n .2 0 1 4
井 冈山大学 学报 ( 自然科 学版 )
J o u na r l o f J i n g g a n g s h a n U n i v e r s i t y( Na t u r a l S c i e n c e ) 3 3
S YNTHES i S AND CHARACTERI ZATI oN oF 2 . M ETHYL. 6 — NI TRoANI LI NE
ZHOU S h i . y a n g , CHE N L i n g
( 1 . C h o n g Qi n g Mu Ge F o o d C o . , L t d . C h o n g q i n g , 4 0 1 5 2 0 C h i n a : 2 . Y u C a i C o l l e g e , S o u t h w e s t Un i v e r s i t y , C h o n g q i n g , 4 0 1 5 2 4 , C h i n a )
文章编号 :1 6 7 4 - 8 0 8 5 ( 2 0 1 4 ) 0 1 — 0 0 3 3 — 0 6
2 一 甲基一 6 一 硝基 苯胺 的合成及表征
周石洋 ,陈 玲2
( 1 . 重庆牧哥食 品有限公司,重庆 4 0 1 5 2 0 ;2 . 西南大学育才学院,重庆 4 0 1 5 2 4 )
摘
要 :以邻硝基苯胺为原料,经 乙酰化 、甲基 化、水解三步反应合成得到 了 目标产物 2 . 甲基. 6 . 硝基 苯胺 ,并采
用I R、 H NMR和 ” C NMR对产物结构进行 了表征 。探讨 了乙酰化反应时催化剂 A 1 C I 用 量 、反应温度 、反应时
间和 乙酸酐 的滴加速率对邻硝基 乙酰苯胺 产率的影响, 以及 甲基化反应中催化剂 A1 C 1 用量、反应温度、反应时
t a r g e t c o mp o u n d 2 - me t h y l 一 6 - n i t r o a n i l i n e wa s s y n t h e s i z e d a n d c h a r a c t e r i z e d b V I R, H N M R n d ”C a NM R. Bo h t i n t h e a c e t y l a t i o n a n d me t h y l a t i o n r e a c t i o n , t h e i n l f u e n c e o f d o s a g e o f c a t a l y s t A1 C 1 3 , r e a c t i o n t e mp e r a t u r e , r e a c t i o n t i me . a n d a d d i n g r a t e o f a c e t i c a n h y d r i d e i n t h e f o பைடு நூலகம் me r nd a a d d i n g r a t e o f d i me t h y l s u l f a t e i n t h e 1 a t t e r we r e i n x  ̄ e s t i g a t e d . Un d e r he t o p t i ma l c o n d i t i o n s . t h e y i e l d o f 2 - me hy t l 一 6 . n i t r o a n i l i n e wa s 9 3 . 9 %.
间和硫酸 二甲酯 的滴加速 率对产物产率的影响 。在最佳合成条件下 ,2 . 甲基 . 6 . 硝基苯胺 的产率可达 9 3 . 9 %。
关键词 :邻硝基苯胺 ;乙酰 化; 甲基化;水解 ;2 . 甲基. 6 一 硝基苯胺
中图分类号 :06 2 5 . 6 3 文献标识码 :A DO I : 1 0 . 3 9 6 9  ̄ . i s s n . 1 6 7 4 — 8 0 8 5 . 2 0 1 4 . 0 1 . 0 0 7
