铬超标自查报告
某电镀铬厂作业危害调查

某电镀铬厂作业危害调查某电镀铬厂作业危害调查铬酐、铬酸、铬酸盐及重铬酸盐等六价铬化合物引起的鼻部损害称为铬鼻病。
从事镀铬作业的电镀厂工人长期接触到铬酸雾,容易发生职业性铬鼻病。
为了解某电镀厂工作场所存在的职业病危害情况,制定有关的预防对策,我们于2021年7月对该厂进行了职业卫生调查,并对作业工人进行了职业健康检查。
对象与方法1.1对象以电镀厂生产车间为调查对象,对车间空气铬酸浓度进行测定。
调查组为23名铬作业工人,男14名,女9名,平均年龄34.9岁(21~48岁),平均工龄3.3a(0.5~14a);对照组为某卷烟厂机修岗位不接触毒物人员25名,男15名、女10名,平均年龄35.8岁(20~44岁),平均工龄3.9a(0.5~13a)。
两组人员个人嗜好、生活.惯相近。
1.2方法1.2.1车间空气铬酸雾浓度测定以江苏建湖兴宇分析仪器厂生产的DCY-2A型双气路大气采样仪为动力采集样本,用冲击式采样瓶(双串联)装5ml蒸馏水为吸收液,流量3L/min,采样时间20min,采用二苯碳酰二肼比色法分析。
1.2.2作业工人职业健康检查询问职业史、病史和自觉症状,进行内科、外科、五官科检查及血液、尿液分析。
1.3执行标准GBZ1-2021工业企业设计卫生标准、GBZ2-2021工作场所有害因素职业接触限值、GBZ12-2021职业性铬鼻病诊断标准。
结果与分析2.1一般情况该厂系一家私有企业,年产值150万元左右。
位于山脚下,占地面积4.5亩,生产区与生活区无截然分开。
生产均为来料电镀,日耗铬酸酐约100kg,生产方式以手工操作为主,车间有通风排毒设施但效果不好,采用24h连续工作两班次运转。
2.2车间空气铬酸雾浓度测定结果分析根据生产特点测定铬酸雾浓度,选择有代表性的劳动者接毒地点作为测定点。
本次调查共测定铬作业点14个,采集样本数84个。
经分析,浓度范围为0~2.332mg/m3,合格点数5个,测定点合格率为35.7%,说明车间内铬污染十分严重。
自查报告胶囊铬超标2次汇报

杭州市萧山区食品药品监督管理局:鉴于市局通知,国家局和省局最新要求,立即暂停了销售媒体曝光的九家药品生产企业生产的所有胶囊剂型产品,公司总经理高度重视立即会与业务科质管科一起组织了自查,与库存展开了核对工作、现将具体自查情况向贵局汇报:经核查本公司购进了媒体曝光的五家药品生产企业生产的胶囊剂型。
现将具体情况统计如下:1、丹东市通远药业;人工牛黄甲硝唑胶囊,20s,现有库存的进销存情况;自2011年12月起从小道医药购进150盒,销售58盒,现封存92盒。
2、通化金马药业;清热通淋胶囊;0.37g*40s。
现有库存的进销存情况;自2011年08月起从小道医药购进45盒,销售10盒,现封存42盒。
通化金马药业;壮骨伸筋胶囊;0.3g*60s。
现有库存的进销存情况;自2011年12月起从小道医药购进33盒,销售7盒,现封存26盒。
3、四川蜀中制药;氨咖黄敏胶囊;10S。
现有库存的进销存情况;自2011年11月起从小道医药购进2300板,销售927板,现封存1373板。
氨咖黄敏胶囊;10S*50板。
现有库存的进销存情况;自2012年02月起从小道医药购进300板,销售134板,现封存166板。
阿莫西林胶囊;0.25g*20s。
现有库存的进销存情况;自2011年10月起从小道医药购进200盒,销售63盒,现封存137盒。
阿奇霉素胶囊; 0.25g*6s。
自2011年12月起从小道医药购进265盒,销售67盒,现封存189盒。
胃康灵胶囊;0.4g*24s。
现有库存的进销存情况;自2011年12月起从小道医药购进22盒,销售9盒,现封存13盒。
诺氟沙星胶囊; 0.1g*12s。
现有库存的进销存情况;自2012年02月起从小道医药购进200板,销售115板,现封存85板。
4、长春海外制药;安神胶囊;60s。
现有库存的进销存情况;自2011年04月起从小道医药购进48盒,销售19盒,现封存29盒。
布诺芬缓释胶囊;0.3g*20s。
xx县食品药品监督管理局铬超标胶囊查处情况汇报

xx县食品药品监督管理局铬超标胶囊查处情况汇报第一篇:xx县食品药品监督管理局铬超标胶囊查处情况汇报xx县食品药品监督管理局查处铬超标空心胶囊及胶囊剂药品查处工作汇报铬含量超标胶囊事件经媒体曝光后,引起公众广泛关注。
为确保公众用药安全,xx县局按照省、市局统一部署,迅速开展严查问题胶囊行动,确保了铬超标空心胶囊及胶囊剂药品在辖区内流通和使用。
现将查处情况报告如下。
一、高度重视,组织领导到位。
根据国家、省、市局部署要求,16日上午,我局紧急召开班子会议,成立由局长为组长的“铬超标胶囊排查工作领导小组”,制定排查工作实施方案,部署相关排查工作。
建立局长为第一责任人,主管副局长为直接责任人,相关股室负责人为具体责任人的责任机制,确保了上级精神与本地实际紧密结合,确保了查处工作有人管、有人抓,有人具体落实。
二、周密部署,企业自查到位。
在第一时间制定下发了《xx县食品药品监督管理局关于进一步加强胶囊剂药品监管的通知》【x食药监(2012)19号】等相关文件5件。
要求全县药品生产、经营、使用单位对国家局通报的铬含量超标产品进行全面自查,全县各涉药单位共上报自查报告300余份。
同时,利用药品电子监管网、手机短信、电话等方式向全县各涉药单位发出紧急公告和通知,及时通报铬超标空心胶囊及胶囊剂药品检测检验情况。
三、迅速行动,监督检查到位。
针对我县市场上可能出现的国家局通报的铬超标胶囊问题药品,我局按照省、市局的统一要求和部署,从4月16日开始,有计划,分步骤,对辖区内药品经营企业和医疗机构进行了拉网式排查。
对县人民医院制剂室、县哮喘医院制剂室及县风湿骨病专科医院使用空心胶囊及其制剂情况进行检查,现场对两家制剂室一家专科医院使用的空心胶囊及制剂进行了封存,并要求将所用药用空心胶囊及制剂逐批次、逐品种送北京普尼科技检测有限公司进行了检验,检验结果全部为合格。
利用我局药品电子监管网实时对辖区内药品零售企业进行监控,发现某药店有销售名单中标示青海省格拉丹东药业有限公司生产,批号1110208的“愈伤灵胶囊”5盒,执法人员当场对该药品供货单位资质及合法票据进行了查验提取,并对上述药品进行了封存,妥善保管、等待进一步处理。
桥亭乡卫生院关于对铬超标药用胶囊和胶囊剂自查情况汇报

桥亭乡卫生院关于对铬超标药用胶囊和胶囊剂自查情况汇报根据《卫生部办公厅关于立即暂停使用媒体曝光的13个铬超标产品的通知》(卫发明电〔2012〕6号)和《关于配合召回和暂停使用部分药品生产企业胶囊剂药品的通知》(卫发明电〔2012〕7号)及自治区卫生厅《关于做好暂停使用部分生产企业铬超标胶囊剂药品工作的通知》(桂卫明电〔2012〕4号)等文件精神,为确保我乡医疗安全,确保公众用药安全,维护患者权益。
我院按照上级统一部署,迅速采取“三到位”措施严查问题胶囊,确保了我院及辖区内村卫生室等经营使用单位及时下架封存问题胶囊药品,暂停销售和使用国家局通报的9家生产企业的所有胶囊剂药品。
现将自查情况汇报如下:一、领导重视,组织到位我院接到县卫生局局关于开展铬超标胶囊剂药品自查的紧急通知后,第一时间紧急召开了由领导班子及各科组长等人员参加的自查工作会议,传达学习了上级关于开展铬超标药用胶囊和胶囊剂查处等相关通知精神,成立了以院长任组长,副院长任副组长,各科组长为成员的铬超标药用胶囊和胶囊剂自查工作领导小组,明确了任务,落实了责任。
二、通知及时,自查到位1、在第一时间迅速向全乡村卫生室、个体诊所转发了卫生局《关于配合召回和暂停使用部分药品生产企业胶囊剂药品的通知》(平卫字〔2012〕55号)文件精神,要求各村卫生室对国家局通报的9家企业、17个品种共计26个批次铬含量超标产品进行自查,如发现有上述26个批次铬含量超标产品必须全面清理,立即下架封存,并及时上报乡卫生院,待国家局和相关检验机构检验合格并公布后方可恢复销售和使用。
2、我院在监督村卫生室、个体诊所自查的同时,组织医务人员在本院对国家局通报的9家企业、17个品种共计26个批次铬含量超标产品进行彻底清查。
3、经过自查汇总,我院及全乡村卫生室、个体诊所均无国家局通报的9家企业、17个品种共计26个批次铬含量超标产品。
三、迅速行动,督查到位我院按照上级的要求和部署,对辖区内村卫生室进行了排查,截止5月7日,共出动22人次,车辆11台次,检查桥亭乡辖区8个行政村11家村卫生室1家个体诊所的所有药品进行了全面清查,检查未发现有国家局通报的9家企业、17个品种共计26个批次铬含量超标产品。
XXX药店铬超标胶囊自查表
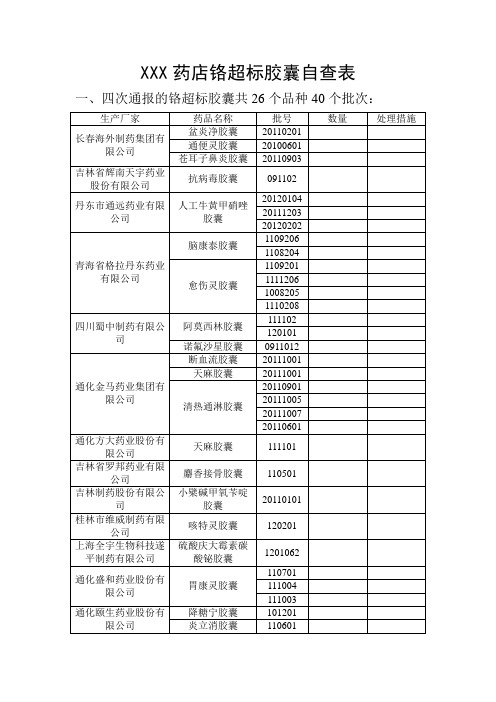
XXX药店铬超标胶囊自查表一、四次通报的铬超标胶囊共26个品种40个批次:生产厂家药品名称批号数量处理措施长春海外制药集团有限公司盆炎净胶囊20110201 通便灵胶囊20100601 苍耳子鼻炎胶囊20110903吉林省辉南天宇药业股份有限公司抗病毒胶囊091102丹东市通远药业有限公司人工牛黄甲硝唑胶囊201201042011120320120202青海省格拉丹东药业有限公司脑康泰胶囊11092061108204 愈伤灵胶囊1109201111120610082051110208四川蜀中制药有限公司阿莫西林胶囊111102120101 诺氟沙星胶囊0911012通化金马药业集团有限公司断血流胶囊20111001 天麻胶囊20111001清热通淋胶囊20110901201110052011100720110601通化方大药业股份有限公司天麻胶囊111101 吉林省罗邦药业有限公司麝香接骨胶囊110501吉林制药股份有限公司小檗碱甲氧苄啶胶囊20110101桂林市维威制药有限公司咳特灵胶囊120201上海全宇生物科技遂平制药有限公司硫酸庆大霉素碳酸铋胶囊1201062通化盛和药业股份有限公司胃康灵胶囊110701111004111003通化颐生药业股份有限公司降糖宁胶囊101201 炎立消胶囊110601110302 通化金恺威药业有限公司麝香接骨胶囊110601修正药业集团股份有限公司芬布芬胶囊100906 酚咖麻敏胶囊111010110114 羚羊感冒胶囊100901上海皇象铁力蓝天制药有限公司胃康灵胶囊20120102安徽仁和药业有限公司盐酸克林霉素胶囊120201二、上述17家药品生产企业生产的其他口服胶囊品种情况:产地药品名称批号数量处理措施(公章)年月日。
三圣乡药品流通环节铬超标有关产品查处工作小结

三圣乡食品药品监督协管站药品流通环节铬超标有关产品查处工作小结根据国家食品药品监督管理局《关于进一步做好铬超标药用胶囊查处工作的通知(特急)》(国食药监电〔2012〕8号)和湖南省食品药品监督管理局《关于进一步做好药品流通环节铬超标有关产品查处工作的通知》(湘食药监明电〔2012〕18号)以及《石门县食品药品监督管理局关于做好药品流通环节铬超标有关产品查处工作的通知》石食药监函〔2012〕2号精神,根据相关精神我乡食品药品监督协管站,迅速落实辖区药品流通环节铬超标有关产品查处工作任务,现就本次查处工作情况小结如下: 4月26日,我乡食品药品监督协管站组织公卫办全体人员对辖区卫生院、分院、村卫生室、药品零售企业,通报的9家药品生产企业生产的铬超标药用空心胶囊产品,开展突击检查处理工作。
为了将工作落到实处成立了由公卫办副主任李绍玉任组长,刘林任副组长,公卫办其他人员为成员的铬超标胶囊药品查处行动工作领导小组,同时落实了工作任务和要求,一是要求各涉药单位高度重视,迅速行动,认真自查,切实确保群众用药安全;二是要求各涉药单位立即暂停销售和使用涉及的批次药品;三是要求统计各涉药单位涉及批次药品的购销、库存和使用情况,上报食品药品监督管理局;四是要求各涉药单位要进一步完善质量管理制度,认真把好质量验收关,严禁从非法渠道购买明胶空心胶囊。
五是按照职责负责辖区内相关产品的核查,对违反规定销售使用药用空心胶囊的单位,将依法上报县药监局严肃查处。
查处行动共分为3个工作小组,出动车辆3台次,开展为期两天的专项检查活动,此项查处行动被查单位共39家,其中村卫生室29家,零售药店7家,卫生院分院3家,共有16个单位存在着数量不等的相关产品。
查出涉嫌药品品种有15个,总数量9518粒。
其中布洛芬胶囊0.3克1510粒、阿莫西林胶囊0.5克1270粒、0.25克2648粒、胃康灵胶囊0.4克1008粒、斯达舒胶囊16粒装480粒、复方氨酚烷胺胶囊0.25克528粒、抗病毒胶囊0.3克360粒、阿奇霉素胶囊0.25克478粒、抗菌消炎胶囊0.52克352粒、头孢氨苄甲氧苄啶胶囊0.125克216粒、布洛芬缓释胶囊0.3克36粒、安神胶囊0.25克60粒、法莫替丁胶囊20毫克24粒、六味地黄胶囊0.3克144粒、头孢克肟胶囊0.1克32粒。
2023处方点评自查报告

2023处方点评自查报告2023处方点评自查报告1县食品药品监督管理局:根据0000〔〕21号文件《关于印发全县药品生产流通领域集中整治行动工作方案的通知》精神,我0立足实际,突出重点,对本0药品安全管理工作进行全面自查自纠,现将自查情况汇报如下:一、加强领导,严格落实药品安全责任。
3月10日,卫生院成立了由院长、副院长、科主任、药房人员等组成的卫生院药品安全集中整治工作领导小组,由领导小组实行统筹用药安全专项整治工作,组织开展了药品安全形势分析,及时消除了本院的药品安全隐患。
二、广泛宣传,着力营造良好的安全用药环境。
3月15日我院组织开展药品安全知识讲座,加强合理用药和基本药物知识的宣传教育,使本院职工牢固树立用药安全意识,规范医疗行为,提高用药水平,确保用药安全。
三、高度重视,积极开展药品安全自查活动。
3月25日我院组织对中西药房所有库存药品进行逐一清查,清查项目包括药品生产企业、批准文号、有效期、外观质量等,清查未发现以食品、消毒产品、保健食品、冒充药品使用的情况,未发现过期失效、霉烂变质及国家食品药品监督管理局公布的铬含量超标药品。
四、规范进药,优先使用基本药物。
本院使用的基本药物采购一律通过00省医药集中采购平台网上报送采购计划,由省基本药物配送招标企业进行统一配送,所有药品一律进行零差率销售。
五、严格把关,切实加强药品质量管理。
购进的药品严格按照规定逐一验收,并建立了真实,完整的'药品购进验收记录,做到每个批次、每个品种质量验收合格登记入库,指定专人每天登记中西药房及库房室内温湿度,做好药品的在库养护工作,药品储存按要求分类陈列和存放。
药品在出库调剂发放时杜绝霉烂破损、风化变色、过期失效等质量问题,把药品质量责任落实到每个岗位责任人。
六、提高认识,严格落实各项规章制度。
根据《处方管理办法》和《抗菌药物临床应用指导原则》,我院积极落实处方点评制度,由专人定期对卫生院处方质量进行点评分析,并将处方点评结果通过公示栏刊登。
药品管理自查报告(15篇)

药品管理自查报告(15篇)药品管理自查报告1根据《医疗机构药品监督管理办法(试行)》及上级有关规定,我院于12月28日组织相关人员,对本院的药品质量管理情况进行了年度自查,现将自查情况汇报如下:一、制定并完善了《药品首次购进企业和品种合法资质审核制度》、《药品购进和验收管理制度》、《特殊管理药品管理制度》等17项管理制度。
二、为了强化从源头防止假劣药品流入医院,严把药品购进关,从正规渠道购进药品,确保人民用药安全有效。
三、认真做好药品的`验收、入库、日常养护和药品的效期管理。
出入库记录、养护记录及温湿度、冰箱温度登记规范。
四、特殊管理药品做到专人专柜管理,有专用帐册、专用处方、专册登记,做好逐日消耗记录。
并配备人员24小时值班,防止失窃。
五、做好处方点评工作,规范中药饮片和抗菌药物管理。
六、认真做好药品不良反应事件监测报告工作。
七、接受药品监督管理部门的监督检查及整改落实情况:本年度药品监督管理部门监督检查中发现有:温湿度计送质量监督检测部门进行校准;药品待验区、合格区、不合格区和退货区设置不合理等情况,现已经全部整改到位。
今后,我们要进一步加强对医院药品质量的管理工作,组织医务人员认真学习《医疗机构药品监督管理办法(试行)》、《处方管理办法》、《医疗机构管理条例》等相关法律法规知识,建立健全相关管理制度和奖罚措施,明确责任义务,做到依法行医,确保医疗安全。
药品管理自查报告2我院至上而下高度重视药品使用质量的管理,严格按照《药品管理法》、《药品管理法实施条例》以及《江苏省医疗机构药品使用质量管理规范》等法律、法规的要求,加强对药品质量的管理,现将我院对药品质量管理自查情况汇报如下:1、我院药品质量管理组织和人员能认真履行管理职责按照《药品管理法》、《江苏省医疗机构药品使用质量管理规范》规定,我院成立了药品质量监督领导小组,负责我院药品质量管理相关制度的制定,以及指导和监督我院药品质量管理工作,职能职责明确,并将药品质量和安全管理纳入科室责任目标进行定期检查和考核。
卫生院铬超标自查报告

白卫发【2012】24号
白王卫生院关于对铬超标胶囊剂药品的
自查报告
泾阳县药监局:
根据泾阳县药监局相关文件精神,现就我院及相关卫生室药品使用情况做一汇报
一、思想高度重视,组织领导到位
我院接到县药监局关于对254家生产企业的669批次铬超标胶囊剂药品的紧急通知后,第一时间紧急召开职工及乡医会议,传达县卫生局及药监局关于开展铬超标药用胶囊的查处等相关通知精神,成立了以李胜利院长为组长,郑德刚为副组长,赵丹、王吉利、王健及乡医为成员的工作领导小组,明确任务,落实责任,确保专人管,专人抓,工作落实到人。
二、通知及时,自查到位
我院在接到药监局通知的第一时间向各卫生室紧急通知,要求将全部胶囊制剂药品全部下架,封存,给乡医发放铬超标胶囊剂药品名单批次表,并进行网络公布,要求乡医一一清查,并进行登记,向卫生院汇报;经过自查,一家卫生室发现存在成都地奥制药集团的地奥心血康胶囊10盒,生产日期为2012.01.16批号为1201042有效期2014.01.15,先已销售出5盒,剩余5盒,现已封存;我院及余17家卫生室药品未发现存在254家生产企业的669批次铬超标胶囊剂药品。
向药品使用单位要求全部胶囊制剂药品必须要有质检报告,才可接收。
三、郑重承诺,确保安全
我院及相关18家卫生室郑重承诺,绝不销售、使用铬超标胶囊剂药品,积极配合监管部门监督检查工作,绝不隐瞒事实、弄虚作假和干扰执法。
白王卫生院
二零一二年五月三十日
抄报:泾阳县药监局,档(二)。
铬超标药用胶囊及胶囊剂产品自查报告(通用3篇)

铬超标药用胶囊及胶囊剂产品自查报告(通用3篇)铬超标药用胶囊及胶囊剂产品篇1县食品药品监督管理局:铬超标药用胶囊事件被媒体曝光以来,引起公众广泛关注。
为确保公众用药安全,我院按照县食品药品监督管理局统一部署,迅速在我辖区开展了铬超标药用胶囊及胶囊剂产品清理查处工作,暂停销售使用、下架、封存了涉案企业生产的所有胶囊剂药品。
现将查处情况通报如下:1、高度重视、组织领导到位按照《城固县食品药品监督管理局关于进一步做好铬超标药用胶囊及胶囊剂产品整治工作的紧急通知(城食药监发【】号)》的文件精神,我院第一时间组织我院职工、辖区村卫生室及个体诊所工作人员学习了上级有关文件精神,并将已经公布的15个厂家33个品种的铬超标胶囊剂产品目录印发给每个卫生室及个体诊所工作人员,使所有相关人员明确了认识。
结合我院实际,成立了以院长熊有春任组长、副院长张军、焦宏任副组长、彭丽、宁海如、尚凤同志为成员的铬超标药用胶囊及胶囊剂产品清理查处工作领导小组,确保了此项工作顺利进行。
2、强化责任、自查到位我们在第一时间要求我院药剂科、辖区村卫生室及个体诊所,对目前通报的15家药品生产企业的33个批次的铬超标胶囊药品和其他胶囊剂药品进行自查,全面清理、领导小组于本月6日对我院药房、药库、辖区村卫生室及个体诊所的所有药品进行了检查,根据目前清查情况,我院及辖区村卫生室及个体诊所无通报的15家药品生产企业的33个批次的铬超标胶囊药品,清查出该15家药品生产企业的其他胶囊剂药品共6个厂家的6个品种:修正药业集团股份有限公司批号为110403的维生素E烟酸酯胶囊34盒、丹东市通远药业有限公司批号为20120117的头孢氨苄甲氧苄啶胶囊27盒及批号为20120208的头孢氨苄甲氧苄啶胶囊4盒、长春海外制药集团有限公司批号为20110902的安神胶囊147粒、通化金马药业集团股份有限公司批号为20111114的天麻胶囊100粒、桂林市维威制药有限公司批号为20111103的咳特灵胶囊300粒、四川蜀中制药股份有限公司批号为120102的诺氟沙星胶囊200板,以上药品均已下架、登记备案、责令暂停销售使用。
铬超标

1,青海省格拉丹东药业有限公司生产的脑康泰胶囊(产品批号:1108204),所用药用胶囊铬含量为39.064mg/kg。
2,青海省格拉丹东药业有限公司生产的愈伤灵胶囊(产品批号:1008205),所用药用胶囊铬含量为3.46mg/kg。
3,长春海外制药集团有限公司生产的盆炎净胶囊(产品批号:20110201),所用药用胶囊铬含量为15.22mg/kg。
4,长春海外制药集团有限公司生产的苍耳子鼻炎胶囊(产品批号:20110903),所用药用胶囊铬含量为17.65mg/kg。
5,长春海外制药集团有限公司生产的通便灵胶囊(产品批号:20100601),所用药用胶囊铬含量为37.26mg/kg。
6,丹东市通远药业有限公司生产的人工牛黄甲硝唑胶囊(产品批号:20111203),所用药用胶囊铬含量为10.48mg/kg。
7,吉林省辉南天宇药业股份有限公司生产的抗病毒胶囊(产品批号:091102),所用药用胶囊铬含量为3.54 mg/kg。
8,四川蜀中制药股份有限公司生产的阿莫西林胶囊(产品批号:120101),所用药用胶囊铬含量为2.69 mg/kg。
9,四川蜀中制药股份有限公司生产的诺氟沙星胶囊(产品批号:0911012),所用药用胶囊铬含量为3.58 mg/kg。
10,修正药业集团股份有限公司生产的羚羊感冒胶囊(产品批号:100901),所用药用胶囊铬含量为4.44mg/kg。
11,通化金马药业集团股份有限公司生产的清热通淋胶囊(产品批号:20111007),所用药用胶囊铬含量为87.57mg/kg。
12,通化盛和药业股份有限公司生产的胃康灵胶囊(产品批号:111003),所用药用胶囊铬含量为51.45mg/kg。
13,通化颐生药业股份有限公司生产的炎立消胶囊(产品批号:110601),所用药用胶囊铬含量为181.54mg/kg。
铬超标药用胶囊及胶囊剂产品自查报告

铬超标药用胶囊及胶囊剂产品自查报告一、背景近期,我公司发现市场上出现了一些关于我公司生产的铬超标药用胶囊及胶囊剂产品的负面报道。
为了确保消费者的健康和安全,我公司决定对我公司产品进行全面自查,以确保产品质量符合相关法规和标准。
二、自查过程1. 收集资料:我公司收集了相关的法规、标准、规范和文件,并对生产过程中的各个关键环节进行了梳理和总结。
2. 样品检测:我公司对部分批次的药用胶囊及胶囊剂产品进行了抽样检测,检测结果符合相关标准要求。
3. 内部检查:我公司对生产过程中的各个关键环节进行了自查,包括原料采购、生产工艺、质量控制等方面,确保不存在任何质量问题。
4. 外部审计:我公司邀请了专业的第三方审计机构对我公司的生产过程进行了全面审计,确保生产过程中的各个环节符合相关法规和标准。
三、自查结果经过全面自查,我公司发现存在以下问题:1. 部分批次的药用胶囊铬含量超标,超出国家标准要求。
2. 生产过程中存在操作不规范的情况,如清洗不彻底、烘干温度控制不当等。
3. 原料采购过程中存在把关不严的情况,部分原料质量不符合要求。
针对以上问题,我公司已经采取了以下措施:1. 立即召回所有涉及批次的药用胶囊及胶囊剂产品,并积极配合相关部门的调查和处置工作。
2. 对相关责任人进行了严肃处理,加强了员工的质量意识和培训工作。
3. 对生产设备进行了全面检修和改造,提高了生产过程中的自动化和精确度。
4. 加强了原料采购的管理和验收工作,建立了严格的供应商管理制度。
5. 完善了质量管理体系,加强了质量监督和检查工作,确保产品质量符合相关法规和标准。
四、总结与展望通过本次自查,我们深刻认识到了在产品质量控制方面存在的不足和问题,并采取了一系列有效的措施加以改进。
我们深知产品质量是企业的生命线,只有确保产品质量合格,才能赢得消费者的信任和支持。
未来,我们将继续加强质量管理工作,提高产品质量和安全水平,为消费者提供更加安全、可靠、放心的药品。
高值耗材自查报告通用版

高值耗材自查报告通用版1. 背景介绍高值耗材是医院中使用频率较高、价格较贵的医疗器械产品。
为了确保医疗机构在采购、使用和管理高值耗材时符合标准和规范要求,提高医疗质量和安全水平,各医疗机构应定期进行自查。
2. 自查目的自查旨在全面检视医疗机构高值耗材的采购、使用、管理等环节,发现存在的问题并采取相应措施加以解决,确保高值耗材的使用达到规范要求,提升医疗服务质量与安全性。
3. 自查内容3.1 高值耗材采购管理3.1.1 高值耗材采购计划的编制是否符合实际需求;3.1.2 供应商的选择和挑选是否经过合理程序;3.1.3 采购合同的签订和履行情况;3.1.4 采购金额与高值耗材的实际用量是否匹配;3.1.5 采购记录的保存和归档是否规范。
3.2 高值耗材库房管理3.2.1 高值耗材库房的布局和环境是否符合要求;3.2.2 高值耗材的入库、出库和库存管理是否规范;3.2.3 高值耗材的保管和贮存条件是否符合标准;3.2.4 高值耗材的灭菌和消毒措施是否到位;3.2.5 库房人员的培训和管理是否跟进。
3.3 高值耗材使用管理3.3.1 高值耗材的领用和使用是否按照临床需要;3.3.2 高值耗材的分发和配置是否科学合理;3.3.3 高值耗材使用记录的填写和保存是否规范;3.3.4 高值耗材的消毒和清洁操作是否符合标准;3.3.5 高值耗材的维修和报废处理是否及时有效。
4. 自查方法4.1 可结合医疗器械相关管理规定和标准,从采购、库房和使用等方面制定自查细则;4.2 审查相关文件和记录,检查应用系统,观察现场操作;4.3 采取随机抽查、询问人员或组织讨论等形式获取信息;4.4 对发现的问题进行整理、归类和分析,提出改进意见。
5. 自查结果与改进5.1 对自查结果进行总结和分析;5.2 对存在的问题进行详细描述和整改建议;5.3 制定改进方案和时间表,明确责任人;5.4 完成改进措施后进行内部核查,确保问题得到解决。
院感自查报告3篇

院感自查报告3篇院感自查报告1 按照桂卫医【20xx】188号精神,深入贯彻落实《医院感染管理办法》认真查找医疗机构在院内感染管理,报告和处置方面存在的问题,进一步加强医院感染管理,有效预防和控制传染病病原体,耐药菌,条件致病菌及其他病原微生物的医院感染和医源性感染,增强医院防治能力,保障人民群众的健康和生命安全。
院领导高度重视,院长亲自组织,抓好落实,从建立组织,完善制度,职责,到一线督察,有重点,有部位,有措施,全面规范科学的开展了院内感染管理,自查自纠工作。
一、加强组织领导、保证院内感染管理工作的顺利开展。
我院成立了院内感染管理小组:在以院长为首的院感组负责全院的控制工作,并对下级科室进行指导。
认真抓好日常工作,定期、不定期对各科的院内感染控制工作进行督促、检查,对全院的相关数据进行收集、统计,并向医院领导小组汇报。
各临床科室有专人负责本科室的监控工作,按时向院感组汇报有关情况。
由于工作层层落实,保证了我院院内感染管理工作的顺利开展。
二、认真开展自查自纠通过几天的自查我们还存在诸多问题:⑴职工院内感染知识与控制意识浅薄。
⑵部分科室消毒硬件配备不全。
⑶院内感染控制制度不全面。
⑷院内感染控制细节做得不够。
⑸院内感染登记不全。
针对我院存在的问题院内感染管理小组逐一进行分析,想办法,找措施,解决存在的实际问题:⑴建立组织明确职责,责任到人。
⑵健全完善制度约束人。
⑶安装紫外线灯管,配置消毒液等。
⑷制定院内感染培训计划,提高职工思想意识。
⑸开展室内室外卫生大清扫。
⑹做好院内感染相关活动的登记工作等。
三、进一步完善管理制度并贯彻落实医院感染管理制度是搞好医院感染的基础和重要保证。
制定一整套科学实用的.管理制度,健全完善了院内感染管理、各科室消毒隔离、院内感染报告、危重急死亡病例讨论,特殊病例转诊,污水污物处理等制度。
来规范医院有关人员的行为。
加强制度的建设和学习,并认真贯彻执行,对于提高防范意识、降低医院感染的发病率极为重要。
铬超标自查报告

铬超标自查报告随着现代工业的发展和人类社会的进步,环境问题引起了越来越多的关注。
作为企业的一份子,我们必须要对环境问题负起一定的责任。
铬超标自查报告就是企业环保自我监测的一种方式,以下是我公司的铬超标自查报告。
一、报告背景我公司位于广东省,从事电子零部件的生产与销售。
铬超标自查报告是在我公司环境保护部门的指导下,由质量部门负责完成的。
本次自查主要针对公司的废水和废气进行监测和分析。
二、自查方法和过程1、废水监测(1)选择监测点:通过了解我公司的生产情况,确定了菜单文具厂生产区和液晶显示屏生产区各一个监测点。
(2)取样操作:首先清洗取样器,然后用取样器在废水取样点位处填满样品,避免有气泡和水滴产生。
(3)检测方法:使用国家标准GB/T11943-2002《工业废水中重金属总量的测定》和GB/T16889-2008《工业废水中六价铬的测定》的方法,对废水进行监测。
(4)分析数据:根据检测报告,我们发现菜单文具厂和液晶显示屏生产区的废水中六价铬浓度均超过了国家标准排放限值,分别为3.17mg/L和3.42mg/L。
2、废气监测(1)选择监测点:根据我公司生产的特点,我们选择了烘干车间、喷漆车间和蒸汽锅炉房三个监测点。
(2)取样操作:在监测点使用瓶塞式采样器取样,保持采样器底部离底板10cm左右,然后将采样器旋紧。
(3)检测方法:使用国家标准GB/T 16157-2012《稀释对称截面扩散雾化光谱法测定大气中苯类和芳香烃类化合物的方法》和HG/T 3558-2012《有机物气相色谱法》的方法,进行废气监测。
(4)分析数据:根据检测报告,我们发现烘干车间、喷漆车间和蒸汽锅炉房的废气中含有苯系物质和其他有机化合物,超过了国家标准排放限值,分别为15.2mg/m³、14.3mg/m³和15.5mg/m³。
三、自查结果分析及改进措施1、废水的自查结果分析根据检测结果,我公司废水中六价铬超过了国家标准排放限值,这说明公司的生产过程中放出了较多的铬。
除铬实验报告

一、实验目的1. 了解铬污染的来源及危害。
2. 掌握除铬实验的基本原理和方法。
3. 评估不同除铬方法的效率。
二、实验原理铬污染主要来源于工业废水、废气和固体废弃物。
其中,六价铬(Cr6+)是一种强致癌物质,对人体和环境具有极大的危害。
本实验主要采用化学沉淀法进行除铬,通过加入适量的沉淀剂使Cr6+形成不溶于水的沉淀物,从而实现除铬的目的。
三、实验材料与仪器1. 材料:工业废水、NaOH、Ca(OH)2、Na2S、H2O2、硫酸铝、硫酸铁、氢氧化钠等。
2. 仪器:pH计、滴定管、烧杯、玻璃棒、滤纸、漏斗等。
四、实验步骤1. 准备实验试剂和仪器。
2. 取一定量的工业废水置于烧杯中,用pH计测定其pH值。
3. 将NaOH溶液滴加至废水中,调节pH值至8.5~9.5,观察沉淀现象。
4. 用滴定管向沉淀物中加入Ca(OH)2溶液,观察沉淀是否溶解。
5. 分别向沉淀物中加入Na2S、H2O2、硫酸铝、硫酸铁等试剂,观察沉淀变化。
6. 对比不同沉淀剂对Cr6+的去除效果,记录实验数据。
五、实验结果与分析1. 调节pH值至8.5~9.5时,废水中Cr6+形成沉淀,说明此时Cr6+与OH-反应生成Cr(OH)3沉淀。
2. 加入Ca(OH)2溶液后,沉淀物未溶解,说明Ca(OH)2对Cr6+的去除效果不明显。
3. 加入Na2S、H2O2、硫酸铝、硫酸铁等试剂后,沉淀物溶解,说明这些试剂对Cr6+有较好的去除效果。
4. 对比不同沉淀剂对Cr6+的去除效果,发现Na2S、H2O2、硫酸铝、硫酸铁的去除效果较好,其中Na2S的去除效果最佳。
六、实验结论1. 化学沉淀法是一种有效的除铬方法,可用于处理含Cr6+的工业废水。
2. 在本实验中,Na2S、H2O2、硫酸铝、硫酸铁等试剂对Cr6+有较好的去除效果,其中Na2S的去除效果最佳。
3. 在实际应用中,可根据废水中Cr6+的浓度和含量,选择合适的沉淀剂和除铬方法。
七、实验注意事项1. 实验过程中,注意控制pH值,避免过高或过低影响除铬效果。
钢铁行业自查报告

钢铁行业自查报告近年来,随着国家经济的快速发展,钢铁行业也在不断壮大。
然而,随之而来的环保问题与产能过剩问题也不断浮现,为此,国家及相关部门对钢铁企业进行了多次自查和整改,以确保钢铁行业的可持续发展。
本文将对钢铁行业一次自查的报告进行分析和总结。
该自查报告的主要内容涵盖以下几个方面:一是环保问题,二是生产安全,三是产能过剩,四是技术创新,五是企业合规管理。
其中,环保问题是最为突出的一方面。
环保问题是钢铁企业一直面临的难题。
而在该自查报告中,环保问题被列为了首要问题。
通过对报告的分析,我们可以发现,钢铁企业在环保方面所存在的问题主要有以下几个方面:首先,是散乱污企业和一些大型钢铁企业存在环保问题。
这主要表现在污染排放治理方面,污染物排放不达标、污染防治设施缺乏、突出违法排污等问题比较突出。
其次,是钢铁企业在生产过程中排放大量二氧化碳等温室气体。
这不仅影响了环境,也对全球气候环境造成了影响,并且由于钢铁行业的产能过剩,这种情况更加显著。
针对以上问题,该自查报告提出了以下改进措施:一是加强对散乱污企业的整治力度,同时通过整合优化山西省内产业布局结构和优势,对钢铁行业实施区域性差异化整治。
二是优化钢铁生产方式,推动绿色钢铁技术开发和应用,并促进能源转型,增大新能源使用比例。
三是加强环保监管和执法力度,并建立联防联控、制度联动、信息共享的三联机制,实现对违法违规行为的及时发现和快速处理。
一次自查不仅是对企业的警醒,更是对企业全面问题的总结。
该自查报告所反映的钢铁企业问题,是在企业的日常经营中长期形成的,只有持续推进问题的解决方案才能最终将问题消除。
总的来说,钢铁行业在未来还需要进一步的技术和管理创新,加强环保治理力度,建立良好的社会形象,这样才能够保障钢铁行业的可持续发展,同时也能够为国民经济的发展做出更大的贡献。
广东东莞辐射事故事故自查报告

广东东莞辐射事故事故自查报告事故自查报告,关于广东东莞辐射事故。
在 XX 年1月18日,由于非法违规生产和销售不符合国家标准的焊接材料,导致一些存放已久的含有超量对人体健康有害的金属元素铅、镉等的旧电池因外壳破裂而泄露出来的有毒物质直接污染环境,造成该厂周边环境空气受到严重污染,危及周围居民身体健康,并造成了很大的财产损失。
为此,根据《中华人民共和国突发事件应对法》第二十条之规定,特向上级部门做如下汇报:经初步核实,这次事故是由于某公司在未取得相关资格证书的情况下擅自进行生产所引起的。
该企业没有按照要求建设防护距离,也没有配备必须的安全保卫措施,更谈不上制订切实可行的应急救援方案。
同时,还缺乏专职管理员负责日常检查维修,无任何应急处置能力。
目前,该企业已被依法吊销营业执照,其主要负责人正在接受调查。
现场监测结果表明,该企业排放废水中总铬浓度超过国家标准限值2.5倍;排放废气中总汞浓度超过国家标准限值3.6倍;排放烟尘中总砷浓度超过国家标准限值0.7倍。
根据国务院批转的环境保护部《关于加强环境监督管理,严肃查处违反环评制度行为的通知》(国办发[1999]56号)精神,请你局迅速组织有关单位开展环境影响跟踪监测,确认企业污染治理设施运行效率与达标状态,提交企业污染治理设施运行效率与达标状态的分析报告。
请贵阳市环境监察支队协助我省完善环境监察机构网络,尽快将涉嫌犯罪的企业或个人移送当地公安机关追究刑事责任。
请你厅会同省环保局派员参加调查处理工作。
我们立即启动了应急预案,采取紧急措施控制污染源,疏散群众,封锁现场,禁止无关人员进入,避免了污染面积扩大。
截至20日晚10点,现场清理工作基本完毕,共收集固体废弃物约500吨,液体废弃物约300吨,有毒化学品约200桶,并用密闭车辆运往指定地点妥善处理。
我们已委托贵州省环科院对事故区域土壤和水体进行检验,并邀请省疾病预防控制中心对事故区域内的食品、饮用水等进行抽样检验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
下寺镇中心卫生院
关于对铬超标药品自查情况的报告
县卫生局、县药品食品监督管理局:
自“毒胶囊”事件曝光后,引起社会广泛关注,成为舆论焦点之一。
根据县卫生局和县药品食品监督管理局的统一部署,我院立即对本院及各村级卫生站的药品进行了严格自查。
现将自查情况报告如下:
一、思想高度重视,组织领导到位
我院接到县药监局关于铬超标胶囊剂药品的紧急通知后,第一时间紧急召开职工及乡医会议,传达县卫生局及药监局关于开展铬超标药用胶囊的查处等相关通知精神,成立了以王虎生院长为组长,林青斌为副组长,赵国铭、母春梅、王亚东及乡医为成员的工作领导小组,明确任务,落实责任,确保专人管,专人抓,工作落实到人。
二、通知及时,自查到位
我院在接到药监局通知的第一时间向各卫生站紧急通知,要求将全部胶囊制剂药品全部下架,封存,给乡医发放铬超标胶囊剂药品名单批次表,要求乡医一一清查,并进行登记,向卫生院汇报;经过自查,我院及各村卫生站均未发现铬超标药品。
三、郑重承诺,确保安全
我院及相关16家卫生室郑重承诺,绝不销售、使用铬超标胶囊剂药品,积极配合监管部门监督检查工作,绝不隐瞒事实、弄虚作假和干扰执法。
二〇一二年五月三十日。
