2013年福建省化学竞赛预赛试题答案及评分标准
2013年福建省高中学生化学竞赛预赛试题

2013年福建省高中学生化学竞赛预赛试题1.(2013福建初赛)I2和S2O32-间发生的是一个速率快、定量进行的反应,常用在分析化学中。
(1)写出化学反应离子方程式;(2)通常该反应在近中性条件下进行,为什么?(3)若把I2液滴入S2O32-液,即使在碱性液(pH≈11)中,也能发生定量反应。
为什么?(4)硫代硫酸钠在药剂中常用作解毒剂,可解卤素单质(如Cl2)、重金属离子(如Hg2+)及氰化钾中毒。
写出化学反应方程式。
2.(2013福建初赛)元素A在n=5,l=0的轨道上有一个电子,它的次外层l=2的轨道上电子处于全充满状态;元素B与A在同一周期,若A、B的简单离子混合则有难溶于水的黄色沉淀AB生成;黄色沉淀AB可溶于氰化钾溶液,再加入含有C的简单阴离子溶液后又有黑色沉淀生成,该黑色沉淀可溶于硝酸,并产生乳白色沉淀、同时放出刺激性气体。
(1)写出元素A、B、C的价层电子构型;(2)A、B、C各处于第几周期第几族?(3)写出题目中涉及到的化学反应的离子方程式。
3.(2013福建初赛)在地球的电离层中,可能存在以下离子:ArCl+、OF+、NO+、PS+、SCl+。
(1)说明这些离子中心原子的杂化方式;(2)预测哪一种离子最稳定?哪一种离子最不稳定?说明理由。
4.(2013福建初赛)氮是最常见的元素,其化合物用途十分广泛,回答下列问题:(1)为什么在N3-离子中,两个N-N键的键长相等,而在HN3中却不相同?(2)CO与N2是等电子体,具有完全相同的分子轨道和一些类似的性质,但为什么CO和金属形成配合物要比N2容易?(3)氮气常用作保护气体,其中所含的微量氧可通入连二亚硫酸钠的碱性溶液除去。
写出化学反应方程式。
(4)实验室中NH4NO3热分解制得的N2O中混有少量NO,如何使用简单的方法除去?并写出化学反应方程式。
(5)NaNO3和NaNO2均为白色固体,如何鉴别?并写出化学反应的离子方程式。
5.(2013福建初赛)同温(300K)、同体积(气相、液相体积均相同)的A、B两瓶液体中通入同量的CO2(g),其中,A瓶液体为蒸馏水,B瓶液体为石灰水。
省高中学生化学竞赛(预赛)试题答案

年福建省高中学生化学竞赛(预赛)试题答案 题号 一 二 三 四 五 六 七 八 九 十 十一 总分 得分一、 分 ()于酸性溶液中混合等物质的量的和,生成哪些氧化还原产物,它们的物质量的比是多少?()用漂白粉漂白物料时,常采用以下步骤:将物料浸入漂白粉溶液,然后暴露在空气中;将物料浸在稀盐酸中;将物料浸在大苏打溶液中,最后取出放在空气中干燥;试说明每一步处理的作用,并写出有关的反应方程式。
答:() 残骛楼諍锩瀨濟溆塹籟婭骒。
所余 将和() 作用生成() (分)生成、、,其物质的量比为 : : 。
(分) ()吸收释放出而进行漂白:(分)酽锕极額閉镇桧猪訣锥顧荭。
除掉()和钙盐: () (分)彈贸摄尔霁毙攬砖卤庑诒尔。
除漂白过程中放出的:(分)謀荞抟箧飆鐸怼类蒋薔點鉍。
二、(分)设计以银币(约含%)为原料制备硝酸银和胆矾的简单步骤并写出有关的化学反应方程式。
答:第一步,将银币溶于并蒸发结晶,得和()混合晶体:↑() ↑ (共分,叙述分,方程式各分)厦礴恳蹒骈時盡继價骚卺癩。
第二步,将混合晶体在 ℃加热分解,不分解,而()分解成,再用水浸取分解产物,过滤。
前者进入溶液,后者作为沉淀滤出,将它溶于后蒸发结晶得胆矾:茕桢广鳓鯡选块网羈泪镀齐。
() ↑ ↑ ·(胆矾) (共分,叙述分,方程式各分)鹅娅尽損鹌惨歷茏鴛賴縈诘。
第三步,将上步滤液蒸发结晶,得产品。
(分) 三、(分)氮、磷、铋都是族元素,它们都可以形成氯化物,例如:、、和。
试问:籟丛妈羥为贍偾蛏练淨槠挞。
() 为什么不存在及而有? () 请写出、、水解反应反应方程式。
()热电材料() 的性质在由正值变负值时会发生急剧的变化,欲使由 变到 ,应在 () 中加碲多少克?頌圣鉉儐歲龈讶骅籴買闥。
(相对原子质量: , ) 答:()氮为第二周期元素,只有、轨道,最大配位数为。
故只能形成不可能有。
(分)渗釤呛俨匀谔鱉调硯錦鋇絨。
磷为第三周期元素,有、、轨道,既可以杂化轨道成键,也可以以杂化轨道成键,最大配位数为。
中国化学会2013年全国高中学生化学竞赛(省级赛区)试题及答案

第27届中国化学奥林匹克(初赛)试题、解答、评分标准及评分细则第1题(12分) 写出下列化学反应的方程式1-1 加热时,三氧化二锰与一氧化碳反应产生四氧化三锰。
1-2 将KCN 加入到过量的CuSO 4水溶液中。
1-3 在碱性溶液中,Cr 2O 3和K 3Fe(CN)6反应。
1-4 在碱性条件下,Zn(CN)42?和甲醛反应。
1-5 Fe(OH)2在常温无氧条件下转化为Fe 3O 4。
1-6 将NaNO 3粉末小心加到熔融的NaNH 2中,生成NaN 3(没有水生成)。
1-1 3Mn 2O 3+CO =2Mn 3O 4+CO 2 2分1-2 4CN ?+2Cu 2+=2CuCN +(CN)2 2分1-3 Cr 2O 3+6Fe(CN)63?+10OH ? =2CrO 42?+6Fe(CN)64?+5H 2O 2分1-4 Zn(CN)42?+4H 2CO +4H 2O =4 HOCH 2CN +Zn(OH) 42?? 2分1-5 3Fe(OH)2=Fe 3O 4+H 2+2H 2O 2分1-6 NaNO 3+3NaNH 2=NaN 3+NH 3+3NaOH 2分1方程式正确才能得满分。
2若全部物质皆写对而未配平,可得1分。
第2题(23分) 简要回答或计算2-1 Bi 2Cl 82-离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi原子的杂化轨道类型。
Bi 2Cl 82-的结构:ClClBi Cl ClCl 2-或Cl Cl Cl Cl Cl 2- 2分.......未画成楔形键不扣分;不画电子对不扣分;若画了电子对且画成如上图(蓝)所示的连线,则与电子对相连的线不画成虚线(左)、虽画成虚线但远离Bi 原子,扣0.5分?杂化轨道类型:sp 3d 2 1分2-2在液氨中,E θ(Na +/Na)=-1.89V ,E θ(Mg 2+/Mg)=-1.74V ,但可以发生Mg 置换Na 的反应:Mg +2NaI =MgI 2+2Na ,指出原因。
2011年-2013年福建高中化学竞赛试卷及答案不含有机部分

2011年福建省高中学生化学竞赛预赛试题第1题(11分)加工松花蛋时,要将纯碱、石灰、盐、黄丹粉按一定比例混合,再加上泥和糠裹在鸭蛋外面,两个星期后,美味可口的松花蛋就制成了。
1-1写出黄丹粉的化学式,设计一个简单的实验检验松花蛋中是否含有铅。
1-2,判断单质铅是否易溶于稀HCl 、浓H 2SO 4、热浓H 2SO 4、浓HCl ,并写出反应式。
第2题(8分)回答下列问题:2-1在酸性溶液中,NaNO 2与KI 反应可得到NO ,有两种操作步骤: (a)先将NaNO 2酸化后再滴加KI ; (b)先将KI 酸化后再滴加NaNO 2。
哪种方法制得的NO 更纯?为什么?2-2实验室少量的氮气可用氯化铵和亚硝酸钠制备,制备出的氮气常混有NO ,可通入硫酸亚铁溶液除去,写出化学反应方程式。
2-3为什么NF 3常温不水解,而NCl 3常温可以水解?写出水解产物。
第3题(10分)某元素A 能直接与VIIA 族某元素E 反应生成A 的最高氧化态化合物D , D 为一种无色透明的液体,沸点为77℃,不易燃烧,易挥发,其蒸气对空气的相对密度约为5.31倍。
在D 中E 的含量占92.2%。
回答下列问题:(原子量F-19.0;Cl-35.5;Br-79.9; I-126.9) 3-1 指出A 元素的名称,并指出属于第几周期、第几族,写出其核外价电子排布;3-2写出化合物D 的分子式,画出其构型,说明中心原子的杂化方式;3-3分析化合物AO 作为配体的成键方式。
3-1 按题意化合物D 为AE x ,则x M AE = 5.31 ⨯ 29 = 154M A = 154 ⨯ (1 - 0.922) = 12故为A 为碳,第二周期,IV A 族,价层电子排布2s 22p 2 (4分) 3-2 根据碳的价态, AE x x = 4,M E = 154 ⨯ 0.922 ÷4 = 35.5 所以E 为Cl 。
(1分) 化合物D 为CCl 4, sp 3杂化 (3分)3-3 CO作为配位体的成键方式是:它的孤电子对给予金属原子的空轨道形成σ键,同时CO分子中的反键轨道(π2p*)和接受金属原子的d电子的反馈,形成反馈键。
2013年初三化学竞赛试题及答案

2013年化学竞赛预选试题(卷)说明:可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Cl—35.5 Na—23 Al—27K—39 Ca—40 Mn—55 Fe——56 Cu—64 Zn—65 Ag—108 Ba—137考试时间:120分钟第Ⅰ卷(选择题,共40分)一、选择题(本题包括20个小题,每小题2分,共40分。
每小题有1个或2个选项符合题意。
若有两个答案的错1 个不得分,漏选1个扣1 分。
)1.古诗词是古人为我们留下的宝贵精神财富。
下列诗句中只涉及物理变化的是A.野火烧不尽,春风吹又生B.春蚕到死丝方尽,蜡炬成灰泪始干C.只要功夫深,铁杵磨成针D.爆竹声中一岁除,春风送暖入屠苏2.实验室使用大理石和盐酸反应制取的CO2是不纯净的,为证明该气体中含有多种物质,所用的试剂及使用顺序正确的是A.无水硫酸铜、硝酸银溶液、石灰水B.浓硫酸、氢氧化钠溶液、石灰水C.硝酸银溶液、石灰水、无水硫酸铜D.氯化钙、石蕊试液、水3.由石灰石、水、苏打为原料制取烧碱的过程中,未发生的化学反应类型是A.分解反应B.化合反应C.置换反应D.复分解反应4.下列实验中所选用的仪器或操作合理的是A.用托盘天平称量5.85g氯化钠晶体B.用酸式滴定管量取25.00mL酸性高锰酸钾C.用湿润pH试纸测定某H2SO4溶液的pHD.用瓷坩埚(含有二氧化硅)灼烧碳酸钠晶体5.“绿色绿色是将反应物全部转化为期望的产物,使原子的利用率达到100%,以昼减少有害物质生成的化学工艺理念。
下列符合“绿色化学”要求的是A.湿法冶铜:Fe+CuSO4=FeSO4+CuB.高炉炼铁:Fe2O3+3CO=2Fe+3CO2C.制氧气:2KMnO4△K2MnO4+MnO2+O2↑D.用乙烯(C2H4)为原料制取乙二醇(C2H6O2):C2H4+H2O2→C2H6O26.下列说法中,你认为科学的是A. 臭氧在一定条件下能转化为有毒气体B.多吃腌制食品能防癌C.生理盐水含食盐的量越高越好D.活性炭可以制作冰箱的除味剂7.同学们在做实验时发现,将镁条放入某CuCl2溶液中,镁条表面有气泡产生。
最新福建省化学竞赛预赛试题答案及评分标准

2013年福建省高中学生化学竞赛预赛试题
答案及评分标准
第1题(10分)
1-11分
1-22分
1-3 1分
1-46分,每个反应方程式2分
第2题(10分)
2-2 3分,每个1分
3-15分,每个1分
第4题(10分)
4-12分
4-22分
CO与N2是等电子体,共14个电子,在它们的分子轨道表示式中有6个成键电子,相当于1个σ键,2个π键。
但由于CO分子是异核双原子分子,其中1个π键相当于由氧原子向碳原子提供的π配键。
这样在C原子上就有较多的负电荷,C原子上电子密度较大,从而使其有较强的配位能力,所以易与一些过渡元素形成羰基化合物。
4-32分
4-5 2分
5-16分
5-2 4分
第6题(10分)
在计算式中,未带入单位不扣分。
但计算结果表示应考虑有效数字和单位。
本题所有求算结果均为三位有效数字,第一次有效数字错误扣0.5分;求算物理量均需正确标注单位,第一次单位错误扣0.5分,但有效数字和单位错误累计扣分不超过1分。
未给出中间结果计算值,只要表达清楚、最终结果计算合理可追加得分。
7-1 5分
7-2 5分
第8题(10分)
8-16分,每个结构式1分,C,D结构简式正确但未用立体结构式表示或立体结构表达
8-24分,每个结构式1分,H1,H2结构简式正确但未用立体结构式表示或立体结构表达错误的,每个给0.5分。
第9题(10分)
9-1 8分,每个1分
9-21分
第10题(10分)
10-1 1分
10-2 9分,每个1分。
初中福建化学竞赛试题

初中福建化学竞赛试题福建省化学竞赛试题一、选择题(每题2分,共20分)1. 下列物质中,属于混合物的是:A. 氧气B. 矿泉水C. 液态氮D. 纯水2. 根据化学方程式计算时,需要考虑的因素不包括:A. 反应物的摩尔质量B. 反应物的化学计量数C. 反应物的浓度D. 反应物的摩尔比3. 以下哪个元素的原子序数是11?A. 氢B. 钠C. 氧D. 碳4. 根据质量守恒定律,化学反应前后不会改变的是:A. 元素的种类B. 物质的总质量C. 分子的个数D. 物质的化学性质5. 下列哪项不是化学变化的特征?A. 有新物质生成B. 伴随能量变化C. 反应速率快D. 有颜色变化6. 根据酸碱中和反应的实质,下列说法正确的是:A. 酸中的H+与碱中的OH-结合生成水B. 酸中的OH-与碱中的H+结合生成水C. 酸中的H+与碱中的H+结合生成水D. 酸中的OH-与碱中的OH-结合生成水7. 金属活动性顺序表中,位于氢前面的金属可以:A. 与水反应生成氢气B. 与酸反应生成氢气C. 与氧气反应生成氢气D. 与水、酸和氧气都不反应8. 根据溶液的酸碱性,下列说法不正确的是:A. 酸性溶液的pH值小于7B. 中性溶液的pH值等于7C. 碱性溶液的pH值大于7D. pH值等于0的溶液是中性溶液9. 根据金属的化学性质,下列说法错误的是:A. 金属可以与氧气反应B. 金属可以与酸反应C. 金属可以与盐溶液反应D. 金属不与任何物质反应10. 下列化合物中,属于有机化合物的是:A. 水B. 二氧化碳C. 甲烷D. 硝酸二、填空题(每空1分,共10分)11. 化学方程式2H2 + O2 → 2H2O中,反应物和生成物的摩尔比是_________。
12. 根据元素周期表,第18族元素都是_________。
13. 氧化还原反应中,失去电子的物质被称为_________。
14. 根据化学式H2O,水分子中含有_________个氢原子和_________个氧原子。
2013年全国化学竞赛初赛模拟试卷3含答案

2013年全国化学竞赛初赛模拟试卷3(时间:3小时 满分:100分)题 号 1 2 3 4 5 6 7 8 9 10 11 满 分988510111079914H 1.008 相对原子质量 He4.003Li 6.941 Be 9.012B 10.81C 12.01 N 14.01 O 16.00 F 19.00 Ne 20.18Na 22.99 Mg 24.31 Al 26.98 Si 28.09 P 30.97 S 32.07 Cl 35.45 Ar 39.95 K 39.10 Ca 40.08 Sc 44.96 Ti 47.88 V 50.94 Cr 52.00 Mn 54.94 Fe 55.85 Co 58.93 Ni 58.69 Cu 63.55 Zn 65.39 Ga 69.72 Ge 72.61 As 74.92 Se 78.96 Br 79.90 Kr 83.80 Rb 85.47 Sr 87.62 Y 88.91 Zr 91.22 Nb 92.91 Mo 95.94 Tc [98] Ru 101.1 Rh 102.9 Pd 106.4 Ag 107.9 Cd 112.4 In 114.8 Sn 118.7 Sb 121.8 Te 127.6 I 126.9 Xe 131.3 Cs 132.9 Ba 137.3 La -Lu Hf 178.5 Ta 180.9 W 183.8 Re 186.2 Os 190.2 Ir 192.2 Pt 195.1 Au 197.0 Hg 200.6 Tl 204.4 Pb 207.2 Bi 209.0 Po [210] At [210] Rn [222] Fr [223] Ra [226] Ac -LrRf Db Sg Bh Hs Mt Ds第一题(9分)利用质谱仪来分析分子构造已经成现代化学重要的技术,其原理为利用电子撞击分子(M )使它产生阳离子团(M +)或分子裂解产生的阳离子团在磁场飞行的差异,而侦测各种离子,图谱的横坐标为质量与电荷比(m/z ),纵坐标为强度代表所产生粒子数的多寡。
高中学生化学竞赛预赛试题答案及评分标准
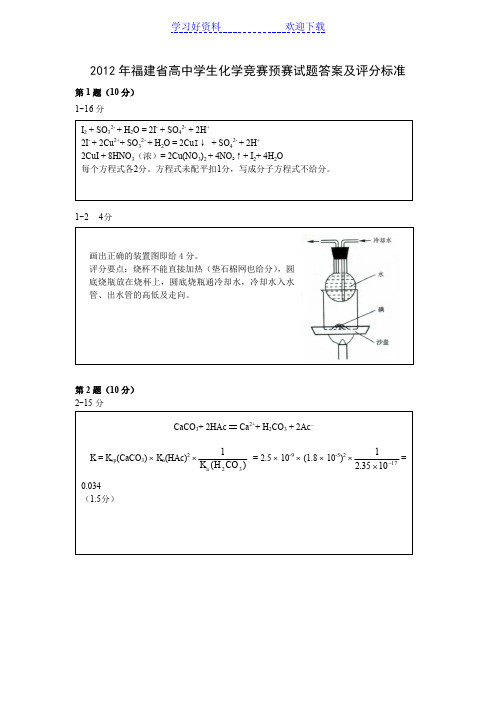
+ 2Ac -
⨯ (1.8 ⨯ 10-5)2 ⨯12351017
.⨯-2012年福建省高中学生化学竞赛预赛试题答案及评分标准
第1
题(10分) 1-16分 1-2 4分
第2题(10分) 2-15分
2-23分
第3题(11分)
3-14分,每个图2分。
(不要求标出键角、键长,但基本形状要相同)
3-24分
3-33分
第4题(9分)4-1 3分
4-23分
4-33分
第5题(10分)
5-17分
5-2 3分
第6题(10分)
6-1 4分,每个原子核外电子排布2分。
6-2 6分,每个分子2分。
第7题(10分)
评分总则:在计算式中,未带入单位不扣分。
但计算结果表示应考虑有效数字和单位。
本
题所有求算结果均为四位有效数字,第一次有效数字错误扣0.5分;求算物理量均需正确标注单位,第一次单位错误扣0.5分,但有效数字和单位错误累计扣分不超过1分。
7-14分
7-22分
第8题(15分)
8-22分
8-4 0.5分
第9题(6分)
9-1 2分,每个0.5分
9-22分,B,E,H每少写一个扣0.5分,多写的每2个扣0.5分,但扣分最高不超过2分。
9-32分
第10题(9分)
10-16分,每个1分。
化学竞赛试题(含答案)
化学竞赛决赛试题(满分100分100分钟)可能用到的相对原子质量:H-1 C-12 N—l4O一l6F-19 Mg一24 P一31 S一32 Cl一35.5 K一39 Ca一40 Fe一56 Cu一64 Zn-65一、选择题(本题包括20个小题,每小题2分,共40分;每小题有1个或2个选项符合题意。
若有两个答案的错选l个不得分,漏选1个扣l分。
请将答案填在下方的表格内)1.世界环境日为每年的6月5日,它的确立反映了世界各国人民对环境问题的认识和态度,表达了人类对美好环境的向往和追求。
2011年世界环境日的主题是“森林:大自然为您效劳”,旨在配合联合国国际森林年,强调森林的生态价值,提高人们森林保护意识。
下列标记是2011年国际环境日标识的是2.2011年我国用“长征2号FT1”型运载火箭成功地将“天宫一号”送入指定轨道,其后,天宫一号与神舟八号实现了成功对接。
这是我国航天领域又一重大突破。
“长征2号FT1”型运载火箭在升空时发生的下列变化中,属于化学变化的是A.火箭点火B.导流槽内的水受热汽化C.隔热材料脱落D.整流罩脱落3.欧洲科研人员成功“抓住”反氢原子长达一千秒,是2011年世界十大科技新闻之一。
科学家认为,组成物质的基本粒子,如电子、质子、中子等,都有各自的反粒子,它们在质量上以及其他方面与它对应的粒子一模一样,但所带的电荷正负恰恰相反。
粒子与反粒子碰到一起会同归于尽,化作一束强光,这种现象称之为湮灭。
有反粒子就可能形成反物质、反世界。
较长时间“抓住”反氢原子,有利于对反物质性质进行精确研究。
下列关于反氢原子的叙述不正确的是A.反氢原子中有一个带负电荷的质子B.反氢原子的相对原子质量为lC.反氢原子中有一个带正电荷的电子D.反氢原子带一个单位负电荷4.我国科学家屠呦呦因为“发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获拉斯克奖。
青蒿素是治疗疟疾的特效药,青蒿素分子式为C15H22O5。
2013年福建省高中化学竞赛模拟试卷

2021年高中化学竞赛模拟试卷题号 1 2 3 4 5 6 7 8 9 10 总分满分 6 10 8 12 9 9 10 20 8 8 100得分第1题 (共6分) 试验室制备少量硅一般接受镁粉还原SiO2的方法,然后用稀盐酸洗涤产品以除去杂质。
某同学在进行上述操作时,在制得的产品中加HCl洗涤时突然起火。
(1)请用化学方程式解释:①稀盐酸洗涤产品可除去哪些主要杂质?②为什么加HCl洗涤时突然起火?(2)请设计一个试验来验证你的解释。
(不必画出装置图,也不必指出具体化学药品,不要写方程式,只要简明指出方法。
)第2题.(10分)(1) 磷和氢能组成一系列的氢化物,如PH3,P2H4,P12H16等。
其中最重要的是PH3。
PH3称为膦,它是一种无色剧毒的有类似大蒜臭味的气体。
它可由NaOH和白磷反应来制备,其制备反应的化学方程式为,P2H4的沸点比PH3 (填“高”或“低”),缘由是。
(2) ①依据VSEPR理论,SCl3+和ICl4-的空间构型分别是和,S和I分别以和杂化轨道同Cl形成共价键。
② SCl3+和PCl3是等电子体,其S-Cl键键长 (填>、=或<)P-Cl键键长,缘由是。
第3题 (共8分)铝是一种重要的金属材料,广泛用于制作导线、结构材料和日用器皿,铝合金大量用于飞机和其它构件的制造。
十九世纪曾以电解熔融氧化铝的方法制备金属铝,当时铝由于价格昂贵而只被贵族用作装饰品。
现代工业上是通过在1000℃左右的高温下电解氧化铝和冰晶石(Na3AlF6)的熔融液制备铝的。
请回答下列问题:(1) 现代工业电解制备铝过程中正极和负极实际发生的反应分别为:在正极放电产生;在负极放电产生。
(2) 电解反应方程式为。
(3) 以现代工业方法制备的铝价格下降的可能缘由是:。
(4) 若电流效率为75%,则制备1kg金属铝需以10A电流电解小时。
(5) 电解NaCl-AlCl3熔融液制备铝比电解Al2O3-Na3AlF6的熔融液制备铝节省电能约30%,为什么现在仍用后一种方法制备铝?。
2013年福建省化学竞赛复赛赛前练习一:配位化合物(含详细答案)

2013年福建省化学竞赛复赛赛前练习一:配位化合物沙县一中罗仙福2013-06-051.写出下列各配合物或配离子的化学式(1) 硫酸四氨合铜(II) (2) 二氰合银酸根离子(3) 二羟基·四水合铝(III)离子(4) 三氯·(乙烯)合铂(II)酸钾(5) 四硫氰·二氨合铬(III)酸铵(6) 顺式—二氯二氨合铂(II)2、(2011全国初赛第2题11分)2-1画出2,4-戊二酮的钠盐与Mn3+形成的电中性配合物的结构式(配体用O O表示)。
2-2 已知该配合物的磁矩为4.9玻尔磁子,配合物中Mn的未成对电子数为。
2-3 回答:该化合物有无手性?为什么?2-4 画出2,4-戊二酮负离子的结构简式(必须明确其共轭部分),写出其中离域π键的表示符号。
2-5橙黄色固体配合物A的名称是三氯化六氨合钴(Ⅲ),是将二氯化钴、浓氨水、氯化铵和过氧化氢混合,以活性炭为催化剂合成的。
机理研究发现,反应过程中首先得到Co(NH3)62+离子,随后发生配体取代反应,得到以新配体为桥键的双核离子B4+,接着发生桥键断裂,同时2个中心原子分别将1个电子传递到均裂后的新配体上,得到2个C2+离子,最后C2+离子在活性炭表面上发生配体取代反应,并与氯离子结合形成固体配合物A。
写出合成配合物A的总反应方程式;画出B4+和C2+离子的结构式。
3.化合物的种类繁多,一个重要的因素是许多化合物存在同分异构现象(isomerism),试画出(Me2PCH2CH2PMe2)2Fe(CO)的所有可能的立体异构体。
(Me = CH3)。
在结构式中Me2PCH2CH2PMe2可简化成 P(双齿配体)4、配合物A是1936年由Jensen合成的,它的化学式为Ni[P(C2H5)3]2Br3。
化合物呈顺磁性,有极性,但难溶于水,易溶于苯,其苯溶液不导电,试画出配合物A所有可能的几何异构体。
若存在对映体,请标明对映关系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2013年福建省高中学生化学竞赛预赛试题
答案及评分标准
第1题(10分)
1-11分
1-22分
1-3 1分
1-46分,每个反应方程式2分
第2题(10分)
2-2 3分,每个1分
第3题(10分)
3-15分,每个1分
第4题(10分)4-12分
4-22分
4-32分
4-5 2分
第5题(10分)5-16分
5-2 4分
第6题(10分)
第7题(10分)
在计算式中,未带入单位不扣分。
但计算结果表示应考虑有效数字和单位。
本题所有求算结果均为三位有效数字,第一次有效数字错误扣0.5分;求算物理量均需正确标注单位,第一次单位错误扣0.5分,但有效数字和单位错误累计扣分不超过1分。
未给出中间结果计算值,只要表达清楚、最终结果计算合理可追加得分。
7-1 5分
7-2 5分
第8题(10分)
8-16分,每个结构式1分,C,D结构简式正确但未用立体结构式表示或立体结构表达错误的,每个给0.5分。
8-24分,每个结构式1分,H1,H2结构简式正确但未用立体结构式表示或立体结构表达错误的,每个给0.5分。
第9题(10分)
9-1 8分,每个1分
9-21分
第10题(10分)
10-1 1分
10-2 9分,每个1分。
