第2节 物质的酸碱性(第二课时)
浙教版科学九年级上册_《物质的酸碱性》名师教案(第2课时)

pH为4 ~6的土壤会使 农作物根系发黑;pH为8以上的土壤会腐蚀农作物并板结成块。盐碱地的 pH多在9以上,草木难生。
活动:检验家用溶液酸碱性
学生阅读:
pH试纸——石蕊试纸是波义耳用石蕊浸液把纸浸透,然后烤干,制成的。现今的pH试纸上有甲基红、溴甲酚绿、百里酚蓝这三种指示剂,在不同PH值的溶液中均会按一定规律变色。甲基红的变色范围是pH4.4(红)--6.2(黄),溴甲酚绿的变色范围是pH3.6(黄)--5.4(绿),百里酚蓝的变色范围是pH6.7(黄)--7.5(蓝)。
版本科目年级课时教学设计
课题
物质的酸碱性
单元
第一单元
学科
科学
年级
九年级上
学习
目标
1、知道物质酸碱性强弱可用PH值的高低来表示,会用PH试纸和标准比色卡测定物质酸碱性的强弱。
2、知道物质酸碱性强弱与我们生活的密切关系及酸雨对环境的危害,对学生进行环保教育。
重
总结:物质的酸碱性强弱与我们生活息息相关,为了了解和控制物质的酸碱性,我们需要测定物质酸碱性的强弱。
pH 是反映物质酸碱性强弱的指标,它的范围通常在0~14 之间。pH越低,酸性越强;pH 越高,碱性越强;pH 等于7 的物质呈中性。
测定物质酸碱性强弱最常用、最简单的方法是使用pH 试纸。
PH试纸简介
人的汗液的pH大约为5.5 ~6.6。
洗衣皂、香皂、药皂的pH也有所不同。 洗衣皂的pH高,碱性强,适用于洗衣物;香皂、药皂的pH 低,适用于洗 脸、洗澡。
牛奶的 pH 通常小于 7,
酱油的 pH 为4.8 左右,
番茄的 pH≤4.5。
生鲜肉的pH 为7.0~7.4 之间,生肉久放后,由于肉中蛋白质凝固,失去一 些水分,pH变为5.4~5.5。
第2节物质的酸碱性(PPT课件(初中科学)30张)

角度2 自制酸碱指导剂
典例6 用酒精和水浸泡蝴蝶兰花瓣可得到紫色溶液,该溶液遇酸溶液显红色,遇碱 溶液显黄色。下列说法正确的是( C ) A.该紫色溶液与酸作用显红色是物理变化 B.能使该紫色溶液显黄色的一定是碱溶液 C.将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色 D.该紫色溶液不可用作酸碱指导剂
[解析] 由题表中信息可知,白醋呈酸性,能使紫甘蓝提取液显红色,碳酸钠溶液呈 碱性,能使紫甘蓝提取液显绿色,食盐溶液呈中性,能使紫甘蓝提取液显蓝色,即
碱性溶液能使紫甘蓝提取液显绿色。橙汁和苹果汁呈酸性,蒸馏水呈中性,石灰水
呈碱性,故石灰水能使紫甘蓝提取液显绿色。
知识点3 溶液酸碱性的强弱程度 重点
实验 取4支试管,分别加入稀硫酸、稀盐酸、氢氧化钠溶液、氢氧化钙溶液。然后在4支 操作 试管内分别滴入几滴紫色石蕊试液,视察并记录石蕊试液在4种溶液中呈现的颜色
实验 图示
现象 结论
溶液呈红色
溶液呈红色
溶液呈蓝色
溶液呈蓝色
2.酸显示出不同颜色的物质,叫做酸碱指导剂,通
常简称指导剂。
(2)常用指导剂及其在酸性、碱性溶液中的颜色
指导剂 石蕊试液(紫色) 酚酞试液(无色)
蓝色石蕊试纸 红色石蕊试纸
酸性溶液 红色 无色 红色 不变色
碱性溶液 蓝色 红色 不变色 蓝色
注意 不能使无色酚酞试液变色的溶液不一定是酸性溶液,也可能是中性溶液。
特别提醒 (1)明确变色物质:指导剂与酸性或碱性溶液混合后,是指导剂变色,而不是酸 性或碱性溶液变色。例如,不能说酸遇到紫色石蕊试液变红,也不能说碱遇到无色 酚酞试液变红。
浙教版 九年级上册 1.2 物质的酸碱性(第2课时导学案设计)

第2节物质的酸碱性(第2课时)一、酸碱指示剂:取4支试管,分别加入稀硫酸、稀盐酸、氢氧化钠溶液、氢氧化钙溶液。
然后在4支试管内分别滴入几滴紫色石蕊试液,如图。
观察石蕊在4种溶液中呈现的颜色。
在稀硫酸中:石蕊变在稀盐酸中:石蕊变在氢氧化钠溶液中:石蕊变在氢氧化钙溶液中:石蕊变实验表明:酸能使紫色石蕊试液变色,碱能使紫色石蕊试液变色。
紫色石蕊试液遇酸变,遇碱变;无色酚酞试液遇酸,遇碱变。
二、溶液酸碱性的强弱程度1.溶液的酸碱度——pH值1)反映物质的指标2)取值范围:之间3)物质酸碱性强弱的测定pH<7,性,数值越,酸性越;pH>7,性,数值越,碱性越;pH=7,性2.最常用、最简单、比较粗略的方法是使用。
1)原理:在性强弱不同的溶液里显示不同2)组成:(色);标准3)测定方法:用的蘸取被测试的溶液,在pH试纸上。
将试纸显示的与标准比色卡,看与哪种颜色最,从而确定被测溶液的。
检验身边物质的酸碱性(利用pH试纸)用玻璃棒分别蘸取少许稀盐酸、稀硫酸、稀氢氧化钠、橙汁、蔗糖水、牛奶、番茄汁、肥皂背诵任务A.酸碱指示剂1.酸碱指示剂:在酸性或碱性溶液里能显示出不同颜色的物质,简称指示剂1)某溶液滴入无色酚酞试液不变色,该溶液不一定是酸性溶液,也可能是中性溶液2)指示剂遇酸性或碱性溶液变色的过程是化学变化3)不溶于水的酸或碱不能使指示剂变色,如氢氧化铜是一种难溶于水的碱,它不能使无色酚酞试液变红B.溶液酸碱性的强弱程度1.pH和酸碱性1)pH是反映物质酸碱性强弱的指标,且范围通常在0~14之间2)pH和酸碱性2.测定物质酸碱性强弱1)用品:pH试纸2)方法:用洁净的玻璃棒蘸取被测试的溶液,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,看与哪种颜色最接近,从而确定被测溶液的pH3)用pH试纸测试的方法比较粗略,精确的测试可使用一种称为酸度计的仪器。
第2节物质的酸碱性(PPT课件(初中科学)29张)

碱性溶 液
蓝色 红色 不变色 蓝色
归纳总结
石蕊遇酸变红,遇碱变蓝; 酚酞遇酸不变色,遇碱变红。
课堂讲授
自制酸碱指导剂
1、取一些月季花、菊花、丝瓜花、一串 红等植物的花、果、枝叶切碎、捣烂,用 酒精浸制,所得的浸出液可以作为酸碱指 导剂。
2、取食盐水、白醋、石灰水加以实验。并记 录变色情况。
A.H+、NO3-、SO42- B.OH-、Ba2+ C.H+、Na+、SO42- D. Na+ 、Ba2+、 Cl-
5.某一溶液的pH=2,该溶液呈 酸 性,它能使紫色石蕊试液 无色酚酞试液 不变色,使蓝色石蕊试纸变 蓝 色。
红 色,
6.下表列出了家庭中某些物质的pH:
物质
醋
pH
3
牙膏 9
食盐溶液 7
课堂讲授 溶液酸碱性的强弱程度
1.pH是反应物质酸碱性强弱的指标。它的范围通常在 0至14之间。
2.pH与溶液酸碱性之间的关系。 pH<7 溶液呈酸性,pH越小,酸性越强。 pH=7 溶液呈中性 pH>7 溶液呈碱性,pH越大,碱性越强
课堂讲授
pH 是反应物质酸碱性强弱的指标,它的范 围通常在0~14 之间。pH越低,酸性越强;pH 越高,碱性越强;pH 等于7 的物质呈中性。
第1章 物质及其变化
第2节 物质的酸碱性
合作学习
你有过呕吐的经历吗?你感到胃液 是什么味道的?
酸的
想一想
合作学习
归纳总结
一、一些物质的电离
1、离子: 带电的原子或原子集团。 带正电荷的叫阳离子。 带负电荷的叫阴离子。
2、电离: 一些物质溶解于水或受热融化时, 产生自由移动的离子的过程,叫做 电离。
最新浙教版九年级科学《物质的酸碱性》第二课时优秀课件

1
通过观察实验现象,分析酸和碱的性质及反应 规律。
2
利用分类的方法,探究酸和碱的化学性质。
3
学会使用实验仪器进行酸碱中和反应的实验操 作。
情感态度价值观
培养对化学学科的兴趣和好奇 心。
增强探究意识和实践能力,树 立科学态度和创新意识。
了解酸和碱在生活和生产中的 应用,体会化学知识的重要性
。
02
教学内容及重点难点
通过课堂互动手段,促进师生之间的交流和 互动,提高教学效果。
04
教学步骤及时间安排
导入新课
复习巩固
复习上一节课学习的物质的分 类。
情境创设
通过生活中的一些常见的物质, 如醋、柠檬汁等,引出酸和碱的 概念。
提出问题
什么是酸?什么是碱?它们具有什 么性质?
进行新课
实验探究
通过实验探究常见酸和碱的性质,例如酚酞溶液 遇酸变红色,遇碱变蓝色等。
பைடு நூலகம்
教学内容
酸碱指示剂的概念及原理 常见酸碱指示剂的使用
酸碱中和反应的原理及应用
重点难点
酸碱指示剂的变色原理及使用条件 酸碱中和反应的原理及实验操作注意事项
03
教学方法与手段
教学方法
情境创设法
通过创设真实的情境,引导学生进 入酸碱知识的学习。
问题驱动法
通过设置问题串,引导学生思考和 解决与酸碱有关的问题。
小组合作法
通过小组合作,培养学生的协作和 交流能力。
实验探究法
通过实验探究,培养学生的实践能 力和科学精神。
教学手段
多媒体辅助手段
实验教学手段
通过多媒体辅助手段,帮助学生更好地理解 和掌握酸碱知识。
通过实验教学手段,帮助学生更好地理解和 掌握酸碱实验技能。
第2节 物质的酸碱性 第2课时 课件

则土壤的pH的变化与浇灌的次数之间的关系符合图中的( D )
A.
B.
C.
D.
4.根据下列实验现象可以判断某溶液一定呈碱性的是( B )
A.常温下,测得溶液的pH<7 B.溶液中滴入酚酞显红色
C.溶液中滴入石蕊显红色
D.溶液中滴入酚酞不显色
课堂总结
三、溶液酸碱性的强弱程度
1、pH 是反映物质酸碱性强弱的指标,它的范围通常在0~14 之间。 pH越低,酸性越强用洁净的玻璃棒蘸取被测试的溶液, 滴在pH 试纸上,将试纸显示的颜色与标 准比色卡对照,看与哪种颜色最接近, 从 而确定被测溶液的pH。根据pH便可判断 溶液的酸碱性强弱。 3、pH试纸能显示酸性的强弱(定量测定酸碱度),而酸碱指 示剂则只能指示溶液是否显酸性(定性测定酸碱性)。
知识拓展
用pH试纸测试的方法比较粗略,精确的测试可使用一 种称为酸度计的仪器。
pH酸度计是由电极和电计两部 分组成。使用中若能够合理维护 电极、按要求配制标准缓冲液和 正确操作电计,可大大减小pH示 值误差,从而提高化学实验、医 学检验数据的可靠性。
知识拓展
我们身边物质的pH
(1)人体血液的pH为7.39 ~ 7.45。当血液的pH降到7.0以下或升到7.8 以上 时,人就有生命危险。 (2)人的汗液的pH大约为5.5 ~6.6。 (3)洗衣皂、香皂、药皂的pH也有所不同。 洗衣皂的pH高,碱性强,适用于 洗衣物;香皂、药皂的pH 低,适用于洗 脸、洗澡。 (4)牛奶的 pH 通常小于 7, (5)酱油的 pH 为4.8 左右, (6)番茄的 pH≤4.5。 (7)生鲜肉的pH 为7.0~7.4 之间,生肉久放后,由于肉中蛋白质凝固,失去 一 些水分,pH变为5.4~5.5。 (8)食用醋酸的pH 为3 左右。 (9)pH为4 ~6的土壤会使农作物根系发黑;pH为8以上的土壤会腐蚀农作物 并板结成块。盐碱地的 pH多在9以上,草木难生。
新浙教版九年级上册 物质的酸碱性 两课时

什么是酸 1.我们熟悉的有酸味的物质有:
2、电离通式:酸= H + 酸根阴离子 3.酸的涵义:
电离时产生的阳离子全部是氢离子的化 合物 叫做酸.
2020/3/31
四.酸碱指示剂 1).定义:在酸或碱溶液里能显示出不同颜色的物
质叫做酸碱指示剂. 2)常见的酸碱指示剂有:
紫色石蕊试液和无色酚酞试液. 3)作用: 可以定性地测量溶液的酸碱性. 4)实验结论
剂2020则/3/31只能指示溶液是否显酸性(定性测定酸碱性)
pH试纸能显示酸性的强弱(定量测 定酸碱度),而酸碱指示剂则只能指 示溶液是否显酸性(定性测定酸碱 性)。
2020/3/31
4、溶液酸碱性与生命活动的关系
(1)溶液酸碱性与人体健康的关系
(2)溶液酸碱性与生活的关系 a b
c (3)溶液酸碱性与农业生产的关系
2020/3/31
2、写出下列物质的电离方式: H2CO3 = 2H+ +CO3 2-
Ca(OH)2 = Ca2+ + 2OH -
Na2CO3 = 2Na+ +CO3 2-
CuSO4 = Cu2+ + SO42-
BaCl2 = Ba2+ + 2Cl -
NaHSO 2020/3/31
4
= Na++H++SO42-
物质 醋 牙膏 食盐溶液 肥皂水
PH
3
9
7
10
上述物质能使无色酚酞试液变红色的
是 牙膏、 肥皂水 .
2020/3/31
5、下列物质不属于酸的是( B )
A、HNO3 B、NaHCO3 C、H3PO4
D、HI
最新浙教版九年级科学《物质的酸碱性》第二课时优秀课件

在化学工业中,酸和碱是重要的原料,可用于合成有机物、制造药物等;在环境保护中,酸和碱可用于处理废 水、废气等;在生物科学中,酸和碱对生物体的生理功能和代谢过程具有重要影响。此外,酸和碱还用于日常 生活和农业生产中,如清洁剂、化妆品等。
03
教学重点与难点
教学重点与难点
教学重点
• 掌握判断物质酸碱性的方法 • 理解酸碱指示剂的原理和应用 • 学会使用酸碱指示剂测定物质的酸碱性
3
合作学习法
采用小组合作的形式,让学生在合作学习中互 相交流、讨论、解决问题,培养学生的团队合 作精神和协作能力。
教学手段
多媒体辅助教学
利用课件、视频、图片等多种多媒体手段,将抽 象的概念和规律形象化、生动化,提高学生的学 习效果和理解能力。
网络学习
利用网络平台,提供丰富的学习资源和学习环境 ,方便学生进行自主学习和拓展学习,提高学生 的学习效果和学习效率。
详细描述
酸是指电离时产生的阳离子全部是氢离子的化合物,碱是指 电离时产生的阴离子全部是氢氧根离子的化合物,盐是指由 金属阳离子(或铵根离子)和酸根离子结合而成的化合物。 这些物质在溶液中表现出不同的酸碱性。
酸、碱、盐的性质
总结词
酸、碱、盐的性质是多种多样的,它们在 溶液中具有不同的酸碱性,并且具有一些 通性。
02
学习并掌握酸碱指示剂的使用方法。
03Βιβλιοθήκη 学会使用化学方程式进行计算。
情感态度与价值观
1
培养学生严谨求实、勇于探索的科学精神。
2
增强学生对化学的热爱和对生活现象的关注。
3
通过小组合作,培养学生的团队合作精神。
02
教学内容与过程
酸、碱、盐的组成
九年级科学第2节 物质的酸碱性(2)

第2节 物质的酸碱性
样品 水
柠檬汁 白醋 盐酸
肥皂水 洗涤剂 4%氢氧化钠溶液氢氧化钠溶液
pH试纸试纸
紫色石蕊试液
第2节 物质的酸碱性
[问题探究] 检验溶液酸碱性的方法有哪些?
[思考交流] _____________________________________________________ _____________________________________________________
第2节 物质的酸碱性
[情景展示3]
NaOH===Na++OH- Ca(OH)2===Ca2++2OH-
KOH===K++OH-
第2节 物质的酸碱性
[情景分析] 常见的碱性物质有烧碱(NaOH)、熟石灰[Ca(OH)2]、氢氧化钾(KOH)、 氨水(NH3的水溶液),这些碱性物质含有碱。 [问题探究] 碱在水溶液中电离时,生成的离子有什么共同特点?
探究点二 酸碱指示剂
[情景展示1]
观察实验,并记录实验现象。 在稀硫酸中:_________________________。 在稀盐酸中:_________________________。 在氢氧化钠溶液中:___________________。 在氢氧化钙溶液中:___________________。
第2节 物质的酸碱性
3.常见指示剂和它们在酸性、碱性溶液中的颜色变化
指示剂
紫色石蕊试液 无色酚酞试液 (只检验碱性)
酸性溶液 (pH<7) 变____红____
不变色(无色)
碱性溶液 (pH>7)
变___蓝_____
中性溶液(pH= 7)
不变色(紫色)
变___红_____ 不变色(无色)
《物质的酸碱性》PPT(第2课时)

2.取适量的紫卷心菜、胡萝卜两种样品,分别在研钵中捣烂, 加入酒精溶液(乙醇与水的体积比为1∶1)进行浸泡,并用纱
点 分
布将浸泡出的汁液挤出,分别加入下列溶液中,观察并记录颜
类 练
色情况如下:
溶液
白醋
食盐水
纯碱溶液
紫卷心菜汁
红色
蓝紫色
绿色
胡萝卜汁
橙色
橙色
橙色
解析知识要
(1)在实验中纱布所起的作用是将样品渣与汁液分离(或过滤) 。 (2)上述汁液可用作酸碱指示剂的是 紫卷心菜汁 , 其理由是
资料下载: . /ziliao/
范文下载: . /fanwen/
试卷下载: . /shiti/
教案下载: . /jiaoan/
ppt论坛: . .cn
ppt课件: . /kejian/
语文课件: . /kejian/yuwen/ 数学课件: . /kejian/shuxue/
英语课件: . /kejian/yingyu/ 美术课件: . /kejian/meishu/
物质及其变化
第
1
第2节 物质的酸碱性
章
第2课时
-.
-
解析知识要
知识点 1 酸碱指示剂 1.溶液的酸碱性可以用 石蕊试液 和 酚酞试液 两种常用的
点
分 酸碱指示剂来检验;还可以用蓝色石蕊试纸或红色石蕊试纸
类 练
来检验,蓝色石蕊试纸遇到 酸 性溶液能变红,红色石蕊试
纸遇到 碱 性溶液能变蓝。
解析知识要
C.用玻璃棒蘸取待测液滴在pH试纸上,将试纸与标准比色 卡对比
解析知识要
D.用胶头滴管吸取待测液滴到pH试纸上,3 min后将试纸与 标准比色卡对比
浙教版科学九上1.2《物质的酸碱性(第二课时)》教学课件

上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较( )
由此可见,柠檬汁( )
人的汗液的pH 大约为5.
由此可见,柠檬汁( )
牛奶的pH 通常小于7,酱油的pH 为4.
3,在苹果汁中滴入紫色石蕊试液,显示的颜色是( )
3、现有白纸、溶质质量分数为10%的NaOH的溶液 A ,5%的H2SO4溶液 B, 5%的紫色石蕊溶液C,试设计《“雨” 落叶出红花开》
A . 显酸性 B. 显碱性 1、小明同学在实验室中测定某未知溶液的pH,他的实验操作如下:先用蒸馏水将PH试纸润湿,然后用玻璃棒蘸取待测试液于pH试纸
上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较( )
C . 显中性 D. 无法确定 紫色石蕊试液无色酚酞试液
3,在苹果汁中滴入紫色石蕊试液,显示的颜色是( ) 由此可见,柠檬汁( )
C、水(pH=7)
D、肥皂(pH=8.9)
6、人体中几种体液的正常pH值范围如下表:
唾液
胃液
血液
小肠液 胆汁
6.6-7.1 0.9-1.5 7.35-7.45 7.6 7.1-7.3
所列体液中酸性最强的是( D), 碱性最强的是( E )
(A)唾液 (B)血液 (C)胆汁 (D)胃液(E)小肠液
思维拓 1、小展明:同学在实验室中测定某未知溶液的pH,他的
2、实验室常见的指示剂种类: 紫色石蕊试液 无色酚酞试液
活动: P7图1-13用石蕊试液判断酸碱性
取4支试管,分别加入稀硫酸、稀盐酸、氢氧化钠 溶液、氢氧化钙溶液。然后再4支试管内分别滴入 几滴紫色石蕊试液,如图所示,观察并记录石蕊 试液在4种溶液中呈现的颜色。
在稀硫酸中:__红_色___ 在稀盐酸中:__红_色___ 在氢氧化钠溶液中:_蓝__色__ 在氢氧化钙溶液中:_蓝__色__
第2节 物质的酸碱性(第二课时)PPT课件

写在最后
经常不断地学习,你就什么都知道。你知道得越多,你就越有力量 Study Constantly, And You Will Know Everything. The More
You Know, The More Powerful You Will Be
结束语
感谢聆听
不足之处请大家批评指导
Please Criticize And Guide The Shortcomings
讲师:XXXXXX XX年XX月XX日
贫瘠的盐碱地
被酸雨危害的森林
1、土壤的酸碱性直接影响农作物的生长。 已知某地区土壤显弱碱性,参照下表,从 土壤酸碱性考虑,在该地区适宜种植的作 物是( B )
小麦:5.5~6.5
油菜:5.8~6.7
西瓜:6.0~7.0
甘草:7.2~8.5
A、西瓜 B、甘草 C、小麦 D、油菜
2、蜜蜂的刺中含有酸性物质,当我们不小心被蜜
怎样判断 物质的酸 碱性呢?
石蕊
酚酞
氢氧化钙溶液 氢氧化钠溶液
稀盐酸 稀硫酸
石蕊
酸溶液能使紫色石蕊试液变红色 碱溶液能使紫色石蕊试液变蓝色
物质酸碱性的测定:
方法 现象
结论
变红色:是酸性溶液 使用紫色 石蕊试液 变蓝色:是碱性溶液
不变色:是中性溶液
在酸性或碱性物质里能 显示出不同颜色的物质
实验过程中物质的颜色变化
试剂 水
柠檬ቤተ መጻሕፍቲ ባይዱ 白醋 盐酸
肥皂水 洗涤剂
4%氢氧化钠溶液
pH试纸
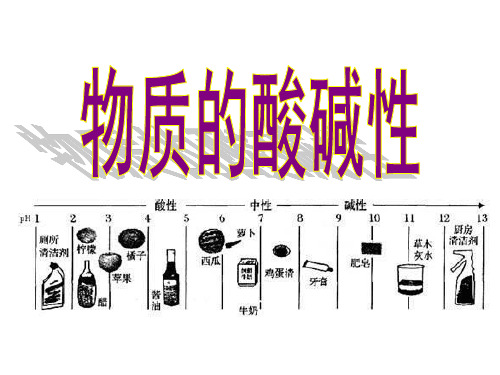
7 4 3 1 10 12 13
紫色石蕊试液
紫色 红色 红色 红色 蓝色 蓝色 蓝色
根据下表,回答问题:
物质的酸碱性(2)PPT课件(初中科学)

2、碱性物质:
强碱:氢氧化钠、氢氧化钾、 氢氧化钙、氢氧化钡、
弱碱性物质:小苏打、纯碱、 洗涤剂、
与酸相类似,许多碱在水中电离时,生成的阴 离子都是相同的一种粒子,所不同的是这种粒 子是氢氧根离子(OH-)
电离方程式
NaCl KNO3
=== Na+ + Cl=== K+ + NO3-
NaOH === Na+ + OH-
pH
中 酸性 性
碱性
数值
越小,
酸性 越强 0 1 2 3 4 5 6 7 8 9 10 1112 13 14
pH 数值 越大, 碱性 越强
pH数值越低,酸性越强;pH数值越高,碱 性越强;pH数值等于7的物质呈中性。
四、物质酸碱性强弱(PH)的测定
1、最常用、最简单、比较粗略的方法是 使用____P_H_试__纸______。
测定下列物质的酸碱性强弱
①菠萝汁 pH≈3
酸性较强的有(
)
②醋
pH ≈ 3
③自来水 pH ≈ 6.8
酸性较弱的有(
)
④洗洁精 pH ≈ 7
中性的有 (
)
⑤牙膏 pH ≈ 8
⑥汽水
pH ≈ 5.5 碱性较强的有 (
)
⑦胃舒平药片pH ≈ 8
碱性较弱的有(
)
⑧洗发液 pH ≈ 8
⑨土壤浸出液 pH ≈ 7
酸雨的危害
背景知识介绍:
酸雨
一般指PH小于5.6的雨、雪或其它情势的大气降水。
酸雨给人类带来的危害极大。仅美国因酸雨对建筑物和材料造成
的损失每年达20亿美元;我国仅川黔和两广四省,1988年因酸雨
物质的酸碱性2课件---浙教版科学九年级上册

实验二:室温时,向4支试管中分别加入相同体积的以下4种物质,各滴加3滴黑枸杞提取液。实验 结果如上: 根据实验,回答下列问题: (1)炉具清洁剂的pH约为__1_3_____。 (2)根据实验现象,不能确定牛奶呈中性的理由是_呈__紫_色__时__。pH 可能是 6 也可能是 7, 故不能判定是中性 (3)小苏打溶液的pH为8.3,向小苏打溶液中加3滴黑枸杞提取液,再滴入pH为4的稀盐酸至过量, 观察到的实验现象是_溶__液__由__蓝_。色变紫色,最后变成浅紫色。
pH与人体健康
pH与农业生产
(1)化工生产中许多反应必须在一定的pH溶液里才能进行; (2)农业生产中农作物一般适宜在pH为7或者接近7的土壤中生长;
西瓜~
苹果树~
小麦~
【课堂小结】
பைடு நூலகம்
【课堂练习】
1.一些食物的pH值如下:葡萄-,苹果-,牛奶-,鸡蛋清-,则 D
下列说法正确的是( )
C
A、胃酸过多的人应多吃苹果
❀pH值:反映物质酸碱性强弱的指标。
pH的范围:在 0 ~ 14 之间 pH<7溶液为酸性,pH越小酸性越强; pH=7溶液为中性; pH>7溶液为碱性,pH越大碱性越强。
读数读 取整数
pH试纸使用方法:
NaOH溶液?
洗涤擦干
稀盐酸
放 →蘸
→滴
→读
pH试纸使用方法:
√
××
pH试纸是否可以伸入溶液中,为什么?
用水湿润过的pH试纸,再测待测液,溶液的pH将( ) A. 变大 B.不变 C.变小 D.前三者均有可能
稀HCl的pH=2 NaCl溶液pH=7 NaOH溶液pH=12
《物质的酸碱性》PPT(第二课时)

4.常见的碱 NaOH、Ca(OH)2、KOH、Ba(OH)2 等
5.酸碱指示剂 紫色石蕊试液; 无色酚酞试液
上一页 下一页
指示剂
石蕊试液(紫色) 酚酞试液(无色)
蓝色石蕊试纸 红色石蕊试纸
酸性溶液 (pH<7)
红色
碱性溶 液 (pH>7)
蓝色
无色
红色
红色 不变色
不变色 蓝色
上一页 下一页
用紫色石蕊试液测定物质的酸碱性,有什么缺点?
紫色石蕊试液虽然能够测定物质的酸碱性,但不能反 映酸碱性的强弱程度。
上一页 下一页
三、溶液酸碱性的强弱程度
1.测定溶液酸碱性强弱的意义 土壤的酸碱性的强弱对农作物生长有很大的影 响。所以,测定土壤的酸碱性非常必要。
上一页 下一页
土地的盐碱化使土壤碱性增强。
碱性土壤会腐蚀农作物并板结成块,草木难生。 上一页
下一页
工业废气的过量排放,雨水酸 性过强,形成酸雨。
被酸雨伤害的树木
上一页 下一页
2.物质酸碱性强弱的测定 (1)pH值
pH是反映物质酸碱性强弱的指标。 范围通常在 0 ~14 之间。
上一页 下一页
pH等于7 呈中性。 pH小于7 的呈酸性;pH大于7 的呈碱性。 pH越低,酸性越强;pH越高,碱性越强;
上一页 下一页
用pH试纸测试溶液酸碱性的方法有什么缺点? 用pH试纸测试的方法比较粗略。 精确的测试可使用一种称为酸度计的仪器。
上一页 下一页
1.用玻璃棒分别蘸取少许水、柠檬汁、白醋、盐酸、肥 皂水、洗涤剂、4% 氢氧化钠溶液,滴在 pH 试纸中部, 观察试纸的颜色变化。
上一页 下一页
2.在白色点滴板的空穴(或小试管)里分别滴入几滴上 述样品,再滴加2~3滴紫色石蕊试液,观察其颜色的变 化,并将上述实验结果都填入表1-3中。
浙教版九年级科学上册1.2物质的酸碱性第二课时

活动: 在白色点滴板的空穴中滴入几滴样品
后加入2 ~ 3滴石蕊试液
注意:不要
将滴管接触
点滴板,不
要将滴管放
样品
错试剂瓶。
这节课你学了什么?
四.酸碱指示剂
1).定义:
在酸或碱溶液里能显示出不同颜色的物质叫做 酸碱指示剂.
2)常见的酸碱指示剂有:
紫色石蕊试液和无色酚酞试液.
3)作用: 可以定性地测量溶液的酸碱性.
2.下表列出了家庭中某些物质的PH:
物质 醋 牙膏 食盐溶 肥皂
液
水
PH 3
9
7
10
上述物质能使无色酚酞试液变红色的 是 牙膏、 肥皂水 .
3.将一定质量分数的硫酸溶液加水稀释, 下图正确表示PH变化的是( A )
3、思考:一位科学家在做研究时不小心将 盐酸滴到了紫花上,紫花逐渐变红色。看到 这么个现象,许多问题在他的脑子里涌现出 来,如果你是那个科学家,你会有什么问题, 你会有什么想法?
菊 花
月季
丝
一
瓜
串
红
2)取食盐水、白醋、石灰水等试验,它们分别 能使上述自制酸碱指示剂变什么颜色?
溶液酸碱性的强弱程度
你知道什么是酸雨吗?盐碱地里为什么很多植物都 无法生长呢。为了了解和控制物质的酸碱性,我们 需要测定物质酸碱性的强弱。
四、溶液酸碱性的强弱程度
pH
pH 是反映物质酸碱性强弱的指标,它的范围 通常在0~14 之间。pH越低,酸性越强;pH 越高,碱性越强;pH 等于7 的物质呈中性。
4)实验结论
①pH试纸能显示酸性的剂变色,其中能使紫色石蕊试液变红 色,使无色酚酞试液不变色。 五、自制酸碱指示剂
练习
1.某一溶液的PH=2,该溶液呈 酸 性,它能使
物质的酸碱性(第二课时)(2021年初中科学浙教版)

2、常见的酸碱指示剂有:
蓝色石蕊试纸 紫色石蕊试液 无色酚酞试液
红色石蕊试纸
新知讲解
活动: 教材P7
实验表明:酸能使紫色石蕊试液变__红_____色, 碱能使紫色石蕊试液变__蓝_____色。
新知讲解
常见指示剂及其在酸性、碱性溶液中的颜色
pH:表示溶液酸碱性的强弱程度 PH的测定方法: 用洁净的玻璃棒蘸取被测试的溶液,滴在pH 试纸上,将
试纸显示的颜色与标准比色卡对照,看与哪种颜色最接近 ,从而确定被测溶液的pH。
课堂练习
1、蜜蜂的刺中含有酸性物质,当我们不小心被蜜蜂刺着后,应用下边哪
种物质冲洗( D)
(已知显酸性物质与碱性物质反应时酸性会减弱) A.酱油(pH=4.8) B.牛奶(pH=5.6) C.水(pH=7) D.肥皂(pH=8.9)
2、某一无色溶液PH=2,该溶液呈( 酸)性,它能使紫色石蕊试液变(
)色,无红色酚酞试液(
),使蓝色不石变蕊色试纸变 ( )色.
红
课堂练习
3、下表列出了家庭中某些物质的PH:
物质 醋
PH
3
牙膏 食盐溶液 肥皂水
9
7
10
上述物质能使无色酚酞试液变红色的是 牙膏、肥皂水
.
4、把一朵红色的牵牛花泡在肥皂水里,这时牵牛花中的花青素就变成了
季
花
丝
一
瓜
串
红
见表1-2 某些花浸出液的变色情况
新知讲解
石蕊试液虽然能够测定物质的酸碱性,但不能反映酸碱性的强弱, 而物质酸碱性的强弱却与我们的生活密切相关。
需要测定物质酸碱性的强弱
物质的酸碱性二)—浙教版九年级科学上册课件(共28张PPT)
贫瘠的盐碱地
被酸雨危害的森林
1、天然降水的PH通常为6.5,请说明原因
2、用洁厕净(主要成分是盐酸),除去污垢中的 碳酸钙
3、石灰水敞口放置于空气中,溶液PH如何变化, 原因是?
A 紫色 B 红色 C 蓝色 D 无色
2、某无色溶液能使无色酚酞试液变红, 则该溶液能使紫色石蕊试液变( ) C
A 紫色 B 红色 C 蓝色 D 无色
向某溶液滴入无色酚酞试液后仍无 色,若向该溶液中滴加紫色石蕊试液,
则( C )
A.一定显红色 B.可能显蓝色 C.可能仍为紫色,也可能显红色 D.一定显无色
pH数值越小,酸性越强; pH数值越大,碱性越强; pH数值等于7的物质呈中性。
1、用洁净的玻璃棒蘸取被测试的硫酸溶液和氢氧化钠 及酒精溶液,滴在湿润的pH 试纸上,将试纸显示的颜 色与标准比色卡对照。
待测液如果是酸性的,测量值偏大
待测液如果是碱性的,测量值偏小
待测液如果是中性的,测量值不变 2、雪碧等碳酸饮料的PH小于7,若晃动后打开瓶盖, PH有什么变化? 偏大
PH
A
对于碱性溶液来说,加水后,溶液碱 性减弱,PH减小,逐渐接近于7,但
总不会等于7。
7
B
0
对于酸性溶液来说,加水后,溶液酸 性减弱,PH增大,逐渐接近于7,但 总不会等于7。
加水体积
人们通常把pH小于5.6的雨水 称为酸雨。
大多数农作物适宜在接近中性的土壤中生 长,酸性太强或碱性太强的土壤都不适宜农作 物的生长。
3、小王同学测出农夫山泉饮用天然水PH约为7.3 4、小张同学测出实验用硫酸溶液PH为0 5、PH=1的溶液一定是酸
测定物质酸碱性强弱 最常用、最简单的方 法是使用pH 试纸,用 p H试纸测试的方法比 较粗略,精确的测试 可使用一种称为酸度 计的仪器。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
土壤的酸碱性的强弱对农作物生长有很大的 影响。所以,测定土壤的酸碱性非常必要。
Copyright 2004-2015 版权所有 盗版必究
土地的盐碱化使土壤碱性增强。
碱性土壤会腐蚀农作物并板结成块。草木难生。
Copyright 2004-2015 版权所有 盗版必究
牛奶的pH 通常小于 7,酱油的pH 为4.8 左右,番茄的 pH ≤ 4.5。生鲜肉的pH为7.0 ~ 7.4 之间,生肉久放后, 由于肉中蛋白质凝固,失去一些水分,pH变为5.4~5.5。 食用醋酸的pH为3左右,因为酸性 环境可抑制细菌的繁 殖,所以人们喜欢在一些食物中加入少许食用醋酸,这 样既能使食品不易变质,又可增加风味。 土壤的酸碱性的强弱对农作物生长有很大的影响,各种 农作物对pH有一定的适应 性。一般来说,中性土壤最 适宜于微生物生长繁殖,有利于土壤中有机质向有效养 分转化,促进农作物生长。pH为4 ~6 的土壤会使农作 物根系发黑;pH为8以上的土壤会腐蚀农作物并板结成 块。盐碱地的pH多在9以上,草木难生。
Copyright 2004-2015 版权所有 盗版必究
一般的雨水具有微弱的酸性,但有些地方由于工 业废气的过量排放,雨水酸性过强,形成酸雨。
被酸雨伤害的树木
Copyright 2004-2015 版权所有 盗版必究
2、物质酸碱性强弱的测定 (1)pH值
pH是反映物质酸碱性强弱的指标。 范围通常在 0 ~14 之间。pH等于7 呈中性。 pH小于7 的呈酸性;pH大于7 的呈碱性。
第2课时
Copyright 2004-2015 版权所有 盗版必究
溶液酸碱性强弱
1、酸的定义 电离时生成的阳离子全部都是氢离子的化合物 2、常见的酸 HCl 、H2SO4、HNO3、H2CO3、醋酸等
3、碱的定义 电离时生成的阴离子全部都是氢氧根离子的 化合物
4、常见的碱 NaOH、Ca(OH)2、KOH、Ba(OH)2 等 5、酸碱指示剂
1、用洁净的玻璃棒蘸取被测试的溶液;
2、滴在pH试纸上; 3、将试纸显示的颜色与标准比色卡对照; 4、看与哪种颜色最接近,从而确定溶液的pH。
Copyright 2004-2015 版权所有 盗版必究
用pH试纸测试溶液酸碱性需要注意哪些问题?
1、试纸不可直接伸入溶液中。
2、不能先用蒸馏水将pH试纸润湿。 (因为润湿试纸相当于稀释被检测的溶液, 这会导致检测不准确) 用pH试纸测试溶液与红蓝石蕊试纸测试溶液 有什么不同? pH试纸能显示酸碱性的强弱(定量测定酸碱 度),而红蓝石蕊试纸则只能指示溶液是否 显酸性或碱性(定性测定酸碱性)。
Copyright 2004-2015 版权所有 盗版必究
我们身边物质的pH pH 是定量反映物质酸碱性强弱的重要指标, 它与我们的生活密切相关。 人体血液的pH为7.39 ~ 7.45。当血液的 pH降 到7.0以下或升到7.8以上时,人就有生命危险。 人处在通风不良的环境中时间过长,吸入的二 氧化碳过多,血液中二氧化碳的含量增大,酸 性就会增强,从而引起恶心、头晕等症状。 人的汗液的pH大约为5.5~6.6。洗衣皂、香皂、 药皂的pH也有所不同。洗衣皂的pH高,碱性 强,适用于洗衣物 ;香皂、药皂的pH低,适 用于洗脸、洗澡。
Copyright 2004-2015 版权所有 盗版必究
3.实验测得人体内一些体液的pH如下,其中酸性 最强的是-----------------------------------------( B ) A.唾液:6.6~7.1 B.胃液:0.9~1.5 C.汗液:6.6~7.6 D.血浆:7.35~7.45 4.某同学测定某NaOH溶液的pH时,先将pH试纸 用蒸馏水润湿,再将待测液滴在试纸上,然后与 标准比色卡对照得到溶液的pH,则该学生测得 的pH(比溶液实际pH)-------------------------- B ( ) A、偏高 B、偏低 C、相等 D、无法判断 5.用pH试纸测试物质酸碱性的强弱,测得的pH 碱性 越强;pH越低,______ 酸性 越强。当 越高,_____ 中 性。 pH=7 时,物质呈 ____
Copyright 2004-2015 版权所有 盗版必究
表1—3 实验过程中物质的颜色变化 试剂 蒸馏水 pH试纸
7 4
紫色石蕊试液
紫色 红色 红色 红色 蓝色
柠檬汁 白醋
盐酸 肥皂水 洗涤剂
4%氢氧化钠溶液
3
1 10
12
13
蓝色
蓝色
不同物质酸碱性的强弱程度不同; 你能得出什么结论? __________________________ pH 试纸显示酸碱性的强弱程度,而酸碱指示剂只能指示酸碱性 。 ___________________________________________
pH 水中加碱 酸中加碱
碱中加水
7 酸中加水 碱中加酸
溶液B
溶液A
0
Copyright 2004-2015 版权所有 盗版必究
水中加酸 加溶液B质量
三、溶液酸碱性的强弱程度
1、测定溶液酸碱性强弱的意义 了解和控制物质的酸碱性,我们需要测定物 质酸碱性的强弱。 2、物质酸碱性强弱的测定 (1)pH值 范围通常在 0 ~14 之间。pH等于7 呈中性。 pH小于7 的呈酸性;pH大于7 的呈碱性。 pH越低,酸性越强;pH越高,碱性越强; (2)测定方法 测定物质酸碱性强弱最常用、最简单的方 法是使用pH试纸。
Copyright 2004-2015 版权所有 盗版必究
1、土壤的酸碱性直接影响农作物的生长。已知 某地区土壤显弱碱性,参照下列作物适宜的PH值, 小麦:5.5~6.5 油菜:5.8~6.7 西瓜:6.0~7.0 甘草:7.2~8.5 从土壤酸碱性考虑,在该地区适 宜种植的作物是----------------------------------( B ) A.西瓜 B.甘草 C.小麦 D.油菜 2.用pH试纸测定溶液酸碱度的正确操作是( C ) A.把试纸浸在待测液中 B.把待测液倒在试纸上 C.用玻璃棒蘸取待测液滴在试纸上 D.把试纸放在待测液上方,让待测液蒸气熏试纸
Copyright 2004-2015 版权所有 盗版必究
我们生活中一些物质的pH
用pH试纸测试稀盐酸、稀硫酸、稀硝酸、醋 酸、碳酸的酸碱度,并比较它们的酸性强弱。
HCl 、H2SO4、HNO3、H2CO3、醋酸
强 酸
Copyright 2004-2015 版权所有 盗版必究
弱 酸
两种pH值不同的溶液相混合,pH值的变化规律:
Copyright 2004-2015 版权所有 盗版必究
紫色石蕊试液; 无色酚酞试液
指 示
剂
酸性溶液 (PH<7)
碱性溶 液 (PH>7)
石蕊试液(紫色) 酚酞试液(无色)
红色
蓝色 红色 不变色 蓝色
无色
红色 不变色
蓝色石蕊试纸
红色石蕊试纸
用紫色石蕊试液测定物质的酸碱性,有什么缺点?
紫色石蕊试液虽然能够测定物质的酸碱性, 但不能反映酸碱性的强弱程度。
Copyright 2004-2015 版权所有 盗版必究
Copyright 2004-2015 版权所有 盗版必究
Copyright 2004-2015 版权所有 盗版必究
用pH试纸测试溶液酸碱性的方法有什么缺点?
用pH试纸测试的方法比较粗略。 精确的测试可使用一种称为酸度计的仪器。
Copyright 2004-2015 版权所有 盗版必究
1.用玻璃棒分别蘸取少许水、柠檬汁、白醋、 盐酸、肥皂水、洗涤剂、4% 氢氧化钠溶液, 滴在 pH 试纸中部,观察试纸的颜色变化。 2.在白色点滴板的空穴(或小试管)里分别 滴入几滴上述样品,再滴加2~3滴紫色石蕊 试液,观察其颜色的变化,并将上述实验结 果都填入表1-3中。
pH越低,酸性越强;pH越高,碱性越强;
Copyright 2004-2015 版权所有 盗版必究
(2)测定方法
测定物质酸碱性强弱最常用、最简单的方 法是使用pH试纸。
pH试纸在酸碱性强 弱不同的溶液里会 显示出不同的颜色。
Copyright 2004-2015 版权所有 盗版必究
pH试纸使用方法:
