2011届高考化学乙醇复习课件
合集下载
高考化学总复习课件乙醇乙酸基本营养物质

解题思路与方法
针对高考化学中常见的题型和考点,总结相应的 解题思路和方法,如有机物合成路线的设计、反 应条件的控制、官能团的转化等,提高学生的解 题效率。
实验操作与现象分析
加强实验操作的训练,熟悉乙醇乙酸等物质的实 验操作要点和注意事项,提高对实验现象的观察 和分析能力。
模拟训练与反思
进行大量的模拟训练,通过做题、反思、总结的 过程,不断提高自己的应试能力和水平。同时, 关注历年高考真题的命题趋势和变化,做到心中 有数。
THANKS
感谢观看
基本营养物质的种类与功能
结合高考真题,详细介绍糖类、油脂、蛋白质等 基本营养物质的种类、结构、性质及功能,加深 学生对营养物质的理解。
有机合成与推断
通过分析高考真题中的有机合成与推断题,总结 常见有机物的合成方法、反应条件及产物推断技 巧,提高学生的解题能力。
备考建议与答题技巧
知识梳理与归纳
建议学生对乙醇乙酸、基本营养物质等相关知识 点进行梳理和归纳,形成完整的知识体系,便于 记忆和提取。
通过特定的试剂或操作可以检验葡萄糖、 淀粉、蛋白质等基本营养物质的存在。
实验现象
葡萄糖与新制氢氧化铜悬浊液共热产生砖 红色沉淀;淀粉遇碘变蓝;蛋白质遇浓硝 酸变黄,灼烧有烧焦羽毛的气味。
06
高考真题解析与备考建议
高考真题解析
1 2 3
乙醇乙酸的性质与反应
通过历年高考真题,深入解析乙醇乙酸的性质、 反应机理以及在实验中的应用,帮助学生掌握相 关知识点。
化。
03
乙醇乙酸与营养物质的相互作用
乙醇和乙酸可以影响营养物质的消化、吸收和代谢,进而影响人体健康
和营养状况。因此,在饮食和营养补充方面需要注意适量饮酒和合理搭
针对高考化学中常见的题型和考点,总结相应的 解题思路和方法,如有机物合成路线的设计、反 应条件的控制、官能团的转化等,提高学生的解 题效率。
实验操作与现象分析
加强实验操作的训练,熟悉乙醇乙酸等物质的实 验操作要点和注意事项,提高对实验现象的观察 和分析能力。
模拟训练与反思
进行大量的模拟训练,通过做题、反思、总结的 过程,不断提高自己的应试能力和水平。同时, 关注历年高考真题的命题趋势和变化,做到心中 有数。
THANKS
感谢观看
基本营养物质的种类与功能
结合高考真题,详细介绍糖类、油脂、蛋白质等 基本营养物质的种类、结构、性质及功能,加深 学生对营养物质的理解。
有机合成与推断
通过分析高考真题中的有机合成与推断题,总结 常见有机物的合成方法、反应条件及产物推断技 巧,提高学生的解题能力。
备考建议与答题技巧
知识梳理与归纳
建议学生对乙醇乙酸、基本营养物质等相关知识 点进行梳理和归纳,形成完整的知识体系,便于 记忆和提取。
通过特定的试剂或操作可以检验葡萄糖、 淀粉、蛋白质等基本营养物质的存在。
实验现象
葡萄糖与新制氢氧化铜悬浊液共热产生砖 红色沉淀;淀粉遇碘变蓝;蛋白质遇浓硝 酸变黄,灼烧有烧焦羽毛的气味。
06
高考真题解析与备考建议
高考真题解析
1 2 3
乙醇乙酸的性质与反应
通过历年高考真题,深入解析乙醇乙酸的性质、 反应机理以及在实验中的应用,帮助学生掌握相 关知识点。
化。
03
乙醇乙酸与营养物质的相互作用
乙醇和乙酸可以影响营养物质的消化、吸收和代谢,进而影响人体健康
和营养状况。因此,在饮食和营养补充方面需要注意适量饮酒和合理搭
优秀课件高三化学复习课件:乙醇 (共16张PPT)

[实验现象] a.铜丝红色→黑色→红色反复变化 b.在试管口可以闻到刺激性气味
H H H H 催化剂 2H C—C—H + O2 2H—C— C—H+2H2O
H O H
H O 乙醛
2CH3CH2OH+O2
Cu
Δபைடு நூலகம்
2CH3—CHO+2H2O
小结: H H | | H—C—C —O—H | | H H 2CH3CH2OH+2Na
一、乙醇的物理性质
乙醇俗称酒精,是一种无色,透明而具 有特殊香味的液体,比水轻,乙醇易挥 发,能跟水以任意比混溶。
二、乙醇的分子结构
若取乙醇2.3g,完全燃烧后生成0.1mol二 氧化碳和2.7g水,且乙醇的蒸气的密度是 相同状况下氢气密度的23倍,求乙醇的 分子式。并对照乙烷的结构式推测乙醇 的结构式。
思考: ①金属钠与乙醇反应生成的气体 产物如何检验? ②金属钠保存在煤油中,煤油的 主要成分是各种烷烃(C12~C16) ,烷烃分子中与碳原子相连的氢 原子能被金属钠置换吗?
③实验证明,1mol乙醇与足量金 属钠反应,生成 0.5mol 氢气,说 明每个乙醇分子中有几个氢原子 被金属钠置换出来?
二、乙醇的分子结构
第二单元 食品中的有机化合物
牧 童 遥 指 杏 花 村
借 问 酒 家 何 处 有 ,
把 酒 问 青 天 !
明 月 几 时 有 ?
小知识 啤酒含酒精3%-5% 葡萄酒含酒精6%-20% 黄酒含酒精8%-15% 白酒含酒精50%-70% (以上均为体积分数) 工业酒精 约含乙醇95%以上(质量分数) 无水酒精 99.5%以上(质量分数) 医用酒精 75%(体积分数)
与金属钠反应
乙醇 (最新课件ppt)
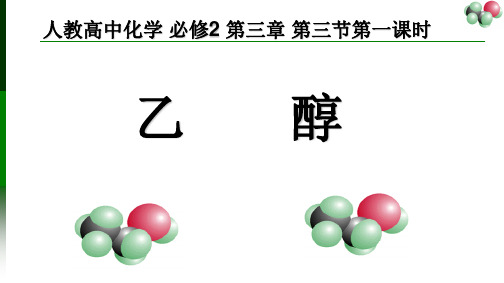
乙醇分子结构探究 1:你认为乙醇的结构式是哪种? 2:请小组交流,设计实验方案,探究 乙醇可能具有的结构式。
1. H2O(H-O-H) Na NaOH + H2↑
2. C 2H6O Na
乙醇分子结构探究
实验3-2 1:用装有钠块的注射器在试剂瓶中抽取约20ml无水乙 醇; 2:针头竖直向下,液体自然流入小烧杯; 3:待液体流尽,倒转注射器,轻轻推动活塞,点燃火 柴靠近针头。
乙醇分子结构探究
钠与水
钠与乙醇
反应现象 实验结论
浮熔游响
钠沉在针筒底部 反应比较缓慢
有气泡产生
钠的密度比水小,比乙醇大, 钠与乙醇的反应不如与水反应剧烈
2C2H5OH + 2Na → 2C2H5ONa+ H2↑ 羟基中的H原子的活泼性:醇<水
乙醇的燃烧反应
点燃
C2H5#43; 3H2O
加入乙醇
重铬酸钾 酸性溶 液
加入乙醇
高锰酸钾 酸性溶液
乙醇的用途
课堂练习
乙醇分子中不同的化学键,如右图:关于乙醇在各种反应 中断裂键的说法不正确的是( ) A.乙醇和钠反应,键①断裂 B.乙醇完全燃烧时键①②断裂 C.在铜催化下和O2反应,键①③断裂 D.在铜催化下和O2反应,键①②断裂
学以致用
乙醇的催化氧化微观分析
氢原子
水
乙醛
乙醇 HH H—C—C—O
-----
HH
-----
碳原子 H
氧原子
HH H—C—C—O
H
乙醇的催化氧化符号表征
2Cu + O2 △ 2CuO
CH3CH2OH + CuO
CH3CHO + Cu +H2O
高二化学乙醇PPT精品课件

• (3)由二甘醇与苯甲酸(
)为原料
可合成二苯甲酸二甘醇酯,可作聚氯乙烯
树脂的增塑剂,请写出该反应的化学方程
式:
____________________________________
____________________________________。
• 【解析】 二甘醇的化学性质与乙二醇相 似,可类比乙二醇的性质分析。
• 提示:根据酯化反应的原理,酸脱羟基、 醇脱氢,则酯水解时也是羧酸部分加羟基、 醇加氢,因此再次到达平衡后仅有乙酸分 子中含有18O。
• 三、酯
• 1.酯的分子结构
• 酸和醇起反应生成的一类有机化合物。其 结构式可用
•
(-R,-R′代表烃基)表示。
• 酯的官能团是“
”。
• 2.酯的物理的 气味。
CH3COOH+NaOH
•
CH3COONa+H2O
• ⑤与盐(如Na2CO3)反应:
CH–3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
– (2)酯化反应
• 乙酸和乙醇发生酯化反应的化学方程式为
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
• [想一想2]向上述乙酸乙酯平衡体系中加入 含有H218O的水,则再次达平衡后含有18O 原子的有机物有哪些?
•
• 灵犀一点:
• 应用以上要点可判断乙醇发生不同类型的 反应时断裂的化学键,也可由断裂的化学 键推断其反应类型,以便于从本质上把握 乙醇的化学性质。
• 【案例1】 早期国内牙膏生产企业使用 甘油作为牙膏中的保湿剂,后来由于国内 甘油供应不足,开始用二甘醇和甘油的混 合物作为牙膏保湿剂。没有它,牙膏就会 很快干裂。二甘醇使用将近20年来,从未 发现问题,但大剂量摄入会损害肾脏。我 国从2009年2月1日开始实施牙膏新标准, 开始禁止使用二甘醇。已知二甘醇的结构 简 式 为 HOCH2CH2OCH2CH2OH , 化 学 性 质与乙二醇相似。请根据你所学知识,完 成下列问题:
乙醇复习PPT演示文稿

点燃
xCO2 + y/2H2O
铜丝放在酒精灯外焰灼 烧,慢慢移向内焰,上下 几次。观察铜丝的变化。
外焰 变黑 内焰 变红 铜丝
实验:把灼热的铜丝插入乙醇中,观察铜丝颜 色变化,并小心闻试管中液体产生的气味。
观看实验演示
铜丝
Δ
插入乙醇 变黑催化氧化
2Cu + O2
△
结构简式:CH3CH2OH 或C2H5OH
三 、乙醇的化学性质
1.与活泼金属反应(如Na、K、Mg、Al等)
①
H H H—C —C—O—H , ①处O—H H 2CH3CH2OH + 2Na 2CH3CH2OH + Mg H
乙醇钠
键断开
2CH3CH2ONa + H2↑ (CH3CH2O)2Mg + H2↑
你知道吗?
在实验室和日常生活中酒精的最常见的 用途是用作燃料和勾兑饮料酒。你能写出 酒精燃烧的化学方程式吗? 你知道酒精在人体内是如何代谢的吗?
2.氧化反应
酒精燃料飞机
酒精火锅
a、燃烧(彻底氧化)
C2H5OH +3O2 → 2CO2+3H2O
点燃
现象:发出淡蓝色火焰,并放出大量热
烃的含氧衍生物燃烧通式: CxHyOz+ (x+y/4-z/2)O2
类比Na与水的反应: H—O—H C2H5—O—H H+ + OH?
观看实验演示
演示:钠与无水酒精的反应
现象:试管中有气体生成,可以燃烧, 烧杯内壁出现水滴,石灰水不变浑浊. 结论:气体是氢气
定 量 实 验 :
实验测定,2.3克(0.05mol )无水酒精可与足量 金属钠反应,收集到标况下0.56 L(0.025mol) 氢气 :n(C2H6O)∶n(H2) =2∶1
xCO2 + y/2H2O
铜丝放在酒精灯外焰灼 烧,慢慢移向内焰,上下 几次。观察铜丝的变化。
外焰 变黑 内焰 变红 铜丝
实验:把灼热的铜丝插入乙醇中,观察铜丝颜 色变化,并小心闻试管中液体产生的气味。
观看实验演示
铜丝
Δ
插入乙醇 变黑催化氧化
2Cu + O2
△
结构简式:CH3CH2OH 或C2H5OH
三 、乙醇的化学性质
1.与活泼金属反应(如Na、K、Mg、Al等)
①
H H H—C —C—O—H , ①处O—H H 2CH3CH2OH + 2Na 2CH3CH2OH + Mg H
乙醇钠
键断开
2CH3CH2ONa + H2↑ (CH3CH2O)2Mg + H2↑
你知道吗?
在实验室和日常生活中酒精的最常见的 用途是用作燃料和勾兑饮料酒。你能写出 酒精燃烧的化学方程式吗? 你知道酒精在人体内是如何代谢的吗?
2.氧化反应
酒精燃料飞机
酒精火锅
a、燃烧(彻底氧化)
C2H5OH +3O2 → 2CO2+3H2O
点燃
现象:发出淡蓝色火焰,并放出大量热
烃的含氧衍生物燃烧通式: CxHyOz+ (x+y/4-z/2)O2
类比Na与水的反应: H—O—H C2H5—O—H H+ + OH?
观看实验演示
演示:钠与无水酒精的反应
现象:试管中有气体生成,可以燃烧, 烧杯内壁出现水滴,石灰水不变浑浊. 结论:气体是氢气
定 量 实 验 :
实验测定,2.3克(0.05mol )无水酒精可与足量 金属钠反应,收集到标况下0.56 L(0.025mol) 氢气 :n(C2H6O)∶n(H2) =2∶1
高中化学乙醇课件

拿轻放,避免撞击和摩擦。
废弃乙醇的处理方法
回收再利用
废弃的乙醇可以通过蒸馏等方法进行回收再利用,减少资 源浪费。
生物降解
乙醇可以被微生物降解,因此可以采用生物处理的方法进 行处理。例如,将废弃乙醇加入活性污泥中,通过微生物 的代谢作用将其降解为无害物质。
燃烧处理
在符合环保要求的前提下,废弃乙醇也可以采用燃烧的方 法进行处理。燃烧产生的热量可以用于发电或供暖等用途 。
储存安全
乙醇应储存在阴凉、通风、干燥 的地方,远离火源和热源。储存 容器应密封良好,防止挥发和泄
漏。
使用安全
在使用乙醇时,应佩戴防护眼镜 、手套等个人防护用品,避免皮 肤接触和吸入其蒸气。操作应在 通风良好的地方进行,避免产生
静电火花。
防火防爆
乙醇易燃易爆,应远离火源和静 电。在搬运和使用过程中,应轻
乙醇的分子结构与化学键
分子结构
乙醇分子由2个碳原子、6个氢原子和1个氧原子组成,呈线 性结构。
化学键
乙醇分子中存在共价键,包括碳-碳键、碳-氢键、碳-氧键和
04
外观与气味
乙醇为无色透明液体,具有特 殊香味。
熔点与沸点
乙醇的熔点为-114.1℃,沸点 为78.3℃。
2. 控制反应温度在约130°C,并加压以 促进反应进行。
步骤
1. 将乙烯通入含有催化剂(如磷酸或硫 酸)的水溶液中。
实验注意事项与操作技巧
注意事项 乙烯气体易燃易爆,操作时应远离火源并注意安全。
催化剂对皮肤有刺激性,需佩戴实验服和护目镜等防护用品。
实验注意事项与操作技巧
• 反应过程中会产生高温和高压,需使用专业设备并严格遵 守操作规程。
05 乙醇对环境的影响及安全 措施
废弃乙醇的处理方法
回收再利用
废弃的乙醇可以通过蒸馏等方法进行回收再利用,减少资 源浪费。
生物降解
乙醇可以被微生物降解,因此可以采用生物处理的方法进 行处理。例如,将废弃乙醇加入活性污泥中,通过微生物 的代谢作用将其降解为无害物质。
燃烧处理
在符合环保要求的前提下,废弃乙醇也可以采用燃烧的方 法进行处理。燃烧产生的热量可以用于发电或供暖等用途 。
储存安全
乙醇应储存在阴凉、通风、干燥 的地方,远离火源和热源。储存 容器应密封良好,防止挥发和泄
漏。
使用安全
在使用乙醇时,应佩戴防护眼镜 、手套等个人防护用品,避免皮 肤接触和吸入其蒸气。操作应在 通风良好的地方进行,避免产生
静电火花。
防火防爆
乙醇易燃易爆,应远离火源和静 电。在搬运和使用过程中,应轻
乙醇的分子结构与化学键
分子结构
乙醇分子由2个碳原子、6个氢原子和1个氧原子组成,呈线 性结构。
化学键
乙醇分子中存在共价键,包括碳-碳键、碳-氢键、碳-氧键和
04
外观与气味
乙醇为无色透明液体,具有特 殊香味。
熔点与沸点
乙醇的熔点为-114.1℃,沸点 为78.3℃。
2. 控制反应温度在约130°C,并加压以 促进反应进行。
步骤
1. 将乙烯通入含有催化剂(如磷酸或硫 酸)的水溶液中。
实验注意事项与操作技巧
注意事项 乙烯气体易燃易爆,操作时应远离火源并注意安全。
催化剂对皮肤有刺激性,需佩戴实验服和护目镜等防护用品。
实验注意事项与操作技巧
• 反应过程中会产生高温和高压,需使用专业设备并严格遵 守操作规程。
05 乙醇对环境的影响及安全 措施
化学课件《乙醇》优秀ppt15 人教课标版

HH
1、与活泼金属的反应
书写:乙醇与钠、钾的反应?
反应的原因?
HH
H CC O H
HH
3、氧化反应
(1)可燃性[演示]
作内燃机燃料
CH3CH2OH+O2 点燃 2CO2+3H2O(液)+1367KJ
CxHyO+(x+y/4-1/2)O2 点燃 xCO2+y/2H2O
(2)催化氧化[演示]
HH H C度小于水
物
理 2、能溶于水,与水按任意比例混合,能溶 性 解多种有机物、无机物 质 3、易挥发,沸点78℃
常 4、饮用酒中含酒精。啤酒的度数指麦芽含量,
识 陈酒特香
与 用
5、75%(V/V)的酒精可用于医疗消毒
途 6、无水酒精的制取:酒精的水溶液蒸馏
强吸水剂
恒沸混合物(95.57%酒精) 蒸馏
OH OH
n C H 2 C H 2 催化剂
OH OH
CH2 O
CH2
CH2 CH2
O + H2O
[ C H 2 C H 2 O ]n + n H 2O
(2)催化氧化
C H 2 C H 2 O2
Cu
OH OH
H C C H +H2O
OO
三、丙三醇
CH2 OH CH OH
1、物性:无色、粘稠、C有H 甜2 味O H的液体。密度: 1.2619g/cm3。沸点:290 ℃。吸湿性。能跟水和乙醇 任意比混合。
94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰·拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉·班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳]
1、与活泼金属的反应
书写:乙醇与钠、钾的反应?
反应的原因?
HH
H CC O H
HH
3、氧化反应
(1)可燃性[演示]
作内燃机燃料
CH3CH2OH+O2 点燃 2CO2+3H2O(液)+1367KJ
CxHyO+(x+y/4-1/2)O2 点燃 xCO2+y/2H2O
(2)催化氧化[演示]
HH H C度小于水
物
理 2、能溶于水,与水按任意比例混合,能溶 性 解多种有机物、无机物 质 3、易挥发,沸点78℃
常 4、饮用酒中含酒精。啤酒的度数指麦芽含量,
识 陈酒特香
与 用
5、75%(V/V)的酒精可用于医疗消毒
途 6、无水酒精的制取:酒精的水溶液蒸馏
强吸水剂
恒沸混合物(95.57%酒精) 蒸馏
OH OH
n C H 2 C H 2 催化剂
OH OH
CH2 O
CH2
CH2 CH2
O + H2O
[ C H 2 C H 2 O ]n + n H 2O
(2)催化氧化
C H 2 C H 2 O2
Cu
OH OH
H C C H +H2O
OO
三、丙三醇
CH2 OH CH OH
1、物性:无色、粘稠、C有H 甜2 味O H的液体。密度: 1.2619g/cm3。沸点:290 ℃。吸湿性。能跟水和乙醇 任意比混合。
94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰·拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉·班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳]
化学课件《乙醇》优秀ppt34(4份打包) 人教课标版1

97.有三个人是我的朋友爱我的人.恨我的人.以及对我冷漠的人。 爱我的人教我温柔;恨我的人教我谨慎;对我冷漠的人教我自立。――[J·E·丁格] 98.过去的事已经一去不复返。聪明的人是考虑现在和未来,根本无暇去想过去的事。――[英国哲学家培根] 99.真正的发现之旅不只是为了寻找全新的景色,也为了拥有全新的眼光。――[马塞尔·普劳斯特] 100.这个世界总是充满美好的事物,然而能看到这些美好事物的人,事实上是少之又少。――[罗丹] 101.称赞不但对人的感情,而且对人的理智也发生巨大的作用,在这种令人愉快的影响之下,我觉得更加聪明了,各种想法,以异常的速度接连涌入我的脑际。――[托尔斯泰] 102.人生过程的景观一直在变化,向前跨进,就看到与初始不同的景观,再上前去,又是另一番新的气候――。[叔本华] 103.为何我们如此汲汲于名利,如果一个人和他的同伴保持不一样的速度,或许他耳中听到的是不同的旋律,让他随他所听到的旋律走,无论快慢或远近。――[梭罗] 104.我们最容易不吝惜的是时间,而我们应该最担心的也是时间;因为没有时间的话,我们在世界上什么也不能做。――[威廉·彭] 105.人类的悲剧,就是想延长自己的寿命。我们往往只憧憬地平线那端的神奇【违禁词,被屏蔽】,而忘了去欣赏今天窗外正在盛开的玫瑰花。――[戴尔·卡内基] 106.休息并非无所事事,夏日炎炎时躺在树底下的草地,听着潺潺的水声,看着飘过的白云,亦非浪费时间。――[约翰·罗伯克] 107.没有人会只因年龄而衰老,我们是因放弃我们的理想而衰老。年龄会使皮肤老化,而放弃热情却会使灵魂老化。――[撒母耳·厄尔曼] 108.快乐和智能的区别在于:自认最快乐的人实际上就是最快乐的,但自认为最明智的人一般而言却是最愚蠢的。――[卡雷贝·C·科尔顿] 109.每个人皆有连自己都不清楚的潜在能力。无论是谁,在千钧一发之际,往往能轻易解决从前认为极不可能解决的事。――[戴尔·卡内基] 110.每天安静地坐十五分钟·倾听你的气息,感觉它,感觉你自己,并且试着什么都不想。――[艾瑞克·佛洛姆] 111.你知道何谓沮丧---就是你用一辈子工夫,在公司或任何领域里往上攀爬,却在抵达最高处的同时,发现自己爬错了墙头。--[坎伯] 112.「伟大」这个名词未必非出现在规模很大的事情不可;生活中微小之处,照样可以伟大。――[布鲁克斯] 113.人生的目的有二:先是获得你想要的;然后是享受你所获得的。只有最明智的人类做到第二点。――[罗根·皮沙尔·史密斯] 114.要经常听.时常想.时时学习,才是真正的生活方式。对任何事既不抱希望,也不肯学习的人,没有生存的资格。
《乙醇》ppt课件14 人教课标版

2、能用来检验酒精中是否含有水的试剂
是( B ) A: CuSO4·5H2O
C: 浓硫酸
B: 无水硫酸铜 D:金属钠
3、乙醇分子中不同的化学键如下图: 当乙醇与钠反应时,① 键断裂;
当乙醇与氧气反应(Cu作催化剂) 时, ①③
键断裂。
⑤ ④ ②① ③
பைடு நூலகம் 光
C H 4 + C l2
C H 3 C l+ H C l
感谢观看,欢迎指导!
C H 3 C H 3
C H 3 C H 2 O H
对比这两组物质性质的差异?
结论:这两组物质性质发生了较大的改变
我们把决定化合物的特殊化学性质的原子或 原子团 叫做官能团
这些有机化合物,从结构上说,都可看成是烃 分子中的氢原子被其它的原子或原子团取代 而衍变成的,因此叫做烃的衍生物
官能团与烃的衍生物的关系
2CH3-CH2 - OH + O2
Cu △
O 2CH3-C-H + 2H2O
1、上述实验中铜丝起到了催化剂 作用 ,乙醇发生
_氧__化____ 反应(填“氧化”和“还原”)
2、根据上述方程式判断反应时乙醇中的化学键变化情
况?
乙醇结构中①、③共价键断裂
3、乙醛能否继续被氧化?
2CH3CHO + O2催化→剂 2CH3COOH
•
7.从自然生态的角度来看,生态平衡 的维护 就是要 维护其 生物物 种的多 样性, 所以维 护社会 和谐的 基础也 就是文 化的多 样性。
•
8.作为最深层次的认同,文化的认同 在维护 民族团 结和和 睦之中 具有最 根本的 作用, 因此就 要建设 好各民 族共同 的精神 家园, 培养中 华民族 的共同 体意识 。
乙醇复习课21页PPT

▪
27、只有把抱怨环境的心情,化为上进的力量,才是成功的保证。——罗曼·罗兰
▪
28、知之者不如好之者,好之者不如乐之者。——孔子
▪
29、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达·芬奇
▪
30、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华
谢谢!
Hale Waihona Puke 21乙醇复习课41、俯仰终宇宙,不乐复何如。 42、夏日长抱饥,寒夜无被眠。 43、不戚戚于贫贱,不汲汲于富贵。 44、欲言无予和,挥杯劝孤影。 45、盛年不重来,一日难再晨。及时 当勉励 ,岁月 不待人 。
▪
26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭
化学课件《乙醇》优秀ppt33(8份打包) 鲁科版

87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯·瑞斯] 88.每个意念都是一场祈祷。――[詹姆士·雷德非]
89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰]
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
④.此反应可检验-OH的存在,可计算分子中 -OH数目
牛刀小试
16g某一元醇与足量的金属钠完全反应,在标
准状况下得到5.6L氢气。该物质可能 A
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
思考 : O—H键最易断裂,那么C—H键和C—O键能否断 裂呢?
2、乙醇的氧化反应 点燃
(1)燃烧 CH3CH2OH+3O2 2 CO2+3 H2O 现象:淡蓝色火焰,放出大量的热。
H2、CO、CH4、乙醇、硫 思考 : 1mol乙醇的耗氧量和哪种烃是一样的?
例:在常压和100oC条件下,把乙醇汽化为蒸 气,然后和乙烯以任意比例混合,混合气体的 体积为VL。将其完全燃烧,需消耗相同条件
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰]
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
④.此反应可检验-OH的存在,可计算分子中 -OH数目
牛刀小试
16g某一元醇与足量的金属钠完全反应,在标
准状况下得到5.6L氢气。该物质可能 A
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
思考 : O—H键最易断裂,那么C—H键和C—O键能否断 裂呢?
2、乙醇的氧化反应 点燃
(1)燃烧 CH3CH2OH+3O2 2 CO2+3 H2O 现象:淡蓝色火焰,放出大量的热。
H2、CO、CH4、乙醇、硫 思考 : 1mol乙醇的耗氧量和哪种烃是一样的?
例:在常压和100oC条件下,把乙醇汽化为蒸 气,然后和乙烯以任意比例混合,混合气体的 体积为VL。将其完全燃烧,需消耗相同条件
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
化学课件《乙醇》优秀ppt35 人教课标版

项目 物质
水
金属钠的变化
气体燃烧现 象
钠浮在水面上,熔 气体在空 成闪亮的小球,四 气中燃 处游动,发出“嘶 烧,发出 嘶”响声。钠球迅速淡蓝色火 变小,最后消失 焰
检验产物
溶液加酚酞后 变红,生成了 碱
乙醇
钠沉于无水酒精 底部,不熔成闪亮 的小球,也不发出 响声,反应缓慢
气体在空 倒扣在火焰上方的干 气中燃烧,燥烧杯内壁有水珠, 发出淡蓝 再向烧杯中加入澄清
溶解性: 跟水以任意比互溶 能够溶解多种无机物和有机物
比较下列分子的异同,分析乙醇分子 的结构:
乙烷
乙醇
水
2、分子结构
化学式: C2H6O HH
结构式:H C—C—O—H 乙醇分子的比例模型
HH 结构简式:CH3CH2OH
或C2H5OH
这一原子团--羟基 写作-OH
练习
1、比较乙烷和乙醇的结构,下列说法错误的 是( B )
A、1:1
B、2:1
C、1:2
D、任意比
85.每一年,我都更加相信生命的浪费是在于:我们没有献出爱,我们没有使用力量,我们表现出自私的谨慎,不去冒险,避开痛苦,也失去了快乐。――[约翰·B·塔布] 86.微笑,昂首阔步,作深呼吸,嘴里哼着歌儿。倘使你不会唱歌,吹吹口哨或用鼻子哼一哼也可。如此一来,你想让自己烦恼都不可能。――[戴尔·卡内基]
6、能证明乙醇分子中有一个羟基的是 (C )
A、乙醇完全燃烧生成CO2和H2O B、乙醇能与水以任意比混溶
C、0.1 mol乙醇与足量钠反应只能生成 0.1 g氢气
D、乙醇在铜催化下可被氧化
7、乙烯和乙醇的混合气体V L,完全燃烧 生成CO2和H2O ,消耗相同状态下的O2 3V L,则混合气体中乙烯和乙醇的体积 比为( D )
化学课件《乙醇》优秀ppt26 人教课标版
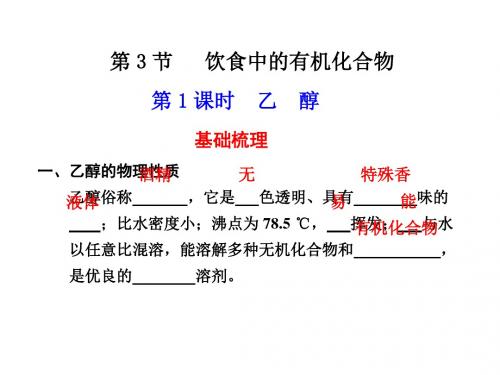
醇的沸点高,钠在乙醇中反应不会熔化成小球,B 不正
确;钠与乙、B、C 三种醇同足量的金属钠完全反应,在相同条件下
产生相同体积的氢气,消耗这三种醇的物质的量之比为
3∶6∶2,则 A、B、C 三种醇分子里羟基数之比为( D )
A.3∶2∶1
B.2∶6∶3
C.3∶1∶2
解析 鉴别物质的主要依据是物质的不同性质。乙醇和苯
在物理性质方面最主要的一点区别就是乙醇可与水以任
意比互溶,而苯不溶于水;虽然 NaOH 溶液不能与乙醇和
苯反应,但乙醇能与 NaOH 溶液混溶,而苯与 NaOH 溶液
混合会分层。化学性质方面,乙醇可以与金属钠反应,而
苯不能与金属钠反应;乙醇、苯都是良好的有机溶剂,能
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
所以铜片的质量不变。常见的能把黑色 CuO 还原为红色的
Cu 的物质有:气体 CO、H2、NH3、固体 C、液体醇类。
4.在焊接铜漆包线的线头时,常先把线头放在火上烧一下, 以除去漆层,并立即在酒精灯中蘸一下,再焊接。为什么 要用酒精灯处理后焊接?试用化学方程式说明 _______________________________________________。
解析 把 C3H7OH 变成 C3H6·H2O 形式后氧的质量分数为 8%,则 H2O 的质量分数为 9%,C3H6 和 C6H12 最简式为 CH2。则碳的质量分数为(1-9%)1124=78%,氢的质量分数:
高考一轮复习乙醇ppt课件

RX+H2O
浓硫酸 1700C R′COOR+H2O
问题4:常见的醇类? 6.常见的醇 甲醇:结构简式: 中毒。
,工业酒精中含甲醇,饮用含甲醇的酒精易引起 CH3OH
甘油
【思维延伸】 烯烃、卤代烃、醇之间的转化关系
有机金三角 “有机金三角”既可以实现有机物类别的转换(官能团的变 换),又可以增长或缩短碳链,增加或减少官能团的数目, 在有机物的合成与推断中有极其重要的作用,是有机化学中 核心转化关系。
变式练习
1.分子式为C4H10O并能与金属钠反应放出氢气的有机化
合物有
()
A.3种 B.4种 C.5种
D.6种
解析:符合分子式为C4H10O的有机物类型可为饱和一元醇或 醚,能与金属钠反应放出H2则为饱和一元醇,故属于饱和一 元醇的同分异构体共有:CH3CH2CH2CH2OH、
答案:B
考点2 醇类的催化氧化和消去反应规律
CH3CH2OH+ HBr―→CH3CH2Br+H2O
反应类型 置换反应 _氧_化__反__应___ _消_去__反__应___ _取_代__反__应___ _取_代__反__应___
断裂的 价键
e
__c_、_e___ _a_、__d___
_e_、__d___ __d___
【例1】 (2010·湖南省长沙市检测题)乙醇分子中不同的化学 键如下 图:
答案:C
共 104 页
22
6.根据下表中烃的衍生物的分子式排列规律,判断空格中的有机物是( )
A.C5H12O2 C.C4H10O2
B.C5H10O D.C5H10O2
答案:D
共 104 页
23
反应的是( )
A.
B.(CH3)2CHOH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
.O H
不显电性 不能独立存在 组成元素相同
﹕﹕
. O ]- [ . H
带一个单位的负电荷 能独立存在
﹕ ﹕
2.下列有关乙醇的物理性质的应用中不正确的是( A ) .下列有关乙醇的物理性质的应用中不正确的是 A.由于乙醇的密度比水小,所以乙醇中的水可以通过 由于乙醇的密度比水小, 由于乙醇的密度比水小 分液的方法除去 B.由于乙醇能够溶解很多有机物和无机物,所以可用 由于乙醇能够溶解很多有机物和无机物, 由于乙醇能够溶解很多有机物和无机物 乙醇提取中药的有效成分 C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾 由于乙醇能够以任意比溶解于水, 由于乙醇能够以任意比溶解于水 兑各种浓度的酒 D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子 由于乙醇容易挥发, 由于乙醇容易挥发 所以才有熟语“ 深”的说法 3.在下列物质中 分别加入金属钠 不能产生氢气的是 A ) 在下列物质中,分别加入金属钠 不能产生氢气的是( 在下列物质中 分别加入金属钠,不能产生氢气的是 A. 苯 B、蒸馏水 、 C、无水酒精 D、75%的酒精 、 、 %
H H A: ① C: ③ B: ② D: ④ H
④
C—C—O—H H
③
H② ①
8.司机是否酒后驾车 可通过对其呼出的气体 司机是否酒后驾车,可通过对其呼出的气体 司机是否酒后驾车 进行检验而查出,所利用的化学反应如下 所利用的化学反应如下: 进行检验而查出 所利用的化学反应如下
2CrO3(红色 红色)+3C2H5OH+3H2SO4 → 红色 Cr2(SO4) 3(绿色 绿色)+3CH3CHO+6H2O 绿色
第三章 有机化合物
第三节
生活中两种常见的有机物
乙醇
1.白日放歌须纵 酒 ,青春作伴好还乡。 白日放歌须纵___,青春作伴好还乡。 白日放歌须纵 2.明月几时有,把___问青天。 明月几时有, 酒 问青天 问青天。 明月几时有 3.借问 酒家 何处有,牧童遥指杏花村。 借问_____何处有 牧童遥指杏花村。 何处有, 借问 4.何以解忧,唯有_____。 何以解忧,唯有 杜康 。 何以解忧
外焰 变黑 内焰 变红 铜丝
实验:把灼热的铜丝插入乙醇中, 实验:把灼热的铜丝插入乙醇中,观察铜丝颜 色变化,并小心闻试管中液体产生的气味。 色变化,并小心闻试管中液体产生的气味。
观看实验演示
铜丝
插入乙醇 变黑 溶液中
又变红 又变红 有刺激性气味
b、催化氧化 、
2Cu + O2 C2H5OH+CuO
据C、H、O元素在有机物中的价键特 大家能否推测乙醇的分子结构? 征,大家能否推测乙醇的分子结构?
A式 式 H H B式 式
① ②
H O H—C H
H C—H H
①
H—C—C—O—H H H
两者间是什么关系? 两者间是什么关系?究竞那一个是乙 醇分子的结构式?要由实验确定。 醇分子的结构式?要由实验确定。
结构简式: 结构简式:CH3CH2OH 或C2H5OH
三 、乙醇的化学性质
1.与活泼金属反应 如Na、K、Mg、Al等) 与活泼金属反应(如 、 、 、 等
①
H H H—C —C—O—H , ①处O—H
键断开
H 2CH3CH2OH + 2Na 2CH3CH2OH + Mg
H 2CH3CH2ONa + H2↑
【问题】
如何由工业酒精制取无水酒精? ⑴ 如何由工业酒精制取无水酒精? 用工业酒精与新制生石灰混合蒸馏, 用工业酒精与新制生石灰混合蒸馏, 可得无水酒精。 可得无水酒精。 如何检验酒精是否含水? ⑵ 如何检验酒精是否含水? 用无水硫酸铜检验
二、乙醇的分子结构
问题探究: 问题探究: 实验测定分子式为 C2H6O , 根
为什么乙醇 能与水 以任意比互溶? 以任意比互溶
小常识
工业酒精 无水酒精 医用酒精 饮用酒 约含乙醇96%以上(质量分数) 约含乙醇96%以上(质量分数) 96 99.5%以上(质量分数) 99.5%以上(质量分数) 以上 75%(体积分数) 75%(体积分数) 视度数而定体积分数。 视度数而定体积分数。 啤酒的度数指麦芽含量
定 量 实 验 :
实验测定,2.3克(0.05mol )无水酒精可与足量 克 实验测定 无水酒精可与足量 金属钠反应,收集到标况下 金属钠反应 收集到标况下0.56 L(0.025mol) 收集到标况下 氢气 :n(C2H6O)∶n(H2) =2∶1 ∶ 实验结论:乙醇的结构式应为_______, 实验结论:乙醇的结构式应为 A式 ,
乙醇钠
(CH3CH2O)2Mg + H2↑
乙醇镁
该反应属于
取代
反应。
想一想:实验现象说明了什么问题 实验现象说明了什么问题? 实验现象说明了什么问题
项目 物质 水 乙醇 金属钠的 变化
浮、游、球、响
气体燃烧 现象
火焰呈淡蓝色
检验产物
反应后的溶液加入酚 变红,说明有碱性 酞,变红 说明有碱性 变红 物质生成 干燥小烧杯有水珠, 干燥小烧杯有水珠, 加入澄清石灰水无 明显变化
练习:试判断下列醇能否发生催化氧化的反应 练习:试判断下列醇能否发生催化氧化的反应: CH3CH2CH2OH (CH3)3CCH2OH CH3CH(OH)CH3
的碳原子上必须有H, 结论:连接-OH的碳原子上必须有 才发 的碳原子上必须有 结论:连接 去氢氧化(催化氧化 催化氧化) 生去氢氧化 催化氧化
一、乙醇的物理性质
颜 气 状 密
H O
H O
色: 无色透明 H H H O 味: 特殊香味 态: 液体 C2H5 度: 比水小 乙醇与水分子间形成氢键 200C时的密度是 时的密度是0.7893g/cm3 时的密度是 挥发性: 易挥发,沸点78℃ 挥发性: 易挥发,沸点 ℃ 溶解性: 溶解性: 跟水以任意比互溶 能够溶解多种无机物和有机物
5、将等质量的铜片在酒精灯上加热后,分别 、将等质量的铜片在酒精灯上加热后, 插入下列溶液中,放置片刻 放置片刻,铜片质量增加的 插入下列溶液中 放置片刻 铜片质量增加的 是c ( ) A.硝酸 B.无水乙醇 C.石灰水 D.盐酸 硝酸 无水乙醇 石灰水 盐酸
6、能用来检验酒精中是否含有水的试剂 是( B ) A: CuSO45H2O B: 无水硫酸铜 C: 浓硫酸 D:金属钠 7:与钠反应时在何处断键( A )
你知道吗? 你知道吗 在实验室和日常生活中酒精的最常见的 用途是用作燃料和勾兑饮料酒。 用途是用作燃料和勾兑饮料酒。你能写出 酒精燃烧的化学方程式吗? 酒精燃烧的化学方程式吗? 你知道酒精在人体内是如何代谢的吗? 你知道酒精在人体内是如何代谢的吗?
2.氧化反பைடு நூலகம் .
酒精燃料飞机
酒精火锅
a、燃烧(彻底氧化) 燃烧(彻底氧化)
C2H5OH +3O2 → 2CO2+3H2O
点燃
现象:发出淡蓝色火焰,并放出大量热 发出淡蓝色火焰,
烃的含氧衍生物燃烧通式: 烃的含氧衍生物燃烧通式 CxHyOz+ (x+y/4-z/2)O2
点燃
xCO2 + y/2H2O
铜丝放在酒精灯外焰灼 铜丝放在酒精灯外焰灼 外焰 慢慢移向内焰 内焰, 烧,慢慢移向内焰,上下 几次。观察铜丝的变化。 几次。观察铜丝的变化。
乙醇 乙醇脱氢酶
微 粒 体 乙 醇 氧 化 系 统
乙醛 CH3CHO 乙醛脱氢酶 (ALDH)
乙
CO2+H2O
判断酒后驾车的方法: 判断酒后驾车的方法:
使驾车人呼出的气体接触 载有经过硫酸酸化处理的强 氧化剂三氧化铬( 氧化剂三氧化铬(Cr03)的 硅胶,如果呼出的气体中含 硅胶, 有乙醇,乙醇会被Cr0 有乙醇,乙醇会被Cr03氧化 成乙醛, 成乙醛,而Cr03会被还原为 硫酸铬。 硫酸铬。三氧化铬和硫酸铬 的颜色不同。 的颜色不同。 CH3CH2OH Cr03(暗红色) 暗红色) CH3CHO Cr2(SO4)3 (绿色) 绿色)
被检测的气体的成分是________,上述反应 被检测的气体的成分是 C2H5OH , 中的氧化剂是_________还原剂是C2H5OH。 还原剂是 ______ 中的氧化剂是 CrO3
问题:如何设计实验确认? 问题:如何设计实验确认?
类比Na与水的反应: 类比Na与水的反应: Na与水的反应 H—O—H C2H5—O—H H+ + OH?
观看实验演示
演示:钠与无水酒精的反应 演示:
现象:试管中有气体生成,可以燃烧, 现象:试管中有气体生成,可以燃烧, 烧杯内壁出现水滴,石灰水不变浑浊. 烧杯内壁出现水滴,石灰水不变浑浊. 结论: 结论:气体是氢气
古往今来无数咏叹酒的诗篇都证明酒是一 种奇特而富有魅力的饮料。 种奇特而富有魅力的饮料。那么同学们可知酒 的主要化学成分是什么?它的分子式如何写? 的主要化学成分是什么?它的分子式如何写? 它有哪些主要性质和用途? 它有哪些主要性质和用途?这节课我们一起来 学习和研究。 学习和研究。
阅读教材,归纳总结乙醇的 物理性质。
△
2CuO
CH CHO+H O+Cu 3 2 乙醛
Cu
总反应方程式: 总反应方程式:
2C2H5OH+O2 2CH3CHO+2H2O
工业上利用该反应制取乙醛
醇氧化机理: 醇氧化机理: 机理
② ①
R1 2 R2—C—O—H + O=O H
③ ①-③位断键 ③
R1
Cu 2 R2—C=O + 2H2 O △ 生成醛或酮 原 理
4、比较乙烷和乙醇的结构,下列说法错误的是( B ) 、比较乙烷和乙醇的结构,下列说法错误的是( A.两个碳原子都以单键相连 两个碳原子都以单键相连 B.分子里都含有6个相同的氢原子 分子里都含有6 分子里都含有 C. 乙醇可以看成是乙烷分子中的一个氢原子被羟基 取代后的产物 D.乙醇与钠反应非常平缓,所以乙醇羟基上 .乙醇与钠反应非常平缓, 的氢原子不如水中的氢原子活泼
