与手性有关的术语
手性与手性分子
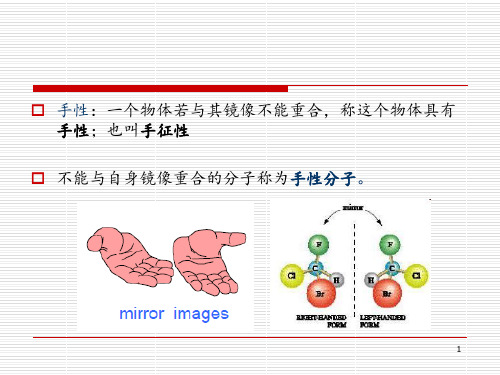
药理活性差异示例
4
生命与手性
作为生命的基本结构单元,氨基酸也有手性之分。也就是说,生 命最基本的东西也有左右之分。
惊人的发现---组成地球生命体的几乎都是左旋氨基酸,而没有右 旋氨基酸。
我们已经发现的氨基酸有20多个种类,除了最简单的甘氨酸以外, 其它氨基酸都有另一种手性对映体! 那么,是不是所有的氨基酸 都是手性的呢?答案是肯定的。
7
检验手性的最好方法就是,让一束偏振光通过它,使偏振光发生 左旋的是左旋氨基酸,反之则是右旋氨基酸。
5
生命与手性
通过这种方法的检验,人们发现了一个令人震惊的事实,那就是除 了少数动物或昆虫的特定器官内含有少量的右旋氨基酸之外,组成 地球生命体的几乎都是左旋氨基酸,而没有右旋氨基酸。
因为人是由左旋氨基酸组成的生命体,它不能很好地代谢右旋分子, 所以食用含有右旋分子的药物就 会成为负担,甚至造成对生命体的 损害。
由于 “反应停”的教训,现在的药物在研制成功后,都要经过严格 的生物活性和毒性试 验,以避免其中所含的另一种手性分子对人体 的危害。
6
ቤተ መጻሕፍቲ ባይዱ 生命与手性
在化学合成中,这两种分子出现的比例是相等的,所以对于医药 公司来说,他们每生产一公斤药物, 还要费尽周折,把另一半分 离出来。如果无法为它们找到使用价值的话,它们就只能是废物。 在环境保护法规日益严厉的时代,这些废品也不能被随意处置, 考虑到可能对公众健康产生的危害,这些工业垃圾的处理也是一 笔不小的开支。
2
药用价值
手性是生命过程的基本特征,构成生命体的有机分子绝大多数都 是手性分子。
人们使用的药物绝大多数具有手性,被称为手性药物。
手性药物和它的“镜像”(即对映体),两者之间在药力、毒性 等方面往往存在差别,有的甚至作用相反。
第二十五章手性药物

10、立体选择性反应和立体专一性反应 (stereoselective reaction, stereospecefic reaction)
▪ 如果一个反应不管反应物的立体化学如何,生成 的产物只有一种立体异构体(或有两种立体异构 体时,其中一种异构体占压倒优势),这样的反 应被称之为立体选择性反应。
▪ 更为广义的不对称合成的定义为,一个反 应,其中底物分子整体中的非手性单元由 反应剂以不等量地生成立体异构产物的途 径转化为手性单元。也就是说,不对称合 成是一个过程,它将潜手性(prochiral) 单元转化为手性单元,使得产生不等量的 立体异构产物。
一个成功的不对称反应的标准
▪ 1)高的对映体过量(e.e); ▪ 2)用于不对称反应的反应剂应易于制备
第二十五章 手性药物
第一节 手性药物概述 第二节 与手性药物有关的几个重要术语 第三节 手性药物的通用制造方法与技术 第四节 手性药物的生物不对称合成原理 第五节 典型手性药物制造技术及工艺
第一节 手性药物概述
手性 是用来表达化本物分子结构不对称性的术 语。如同人的左手和右手不对称,不能相互叠合, 彼此的关系如同实物与镜像。
➢(7)两种对映体中,一种对映体为另一对映体 的竞争性拮抗剂。如左旋异丙肾上腺素是β受体激动
剂,而右旋异丙肾上腺素则为其竞争性拮抗剂,且两者 与β受体的亲和性相当 。
下图,表25-1为一些药物或化合物异构体的不 同药理活性或其它特性 :
药物或化合物名称
构型
沙利度安
R
(thalidomide)
S
氯霉素
▪ 不对称合成常常也被称之为手性合成。最 初的定义为,不对称合成是一个用纯手性 试剂通过非手性底物的反应形成光学活性 化合物(optically active compound)的 过程,即从一个具有对称构造的化合物产 生光学活性物质的反应过程。
有机化学基础知识点整理手性和对映体的概念

有机化学基础知识点整理手性和对映体的概念手性和对映体是有机化学中重要的概念和基础知识点。
本文将对手性和对映体进行整理和讲解,以帮助读者更好地理解和掌握这一概念。
一、手性的定义和特点在化学中,手性是指具有非对称性质的分子或化合物。
一个手性分子无法与其镜像重叠,就像我们的左右手无法完全重叠一样。
手性分子有两个重要特点:1. 非对称性:手性分子的结构中存在至少一个不对称碳原子,也称为手性碳原子。
这个碳原子上连接的四个基团必须是不同的,不能相互交换。
2. 手性中心:由于手性碳原子的存在,手性分子的结构中存在一个或多个手性中心。
手性中心是指一个原子与四个不同基团连接而成的立体中心。
二、对映体的概念和特点对映体是由手性分子通过镜面对称操作而得到的立体异构体。
对映体之间具有以下特点:1. 镜像对称:对映体的结构在三维空间中是非重叠的镜像关系,就像左右手一样。
它们有相同的分子式和结构式,但在物理性质上有着明显的差异。
2. 光学活性:对映体对平面偏振光有旋光作用,这是由于对映体的结构不对称导致的。
一种对映体可以将偏振光偏转为左旋光,而另一种对映体则将其偏转为右旋光。
三、手性和对映体的重要性手性和对映体的研究对于理解和掌握有机化学的许多领域都具有重要意义:1. 药物研发:手性药物的合成和分离是当今药物研发的重要问题之一。
对映体之间的药理活性差异可能导致一种对映体产生疗效,而另一种对映体则可能产生副作用或无效。
2. 生命科学:生物体内的很多分子都是手性的,包括氨基酸、脂肪酸、糖类等。
对映体对生物体的生物活性和代谢途径有着显著的影响。
3. 光学材料:手性分子的存在使得光学材料能够对光的偏振状态进行调节,可以应用于光学元件、液晶显示器等领域。
4. 催化剂设计:手性催化剂的使用可以提高有机反应的催化效率和选择性。
对映体的选择对于催化剂的活性和特异性具有重要影响。
四、手性和对映体的应用举例1. 左旋与右旋乳酸:乳酸是一种常见的有机酸,存在两种对映体:左旋乳酸和右旋乳酸。
名词解释手性

名词解释手性1. 制药工艺学(Pharmaceutical Technology):是研究各类药物生产制备的一门学科;它是药物研究、开发和生产中的重要组成部分,它是研究、设计和选择最安全、最经济、最简便和先进的药物工业生产途径和方法的一门学科。
2.化学制药工艺学:化学制药工艺学是药物研究、开发和生产中的重要组成部分,是研究药物的合成路线、合成原理、工业生产过程及实现生产最优化的一般途径和方法。
它是研究、设计和选择最安全、最经济、最简便和先进的药物工业生产途径和方法的一门学科。
3.制剂工艺学:是综合应用药剂学、物理化学、药物化学、应用化学、药理学、生物学等学科的知识,研究药物剂型的生产工艺、设备及质量控制,按照不同的临床医疗要求,设计、制造不同的药物剂型。
4.新药研发:新药研究与开发应包括新药从实验室研究到生产上市,扩大临床应用的整个过程,是制药工艺学研究的一个基本内容。
制药工业是一个以新药研究与开发为基础的工业。
5.清洁技术:制药工业中的清洁技术就是用化学原理和工程技术来减少或消除造成环境污染的有害原辅材料、催化剂、溶剂、副产物;设计并采用更有效、更安全、对环境无害的生产工艺和技术。
其主要研究内容有:(1)原料的绿色化(2)催化剂或溶剂的绿色化(3)化学反应绿色化(4)研究新合成方法和新工艺路线。
1.全合成制药:是指由化学结构简单的化工产品为起始原料经过一系列化学合成反应和物理处理过程制得的药物。
由化学全合成工艺生产的药物称为全合成药物。
2.半合成制药:是指由具有一定基本结构的天然产物经化学结构改造和物理处理过程制得的药物。
这些天然产物可以是从天然原料中提取或通过生物合成途径制备。
3.手性制药:具有手性分子的药物4.药物的工艺路线:具有工业生产价值的合成途径,称为药物的工艺路线或技术路线。
5. 倒推法或逆向合成分析(retrosynthesisanalysis):从药物分子的化学结构出发,将其化学合成过程一步一步逆向推导进行寻源的思考方法称为追溯求源法,又称倒推法、逆合成分析法。
第二讲 手性概述

① 对称面 (m) 如果一个分子的所有原子都处在一个平面 上,或者有一个能把分子分为物体和镜像两部 分的平面,该平面称为这个分子的对称面。 如果一个分子能够被一个平面分割成两个 部分,而这两个部分刚好互为实物与镜像关系 ,那么这个平面即为此分子的对称平面,该分 子则具有平面对称因素,这就是一个对称分子 ,它和它的镜像能够彼此重叠,所以分子是非 手性分子。
非对映异构体(diastereoisomers) 非对映异构体 (diastereoisomers) 是指分子具有二个 或多个手性中心,并且分子间为非镜像的立体异构体。 具有一个以上手性中心的化合物存在许多对对映异构 体或非对映异构体。非对映体被定义为具有相同化学组成 ,但不是镜像,在分子中的一个或多个不对称中心具有不 同的构型而彼此不同的物质。非对映异构体之间不呈镜面 对称,具有不同的物理性质,其混合物能够被分离。例如 ,2-氯-3-羟基丁烷,可以画出四个不同的结构:二对对映体 化合物,四个非对映体化合物。
D和L异构体 D和L用于标记分子的绝对构型,传统上常用于标记生化 过程中的重要化合物。它们本身并不具有专一性并且也不 能确定旋光的方向。D/L标记需要参照化合物,一般按照与 D-或L-甘油醛的绝对构型的实验化学关联而指认。D/L标记 常被用来描述氨基酸或糖。此外,现在已经很少使用 D 和 L 标记。也常用小写的 d 和 l 来表示,它仅仅与偏振光的旋转 方向有关。 (+)- 甘油醛的构型被指定为 D 构型, (-)- 甘油醛为 L 构型 ,其他分子构型与(+)-甘油醛构型相似的标记为D,与(-)-甘 油醛相似的标记为L。 (Fischer惯例)
构象异构体 如果两个或两个以上的化合物通过 σ 键的旋转而相关, 则互称为构象异构体。构象异构体为立体异构体的一种。 碳是四价原子,能够形成四根共价键。一旦形成键,这 些键将指向四面体的四角。然而,一旦存在一个以上的四面 体中心,这些四面体之间将有一系列不同的空间排列方式。 举一个简单的例子,乙烷具有两个sp3碳中心。随着碳-碳键的 旋转能够画出多种结构,其中有两种极限式:其中一种结构式 中所有的键相互重叠(重叠式),另一种结构式中所有的键相 互离得尽可能地远(交叉式) 。
有机化学基础知识手性与不对称合成

有机化学基础知识手性与不对称合成有机化学基础知识:手性与不对称合成在有机化学中,手性和不对称合成是两个重要的概念。
手性是指分子或化合物具有非重叠的镜像对称结构,分为左旋(S)和右旋(R)两种构型。
不对称合成则是指通过反应使得手性化合物生成的过程。
手性与不对称合成的重要性在于它们在生物学、药物学和有机合成领域具有广泛应用。
手性分子在生物体中扮演重要的角色,药物分子的手性性质直接影响其在体内的活性和毒性。
此外,许多有机合成过程中需要获得高立体选择性的产物,这就需要使用不对称合成方法。
一、手性的定义与属性手性(chirality)是指分子或化合物不能与其镜像完全重合的性质。
简单来说,手性分子就像是左右手,无法完全重叠,这是由于手性分子的立体结构具有非对称性。
手性的性质包括以下几个方面:1. 手性分子无旋转轴或镜面反射面:旋转或镜面反射一个手性分子,无法使其和源分子完全重合,这就是左旋和右旋构型的来源。
2. 左旋(S)和右旋(R)构型:对于手性分子,以手的方式分别沿顺时针和逆时针方向围绕分子中心生成立体结构,可得到左旋(S)和右旋(R)构型,确定手性分子的构型是有机化学的重要内容。
3. 光学活性:左旋和右旋构型的手性分子之间可以通过手性光学活性来区分,其中旋光(optical rotation)是一种常用的手性分析方法。
二、手性分子的来源手性分子的来源多种多样,包括以下几种常见的方式:1. 手性衍生物:通过对不对称化合物的反应进行处理,引入手性基团,从而生成手性产物。
2. 手性诱导:在合成过程中,通过使用手性诱导剂,使得产物具有手性结构。
3. 手性模板:在有机合成中,通过使用手性模板,使得反应生成具有手性结构的产物。
4. 生物来源:许多生物体内产生的分子都是手性的,因此通过利用生物体提取或合成方式,可以获得手性分子。
三、不对称合成方法不对称合成是指通过有选择性地控制反应条件、底物结构或合成步骤,使得手性化合物生成的合成方法。
有机化学中的手性概念与立体异构体

有机化学中的手性概念与立体异构体有机化学是研究有机物结构、合成和性质的科学领域。
在有机化学中,手性(chirality)是一个重要的概念,涉及到分子的空间结构和立体异构体的存在。
本文将介绍手性的定义,手性的表现形式以及立体异构体的种类与分类。
一、手性的定义手性是指物体不与其镜像完全重合的性质。
也就是说,一个手性分子的镜像结构与原分子并不相同。
这种不对称性在有机化学中非常常见,并且对于分子的性质和功能有着重要的影响。
二、手性的表现形式手性可以通过不同的方式表现出来,其中最常见的是手性中心、手性轴和手性面。
1. 手性中心手性中心是指分子中一个碳原子上的四个取代基围绕着该碳原子排列成一个四面体的结构。
当这四个取代基中的任意两个取代基不能通过旋转互相重合时,就存在手性中心。
2. 手性轴手性轴是指分子中存在着旋转对称性,但在沿着该旋转轴方向的一侧存在着不同的官能团取代的情况。
这种情况下,分子仍然是手性的。
3. 手性面手性面是指分子中的一个平面,该平面上的取代基不能通过翻转互相重合。
例如,苯环上的取代基就可以形成手性面。
三、立体异构体的种类与分类立体异构体是指在空间结构上相互非重合、形状不同的同分异构体。
根据手性的不同表现形式,立体异构体可以分为两类:对映异构体和旋光异构体。
1. 对映异构体对映异构体是指存在手性中心的分子,其镜像结构与原结构不完全重合。
两个对映异构体是非重叠的、无法相互转化的,它们构成了一对对映异构体。
2. 旋光异构体旋光异构体是指分子对极性光的旋光性质呈现不同的现象。
旋光异构体包括旋光异构体和旋光体系。
旋光异构体在化学反应中的行为和性质常常有所不同。
根据旋光性质的不同,旋光异构体可以分为两类:左旋异构体和右旋异构体。
这两种异构体的旋光度(旋光光度的绝对值)和旋光方向都是不同的。
四、手性在生物体中的重要性手性在生物体中具有重要的作用和意义。
一方面,生物体内的许多分子都是手性的,比如葡萄糖、氨基酸等。
与手性相关的术语

(1)D/L和d/la. D或L指分子的绝对构型,按照与参照化合物D—或L—甘油醛的绝对构型并通过实验化学关联来指定,常用于氨基酸或碳水化合物,但最好使用R和S来表示。
b. d或l右旋或左旋,按照实验测定,化合物能将单色平面偏振光的平面向顺时针方向或向逆时针力向旋转向定。
应指出的是,化合物的右旋和左旋与该化合物的绝对构型并无直接的联系。
(2)立体异构体、非对映异构体和对映体a.立体异构体(stereoisomers) 其分子由相同数日和相同类型的原子组成,是具有相同的连接方式但构型不同的化合物。
b.非对映异构体(diastereoisomers)对于分子中具有两个或多个小对称中心,并且其分子互相不为实物和镜像的立体异构体。
例如,D—赤藓糖和D—苏力糖。
常简称为“非对映体”。
非对映体也在立体异构体的范畴之内。
c.对映体(enantiomers) 其分子互相为不可重合的实物和镜像的立体异构体。
(3)对映体过量和对映选择性a.对映体过量(enantiomeric excess,e.e.)在两个对映体(El和E2)的混合物中,假定El的量大于E2,则对映体El过量的百分数称为El的对映体过量,以e.e.表示。
e.e. =[(El - E2 )/(El + E2 )]×100%b.对映选择性(enatioselectivity)一个化学反应中,产生的某一对映体多于其他对映体的程度。
(4)光学活性、光学异构体和光学纯度a.光学活性(optical activity) 实验观察到的化合物将单色平面偏振光的平面向观察者的右边或左边旋转的性质。
b.光学异构体(optical isomers)对映体的同义词,但现在已不常用,因为有一些对映体在某些偏振光波长下并无光学活性。
c.光学纯度(optical purity)根据实验测定的旋光度,在两个对映异构体的混合物中,一个对映体所占的百分数。
现在常用对映体纯度来代替。
有机化学基础知识分子的立体化学

有机化学基础知识分子的立体化学有机化学是研究含碳的化合物的分子结构、性质、合成、反应以及它们在生物体系中的作用的科学。
其中,分子的立体化学是有机化学中至关重要的一部分。
本文将介绍有机化学中分子的立体化学基础知识,包括手性,立体异构体及其命名以及手性分子的光学活性。
一、手性分子的手性是指其镜像不能重合的特性。
由于碳原子可以形成四个互不相同的键,大部分有机化合物都可以具有手性。
手性分子包括两种类型:手性中心和轴手性。
1. 手性中心手性中心是指分子中的一个碳原子,它与四个不同的基团连接。
手性中心的碳原子通常以S(拉丁语 sinister )和R(拉丁语 rectus)表示,分别代表左旋和右旋的空间构型。
2. 轴手性轴手性是指分子中存在一个对称轴,该对称轴可以将分子分为两个不可重合的镜像体。
轴手性是由于分子的非完全对称所导致的,在立体异构体中较为常见。
二、立体异构体及其命名立体异构体是指分子在空间排列上存在不同的构型,从而导致其化学性质和生物活性的差异。
立体异构体包括构象异构体和对映异构体。
1. 构象异构体构象异构体是指分子在空间上能够互相转换,但又不能通过化学反应相互转化的异构体。
最常见的构象异构体是旋转受限的双键环状化合物,如环烯烃和环烷烃。
2. 对映异构体对映异构体是指分子的镜像体,在化学和物理性质上没有差异,但与其他手性物质的相互作用不同。
对映异构体是由于分子的手性中心或轴手性所引起的。
对映异构体的命名通常使用R/S命名法或者D/L命名法,其中R/S命名法适用于手性中心,而D/L命名法适用于糖类和氨基酸等化合物。
这些方法可以准确地描述分子在空间中的立体排列。
三、手性分子的光学活性手性分子的光学活性是指它们对平面偏振光有选择性地旋转偏振面的性质。
手性分子旋光的方向可以是顺时针旋光(右旋)或逆时针旋光(左旋),分别用(+)和(-)表示。
对于含有手性中心的分子,不对称的环境可以导致光学活性。
手性分子的光学活性在药物、农药、香料等领域具有重要的应用价值。
第二讲 手性概述

手性与人类健康: “反应停”悲剧
O N NH O O O
(R)-thalidomide
O O N H O N O
(S)-thalidomide
反应停: 五十年恩怨
沙利度胺的S-异构体可导致严重的致畸性
1957年~1962年,造成数 万名婴儿严重畸形。 进一步研究表明,其致畸 作用是由沙利度胺其中的 一个异构体(S-异构体) 引起的,而R-构型即使大 剂量使用,也不会引起致 畸作用。
有机分子手征性的发现
1848年,法国化学家巴斯顿 (L.Pasteur, 1822~1895) 发现酒石酸两种不同的存在 形式: 左旋酒石酸 右旋酒石酸
图:巴斯顿把酒石酸晶体分 开成两个镜像异构体
1966 年 , 凯 恩 (R.S.Cahn) 、 英 戈 德 (C.K.Ingold) 和普雷洛格 (V.Prelog) 三人认为引 起旋光性的唯一原因,是 “分子本身的结构和它 的镜像不能重合”,于是将不对称和非对称分子 一律称为手性分子(chiral molecule)。由此,他 们建议把分子本身和它的镜像不能重合的分子, 定义为手性分子.把不对称碳原子,改称为手性 碳原子,并提出了规定手性碳原子绝对构型的新 方法R/S构型规定法。这些建议已被国际纯粹与应 用化学联合会(IUPAC)所接受,为世界化学界所公 认。这样,结构和旋光性间的关系可简化为:手性 分子呈现旋光性,非手性分子则不呈现旋光性。
手性与生命现象:氨基酸、糖、蛋白质、DNA都是手性的;
手性与人类健康:“反应停”事件与FDA手性药物指导原 则,药物中近50%具有手性,开发中的有2/3以上是手性的; 手性与环境:手性技术与手性产品符合绿色化学原则; 手性与材料和信息科学:手性液晶显示、手性传感、手性 分离等; 手性技术与国民经济:巨大的手性药物和手性化学品市场, 2003年>1600亿美元,预计2010>2000亿美元。国内手性化 学品、手性药物及原料药销售额估计在 200 亿,仅占医药 工业销售额2751亿的10%左右。 手性技术壁垒:手性药物安全规则与加入 WTO 后手性技术 的知识产权问题。
手性概念的提出

手性概念的提出
手性概念最早是由法国科学家路易斯. 帕斯图尔于1824年提出的。
他在研究结晶物质时发现,有些结晶物质的镜像能够使得左右对称,而有些则不能。
他将这种现象称为“手性”(chirality),并提出了手性分子的概念。
帕斯图尔通过观察结晶物质在偏光下的旋光性质,发现它们能够使光线发生旋光现象,而其镜像物质则会产生相反方向的旋光。
这种旋光性质在二十世纪初被利用于判断化学物质的结构和性质。
后来,随着化学研究的深入,人们发现很多化合物都是手性的,例如氨基酸、糖类等有机分子。
这些手性分子具有非对称的结构,无法与其镜像重叠。
由于手性分子的存在,使得化学研究和应用领域出现了许多新的问题和挑战。
手性概念的提出对化学、生物学、医药和材料科学等领域有着重要影响。
在生物学中,手性分子在生物体内的代谢、药物作用、蛋白质结构等方面起着关键作用。
在医药领域,手性药物的研究和合成也成为重要的研究方向。
在材料科学中,手性分子的配位或组装能够产生新的功能材料。
总的来说,手性概念的引入为许多领域的研究提供了新的角度和思路,对于理解和利用手性分子的特殊性质具有重要意义。
什么叫手性药物_手性药物是什么

什么叫手性药物_手性药物是什么手性药物可能你连听都没听过,更不可能知道什么叫手性药物,那么你知道什么叫手性药物吗?下面是为你整理的什么叫手性药物的相关内容,希望对你有用!手性药物的概念手性(Chirality)是自然界的本质属性之一。
作为生命活动重要基础的生物大分子,如蛋白质、多糖、核酸和酶等,几乎全是手性的,这些小分子在体内往往具有重要生理功能。
目前所用的药物多为低于50个原子组成的有机小分子,很大一部分也具有手性,他们的药理作用是通过与体内大分子之间严格手性匹配与分子识别实现的。
含手性因素的的化学药物的对映体在人体内的药理活性、代谢过程及毒性存在显著的差异。
当前手性药物的研究已成为国际新药研究的主要方向之一。
绝大多数的药物由手性分子构成,两种手性分子可能具有明显不同的生物活性。
药物分子必须与受体(起反应的物质)分子几何结构匹配,才能起到应有的药效,就如右手只能带右手套一样。
因此,往往两种异构体中仅有一种是有效的,另一种无效甚至有害。
手性药物的合成方法从天然产物中提取是获得手性药物的最基本方法之一但天然的原料是有限的不能够获得大量的低价药物。
外消旋体拆分法的化学拆分需要选择适当的溶剂,更为关键的是找出一个很合适的拆分剂是这是十分困难的。
对外消旋底物进行不对称水解拆分制备手性化合物缺点是必需先合成外消旋目标产物,拆分的最高收率不会超过50%。
酶催化手性药物合成与化学法相比,微生物酶转化法的立体选择性强,反应条件温和,操作简便,成本较低,污染少,且能完成一些在化学反应中难以进行的反应。
然而,有些生物催化剂价格较高,对底物的适用有一定的局限性。
具有高区域和立体选择性、反应条件温和、环境友好的特点。
化学合成的前三类方法都要使用化学计量的手性物质。
虽然在某些情况他们可以回收重新使用。
但试剂价格昂贵不宜使用于生产中等价格的大众化手性药物。
不对称催化法,它具有手性增殖、高对映选择性、经济,易于实现工收化的优点,是最有希望、最有前途的合成手性性药物的方法。
医海泛舟:手性·药物的手性·手性药物

医海泛舟:手性·药物的手性·手性药物手性是指实物与其镜像的关系,如同人的两只手一样,左手的镜像是右手,二者不能重合。
这种实物与其镜像不能重合的性质就叫做手性。
如果一种药物具有手性因素,该药物就是手性药物。
目前,世界上使用的化学药物总数大约有1900种,手性药物占50%以上。
在200种常见的临床药物中,手性药物多达114种。
随着手性药物在生命科学领域的广泛应用,手性药物已成为国际医药研究的重要方向。
上世纪70年代发展起来的手性催化技术是获得手性药物最先进的方法,但由于构成手性催化剂的手性配体很难合成、严重的毒副作用、繁复的生产过程和高昂的生产费用制约了其中一些药品的推广应用,因而制约了它的进一步发展。
因而在简化生产工艺、降低生产成本方面,中国工程院院士、教授张生勇及其团队研究成果取得重大突破。
1 手性手性是自然界的普遍特征。
构成自然界物质的一些手性分子虽然从原子组成来看是一摸一样,但其空间结构完全不同,他们构成了实物和镜像的关系,也可比喻成左右手的关系,所以叫做手性分子。
在生命的产生和演变过程中,自然界往往对一种手性有所偏爱,如自然界中,糖的构型为D-构型,氨基酸为L-构型,蛋白质和DNA的螺旋构象又都是右旋的,等等。
因此,分子手性在自然界生命活动中起着极为重要的作用。
人类的生命本身就依赖于手性识别。
如人们对L一氨基酸和D一糖类能够消化吸收,而其对映体对人类没有营养价值,或有副作用。
人们对手性的研究可以追溯到1874年第一位化学诺贝尔奖获得者Jhvan。
当时他就提出了具有革命性的理论化学分子为三维结构,一些化合物存在两种构像,且两者互为镜像。
1886年,科学家报道了氨基酸类对映体引起人们味赏感受的差别。
1956年Pfeifer根据对映体之间药理活性的差异,总结出:一个药物的有效剂量越低,光学异构体之间药理活性的差异就越大。
即在光学构体中,活性高的异构体与活性低的异构体之间活性比例越大,作用于某一受体或酶的专一性越高,作为一个药物它的有效剂量就越低。
有机化学基础知识点整理手性与对映体

有机化学基础知识点整理手性与对映体手性与对映体是有机化学中的重要概念。
在分子结构中,手性指的是分子或化合物具有不对称碳原子,并且这个不对称碳原子周围分子的排列方式有两种镜像对称的方式。
这种情况下,分子会存在两个非重叠的镜像体,分别被称为对映体。
对映体在空间结构上相互镜像对应,但无法通过旋转、挪动等操作使其完全重合。
本文将对手性与对映体的概念、性质、分类以及应用进行详细介绍。
一、手性的概念和性质1.1 手性的定义手性是指分子或化合物具有不对称碳原子,使得其周围的分子排列方式存在两种非重叠的镜像对称的情况。
1.2 手性分子的特点手性分子具有以下特点:(1)无法通过旋转、挪动等操作使其与其镜像体完全重合;(2)具有旋光性,即对旋光的导致和响应;(3)对手性诱导拆分剂等具有选择性。
二、对映体的定义和性质2.1 对映体的定义对映体是指手性分子在空间结构上的两个非重叠镜像体。
2.2 对映体的性质对映体具有以下性质和特点:(1)相互间无法通过旋转、挪动等操作使其重合;(2)具有相同的物理化学性质,如沸点、熔点等;(3)对旋光性相反,并且对不同手性构型的有光学活性物质旋光角度相等、但方向相反。
三、手性的分类根据手性分子或化合物的不对称碳原子的数目,手性分为单手性和多手性。
3.1 单手性单手性是指手性分子中只有一个不对称碳原子,因而只有一对对映体。
3.2 多手性多手性是指手性分子中含有多个不对称碳原子,因而拥有多对对映体。
四、手性的应用手性分子及对映体在有机合成、药物研发、生物活性研究等领域具有重要应用价值。
4.1 有机合成手性分子的对映体具有不同的化学性质,可以用作手性诱导剂、手性催化剂、手性配体等,用于合成具有高度立体选择性的化合物。
4.2 药物研发手性药物存在于临床实践中的广泛应用。
对映体间的差异可能导致不同的药理活性、毒理学效应和药代动力学现象,因此手性药物的合成、分离和评价具有重要意义。
4.3 生物活性研究手性分子在生物活性研究中具有重要作用,手性分子的生物活性通常是由其特定的构象和立体结构决定的。
奇妙的手性——关于化学手性的探究

奇妙的手性——关于化学手性的探究一、引言在我们的日常生活中,有很多物质都是手性的,包括药物、食品添加剂、香精等。
虽然这些物质的分子结构几乎相同,但它们也许具有截然不同的生理和化学性质。
原因在于分子的手性(chirality)不同。
那么什么是手性?手性分子又为什么会具有这样的特性呢?二、什么是手性?手性,英语为Chirality,通常也称偏光性。
手性是指分子具有非对称性,这是由于分子结构中所存在的一个空间反演中心点的缺失,使得分子的立体中心结构无法通过旋转或平移与其镜像平面完全重合。
通俗地讲,手性就是左右称谓不同的分子。
例如我们平常常使用的左右手。
我们的左右手形状几乎相同,但是掌心的方向却相反。
无论怎么旋转或是平移,都无法使我们的左右手完全重合。
三、无手性分子和手性分子有什么区别既然手性分子具有非对称性,那么无手性分子和手性分子又有什么区别呢?相较于无手性分子,具有手性的分子具有更为复杂和多样的空间构型。
具体而言,手性分子的图像无法完全与其对称反演结构重合,且仅有一种立体异构体是生物活性的。
以氨基酸为例。
氨基酸分子中的α碳原子中有一个手性中心,它是由于α碳原子上的四个取代基而产生的。
如果只将氨基酸的桥头状部分旋转180度,即相当于进行了一次平面镜对称与旋转,从而与原来的氨基酸的图像完全重合,这个图像并不是氨基酸的对映异构体。
而这个对映异构体与某些生物分子作用时,却很难发挥正常的作用,甚至还可能对身体产生副作用。
实际上,手性分子的生理和化学性质是不同于其对映异构体的。
例如天然产物左旋丙氨酸和右旋丙氨酸所具有的生理作用不同。
这些特性促使手性分子在药物、香精、民生、化工等领域应用广泛。
四、手性的划分手性分子的命名一般采用"L"和"D"两种方式,它们是由于早期研究人员发现葡萄糖的旋光性质导致的。
对于旋转平面极化光(旋光)的方向,旋光方向向左则称为 "L",向右则称为 "D"。
手性分子专业知识讲座

Cl Cl
HOOC C消旋体旳拆分 (1)机械拆分法 (3)选择吸附拆分法 (5)化学拆分法
(2)微生物拆分法 (4)诱导结晶拆分法
小结: 1、了解手性、旋光性、对映异构旳概念 2、熟练掌握构型旳标识措施 3、熟练掌握构型式旳透视式和菲舍尔投影式之间旳 相互转化。
注:
①但凡手性分子,都有旋光性; 非手性分子无旋光性
②一对对映体对偏振光旳作用恰好相反,一种使偏 振光左旋,一种使之右旋,旋光度数值相等。
3)旋光性旳测量 用旋光仪进行测量。
A
A
B
D'
C
D
B'
A'
A'
起偏镜
乳酸
旋光性物质
盛液管
α
目镜(亮)
检偏镜
4)比旋光度
t
l C
α旋光仪中读到旳旋光度; l 盛液管旳长度;(dm) C 溶液旳浓度;(g/ml)
H
H
Br
Br
H
H
CH3 Cl
CH3 Cl CH3
H
Cl
Br H
CH3 CH3
Br H
CH3
CCHH33
H
Br
Cl
H
CH3
五、含一种手性碳原子化合物旳对映异构
1、手性碳:常用“*”表达
CH3C*HCOOH OH
具有一种手性碳原子旳化合物,一定是手性分子。 有一对对映体,其中一种是左旋,一种是右旋。 如乳酸:
作业:1、 (2) (4) (6);2 、(2) (5) ; 4、 (2) (4) ;7
对映体非对映体 对映体
分子中具有n个手性碳旳化合物,最多有 2n 个对映异构 体,有2n-1对对映异构体。
与手性有关chiralityrsdldl旋光

与手性有关chirality r s d l d l 旋光与手性有关:chirality r s d l d l + - 旋光同分异构enantiomorph achiral amphichiral_一向ishoming000手性分子,是化学中结构上镜像对称而又不能完全重合的分子。
碳原子在形成有机分子的时候,4个原子或基团可以通过4根共价键形成三维的空间结构。
由于相连的原子或基团不同,它会形成两种分子结构。
这两种分子拥有完全一样的物理、化学性质。
但是从分子的组成形状来看,它们依然是两种分子。
这种情形像是镜子里和镜子外的物体那样,看上去互为对应。
由于是三维结构,它们不管怎样旋转都不会重合,就像左手和右手那样,称这两种分子具有手性,又叫手性分子。
因此这两种分子互为同分异构体,这种异构的形式成为手性异构,有R型和S型两类。
手性>同分异构 enantiomorph achiral amphichiral" TITLE="与手性有关:chirality R S D L d l + - 旋光同分异构 enantiomorph achiral amphichiral" />手性(chirality)一词源于希腊语词干“手”χειρ (ch[e]ir~),在多种学科中表示一种重要的对称特点。
如果某物体与其镜像不同,则其被称为“手性的”,且其镜像是不能与原物体重合的,就如同左手和右手互为镜像而无法叠合。
手性物体与其镜像被称为对映体(enantiomorph,希腊语意为“相对/相反形式”);在有关分子概念的引用中也被称为对映异构体。
可与其镜像叠合的物体被称为非手性的(achiral),有时也称为双向的(amphichiral)。
手性及手性物质只有两类:左手性和右手性。
有时为了对比,另外加上一种无手性(也称“中性手性”)。
左手性用learus或者L表示,右手性用dexter或者D表示,中性手性用M表示。
手性碳分子

手性碳分子手性碳原子(chiral carbon atom)是指与四个各不相同原子或基团相连的碳原子,用c*表示。
所有含一个手性碳原子的化合物,都有一对对映异构体。
含有两个不相同的手性碳原子的化合物有4个旋光异构体(两对对映异构体)。
判断方法1.手性碳原子一定就是饱和状态碳原子;2.手性碳原子所连接的四个基团要是不同的。
旋光性对大多数有机分子而言,分子的手性主要是由分子中的手性碳原子引起的。
手性分子均具有旋光性,非手性分子均不具有旋光性。
例如,丙酸分子实物与镜像可以完全重叠,分子中存在一个对称平面,没有手性,因此无旋光性;乳酸(2-羟基丙酸)分子实物和镜像不能完全重叠,分子中没有对称面也没有对称中心,具有手性,因此有旋光性。
所以,化合物的手性是产生旋光性的充分和必要条件。
内外消旋体某些化合物分子中存在手性碳原子,但由于分子内存在对称因素,使得分子没有旋光性,如(2r,3s)-酒石酸,此类化合物称为内消旋体。
内消旋体和外消旋体都无旋光性,但外消旋体可拆分为左旋体和右旋体,内消旋体不能拆分。
分类手性碳原子和手性分子的分类。
手性碳原子:把与四个相同原子或基团相连的碳原子称作手性碳原子。
存有不含一个手性碳原子、不含二个手性碳原子、不含三个手性碳原子、不含四个手性碳原子的分子等。
有的分子C99mg手性碳原子。
手性分子的分类:按是否含手性碳原子,可以把手性分子分为具有手性碳原子的手性分子和不具有手性碳原子的手性分子。
但含多个手性碳原子的分子的异构体不一定都是手性分子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
与手性有关的术语
⑴D/L和d/l
a.D或L指分子的绝对构型,按照与参照化合物D—或L—甘油醛的绝对构型并通过实验化学关联来指定,常用于氨基酸或碳水化合物,但最好使用R和S来表示。
b. d或l右旋或左旋,按照实验测定,化合物能将单色平面偏振光的平面向顺时针方向或向逆时针力向旋转向定。
应指出的是,化合物的右旋和左旋与该化合物的绝对构型并无直接的联系。
(2)立体异构体、非对映异构体和对映体
a.立体异构体(s t e r e o i s o m e r s)其分子由相同数日和相同类型的原子组成,是具有相同的连接方式但构型不同的化合物。
b.非对映异构体(d i a s t e r e o i s o m e r s)对于分子中具有两个或多个小对称中心,并且其分子互相不为实物和镜像的立体异构体。
例如,D—赤
藓糖和D—苏力糖。
常简称为“非对映体”。
非对映体也在立体异构体的范畴之内。
c.对映体(e n a n t i o m e r s)其分子互相为不可重合的实物和镜像的立体异构体。
(3)对映体过量和对映选择性
a.对映体过量(e n a n t i o m e r i c e x c e s s,e.e.)在两个对映体(E l和E2)的混合物中,假定E l的量大于E2,则对映体E l过量的百分数称为E l 的对映体过量,以 e.e.表示。
e.e.=[(E l-E2)/(E l+E2)]×100%
b.对映选择性(e n a t i o s e l e c t i v i t y)一个化学反应中,产生的某一对映体多于其他对映体的程度。
(4)光学活性、光学异构体和光学纯度
a.光学活性(o p t i c a l a c t i v i t y)实验观察到的化合物将单色平面偏振光的平面向观察者的右边或左边旋转的性质。
b.光学异构体(o p t i c a l i s o m e r s)对映体的同义词,但现在已不常用,因为有一些对映体在某些偏振光波长下并无光学活性。
c.光学纯度(o p t i c a l p u r i t y)根据实验测定的旋光度,在两个对映异构体的混合物中,一个对映体所占的百分数。
现在常用对映体纯度来代替。
(5)外消旋、内消旋和外消旋化
a.外消旋(r a c e m i c)以外消旋体或两个对映体的等量混合物存在,也以符号(士)示之。
b.内消旋化合物分子内具有两个或多个不对称中心但又有对
称面,因而不能以对映体存在的化合物。
例如内消旋酒石酸。
内消旋化合物用前缀m e s o冠示。
洒石酸有两个不对称中心,因此有一对对映体和一个内消旋体,共3个立体异构体。
c.外消旋化(r a c e m i z a t i o n)一种对映体转化为两个对映体的等量混合物。
如果转化为两个对映体其量不相等,称为部分消旋化。
(6)R e和S i(分别是拉丁文r e c t u s和s i n i s t e r,即左和右)
这些是关于面选择性的立体化学描述。
如图1—9所示,三个取代基a、b、c的C I P优先性顺序为a>b>c,则向着观察者的以顺时针取向的面称为R e,a→b→c以逆时针取向的面称为S i。
(7)顺式/反式(s y n/a n t i)赤式/苏式体(e r y t h r o/t h r e o f o r m)
(a)s y n/a n t i用来描述两个取代基对于环上某平面的相对构型的前缀。
s yn指同侧,而a n t i指异侧。
有时在直链化合物中,也用s y n或a n t i表示这相邻有关取代基在同侧或异侧。
(b)赤式/苏式由碳水化合物的命名而来,用来表述相邻立体中心的相对构型。
赤式异构体指在F i s c h e r投影式中相同或相似取代基在垂直链的同侧;苏式异构体指位于异侧。
(8)旋转轴对称因素(C n)
如果分子中有一条假想直线,当分子以此线为轴旋转360o/n(n=2,3,4…)之后,旋转的分子仍能与未经旋转的分子完全重合,那么这条直线便是该分子的n重对称轴,而该分子具有C n-旋转轴的对称因素。
例如分子16a、16b均为C2旋转轴分子,称分子16具C2对称性。
在不对称合成中会经常遇到具C n对称性的配体。
