chap132胺类化合物 91页PPT文档
胺类化合物的结构与性质

胺类化合物的结构与性质胺类化合物是一类重要的有机化合物,其分子结构含有一个或多个氨基(-NH2)官能团。
它们在生物化学、药物化学、有机合成等领域中具有广泛的应用。
本文将就胺类化合物的结构和性质展开探讨。
一、胺类化合物的结构胺类化合物的分子结构中,氨基官能团与碳原子以共价键相连。
根据氨基原子的数量和位置,胺类化合物可以进一步分为三类:一级胺、二级胺和三级胺。
一级胺的分子中含有一个氨基原子,如甲胺(CH3NH2)和乙胺(C2H5NH2)。
二级胺的分子中含有两个氨基原子,如乙二胺(C2H4(NH2)2)和丁胺(C4H9NH2)。
三级胺的分子中含有三个氨基原子,如三甲胺((CH3)3N)和三乙胺((C2H5)3N)。
二、胺类化合物的性质1. 水溶性:胺类化合物的水溶性随分子量的增加而增加。
一级胺和二级胺可以与水形成氢键,因此水溶性较好。
而三级胺不具备代表性的氢键结构,其水溶性较差。
2. 碱性:由于氨基的存在,胺类化合物表现出一定的碱性。
一级胺和二级胺在水溶液中可以参与酸碱反应,与弱酸生成盐。
三级胺则不能参与酸碱反应,因为它的三个氨基原子全部被烷基或芳香基取代。
3. 氨基氢的活性:胺类化合物的氨基氢具有较强的活性,可被酸、卤素或氧化剂直接取代或氧化,发生不同类型的化学反应。
三、胺类化合物的应用1. 生物化学:胺类化合物在生物体内起着极其重要的作用。
例如,在蛋白质、核酸和维生素等生物大分子中,都存在着胺基。
它们的氨基功能团是蛋白质折叠和结构稳定性的关键要素。
2. 药物化学:许多药物中含有胺基官能团,这是因为胺基官能团可以改变药物的溶解度、吸收性和生物利用度等性质。
例如,普通的抗组胺药物就是基于胺基官能团设计和制造的。
3. 有机合成:胺类化合物作为有机合成中的重要底物或中间体,广泛应用于各种有机合成反应中。
例如,它们可以通过烷基卤化物与氨气反应制备;也可通过Mannich反应、Gabriel合成等方法进行合成。
第十二章胺及其衍生物ppt课件

13 .1.2 胺类化合物的物理性质
脂肪胺:低级胺是气体或易挥发的液体,有特殊气味;
高级胺为固体,一般无气味。6个C以下的胺通常都溶于水.
芳香胺:为高沸点的液体或低熔点的固体,有特殊气
味;一般难溶于水,易溶于有机溶剂;大多具有毒性,某 些芳香胺具有致癌作用。
水溶度:伯、仲、叔三类胺与水形成氢键的能力依次减弱. 沸点:R-NH2、R2NH 分子间形成氢键的能力依次减弱,
单一的电性效应使胺的碱性由强至弱顺序为(气相 中):
R3N > R2NH > R→NH2 > NH3 > > 芳香胺
pKb
3~5
4.75
>9
碱性强度(在水溶液中) : 二甲胺 > 甲胺 > 三甲胺
N原子上连接的基团越多越大,对N上孤对电子的屏 蔽作用越大,N上孤对电子与H+结合就越难,碱性就 越弱。
13 .1.4 胺类化合物的化学性质
2 胺的烃基化
N H 3R S N 2 X R N H 2R XR 2 N H R X R 3 NR X R 4 N + X -
RI > RBr > RCl > RF 1°RX > 2°RX, 3°RX 以消除为主。 3 季铵碱的Hofmann消除反应
季铵碱制备; R 4 N + X -+A g 2 OH 2 OR 4 N + O H -+ A g X
含氮杂环 生物碱
R—NO2
R—NH2 R-CO-NH2 R—CN
Ar—N+2 X-
Ar—N=N—Ar’
-NO2 CH3-NH2 CH3-CO-NH2 CH2=CH-CN
-N+2 Cl-
胺类药物的分析精品PPT课件

间接:对乙酰氨基酚、非那 西丁、醋氨苯砜、贝诺酯。间接 的意思就是需要水解酰胺基。
2 对乙酰氨基酚 ChP(2000) [鉴别] (2)取本品约0.1g,加稀盐 酸5m1,置水浴中加热40分钟,放冷; 取0.5m1,滴加亚硝酸钠试液5滴,摇 匀,用水3ml稀释后,加碱性β-萘酚 试液2m1,振摇,即显红色。
(三)与重金属离子反应 1. 与铜和钴离子反应
盐酸利多卡因
硫酸铜
碳酸钠
蓝紫色
氯仿
黄色
具有N-芳环取代的盐酸利多卡因,在 碳酸钠溶液中与硫酸铜反应生成蓝紫色,容 易转入氯仿中显黄色。盐酸普鲁卡因,盐酸 丁卡因,苯左卡因等都不发生此反应。
盐酸利多卡因 CoCl2 H 亮绿色细小
2.羟肟酸铁盐反应
1 乙醇溶液的澄清度与颜色 2 生产工艺中使用铁粉作还原
(七)IR
盐酸布比卡因 ChP(2000) [鉴别] 本品的红外光吸收图谱与 对照的图谱(光谱集324图)一致 。
四、特殊杂质检查
(一)对乙酰氨基酚
一般以硝基氯苯为原料,水 解后制得对硝基酚,还原成对氨基 酚,再酰化。按药典规定,除检 查酸度,氯化物,硫酸盐,重金 属,水分和炽灼残渣外,还需进 行下列检查:
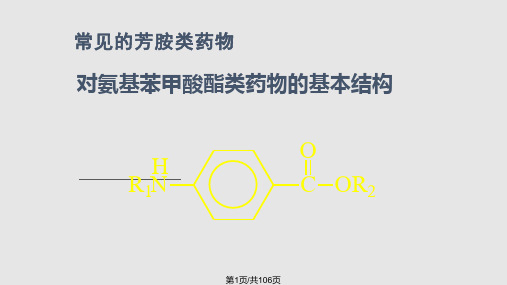
常见的芳胺类药物
一 对氨基苯甲酸酯类药物的基本结
构与主要化学性质
二 (一) 基本结构与典型药物
O
H
R1N
C OR2
都含有对氨基苯甲酸酯的结构母体
H2N
COOC2H5
苯佐卡因
H2N
COOCH2CH2N(C2H5)2 HCl
盐酸普鲁卡因
CH3(CH2)3NH
COOCH2CH2N(C2H5)2 HCl
苯佐卡因 NaOH 乙醇 乙醇 I2 NaOH CHI(3 碘仿臭气,黄色 )
第十五章 胺

胺类 化 合 物
胺的结构、命名和物理性质
胺的碱性和化学性质 芳香族重氮盐的性质和应用 胺的制法和应用 常见的分子重排反应及其历程和应用。 胺的化学性质和主要制备方法;
芳香族重氮盐、烯胺在合成中的应用。
有机化学 精品课程
氨的烃基取代物称为胺,氨分子中一个、两个或三个氢原子 被烃基取代生成的化合物分别称为伯胺、仲胺和叔胺 伯胺和仲胺中分别含有氨基(-NH2)和亚氨基( )
子与质子结合能力降低。
15.3.3 氢氧化四烃基铵
有机化学 精品课程
季铵盐与氢氧化钠不起反应,但用水和氧化银处理,可以转 变为氢氧化四烃基铵
2R4NHX + H2O + Ag2O 2R4NOH + 2Ag2X
也可以用离子交换树脂将卤离子换成氢氧离子 氢氧化四烃基铵为固体,碱性与氢氧化钠相近
有机化学 精品课程
CH3 N+ CH3 OH- 氢氧化三甲乙胺 C2H5
NHCH3
N-CH2CH3 CH3
NHCH3 -Cl
N-甲基苯胺
N-甲基-N-乙基苯胺 CH3 -N H3CCH3
N,N-二甲基对甲基苯胺
3-氯-N-甲基苯胺
§15.2 一元胺的物理性质 15.2.1 熔点、沸点和溶解度源自① ② ③有机化学 精品课程
下列消除产物哪种为主?是否符合Hoffmann规则?
CH3 N+ CH2CH3 CH3 -OH
PhCH2CH2
PhCH CH2 + CH2 CH2 93% 0.4%
CH2=CH O
CH2 CH
CH3
?
OH N+(CH3)3 ?
CH3CCH2 CH CH3 N+(CH3)2 OH-
第十七章胺类 PPT

§17-4 胺得反应
一、烃基化 ( p391)
氨
RX + NH3 → RNH21°胺
RX + RNH2 → R2NH + HX R2N + H2X -
2°胺
RX + R2NH → R3N + HX
R3N + HX -
3°胺
RX + R3N → R4N + X -
CH2NH2 + 3CH3I CH3OH
H2O/OH-
R2NH
分层或沉淀
稀酸
溶解
稀碱
RNH2
R3N
三、 +HNO2(NaNO2/H+) (p394) 鉴别 1°,2°,3°胺
1、 1°胺
(1)RNH2
CH3CH2CH2NH2
NaNO2 HCl
CH3CH2CH2N
NCl
重氮盐(不稳定)
CH3CH2CH2 + Cl- + N2
CH3CH2CH2
与水分子形成氢键得能力: 1°>2°>3°
空间位阻:
3°> 2°>1°
➢ b、p与S/H2O:1°>2°>3° ➢b、p: 1°与2°胺高于相应得烃,低于相应得
醇。 3°胺与相应得烃相近。
三、波谱分析 1、IR
振动类型 伯 胺/cm-1 仲 胺/cm-1 叔 胺/cm-1
N—H
N—H (面内) N—H (面外)
3、结构与性质
➢氮原子得电负性小于氧原子,形成氢键得能力较弱。 ➢胺得化学性质在很大程度上与N原子一个sp3杂化轨 道上得一对孤电子对有关,同时也受N原子上所连烃基 得种类与数目得影响。
140pm
N H
胺和生物碱ppt(完美版)

气体 亚硝酸溶液 黄色油状物
室温下 颜色或-
用途:鉴别几种不同类型的胺
19
• 扩环反应
练习题 13.8
NaCN/HCl
了解
20
(五) 芳环上的取代反应 1、卤代反应(掌握现象,可用于鉴别题)
白色沉淀
苯环有致基团,也不能停在一溴代或二溴代阶段
• 将氨基酰化后,主要得到对位卤代产物 • 将氨基用酸质子化后,主要得到间位卤代产物
六个价电子的中性活泼反应中间体。 一、结构
37
二、化学性质 1、加成反应 与烯、炔烃的π键加成而生成环丙烷衍生物。
液态中,单线态卡宾进行立体专一性加成。 气态中,三线态卡宾进行非立体专一性加成。
了解
38
2、插入反应 常用于环酮的扩大。
熟悉
39
作业
P440-443: 1、2
40
了解
1、与酚的偶合反应
两个芳香基团被 -N=N- 连在一起的化合物称为 偶氮化合物.
pH > 10 时:
pH= 8~10
重氮酸
重氮酸离子 33
了解 2、与芳胺的偶合反应
重氮盐
芳香胺 pH= 5~7
pH < 5 时:
对-N, N-二甲基 氨基偶氮苯(黄
色)
芳香胺形成大量铵盐使其浓度降低,反应终止。
34
水中亲核性:Br - > Cl - > HSO4– > H2O 了解
29
3、被氢原子取代
次磷酸水溶液
用途:除去氨基
了解
30
4、重氮盐的取代反应在合成上的应用(较有用, 亦是考研的考点) 课本 p442: 6(5)
有需要的同学学习
32
第六章胺类药物的分析幻灯片

CH3
HCl
盐酸利多卡因
有无酚羟基?
有无芳香第一胺?
CH3
C4H9 N
NHCO
HCl
CH3
盐酸布比卡因
性质
1. 水解后显芳香第一胺特性:芳酰氨基 利多卡因和布比卡因在酰胺基邻位存在两 个甲基,受空间位阻的影响,较难水解, 因此其水溶液较稳定。
2. 水解产物易酯化:对乙酰氨基酚和醋氨苯 酯,水解后生成醋酸,可在酸性介质中与乙 醇反应,生成醋酸乙酯。
盐酸普鲁卡因 水解 对氨基苯甲酸 + 2-二乙氨基乙醇
对氨基苯甲酸 -CO2 苯胺 [O]
醌类化合物 (黄色)
已黄的注射液不仅疗效下降,且毒性增加
《中国药典》2005年版规定,TLC法检查对氨基苯甲酸
精密量取本品,加乙醇稀释使成为每1ml中 含盐酸普鲁卡因2.5mg的溶液,作为供试品溶液。 取对氨基苯甲酸对照品,加乙醇制成每1ml中含 30g的溶液,作为对照品溶液。取上述两种溶 液各10 l,分别点于含有羧甲基纤维素钠为粘 合剂的硅胶H薄层板上,用苯-冰醋酸-丙酮-甲醇 (14∶1 ∶ 1 ∶ 4)为展开剂,展开后,取出晾 干,用对二甲氨基苯甲醛溶液(2%对二甲氨基 苯甲醛乙醇溶液100ml,加冰醋酸5ml制成)喷 雾显色。供试品溶液如显与对照品溶液相应的 杂质斑点,其颜色与对照品溶液主斑点比较, 不得更深。
(六)氯化物的鉴别反应
盐酸普鲁卡因、盐酸丁卡因、盐酸利多卡 因的水溶液。
供试品+稀硝酸+Ag+
白色凝乳状
+氨试液
溶解+稀硝酸
沉淀
(七)UV
盐酸布比卡因 ChP(2000) [鉴别] (2)取本品,精密称定,按干燥 品计算,加0.01mol/L盐酸溶液制成每1ml 中含0.40mg的溶液,照分光光度法(附录 ⅣA)测定,在263nm与271nm的波长处有 最 大 吸 收 ; 其 吸 收 度 分 别 为 0.53 ~ 0.58 与 0.43~0.48。
【PPT课件】第十三章 胺和酰胺

N H
d+ CH3
139pm 具部分双键性质
147pm
命名:酰基名称+胺(或某胺)——“某酰(某)胺” 内酰胺用希腊字母标明氨基位置。 O CH3-C—NH2 伯酰胺
CH3 O C NHCH3
O CH3 H—C—N-CH3 叔酰胺
仲酰胺
N,N-二甲基甲酰胺 乙酰胺 N-甲基乙酰胺 acetamide N-methyl acetamide Dimethylformamide DMF
O
ph C N
C2H5 ph
N-乙基-N-苯基苯甲酰胺
O CH3 C NH
CH3
O CH3 C N CH2CH3
乙酰苯胺 acetyl aniline
N-甲基-N-乙基乙酰胺 N-ethyl-N-methyl acetamide
O NH
CH3
N H
O
O
δ-己内酰胺 δ-hexanolactam
邻苯二甲酰亚胺 phthalimide
NH3
R—NH2 伯胺
R—N—R’ 叔胺
氨分子中 1个、 2个或 3个 H 原子被烃基 取代,分别生成伯胺 ( 一级胺, 1°) 、仲胺 (二级胺,2°)、和叔胺(三级胺,3°)。
脂肪胺
C2H5-NH2 乙胺 1°胺 伯胺 CH3-NH-C2H5 甲乙胺 2°胺 仲胺 CH3 C2H5-N-CH2CH2CH3 甲乙丙胺 3°胺 叔胺
乙醚-NaOH水溶液提取 乙醚层 C6H5CH2NH2 + C6H5CH2OH NaOH/H2O层 p-CH3-C6H5-ONa
盐酸
乙醚层 C6H5CH2OH 酸液层 C6H5CH2NH3+ NaOH C6H5CH2NH2
篇胺类药物分析PPT课件
(2)电位法 USP(24)
(3)外指示剂法 KI—淀粉糊剂或试纸
2NaNO2+2KI+4HCl→ 2NO+I2+2KCl+2NaCl+2H2O
(4)内指示剂法 中性红 不可逆指示剂
第45页/共106页
4. 测定方法 盐酸普鲁卡因 ChP(2000) 取本品约0.6g,精密称定,照永停
第24页/共106页
2. 硫氰酸盐衍生物
盐酸丁卡因 ChP(2000) [鉴别] (1)取本品约0.1g,加5%醋酸钠 溶 液 10ml 溶 解 后 , 加 25% 硫 氰 酸 铵 溶 液 1ml,即析出白色结晶;滤过,结晶用水 洗 涤 , 在 80℃ 干 燥 , 依 法 测 定 ( 附 录 ⅥC),熔点约为131℃。
第31页/共106页
精密量取本品,加乙醇稀释使成为每1ml 中含盐酸普鲁卡因2.5mg的溶液,作为供试品溶 液。取对氨基苯甲酸对照品,加乙醇制成每1ml 中含30g的溶液,作为对照品溶液。取上述两 种溶液各10 l,分别点于含有羧甲基纤维素钠 为粘合剂的硅胶H薄层板上,用苯-冰醋酸-丙酮甲醇(14∶1 ∶ 1 ∶ 4)为展开剂,展开后,取 出晾干,用对二甲氨基苯甲醛溶液(2%对二甲 氨基苯甲醛乙醇溶液100ml,加冰醋酸5ml制成) 喷雾显色。供试品溶液如显与对照品溶液相应 的杂质斑点,其颜色与对照品溶液主斑点比较, 不得更深。
盐酸普鲁卡因胺
第3页/共106页
酰胺类药物的基本结构
R3
R1
NH C R2
O R4
第4页/共106页
HO
NHCOCH3
对乙酰氨基酚(扑热息痛)
C2H5O
NHCOCH3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
此方法在合成上的 主要问题是什么?
R ' N H 2 RX
碱
RN H R ' +H X ( 碱 吸 收 )
醛酮的还原胺化(亚胺的还原)
R
N H 2R " R
H 2 /N i R
CO
CN R "
C H N HR "
R '
H + R '
R '
N-取代酰胺的还原
O
(1)L iA lH 4
R CN H R '
(3) 当烃基不同,按次序规则“较优”的基团放在后 面;
伯胺 CH3CH2-NH2 NH2-CH2-CH2-NH2
乙乙基胺+胺
乙乙基二+二胺胺
仲胺 CH3NHCH2CH3 CH3CH2-NH-CH2CH3
甲基甲+乙乙基胺+胺
二二乙乙基胺+胺
叔胺
甲基+甲乙乙基异+丙异胺丙基+胺
烷基连在芳胺氮原子上,则在烷基名称 前加“N”字母, 以便与苯环取代物加以区别。
但由于二个异构体间的能垒低(21KJ/mol), 在室温下可以103~105次/s的速度交换,故不能 分离。
R-构型
ΔHR→S = 25 kJ·mol-1 常温下可转化,难于拆分
S-构型
若限制翻转就能拆分出其对映体。例如: 下面化合物就拆分成了一对对对映体。
H3C
N N
N N
CH3 H3C
CH3
R2N R' + HX
R3N X R'
季铵盐
与醛酮的亲核加成反应
O
RNH2 +
C
H+
R'
R"
1o 胺
O
H+
R2NH
+
C
R'CH2
R"
2o 胺
R3N +
3o 胺
O
C
R'
R"
R N
C
R'
R"
亚胺
+ H2O
R
R
N
C
+ H2O
R'CH
R"
烯胺
No Reaction
芳胺烃化的条件要剧烈的多:
N H 2 + C H 3 O H H 2 2 S 5 O - 4 3 ,0 2 a 5 t 0 m O C
芳香族卤代物的取代(第16章)
NaNH2 Ar X
Ar NH2
O2N
R2NH X
O2N
苯炔机理
R N
R
加成-消除 机理
酰胺的 Hofmann 降解
O
C
X 2 / N a O H
A r N H 2
A r N H 2 + C O 2
制备芳香伯胺
例:
O NH3
O O
Cl2 / NaOH
O NaOH
碱性↗
碱性:
脂肪叔胺 > 脂肪仲胺 > 脂肪伯胺 > NH3
芳香胺碱性小于氨和脂肪胺 芳香胺的碱性强弱是:
NH2
NH N
pKb 9.30
13.8
中性
原因:
N H
H
p-π共轭,使N电子云密度降低,碱性比氨弱
(2)溶剂化效应 溶剂化效应是给电子的,N上的H越多,
溶剂化效应越大,形成的铵正离子就越稳定。
H2N
SO2NH2
S.N., 对氨基苯磺酰胺
N
H 2N
SO2 NH
N
S.D., 磺胺嘧啶
NH
H 2N
H2N
SO2 NH C NH2
O
SO2 NH
CH3
H 3C
S.G.,磺胺胍,治肠炎
S.I.Z., 磺胺异恶唑
(重3)氮与化亚反硝应酸的反应
NH2
+ N aN O 2 + H C l 0~5℃
N
+ 2
R NH H H O O O 2 2 2H H HR 2NH H O O 2 2H HR 3N H O H H
碱性: NH3 > 脂肪伯胺 > 脂肪仲胺 > 脂肪叔胺
(3)空间效应
烷基越多
不利于氢键的形成
R R NH
R
溶剂化效应弱
碱性弱
碱性: NH3 > 脂肪伯胺 > 脂肪仲胺 > 脂肪叔胺
碱性影响因素: 电子效应: 3o胺 > 2o胺 > 1o胺 空间效应: 1o胺 > 2o胺 > 3o胺 溶剂化效应:NH3 > 1o胺 > 2o胺 > 3o胺
CH3
叔醇
2. 根据烃基的种类不同分 脂肪胺( aliphatic amine ) R-NH2
芳香胺 (aromatic amine) Ar-NH2
CH 3 NH2
CH 2 NH2
脂肪胺 — 氮原子与脂肪烃基相连
NH2
NH
芳香胺 — 氮原子与芳环直接相连
(二)命名
习惯命名法----简单的胺
(1) 在“胺”之前加烃基来命名; (2) 对仲胺和叔胺, 当烃基相同时, 在前面标出数目;
在试管①中加入苯胺
加入盐酸至酸性
在冰水浴中加入亚硝酸钠 生成重氮盐
将一部分重氮盐加热, 在另一部分重氮盐中加
有大量气泡生成
入β-萘酚
出现红色沉淀
2. 仲胺与亚硝酸反应
脂肪 C H 3 仲胺
NH
H H
N H
H C3H
N
C3H H 3C
C3H
第二节 胺类化合物
故N原子上连有四个不同基团的化合 物 存在着对映体,可以分离出左旋体和右旋体。
N C2H5
H CH 3
C3H
+
N C 2H 5
= C2HCC H2HC 6H 5
N C2H5
CH 3 H
C3H
+N
C 2H 5
= C 6H 5
C2H CH C2H
副反应
RX
R
R
R NH R + R N R + R N R X
R
有多取代产物,分离有难度 2o 或 3o R-X 可能有消除产物
腈、酰胺、肟、腙的还原
H2, Raney Ni
R CN
NH3 LiAlH4
R CH2NH2 (第12章)
O L iA lH 4
RCN H 2
H 2 O R C H 2 N H 2(第12章)
NH
O O
ONa H+
NH2
O ONa NH2
O O
OH
NH2
三.胺类化合物的性质(I)
结构分析
有未共用电子对
• 有碱性 • 有亲核性 • 可被氧化剂氧化
RN H H
RN R H
RNR R
有活泼氢
• 可被强碱夺取 • 可被氧化剂氧化
N
N原子上的孤对电子:
1. 碱性(basicity):
N
2. 亲核性(nucleophilicity):
综合上面因素,碱性大小顺序是:
脂肪仲胺>脂肪伯、叔胺> NH3> 芳香伯胺>芳香仲胺>芳香叔胺
例题14-1
按碱性由强到弱的顺序排列下列化合物。
NH2
C H 2N H 2
NH2
CH3
①
答案:
NO2
②
③
②>①>③>④
NH2 NO2
NO2
④
3.成盐反应
RN2 H+HCl
RN3 H Cl
RN2 H+HOSO3H
芳胺和脂肪胺的结构比较
H H
—NH2 反应中心
碱性
脂肪胺R—NH2 是吸电基
在N原子的孤对电子上 较大
芳胺 Ar—NH2 是供电基
不在N原子而在苯环上 较小
胺的物理性质
物态: 除甲胺、二甲胺、三甲胺、乙胺为气体其他均为 液体或固体。
沸点: 胺与醇相似,也是极性化合物。除叔胺外,伯 胺和仲胺均易生成分子间的氢键。但氮的电负 性小于氧,故胺的沸点比相对分子质量相近的 非极性化合物高,比醇或羧酸的沸点低。
N ( C H 3 ) 2 + H 2 O
与羧酸衍生物的亲核取代反应
O
R N H 2o rR 2 N H+R ' CL
1o or 2o 胺
O R ' CN R (H ) +H L
R
O
R 3 N
+
C R ' L
3o 胺
N oR e a c tio n
叔 胺 —— 有 机 碱
Et3N
CH(CH3)2
N,N-二甲基苯胺 N-甲基-N-乙基苯胺
比较复杂的胺,常以烃类作母体,氨基 作为取代基来命名。例如:
CH3 CH3 CH CH CH2 CH3
NH2
2-甲基-3-氨基戊烷
3一二乙氨基戊烷
二、 胺的结构及物理性质 1. 胺的结构
胺分子中,N原子是以不等性sp3杂化成键 的,其构型成棱锥形。
N H
R C N OH
R' 肟
R C N NH2
R' 腙
H2 / Ni 或 LiAH4
H2 / Ni
R CH NH2
R'
(第10章)
Gabriel 伯胺合成法(请结合上节课内容学习)
