初中化学九下 第6章 基础实验5 配制一定溶质质量分数的氯化钠溶液 课件
化学人教版九年级下册实验活动5一定溶质质量分数的氯化钠溶液的配制

《实验活动5:一定溶质质量分数的氯化钠溶液的配制》教学设计(由于学校装修,故应在实验室完成的本节内容改在教室内完成,且两人一组的实验改为七人的学习小组进行)知识与技能1、学会配制一定溶质质量分数溶液。
2、练习称量、量取、溶解等操作。
3、加深对溶质的质量分数概念的理解。
过程与方法通过学生动手实验,在活动过程中对获取得的信息进行加工处理,从中培养学生的实验操作能力、观察分析能力和交流表达能力等。
情感、态度与价值观通过亲自动手做实验,激发学生的学习兴趣,体验到学有所用的快乐。
教学重点配制一定溶质质量分数溶液的操作步骤。
教学难点实验误差分析。
教材内容分析本节课教学内容是教材中的第五个基础实验。
初步学会配制一定溶质质量分数的溶液以及药品的取用、称量、量取、溶解等基本的实验操作,是初中学生必须具备的基本的实验技能。
当然,化学实验的功能不仅仅在于验证和扩展化学知识、培养实验能力,更为重要的是它能够为学生走近科学提供一种独特的形式、让学生通过亲身的观察、操作和体验,去感受和领悟科学的理念,这对发展学生多种能力具有重要的意义。
学生分析这个实验活动看似简单易行,但在实际教学过程中,不一定能达到预期的效果。
比如说,要是在教学上平铺直叙、内容就显得比较单调,课堂气氛受到影响;由于教学条件限制,学生很少有机会做分组实验,缺少基本的实验操作技能的训练与指导,现在拿过来就让学生完成一整个实验,在活动中会出现大量的操作错误,纠正这些需要占用很多的课堂时间;现在的学生严重脱离生活、生产活动,难以体会到配制一定溶质质量分数的溶液实际应用的意义。
教学方法指导实验引导探究学习方法小组实验问题探究教学过程一.新课导入【情景设置】实际生活和生产中,许多时候我们必须使用溶质质量分数一定的溶液。
比如医院里,我们经常会看到病人输液,许多就是生理盐水(即溶质质量分数为0.9%的食盐水),若高于0.9%,细胞会缩水;低于0.9%细胞会破裂。
所以学会配制溶质质量分数一定的溶液非常重要那么你知道怎样配制一定溶质质量分数的溶液吗?在前面我们讨论了溶液组成的定量表示,这节课我们来学习配制一定溶质质量分数的溶液。
沪教版初中化学九下 第6章 基础实验5 配制一定溶质质量分数的氯化钠溶液 课件PPT

在农业上常常用
10%—20%的食盐 水来选种,人们经
过长期的实验发现, 用15%的食盐水比 较合适。
学习目标
• 1、学习一定溶质质量分数的溶液的配制方法和过程 • 2、通过实验掌握一定溶质质量分数的溶液配制过程
中的基本操作和误差分析 • 3、会由浓溶液稀释配制稀溶液 • 4、体会溶液组成在生活中的应用
活动探究三:ห้องสมุดไป่ตู้溶液稀释配制稀溶液
交流与讨论3:
由浓溶液配制稀溶液的原理和计算依据是什么?
计算的依据:
(1)m(溶质前)= m(溶质后) (2)m(溶液后)= m(溶液前)+ m(水)
例:实验室需要配制10%的稀硫酸200g,需要溶质质量分数为 98%、密度是1.84g/mL的浓硫酸多少毫升?加多少毫升水? (水的密度是1g/mL) 解:设需要浓硫酸的体积为V,需要水的质量为m(水)
活动探究一
如何配制50g 15%NaCl溶液?
m (溶质) 溶液的溶质质量分数 = ———— ×100℅
m (溶液)
活动探究一:配制50g 15%NaCl溶液的方法和步骤
步骤名称
操作方法
1.计算 需氯化钠_7_._5__g,水__4_2_._5_g,则水的体积
________ 为__4_2_._5__mL(水密度为1g/mL)
课堂小结
同学们,本节课你收获了哪些知识?
55.功到自然成,成功之前难免有失败,然而只要能克服困难,坚持不懈地努力,那么,成功就在眼前。 71.当你快乐时,你要想,这快乐不是永恒的。当你痛苦时,你要想,这痛苦也不是永恒的。 34.这个世界不是因为你能做什么,而是你该做什么。 26.不经历风雨,怎么见彩虹。 35.美丽属于自信者,从容属于有备者,奇迹属于执着者,成功属于顽强者。 56.生活不是林黛玉,不会因为忧伤而风情万种。 49.没有退路时潜能就发挥出来了。 17.如果你曾经把失败当成清醒剂,就千万别让成功变成迷魂汤。 57.生命就是一个逐渐支出和利用时间的过程。一旦丧失了时间,生命也就走到了尽头。 12.不要浪费你的生命,在你一定会后悔的地方上。 51.努力向上的开拓,才使弯曲的竹鞭化作了笔直的毛竹。 40.不受天磨非好汉,不遭人妒是庸才。 39.人生意义的大小,不在乎外界的变迁,而在乎内心的经验。 45.人生不售来回票,一旦动身,绝不能复返。
实验活动5 一定溶质质量分数的氯化钠溶液的配制

第九单元 溶液
实验活动5 一定溶质质量分数的氯化钠 溶液的配制
实验导入 实验活动5 一定溶质质量分数的氯化钠溶液的配制
农民在喷施农药的时候浓度既不能太大,也不能 太小,必须在合理的浓度范围内才能发挥最佳效果。
注射用的生理盐水浓度为0.9%, 医用酒精的浓度为75%,这些需要 定量溶液怎样配制呢?
配制质量分数为3%的氯化钠溶液
(1)计算:配制50g质量分数为3%的氯化钠溶液所 需质量分数为6%的氯化钠溶液(溶液的密度为 1.04g/cm3)和水的质量分别为:6%的氯化钠溶液 __2_5_g(体积_2_4__mL);水_2_5__g。
依据:溶液稀释前后,溶质的质量不变。
实验步骤 实验活动5 一定溶质质量分数的氯化钠溶液的配制
A. 12.4%
B. 17.2%
C. 16.9%
D. 12.5%
课堂检测 实验活动5 一定溶质质量分数的氯化钠溶液的配制
2.某同学配制25g3%的NaCl溶液整个操作过程如下图所示。 回答下列问题:
①
②
③
④⑤
(1)配制溶液的正确操作顺序为_②__①__⑤__③__④____ (填序号) ,其中 操作错误的是____①____(填序号)。 (2)用量筒量取液体时,读数时视线要与量筒内_凹__液__面__的__最__低__处__
课堂检测 实验活动5 一定溶质质量分数的氯化钠溶液的配制
基础巩固题
1.配制50g溶质质量分数为15%的氯化钠溶液,
不需要用到的仪器是( A )A.集气瓶B.烧杯C.玻璃棒D.量筒
课堂检测 实验活动5 一定溶质质量分数的氯化钠溶液的配制
基础巩固题
2.实验室用氯化钠配制50g质量分数为6%的氯化钠溶 液。下列说法中不正确的是( C ) A.所需氯化钠的质量为3g B.氯化钠放在托盘天平的左盘称量 C.俯视量筒读数会使所配溶液偏稀 D.所需玻璃仪器有烧杯、玻璃棒、量筒等
实验活动5 一定溶质质量分数的氯化钠溶液的配制

下列情况会导致所配溶液中溶质的质量分数偏高的是 A.蔗糖中混有少量杂质 B.称量时蔗糖和砝码位置放反了(使用了游码) C.用于溶解蔗糖的烧杯洗净后残留有少量的水 D.用量筒量取水时,俯视读数
D (填字母序号)。
练案 化学
练案 化学
液体积×溶液密度。 (2)溶质质量=溶液质量×
溶质的质量分数 。
3.有关溶液的稀释计算 依据:加水稀释前后 溶质 的质量不变。
练案 化学
知识点1配制溶液的步骤与基本操作 1.(2020昆明)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精可有效灭活 病毒。现用95%的酒精配制75%的酒精,一般不会用到的仪器是( B )
1.溶液配制的方法及步骤
配制 方法
操作 步骤
用固体和水配制
①计)
①计算;②量取; ③混匀
常用 仪器
托盘天平、烧杯、玻璃棒、量筒、 胶头滴管和药匙
量筒、烧杯、玻 璃棒、胶头滴管
2.导致溶质质量分数偏小的原因 (1)从操作看可能是:称量时药品和砝码的位置放反,且使用了游码;量取水时仰视读 数;溶解时有溶质撒出等。 (2)从其他因素看可能是:药品不纯;计算错误等。
选项 A B
C
D
实验操作 称量时,将取出的过量氯化钠放回原瓶
溶解氯化钠时用玻璃棒搅拌
称取氯化钠时,在天平两边托盘上各放一张质量相等 的纸 量取所需水时,视线与量筒内液体凹液面的最低处保 持水平
目的分析 节约药品 增大氯化钠的
溶解度
整洁美观
准确读数
练案 化学
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器 有:烧杯、玻璃棒、量筒和 胶头滴管 。
沪教版九年级化学第六章基础实验5配制一定溶质质量分数的氯化钠溶液教学设计

1.采用启发式教学法,引导学生主动探究和学习。通过提问、讨论等方式,激发学生的思维,加深对溶质质量分数概念的理解。
-设计思考题:如何计算溶质质量分数?为什么需要精确称量和准确计量?
-学生讨论:探讨实验过程中可能出现的误差原因及解决办法。
2.实践操作教学,注重培养学生的实验技能。分组进行实验,教师巡回指导,及时纠正操作错误,确保实验顺利进行。
教学设计:
1.导入:通过回顾溶液的概念,引导学生进入本节课的主题。
2.基本概念:讲解溶质质量分数的定义及计算方法,让学生明确实验目标。
3.实验操作:分组进行实验,教师示范操作步骤,学生跟随操作。
a.使用电子天平精确称量氯化钠。
b.使用量筒准确计量水。
c.将氯化钠溶解于水中,搅拌均匀。
d.对配制的氯化钠溶液进行定性分析。
4.注重实验安全,培养学生遵守实验规程,养成良好的实验习惯。
(三)情感态度与价值观
1.激发学生对化学实验的兴趣,培养他们积极主动参与实验的态度。
2.培养学生严谨、细致、科学的实验态度,树立实验数据真实性的观念。
3.使学生认识到化学实验在生产和生活中的实际应用,提高他们的学习责任感和使命感。
4.通过实验,培养学生尊重事实、追求真理的精神,树立正确的价值观。
-分析家中实验与学校实验室实验在器材、操作等方面的异同,探讨如何提高实验准确性和效率。
3.拓展阅读与思考:
-阅读相关资料,了解氯化钠在生活中的其他应用,如腌制、医疗等,并撰写一篇短文,阐述溶质质量分数在这些应用中的作用。
-思考如何将所学溶液配制知识应用于其他溶质的配制,如糖水、盐水等。
4.团队合作与分享:
五、作业布置
为了巩固本节课的学习内容,检验学生对溶质质量分数概念的理解及实验操作技能的掌握,我设计了以下作业:
实验活动5一定溶质质量分数的氯化钠溶液的配制-人教版九年级化学下册教案

实验活动5一定溶质质量分数的氯化钠溶液的配制-人教版九年级化学下册教案实验目的本实验旨在通过实验操作和数据计算掌握一定质量分数的氯化钠溶液的配制方法及相关计算方法。
实验原理氯化钠为一种常见的无机盐,在生活和工业生产中应用非常广泛。
氯化钠的质量分数为溶液中氯化钠质量与溶液总质量之比,通常在化学实验和生产制造中需要制备一定质量分数的氯化钠溶液。
实验材料•氯化钠(NaCl)•滴定管•刻度瓶•常温蒸馏水实验步骤1.称取一定量的氯化钠(NaCl),并记录其质量;2.将称量好的氯化钠溶解在一定量的常温蒸馏水中;3.加入足量的常温蒸馏水,使溶液达到需要的总体积;4.摇晃均匀,得到一定质量分数的氯化钠溶液。
实验注意事项1.称取氯化钠时应准确称取指定数量;2.氯化钠的溶解过程中应注意加热时间和强度,以免发生溅泼等危险情况;3.制备氯化钠溶液时应根据实验需求来科学调整各个参数;4.制备好的氯化钠溶液应充分摇晃均匀,以使各组分充分混合。
实验数据和计算假设需要制备一定质量分数为0.15的氯化钠溶液,总质量为500g。
已知实验室中有质量分数为99%的氯化钠粉末,求需称取多少克氯化钠?计算过程: - 因为氯化钠溶液的质量分数为0.15,所以其质量分数可以表示为:- 0.15 = (质量/总质量) × 100% - 质量 = 0.15 × 总质量 = 0.15 × 500g = 75g - 已知氯化钠粉末的质量分数为99%,因此需要称取的氯化钠质量可以表示为: - 氯化钠质量 = 总质量 × 氯化钠质量分数 = 75g / 0.99 = 75.76g,约为 76g。
实验结果分析通过实验我们成功地制备了一定质量分数的氯化钠溶液。
我们已经了解了氯化钠溶液质量分数的含义及计算方法,并通过实际操作完成了氯化钠溶液的配制。
这项实验不仅增加了我们的操作技能,而且让我们进一步深入了解了溶液配制中的计算方法。
基础实验5 配制一定溶质质量分数的氯化钠溶液(课件)九年级化学下册(沪教版)

配制50g溶质质量分数为15%的氯化钠溶液
【实验过程】
1. 计算 需要氯化钠的质量为_7_.5_g,需要水 42.5ml。
2. 称取氯化钠 使用托盘天平称取之前,先要 调节天平平衡 ;
然后在天平两端分别放上质量相同的纸片,用镊子夹取
5 g的砝码,置于天平 右 (填“左”或“右”)托 盘中,并将游码调到 2.5 刻度。用药匙向天平 左 (填
ቤተ መጻሕፍቲ ባይዱ
【中考链接】
1.(2022·湖南岳阳)化学实验考查时,小芳抽到的考题 是:“配制 40g 质量分数为 18%的氯化钠溶液”,她的
D 实验操作正确的是( )
A
B
A.取氯化钠固体
C.量取 32.8mL 水
C
D
B.称量 7.2g 氯化钠
D.玻璃棒搅拌溶解
【中考链接】
2.(2022·山东烟台)实验室用固体氯化钠配制50g溶质质
(1)需称取氯化钠的质量为 12 g。 (2)图示实验中,正确的操作顺序为②④⑤③(①填序号)。
【中考链接】
(3)①若量取水的体积时仰视读数,其他操作均正确,则 所配制溶液的溶质质量分数 偏小 (选填“偏大”、“偏 小”或“无影响”)。 ②若称量氯化钠固体时托盘天平指针向右偏转,则应
向左盘添加氯化钠 直到天平平衡。 (4)欲配制60g质量分数为5%的氯化钠溶液,需要10%的氯 化钠溶液的质量为 30g 。
【课堂小结】
溶质质量分数偏小的原因
①溶质偏少:药品中含有杂质或发生潮解;称量时药品 和砝码放反了,而且使用了游码;称好的药品倒入烧杯 时有部分撒在烧杯外面或粘在称量纸上;溶质未完全溶 解就装瓶存放。 ②溶剂偏多:量水时仰视读数;烧杯或试剂瓶中有少量 水。
人教版九年级化学下册实验活动5一定溶质质量分数的氯化钠溶液的配制

实验活动5 一定溶质质量分数的氯化钠溶液的配制【实验目的】1.练习配制一定溶质质量分数的溶液。
2.加深对溶质的质量分数概念的理解。
【实验用品】托盘天平、烧杯、玻璃棒、药匙、量筒、细口瓶、胶头滴管。
氯化钠、蒸馏水。
【实验步骤】1.配制50 g质量分数为6%的氯化钠溶液(1)计算:所需氯化钠的质量为_____g;水的体积为_______mL。
(2)称量、量取:用天平称取所需的氯化钠,并放入烧杯中;用______mL量筒量取所需的水,倒入盛有氯化钠的烧杯。
(3)溶解:用玻璃棒搅拌,使氯化钠全部溶解。
(4)装瓶贴上标签。
2.用质量分数为6%的氯化钠溶液(密度为1.04 g/cm3)配制50 g质量分数为3%的氯化钠溶液(1)计算:所需质量分数为6%的氯化钠溶液的质量为_____g(体积为_______mL),水的质量为_______g(体积为mL)。
(2)量取:用_________mL的量筒量取所需的氯化钠溶液和水,倒入烧杯中。
(3)混匀:用玻璃棒搅拌,使溶液混合均匀。
(4)装瓶贴上标签。
【问题与交流】1.在溶解的操作中玻璃棒的作用是什么?2.本次实验中,如果出现配制的溶液溶质质量分数小于6%,你认为可能是什么原因造成?3.教师或小组评价:___________________________________________________1.(2013·北京)配制50 g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )A.蒸发皿B.玻璃棒C.烧杯D.量筒2.(2013·宿迁)配制50 g质量分数为5%的氯化钠溶液,下列说法正确的是( )A.将氯化钠直接放在天平的托盘上称量B.量取水时,仰视量筒读数C.将称好的氯化钠放入量筒中溶解D.为加快固体溶解,用玻璃棒搅拌3.(2013·庆阳)某同学在实验室配制50 g6%的氯化钠溶液,如图所示为部分操作,其中错误的是( )4.(2013·厦门)实验室需要100 g质量分数为3%的氯化钠溶液,配制过程中相关描述正确的是( )A.用3 g氯化钠与100 g水配制得到B.直接用手抓取氯化钠C.氯化钠直接放于天平托盘上称取D.用50 g质量分数为6%的氯化钠溶液与50 g水配制得到5.欲配制100 g质量分数为10%的氯化钠溶液,必须要的仪器组合是( )①托盘天平②烧杯③玻璃棒④100 mL量筒A.①②B.①②③C.①②③④D.①②④6.(2014·福州)实验室用蔗糖配制50.0 g溶质质量分数为10%的蔗糖溶液,下列说法错误的是( )A.用托盘天平称取5.0 g蔗糖B.用量程为10 mL的量筒量取所需的水C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签7.某同学在配制50 g溶质的质量分数为5%的食盐溶液的过程中,称量时将砝码放在左盘(1 g以下用游码),食盐放在右盘;量水时仰视液面读数,这样配制的食盐溶液中溶质的质量分数为( )A.等于5%B.大于5%C.小于5%D.无法确定8.(2014·盐城)实验室配制100 g10%的氯化钠溶液,有关实验操作不正确的是( )A.用托盘天平称取10.0 g氯化钠B.用量筒量取90.0 mL的水C.将称取的氯化钠倒入量筒中溶解D.将配制的溶液装入试剂瓶中,贴上标签9.(2013·乐山)如图是小英同学在实验室用氯化钠固体配制一定质量分数的食盐溶液可能用到的部分仪器:回答下列问题:(1)E仪器的名称是________。
沪教版初中化学九下 第6章 基础实验5 配制一定溶质质量分数的氯化钠溶液 课件

C.实验的步骤为计算、称量、量取、溶解、装瓶贴标签
D.量取水时,用规格为l00mL的量筒
归纳小结
1. 只有经历过地狱般的折磨,才有征服天堂的力量。只有流过血的手指才能弹出世间的绝唱。 43、不管失败多少次,都要面对生活,充满希望。 5、积极向上的心态,是成功者的最基本要素。 75、人类最大的灾难就是自已瞧不起自已。 17、光有奋斗精神是不够的,还需要脚踏实地一步一步地去做。要先分析自己的现状,分析自己现在处于什么位置,到底具备什么样的能力
计算的依据:稀释前 后,溶质的质量不变 。
需加水——g
即:浓溶液的质量×6% = 稀溶液的质量×3%
浓溶液的质量×6% = 50g×3%
浓溶液的质量 = 25g
浓溶液的体积 = 25g÷1.04g/cm3=24ml
需要加水的质量 = 50g-25g = 25g
基础巩固
1、用食盐固体配制100g溶质质量分数为20%的食盐溶液,现有下列操作:
游码的读数
读数要准确,应 以游码的左边缘
为准
2.9g
3.0g
3.1g
配制50克质量分数为6%的氯化钠溶液
实验步骤
计算:按配制要求计算出所需要的溶质和溶剂的
1 量 (固体计算出质量,液体计算出体积)
2
称量:用托盘天平或电子秤
称取所需的氯化钠的质量。
量取:用量筒量取所需的水。
3
4 5
装瓶存放:把配 好的溶液装入试 剂瓶中,贴上标 签。
溶解:把溶质和溶剂混合,用 玻璃棒搅拌至充分溶解即可。
巩固提升
如果没有食盐,手边只有刚刚 配好的6%的氯化钠溶液,而 我们需要50g质量分数为3% 的氯化钠溶液,那怎么办呢?
提示:(水的密度是1.0g/mL 、6% 的氯化钠溶液的密度为1.04g/mL)
2020-2021学年中考化学-基础实验5 配制一定溶质质量分数的氯化钠溶液
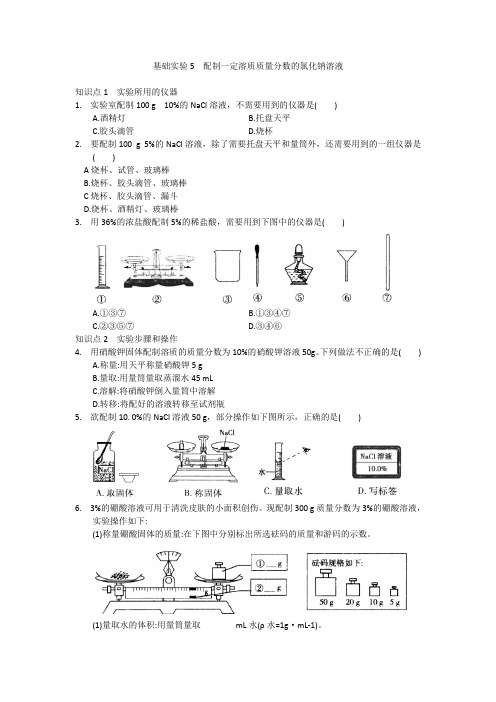
基础实验5 配制一定溶质质量分数的氯化钠溶液知识点1 实验所用的仪器1. 实验室配制100 g 10%的NaCl溶液,不需要用到的仪器是( )A.酒精灯B.托盘天平C.胶头滴管D.烧杯2. 要配制100 g 5%的NaCl溶液,除了需要托盘天平和量筒外,还需要用到的一组仪器是( )A烧杯、试管、玻璃棒B.烧杯、胶头滴管、玻璃棒C烧杯、胶头滴管、漏斗D.烧杯、酒精灯、玻璃棒3. 用36%的浓盐酸配制5%的稀盐酸,需要用到下图中的仪器是( )A.①③⑦B.①③④⑦C.②③⑤⑦D.③④⑥知识点2 实验步骤和操作4. 用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。
下列做法不正确的是( )A.称量:用天平称量硝酸钾5 gB.量取:用量筒量取蒸溜水45 mLC.溶解:将硝酸钾倒入量筒中溶解D.转移:将配好的溶液转移至试剂瓶5. 欲配制10. 0%的NaCl溶液50 g,部分操作如下图所示,正确的是( )6. 3%的硼酸溶液可用于清洗皮肤的小面积创伤。
现配制300 g质量分数为3%的硼酸溶液,实验操作如下:(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数。
(1)量取水的体积:用量筒量取mL水(ρ水=1g·mL-1)。
(2)溶解:用到的玻璃仪器是。
(3)装瓶、贴标签:在下图的标签中填上相应的内容。
知识点3 实验误差分析7. 进行“一定溶质质量分数的氯化钠溶液的配制”实验活动常出现以下错误操作,其中不影响所配溶液溶质质量分数的是( )8. 实验室配制50 g溶质质量分数为5%的氯化钠溶液,请回答下列问题:(1)已知:水的密度为1.0 g·mL-1,需要称取氯化钠g,需要量取水mL。
(2)配制的操作示意图如下,该实验的正确操作顺序为(填字母序号)。
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是(填序号)。
A.氯化钠固体不纯B.称量前天平指针偏左C.称量时,珐码端托盘上忘垫质量相同的纸片D.量取水时,仰视读数E.装瓶时,有少量溶液洒出F.称量时药品和砝码放颠倒(用游码)【作业精选】1. 在“配制一定溶质质量分数.的氯化钠溶液”实验中.下列操作正确的是( )A.甲图表示称取7. 5 g氯化钠B.乙图表示量取42. 5 mL水C.丙图表示溶解氯化钠D.丁图表示向试剂瓶中转移溶液2. 实验室配制50 g溶质质量分数为15%的氯化钠溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识回顾
溶液质量=溶质质量+溶剂质量 即: m(溶液) = m(溶质)+m(溶剂)
溶质的质量分数 =( 溶质质量 ÷溶液质量)×100%
变形公式: ①溶质质量 = 溶液的质量× 溶质质量分数 ②溶剂质量 = 溶液的质量-溶质的质量
课堂·互动探究
配制50克质量分数为6%的氯化钠溶液 ▪ 一、实验目的: ▪ 1.学习一定溶质质量分数溶液的配制方法和过程。 ▪ 2.通过实验,掌握一定溶质质量分数的溶液配制过程中的基本操
左物右码(先加质 量大的法码,再加 质量小的法码); 如果放置正确,物 质质量=砝码质量 + 游码质量; 如果放置错误,物 质质量=砝码质 量—游码质量。
当称量未知质量的物 体时,先加入物体后 加砝码;当准确称量 一定质量的药品时, 要先加砝码、移好游 码后再加药品; 称量完毕,法码回盒, 游码回零。
游码的读数
读数要准确,应 以游码的左边缘
为准
2.9g
3.0g
3.1g
配制50克质量分数为6%的氯化钠溶液
实验步骤
计算:按配制要求计算出所需要的溶质和溶剂的
1 量 (固体计算出质量,液体计算出体积)
2
称量:用托盘天平或电子秤
称取所需的氯化钠的质量。
量取:用量筒量取所需的水。
3
4 5
装瓶存放:把配 好的玻璃棒搅拌至充分溶解即可。
巩固提升
如果没有食盐,手边只有刚刚 配好的6%的氯化钠溶液,而 我们需要50g质量分数为3% 的氯化钠溶液,那怎么办呢?
提示:(水的密度是1.0g/mL 、6% 的氯化钠溶液的密度为1.04g/mL)
难点突破
计算
所需6%的氯化钠溶 液———g(体积——ml),
①溶解;②称取食盐;③过滤;④量取水;⑤计算;⑥蒸发。正确的操作顺
序是(
)
A. ①②③④ B. ⑤②④① C.①③⑤②④① D.①③⑥⑤②④①
2、实验室配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是( )
A.若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
B.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率
C.实验的步骤为计算、称量、量取、溶解、装瓶贴标签
D.量取水时,用规格为l00mL的量筒
归纳小结
山路曲折盘旋,但毕竟朝着顶峰延伸。 瞩目远方,你才会加快步伐;观赏风景,你才会步履轻盈;结伴同行,你才能欢歌笑语;风雨兼程,你才能成功登顶。 业精于勤,荒于嬉;行成于思,毁于随。——韩愈 无论何时,都要做好独自生活的准备。 酒食上得来的朋友,等到酒尽樽空,转眼成为路人。 失败是什么?没有什么,只是更走近成功一步;成功是什么?就是走过了所有通向失败的路,只剩下一条路,那就是成功的路。 生命是一支织梭。 人的成长需要接受四个方面的教育:父母、老师、书本、社会,有趣的是,社会似乎总是与前面三种教给你的背道而驰。 实现梦想比睡在床上的梦想更灿烂。 不要过分仓促地相信和钦佩德育教员:他们说话像天使,生活却像凡人。——约翰逊 如你想要拥有完美无暇的友谊,可能一辈子找不到朋友。 只要你在路上,就不要放弃前进的勇气,走走停停的生活会一直继续。
作。
▪ 二、实验用品: ▪ 食盐(NaCl)、蒸馏水; ▪ 托盘天平(含砝码)、纸片(大小规格相同)、药匙、量筒、胶
头滴管、烧杯、玻璃棒等。
巩固旧知
托盘天平的使用方法及注意事项
1
2
3
4
检查天平是 否平衡(游 码是否在零 刻度处,若 不平衡,需 调节平衡螺 母)
托盘上各放一 张质量相同的 纸(强调:易 潮解的或有腐 蚀性的药品放 在小烧杯里)
计算的依据:稀释前 后,溶质的质量不变 。
需加水——g
即:浓溶液的质量×6% = 稀溶液的质量×3%
浓溶液的质量×6% = 50g×3%
浓溶液的质量 = 25g
浓溶液的体积 = 25g÷1.04g/cm3=24ml
需要加水的质量 = 50g-25g = 25g
基础巩固
1、用食盐固体配制100g溶质质量分数为20%的食盐溶液,现有下列操作:
