李艳梅版有机化学课后习题答案
1李艳梅有机化学

Starch(淀粉)
Gasoline (汽油)
O O H * C R1 C N R2
H N
* n
CmHn
m value around 8
O OH O O CH3
乙酰水杨酸(阿斯匹林)
O OH O O CH3
O OH OH
H3C
C O
O
C O
CH3
Salicylic acid
Acetylsalicylic acid
H3C C O OH
制醋
Dyeing has become am important industry before Zhou dynasty.
茜 草
染色
In ancient ages, mixtures of organic compounds were abstracted from natural products. Chinese traditional drug, dye, and perfume are of this kind.
Milestone of organic chemistry By Wöhler 1865 Bringing forward that carbon is quadrivalent Milestone of structural theory By A. Kekulé
1874
Saturated carbon atoms share tetrahedral topology
Hint
分类的关键:
“性质”!
而不是“组成”
H H
B N
H N B H
B N
H H
1. Organic compounds and organic chemistry 第一部分 有机化合物和有机化学
有机化学课后习题参考答案完整版

有机化学课后习题参考答案完整版⽬录第⼀章绪论 0第⼆章饱和烃 (1)第三章不饱和烃 (5)第四章环烃 (13)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应⽤ (33)第⼋章醇酚醚 (43)第九章醛、酮、醌 (52)第⼗章羧酸及其衍⽣物 (63)第⼗⼀章取代酸 (71)第⼗⼆章含氮化合物 (78)第⼗三章含硫和含磷有机化合物 (86)第⼗四章碳⽔化合物 (89)第⼗五章氨基酸、多肽与蛋⽩质 (100)第⼗六章类脂化合物 (105)第⼗七章杂环化合物 (114)Fulin 湛师第⼀章绪论1.1扼要归纳典型的以离⼦键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于⽔中所得的溶液与NaBr 及KCl 各1mol 溶于⽔中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在⼀起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么?答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于⽔中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离⼦各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在⽔中是以分⼦状态存在,所以是两组不同的混合物。
1.3碳原⼦核外及氢原⼦核外各有⼏个电⼦?它们是怎样分布的?画出它们的轨道形状。
当四个氢原⼦与⼀个碳原⼦结合成甲烷(CH 4)时,碳原⼦核外有⼏个电⼦是⽤来与氢成键的?画出它们的轨道形状及甲烷分⼦的形状。
答案:C+624H CCH 4中C 中有4个电⼦与氢成键为SP 3杂化轨道,正四⾯体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电⼦式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H H HCC HH HH 或b.H C H c.H N Hd.H S H e.H O NOf.OC H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其⽅向。
李艳梅有机化学-20 杂环化合物

SO
4
(CH
H
2
oC
CO)
3
H
25
95 %
PO
3
O
2
4
S SO3H
O S
CH3
20.2.2.2 加成反应
1、催化加氢
N2/Ni O
N2/Ni S
N2/Ni N H
N2/Ni
O
O
N2/Ni
S
S
N2/Ni
N
N
H
H
2、Diels-Alder反应
+ O
+ S
O
30oC
O
O
O
100oC
O
High pressure
氧(杂)茂
O
氮(杂)茂
N H
茂 硫(杂)茂
S
氮苯
N
N N
1,4-二氮苯
1,2-二氮苯
N N
N N
1,3-二氮苯
N 2-氮萘 萘 1-氮萘
N
环上只有一个杂原子时,有时也把靠近杂原子的位置叫α位,其 次是β位,再次为γ位。
β α O
β α
O
γ β α
N
γ β
Nα
20.1.3 杂环化合物的结构
1.44Å 1.35Å
N+ N
H
SO3
C2H4Cl2 3 days, r.t.
100oC
HCl
O SO3 N H
HCl
N SO3 N
H
H
+
C2H4Cl2
S
N
r.t.
SO3
Ba(OH)2
S SO3 Ba2+ 2
有机化学第001章
东晋葛洪《肘后备急方•卷三治寒热诸疟方第十六》
食品安全
① 三聚氰胺
H
NH O
H
H
N
N
N
N HN
O
H
N
O
H
NH
N
H
N
O
H
H NH
H
N
HN
O
N
N
N
H
H
N
O
H
NH O
H
NH
H
N
N
H
N
N HN
O
H
N
N
NH O
H
H
食品安全
② 阿斯巴甜
③ 塑化剂
天门冬酰苯丙氨酸甲酯
1.3B 有机化合物的结构特征(分子结构)
① 同分异构现象普遍存在
C2H6O
CH3CH2OH 乙醇,bp: 78.3 oC
CH3OCH3 甲醚,bp: 23 oC
同分异构体:具有相同的分子式而构造与性质不同 的化合物。
1.3B 有机化合物的结构特征(分子结构)
② 共价键结合 碳/C:有机化合物中的核心原子
1.1C 现代有机化学
1828年 Friedrich Wöhler (GER)
有机化学:含碳化合物的化学 / the chemistry of compounds that contain the element carbon. Definition for “Organic Molecule” Compounds that they contain at least one carbon atom
课程特点
难:内容繁多,理论不够系统 挑战性:逻辑性、系统性。应用性强、实践性强 沉溺于大量反应的记忆 失去了对学科整体的领悟
有机化学清华大学李艳梅版课后题答案

第九章1.苯乙酮(1)(2) 2-(1-甲基)丙基苯甲醛(3)环己酮缩乙二醇(4)1,5,5-三甲基-2-氧代环己甲醛(5)1-苯基-2-甲基-3-羟基-1-丁酮(6)4-甲基-7-氧代-辛醛(7)5-乙基-6-庚烯醛(8)3-丁烯-2-酮(9)(E)-1,4-二苯基-2-丁烯-1,4-二酮苯基苯基甲酮肟(11)5-硝基-2-萘甲醛2.(1)CH=CHCHO (2)CH3OCH(CH3)2(10)对溴(12)1-环丙基-2-丙酮(3)OCH2CCH2CH3(4)OBrCCH2CHCH3(5)CH3CH3O (6)OCH3O(7)NCONH2CH3CH2CCH3(8)CH3CH=CHC=NNHC6H53.(1)乙醛丁醛环戊酮I2NaOH(-)(-)土伦试剂(+)黄色沉淀(+) 银镜反应(-)(2)CH 2CH 2CHO O CH 2CCH 3C 2H 5 CHO土伦试剂(-) (+) 银镜反应 (+) 银镜反应斐林试剂(+) 银镜反应(-)无变化(3)丙醛 丙酮 丙醇 异丙醇I 2 NaOH(-) (+) 黄色沉淀 (-) (+) 黄色沉淀土伦试剂(+) 银镜反应(-)白色固体丙酮饱和亚硫酸氢钠(-)异丙醇(4)戊醛 2-戊酮 环戊酮 (-) (+) 黄色沉淀I 2 NaOH(-)(+) 银镜反应 (-)斐林试剂饱和亚硫酸氢钠(+) 白色固体苯甲醛(-) (-) (-)4.(1)正丁醇>丁酮>乙醚>正戊烷OO H>OO CH 2CHO(2) (3)H> CH 3CHO >O CH 3CCH 3O CH 3CCH 3O CH 3CH 2CCH 3CHO >CHO >>(4)丙酮>丁酮>2-戊酮5.(CH 3)3CCOCH 3COCH 3CH 2CHCH 3 OH以上化合物能发生碘仿反应 6.O-CH 2CCH 2CH 3OCH 3CCH 2CH 3OH -O -CH 3CCH 2CH 3OH-优先进攻酸性强和立体位阻小的氢OHC CH 2CH 3 (I) OHC CH 2CH 3 (II) (I) 烯醇式结构更稳定OCH 2CCHCH 3 BrBr 2OBrCH 2CCH 2CH 3OCH 3CCH 2CH 3H ++ OHCH 3CCH 2CH 3CH 3Br 2CH 27.(1)CH 3CH=CH-CH 2CH 2CH(OCH 3)2 (3) OH C 6H 5COCHCN(4)NHOH CH 3CCH 2CH 3OH(5) CHO CHO(2)BrOCH 3(6)OMgBr Ph (8)OH OOPhPh (9) OH Ph(7)CH 3CH 2OHCH 3COOH(10)CH 2CH 3 OH O(11)OO CH3CH3(12)CH3BrO8.(1)BrOCCH3CH2OHCH2OHHClBrO OCH31) Mg, 无水乙醚2) CO23) H3O+OHOOOCH3H3O+HOO OCCH3CH3OHH2SO4 OCH3O OCCH3NaBH4CH3OO OHCHCH3(2)H2SO4, H2O C CHHgSO4OC CH3NaCNOHC CH3CNH3O+OHC CH3COOH (3)Br +CH3CH2CHO1) Mg, 无水乙醚2)H3O+OH48% HBrBr 1) Mg, 无水乙醚2)D2ODO(4)KMnO4H+OO1) NaOH2)(5)OCH3CH2CH2COClAlCl3Zn-HgHClBr(6)CH3CH2Br(7)HC CHNaNH2NH3H2SO4, H2O HgSO4OCH3CH2CH2CCH2CH2CH2CH3NaC CNaOBr2FeBr+PPh3Ph3P-CH2CH3Br-OPh C CH3CHCH3Ph C CH3CH3CH2CH2BrCH3CH2CH2 C C CH2CH2CH3(8)O3 Zn CHOCHO1) NaOH2)CHO9.(1)OCOOC2H5C2H5ONaOCOOC2H5-Na+CH2OCHCCH3COOC2H5C2H5OHMichael加成COOC2H5-H2OOCH3OC2H5ONa COOC2H5COOC2H5OH3C-O HOOO(2)OONaOH CH 3CCH 2CH 2CCH 3- OOCH 2CCH 2CH 2CCH 3O OH CH 3-H 2OO(3) CH 3HO CCH PhH + -H +CH 3H OH CCH Ph +重排CH 3HH C C OH + Ph重排CH 3H OH C C Ph H+-H + H +PhCOCH 2CH 310.CH 3 CH 3 (A)O CH 3CH 3+CH 3CHOOH CH 3CH 3 CH 3(B)O CH 3 CH 3 CH 3(C)CH 311.OCH 3 OCH 3 CH 3 (A)(B)CHO HClCH 3KMnO 4COOH COOH12.HO(I)HOCH 2CH 2CH 3 (III)O CH 2CCH 3HOOH CH 2CHCH 3 (II)CH 3OCH 2CH 2CH 3 (IV)13.CH3O (I)HOO(II)OCH314.(1)红外光谱,后者在1700 cm-1 附近有醛羰基的红外吸收峰。
2024版清华大学有机化学李艳梅老师课件第14章

目录
• 第十四章概述 • 有机化学反应机理 • 有机合成策略与技巧 • 天然产物中有机化学应用 • 实验室安全与环保要求 • 习题讲解与答疑环节
01
第十四章概述
章节内容与目标
内容
本章主要探讨有机化学反应的机理, 包括亲核取代、消除反应、亲电加 成等反应类型。
节约资源
在实验过程中要注意节约资源,如 减少试剂用量、回收利用废弃物中 的有用物质等。
事故预防与应急处理措施
制定应急预案
实验室必须制定应急预案,明确 应急处理措施和人员分工,以便
在事故发生时能够迅速应对。
配备应急设施
实验室必须配备相应的应急设施, 如灭火器、急救箱、安全出口等, 以便在事故发生时能够及时采取
重要概念及知识点
01
知识点
02
03
04
亲核取代反应的机理及影响因 素。
消除反应的机理及立体化学。
亲电加成反应的机理及其在合 成中的应用。
学习方法与建议
学习方法 认真阅读教材,理解反应机理的基本概念。
通过做习题,加深对反应机理的理解和应用。
学习方法与建议
• 查阅相关文献,了解反应机理的最新研究进展。
脂肪酸的合成与分解代谢途径,甘油 磷脂的代谢途径等。
05
实验室安全与环保要求
实验室安全操作规程
严格遵守实验室规章制度01 Nhomakorabea进入实验室前必须了解并遵守实验室的各项规章制度,如穿戴
实验服、禁止饮食、禁止吸烟等。
正确使用实验器材
02
使用实验器材前必须了解其使用方法和注意事项,确保正确使
用,避免损坏或造成危险。
蛋白质
蛋白质的结构层次(一级、 二级、三级和四级结构)、 性质及其合成与降解。
清华大学有机化学李艳梅老师课件第三章

本章重点:
饱和烃 通式:CnH2n+2
Content
3.1 Structure 3.2 Conformation 3.3 Physical properties and spectrum
data 3.4 Chemical properties 3.5 Preparation (Learn on your own) 3.6 Sources and usages (Learn on your
重叠型构象中,两个C原子上的H原子相距较近, 产生排斥力,而出现空间阻碍效应(Steric effect)。 而在穿插型构象中,两个C原子上H原子的相距较 远,不会出现空间阻碍效应的排斥力,能量较低, 比较稳定。
对“试题一〞的讨论:
在国内外现行的有机化学教科书中,对乙烷分 子的构象问题大多是按上述方式〔空间阻碍效应〕 解释的.
3.2.4 Conformation of the other alkanes Learn on your own
3.3 Physical properties and spectrum data
3.3.1 Physical properties
沸点:
b.p liq—>gas 分子距离恰好为色散力作用范围
C—C , C—H 有一定极性,可反响
特点3:自由基型反响
电负性 C:2.5 H:2.2
不同的C—H键其键能不同,但极性都不大,以
均裂为主
自由基型为主
H CH3CH2CH2CH2 CH2C H
H
• 氧化反响 • 热解 • 异构化 • 自由基取代反响
Cleavage Substitution Oxidation
清华大学有机化学李艳梅全第8章

整理课件
结构推导
30
8.3.7 Polymerization 聚合
乙烯基乙炔 二乙烯基乙炔
整理课件
31
8.4 Preparation (Learn on your own)
8.5 Resource & application (Learn on your own)
49
(A) 经典式的缺点:
1、无法正确反映一些真实结构: 2、一些化合物无法用单一式子准确地描述
整理课件
50
(B) 基本思想: 1931-1933 L. Pauling
“共振论”
当一个分子、离子或自由基按价键规则可以写出一个 以上只有电子分布不同的经典结构式时,它们的真实 结构就是由这些可能的经典式叠加而成的。
RCCH
具有酸性 被亲核-加成
整理课件
25
Nu: -OH, -SH, -NH2, =NH, -CONH2, -COOH /碱
CN- 反应对象:乙炔及端炔 反应:
加成方向:进攻位阻较小的碳
整理课件
26
8.3.5 Reduction 还原
1、催化氢化 生成烷烃:
生成烯烃:
Cat.: Lindlar催化剂(钯附着在CaCO3及少量PbO上) 或 BaSO4为载体的钯催化剂(吡啶中)
这样的经典结构式称为“共振式”或“极限式”
整理课件
51
真实的分子、离子或自由基可认为是这些极限式“杂 化”而产生的“杂化体”
杂化 体
极限 式
共振 式
极限 式
共振 式
整理课件
52
错误概念:混合物 互变异构
大学《有机化学》课后习题答案
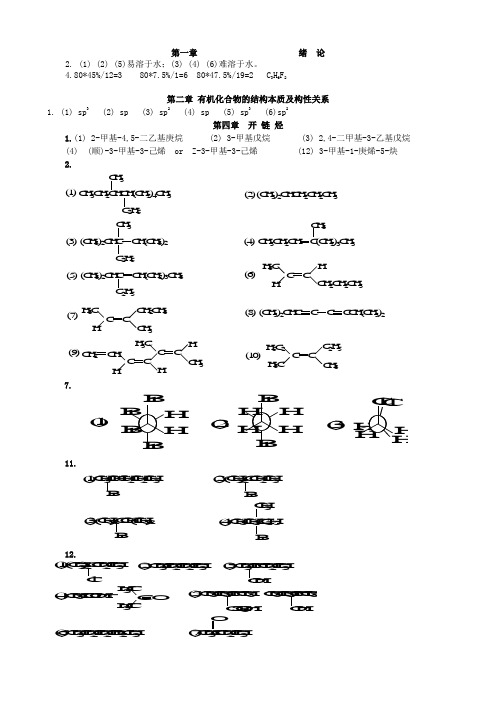
第一章绪论2. (1) (2) (5)易溶于水;(3) (4) (6)难溶于水。
4.80*45%/12=3 80*7.5%/1=6 80*47.5%/19=2 C3H6F2第二章有机化合物的结构本质及构性关系1.(1) sp3 (2) sp (3) sp2 (4) sp (5) sp3 (6)sp2第四章开链烃1.(1) 2-甲基-4,5-二乙基庚烷 (2) 3-甲基戊烷 (3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯 or Z-3-甲基-3-己烯 (12) 3-甲基-1-庚烯-5-炔2.7.11.12.14. (5) > (3) > (2) > (1) > (4) 即: CH2=CHC +HCH 3 >(CH3)3C + >CH 3CH 2C +HCH 3 >CH 3CH 2CH 2C +H 2> (CH 3)2CHC +H 216. (1)(2)(3)17.21AB.10.(1)CH 3-CH=CH 2−−−−−→−+H /KMnO 4CH 3COOH(2)CH 3-C≡CH+HBr(2mol ) CH 3CBr 2CH 3(3)CH 3-3-C=CH 2−−→−2Br CH 3CBr 2CH 2Br 第四章 环 烃 2.1-戊烯 1-戊炔 戊 烷Br 2/CCl 4室温,避光√ 溴褪色√ 溴褪色× × √灰白色1-丁炔 2-丁炔 丁 烷Br 2/CCl 4 室温,避光√溴褪色 × Ag(NH 3)2+√灰白色↓ × ×1,3-丁二烯 1-己炔 2,3-二甲基丁烷Br 2/CCl 4√ 溴褪色 √ 溴褪色 × Ag(NH 3)2+×√ 灰白色↓C(CH 3)3CH 3(1)(2)(3)3.(1)反式CH 3Br(3)顺式4.C H 3B rC lC l +C l C lC O O HH 3CO 2N (C H 3)3C C O O H(1)(2)(3)(4)(5)(6)(7) B rC 2H 5C 2H 5B r +C H 3C O C H 3(C H 3)2C C H (C H 3)2B r(8) 1molCl 2 / h, 苯/无水AlCl 3N H C O C H 3N O 2C H 3C H 3S O 3H(9) (10)7. (2)有芳香性 10.第六章 旋光异构6-32. (1)× (2)× (3)× (4)√ (5)√ (6)√7.2.66120678.58.18][20+=⨯÷+=⨯=l c Dαα第七章 卤 代 烃2、C l C lC l (2)4、第八章 醇、酚、醚1. (1) 3-甲基-3-戊烯-1-醇 (2) 2-甲基苯酚 (3) 2,5-庚二醇 (4) 4-苯基-2-戊醇 (5) 2-溴-1-丙醇 (6) 1-苯基乙醇(7) 2-硝基-1-萘酚 (8) 3-甲氧基苯甲 (9) 1,2-二乙氧基乙烷(乙二醇二乙醚)(1)(2)3、4. (1) 甲醇 分子间氢键 (6) 邻硝基苯酚 分子内氢键、分子间氢键 5、(1)CH 2IH 3COOH(5)(6)HOOCH 3H(7)6、AgNO 3/乙醇,室温白↓× ×AgNO 3/乙醇,加热白↓×OH+OHBrBr(1)(2)10、OH O ClA B C D第九章醛、酮、醌一、命名下列化合物。
李艳梅版有机化学课后习题答案

第一章1、(1) 有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent boud)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异是一种有相同化学式而有不同原子排列的化合物的异构现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极距μ=rq。
它是一个矢量,化学中方向规定为从正电荷中心指向负电荷中心。
(6)诱导效应:在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中两个相邻化学键之间的夹角。
(10) Lewis酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11) 疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2、(1) H:S:H(2)H:N:HH(3)H:C:HHH (4) H:C:HO(5)H:C:O:C:HH HH(6) H:O:P:O:H:O(7)H:C:C::C:HHHH H(8)H:C:C:O:HO:HH (9)C:H3、具有偶极的分子:(1)两H原子中心指向O原子方向;(2)由H原子指向Br原子;(4)H原子指向三个Cl原子的中心方向;(5)乙基指向羟基方向4、(1)正庚烷;(2)异丁烷;(3)异已烷;(4)新戊烷6、酸:Cu2+ FCl3CH3CN碱: NH3CH3NH2 C2H5OC2H5加合物: CH3COOH CH3OH7、(1) CH3COOH/CH3COO-H3O+/H2O(2) H2SO4/HSO4-CH3OH2+/CH3OH(3) HNO3/NO3-(CH3)3NH+/(CH3)3N8、(2)CH3F > (3) CH3Cl > (4) CH3Br > (5) CH3I > (1) CH49、 单键最长,双键次之,叁键最短,单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近。
清华大学有机化学李艳梅老师第9章 ppt课件

2,Wiki百科
燃烧热(kJ/mol): 3264.4
临界温度(℃): 289.5
临界压力(MPa): 4.92
/
辛醇/水分配系数的对数值: 2.15
闪点(℃): -11
引燃温度(℃): 560 爆炸上限%(V/V): 8.0
/
(C) 磺化反应 1 Formation of +E
+SO3H or SO3 as E+
清华大学有机化学李艳梅老师第9章
2 Sulfonation
反应可逆 稀酸加热下可脱去
“保护基团”
清华大学有机化学李艳梅老师第9章
(D) Friedel-Crafts 反应
R + 或 RCO+ as E+
1 Formation of +R or RCO+
清华大学有机化学李艳梅老师第9章
(二)预测反应位点
CH3
定位一致时
定位不一致时
CO OH
(1)一般地,活化基团的作用
超过钝化基团的作用
(2)强活化基团的影响大于
弱活化基团
(3)两个基团的定位能力差
不多时,得混合物
CH3 COOH
CH3
NH2 Cl
CH3
清华大学有机化学李艳梅老师第9章
COOH OCH3
第三类;致钝的邻对位定位基 -F, -Cl, -Br, -CH2Cl
定位基的定位能力
清华大学有机化学李艳梅老师第9章
第一类;致活的邻对位定位基
CH3 E
o-
H
CH3 E H
致活:给电子基团 邻对位定位:
CH3 E H
CH3 E H
CH3
p-
HE
25清华大学有机化学李艳梅老师课件有机化学习题课-1

(7):
3' 4'
1,1’-联环丁烷
(9):
二环[4.4.0]癸烷(桥环化合物)
(10):
二环[4.1.0]庚烷(桥环化合物)
螺[4.4]壬烷(螺环化合物) (11):
(12):
二环[2.2.0]己烷(桥环化合物)
(14):
CH3
三甲基二环[3.2.0]庚烷
7 1
(15):
5
6 4 3
2
7,7-二甲基二环[2.2.1]庚烷
100 65 35 30
150 90 70 60
C
C
Ar C R
O
C
CH
205
C H CH2
25
45
第三章 烷烃
烷烃的系统命名:
1.选主链:选择一个最长的碳链作为主链,视为母体, 称为某烷。(碳链尽可能长) 2.当有一种以上的最长碳链可选时,应选择碳链上取代基 最多的碳链作为母体。(取代基数目尽可能多) 3. 对主链编号:从最靠近取代基的一端开始用阿拉伯数字 对主链编号。(取代基前的数字尽可能小)
7.将下列基团按顺序规则由大到小排列。
C
CH
>
C(CH3)3
> C CH2 >
H H C CH2 C C
CH(CH3)2
>
CH2CH3
> CH3
C C C CH C C
第四章 环烷烃
熟悉简单环烷烃的命名(注意取代基的顺反异构); 掌握桥环化合物的命名,标号原则。
环己烷的各种构象,以及联有取代基时最稳定的构象。
4. 取代基的排列秩序:用阿拉伯数字表示取代基的位置, 用汉字表示相同取代基的个数, 小取代基在前,大取代基在后。
有机化学课后习题参考答案

《有机化学》习题参考答案引 言这本参考答案是普通高等教育“十二五”规划教材《有机化学》(周莹、赖桂春主编,化学工业出版社出版)中的习题配套的。
我们认为做练习是训练学生各种能力的有效途径之一,是对自己所学内容是否掌握的一种测验。
因此,要求同学们在学习、消化和归纳总结所学相关知识的基础上完成练习,即使有些可能做错也没有关系,只要尽心去做就行,因为本参考答案可为读者完成相关练习后及时核对提供方便,尽管我们的有些参考答案(如合成题、鉴别题)不是唯一的。
北京大学邢其毅教授在他主编的《基础有机化学习题解答与解题示例》一书的前言中写道:“解题有点像解谜,重在思考、推理和分析,一旦揭开了谜底,就难以得到很好的训练。
” 这句话很符合有机化学解题的特点,特摘录下来奉献给同学们。
我们以为,吃透并消化了本参考答案,将会受益匪浅,对于报考研究生的同学,也基本够用。
第一章 绪论1-1解:(1)C 1和C 2的杂化类型由sp 3杂化改变为sp 2杂化;C 3杂化类型不变。
(2)C 1和C 2的杂化类型由sp 杂化改变为sp 3杂化。
(3)C 1和C 2的杂化类型由sp 2杂化改变为sp 3杂化;C 3杂化类型不变。
1-2解:(1) Lewis 酸 H + , R + ,R -C +=O ,Br + , AlCl 3, BF 3, Li + 这些物质都有空轨道,可以结合孤对电子,是Lewis 酸。
(2)Lewis 碱 x -, RO -, HS -, NH 2, RNH 2, ROH , RSH这些物质都有多于的孤对电子,是Lewis 碱。
1-3解:硫原子个数 n=5734 3.4%6.0832..07⨯=1-4解:甲胺、二甲胺和三甲胺都能与水形成氢键,都能溶于水。
综合考虑烷基的疏水作用,以及能形成氢键的数目(N 原子上H 越多,形成的氢键数目越多),以及空间位阻,三者的溶解性大小为:CH 3NH 2 >(CH 3)2NH >(CH 3)3N1-5解:32751.4%1412.0C n ⨯==,327 4.3%141.0H n ⨯==,32712.8%314.0N n ⨯==,3279.8%132.0S n ⨯==, 32714.7%316.0O n ⨯==, 3277.0%123.0Na n ⨯==甲基橙的实验试:C 14H 14N 3SO 3Na 1-6解: CO 2:5.7mg H 2O :2.9mg第二章 有机化合物的分类和命名2-1解:(1) 碳链异构(2)位置异构(3)官能团异构(4)互变异构2-2解:(1)2,2,5,5-四甲基己烷(2 ) 2,4-二甲基己烷(3)1-丁烯-3-炔(4)2-甲基-3-氯丁烷(5)2-丁胺(6)1-丙胺(7)(E)-3,4-二甲基-3-己烯(8)(3E,5E)-3-甲基-4,5-二氯-3,5-辛二烯(9)2,5-二甲基-2,4-己二烯(10)甲苯(11)硝基苯(12)苯甲醛(13)1-硝基-3-溴甲苯(14)苯甲酰胺(15)2-氨基-4-溴甲苯(16)2,2,4-三甲基-1-戊醇(17)5-甲基-2-己醇(18)乙醚(19)苯甲醚(20) 甲乙醚(21) 3-戊酮(22 ) 3-甲基-戊醛(23)2,4-戊二酮(24)邻苯二甲酸酐(25)苯乙酸甲酯(26)N,N-二甲基苯甲酰胺(27)3-甲基吡咯(28)2-乙基噻吩(29)α-呋喃甲酸(30)4-甲基-吡喃(31)4-乙基-吡喃(32)硬脂酸(33)反-1,3-二氯环己烷(34)顺-1-甲基-2-乙基环戊烷(35)顺-1,2-二甲基环丙烷2-3解:(1)CH3CHCH3CH3CH3CHCH3CH3C(2)CH3CHCH3CH2CH2CH2CH3C2H5(3)CH3CHCH3CHCH22CH3C2H525(4)C2H5HCH3H(5) H2252CH2CH3(6)(7)HCH3HCH3HH(8)3(9)52H5(10)(11) CH3NO2NO2(12)H3(13) (14)OHCOOHBr(15) BrCHOCH3CH3(16)CH3CH2OH(17) OH(18)OH BrBr(19)OHSO3HNO2(20)OO O(21) O(22)O(23)HCH3HCHO(24)H33(25)NHCH3O(26)NH2NH(27)NHO(28)S(29)NCH2H5OCH2H5(30) CH3(CH2)7CH=CH(CH2)7COOH(31)NH2ONH2(32)H2N-CONH-C-NH2O(33) OOO(34)OCHO2-4解:(1)C H3CH2CH3CH3CHCH3CH3C命名更正为:2,3,3-三甲基戊烷(2)C H3CH2CHCHCH3CH3CH3(3)(4)(5)(6)(7)(8)2-5解:可能的结构式2-6解:(1)(2)CH3C2H5CH2CH2CH3CH2CH2CH2CH3(3)CH3CH3CH2CH2CH3CH3C2H5C2H5C2H5CH2CH2CH3 2-7解:1,3-戊二烯1,4-戊二烯H2CH2CH32CH3H31-戊炔2-戊炔H2C2H5CH3CH CH31,2-戊二烯2,3-戊二烯H2333-甲基-1,2-丁二烯第三章饱和烃3-1解:(1) 2,3,3,4-二甲基戊烷(2) 3-甲基-4-异丙基庚烷(3) 3,3-二甲基戊烷(4) 2,6-二甲基-3,6-二乙基辛烷(5) 2,5-二甲基庚烷(6) 2-甲基-3-乙基己烷(7)2-甲基-4-环丙基自己烷(8)1-甲基-3-乙基环戊烷3-2解:(1)H3332CH3(2)(3) H333(4)(5) (6)3-3解:(1) 有误,更正为:3-甲基戊烷(2) 正确(3) 有误,更正为:3-甲基十二烷(4) 有误,更正为:4-异丙基辛烷(5) 4,4-二甲基辛烷(6) 有误,更正为:2,2,4-三甲基己烷3-4解:(3) > (2) > (5) > (1) > (4)3-5解:BrHH HHBr BrHHHHBrBrHHBrHHBrHHB rHH(A)对位交叉式(B)部分重叠式(C)邻位交叉式(D)全重叠式A>C>B>D3-6解:(1)相同(2)构造异构(3)相同(4)相同(5)构造异构体(6)相同3-7解:由于烷烃氯代是经历自由基历程,而乙基自由基的稳定性大于甲基自由基,故一氯甲烷的含量要比一氯乙烷的含量要少。
清华大学有机化学李艳梅老师1第9章

+ E+ electrophileLeabharlann 加合物 与电子云形成微弱作用
H
slow
E
E
-complex
s -complex
E + H+
中间体碳 正离子
加成-消除机理
Free energy
H Y +Z
+Y Z
Progress of the reaction
Y
Z
Addition product
Y + HZ
Addition product
HO CHO
NH2
2-氨基-5-羟基苯甲醛
OH
COOH
3-羟基苯甲酸
Br HO
NH2
3-氨基-5-溴苯酚
9.3 Spectrum Data & Physical Properties
9.3.1 Spectrum data 9.3.2 Physical properties
9.3.1 Spectrum data
9.5.1 Reduction
(A) Catalytic Hydrogenation 催化加氢
CH2CH3 + 3 H2
Ni, 1750C 180 atm
CH2CH3
如果结构中有C=C或CC,则先还原C=C、CC
(B) Birch Reduction
反应:
Na
NH3(l) + C2H5OH
CH3
7.40 7.29
1.25
7.27 2.60
7.40 7.29
8
7
6
5
4
3
2
1
0
PPM
有机化学第13章参考答案

(2) (CH3)3NCH2CH3Cl
(4) H3C
NH2 CH3
H N (5) H3C
O N CH3
O
CH3 N (7)
(9)
CO2H
H NH2
CH3 (6) H2N H
C2H5
(8)
NHC2H5
CH3
(10) H
NH2
H NH2
CH3
Answer: (1):3-甲基-N-甲基-1-丁胺;(2):氯化三甲基乙基胺;(3):1-氨基甲基萘;(4):2,6-二甲基苯胺;(5): 1-甲基-3-甲氨基吡咯-2,5-二酮;(6):(R)-1-甲基-丙胺;(7):N-甲基-N-苯基苯胺;(8)N-乙基环戊 胺;(9):(S)-3-氨基己酸;(10):(2R,3S)-2,3-二氨基-丁烷。
O (5)
(6)
O
OH CH3
1)SO2Cl2 2)NH3
O H N CH3
NaBH4,BF3.OEt2
H N 1) CH2O,
HCl,EtOH
2)OH-
O NH2 Br2,NaOH
CH3
H N CH3O NO来自1) NKBr
O
2)N2H4
NH2
NH2 CH3
KOH
(7)
N
H
CH3I
NH2
(8)
Me 1)NaNO2,HCl
1. NaN3, DMSO 2. LiAlH4, Et2O
CH2NH2
(2) O2N
NH2
1) NaNO2, H2O, H2SO4 2) 加 热
O2N
(3) O2N
CO2H 1) Zn, HCl 2) NaNO2, HCl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章1、(1) 有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent boud)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异是一种有相同化学式而有不同原子排列的化合物的异构现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极距μ=rq。
它是一个矢量,化学中方向规定为从正电荷中心指向负电荷中心。
(6)诱导效应:在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中两个相邻化学键之间的夹角。
(10) Lewis酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11) 疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2、(1) H:S:H(2)H:N:HH(3)H:C:HHH (4) H:C:HO(5)H:C:O:C:HH HH(6) H:O:P:O:H:O(7)H:C:C::C:HHHH H(8)H:C:C:O:HO:HH (9)C:H3、具有偶极的分子:(1)两H原子中心指向O原子方向;(2)由H原子指向Br原子;(4)H原子指向三个Cl原子的中心方向;(5)乙基指向羟基方向4、(1)正庚烷;(2)异丁烷;(3)异已烷;(4)新戊烷6、酸:Cu2+ FCl3CH3CN碱: NH3CH3NH2 C2H5OC2H5加合物: CH3COOH CH3OH7、(1) CH3COOH/CH3COO-H3O+/H2O(2) H2SO4/HSO4-CH3OH2+/CH3OH(3) HNO3/NO3-(CH3)3NH+/(CH3)3N8、(2)CH3F > (3) CH3Cl > (4) CH3Br > (5) CH3I > (1) CH49、 单键最长,双键次之,叁键最短,单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近。
所以说,叁键最短,单键最长,双键处于中间。
10、C5H12OCH3CH2CH2CH2CH2CH3CH2CH2CHCH3CH3CH2CHCH2CH3OHCH3CHCH2CH23CH3CHCHCH3CH3CH3CCH2CH3CH3OHCH2CHCH2CH3 OH3CH3CCH3CH2OHCH311. C8H10N4O2第二章1、(3)> (2) > (1) > (5) > (4)2、链引发Cl2Cl链增长 Cl +CH3CH3CH3CH2+HCl CH3CH2+Cl2CH3CH2Cl+Cl2CH3CH2CH3CH2CH2CH3CH3CH2+Cl CH3CH2Cl2Cl Cl2链终止反应所经历的过渡态:[Cl- H- CH2CH3] [CH3CH2- Cl- Cl】反应所经历的中间体:CH3CH23、2—甲基丁烷较稳定的构象是:(1)3H3HH(2)CHCH3(3)3H3其中(1)和(2)更稳定。
4、(1)CH3Br HCH3BrH(2)CH2CH3H HCH3ClH(3)CHCl CH3BrH HCH2(4) 3(5)2CH3 H35、(1)CH3Br(2)(3)BrBr(4)C ICH3CH36、 (1) H3C3C(CH3)3(2)H3CHH(3)HHHH7、(2) > (1) > (4) > (3)8、(1) 7,7—二甲基三环[2.2.1.02,6]庚烷(2)三环[3.3.1.13,7]癸烷9、(1)Cl(2)CH(CH3)2(3)Br(4)C(CH3)310、CH3CHCH2CH2CH3CH311、该烷烃的分子式为C8H18。
由于只能生成一种一氯产物,说明该烷烃中的18个氢原子是等性的,其结构式为:(CH3)3C3)3。
12、2—甲基—1—溴丙烷的含量为0.6%,2—甲基--2—溴丙烷的含量为99.4%。
第三章1、(1) CH2CHCH2CH3 (2) CH2C(CH3)2(3)H H3CH CH31—丁烯2—甲基—1—丙烯(E)--2—丁烯(4)H3CH HCH3(5) (6)CH3 (z)—2—丁烯环己烷1—甲基环丙烷2、(3)、(4)为共轭化合物;(1)、(3)、(4)有顺反异构。
3、(1)E型(2)E型(3)Z型(4)E型4、(1)沸点:顺—2—丁烯 > 反—2—丁烯,因为顺式的偶极矩大熔点:反式>顺式,因为反式的对称性好,分子排列紧密。
(2)熔点:2—丁炔>1—丁炔,因为2—丁炔对称好,分子排列紧密。
沸点;2—丁炔>1—丁炔,因为末端炔烃具有较低的沸点。
5、CH2CHCHCCH2CH3HC CHHC HCH2CH3H2C(3Z)—1,3—己二烯(3E)--1,3—己二烯H3CC HCHC CCH3HHH3CCHCHC CHCH3H(2E,4Z)—2,4—己二烯(2Z,4E)--2,4—己二烯H3CC H CCHCH2CH3H3CC CCHCH2H3CH(3Z)—2—甲基—1,3戊二烯(3E)--2—甲基1,3戊二烯H 3C CCHH C CH 3CH 2H 3C CC HCH 3HCCH 2(3Z)—3—甲基—1,3戊二烯 (3E )--3—甲基--1,3戊二烯H 2CCHCCH 2CH 2CH 3H 2CCC2CH 3CH32—乙基—1,3—丁二烯 2,3—二甲基—1,3—丁二烯H 2CC HC HC CH 3CH 34—甲基—1,3—戊二烯6、3+> CH 3+>3+> 2+7、生成的主要产物是4—甲基—3—溴环戊烯。
反应机理为自由基取代历程。
8、(1)H 3CC CH 3BrCH 3(2)CH 2ClOH(3) ClCH 2CH 2CCl 3(4) CH 3CH 2CH COCH 3 (5) CH 3C 2CH 3 (6) BrCH 2CH2Br (7)COOH +O(8)CH3Br(9)CH3OH(10)HHCH3(11)(12)O(13)H 3CCN9、化合物的结构式为:反应式:+2H 2Zn 2OHC+OHC CH 2CH CH3CHO10、(1) 第一步用顺丁烯二酸检验,有沉淀生成为1,3—丁二烯;第二步用溴水检验,不褪色者为丁烷;第三步用酸性高锰酸钾溶液检验,褪色者为1—丁烯;余者为甲基环丙烷。
(2)第一步用硝酸银的氨溶液或氯化亚铜的氨溶液检验,有沉淀者为1-戊炔;第二步用溴水检验,不褪色者为环戊烷;第三步用酸性高锰酸钾溶液检验,褪色者为环戊烯。
余者为乙基环丙烷。
11、(1) p-π共轭,σ-p 共轭 (2) p-π共轭,σ-π共轭(3) p-π共轭 (4) π-π共轭, p-π共轭, σ-p 共轭 12、(1)CH 3C CH 3CH 2CH 3CH 3反应为催化加氢,不生成碳正离子反应过程中不会发生碳正离子的重排(2)CH3-C-CH2-CHCH3CH3CH3I不能生成更稳定的碳正离子,反应过程中不会发生谈真理子的重拍(3)CH3-C-CH2CH2BrCH3CH3反应为自由基加成,不生成碳正离子,反应过程中不会发生碳正离子的重排13、 (3)<(1)<(2) 14、(1)+-Cl15、(1)后一个式子是错误,不符合八偶体结构(2)后一个式子是错误,它的未成对电子数目不对(3)正确(4)两个式子间不是单纯的电子转移,原子位置发生了转变 16、17、 A.环丁烷 B.甲基环丙烷 C.1-丁烯 D.2-甲基丙烯 E.F 为顺势和反式2-丁烯 18、19、AC.CH3CHCCH2CH3CH3第四章 1、(2)CCH(3)CH 2Br(4)(5)32、Br3、(1)对叔丁基甲苯 (2)2-硝基-4-氯甲苯 (3)对乙烯基苯甲酸 (4)2,4,6-三硝基甲苯 (5)2——甲基-3-苯基丁烷4、5、CH 2CH CH+CH26、(2)和(7)(1)CHNO2CH2NO2(3)CH3(4)CH3(5)NH2(6)CCl3(7)(8)3 7、8、9、(1)D>E>A>B>C (2)B>D>E>A>C(3)C>A>D>B (4)C>D>B>A10(!)(2)(3)(5)(6)(7)及其对应体,其中(7)采取椅式构象,,cl在e键上,更稳定11、(1)3,6-二甲基-二硝基苯(2)9,10-二溴菲12、13、四甲基苯的异构体有:(1)CH3(2)333(3)3CH3CHCH其中(3)的对称性最好,熔点最高。
14、A33NO 2B C15、(1)(2)(3)25AlCl 3324Cl h rNaOH 醇24ClFeH+/H OBr FeHNO 324(CH 3)2C=CH 216、(1)有 (2)无(3)无 (4)无(5)有 (6)有 17、(1)(2)CH 2CH 318.A 为19.茚茚满第五章1、(1)旋光性:一些物质能使偏振光震动平面旋转的性质称为旋光性(2)右旋,左旋:有的物质能使偏振光振动平面向右旋转称为右旋,有的物质能使偏振光振动平面向左旋转称为左旋。
(3)对映体:互为实物与镜像而不可重叠的一对异构体。
如左旋乳酸与右旋乳酸是一对对映体。
(4)比旋光度:规定旋光管的长度为1dm ,待测物质溶液的浓度为1g/100mL ,在此条件下测得的旋光度叫做该物质的比旋光度。
(5)手性分子:结构上镜像对称而又不能完全重合的分子。
它们不管怎样旋转都不会重合,就像左手和右手那样,称这两种分子具有手性,又叫手性分子。
(6)构型与构象:构型是指具有一定构造的分子中各原子在空间的排列状况。
构象是指在一定的条件下,由于单键的旋转而产生的分子中各原子(或原子团)在空间的不同排布形象。
(7)手性现象:化学分子的实物与其镜像不能重叠的现象。
(8)手性中心:连有四个不同基团的中心碳原子,就可能是手性分子。
它的空间结构可能存在手性,其中心碳原子就是手性中心。
