YY0572-2015血液透析及治疗相关用水质量标准
YY《血液透析及相关治疗用水》等标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK )等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
YY 0572-2015《血液透析及相关治疗用水》等标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
血液透析及其相关治疗用水新标准

国家食品药品监督管理局(CFDA)前不久发布《血液透析及其相关治疗用水》YY 0572—2015,以取代已执行达十年之久的YY0572—2005,并将从2017年1月1日起实施,过度期1年9个月,的确有点长。
我们还是先看看新标准有哪些新变化和新要求吧?
新标准(YY 0572—2015)与旧标准(YY 0572—2005)相比,增加了对总氯、锑、铍、铊四种化学物最大允许量的要求;提高了对内毒素的控制要求;删除了对氯胺、氯、锡三种化学污染物最大允许量的要求;均比老标准要求高而严了。
透析用水的基本概念与干预水平
透析用水:是指满足于YY 0572-2015要求的且适用于血液透析用途的水,包括透析液的制备用水、透析器的相处理用水、透析浓缩液的制备用水和在线置换液制备用水。
干预水平:污染物浓度,当达到该浓度时应采取干预措施阻断其升高至不可接受的水平。
新标准对微生物与内毒素含量的要求
(1)透析用水中的细菌总量:应不超过100cfu/ml,干预水平是最大允许水平的50%。
(2)透析用水中的内毒素含量:应不超过ml,干预水平是最大允许水平的50%。
新标准对化学污染的最大允许量要求
(1)透析用水中有毒化学物的最大允许量(mg/L):铝、总氯、铜、氟化物、铅、盐酸盐(氮)2、硫酸盐100、锌。
(2)透析溶液中的电解质最大允许量mg/L(mmol/L):钙2、镁4()、钾8()、钠70()。
(3)透析用水中微量元素的最大允许量(mg/L):锑、砷、钡、铍、镉、铬、汞、硒、银、铊。
YY 0572-2015《血液透析及相关治疗用水》等标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
透析液和透析用水质量监测制度
透析液和透析用水质量监测制度
透析液和透析用水质量监测制度
一、做好水处理设备的维护与养护。
二、做好透析用水水质和透析液的监控。
1、透析用水每月进行1次细菌培养,采样部位为反渗水输水管路的末端,细菌数不能超过100cfu/ml。
2、透析液每月进行一次细菌培养,采样部位为透析液进入透析器的位置,细菌数不能超过100cfu/ml。
3、每季度进行一次透析用水、透析液内毒素检测,采样部位同上,要求透析用水内毒素<0.25EU/ml、透析液内毒素<0.5EU/ml。
4、透析用水的化学污染物情况至少每年测定一次,软水硬度及游离氯检测至少每周进行一次,透析用水必须符合中华人民共和国医药业标准《血液透析和相关治疗用水》(YY0572—2015)。
透析用水允许的化学污染物的最大浓度。
YY0572_2016年《血液透析和相关治疗用水》等标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
关于批准发布YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准的公告

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
血液透析中心透析液和透析用水的质量监测制度

血液透析中心透析液和透析用水的质量监测制度
1.每年每台机器应至少进行一次透析液的细菌和内毒素检测。
透析用水和透析液培养方法参照YY0572-2-2015标准规范执行,可选择胰化蛋白脓葡萄糖培养基(TGEA)、R2A营养琼脂培养基或其他确认能提供相同结果的培养基,不能使用血琼脂培养基和巧克力琼脂培养基。
推荐17〜23。
C的培养温度和7天的培养时间。
2,应使用宣试剂法测定内毒素,或其他确认能提供相同结果的检测方法。
3.每月进行一次细菌检测,细菌数量WlOoCFU/ml;细菌数量250CFU∕ml应进行干预。
4.至少每3个月进行一次内毒素检测,透析用水内毒素≤0.25EU∕ml,透析液内毒素W0.5EU∕ml;超过最大允许水平的50%应进行干预。
5.透析用水的细菌或内毒素水平达到干预水平,应对水处理系统进行消毒;透析用水的细菌和内毒素水平合格,而透析液的细菌或内毒素水平超标,应对所有同型号透析机进行透析液细菌和内毒素检测,并校验透析机消毒程序。
对于不符合或达到干预标准的水处理系统和/或透析机,必须重新消毒且符合标准后方可使用。
YY05722015《血液透析及相关治疗用水》等标准

本标准适用于体部X辐射放射治疗立体定向及计划系统。该系统与医用电子加速器配合使用,对体部病变区域进行立体定向放射治疗。本标准规定了体部X辐射放射治疗立体定向及计划系统的术语和试验方法等要求。
(十二)YY0952-2015《医用控温毯》
本标准适用于在医疗机构临床使用环境下,通过控制设备内循环液体的温度,具有对人体进行体外物理升温和/或降温功能,达到辅助调节人体温度目的的设备。本标准规定了医用控温毯的术语、定义、分类、组成、试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。本标准不适用于热垫式治疗仪、仅用于四肢和额头冷/热敷的设备。
(三)YY0599-2015《激光治疗设备准分子激光角膜屈光
治疗机》
本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。本标准替代YY0599-2007《准分子激光角膜屈光治疗机》。
(九)YY 0948-2015《心肺转流系统一次性使用动静脉插管》
本标准适用于心肺转流系统一次性使用动静脉插管,供体外循环施行心脏直视手术时配套心肺转流系统引流或灌注血液使用。本标准规定了无菌的一次性使用动静脉插管的分类与结构、试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
(十)YY0950-2015《气压弹道式体外压力波治疗设备》ﻩ本标准适用于利用压缩空气产生的能量驱动治疗手柄内的子弹体,使子弹体脉冲式冲击治疗头,利用二者的弹性碰撞产生压力波,经皮传导作用于疼痛部位治疗的设备。本标准规定了气压弹道式体外压力波治疗设备的术语、定义、组成、试验方法、检验规则、标志、使用说明书、包装、运输和贮存等要求。本标准不适用于气压弹道式碎石设备。
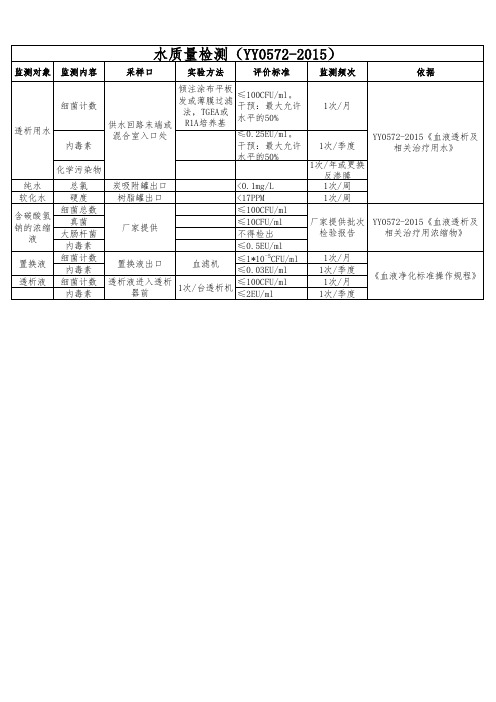
血透室水质量检测(YY0572-2015)
1次/月
1次/季度 1次/年或更 换反渗来自 1次/周 1次/周YY0572-2015《血液透析及 相关治疗用水》
厂家提供
厂家提供批 YY0572-2015《血液透析及 次检验报告 相关治疗用浓缩物》 1次/月 1次/季度 1次/月 1次/季度
内毒素 ≤0.5EU/ml 细菌计数 ≤1*10-5CFU/ml 置换液出口 血滤机 内毒素 ≤0.03EU/ml 细菌计数 透析液进入透析 ≤100CFU/ml 1次/台透析机 器前 内毒素 ≤2EU/ml
《血液净化标准操作规程 》
水质量检测(YY0572-2015)
监测对象 监测内容 实验方法 评价标准 倾注涂布平 板发或薄膜 ≤100CFU/ml。 细菌计数 过滤法, 干预:最大允许 TGEA或R1A培 水平的50% 供水回路末端或 养基 透析用水 混合室入口处 ≤0.25EU/ml。 内毒素 干预:最大允许 水平的50% 化学污染物 纯水 软化水 含碳酸 氢钠的 浓缩液 置换液 透析液 总氯 硬度 细菌总数 真菌 大肠杆菌 炭吸附罐出口 树脂罐出口 <0.1mg/L <17PPM ≤100CFU/ml ≤10CFU/ml 不得检出 采样口 监测频次 依据
YY0572-2015《血液透析和相关治疗用水》等实用标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名.

附件YY 0572-2015《血液透析及相关治疗用水》等 90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
YY0572-2015《血液透析及其相互治疗用水》等规范标准

附件YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准编号、名称及适用范围一、强制性行业标准(共14项)(一)YY 0572-2015《血液透析及相关治疗用水》本标准适用于血液透析、血液透析滤过和在线血液滤过或在线血液透析滤过中制备透析浓缩液、透析液和血液透析器再处理用水。
本标准规定了相关用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
本标准不适用于透析液再生系统。
本标准代替YY 0572-2005《血液透析和相关治疗用水》。
(二)YY 0598-2015《血液透析及相关治疗用浓缩物》本标准适用于血液透析及相关治疗用浓缩物。
本标准规定了浓缩物的化学成分组成及其纯度,微生物污染的监测,浓缩物的处理、度量和标识,容器的要求和浓缩物质量检验所需要的各项测试等要求。
本标准不适用于治疗中浓缩物与透析用水配制成最终使用浓度的混合过程和透析液的再生系统。
本标准代替YY 0598-2006《血液透析及相关治疗用浓缩物》。
(三)YY 0599-2015《激光治疗设备准分子激光角膜屈光治疗机》本标准适用于准分子激光角膜屈光治疗机(以下简称治疗机),治疗机采用193nm准分子激光去除角膜组织来改变角膜形状从而改善视力,主要用于屈光性角膜切削术(PRK)、原位角膜磨镶术(LASIK)等角膜屈光矫正术和治疗性角膜切削术(PTK)。
本标准规定了治疗机的术语、定义、结构、基本参数、试验方法、检验规则、标志、包装、运输和贮存等要求。
本标准替代YY 0599-2007《准分子激光角膜屈光治疗机》。
(四)YY 0603-2015《心血管植入物及人工器官心脏手术硬壳贮血器/静脉贮血器系统(带或不带过滤器)和静脉贮血软袋》本标准适用于多功能系统的贮血器件,该系统可能有整体性的部件,如血气交换器(氧合器)、血液过滤器、祛泡器、血泵等。
本标准规定了对无菌、一次性使用的体外循环心脏手术硬壳贮血器、静脉贮血器系统(带或不带过滤器)和静脉贮血软袋(简称贮血器)的试验方法、标志、标签、使用说明书、包装、运输和贮存等要求。
透析用水微生物检测方法新标准

透析用水微生物检测方法新标准,您知多少?“《血液透析及其相关治疗用水》新标准•新瞧点”新标准YY0572-2015规定透析用水中的细菌总量应不超过100CFU/mL,干预水平就是最大允许水平的50%。
除此以外,新标准内规定的微生物的检测方法与旧标准相比发生了变化,而这个不为人注意的变化将会对未来透析治疗的开展产生巨大并且深远的影响。
【微生物检测方法比较】旧标准YY0572-2005检测微生物方法如下:●方法一:试样应在收集后30min内进行化验或立即放在1℃-5℃下储存,并按常规程序在收集后24h内化验。
采用常规的微生物检验方法(倾注平板法)获得细菌总数计数(标准培养皿计数)。
培养基应为胰蛋白酶大豆琼脂培养基或等价物。
计算菌落数目应在35-37℃培养48h后进行。
48h后呈阴性,可于72h后再检查。
●方法二:即采用膜过滤技术滤除500ml-1000ml水,并在像R2A这样的低营养琼脂培养基上,可在28℃-32℃下培养5天或更长时间。
新标准YY0572-2015检测微生物方法如下:●试样应在收集后4h内进行检测或立即冷藏,并在收集后24h内检测,应采用常规的微生物检测方法(倾注平板法、涂布平板法、薄膜过滤法)获得细菌总数(标准培养皿计数),薄膜过滤法就是首选的检测方法,但不接受接种环法。
●可以参考采用《中华人民共与国药典(二部)》(2010年版)中规定的方法;或培养基宜选用胰化蛋白胨葡萄糖培养基(TGEA)、R2A低营养琼脂培养基或其她确认能提供相同结果的培养基,不能使用血琼脂培养基与巧克力琼脂培养基,推荐使用17-23℃的培养温度与168h(7d)的培养时间,确认能提供相同培养结果的其她培养时间与温度也适用。
新旧标准比较下最重要的变化就在于培养基的选择上。
旧标准下使用的血琼脂培养基与巧克力琼脂培养基就是动物血液加上普通琼脂平板制成的,营养太丰富会杀死水生细菌,所以临床人员在以往的检测得出的大部分结果都就是未检出细菌或者细菌数为零。
透析用水微生物检测方法新标准

透析用水微生物检测方法新标准(总2页)-CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除透析用水微生物检测方法新标准,你知多少?“《血液透析及其相关治疗用水》新标准?新看点”新标准YY0572-2015规定透析用水中的细菌总量应不超过100CFU/mL,干预水平是最大允许水平的50%。
除此以外,新标准内规定的微生物的检测方法与旧标准相比发生了变化,而这个不为人注意的变化将会对未来透析治疗的开展产生巨大并且深远的影响。
【微生物检测方法比较】旧标准YY0572-2005检测微生物方法如下:●方法一:试样应在收集后30min内进行化验或立即放在1℃-5℃下储存,并按常规程序在收集后24h内化验。
采用常规的微生物检验方法(倾注平板法)获得细菌总数计数(标准培养皿计数)。
培养基应为胰蛋白酶大豆琼脂培养基或等价物。
计算菌落数目应在35-37℃培养48h后进行。
48h后呈阴性,可于72h后再检查。
●方法二:即采用膜过滤技术滤除500ml-1000ml水,并在像R2A这样的低营养琼脂培养基上,可在28℃-32℃下培养5天或更长时间。
新标准YY0572-2015检测微生物方法如下:●试样应在收集后4h内进行检测或立即冷藏,并在收集后24h内检测,应采用常规的微生物检测方法(倾注平板法、涂布平板法、薄膜过滤法)获得细菌总数(标准培养皿计数),薄膜过滤法是首选的检测方法,但不接受接种环法。
●可以参考采用《中华人民共和国药典(二部)》(2010年版)中规定的方法;或培养基宜选用胰化蛋白胨葡萄糖培养基(TGEA)、R2A低营养琼脂培养基或其他确认能提供相同结果的培养基,不能使用血琼脂培养基和巧克力琼脂培养基,推荐使用17-23℃的培养温度和168h(7d)的培养时间,确认能提供相同培养结果的其他培养时间和温度也适用。
新旧标准比较下最重要的变化就在于培养基的选择上。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
YY 0 5 7 2 —2 0 1 5代替YY 0 5 7 2 —2 0 0 5血液透析及相关治疗用水W a t e r fo r h a e m o d ia l y s is a n d r e l a t e d th e r a p ie s( IS O 1 3 9 5 9 : 2 0 0 9 , M OD)2 0 1 5 - 03 - 0 2 发布 2 0 1 7 - 0 1 - 0 1 实施国家食品药品监督管理总局发布Y Y 0 5 7 2 — 2 0 1 5-J—刖g本标准按照GB /T 1 . 1 - 2 0 0 9 给出的规则起草。
本标准代替YY 0 5 7 2 —2 0 0 5 《血液透析和相关治疗用水》。
与YY 0 5 7 2 —2 0 0 5 的主要技术差异如下:——增加对总氯、锑、铍、铊四种化学污染物最大允许量的要求;——提高对内毒素的要求;——删除对氯胺、氯、锡等三种化学污染物最大允许量的要求;——增加了附录A( 资料性附录)、附录B ( 资料性附录)。
本标准修改采用国际标准IS O 1 3 9 5 9 : 2 0 0 9 《血液透析及相关治疗用水》。
本标准与IS O 1 3 9 5 9 :2 0 0 9 相比,主要差异如下:——删除已在GB /T 1 3 0 7 4 —2 0 0 9 界定的术语和定义;——增加了附录B ( 资料性附录);——相关技术要求和试验方法有修改。
请注意本文件的某些内容可能涉及专利。
本文件的发布机构不承担识别这些专利的责任。
本标准由国家食品药品监督管理总局提出。
本标准由全国医用体外循环设备标准化技术委员会( S AC /T C 1 5 8 ) 归口。
本标准起草单位:国家食品药品监督管理局广州医疗器械质量监督检验中心。
本标准主要起草人:吴静标、吴伟荣。
本标准于2 0 0 5 年首次发布,2 0 1 5 年第一次修订。
IY Y 0 5 7 2 — 2 0 1 5血液透析及相关治疗用水1 范围本标准规定了血液透析、血液透析滤过和在线(on- line ) 血液滤过或在线(on- line ) 血液透析滤过中制备透析浓缩液和透析液及血液透析器再处理所用水的最低要求。
本标准不涉及水处理设备的操作,亦不涉及由处理水与浓缩物混合后制成供治疗用的透析液。
这些操作只能由专业透析人员负责操作。
本标准不适用于透析液再生系统。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本 ( 包括所有的修改单 ) 适用于本文件。
GB /T 1 3 0 7 4 —2 0 0 9 血液净化术语中华人民共和国药典 ( 二部)( 2010 年版)3 术语和定义3 . 1 3 . 23 . 3GB /T 1 3 0 74 界定的及下列术语和定义适用于本文件。
干预水平 a c t io n l e v e l污染物浓度,当达到该浓度时应采取干预措施阻断其升高至不可接受的水平。
总氯 c h lo r in e to t a l游离氯和结合氯的总和。
注:氯在水中主要以溶解的氯分子 ( 游离氯)或化学物形式(结合氯)的形式存在。
结合氯的主要成分是氯胺,常用于水源消毒。
透析用水 d i a l y s i s w a t e r满足本标准的要求且适用于血液透析用途的水,包括透析液的制备用水、透析器的再处理用水、透析浓缩液的制备用水和在线置换液制备用水。
4 要求4 . 1 微生物要求透析用水中的细菌总数应不超过1 0 0 CFU/m L,干预水平应建立在系统微生物动力学知识之上。
通常,干预水平是最大允许水平的5 0 %。
透析用水中的内毒素含量应不超过0 . 2 5 EU/m L。
必须建立干预水平,通常,是最大允许水平的5 0 %。
注:见A. 1中关于这些要求的历史。
4 . 2 化学污染物透析用水中化学污染物的浓度应不超出表 1 和表 2 的规定。
注:见附录A. 2中对给出值的解释。
当透析用水用于血液透析器的再处理时 ( 清洗、测试和混合消毒剂),应警示用户,透析用水应符合本标准的要求,透析用水应在进入透析器再处理设备的入口处进行检测。
1Y Y 0 5 7 2 — 2 0 1 5 表 1 透析用水中有毒化学物和透析溶液电解质的最大允许量55 . 1 验证和监测透析用水按照4 .1 和4 .2 的规定,透析用水的水质应在安装水处理装置时验证,透析用水水质的监测应在安装后实行。
2Y Y 0 5 7 2 — 2 0 1 55 . 2 透析用水的微生物试验应在透析装置和供水回路的连接处收集试样,取样点应在供水回路的末端或在混合室的入口处。
试样应在收集后4 h 内进行检测,或立即冷藏,并在收集后2 4 h 内检测,应采用常规的微生物检测方法 ( 倾注平板法、涂布平板法、薄膜过滤法 ) 获得细菌总数 ( 标准培养皿计数),薄膜过滤法是首选的检测方法,但不接受接种环法。
可以参考采用《中华人民共和国药典 ( 二部)K2 0 1 0 年版)中规定的方法;或培养基宜选用胰化蛋白胨葡萄糖培养基( T GEA)、R2 A 营养琼脂培养基( R2 A) 或其他确认能提供相同结果的培养基,不能使用血琼脂培养基和巧克力琼脂培养基,推荐使用1 7 °C2 3 °C的培养温度和1 6 8 h( 7 d)的培养时间,确认能提供相同培养结果的其他培养时间和温度也适用。
没有方法可以给出微生物总数。
应使用鲎试剂法测定内毒素,其他确认能提供相同结果的检测方法也适用。
5 . 3 化学污染物的检测方法依照表 1 所中列出的要求,使用的化学分析方法可以参考《中华人民共和国药典 ( 二部)》( 2010 年版),参考美国公共卫生协会的方法、参考美国环保局的方法,或其他等同有效的方法。
表3 列出了每种污染物的检测方法。
表3 化学污染物的分析方法3Y Y 0 5 7 2 — 2 0 1 5表 3 ( 续 )附录 A ( 资料性附录)I S O 1 3 9 5 9 : 2 0 0 9 标准形成和规定的基本依据A . 1 透析用水的微生物学注:本章中的内容是供读者了解IS O 1 3 9 5 9 : 2 0 0 9 标准中微生物限度制定的历史过程。
最初用于制备透析溶液的水是被认为是不需要消毒的。
但是,很多研究已经证明热原反应的发作比率与透析溶液中细菌的数量直接相关( Da w ids a nd Ve jls g a a r d[ 1 3 ] ;Fa v e r o e t a l. [ 1 7 ] ;Fa v e r o e t a l. [ 1 8 ] ),这些研究为1 9 8 2 年出版的关于水质最早的AAMI 标准规定透析用水中2 0 0 CFU/m L 的细菌最高水平提供了基本依据。
后来,欧洲组织使用了一个要更低一些的水平(1 0 0 CFU/m L) 作为他们透析用水的细菌限度,该规定已被IS O 1 3 9 5 9 : 2 0 0 9 标准所采用。
由于从透析液样品的采集到获得检测结果可能需要7 d,而细菌的增殖可能很迅速,因此本标准采用干预水平法进行检测。
干预水平法规定检测者在检测结果超出本标准规定的最大限值之前应启动纠正措施。
很多研究组织已经确认热原反应是由来源于革兰氏阴性细菌的脂多糖和内毒素所引起,并且革兰氏阴性水生细菌已经表现出在经蒸馏、去离子、反渗透和软化处理所制备的透析用水中具有快速倍增的能力。
用这些水制备的透析溶液同样也为这种类型的细菌提供了一个非常好的生长环境。
即使在低水平的微生物污染物时,由透析系统外源性内毒素所引起的热原反应也已经有报道 ( 例如出现在社区供水系统中)(Hindm a ne ta l. M)。
那么,透析用水的内毒素含量设定一个上限值是很有必要的。
AAMI 采用1 EU/m L 的水平作为内毒素的上限值,因为当前使用反渗透法、超滤法或两者都使用的水处理系统能够容易达到这个水平。
同时,欧洲组织规定0 . 2 5 EU/m L 为内毒素的上限值。
在IS O 1 3 9 5 9 :2 0 0 9 标准2 0 0 8 年的修订过程中,0 . 2 5 EU/m L 的限值被列入作为透析用水内毒素的上限值。
A . 2 化学污染物的检测方法以下内容是为帮助读者理解透析治疗用水中化学污染物的注意事项。
Y Y 0 5 7 2 — 2 0 1 5可能存在于透析用水中的需要对其允许水平进行限定的污染物,在IS O 1 3 9 5 9 : 2 0 0 9 标准中被分成三类。
第一类为对透析患者产生毒性的化学物,这些化学物包括氟化物、铝、氯胺、硫酸盐、硝酸盐、铜、锌和铅,将氯包括在内是因为其潜在的毒性。
各类透析患者的氟中毒通常被认为与1 mg /L 的氟化水相关的说法,是被质疑的。
在氟化物对尿毒症骨病的影响作用缺乏共识的情况下,基于慎重起见,在最初规定了透析溶液中氟化物的水平(Ra o a nd Frie dma n™ ) Q后来,有一例由于市政供水中氟化物过量导致的事故被报道,所有8 位透析患者都有中毒症状,其中有一位患者死亡(CDC[ n] )。
用于透析的水仅经过水软化装置进行处理,氟化物浓度高达5 0 mg /L。
如果透析用水使用去离子或反渗透装置处理过,即使不停止透析,可能也不会出现太严重的病症。
另外一个例子中,当所使用的去离子剂耗尽后,1 5 位患者中有1 2 位出现由氟化物中毒所引起的急症( Amow e t a l.[ 5 ] ) ,3 位患者死于心室颤动。
用于制备透析溶液的水中氟化物的浓度高达 2 2 5 mg /L 0推荐铝浓度的最大值是用于阻止这种金属的毒性在患者体内蓄积(Kov a lc hik e t a l [ 2 9 ] ;Ma s uy a mad T a C hib a na [ 3 2 ] )。
用含铝化合物进行水处理的方法改变很可能会造成铝浓度的突然升高。
跟氟化物一样,即使在a n透析用水的化学检测中,铝浓度可能出现显著的增加,水处理也是保证安全性的方法。
氯胺的毒性是不容置疑的(Ea ton e t a l. [ 1 4 ] ),虽然游离氯在氧化血液中的破坏机理还不清楚,但是它具有潜在的高氧化性和可以转化为氯胺的能力,本标准建议在制备透析溶液时避免使用含较高氯的水。
氯在水中可以以游离氯和化合物两种形式存在,氯胺是氯化合物的一种形式,确定氯胺浓度通常需要同时测量总氯和游离氯,比较这两种氯浓度的差异来为氯胺定值,在IS O 1 3 9 5 9 :2 0 0 9 标准2 0 0 8 年的修订过程中,工作组选择通过设置总氯的最大允许水平来简化这种情况,采用与先前氯胺(0 .1 mg /L) 的限量相同的值,因此允许使用一个单一的测试方法。
