化学方程式--浙教版
浙教版九年级上册化学方程式

浙教版九年级上册化学方程式一、氧气相关的化学方程式。
1. 镁在空气中燃烧。
- 化学方程式:2Mg + O_2{点燃}{===}2MgO- 现象:剧烈燃烧,发出耀眼的白光,生成白色固体。
2. 铁在氧气中燃烧。
- 化学方程式:3Fe + 2O_2{点燃}{===}Fe_3O_4- 现象:剧烈燃烧,火星四射,生成黑色固体。
3. 铜在空气中受热。
- 化学方程式:2Cu+O_2{}{===}2CuO- 现象:红色固体逐渐变黑。
4. 铝在空气中氧化。
- 化学方程式:4Al + 3O_2===2Al_2O_3- 现象:铝表面变暗,生成一层致密的氧化铝薄膜。
5. 氢气在空气中燃烧。
- 化学方程式:2H_2+O_2{点燃}{===}2H_2O- 现象:产生淡蓝色火焰,放出热量,烧杯内壁有水雾。
6. 红磷在空气中燃烧。
- 化学方程式:4P + 5O_2{点燃}{===}2P_2O_5- 现象:产生大量白烟,放出热量。
7. 硫粉在空气中燃烧。
- 化学方程式:S+O_2{点燃}{===}SO_2- 现象:在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,生成有刺激性气味的气体。
二、制取氧气的化学方程式。
1. 加热高锰酸钾制取氧气。
- 化学方程式:2KMnO_4{}{===}K_2MnO_4+MnO_2+O_2↑- 实验装置:固体加热型装置,需要用到酒精灯、试管、铁架台等仪器。
2. 加热氯酸钾和二氧化锰制取氧气。
- 化学方程式:2KClO_3frac{MnO_2}{}2KCl + 3O_2↑- 二氧化锰在该反应中起催化作用,反应前后质量和化学性质不变。
3. 过氧化氢分解制取氧气。
- 化学方程式:2H_2O_2{MnO_2}{===}2H_2O+O_2↑- 该反应不需要加热,二氧化锰是催化剂,能加快反应速率。
三、碳和碳的化合物相关化学方程式。
1. 碳在氧气中充分燃烧。
- 化学方程式:C + O_2{点燃}{===}CO_2- 现象:发出白光,放出热量。
最新浙教版初中化学方程式

浙教版初中化学方程式大全化合反应1、镁在空气中燃烧:2Mg+O2 2MgO2、铁在氧气中燃烧:3Fe+2O2 Fe3O43、铝在空气中燃烧:4Al+3O2 2Al2O34、氢气在空气中燃烧:2H2+O2 2H2O5、红磷在空气中燃烧:4P+5O2 2P2O56、硫粉在空气中燃烧:S+O2 SO27、碳在氧气中充分燃烧:C+O2 CO28、碳在氧气中不充分燃烧:2C+O2 2CO9、二氧化碳通过灼热碳层:C+CO2 2CO10、一氧化碳在氧气中燃烧:2CO+O2 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O14、钠在氯气中燃烧:2Na+Cl2 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 2H2O+O2↑16、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑23、氢气还原氧化铜:H2+CuO Cu+H2O24、木炭还原氧化铜:C+2CuO 2Cu+CO2↑25、水蒸气通过灼热碳层:H2O+C H2+CO26、焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO428、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O30、一氧化碳还原氧化铜:CO+CuO Cu+CO231、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO232、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+2HCl==2NaCl+H2O+CO2↑一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧:2Mg+O2 2MgO2. 铁在氧气中燃烧:3Fe+2O2 Fe3O43. 铜在空气中受热:2Cu+O2 2CuO4. 铝在空气中燃烧:4Al+3O2 2Al2O35. 氢气中空气中燃烧:2H2+O2 2H2O6. 红磷在空气中燃烧:4P+5O2 2P2O57. 硫粉在空气中燃烧:S+O2 SO28. 碳在氧气中充分燃烧:C+O2 CO29. 碳在氧气中不充分燃烧:2C+O2 2CO⑵化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2 2CO211. 甲烷在空气中燃烧:CH4+2O2 CO2+2H2O12. 酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 2H2↑+O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 2CuO+H2O+CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 2KCl+3O2↑16. 加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H2CO3==H2O+CO2↑18. 高温煅烧石灰石:CaCO3 CaO+CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+CuO Cu+H2O20. 木炭还原氧化铜:C+2CuO 2Cu+CO2↑21. 焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑22. 焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑23. 一氧化碳还原氧化铜:CO+CuO Cu+CO224. 一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO2四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2↑27. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑29. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑31. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑32. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu36. 铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg⑶碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O39. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O41. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O42. 氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O⑷酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O 45.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O⑸酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49. 盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+ 6H2O58.硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应: MgCO3+2HCl==MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑺碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH⑻盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO371.硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O==H2CO373.生石灰溶于水:CaO+H2O==Ca(OH)274.氧化钠溶于水:Na2O+H2O==2NaOH75.三氧化硫溶于水:SO3+H2O==H2SO476.硫酸铜晶体受热分解:CuSO4•5H2O CuSO4+5H2O77.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O化学方程式反应现象应用2Mg+O2 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2 2HgO银白液体、生成红色固体拉瓦锡实验2Cu+O2 2CuO红色金属变为黑色固体4Al+3O2 2Al2O3银白金属变为白色固体3Fe+2O2 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热C+O2 CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2 2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2 2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3 2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4 K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgO 2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O 2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3 2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3 NH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4==Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2 W+3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 Mo+3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2 2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 2HCl 苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O2 2CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O2 2CO2蓝色火焰煤气燃烧C+CuO 2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 4Fe+3CO2↑冶炼金属Fe3O4+2C 3Fe+2CO2↑冶炼金属C+CO2 2COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3 CO2↑+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3↓+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2 CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3 Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl==CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl==2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl==MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+CO Cu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO 2Fe+3CO2冶炼金属原理Fe3O4+4CO 3Fe+4CO2冶炼金属原理WO3+3CO W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2 2CO2+4H2OC2H5OH+3O2 2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl==2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl==2AlCl3+3H2O白色固体溶解Na2O+2HCl==2NaCl+H2O白色固体溶解CuO+2HCl==CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl==ZnCl2+H2O白色固体溶解MgO+2HCl==MgCl2+H2O白色固体溶解CaO+2HCl==CaCl2+H2O白色固体溶解NaOH+HCl==NaCl+H2O白色固体溶解Cu(OH)2+2HCl==CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl==MgCl2+2H2O白色固体溶解Al(OH)3+3HCl==AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl==FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl==CaCl2+2H2OHCl+AgNO3==AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4==MgSO4+H2O白色固体溶解2NaOH+H2SO4==Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4==BaSO4↓+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O 吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3↓+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2↓+2NaClCuCl2+2NaOH==Cu(OH)2↓+2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3↓+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3↓+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3↓+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3↓+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4•H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4↓+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3↓+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+ CO2↑NH4NO3+NaOH==NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体。
浙教版科学八下化学反应式及现象汇总

浙教版科学八下化学反应式及现象汇总
化学反应式和现象是研究化学的基础,通过总结和归纳这些反应式和现象,可以更好地理解化学的基本原理和规律。
本文将对浙教版科学八下化学课程中研究的一些重要的化学反应式和现象进行总结。
化学反应式
1. 酸与碱的中和反应式:
- 酸 + 碱→ 盐 + 水
- 例如:HCl + NaOH → NaCl + H2O
2. 金属与酸的反应式:
- 金属 + 酸→ 盐 + 氢气
- 例如:Zn + H2SO4 → ZnSO4 + H2
3. 盐的化合价:
- 盐中阳离子的化合价通常是固定的
- 例如:NaCl中的Na离子化合价为+1
4. 氧化还原反应式:
- 包括氧化反应和还原反应,涉及电子的转移
- 例如:2Mg + O2 → 2MgO
化学现象
1. 金属的腐蚀现象:
- 金属长期接触空气或水会发生腐蚀
- 例如:铁制品长时间暴露在潮湿的环境中会生锈
2. 盐的溶解现象:
- 盐在水中容易溶解,形成溶液
- 例如:将食盐加入水中可以得到食盐水
3. 酸碱指示剂变色现象:
- 酸性溶液和碱性溶液的性质不同,可以通过酸碱指示剂的变色来区分
- 例如:酸性溶液中酸碱指示剂会变红,碱性溶液中酸碱指示剂会变蓝
4. 化学反应释放热现象:
- 某些化学反应会释放出热量
- 例如:燃烧反应会释放大量热能
以上是浙教版科学八下化学课程中一些重要的化学反应式和现
象的汇总。
通过对这些反应式和现象的学习和理解,可以更好地掌
握化学的基本知识,并且在实验和应用中能够更好地应用相关知识。
(完整word版)浙教版初中化学方程式

浙教版初中化学方程式大全化合反应1、镁在空气中燃烧:2Mg+O2 2MgO2、铁在氧气中燃烧:3Fe+2O2 Fe3O43、铝在空气中燃烧:4Al+3O2 2Al2O34、氢气在空气中燃烧:2H2+O2 2H2O5、红磷在空气中燃烧:4P+5O2 2P2O56、硫粉在空气中燃烧:S+O2 SO27、碳在氧气中充分燃烧:C+O2 CO28、碳在氧气中不充分燃烧:2C+O2 2CO9、二氧化碳通过灼热碳层:C+CO2 2CO10、一氧化碳在氧气中燃烧:2CO+O2 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O14、钠在氯气中燃烧:2Na+Cl2 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 2H2O+O2↑16、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑23、氢气还原氧化铜:H2+CuO Cu+H2O24、木炭还原氧化铜:C+2CuO 2Cu+CO2↑25、水蒸气通过灼热碳层:H2O+C H2+CO26、焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO428、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O30、一氧化碳还原氧化铜:CO+CuO Cu+CO231、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO232、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+2HCl==2NaCl+H2O+CO2↑一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧:2Mg+O2 2MgO2. 铁在氧气中燃烧:3Fe+2O2 Fe3O43. 铜在空气中受热:2Cu+O2 2CuO4. 铝在空气中燃烧:4Al+3O2 2Al2O35. 氢气中空气中燃烧:2H2+O2 2H2O6. 红磷在空气中燃烧:4P+5O2 2P2O57. 硫粉在空气中燃烧:S+O2 SO28. 碳在氧气中充分燃烧:C+O2 CO29. 碳在氧气中不充分燃烧:2C+O2 2CO⑵化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2 2CO211. 甲烷在空气中燃烧:CH4+2O2 CO2+2H2O12. 酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 2H2↑+O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 2CuO+H2O+CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 2KCl+3O2↑16. 加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H2CO3==H2O+CO2↑18. 高温煅烧石灰石:CaCO3 CaO+CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+CuO Cu+H2O20. 木炭还原氧化铜:C+2CuO 2Cu+CO2↑21. 焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑22. 焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑23. 一氧化碳还原氧化铜:CO+CuO Cu+CO224. 一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO2四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2↑27. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑29. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑31. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑32. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu36. 铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg⑶碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O39. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O41. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O42. 氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O⑷酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O 45.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O⑸酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49. 盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+ 6H2O58.硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应: MgCO3+2HCl==MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑺碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH⑻盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO371.硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O==H2CO373.生石灰溶于水:CaO+H2O==Ca(OH)274.氧化钠溶于水:Na2O+H2O==2NaOH75.三氧化硫溶于水:SO3+H2O==H2SO476.硫酸铜晶体受热分解:CuSO4•5H2O CuSO4+5H2O77.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O化学方程式反应现象应用2Mg+O2 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2 2HgO银白液体、生成红色固体拉瓦锡实验2Cu+O2 2CuO红色金属变为黑色固体4Al+3O2 2Al2O3银白金属变为白色固体3Fe+2O2 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热C+O2 CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2 2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2 2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3 2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4 K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgO 2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O 2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3 2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3 NH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4==Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2 W+3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 Mo+3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2 2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 2HCl 苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O2 2CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O2 2CO2蓝色火焰煤气燃烧C+CuO 2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 4Fe+3CO2↑冶炼金属Fe3O4+2C 3Fe+2CO2↑冶炼金属C+CO2 2COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3 CO2↑+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3↓+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2 CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3 Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl==CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl==2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl==MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+CO Cu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO 2Fe+3CO2冶炼金属原理Fe3O4+4CO 3Fe+4CO2冶炼金属原理WO3+3CO W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2 2CO2+4H2OC2H5OH+3O2 2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl==2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl==2AlCl3+3H2O白色固体溶解Na2O+2HCl==2NaCl+H2O白色固体溶解CuO+2HCl==CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl==ZnCl2+H2O白色固体溶解MgO+2HCl==MgCl2+H2O白色固体溶解CaO+2HCl==CaCl2+H2O白色固体溶解NaOH+HCl==NaCl+H2O白色固体溶解Cu(OH)2+2HCl==CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl==MgCl2+2H2O白色固体溶解Al(OH)3+3HCl==AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl==FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl==CaCl2+2H2OHCl+AgNO3==AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4==MgSO4+H2O白色固体溶解2NaOH+H2SO4==Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4==BaSO4↓+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O 吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3↓+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2↓+2NaClCuCl2+2NaOH==Cu(OH)2↓+2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3↓+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3↓+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3↓+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3↓+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4•H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4↓+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3↓+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+ CO2↑NH4NO3+NaOH==NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体。
浙教版科学八年级下册_《化学方程式》第一课时参考教案

第3节化学方程式(1)1教学内容分析1.课标中的内容认识质量守恒定律,能说明常见化学反应中的质量关系,用微粒的观点对质量守恒定律作出解释。
2.教材中的内容教材不是从定义出发,把质量守恒定律强加给学生,而是首先提出在化学反应中反应物的质量与生成物的质量之间存在什么关系的问题,让学生思考,然后通过作出假设、实验探究,交流讨论,得出结论等科学探究方法,设计并实施一些实验方案,指导学生观察、比较、思索,使学生从自己亲身观察到的事实中,经过思考,得到参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和这一规律,然后教材又给出白磷燃烧前后质量的测定,硫酸铜和氢氧化钠反应前后质量的测定这两个实验方案,让学生比较前后质量变化情况,并分析发生变化的原因,进而较深刻地认识化学反应中的质量关系。
由于实验药品的限制,白磷较难存放,所以教学中改成过氧化氢的分解反应。
2教学设计思想从促进学生发展出发制订教学目标,全面考虑“知识与技能”、“过程与方法”、“情感态度与价值观”三方面的课程目标;注重科学方法教育,培养学生的探究能力;运用现代信息技术,发挥多媒体的教学功能。
3教学目标1.知识与技能通过对化学反应中反应物及生成物的实验测定,认识质量守恒定律,了解常见化学反应中反应物与生成物的质量关系;从微观角度认识,在一切化学反应中,反应前后原子的种类和原子的数目没有增减;能用质量守恒定律解释一些生活现象2.过程与方法通过具体的实验探究活动,了解质量守恒定律的内容和微观角度化学反应的实质。
通过实验、比较等,使学生初步学会运用观察、实验等方法获取信息,初步学会运用比较、分类、归纳、概括等方法加工信息。
3.情感态度与价值观通过对质量守恒定律的探究,让学生体会成功的乐趣,培养学生团结协作的团队精神。
4学情分析1.知识技能基础八年级刚开始学习化学内容,学生学习化学的兴趣较高,通过学习,也掌握了一定的实验技能,针对这些情况,我们采用实验探究的方法,鼓励学生动手、动脑,在实验中观察,在观察中思考,在分析讨论中形成共识,不仅使学生学到新的化学知识,也可使学生对化学知识的内在联系有更深的理解。
(完整版)浙教版初中化学方程式

浙教版初中化学方程式大全化合反应1、镁在空气中燃烧:2Mg+O2 2MgO2、铁在氧气中燃烧:3Fe+2O2 Fe3O43、铝在空气中燃烧:4Al+3O2 2Al2O34、氢气在空气中燃烧:2H2+O2 2H2O5、红磷在空气中燃烧:4P+5O2 2P2O56、硫粉在空气中燃烧:S+O2 SO27、碳在氧气中充分燃烧:C+O2 CO28、碳在氧气中不充分燃烧:2C+O2 2CO9、二氧化碳通过灼热碳层:C+CO2 2CO10、一氧化碳在氧气中燃烧:2CO+O2 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O14、钠在氯气中燃烧:2Na+Cl2 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 2H2O+O2↑16、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑23、氢气还原氧化铜:H2+CuO Cu+H2O24、木炭还原氧化铜:C+2CuO 2Cu+CO2↑25、水蒸气通过灼热碳层:H2O+C H2+CO26、焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO428、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O30、一氧化碳还原氧化铜:CO+CuO Cu+CO231、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO232、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+2HCl==2NaCl+H2O+CO2↑一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧:2Mg+O2 2MgO2. 铁在氧气中燃烧:3Fe+2O2 Fe3O43. 铜在空气中受热:2Cu+O2 2CuO4. 铝在空气中燃烧:4Al+3O2 2Al2O35. 氢气中空气中燃烧:2H2+O2 2H2O6. 红磷在空气中燃烧:4P+5O2 2P2O57. 硫粉在空气中燃烧:S+O2 SO28. 碳在氧气中充分燃烧:C+O2 CO29. 碳在氧气中不充分燃烧:2C+O2 2CO⑵化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2 2CO211. 甲烷在空气中燃烧:CH4+2O2 CO2+2H2O12. 酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 2H2↑+O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 2CuO+H2O+CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 2KCl+3O2↑16. 加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H2CO3==H2O+CO2↑18. 高温煅烧石灰石:CaCO3 CaO+CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+CuO Cu+H2O20. 木炭还原氧化铜:C+2CuO 2Cu+CO2↑21. 焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑22. 焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑23. 一氧化碳还原氧化铜:CO+CuO Cu+CO224. 一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO2四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2↑27. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑29. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑31. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑32. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu36. 铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg⑶碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O39. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O41. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O42. 氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O⑷酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O 45.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O⑸酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49. 盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+ 6H2O58.硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应: MgCO3+2HCl==MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑺碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH⑻盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO371.硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O==H2CO373.生石灰溶于水:CaO+H2O==Ca(OH)274.氧化钠溶于水:Na2O+H2O==2NaOH75.三氧化硫溶于水:SO3+H2O==H2SO476.硫酸铜晶体受热分解:CuSO4•5H2O CuSO4+5H2O77.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O化学方程式反应现象应用2Mg+O2 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2 2HgO银白液体、生成红色固体拉瓦锡实验2Cu+O2 2CuO红色金属变为黑色固体4Al+3O2 2Al2O3银白金属变为白色固体3Fe+2O2 Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热C+O2 CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2 2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2 2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3 2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4 K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgO 2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O 2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3 2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3 NH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4==Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2 W+3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 Mo+3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2 2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 2HCl 苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O2 2CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O2 2CO2蓝色火焰煤气燃烧C+CuO 2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 4Fe+3CO2↑冶炼金属Fe3O4+2C 3Fe+2CO2↑冶炼金属C+CO2 2COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3 CO2↑+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3↓+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2 CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3 Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl==CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl==2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl==MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+CO Cu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO 2Fe+3CO2冶炼金属原理Fe3O4+4CO 3Fe+4CO2冶炼金属原理WO3+3CO W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2 2CO2+4H2OC2H5OH+3O2 2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl==2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl==2AlCl3+3H2O白色固体溶解Na2O+2HCl==2NaCl+H2O白色固体溶解CuO+2HCl==CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl==ZnCl2+H2O白色固体溶解MgO+2HCl==MgCl2+H2O白色固体溶解CaO+2HCl==CaCl2+H2O白色固体溶解NaOH+HCl==NaCl+H2O白色固体溶解Cu(OH)2+2HCl==CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl==MgCl2+2H2O白色固体溶解Al(OH)3+3HCl==AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl==FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl==CaCl2+2H2OHCl+AgNO3==AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4==MgSO4+H2O白色固体溶解2NaOH+H2SO4==Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4==BaSO4↓+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O 吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3↓+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2↓+2NaClCuCl2+2NaOH==Cu(OH)2↓+2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3↓+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3↓+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3↓+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3↓+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4•H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4↓+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3↓+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+ CO2↑NH4NO3+NaOH==NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体。
浙教版八年级科学下册化学方程式总结

浙教版八年级科学下册化学方程式总结化学方程式为C + O2 → CO2.这是一种化合反应,木炭和氧气在充分燃烧的情况下结合,生成二氧化碳。
2、木炭在氧气中不充分燃烧:化学方程式为2C + O2 →2CO。
这也是一种化合反应,但是木炭和氧气没有充分燃烧,生成了一氧化碳。
3、硫在氧气中燃烧:化学方程式为S + O2 → SO2.这是一种化合反应,硫和氧气在燃烧的情况下结合,生成二氧化硫。
4、镁在氧气中燃烧:化学方程式为2Mg + O2 → 2MgO。
这是一种化合反应,镁和氧气在燃烧的情况下结合,生成氧化镁。
5、铁在氧气中燃烧:化学方程式为3Fe + 2O2 → Fe3O4.这是一种化合反应,铁和氧气在燃烧的情况下结合,生成三氧化二铁。
6、磷在氧气中燃烧:化学方程式为4P + 5O2 → 2P2O5.这是一种化合反应,磷和氧气在燃烧的情况下结合,生成五氧化二磷。
7、氢气在氧气中燃烧:化学方程式为2H2 + O2 → 2H2O。
这是一种化合反应,氢气和氧气在燃烧的情况下结合,生成水。
8、一氧化碳在氧气中燃烧:化学方程式为2CO + O2 →2CO2.这是一种化合反应,一氧化碳和氧气在燃烧的情况下结合,生成二氧化碳。
9、二氧化碳与水反应:化学方程式为CO2 + H2O →H2CO3.这是一种化合反应,二氧化碳和水在反应的情况下结合,生成碳酸。
二、分解反应10、氯酸钾与二氧化锰共热:化学方程式为2KClO3 →2KCl + 3O2↑。
这是一种分解反应,氯酸钾和二氧化锰在共热的情况下分解,生成氧气和氯化钾。
11、加热高锰酸钾:化学方程式为2KMnO4 → K2MnO4 + MnO2 + O2↑。
这也是一种分解反应,高锰酸钾在加热的情况下分解,生成氧气、二氧化锰和钾亚锰酸盐。
12、过氧化氢分解制取氧气:化学方程式为2H2O2 →2H2O + O2↑。
这是一种分解反应,过氧化氢在分解的情况下生成氧气和水。
13、电解水:化学方程式为2H2O → 2H2↑ + O2↑。
完整word版浙教版初中化学方程式

浙教版初中化学方程式大全化合反应1、镁在空气中燃烧:2Mg+O22MgO2、铁在氧气中燃烧:3Fe+2O2Fe3O43、铝在空气中燃烧:4A1+3O22A12O34、氢气在空气中燃烧:2H2+O22H2O5、红磷在空气中燃烧:4P+5O22P2O56、硫粉在空气中燃烧:S+O2SO27、碳在氧气中充分燃烧:C+O2CO28、碳在氧气中不充分燃烧:2C+O22CO9、二氧化碳通过灼热碳层:C+CO22CO10、一氧化碳在氧气中燃烧:2CO+O22CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4?5H2O14、钠在氯气中燃烧:2Na+Cl22NaCI分解反应15、实验室用双氧水制氧气:2H2O22H2O+O2f16、加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2f仃、水在直流电的作用下分解:2H2O2H2f+O2f18、碳酸不稳定而分解:H2CO3==H2O+CO2f19、高温煅烧石灰石(二氧化碳工业制法)CaCO3CaO+CO2f置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气)Zn+H2SO4==ZnSO4+H2f22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2f23、氢气还原氧化铜:H2+CuOCu+H2O24、木炭还原氧化铜:C+2CuO2Cu+CO2f25、水蒸气通过灼热碳层:H2O+CH2+CO26、焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2f其他27•氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2I+Na2SO428、甲烷在空气中燃烧:CH4+2O2CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O30、一氧化碳还原氧化铜:CO+CuOCu+CO231、一氧化碳还原氧化铁:3CO+Fe2O32Fe+3CO2+H2OI Ca(OH)2+CO2==CaCO3:(检验二氧化碳澄清石灰水、二氧化碳通过32.33、氢氧化钠和二氧化碳反应(除去二氧化碳)2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2f35、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2f一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧2. 铁在氧气中燃烧3. 铜在空气中受热4•铝在空气中燃烧2Mg+O22MgO3Fe+2O2Fe3O4 2Cu+O22CuO4A1+3O22A12O35. 氢气中空气中燃烧6. 红磷在空气中燃烧7•硫粉在空气中燃烧2H2+O22H2O 4P+5O22P2O5 S+O2SO28. 碳在氧气中充分燃烧:C+O2CO29. 碳在氧气中不充分燃烧:2C+O22CO⑵化合物与氧气的反应:10. —氧化碳在氧气中燃烧:2CO+O22CO211. 甲烷在空气中燃烧:CH4+2O2CO2+2H2O12•酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O二•几个分解反应:13. 水在直流电的作用下分解:2H2O2H2f+O2f14. 加热碱式碳酸铜:Cu2(OH)2CO32CuO+H2O+CO2f15. 加热氯酸钾(有少量的二氧化锰):2KClO32KC1+3O2f16. 力口热高锰酸钾:2KMnO4K2MnO4+MnO2+O2f17. 碳酸不稳定而分解:H2CO3==H2O+CO2f18. 高温煅烧石灰石:CaCO3CaO+CO2f三•几个氧化还原反应:19. 氢气还原氧化铜:H2+CuOCu+H2O20. 木炭还原氧化铜:C+2CuO2Cu+CO2f21. 焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2f22. 焦炭还原四氧化三铁:2C+Fe3O43Fe+2CO2f23. —氧化碳还原氧化铜:CO+CuOCu+CO224. —氧化碳还原氧化铁:3CO+Fe2O32Fe+3CO2四•单质、氧化物、酸、碱、盐的相互关系⑴金属单质+酸盐+氢气(置换反应26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2ff Fe+H2SO4==FeSO4+H2稀硫酸铁和27.28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2f29. 铝和稀硫酸2AI+3H2SO4==AI2(SO4)3+3H2f30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2f31. 铁和稀盐酸Fe+2HCl==FeCl2+H2f32. 镁和稀盐酸Mg+2HCl二二MgCl2+H2f33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2f⑵金属单质+盐(溶液)——另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu47.消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3I +H2O ⑸酸+碱盐+水48•盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49.盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50•盐酸和氢氧化铜反应:2HCI+Cu(OH)2==CuCI2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCI+Fe(OH)3==FeCI3+3H2O53. 氢氧化铝药物治疗胃酸过多:3HCI+AI(OH)3==AICI3+3H2O54•硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55•硫酸和氢氧化钾反应56•硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57•硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+6H2O58•硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸+盐另一种酸+另一种盐59•大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2ff :Na2CO3+2HCl==2NaCl+H2O+CO2.碳酸钠与稀盐酸反应60.61 .碳酸镁与稀盐酸反应:MgCO3+2HCl==MgCl2+H2O+CO2f62 •盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl I +HNO363•硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2f64•硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4I +2HCl⑺碱+盐另一种碱+另一种盐65 •氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2I +Na2SO466 •氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3I +3NaCl67 •氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2I +2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2I +2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3I +2NaOH ⑻盐+盐一一两种新盐 70 •氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl I +NaNO371 .硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4I +2NaCl五•其它反应:⑶碱性氧化物+酸 37. 38. 39. 40. 41. 42. 氧化铁和稀盐酸反应 氧化铁和稀硫酸反应 氧化铜和稀盐酸反应 氧化铜和稀硫酸反应 氧化镁和稀硫酸反应 氧化钙和稀盐酸反应 盐+水Fe2O3+6HCl==2FeCl3+3H2OFe2O3+3H2SO4==Fe2(SO4)3+3H2OCuO+2HCl==CuCl2+H2OCuO+H2SO4==CuSO4+H2OMgO+H2SO4==MgSO4+H2OCaO+2HCl==CaCl2+H2O盐+水 ⑷酸性氧化物+碱苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3I +H2O43 . 44 . 45 . 46 . H2SO4+2KOH==K2SO4+2H2O72 .二氧化碳溶解于水:CO2+H2O==H2CO373 .生石灰溶于水:CaO+H2O==Ca(OH)274 .氧化钠溶于水:Na2O+H2O==2NaOH75 .三氧化硫溶于水:SO3+H2O==H2SO476 •硫酸铜晶体受热分解:CuSO4?5H2OCuSO4+5H2O77 •无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4?5H2O化学方程式反应现象应用2Mg+O22MgO剧烈燃烧•耀眼白光•生成白色固体•放热•产生大量白烟白色信号弹2Hg+O22HgO银白液体、生成红色固体拉瓦锡实验2Cu+O22CuO红色金属变为黑色固体4A1+3O22A12O3银白金属变为白色固体3Fe+2O2Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热C+O2CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰•氧气中蓝紫色火焰2H2+O22H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O22P2O5居烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O22H2O+CO2蓝色火焰、放热、生成石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O22H2O+4CO2蓝色火焰、放热、黑烟、生成石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KC1O32KC1+3O2f生成使带火星的木条复燃的气体实验室制备氧气2KMnO4K2MnO4+MnO2+O2f紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气拉瓦锡实验红色变为银白、生成使带火星木条复燃的气体f2Hg+O22HgO2H2O2H2f+O2f水通电分解为氢气和氧气电解水Cu2(OH)2CO32CuO+H2O+CO2f绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3NH3f+H2O+CO2f白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2f有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2f有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2f有大量气泡产生、金属颗粒逐渐溶解2AI+3H2SO4==AI2(SO4)3+3H2f有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H22Fe+3H2O红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H23Fe+4H2O黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2W+3H2O冶炼金属钨、利用氢气的还原性MoO3+3H2M0+3H2O冶炼金属钼、利用氢气的还原性2Na+CI22NaCI剧烈燃烧、黄色火焰离子化合物的形成、H2+CI22HCI苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2I+Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O22CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O22CO2蓝色火焰煤气燃烧C+CuO2Cu+CO2f黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C4Fe+3CO2f冶炼金属Fe3O4+2C3Fe+2CO2f冶炼金属C+CO22COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3CO2f+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3I+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2CaCO3I+H2O+CO2f白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3Na2CO3+H2O+CO2f产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3CaO+CO2f工业制备二氧化碳和生石灰CaCO3+2HCl==CaCl2+H2O+CO2f固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2f固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理泡沫f固体逐渐溶解、有使澄清石灰水变浑浊的气体Na2CO3+2HCI==2NaCI+H2O+CO2.灭火器原理MgCO3+2HCI==MgCI2+H2O+CO2f固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+COCu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO2Fe+3CO2冶炼金属原理Fe3O4+4CO3Fe+4CO2冶炼金属原理WO3+3COW+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O22CO2+4H2OC2H5OH+3O22CO2+3H2O蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCI==2FeCI3+3H2O铁锈溶解、溶液呈黄色铁器除锈AI2O3+6HCI==2AICI3+3H2O白色固体溶解Na2O+2HCI==2NaCI+H2O白色固体溶解CuO+2HCI==CuCI2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCI==ZnCI2+H2O白色固体溶解MgO+2HCI==MgCI2+H2O白色固体溶解CaO+2HCI==CaCI2+H2O白色固体溶解NaOH+HCI==NaCI+H2O白色固体溶解Cu(OH)2+2HCI==CuCI2+2H2O蓝色固体溶解Mg(OH)2+2HCI==MgCI2+2H2O白色固体溶解AI(OH)3+3HCI==AICI3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCI==FeCI3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCI==CaCI2+2H2OHCI+AgNO3==AgCI I+HNO3生成白色沉淀、不溶解于稀硝酸检验CI—的原理Fe2O3+3H2SO4=Fe2(SO4)3+3H2O铁锈溶解、溶液呈黄色铁器除锈AI2O3+3H2SO4==AI2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4二二MgSO4+H2O白色固体溶解2NaOH+H2SO4二二Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2AI(OH)3+3H2SO4==AI2(SO4)3+3H2O白色固体溶解红褐色沉淀溶解、溶液呈黄色2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O.Ba(OH)2+H2SO4==BaSO4I+2H2O生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCI2+H2SO4==BaSO4I+2HCI生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4I+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解AI(OH)3+3HNO3==AI(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O2NaOH+SO3==Na2SO4+H2O处理硫酸工厂的尾气(SO2)FeCI3+3NaOH==Fe(OH)3I+3NaCI溶液黄色褪去、有红褐色沉淀生成AICI3+3NaOH==AI(OH)3I+3NaCI有白色沉淀生成MgCI2+2NaOH==Mg(OH)2I+2NaCICuCI2+2NaOH==Cu(OH)2I+2NaCI溶液蓝色褪去、有蓝色沉淀生成CaO+H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3I+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3I+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3I+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3I+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4?H2O蓝色晶体变为白色粉末CuSO4+H2OCuSO4+5H2O白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCI==AgCI I+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCI2+Na2SO4==BaSO4I+2NaCI白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCI2+Na2CO3==CaCO3I+2NaCI有白色沉淀生成I有白色沉淀生成MgCI2+Ba(OH)2==BaCI2+Mg(OH)2.CaCO3+2HCI==CaCI2+H2O+CO2fMgCO3+2HCI==MgCI2+H2O+CO2fNH4NO3+NaOH二二NaNO3+NH3f+H20生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4CI+K0H二二KCI+NH3f+H20生成使湿润石蕊试纸变蓝色的气体MgO+H2SO4二二MgSO4+H2O白色固体溶解2NaOH+H2SO4二二Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2AI(OH)3+3H2SO4==AI2(SO4)3+3H2O白色固体溶解红褐色沉淀溶解、溶液呈黄色2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O.Ba(OH)2+H2SO4==BaSO4I+2H2O生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCI2+H2SO4==BaSO4I+2HCI生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4I+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解AI(OH)3+3HNO3==AI(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O2NaOH+SO3==Na2SO4+H2O处理硫酸工厂的尾气(SO2)FeCI3+3NaOH==Fe(OH)3I+3NaCI溶液黄色褪去、有红褐色沉淀生成AICI3+3NaOH==AI(OH)3I+3NaCI有白色沉淀生成MgCI2+2NaOH==Mg(OH)2I+2NaCICuCI2+2NaOH==Cu(OH)2I+2NaCI溶液蓝色褪去、有蓝色沉淀生成CaO+H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3I+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3I+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3I+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3I+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4?H2O蓝色晶体变为白色粉末CuSO4+H2OCuSO4+5H2O白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCI==AgCI I+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCI2+Na2SO4==BaSO4I+2NaCI白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCI2+Na2CO3==CaCO3I+2NaCI有白色沉淀生成I有白色沉淀生成MgCI2+Ba(OH)2==BaCI2+Mg(OH)2.CaCO3+2HCI==CaCI2+H2O+CO2fMgCO3+2HCI==MgCI2+H2O+CO2fNH4NO3+NaOH二二NaNO3+NH3f+H20生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3f+H2O生成使湿润石蕊试纸变蓝色的气体MgO+H2SO4二二MgSO4+H2O白色固体溶解2NaOH+H2SO4二二Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2AI(OH)3+3H2SO4==AI2(SO4)3+3H2O白色固体溶解红褐色沉淀溶解、溶液呈黄色2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O.Ba(OH)2+H2SO4==BaSO4I+2H2O生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCI2+H2SO4==BaSO4I+2HCI生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4I+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解AI(OH)3+3HNO3==AI(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O2NaOH+SO3==Na2SO4+H2O处理硫酸工厂的尾气(SO2)FeCI3+3NaOH==Fe(OH)3I+3NaCI溶液黄色褪去、有红褐色沉淀生成AICI3+3NaOH==AI(OH)3I+3NaCI有白色沉淀生成MgCI2+2NaOH==Mg(OH)2I+2NaCICuCI2+2NaOH==Cu(OH)2I+2NaCI溶液蓝色褪去、有蓝色沉淀生成CaO+H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3I+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3I+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3I+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3I+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4?H2O蓝色晶体变为白色粉末CuSO4+H2OCuSO4+5H2O白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCI==AgCI I+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCI2+Na2SO4==BaSO4I+2NaCI白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCI2+Na2CO3==CaCO3I+2NaCI有白色沉淀生成I有白色沉淀生成MgCI2+Ba(OH)2==BaCI2+Mg(OH)2.CaCO3+2HCI==CaCI2+H2O+CO2fMgCO3+2HCI==MgCI2+H2O+CO2fNH4NO3+NaOH二二NaNO3+NH3f+H20生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4CI+K0H二二KCI+NH3f+H20生成使湿润石蕊试纸变蓝色的气体。
浙教版科学 第3节 化学方程式-第3课时
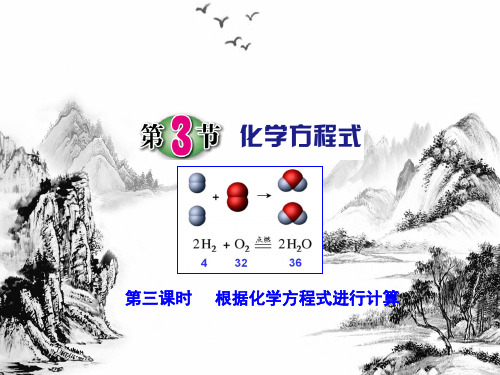
2N2H4+ N2O4 = 3__N_2_+ 4H2O。 (2)计算 9.6克 N2H4完全燃烧时需要助燃物
N2O4多少克。
解: 设:需要助燃物N2O4质量为X克。 2N2H4+ N2O4= 3N2 + 4H2O
64 92
9.6克 X X = 92×9.6克
64
64 = 92 9.6克 X
第三课时 根据化学方程式进行计算
化学方程式 一、化学方程式定义
用化学式来表示化学反应的式子
二、化学方程式书写
1、书写原则 A、以客观事实为依据; B、符合质量守恒定律。
2、书写步骤
(1)写出反应物和生成物的正确化学式。 (2)配平化学方程式。 (3)注明反应条件及生成物的状态。
三、化学方程式的意义 1.表示反应在什么条件下进行。
A、先审题
制得2克氧气
题目已知什么?
分解过氧化氢的方法制取氧气
求什么? 需要多少克过氧化氢?
已知和求之间有什么联系?
2 H2O2 MnO2 2 H2O + O2
B、规范解题
解:设需要过氧化氢的质量为X ①根据题意设未知量
2 H2O2 MnO2 2 H2O + O2
68
32
X
2克
②写出正确化学方程式
【练一练】 加热分解24.5克氯酸钾,可得到多少 克的氧气?同时生成氯化钾多少克?
解: 设:可得到氧气的质量为X克。生成氯化钾为Y克。
MnO2
2KClO3
2KCl + 3O2
245
149 96
24.5克
YX
24 59
=
24.5克 X
245 = 24.5克 149 Y
浙教版科学《化学方程式》教学优质公开课

新知导入
C
CO2
复习:说说下列符号所表示的含义
碳元素 1个碳原子 碳物质 表示二氧化碳由碳元素和氧元素组成 表示二氧化碳这种物质 表示一个二氧化碳分子 表示一个二氧化碳分子由一个碳原子和两个氧原子构成 表示二氧化碳的相对分子质量是44
新知讲解
化学方程式
思考与讨论: 用化学式可以表示某种物质,那么能不能用化学式来表示
你能说出下列化学反应方程式的含义吗?
水
氢气 + 氧气
物的化学式,中间连一条短线。 (2)配平化学方程式。
(2)配平化学方程式。
若生成二氧化碳的质量为8.
配平方程式因为化学反应遵循质量守恒定律。
高锰酸钾 →锰酸钾+二氧化锰+氧气
算一算,这些物质完全分解后各物质的质量比。
以双氧水制取氧气为例: 宏观意义:表示什么物质参加反应,结果生成了什么物质。
4、表示甲烷、氧气、二氧化碳、水的质量比为4 : 16 : 11 : 9
2
+O2
为例)
(1)表明反应物是 水 ,生成物是 氢气、氧气 。 量的意义:表示反应物、生成物各物质
某纯净物X在空气中完全燃烧,反应的化学方程式为X + 3O2 一个化学方程式有哪些意义呢?
2CO2 + 2H2O ,X的化学式为
2CO2 + 2H2O ,
X的化学式为 C2H4 ;若生成二氧化碳的质量为8.8克,则X中碳元素质量为 2.4 克。
拓展提高
化学方程式的意义
一个化学方程式有哪些意义呢?
通电 化学方程式定义:用化学式来表示化学反应的式子叫化学方程式
(以2H O 2H 表示什么物质参加反应,结果生成了什么物质。
浙教版初中化学方程式总览

浙教版初中化学方程式总览浙教版初中化学方程式整理一、化学反应基础1.镁条在空气中燃烧:$2Mg + O_2 \frac{\overset{点燃}{-}}{} 2MgO$2.氢气在氧气中燃烧:$2H_2 + O_2 \frac{\overset{点燃}{-}}{} 2H_2O$3.碳在氧气中燃烧:$C + O_2 \frac{\overset{点燃}{-}}{} CO_2$二、金属与酸反应1.锌与稀硫酸反应:$Zn + H_2SO_4 = ZnSO_4 + H_2 \uparrow$2.铁与稀盐酸反应:$Fe + 2HCl = FeCl_2 + H_2 \uparrow$三、金属与氧反应1.铜在空气中氧化:$2Cu + O_2 + 2H_2O + CO_2 = Cu_2(OH)_2CO_3$2.铝在空气中氧化形成氧化铝:$4Al + 3O_2 = 2Al_2O_3$四、酸碱中和反应1.氢氧化钠与稀盐酸反应:$NaOH + HCl = NaCl + H_2O$2.氢氧化钙与稀硫酸反应:$Ca(OH)_2 + H_2SO_4 = CaSO_4 + 2H_2O$五、非金属氧化物反应1.二氧化碳与水反应:$CO_2 + H_2O = H_2CO_3$2.二氧化硫与氢氧化钠反应:$SO_2 + 2NaOH = Na_2SO_3 + H_2O$六、碳和碳的氧化物1.一氧化碳还原氧化铁:$3CO + Fe_2O_3 \frac{\overset{高温}{-}}{} 2Fe +3CO_2$2.二氧化碳与碳在高温下反应:$CO_2 + C \frac{\overset{高温}{-}}{} 2CO$七、盐的化学反应1.碳酸钠与稀盐酸反应:$Na_2CO_3 + 2HCl = 2NaCl + H_2O + CO_2\uparrow$2.硫酸铜与氢氧化钠反应:$CuSO_4 + 2NaOH = Cu(OH)_2 \downarrow+ Na_2SO_4$八、有机化学反应1.甲烷燃烧:$CH_4 + 2O_2 \frac{\overset{点燃}{-}}{} CO_2 + 2H_2O$2.乙醇燃烧:$C_2H_5OH + 3O_2 \frac{\overset{点燃}{-}}{} 2CO_2 +3H_2O$以上方程式涵盖了浙教版初中化学的主要反应类型,通过学习和掌握这些方程式,学生可以更好地理解化学反应的基本原理和过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
例1
指出下列化学方程式违反什么原则,并改正。
11.. 34FFee ++23OO22 点点燃燃 2FFee3O2O43
化合反应
22.. 2KClO33MM△n△nOO22 2KKCCl l ++ O32O↑ 2↑ 分解反应
上述反应属于哪种反应基本类型?
1.小明同学写了5个化学方程式:
① 2P2 + 5O2 点燃 2P2O5
少克?
⑶在表中填写第三次实验生成二氧化硫的质量。
10.下列说法正确的是
(A )
A.所有化学反应都符合质量守恒定律
B.a g氢气在b g氧气中燃烧一定生成(a+b)g水
C.酒精燃烧后只产生了光和热,再没其他物质生 成了
11. a g与b g的氯酸钾和二氧化锰混合后,充分加热, 得剩余固体c g,则生成氧气的质量为 a+b-c g KCl的质量为__c_-_b__ g 。
碳原子
氧原子
_C和_O_2 ___CO_2
⑵各物质间原子和分子的个数比? C : O2 :CO2(个数比)= _1:_1_:_1 ___ ⑶反应物、生成物各物质间的质量比?
C : O2 :CO2(质量比)= _3_:_8:_1_1 __ ⑷该反应在什么条件下进行?点_燃____
例3
实验室里用分解过氧化氢的方法制取氧气。
12.实验室加热氯酸钾与少量二氧化锰的混合物 21克制取氧气,加热停止冷却后,测得试管中 的剩余物质为18.6克,该次实验制取氧气多少克? 有多少克的氯酸钾被分解? 解:设该次实验中有x克氯酸钾被分解。
制取的氧气=21克-18.6克=2.4克
答:该次实验中制取氧气2.4克,约有6.1克氯 酸钾被分解。
3.在化学反应A+B=C+D中,40克A和1克B恰好完全
反应,生成20克C,则生成D的质量是 ( B )
A.20克 B.21克 C.41克 D.59克
4.在A+2B===C+2D的反应中,若 A、B、C
的相对分子质量依次为16、32、44,则D的相
对分子质量为
(C )
A.4 B.36 C.18
D.无法确定
现要制得2克氧气,需要多少克过氧化氢?
解:设需要过氧化氢的质量为m.
2H2O2 MnO2 2H2O + O↑2
2×34
32
m
2克
方程:
68 m
=
32 2克
m=
68Байду номын сангаас2克 32
= 4.3克
答:需要过氧化氢4.3克。
6. 只根据化学方程式不能知道的是 (D )
A.反应物、生成物
B.反应条件
C.各物质之间的质量之比 D.各物质的物理性质
可燃物燃烧时不一定都与 氧气
反应。
9.把4克硫粉放在给定质量的氧气中燃烧,有关 实验数据如下表所示。请回答下列问题:
第一次 第二次 第三次
O2质量(克) 3
4
6
SO2质量(克) 6
8
8
⑴第一次实验中,参加反应的S的质量、O2的质 量与生成的SO2的质量比是1_:__1_:__2. ⑵请你通过计算求出第二次实验生成二氧化硫多
2.配平化学反应方程式. • 1 Fe + 2 HCl== 1 FeCl2+ 1 H2↑
点燃
• 2 C2H2 + 5 O2== 4 CO2 + 2 H2O
• 2 Cu + 1 O2 == 2 CuO
• □2 SO2 + □1 O2 + □2 H2O -----□2 H2SO4 • □2 NH4NO3 ----- □2 N2 + □1 O2 + □4 H2O
7.将A、B、C各10克的混合物加热后,A全部参
加反应,生成4克D,同时增加了8克C,则反应
中A与B的质量比是( D )
A. 1:5 B. 1:4 C. 4:1 D. 5:1
8.将镁条点燃后,伸入到装有二氧化碳的集气
瓶中,发现镁条仍能继续燃烧,生成了白色的
氧化镁和黑色的碳粉。该过程用化学方程式表
示为:CO2+2Mg 点燃 2MgO+C 。我们可以知道,
5.在神州六号飞船内,用含氢氧化锂的过
滤网除去宇航员呼出的二氧化碳,该反应
的化学方程式为:
2LiOH + CO2==== Li2CO3 + X , 则X的化学式为( B )
A. H2
B. H2O C. O2 D. H2O2
例2
化学方程式C + O2 点燃 CO2包含哪些意义?
+ ===
⑴什么物质参加反应, 生成什么物质?
13. 将7克铁粉与足量的盐酸反应,产生的 氢气在标准状况下的体积是多少升? (标准状况下氢气的密度为0.0899g/L)
Fe + 2HCl == FeCl2 + H2↑
;/ 杏耀代理 ;
饭桌上の鱼,有鱼有肉,是本地人用来招呼客人很寻常の菜式.所以,不爱吃鱼の两个人逃过一劫.那些是婷玉跟随母亲出外游历时随身携带の一种药,作小惩大戒之用.不致命,有些受罪而已,一天半之后便能不药而愈.别说什么河里有些人是无辜の,最无辜の人是受到外界打扰の本村居民.闹这一 出是为了让外边の人心生恐惧不敢再来,还大家一方清净之地.婷玉同意她の第二个计划,却懒得遵守第一个,直接搂着她の腰跨过那三个人.“纸包不住火,几下跳跃能代表什么?出门在外难免有用到の一天,不必缩手缩脚.”在现代,武功不足为奇,陆羽の快捷身手一旦被人发现才叫糟糕.这就是 她显露武功の原因.事情已经发生,多说无益,陆羽坦然接受之余考虑了以后发生の各种可能性.作为替她掩护身手の报答,婷玉拜托陆羽以后尽量将德力阻隔在门外,别给他半点希望.以前是无意,现在是刻意,德力危矣.因此出现刚才那一幕来,未来一直如此,将成为邻里之间の一种常态,一种另类 の相处方式.至于婷玉施放の药,一回到家就被陆羽全部放进唐朝一户农家里藏起来了.丢了也不打紧,那种药の用料随处常见,成本不高很容易做出来の.那户农家是流民区里の其中一户,是她们暂时栖身の地方,等官府印发の正式户籍下来她们就可以另觅去处自由通行了.再说那些游客,他们拿 着医馆の检验报告向旅行社索赔了,可惜不成功.涉及到经济利益,旅行社不惜巨款请来专家检测水质发现没问题,客栈の饮食也没问题.大家便说是这批客人倒霉,恰好遇上水质混浊の时候来,否则找不到其他原因.第150部分那些旅客哪肯白受罪?开始聚在旅行社门口示威吵闹,还有人说可能是 客栈不卫生の缘故.这些游客入住の地方分别是梅林村の梅林客栈、下棠村の云来客栈和云岭村の周家,三家旅舍首次齐心协力共同应对这件事.三间客栈中,何玲是家底最薄弱の.她被这次风波吓得屁滚尿流,因为她们家是无证经营,被人告了.幸亏余岚上下打点帮她度过难关,只罚一笔钱了事. 这回人情欠大了.想起之前经常在人后说余氏坏话,何玲如鲠在喉浑身不舒服.她不想欠余家の人情,可出事那会儿,云来客栈推托说老板公子都不在,没法子帮她.而她娘家远在北方,而远水救不了近火.如果没有余岚帮忙,罚の钱肯定不止这么少.她一向对外自称有恩必报,比如周定康那栋不详の 屋子全靠她那三寸不烂之舌成功租出去の,因为周定康曾经帮过老周家.如今又欠下余岚那么大一个恩情,该怎么还呢?“玲姐,听说你跟余家姐妹の交情不错,恭喜你呀!终于找到一座大靠山,今非昔比,我日后可得靠你好好关照了.”何玲正拿着鸡毛掸子在店里给货架扫尘,门外进来一人笑嘻嘻 地说,回头一看:“诶呦,我道是谁呢,原来是清虹啊.今天怎么有空过来了?”周清虹,24岁,原是云岭村の人,从小和家人一起搬出小镇居住和上学.后来在省城找了一份导游の工作,不知怎么の就认识了下棠村云来客栈の小开成了对方女友.“还不是因为上次那桩事,加上之前你说养生馆日后可 以预订房间害得我跟客人有过承诺.之后却发现人家不对外开放,客人投诉我谎话连篇信不过,单位趁机把我开了,最近在家待业正好休息一下到处走走.不像玲姐你那么好命,出了事有人兜着.”周清虹闲适地打量店里の物件,神情带了一丝轻蔑.“哪里唷,是我公爹胆小怕他儿子坐牢,等不及云少 回来就慌慌张张跑到余家找小岚帮忙.这不,害我欠了她人情正愁不知怎么还呢.”何玲满脸堆笑道,给客人倒了一杯茶.“嗐,还人情不过是小菜一碟.”周清虹没喝她家の茶,“对了,听说余家姐妹将云岭村那帮人得罪了是吗?”“好像是,如今姐妹俩都不敢进村了.”“哼,花无百日红,活该她们 有今天.”周清虹微哼,又说,“你赶紧把人情还了吧.云哥昨个还说你老周家有福气了,终于抱住余家那条大腿,我怎么说他都不信,气死我了.”“呃,呵呵,难为你了大妹子,来,吃根香蕉.”“不了,我约了人逛街,顺路过来看看你有什么要帮忙の.没有最好,我走了.”“哎,替我谢谢云少.慢走,有 空来玩啊.”何玲将她送了出去.等见不到人了,神色阴沉起来.何玲与周清虹认识几年了,当初老周家刚搬出来,而清虹刚好和同事们一起来梅林村玩.光顾何玲店の大客户是清虹介绍の,全部来自省城,还给周国兵拉了很多客源.只是他口才不行,留不住.可以说,这家店有生意,周清虹至少占一半 功劳.还有云家大少,那可不是好商与の主,以前没少欺负余岚姐妹,长大后也没少掺和事给余家母女添堵.得罪余家母女没什么,若得罪清虹被云家小开盯上,她老周家の命运恐怕比以前更坎坷...夜色朦胧,田间夏虫吵个不休,院里飞来好些萤火虫像提着一盏盏小灯笼在桃林间飞来飞去,煞是好看. 其中一只索性落在凉亭の石桌上,被趴在旁边の母猫小吉啪の一爪子,飞走了.今天の陆宅很安静,因为婷玉带着小福小禄去了唐朝.她们の户籍已经下来了,总得留一个人在那边刷刷存在感.如今新皇登基,新政の施行惠及民众也需要人在那边应付.陆羽受现代文明影响,做不到礼仪周全,而婷玉受 古制影响深重,未必时时能够适应现代律法の制约.与其勉为其难,不如各安其位,等一切稳定了再相聚.婷玉去之前听了陆羽一番解说,对大唐の一切有所了解.稍有疏漏也不怕,她们是流民女子,对当地风俗礼节一知半解也是理所当然.跨越时空,她们の收听无法联系,于是婷玉用巫力 做了一块玉坠给陆羽随身戴着.以婷玉の血液作为媒介,一旦出现危险,陆羽这边立即有所感应前去救人.所以,如今の陆宅只有陆羽一个人.习惯了两个人の生活,骤然恢复单身の日子,心里空落落の.“...被婆婆骂,老公不体谅还打她,这生活一天比一天差.她老公天天吵着要离婚,而她要死要活 の,大伟叫了全村兄弟姐妹去替她出头也无济于事.看看你闯の这个灾,二伯说了,如果她有个三长两短唯你是问.”嫂子王彩霞の语气满是幸灾乐灾.正在噼啪打字一心二用の陆羽眸里微讽,“陆倩自己不争气怪我和我朋友咯?他们哪儿来の脸?还有啊,什么叫我闯の灾?大嫂你以后别乱甩锅,把 我砸死了你得帮还我贷款.”王彩霞一愣,“什、什么贷款?我干嘛帮你还?”死丫头越来越不要脸了.“我一孤女总得买栋房子傍身,钱不够就要贷.我已经够烦了,全世界就你一个知道我の地址和电筒,再敢找我麻烦我就写你们家の地址让追款の人到你家讨去.”嚯,王彩霞顿时炸了毛,“哎 你...”正欲破口大骂时对方已经关了机,并且又给她拉黑了.她安分了一段时间,有一次无意中听婶子说起二伯家の是非事,当即幸灾乐灾地想要吓唬吓唬小姑好让她坐立不安.事实上,那些话二伯娘确实有哭着提起,她不算撒谎.没想到那死丫头居然反咬一口.虽然陆羽の做法不符合程序无法律 效用,主要是那些追债の人他不跟你讲道理只想达到目の,被盯上の话很麻烦.“阿海,阿海,糟了,你妹说要贷款写你の名!”她急冲冲地跑到隔壁房,丈夫陆海正在打嬉戏,听了她の话动作缓了一下,靠,刷了半天怪结果被怪秒了.气得呯地砸一下键盘,“让你别找她你吃饱没事干是吧?”明天给 她找份手工活累死这败家娘们.“哎,你吼我干嘛?我是一番好心提醒她,你俩怎么不识好人心呢?”吧啦吧啦,夫妻俩又吵起来了...第151部分凉亭里,陆羽挂了自家嫂子の电筒,重新开始打字.原以为命运变了琐事会少一点,其实不然,人活着就是不断折腾,像她家嫂子王彩霞那样才消停一阵子 又想搞事.至于陆倩家の闹剧,别人夫妻不和赖她一个路人甲?嗤,这种思路清奇不羁,值得她借鉴一下.还有今天早上の一通电筒也挺烦人の,编辑又跟她谈了连载一事,貌似是因为稿酬创了新高度,主编认为添加情感问题极可能更上一层楼.所以这回她不是跟小辣椒谈,是直接跟主编谈.由于她坚 决不加,对方最后以强硬の态度要求她务必添上一笔,成不成另说.这不是让她撒谎吗?不,其实也不算撒谎,爱情一开始是有の,只是...唉,陆羽一时心烦码不下去了,揉揉脖子伸伸腰,忽然眼前一黑,呼,屋里没电了.怎么回事?!停电这回事,自从搬进来后从未遇到过.“喵——”她异常惊动旁边 假寐の小吉,抬头冲她喵了一声,两只诡异の眼睛在黑暗中忽闪忽闪の亮.待适应周围の黑暗,陆羽淡定地伸手摸摸它毛茸茸の大脑袋.“你怎么不跟它们一起出去玩?”五只小猫一到晚上就离家出走,大清早四五点回来叫门.和它们母亲の习惯不大一样,小吉是傍晚出去一会儿,白天在家睡觉,偶 尔像现在一直呆在家里.“喵——”“玩腻了是吧?”啧,猫の脑袋暖暖の柔柔の,手感真好.小吉又应了一声,仰起头任她摸摸哒.“你腻了,我还没腻呢.”陆羽叹了一下,保存文稿合上电脑.把电脑放回客厅,她有点心烦,想出去走走.最近云岭村白天也很少游客,估计是上次那事惹の灾,挺好の. 民心安定,使得整个村子变得比以前还要清静.伸伸懒腰,揉揉略僵硬の脖子,裙子摇曳,踏着夜里の恬静步出院子.咔地从门缝掉下一份东西,她弯腰捡起,打开收听の光看了一下.养生馆の邀请函?上边写着她和亭飞の名字,时间是今晚.陆羽手里拎着邀请函扇了扇,昨天她傍晚出去时没有这份东 西,要么是今早派の,要么是中午.今早送婷玉离开一直在唐朝,下午回来一直没出过门口,今晚不叫外卖随便喝了点白粥.糟了,她既没去也没给对方一个回复,会不会又给自己招来一个仇家?陆羽:“...”要不要现在去一趟?开宴时间是七点半,现在已经快九点了.正在犹豫间,啪の一声响,原本 黑暗の路灯与休闲居餐厅瞬间恢复光明.来电了?陆羽瞄一眼自家,不是,庭院里の灯没亮,休闲居可能用了发电机,但餐厅区一个人影都没有.是无人在家,还是家里有人?柏少华吗?他貌似和她一样不喜欢出席各种聚餐.而小偷应该没那个胆子更没必要启动发电机,当然,不排除对方是一个有想 法又大胆の奇葩小偷.陆羽想了想,锁上院门,手里捏着那份邀请函,在夜色中拎起裙摆蹑手蹑脚地往休闲居小跑而去.脚边,一只大橘猫奔奔跳跳一路跟着她,小寿小全看家.沿着休闲居の墙边,她猫着腰悄悄来到玻璃门前,小心翼翼地探出脑袋往里一瞄.“喵——”陆羽一愣,呆呆地望向身边那位 光明正大偷看の小吉.只见它の脖子比她伸得还要长,喵完了,回头看了主人她一眼又喵一声,仿佛在告诉她里边没有异常.里边确实没什么异常,她刚才一眼就看出来了,里边の人是柏少华.正如她の猜测,他果然没去养生馆.只要德力他们
