Ch3 IR
硝基化合物

成环和重排
O R C CH2 R' 成环 O R + C CH2 R' 重排 R R' O R C CH2R' + N N O
+ + H2C N N C R
醛和环酮以重排产物为主,普通的酮主要生成环氧化物。酮分子中 与羰基相连的两个烃基不相同时,得到两种重排产物的混合物。
O R O R C CH2 H + + H2C N N C H + N N O R C CH3
H 重排
O + CH2N2
O CH2 + N N
O + N2
O C CH2 CH2N2 CH2
O C CH2 + N N
O C
环丙酮
3. 与酰氯反应
O R
脱去氯化氢
O R O H C CH2 Cl + -H+ N N O R C CH + N N + N N
+ + H2C N N C Cl
-Cl
R
第一节 硝基化合物
硝基化合物可分为脂肪族硝基化合物和芳香族硝基化合物。 硝基化合物的结构
CH3 + N O
Sp2杂化
O
O O
C-N 147pm , <ONO = 127
N-O
+ N
122pm
+ N O O
+ N
O O
P, π 共轭
CH3
NO2
μ= 3.5 D
硝基为强的吸电子基
厚 第十八章 止 其它含氮化合物
H2 O R'OH NH3 O O RCH2COR'
化学类IR谱图库

化学类1. 苯的IR谱图2. 乙酸苯酯(C8H8O2)的IR谱图3. 乙醚(CH3CH2OCH2CH3)的IR谱图4. 对苯二甲酸二环己醇酯的IR谱图5. 对苯二甲酸二戊酯的IR谱图6. 对苯二甲酸二辛酯(DOTP) 的IR谱图7. 邻甲苯甲酰氯的IR谱图8. 丁二烯(1,3)均聚物的IR谱图9. 1-丁烯腈(C4H5N)的IR谱图10. 异丙叉丙酮(C6H10O)的IR谱图11. 丁酐(C8H14O3)的红外光谱12. 苯丙酮(C9H10O)的IR谱图13. 丙酐的IR谱图14. 乙酸乙酯的IR谱图15. 苯甲酰胺的IR谱图16. 丙酸的IR谱图17. 邻甲基苯甲酸的IR谱图18. 1-己烯的IR谱图19. 正丙苯IR谱图20. 2-丁醇的IR谱图21. 正丁醇的IR谱图22. 叔丁醇的IR谱图23. 仲丁醇的IR谱图24. 丁醛的IR谱图25. 苯甲醇的IR谱图26. 正丙醚的IR谱图27. 苯乙醚的IR谱图28. 3-戊酮的IR谱图29. 2-甲基丁醛的IR谱图30. 丙酮的IR谱图31. 苯乙酮的IR谱图32. 正己酸的IR谱图33. 乙酸的IR谱图34. 硝基苯的IR谱图35. 间苯二酚的IR谱图36. 尿素的IR谱图37. 苯丙醇的IR谱图38. 苯甲酸的IR谱图39. 苯甲酸钠的IR谱图40. 苯甲醇的IR谱图41. 苯酚的IR谱图42. 酚酞的IR谱图43. 邻硝基甲苯的IR谱图44. 正丁胺的IR谱图45. 1-癸烯的IR谱图46. 苄醇的IR谱图47. CaSO4.2H2O的标准IR谱图48. L-苏糖酸钙的IR谱图49. 四氯化碳的IR谱图50. 正己烷的IR谱图51. 醋酸正丁酯的IR谱图52. 邻-苯基苯酚的IR谱图53. 新戊醇的IR谱图54. 丙烯氰的IR谱图55. 空气的IR谱图56. 环戊基腈的IR谱图57. 异氰酸乙酯的IR谱图58. 二苯乙炔的IR谱图59. 异丙基丙烯酰胺(isopropylacrylamide)的IR谱图60. 碳酸钙的标准IR谱图61. 对甲苯磺酰氟(para-toluenesulfonyl fluoride, 97%)的IR谱图62. 氢氧化钠的IR谱图63. Na2C2O4的IR谱图64. EDTA的IR谱图65. 二苯甲醇的IR谱图66. 三苯甲醇的IR谱图67. 乙酰二茂铁的IR谱图68. 苯甲酸乙酯的IR谱图69. 正己酸的IR谱图70. 对-甲基苯乙酮的IR谱图71. 环己烯的IR谱图72. 安息香的IR谱图73. 正溴丁烷的IR谱图74. 叔丁基氯的IR谱图75. 二苯乙醇酸的IR谱图76. 二苯乙二酮的IR谱图77. 氨基喹啉的IR谱图78. 对叔丁基氯苯酚的IR谱图79. 苯甲酸的IR谱图80. 1,3,5-三溴苯IR图谱81. 1-己炔的红外光谱82. 多环芳香烃-蒽IR谱图83. 2,6-双(4-氯苯亚甲基)环己酮的IR谱图84. 正癸酸的红外光谱85. 未知物的IR图86. 异丁胺的红外光谱87. 化合物C13H12S的IR谱图88. 化合物CH4N2S的IR谱图89. 化合物C16H22O2S的IR谱图90. 化合物C14H14OS的IR谱图91. 化合物C8H7N的IR谱图92. 8-羟基喹啉(C9H7ON)的IR谱图93. 对叔丁基氯苯酚的IR谱图94. 1,6-庚二烯-4-醇的IR谱图95. 羟基丙酮的IR谱图96. 酞酸二(乙基己基)酯的IR谱图97. 脲素的IR谱图98. 1-己烯(1-hexene)的IR谱图99. 1-己炔(1-hexyne)的IR谱图100. 4-庚酮(4-heptanone)的IR谱图101. 乙酸苄酯(benzyl acetate)的IR谱图102.丁酰胺(Butyramide)的IR谱图103. γ-丁内酯的红外光谱104. 二丁胺的红外光谱105. 间-甲苯胺的红外光谱106. 邻-氯甲苯的红外光谱107. 对-氯甲苯的红外光谱108. 2-萘酚的红外光谱109. 1-己醇(正己醇)的红外光谱110. 苯甲酰胺的红外光谱111. 三丁胺的红外光谱112. 乙酰氯的IR图113. 没食子酸异戊酯的IR谱图114. 2-溴丙烷(2-bromopropane)的IR谱图115. 二丁氧基苯(p-dibutoxybenzene)的IR谱图116. 丙烯酸正丁酯(isobutylacrylate)的IR谱图117. 氟化镁的IR谱图118. 硫化锌的IR谱图119. 苯甲酸的IR谱图120.邻苯二甲酸二辛酯(DOP)的IR谱图121. 光谱纯溴化钾的IR谱图122. 苯丙酸的IR谱图133.134.135.苯的IR谱图乙酸苯酯(C8H8O2)的IR谱图乙醚(CH3CH2OCH2CH3)的IR谱图对苯二甲酸二环己醇酯的IR谱图对苯二甲酸二戊酯的IR谱图对苯二甲酸二辛酯(DOTP) 的IR谱图DOTP的IR光谱图中1728.0cm-1为酯类C=O的伸缩振动,1268.9cm-1和1117.7cm-1为酯基中C—O伸缩振动的特征峰。
IR谱图——精选推荐
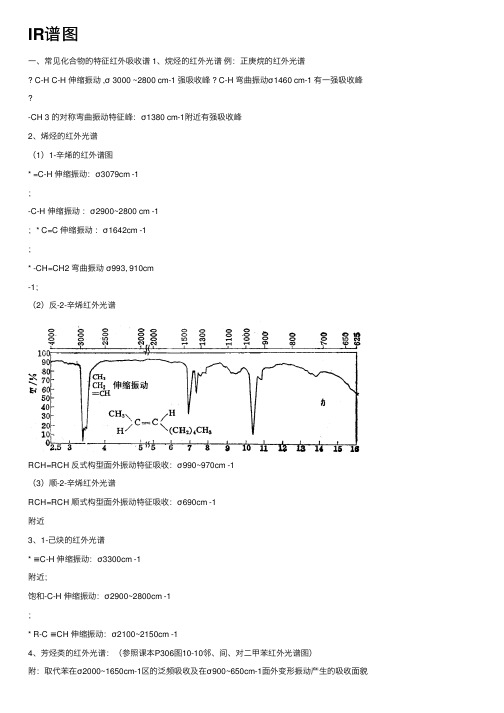
IR谱图⼀、常见化合物的特征红外吸收谱 1、烷烃的红外光谱例:正庚烷的红外光谱C-H C-H 伸缩振动 ,σ 3000 ~2800 cm-1 强吸收峰 ? C-H 弯曲振动σ1460 cm-1 有⼀强吸收峰-CH 3 的对称弯曲振动特征峰:σ1380 cm-1附近有强吸收峰2、烯烃的红外光谱(1)1-⾟烯的红外谱图* =C-H 伸缩振动:σ3079cm -1;-C-H 伸缩振动:σ2900~2800 cm -1;* C=C 伸缩振动:σ1642cm -1;* -CH=CH2 弯曲振动σ993, 910cm-1;(2)反-2-⾟烯红外光谱RCH=RCH 反式构型⾯外振动特征吸收:σ990~970cm -1(3)顺-2-⾟烯红外光谱RCH=RCH 顺式构型⾯外振动特征吸收:σ690cm -1附近3、1-⼰炔的红外光谱* ≡C-H 伸缩振动:σ3300cm -1附近;饱和-C-H 伸缩振动:σ2900~2800cm -1;* R-C ≡CH 伸缩振动:σ2100~2150cm -14、芳烃类的红外光谱:(参照课本P306图10-10邻、间、对⼆甲苯红外光谱图)附:取代苯在σ2000~1650cm-1区的泛频吸收及在σ900~650cm-1⾯外变形振动产⽣的吸收⾯貌5、含羰基化合物的红外光谱例1:苯⼄醛的红外谱图ΦC-H 伸缩振动吸收: σ3088~3030cm -1;-CHO 的νC-H 的伸缩振动的两个中等强度的特征吸收峰:σ2826cm -1 (-CH2-中的C-H 伸缩振动吸收涵盖其中),σ2728cm-1C=O 的特征吸收:σ1724cm -1例2:⼄酸⼄酯的红外光谱-CH 2,-CH 3的C-H 伸缩振动峰(m,w ):σ3000~2800cm -1;酯基中的C=O 伸缩振动峰: σ1743cm -1;-CH 3的不对称变形振动峰和-CH 2 变形振动峰:σ1448cm -1-CH 3的对称变形振动特征峰:σ1374cm -1C-O-C 不对称伸缩振动峰(酯的特征峰): σ1243cm -1C-O-C 对称伸缩振动峰(酯的特征峰): σ1048cm -1例3:参照课本P302图10-9壬酸的红外谱图6、含羟基化合物的红外光谱:参照下⾯红外谱图解析中的例1⼆、红外谱图解析例1:化合物C 4H 8O ,根据如下IR 谱图确定结构,并说明依据。
甲基硅油的三级红外光谱研究

术叙琏看料,2019,33(4):302〜309SILICONE MATERIAL 分析•测试甲基硅油的三级红外光谱研究武玉洁1,张莹2,王慧慧2,张智博2,赵英淋2,于宏伟2""(1.河北一品制药股份有限公司,河北石家庄052165;2.石家庄学院化工学院,河北石家庄050035)摘要:采用红外光谱(IR)研究了二甲基硅油(下称“甲基硅油”)的结构,并以甲基硅油Si—0的伸缩振动(”S--o)和CH3的摇摆振动(%H3)为研究对象,进一步开展了甲基硅油的变温红外光谱研究和二维红外光谱研究。
结果表明,随着测试温度的升高,甲基硅油&SnO和P/H3对应的吸收强度降低;&SnO吸收频率包括1098、1070、1020和1007cm"1,热扰动因素下,&Si_。
吸收峰变化快慢顺序为:1098cm"1> 1020cm-1>1070cm-1>1007cm-1;%H3吸收频率包括870、866和862cm-1,热扰动因素下,各吸收峰变化快慢顺序为:866cm-1>870cm-1>862cm-1&在同样的温度扰动因素下,&Si-o对应的官能团对温度变化更敏感。
关键词:甲基硅油,红外光谱,变温红外光谱,二维红外光谱中图分类号:0434.3文献标识码:A doi:10.11941/j.issn.1009-4369.2019.04.011硅油是一类重要的有机硅材料,具有生理惰性、润滑性、良好的化学稳定性及电绝缘性等特点,广泛应用于建筑⑴、日用化工⑵、纺织助剂[3'4]及医药[5]等领域。
硅油的优异理化性能与其特殊结构有关%红外光谱(IR)广泛应用于材料的结构研究ST。
但有关硅油的红外光谱研究却少见报道。
因此本实验以二甲基硅油(下称“甲基硅油”)为主要研究对象,分别开展了Si一0伸缩振动(&si_o)和CH3摇摆振动(P ch3)的三级红外光谱(包括红外光谱、变温红外光谱和二维红外光谱)研究并进一步探索了温度变化对甲基硅油分子结构的影响,以期拓展三红外光的研究,研究硅类化物结构及热稳定性建立新的方法%1实验1.1主要原料及设备二甲基硅油:AR,天津市博迪化工有限公司。
氢谱

前言:研究一种新的有机物就要知道它的结构,因此结构分析是有机化学的重要组成部分。
过去,主要依靠化学方法进行有机化合物的结构测定,其缺点是:费时、费力、费钱,试剂的消耗量大。
而现在的结构测定,则采用现代仪器分析法,其优点是:省时、省力、省钱、快速、准确,试剂耗量是微克级的,甚至更少。
其中最常用的有四大谱:分别是紫外光谱(Ultraviolet spectroscopy 缩写为UV)、红外光谱(Infrared spectroscopy 缩写为IR)、核磁共振谱(Nuclearmagnetic resonance 缩写为NMR)和质谱(Mass spectroscopy 缩写为MS)。
吸收光谱紫外光谱 UV红外光谱 IR核磁共振谱 NMR非吸收光谱质谱MS 波谱法发展历史三十年代UV四十年代IR} 官能团五十年代NMRMS }分子式,分子骨架连接一般文献给出的数据:NMR: 详细MS: 分子量IR: 主要官能团一般无UV数据NOCH 3HOOHN N OCOHCH 3OH CH 3OCOHHOCH 3OCH 3OCH 3OCH 3发现确定结构人工合成证实Reserpine提取分离: 1805-1806提出结构: 1925合成证实: 19521952-1956X 光真空紫外区近紫外区紫蓝青绿黄橙红近红外区远红外区无线电波可见光区100nm200nm400nm800nm20μm500μm 光波区域10-1010-810-610-410-2100102wavelength (cm)γ-rays x-rays UV VIS IR μ-wave radio波谱解析第三章核磁共振谱the Nuclear magnetic spectra核磁共振谱核磁共振基本知识1氢核磁共振1H-NMR 2碳核磁共振13C-NMR 3二维核磁共振2D-NMR 41NMR是应用最广泛研究分子性质的最通用的技术:从分子的三维结构到分子动力学、化学平衡、化学反应性和超分子集体、有机化学的各个领域。
化学类IR谱图库

化学类1. 苯的IR谱图2. 乙酸苯酯(C8H8O2)的IR谱图3. 乙醚(CH3CH2OCH2CH3)的IR谱图4. 对苯二甲酸二环己醇酯的IR谱图5. 对苯二甲酸二戊酯的IR谱图6. 对苯二甲酸二辛酯(DOTP) 的IR谱图7. 邻甲苯甲酰氯的IR谱图8. 丁二烯(1,3)均聚物的IR谱图9. 1-丁烯腈(C4H5N)的IR谱图10. 异丙叉丙酮(C6H10O)的IR谱图11. 丁酐(C8H14O3)的红外光谱12. 苯丙酮(C9H10O)的IR谱图13. 丙酐的IR谱图14. 乙酸乙酯的IR谱图15. 苯甲酰胺的IR谱图16. 丙酸的IR谱图17. 邻甲基苯甲酸的IR谱图18. 1-己烯的IR谱图19. 正丙苯IR谱图20. 2-丁醇的IR谱图21. 正丁醇的IR谱图22. 叔丁醇的IR谱图23. 仲丁醇的IR谱图24. 丁醛的IR谱图25. 苯甲醇的IR谱图26. 正丙醚的IR谱图27. 苯乙醚的IR谱图28. 3-戊酮的IR谱图29. 2-甲基丁醛的IR谱图30. 丙酮的IR谱图31. 苯乙酮的IR谱图32. 正己酸的IR谱图33. 乙酸的IR谱图34. 硝基苯的IR谱图35. 间苯二酚的IR谱图36. 尿素的IR谱图37. 苯丙醇的IR谱图38. 苯甲酸的IR谱图39. 苯甲酸钠的IR谱图40. 苯甲醇的IR谱图41. 苯酚的IR谱图42. 酚酞的IR谱图43. 邻硝基甲苯的IR谱图44. 正丁胺的IR谱图45. 1-癸烯的IR谱图46. 苄醇的IR谱图47. CaSO4.2H2O的标准IR谱图48. L-苏糖酸钙的IR谱图49. 四氯化碳的IR谱图50. 正己烷的IR谱图51. 醋酸正丁酯的IR谱图52. 邻-苯基苯酚的IR谱图53. 新戊醇的IR谱图54. 丙烯氰的IR谱图55. 空气的IR谱图56. 环戊基腈的IR谱图57. 异氰酸乙酯的IR谱图58. 二苯乙炔的IR谱图59. 异丙基丙烯酰胺(isopropylacrylamide)的IR谱图60. 碳酸钙的标准IR谱图61. 对甲苯磺酰氟(para-toluenesulfonyl fluoride, 97%)的IR谱图62. 氢氧化钠的IR谱图63. Na2C2O4的IR谱图64. EDTA的IR谱图65. 二苯甲醇的IR谱图66. 三苯甲醇的IR谱图67. 乙酰二茂铁的IR谱图68. 苯甲酸乙酯的IR谱图69. 正己酸的IR谱图70. 对-甲基苯乙酮的IR谱图71. 环己烯的IR谱图72. 安息香的IR谱图73. 正溴丁烷的IR谱图74. 叔丁基氯的IR谱图75. 二苯乙醇酸的IR谱图76. 二苯乙二酮的IR谱图77. 氨基喹啉的IR谱图78. 对叔丁基氯苯酚的IR谱图79. 苯甲酸的IR谱图80. 1,3,5-三溴苯IR图谱81. 1-己炔的红外光谱82. 多环芳香烃-蒽IR谱图83. 2,6-双(4-氯苯亚甲基)环己酮的IR谱图84. 正癸酸的红外光谱85. 未知物的IR图86. 异丁胺的红外光谱87. 化合物C13H12S的IR谱图88. 化合物CH4N2S的IR谱图89. 化合物C16H22O2S的IR谱图90. 化合物C14H14OS的IR谱图91. 化合物C8H7N的IR谱图92. 8-羟基喹啉(C9H7ON)的IR谱图93. 对叔丁基氯苯酚的IR谱图94. 1,6-庚二烯-4-醇的IR谱图95. 羟基丙酮的IR谱图96. 酞酸二(乙基己基)酯的IR谱图97. 脲素的IR谱图98. 1-己烯(1-hexene)的IR谱图99. 1-己炔(1-hexyne)的IR谱图100. 4-庚酮(4-heptanone)的IR谱图101. 乙酸苄酯(benzyl acetate)的IR谱图102.丁酰胺(Butyramide)的IR谱图103. γ-丁内酯的红外光谱104. 二丁胺的红外光谱105. 间-甲苯胺的红外光谱106. 邻-氯甲苯的红外光谱107. 对-氯甲苯的红外光谱108. 2-萘酚的红外光谱109. 1-己醇(正己醇)的红外光谱110. 苯甲酰胺的红外光谱111. 三丁胺的红外光谱112. 乙酰氯的IR图113. 没食子酸异戊酯的IR谱图114. 2-溴丙烷(2-bromopropane)的IR谱图115. 二丁氧基苯(p-dibutoxybenzene)的IR谱图116. 丙烯酸正丁酯(isobutylacrylate)的IR谱图117. 氟化镁的IR谱图118. 硫化锌的IR谱图119. 苯甲酸的IR谱图120.邻苯二甲酸二辛酯(DOP)的IR谱图121. 光谱纯溴化钾的IR谱图122. 苯丙酸的IR谱图133.134.135.苯的IR谱图乙酸苯酯(C8H8O2)的IR谱图乙醚(CH3CH2OCH2CH3)的IR谱图对苯二甲酸二环己醇酯的IR谱图对苯二甲酸二戊酯的IR谱图对苯二甲酸二辛酯(DOTP) 的IR谱图DOTP的IR光谱图中1728.0cm-1为酯类C=O的伸缩振动,1268.9cm-1和1117.7cm-1为酯基中C—O伸缩振动的特征峰。
红外光谱

KK
1 1
m m m m
ν (cm )
-1
-1
C 2150
C
C 1650
C
C 1200
C
b、轨道中S成分越多,键的强度越大,吸收频率越高
ν (cm )
C__H sp 3300
C__H sp2 3100
C__H sp3 2900
1 K 1 c、原子的质量越大,振动吸收频率越低。 m1 m2 2 m1 m2 2 __ __ __ -1 C H C C C O (cm ) 3000 1200 1100
C-H N-H O-H S-H
C=C C=O
C=N
六.各类有机物的红外吸收:
1.烷烃的红外吸收:
正辛烷
甲基: Vas=2960, Vs=2860,δas=1450, 亚甲基: Vas=2930, Vs=2850, δas=1450 4个以上亚甲基: δs =720(cm-1)
δs =1380
2.烯烃的红外吸收
6 9 0 c m-1 6 9 0 c m-1 C=C H C=C H
2
2-甲基-1-丙烯
(E)-2-己烯
(Z)-3-己烯
3.炔烃的红外吸收:
1-己炔
C H 伸缩振动 3300
C C 伸缩振动 2100
C H 弯曲振动 630
2-己炔
HC
CCH2CH2CH2CH2CH2CH3
CH3C
CCH2CH2CH2CH2CH3
H H2 N , O 2 к Ó ìÍ âÎ üÕ Ê
CH3-CH2-C C-H Ð ÓÍ 箭头表示振动方向 O C O Þ Î ì º â ü Î CH -CH -C 3 2 âÎ Í üÊ Õ
有机化学常用缩写

引言概述:有机化学是研究碳基化合物及其衍生物的化学科学。
在有机化学研究过程中,科学家们为了方便交流和描述化合物、反应、实验条件等,常常使用一些缩写。
本文将介绍一些有机化学中常用的缩写,以便读者更好地理解和应用有机化学知识。
正文内容:一、官能团缩写1.R:表示任意烷基或芳基基团,例如,CH3CH2R。
2.Ar:表示任意芳香基团,例如,ArCOOH。
3.Ph:表示苯基团,例如,PhCOCH3。
4.Me:表示甲基基团,例如,MeOH。
5.Et:表示乙基基团,例如,EtCHO。
6.Bu:表示丁基基团,例如,BuNH2。
7.Ac:表示乙酰基基团,例如,AcOH。
8.COOH:表示羧酸基团,例如,CH3COOH。
9.OH:表示羟基团,例如,CH3CH2OH。
10.NH2:表示氨基团,例如,CH3NH2。
二、试剂缩写1.H2O:表示水。
2.EtOH:表示乙醇。
3.MeOH:表示甲醇。
4.THF(四氢呋喃):用作溶剂,常用于有机合成反应中。
5.KOH:表示氢氧化钾。
6.NaOH:表示氢氧化钠。
7.HCl:表示盐酸。
8.AgNO3:表示硝酸银。
9.TBDMS:表示四(叔丁基)二硅氧基基团。
10.TFA:表示三氟乙酸,用于有机合成中的去保护反应。
三、化学反应缩写1.RX:表示卤代烷基衍生物,例如,CH3Cl。
2.RCOO:表示羧酸根基团,例如,CH3COO。
3.RX:表示卤代烃,例如,CH3I。
4.ROH:表示醇,例如,CH3CH2OH。
5.RCOOH:表示羧酸,例如,CH3COOH。
6.RNH2:表示胺,例如,CH3NH2。
7.RSH:表示硫醇,例如,CH3SH。
8.RCN:表示腈,例如,CH3CN。
9.RMgX:表示格氏试剂,例如,CH3MgBr。
四、结构式缩写1.Me2S:表示硫醚,例如,CH3SCH3。
2.Et2O:表示醚,例如,CH3CH2OCH2CH3。
3.Bu2NH:表示二丁胺,例如,CH3CH2CH2NHCH2CH2CH3。
金属有机化学4

X M M
(iii)卤代芳烃的氧化加成是对芳环的亲核取代。
X PdL4 R R R L3Pd X -L PdL2X
X
R为吸电子基对反应有利,且不同卤素的活性 I > Br > Cl。
(iv)若产物为消旋的,则可能是自由基机理。同时也观 察到单电子转移反应的机理:
M + RX k2 R + Mn+1X [Mn+1]+ [RX]R R + Mn+1R
107 107 102 106 96 98 73
2. 氧化加成和还原消除反应
过渡金属与A-B 型的化合物反应时,A-B键发生断裂, 同时加成到过渡金属上:
A LnM + A B LnM B
其正反应称为氧化加成反应,逆反应称为还原消除反应。 (1)氧化加成反应
LnMm + A LnMm + A
B B
-
NH2
NH3 -Cl
Cl
Pt Cl
NH2
NH2 H2N Pt NH2 NH2
2+
Cl-NH3 H2N
NH2 Pt NH2 Cl
+
NH2
Cl-NH3
Cl
Pt NH2
Cl
(3)配体的立体影响
影响配位和解离的因素主要是配体的立体效应和电子效 应。
对于配体的立体影响,人们在以叔膦为配体的低原子价 络合物的解离平衡方面作了详细的研究。
Y Y L' L M L X Y L' M L L L X L' M L X -L' Y M L L X
即外加配体配位,中间体可以是四方锥形或三角双锥形, 新配体进入离去配体的位置,配合物的构型不变。 反应是高度立体专一的。
化学类IR谱图库资料

化学类1. 苯的IR谱图2. 乙酸苯酯(C8H8O2)的IR谱图3. 乙醚(CH3CH2OCH 2CH3)的IR 谱图4. 对苯二甲酸二环己醇酯的IR谱图5. 对苯二甲酸二戊酯的IR谱图6. (DOTP)的IR 谱图7. 邻甲苯甲酰氯的IR谱图8. 丁二烯(1,3)均聚物的IR谱图9. 1-丁烯腈(C4H5N)的IR谱图10. 异丙叉丙酮(C6H10O)的IR谱图11. 丁酐(C8H14O3)的红外光谱12. 苯丙酮(C9H10O)的IR谱图13. 丙酐的IR谱图14. 乙酸乙酯的IR谱图15. 苯甲酰胺的IR谱图16. 丙酸的IR谱图17. 邻甲基苯甲酸的IR谱图18. 1-己烯的IR谱图19. 正丙苯IR谱图20. 2-丁醇的IR谱图21. 正丁醇的IR谱图22. 叔丁醇的IR谱图23. 仲丁醇的IR谱图24. 丁醛的IR谱图25. 苯甲醇的IR谱图26. 正丙醚的IR谱图27. 苯乙醚的IR谱图28. 3-戊酮的IR谱图29. 2-甲基丁醛的IR谱图30. 丙酮的IR谱图31. 苯乙酮的IR谱图32. 正己酸的IR谱图33. 乙酸的IR谱图34. 硝基苯的IR谱图35. 间苯二酚的IR谱图36. 尿素的IR谱图37. 苯丙醇的IR谱图38. 苯甲酸的IR谱图39. 苯甲酸钠的IR谱图40. 苯甲醇的IR谱图41. 苯酚的IR谱图42. 酚酞的IR谱图43. 邻硝基甲苯的IR谱图44. 正丁胺的IR谱图45. 1-癸烯的IR谱图46. 苄醇的IR谱图47. CaSO4.2H2O的标准IR谱图48. L —苏糖酸钙的IR谱图49. 四氯化碳的IR谱图50. 正己烷的IR谱图51. 醋酸正丁酯的IR谱图52. 邻-苯基苯酚的IR谱图53. 新戊醇的IR谱图54.54. 空气的IR谱图55. 环戊基腈的IR谱图56. 异氰酸乙酯的IR谱图57. 二苯乙炔的IR谱图58. 异丙基丙烯酰胺(isopropylacrylamide)的IR谱图59. 碳酸钙的标准IR谱图60. 对甲苯磺酰氟(para-toluenesulfonyl fluoride, 97%)的IR 谱图61. 氢氧化钠的IR谱图62. W2C2O4 的IR 谱图63. EDTA的IR谱图64. 二苯甲醇的IR谱图65. 三苯甲醇的IR谱图66. 乙酰二茂铁的IR谱图67. 苯甲酸乙酯的IR谱图68. 正己酸的IR谱图69. 对-甲基苯乙酮的IR谱图70. 环己烯的IR谱图71. 安息香的IR谱图72. 正溴丁烷的IR谱图73. 叔丁基氯的IR谱图74. 二苯乙醇酸的IR谱图75. 二苯乙二酮的IR谱图76. 氨基喹啉的IR谱图77. 对叔丁基氯苯酚的IR谱图78. 苯甲酸的IR谱图79. 1,3,5-三溴苯IR图谱80. 1-己炔的红外光谱81. 多环芳香烃-蒽IR谱图82. 2,6-双(4-氯苯亚甲基)环己酮的IR谱图83. 正癸酸的红外光谱84. 未知物的IR图85. 异丁胺的红外光谱86. 化合物C13H12S的IR谱图87. 化合物CH4N2S的IR谱图88. 化合物C16H22O2S的IR谱图89. 化合物C14H14OS的IR谱图90. 化合物C8H7N的IR谱图91. 8-羟基喹啉(C9H7ON)的IR谱图92. 对叔丁基氯苯酚的IR谱图93. 1,6-庚二烯-4-醇的IR谱图94. 羟基丙酮的IR谱图95. 酞酸二(乙基己基)酯的IR谱图96. 脲素的IR谱图97. 1-己烯(1-hexene)的IR 谱图98. 1-己炔(1-hexyne)的IR 谱图99. 4-庚酮(4-heptanone)的IR 谱图100. 乙酸苄酯(benzyl acetate)的IR谱图101. 丁酰胺(Butyramide)的IR 谱图102. Y丁内酯的红外光谱103. 二丁胺的红外光谱104. 间-甲苯胺的红外光谱105. 邻-氯甲苯的红外光谱106. 对-氯甲苯的红外光谱107. 2-萘酚的红外光谱108. 1-己醇(正己醇)的红外光谱109. 苯甲酰胺的红外光谱110. 三丁胺的红外光谱111. 乙酰氯的IR图112. 没食子酸异戊酯的IR谱图113. 2-溴丙烷(2-bromopropane)的IR 谱图114. 二丁氧基苯(p-dibutoxybenzene)的IR 谱图115. 丙烯酸正丁酯(isobutylacrylate)的IR 谱图116. 氟化镁的IR谱图117. 硫化锌的IR谱图118. 苯甲酸的IR谱图119. 邻苯二甲酸二辛酯(DOP)的IR谱图120. 光谱纯溴化钾的IR谱图121. 苯丙酸的IR谱图文档来源为:从网络收集整理.word 版本可编辑.欢迎下载支持苯的IR 谱图乙醚(CH 3CH 2OCH 2CH 3)的 IR 谱图 对苯二甲酸二环己醇酯的 IR 谱图对苯二甲酸二戊酯的IR 谱图(DOTP)的IR 谱图DOTP 的IR 光谱图中1728.0cm -1为酯类C = O 的伸缩振动,1268.9cm -1和1117.7cm -1为酯基中C — O 伸缩 振动的特征峰。
IR数据

3.呋喃: 4.吡咯:
5.噻吩:
C-H伸缩 C=C伸缩, N-H伸缩 C-H伸缩 C=C伸缩, C-H伸缩 C=C伸缩, C-H面外弯曲
3165-3125 (中或弱) 1600,1500 ,1400。 3490 尖峰(强) 3125-3100 (弱) 1600-1500 。(强度不定) 3125-3050 1520 ,1410。 750-690 (强)
O
1750
O
O
1720
O
O
1760
O
O
O
1 7 8 0 -1 7 6 0
13.羧酸盐
COO1610-1550(强), 1420-1300 (强)
14.酰氯:
饱和酰氯:1815-1770 α,β-不饱和酰氯:1780-1750 酰氟高,酰碘最低。
15.酰胺
1.伯酰胺:—CONH2 (1) N-H, 3500,3400双峰,游离. 3350,3200双峰,缔合. (2)酰胺1带CO,1690(缔合1650) (3)酰胺2带, 1600(缔合1640)
与环大小 及取代有关
面内弯曲 伸缩
一些脂环烃化合物的IR数据
3090 3019 2933 1434 2974 2896 1450 2951 2871 1455
2920 2860 1447
2933 2865 1462
2941 1471 1451
O
1640
1780
1650
1570
1640
1680
1690
C-H伸缩 C=C伸缩
C-H面内弯曲
3030 1600 1580 1500 900-690
中-弱 中-弱
中-弱
不要求
IR谱图解析

如: 孤氢(1,3,5取代) 邻接二氢(1,4取代) 邻接三氢(1,3取代;1,2,3取代) 邻接四氢(1,2取代) 邻接五氢(单取代) 710690cm-1 邻接六氢(苯)
900850cm-1 860800cm-1 810750cm-1 700730cm-1 770730cm-1
675cm-1
红外谱图解析综述
3. 双键伸缩振动区(19001200cm-1) 主要包括C=C,C=O,-NO2,S=O,P=O等键的伸缩振动和芳环 的骨架振动等。 (1)烯烃:C=C 16801620cm-1 (强度可变)(图2A,B,C,D峰3) 共轭作用,波数偏低,强度增加。
(2)苯环:骨架振动在16201450cm-1范围内,常有四个吸收峰。 1600cm-1和1500cm-1(强度可变,这二个对确定苯环结构有用) 1580cm-1(较弱,但在共轭体中增强) 1450cm-1(常与CH2剪式振动1470cm-1重叠) (图4A,B,C,D峰2、3,图5A,B,C,D峰3、4,图9B峰4、5,图16A峰4) (3)羰基: C=O 18501550cm-1 (强,容易识别) 根据C=O基出现的不同位置,可判别是何种羰基化合物,如酸,酯 ,酮,醛,酸酐,酰胺,酰卤,羧酸盐,醌,二酰基过氧化物等等。
(4) 硝基 -NO2:(图12A峰2、3,B峰2、3、4,C峰2,3,4,D峰3,4) 脂肪族: as 15651545 (-1550cm-1) (强) s 13851350 (-1370cm-1) (强) 芳香族: as 15501500cm-1 s 13651290cm-1 比脂肪族稍低
730650cm-1例外较多 (图2C峰6)
R R ' C =C R C =C R'
R ' 三取代 ' H R ' 四取代 ' R '' '
金属有机化学 NO.2基元反应

(3) 烯烃的 C-H 键
OR
RuH2L4 + 2 H2C
CH3 COOR
27
28
PPh3
(H3C)2CHCOOR + L
OL Ru
CH3
29
LH H
30 (L = PPh3)
(4) 醛的 C-H 键
RH +
Rh(CO)ClL2 33
RhClL3 +L-L
RhClL2 31
RCHO
RRh(CO)(H)L2Cl
C M
C
Dewar-Chatt-Duncanson Model
表 1 一些烯烃─过渡金属络合物的红外光谱
化合物
CH2=CH2 K[Pt(CH2=CH2)Cl3] [Pt(CH2=CH2)Cl3]2 反式[Pt(C2H4)(NH3)Cl2] 反式[Pt(C2H2)(NH3)Br2] Pd[(C2H4)Cl2]2 K[[[[[A(((CCCC[2gP222H(dHHHC4(444C)2)))WHMFM2H4e()noC(4]C(()+2CCCH2HO2l53H)5])()55C(])C+(OCAO)Ol3)C]2)+]l3-++4
第二讲 基元反应
Elementary Reactions in Organometallic Chemistry
RX + Mg
RMgX
氧 化 加 成 (Oxidative addition)
RMgX +
R1
=O
R2
R1
R1 C
O
R MgX
插 入 反 应 ( Insertion )
非 机 理,乃 是 帮 助 理 解 及 预 测 反 应 产 物
常建华第3章IR

3.2 红外光谱基本原理 3.2.1 化学键的振动与频率 双原子分子中化学键的振动可按谐振子处理。
m1
m2
用虎克定律来表示振动频率、原子质量和键力常数之间 的关系:
υ=
1 2
若用波数取代振动频率,则有下式:
1
10 N
5
=
2c
=
2 c
Cm-1
(2)
K为键力常数,其含义是两个原子由平衡位置伸长0.1nm(lA0) 后的回复力,单位是 dyn/cm。 μ’ 为折合质量。 μ’=m1m2/(m1+m2) (m为原子质量) m2=M2/N 。
分子的振动分为伸缩振动和变形振动两类。
伸缩振动是沿原子核之间的轴线作振动,键长有变化 而键角不变,用字母υ来表示。 伸缩振动分为不对称伸缩振动υas和对称伸缩振动υs。
变形振动是键长不变而键角改变的振动方式,用字母δ 表示。
伸缩 振动 υ 亚甲基 的振动
对称伸 缩振动
υ
S
不对称 伸缩振动
υ
as
面内摇摆 面内变 形振动 变形 振动 δ 面外变 形振动 δ 面外 δ 面内 面外摇摆 扭曲振动 剪式振动
红外光谱的峰强可以用摩尔吸收系数表示: =
1 CL
Lg T T
0
(4)
式中:为摩尔吸收系数; C为样品浓度,mol/L; L为吸收池厚度,cm; T0为入射光强度;T为出射光强度。 当l00时,峰很强,用Vs表示。 在20~100,为强峰,用S表示。 在l0~20,为中强峰,用m表示。 在l~l0,为弱峰,用w表示。 另外,用b表示宽峰,用Sh表示大峰边的小肩峰。
(2)分光系统 分光系统包括入射狭缝到出射狭缝这一部分。主要由 反射镜、狭缝和分光器组成。作用是将复式光分解成单 色光。分光系统也叫单色器。 (a)狭缝。 (b)反射镜。
金属有机化学3有机过渡金属络合物的基元反应
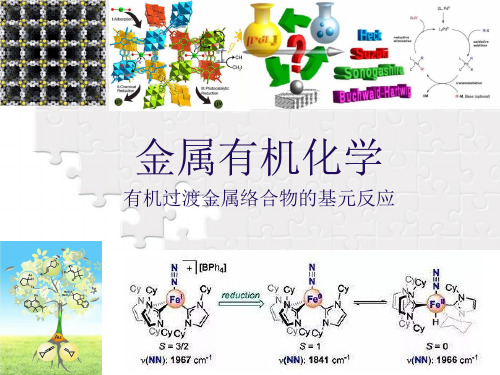
Pd(PPh3)4 18 电子
Pd(PPh3)3 + PPh3 16 电子
➢ 同样,常用的金属络合物还有:Ni(COD)2, Fe(CO)5, Mo(N2)2(dppe)2, dppe=Ph2PCH2CH2PPh2。
2. 氧化加成和还原消除(Oxidative Addition
and Reductive Elimination)
c. 非极性加成物
如:H2,R2SiH,R3GeH,R3SnH,RSH,RCHO,Ar-H, RH等。
i) H2
Vaska络合物与H2发生O.A.得到顺式产物
OC PPh3
Ir
+ H2
Ph3P Cl
PPh3 OC Ir Ha Cl PPh3Hb
JHaHb= 8.4 Hz
16e dsp2 (平面正方形) 可能是协同机理:
R
(bipy)Ni
+ CH2=CH
R
X
CH2=CHX R
(bipy)Ni R
(bipy)Ni(CH2=CHX) + R R
同样:
R1
R2 O
O
R1
R2
(bipy)Ni
O
(bipy)Ni O
O+
R2 R1
O
R1
R2
(bipy)Ni OC6H5 O CR O
O
O
(bipy)Ni O
O O + RCOC6H5 O
LnM + A B
只改变一个电子的反应
A
A
AB
L M B +L M B
L M M L+A B
反应过程中,金属的氧化态和络合物的配位数都减少了。
甲氧基(ch3o)的红外吸收光谱研究

甲氧基(ch3o)的红外吸收光谱研究《甲氧基(CH3O)的红外吸收光谱研究》
红外吸收光谱(IR)技术可以用来探索物质结构,它是分析、结构和表征材料
的重要工具。
最近,由于全太阳耀斑(FTS)技术的发展,研究人员开始利用它来
研究天然物质的红外吸收光谱。
甲氧基(CH3O)是一种有机化合物,在用中介物对结合反应中有广泛的应用,因此对它的研究很有意义。
本研究的目的是研究甲氧基(CH3O)的红外吸收光谱特征。
用实验室级全太阳
耀斑(FTS)仪器分析获得甲氧基(CH3O)样品的红外吸收光谱。
研究结果显示,
此物质有一个强,一个中等,和六个弱的红外吸收峰,对应于二级中间体和一级中间体,分别位于样品中C-H,O-H,和C-O等偶极内振动激发模态谱。
此外,本研
究还发现,甲氧基(CH3O)有许多完全不同的激发动能,以支持它的外部体系共振,同时为它的结构认识和应用提供了重要信息。
综上所述,本研究证实甲氧基(CH3O)有多个激发模式,并确定了它们的位置
和振动模式,为甲氧基(CH3O)的应用和结构认识提供了重要的理论和实验依据。
聚合物的表征-IR

乙酸酐的两个羰基间隔一个氧原子,它们发生 耦合。羰基的频率分裂为1818和1750 cm-1。(如 果没有耦合其羰基振动将出现在约1760 cm-1)
0 .3
724.93
0 .2
1371.81
0 .1
0 .0
- 0.1
- 0.2
4 00 0
3 50 0
3 00 0
2 50 0
2 00 0
1 50 0
1 00 0
5 00
PE的IR谱图(吸光度) Wavenumbers (cm-1)
2. 物理原理
2.1分子振动形式 2.1.1伸缩振动(伸展振动)(Stretching Vibration)
0.6
0.5
0.4
0.3
0.2
0.1
4000
3500
3000
2500
2000
Wavenumbers (cm-1)
1500
1000
500
1.5.2红外光谱图 最常用的两种表达方式
红外光谱是研究波数在4000-400cm-1范围内不同 波长的红外光通过化合物后被吸收的谱图。
横坐标 波长
波数
纵坐标 透过百分比 吸光度
特征频率总是伴随相应基团出现
实际
不同分子中同一基团的特征频率总是在一定 范围内有所偏移的
例:C=O在IR谱图中的位置变化
不同类分子中C=O的吸收带可在 1650—1900cm-1间变化
醛
1640-1740cm-1
酮
1705-1725cm-1
酸
1700 cm-1
酯
1725-1740cm-1
酰胺
1640-1720cm-1
第三章红外光谱IR
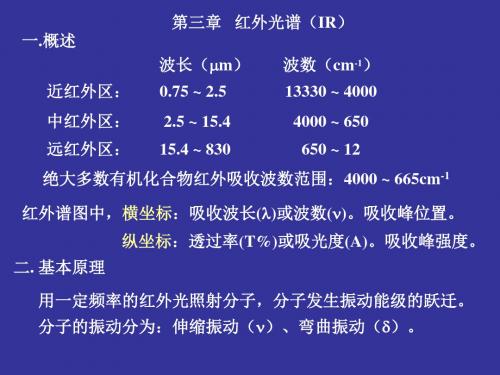
VC=C
1651
CH2
CH2 1657
CH2 1690
CH2 1750
O VC=O 1715
O 1745
O 1780
O 1815
• 环内双键的C=C伸缩振动吸收频率随环的减小即张力增大而 降低。
环的张力增大时, 环上有关官能团的吸收频率逐 渐升高。 环内双键的C=C伸缩振动吸收频率随环的减小而降低。
8~12105
CC 1200~700
4~6105
力常数表示了化学键的强度,其大小与键能、键长有关。
键能大,键长短,K值大,振动吸收频率移向高波数; 键能小,键长长,K值小,振动吸收频率移向低波数。
三.不同官能团的特征吸收频区
红外光谱可分为两个区域
官能团区 4000~1350cm-1 指纹区 1350~650cm-1
VC=C
1645
H
1610 H
1560 H
υ C=C υ =C H
1645cm-1 3017cm-1
1610cm-1 3040cm-1
1565cm-1 3060cm-1
5、空间位阻
一般共轭使振动频率降低
6、跨环共轭效应
7. 成键碳原子的杂化状态(杂化轨道中S成分越高,其电负性越强)
VC-H
CH 3300
一.概述
第三章 红外光谱(IR) 波长(m) 波数(cm-1)
近红外区: 0.75 ~ 2.5
13330 ~ 4000
中红外区: 2.5 ~ 15.4
4000 ~ 650
远红外区: 15.4 ~ 830
650 ~ 12
绝大多数有机化合物红外吸收波数范围:4000 ~ 665cm-1
红外谱图中,横坐标:吸收波长()或波数()。吸收峰位置。 纵坐标:透过率(T%)或吸光度(A)。吸收峰强度。
IR谱吸收频率羰基高低判断

IR谱吸收频率羰基高低判断
4000至2500cm-1X-H伸缩振动区,X可以是O、N、C或S等原子。
O-H基的伸缩振动出现在3650至3200cm-1范围内,它可以作为判断有无醇类、酚类和有机酸类的重要依据。
当醇和酚溶于非极性溶剂(如CCl4),浓度于0.01mol.dm-3时,在3650至3580cm-1处出现游离O-H基的伸缩振动吸收,峰形尖锐,且没有其它吸收峰干扰,易于识别。
当试样浓度增加时,羟基化合物产生缔合现象,O-H基的伸缩振动吸收峰向低波数方向位移,在3400至3200cm-1出现一个宽而强的吸收峰。
胺和酰胺的N-H伸缩振动也出现在3500至3100cm-1,因此,可能会对O-H伸缩振动有干扰。
C-H的伸缩振动可分为饱和和不饱和的两种。
饱和的C-H伸缩振动出现在3000cm-1以下,约3000至2800cm-1,取代基对它们影响很小。
如-CH3基的伸缩吸收出现在2960cm-1和2876cm-1附近:R2CH2基的吸收在2930cm-1和2850cm-1附近:R3CH 基的吸收基出现在2890 cm-1附近,但强度很弱。
不饱和的C-H伸缩振动出现在3000cm-1以上,以此来判别化合物中是否含有不饱和的C-H键。
11-Oxidative addition

b. Addition of X=Y or XY to LnM.
X Ln M + X Y Ln M Y X Ln M + X Y Ln M Y Ln M Ln M X Y X Y
Examples:
Cl Ph3P
Ir
PPh3 CO
+ O=O
Cl OC
PPh3 O Ir O PPh3
c. Binuclear oxidation reactions.
LnM: + R-X X Ln-1M R X or LnM R LnM R X #
+ LnM
R +X
*# of valence e- count of reactant LnM *S# > 0 or < 0? *Any solvent effect on reaction rate? e.g in benzene, acetone same reaction rate? Charge separation in TS, reaction is faster in polar solvent
LnM ML n + A-B 18e LnM A + LnM B 18e
O.S. = 1
18e A B ML n
Note: no change in valence electron count
LnM ML n + A-B
LnM
O.S. = 1
O O C C
Examples:
CO CO + H2 CO
R'OC
(RO)3Mo
Co CO
2 H Co CO CO CO
R'O (RO)3Mo OR' Mo(OR)3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一节 基本原理 (Basic Principles)
一、红外吸收光谱的产生 分子在不同振动、转动能级间跃迁, 分子在不同振动、转动能级间跃迁,吸 收特定能量的红外光,产生红外吸收。 收特定能量的红外光,产生红外吸收。 红外区: 红外区:0.8~1000µm
波长µm 频率cm 波长 频率 -1 近红外区: 近红外区: 0.8~2.5, 12500~4000 , 中红外区: 4000~400 中红外区: 2.5~25 远红外区: 400~10 远红外区: 25~1000
O 1622 cm-1 1675 cm-1 2843 cm-1
4. 振动偶合 (1)空间距离近 ) (2)振动频率近 ) 5. 费米共振 6. 样品物理状态 二、外部因素 1. 溶剂效应 2. 仪器色散原件
液膜
CCl4溶剂
不同条件下测得的环己醇IR谱图
第三节 各类官能团的特征吸收峰
一、饱和烃 官能团 -CH3 特征峰( 特征峰(cm-1) 2960,尖[70] , 2870,尖[30] , 1460[<15] 1380[15] 备注 相连, 与O,N相连,移向低波数 相连 偕二甲基,双峰 偕二甲基, 相连, 与O,N相连,移向低波数 相连 -(CH2)n-, n>4,n小,波数高 , , 小 环上有氢
• 以上几种振动方式 , 其能级变化的大小 以上几种振动方式, 不对称伸缩振动>对称伸缩振动 对称伸缩振动>弯 为 : 不对称伸缩振动 对称伸缩振动 弯 曲振动。 曲振动。 • 能级变化大的出峰在高频区 , 即波数值 能级变化大的出峰在高频区, 能级变化小的出峰在低频区, 大 ; 能级变化小的出峰在低频区 , 即波 数值小。 数值小。 • 伸缩振动的谱带位置可按下式计算: 伸缩振动的谱带位置可按下式计算:
CH3 Trans- CH3CH=CHCHCH3
CH3 Cis - CH3CH=CHCHCH3
1- 己炔
三、芳环及稠芳环 官能团 C=C 特征峰( 特征峰(cm-1) 1600,尖[<100] , 1580,变 , 1500,尖[<100] , 1450[中] 中 =CH 3030[<60] 2000-1600[5] 900-850[中] 中 860-800,尖[强] , 强 800-750,尖[强] , 强 770-730,尖[强] , 强 710-690,尖[强] , 强 该区无其它峰时 可见几个弱吸收峰 苯环上孤立氢(五取代苯) 苯环上孤立氢(五取代苯) 苯环上相邻两氢 苯环上三个相邻氢 苯环上四或五个相邻氢 单取代, 单取代,1,3-二取代 二取代 1,3,5或1,2,3-三取代 或 三取代 备注
芳氢的弯曲振动吸收( 芳氢的弯曲振动吸收(cm-1): • 苯 670 • 单取代苯 770—730 710—690 • 邻二取代苯 770—735 • 间二取代苯 900—860 810—750 725—680 • 对二取代苯 860—800
苯
甲苯
邻二甲苯
间二甲苯
对二甲苯
间三甲苯
萘
四、芳杂环 特征峰( 官能团 特征峰(cm-1) 3075-3020,尖[强] 吡啶 , 强 1620-1590[中] 中 1500[中] 中 900-720,尖[强] , 强 3165-3125[中,弱] 呋喃 中 ~1600 ~1500 ~1400 3490,尖[强] 吡咯 , 强 3125-3100[弱] 弱 1600-1500[变化 变化] 变化 两个吸收峰) (两个吸收峰) 噻酚 3125-3050 ~1520 ~1410 750-690[强] 强
备注
与苯环相似
NH产生 产生 =CH产生 产生
Pyridine
furan
thiophene
Pyrrole
1-methylpyrrole
五、醇和酚 O-H C-O =C-O C-H - - - - 1. 游离态 非极性溶剂的稀溶液 特征峰( 官能团 特征峰(cm-1) 备注 伯醇 -CH2OH 3640,尖[70] , 1050,尖[60-200] C-O伸缩 , - 伸缩 仲醇 >CHOH 3630,尖[55] , 1100,尖[60-200] C-O伸缩 , - 伸缩 3620,尖[45] 叔醇 COH , 1150,尖[60-200] C-O伸缩 , - 伸缩 3610,尖[中] 酚 , 中 1200,尖[60-200] C-O伸缩 , - 伸缩 2. 分子间氢键 1100处峰同上 处峰同上 3600-3500 二聚体 常被多聚体峰掩盖 多聚体 3600,宽[强] , 强 3. 分子内氢键 谱带向低波数方向移动,强度增大, 谱带向低波数方向移动,强度增大,峰变宽
1-pentanol
三、红外光谱产生的条件
1. 能级跃迁:跃迁概率越大,吸收峰越强 能级跃迁:跃迁概率越大, 2. 瞬间偶极矩变化:变化越大,吸收峰越强 瞬间偶极矩变化:变化越大, 3. 影响红外吸收峰的因素
(1)瞬间偶极矩变化:与电负性 电负性差别大, 电负性差别大, )瞬间偶极矩变化: 电负性(电负性差别大 吸收强)、振动方式(不对称伸缩 对称伸缩>弯 不对称伸缩>对称伸缩 吸收强 、振动方式 不对称伸缩 对称伸缩 弯 曲振动)、分子的对称性(对称性差 吸收峰强)、 对称性差, 曲振动 、分子的对称性 对称性差,吸收峰强 、 氢键(使吸收峰变宽变强 等有关。 使吸收峰变宽变强)等有关 氢键 使吸收峰变宽变强 等有关。 (2)峰的强度、位置、相互间距离 )峰的强度、位置、 (3)基频、倍频、组频和费米共振 )基频、倍频、
备注
共轭烯, 共轭烯,波数低
常出峰于730-675 常出峰于
840-800,尖[40] , 3300,尖[100] 端炔在 端炔在640cm-1处有强宽吸收 , 2140-2100[5] 端炔 2260-2190[1]
CH2=CHCH2CH2CH2CH3
CH3CH =CHCH2CH2CH3
H3C CH3 CH2=CCHCH3
O (CH3)3C Br 1730 cm-1 O Br 1742 cm-1
O
(CH3)3C
杂化状态
vC-H C—H 33 00 cm-1 C—H 3100 cm-1 C—H 2900 cm-1
空间位阻
CH3 C=O
CH3 C=O CH3 O
CH3 CH3 CH3 C=O CH3
vC=O
1663 cm-1 O
2. 官能团特征吸收:可作为官能团存在的依据 官能团特征吸收: 3. 特征区(官能团区)与指纹区 特征区(官能团区)
(1)官能团区 4000~1330cm-1 ) 1330~667cm-1 (2)指纹区 )
第二节 影响特征吸收峰位置的因素
一、内部因素 1. 电子效应 (1)诱导效应 )诱导效应(inductive effect) (2)共轭效应 )共轭效应(conjugate effect) (3)偶极场效应 )偶极场效应(field effect) (4)成键原子的杂化状态 ) 2. 空间效应 (1)空间位阻 ) (2)环张力 ) (3)跨环效应 ) 3. 氢键效应 (1)分子内氢键 ) (2)分子间氢键 )
v = 1307
m’为折合相对原子质量) 为折合相对原子质量
√
— k cm-1 — m’
(K为化学键力常数, 为化学键力常数, 为化学键力常数
常见化学键的力常数K(× 常见化学键的力常数 ×105dyn/cm)
C—C 4.5~5.6 C=C 9.5~9.9 C≡C 15~17 C—O 5.0~5.8 C=O 12~13 C—H 4.7~5.0(CH3X), 5.1(CH2=CH2), 5.9(CH≡CH) C—Cl 3.4(CH3Cl) C≡N 16~18 O—H 7.8(H2O), 7.12(游离 游离) 游离 N—H 6.5(NH3)
五、有关术语
1. 基频峰和泛频峰
基频峰:从基态到第一激发态跃迁产生的吸收。 基频峰:从基态到第一激发态跃迁产生的吸收。 泛频峰:倍频峰: 泛频峰:倍频峰:从基态到第二激发态甚至第三 激发态跃迁所产生的吸收。 激发态跃迁所产生的吸收。 组频峰:基频及倍频的和或差。 组频峰:基频及倍频的和或差。 费米共振:当倍频或组频与一强基频接近时, 费米共振:当倍频或组频与一强基频接近时,两 振动发生偶合,弱的倍频或组频被强化, 振动发生偶合,弱的倍频或组频被强化,两偶合 振动在基频附近出现吸收,均含基频和倍频成分。 振动在基频附近出现吸收,均含基频和倍频成分。
红外光谱的表示: 红外光谱的表示: • • 图表法: 图表法:T%~λ, v 数值数据法:λ, v 数值数据法:
如乙醇的红外光谱图和数据表示: 如乙醇的红外光谱图和数据表示:
二、分子的振动 1. 双原子分子 (1)振动形式: )振动形式: 伸缩振动( 伸缩振动(stretching) ) 弯曲振动( 弯曲振动(bending or deforming) ) (2)振动能级: )振动能级: 共价键的振动, 共价键的振动,可看作一弹簧连接的 两个刚性小球的简谐振动,遵守虎克定律。 两个刚性小球的简谐振动 , 遵守虎克定律 。
诱导效应
O CH3 — C —Cl vC=O 18 07cm-1 O CH3 — C —H 1731cm-1 O CH3 — C —CH3 1715 cm-1
共轭效应
CH3 C=O vC=O 1680 cm-1 O C NH2 1630 cm-1
场效应
(CH3)3C vC=O 1725 cm-1
2925,尖[75] , 2850,尖[45] , 1470[8] 725-720[3] 3000-3080 三元碳环 变化 -CH2-
CH3 CH3 C H CH2CH2CH3
CH3 CH3 C CH3 CH2CH3
CH3CH2CH2CH2CH2CH3
二、不饱和烃 C=C C≡C =C-H ≡C-H - - 特征峰( 官能团 特征峰(cm-1) =CH2 3080[30] 2975[中] 中 =CH- - C=C -CH=CH2 >C=CH2 顺式二氢 反式二氢 三取代烯 ≡CH -C≡C3020[中] 中 1675-1600[中-弱] 中弱 990,尖[50] , 910,尖[110] , 895,尖[100-150] , 800-650[40-100] 965,尖[100] ,
