高一化学同分异构现象1
烷烃同分异构体的书写方法和技巧-高一化学(人教版2019必修第二册)

①同分 ②异构
②具有相同分子式不同结构的化合物互称为同分异构体
概念 内涵
分子式相同: 同相对分子量、同组成元素、同质量分数、同最简式;
结构不同 : 原子连接方式不同、原子的连接顺序不同、不同物质;
烷 烃 同 分 异 构 体 的 书 写 方法 ——减碳链法 主链由长到短 支链由整到散
等效氢的判断
①同一碳原子上的氢原子等效; CH4 CH3CH3 CH3
②同一碳原子上所连接甲基上的氢原子等效;CH3-C-CH3
③处于镜面对称位置上的氢原子等效
CH3
CH3CH2CH2CH2CH3 ① ② ③② ①
【例题】分析乙烷、丙烷分别与Cl2反应可能的一元取代产物的结构简式
CH3—CH3 CH3—CH2Cl
4CH3
1 21 CH3-CH2-CH3 2种
[延伸拓展]一卤代物只有一种的烷烃必须符合什么规律?写
出碳原子数小于10的这些烷烃的结构简式.必须具有高度对称结构
H
HH
HCH
H CH3
H换 —CH3
HCCH
HH
CH3 CH3
H换 —CH3
H3C C CH3
H3C C C CH3
CH3
CH3 CH3
有机物同分异构体数目判断的技巧
3.某烃的一种同分异构体只能生成一种一氯代物,此烃可能是
A. CH4
B. C2H6
C. C3H8
AB E
D. C4H10 E. C5H12
4.下列化学式能代表一种纯净物的是( A )
A. C3H8 B. C4H10 C. C5H12 D.C2H4Br2
2020学年新教材高中化学有机化合物中的官能团、同分异构现象与同分异构体教案鲁科版必修二

第2课时有机化合物中的官能团、同分异构现象与同分异构体[核心素养发展目标] 1.认识有机化合物中官能团的作用,形成“结构决定性质”的观念,能从微观认识有机化合物的结构特点,提高“宏观辨识与微观探析”的能力。
2.理解同分异构体的概念,学会判断及书写简单烷烃的同分异构体,能从简单烷烃的球棍模型和空间填充模型认识有机物的结构特点和同分异构现象,培养“模型认知”和“科学探究”的精神。
一、有机化合物中的官能团1.实验探究乙酸、柠檬酸、乙醇性质不同的原因操作现象Ⅰ、Ⅱ试管中的CaCO3逐渐溶解,生成无色无味气体Ⅲ试管中无明显现象结论乙酸和柠檬酸有酸性,乙醇无酸性解释及结论:三者的结构简式分别为乙酸;柠檬酸;乙醇CH3CH2OH,乙酸和柠檬酸都能和CaCO3反应生成CO2,而乙醇不能和CaCO3反应。
原因是乙酸和柠檬酸都含有相同的原子团——羧基(—COOH),羧基有酸性。
2.官能团比较活泼、容易发生反应并决定着某类有机化合物共同特性的原子或原子团,决定了有机化合物的化学特性。
指出下列物质的官能团名称及结构:(1)CH2==CH2碳碳双键;(2)CH3OH羟基—OH;(3)CH3—COOH羧基;(4)酯基。
3.烃的衍生物像醇、羧酸、酯这些有机化合物可以看作烃分子中的氢原子被其他原子或原子团代替后的产物,这类有机化合物统称为烃的衍生物。
(1)CH4和CH3CH3性质相似,是因为它们都含有相同的官能团—CH3(×)提示CH4和CH3CH3属于烷烃,烷烃分子中不含官能团,—CH3不是官能团。
(2)乙酸和柠檬酸都能使石蕊溶液变红是因为它们都有相同的官能团(羧基)(√)提示乙酸()含有,柠檬酸含有,羧基有酸性。
(3)丙烯(CH3CH==CH2)可以认为CH4分子中的一个H原子被—CH==CH2原子团代替,因此丙烯为烃的衍生物(×)提示烃的衍生物是烃分子中的氢原子被其他原子或原子团代替后的产物,这里的其他原子或原子团不能为烃基,故丙烯仍为烃类。
有机化合物的同分异构现象

官能团异构
官能团种类不同
具有相同分子式但官能团种类不同的化合物,例如乙醇和 甲醚。
官能团数量不同
具有相同分子式但官能团数量不同的化合物,例如丙醛和 丙酮。
官能团位置不同
除了位置异构中所提到的官能团位置不同外,还包括具有 相同分子式但官能团在环上位置不同的化合物,例如邻二
甲苯、间二甲苯和对二甲苯。
03
立体异构
几何异构
烯烃的顺反异构
由于双键两端碳原子连接的基团不同,导致烯烃存在顺式和 反式两种异构体。
环烷烃的构象异构
环烷烃由于碳链的空间排列方式不同,可以形成不同的构象 异构体,如椅式构象和船式构象。
对映异构
手性碳原子
连接四个不同基团的碳原子称为手性碳原子,具有旋 光性。
量子化学计算
基于量子力学原理,对分子的电子结构和性质进行计算。量子化学计算 可以揭示分子的电子云分布、键能、反应机理等详细信息。
03
化学信息学
结合计算机科学和化学知识,对大量化学数据进行处理和分析。化学信
息学可以帮助发现新的同分异构体,预测其性质和活性,并优化合成路线。Fra bibliotek THANKS
感谢观看
结构鉴定
通过同分异构体的分离和鉴定,确定天然产物的确切结构。
立体化学分析
利用同分异构体的立体化学性质,解析天然产物的立体构型。
生物活性研究
比较同分异构体的生物活性差异,揭示天然产物的生物活性机制。
药物设计与开发
药物分子设计
01
基于同分异构体的不同生物活性,设计具有特定药理作用的药
物分子。
药物代谢研究
重难点13 同分异构体的判断与书写-2019-2020学年高一化学重难点探究(人教版必修二)

2019-2020学年高一化学重难点探究(人教版必修二)重难点13 同分异构体的判断与书写方法探究1.同分异构体的种类、书写思路2.常用的同分异构体的推断方法(1)由烃基的异构体数推断判断只有一种官能团的有机物的同分异构体种数时,根据烃基的异构体数判断较为快捷。
如判断丁醇的同分异构体时,根据组成丁醇可写成C4H9—OH,由于丁基有4种结构,故丁醇有4种同分异构体。
(2)由等效氢原子推断碳链上有几种不同的氢原子,其一元取代物就有几种同分异构体。
一般判断原则:①同一种碳原子上的氢原子是等效的;②同一碳原子所连甲基上的氢原子是等效的;③处于镜面对称位置上的氢原子是等效的。
(3)用替换法推断如一个碳碳双键可以用环替换;碳氧双键可以用碳碳双键替换并将氧原子移到他处;又如碳碳三键相当于两个碳碳双键,也相当于两个环。
不同原子间也可以替换,如二氯苯C6H4Cl2有3种同分异构体,四氯苯C6H2Cl4也有3种同分异构体。
(4)用定一移一法推断对于二元取代物同分异构体的判断,可固定一个取代基的位置,再改变另一个取代基的位置以确定同分异构体的数目。
3.同分异构体的书写口诀主链由长到短;支链由整到散;位置由心到边(一边走,不到端,支链碳数小于挂靠碳离端点位数);排布由对到邻再到间;最后用氢原子补足碳原子的四个价键。
典例剖析例1 (2020·资中县第三中学高一月考)下列烷烃在光照下与氯气反应,能生成三种一氯代烃的是( ) A.CH3CH2CH2CH3B.C.D.答案C解析 A.分子结构中有两种化学环境不同的氢原子,则有两种一氯代物,故A错误;B.分子结构中有一种化学环境不同的氢原子,则有一种一氯代物,故B错误;C.分子结构中有三种化学环境不同的氢原子,则有三种一氯代物,故C正确;D.分子结构中有四种化学环境不同的氢原子,则有四种一氯代物,故D错误;综上所述,答案为C。
【点睛】同一个碳原子上的氢原子,为化学环境相同的氢原子,同一个碳上连接的甲基上的氢原子,也为化学环境相同的氢原子。
烷烃的同系物和同分异构体-高一化学同步精品课件(人教版2019必修第二册)

结构相似,组成上差一个或n个CH2
有机物
C2H6、C4H10
相同分子式,不同结构的化合物
化合物
CH3(CH2)3CH3、C(CH3)4
同位素、同素异形体、同系物、同分异构体的比较
①O2和O3②CH3CH3和CH3CH2CH2CH3 和 ④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2C(CH3)2CH2CH3和 CH3CH2CH(CH3)CH(CH3)CH3
② CH2=CH2和
③ CH4 和 CH3CH3
④ CH3CH2CH3 和
否
否
是
是
⑤
否
分子组成上不是相差“—CH2—”
结构不相似
分子式相同,分子组成上没有相差“—CH2—”
②和④
3、同系物判断的三个关键点①“同”——必须属于同一类物质,通式也相同②“似”——结构相似,是指化学键类型相似,分子中各原子的结合方式相似。(即两种物质属于同一类物质)③“差”——组成上相差n个CH2原子团(n≥1)。同系物一定具有不同的碳原子数(或分子式)
4
2 3
——找准称轴、点、面
CH3CH2CH2CH2CH3
对称轴
③ ② ① ② ③
对称点
①
②
②
②
③
③
③
③
对称点
对称面
①
②
①
①
等效氢法
化学性质相似的物质不一定是同系物
相对分子质量
同系物的相对分子质量一定不相同,相差14n
思考与讨论
正丁烷和异丁烷的分子式的分子式都是C4H10。它们是否为同一种物质?
CH3CH2CH2 CH3
正丁烷
异丁烷
甲烷,乙烷和丙烷的结构只有一种,丁烷却有两种不同的结构(如上图),一种是碳原子形成直链的正丁烷,另一种是带有支链的异丁烷。二者的组成虽然相同,但分子中原子的结合顺序不同,即分子结构不同,因此性质就存在一定差异,是两种不同的化合物。
同系物同分异构体课件-高一化学人教版(2019)必修第二册

结构有 A.3种
√B.4种
C.5种
D.6种
链状烷烃的通式为CnH2n+2,相对分子质量为100,则有12n+2n+2 =100,解得n=7,所以该烷烃的分子式为C7H16,分子中含有4个甲
基的结构有
、
、
、
,共4种。
2.写出戊烷(C5H12)所有的结构简式并标明不同化学环境氢原子的种类:
CH3CH2CH2CH2CH3(3种)、
。
1234
(2)丙烷的结构简式为_C_H__3C__H_2_C_H__3 _。 丙烷的分子式为C3H8,其结构简式为CH3CH2CH3。
1234
(3)分子中含30个氢原子的链状烷烃的分子式为_C__14_H_3_0_。 由链状烷烃的分子通式CnH2n+2(n为正整数)可知,2n+2=30,n=14, 其分子式为C14H30。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
2.正丁烷和异丁烷互为同分异构体的依据是 A.相对分子质量相同,但分子的空间结构不同 B.两种化合物的组成元素相同,各元素的质量分数也相同 C.具有相似的化学性质和物理性质
√D.分子式相同,但分子内碳原子的连接方式不同
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
正丁烷、异丁烷的分子式都为C4H10,但正丁烷没有支链,而异丁烷 带有支链,二者分子内碳原子的连接方式不同,所以二者互为同分 异构体。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
3.(2022·嘉兴高一检测)在下列结构的有机物中,属于同分异构体的正确
组合是
①CH3—CH2—CH2—CH2—CH3 ②CH3—CH2—CH2—CH2—CH2—CH3
第七章有机化合物(单元知识清单)高一化学(人教版)(1)

第七章有机化合物单元知识清单【知识导引】一、几种常见的烃二、常见烃的含氧衍生物三、基本营养物质【知识清单】一、⎪⎪认识有机化合物知识点一、烷烃的结构1.碳原子的成键特点—有机物种类繁多的原因(1)原子结构:碳原子有四个未成对电子,可形成四个价键;碳原子可与其他原子成键,碳原子间也可成键。
(2)成键特点:①碳原子间成键方式的多样性:碳原子之间形成碳碳单键(C C)、碳碳双键()、碳碳三键(—C≡C—)。
①碳原子间连接方式的多样性:多个碳原子之间可结合成碳链或碳环,如下图所示。
①碳原子数目灵活性:有机物分子可能只含有一个或几个碳原子,也可能是成千上万个碳原子①碳原子还可以和H、O、N、S、P、卤素等多种非金属原子形成共价键。
2.烷烃的结构特点(1)结构特点:C—C单键、饱和(碳原子剩余的价键全部与H结合,每个碳原子均形成4条价键)、链状(碳原子结合形成的碳链可以是直链,也可以含有支链)。
(2)通式:C n H2n+23.烷烃的命名若碳原子数不多于10时,依次用天干表示,碳原子数大于10时,以汉字数表示;若碳原子相同,结构不同时,用正、异、新表示。
4.甲烷的组成与结构特点知识点二、同分异构体与同系物1.烷烃的同分异构体(1)概念:化合物具有相同的分子式,但具有不同结构的现象叫同分异构现象,具有同分异构现象的化合物互称为同分异构体。
①书写原则:主链由长到短,支链由整到散,位置由心到边①书写步骤:一是先写出碳原子数最多的主链;二是写出少一个碳原子的主链,另一个碳原子即—CH3作为支链,连在主链中心对称线一侧非端点的某碳原子上;三是写出少二个碳原子的主链,另两个碳原子作为—CH2CH3或两个—CH3作为支链,连在主链中心对称线一侧或两侧非端点的某碳原子上。
(2)烷烃一元取代物同分异构体数目2.烷烃的同系物判断(1)概念:结构相似,在分子组成上相差一个或若干个CH 2原子团的化合物互称同系物。
(2)性质:同系物具有相似的化学性质,物理性质具有递变规律,如 C 2H 6、C 3H 8、C 4H 10等烷烃的密度、点、沸点呈逐渐增大(升高)的趋势。
新人教版高一化学必修第二册有机化学基础-同分异构体(基础版)(WORD版含解析)
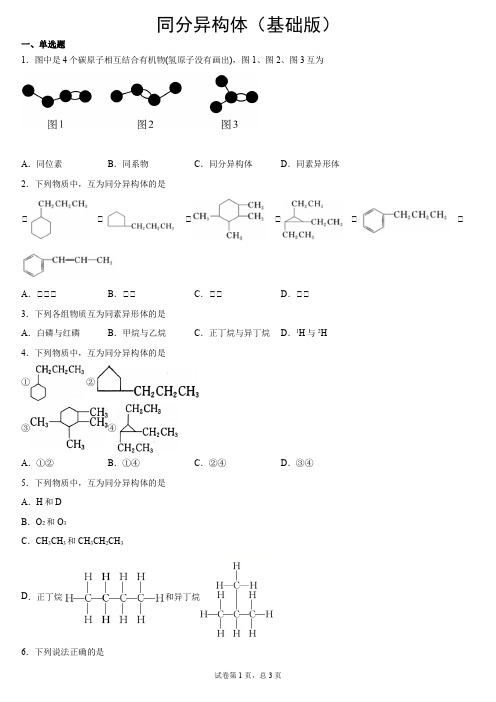
15.B
【分析】
分子式相同,结构不同的有机物互为同分异构体。
【详解】
①和④虽都有5个碳原子,但结构相同,属于同种物质,而②③⑤都含6个碳原子,且都属于烷烃,分子式相同,故互为同分异构体,B项正确;
答案选B。
16.B
【分析】
【详解】
A.同分异构体是指具有相同的分子式且空间结构不同的一类物质,所以其具有相同的相对分子质量,而具有相同的相对分子质量的物质不一定为同分异构体,如NO和C2H6,故A错误;
D.乙醚的分子式为C4H10O,乙醇的分子式为C2H6O,两者分子式不同,因此,两者不能互称同分异构体,D不正确。
综上所述,本题选B。
7.C
【详解】
A.35Cl和37Cl互为同位素 ,故A不选;
B.CH3CH2OH和CH3OCH3分子式相同,结构不同,属于同分异构体 ,故B不选;
C.O2和O3同种元素形成的结构不同的单质 ,互为同素异形体,故C选;
综上所述答案为A。
13.C
【详解】
同位数是指具有相同质子数而不同中子数的同一元素的不同原子之间的互称,据此分析解题:
A.H2与D2均是H2分子,不是原子,属同一物质,A不合题意;
B.氧气与臭氧是分子,不是原子,属于同素异形体关系,B不合题意;
C.12C与14C是两种碳原子,是C元素的两种同位素,C符合题意;
D.干冰和CO2是同一种物质,故D不选;
故选:C。
8.B
【详解】
A.O2与O3都是氧元素组成的不同单质,互为同素异形体,故A不符合题意;
B. 与 是碳元素的两种核素,质子数相同、中子数不同,互为同位素,故B符合题意;
C.H2O与H2O2是氢和氧组成的两种物质,故C不符合题意;
同分异构体-教学设计
这节课的成功之处也能在之后学生的学习过程中表现在以下几个方面:
1.学生感觉到有机化学很有趣,不枯燥。
2.学生学习烷烃的命名时,辨析烷烃结构时会借助想象模型来思考遇到的问题。
3.多个碳原子的同一物质的结构简式的不同写法能够做到快速准确的判断。
八、板书设计
主板书:
同分异构现象:化合物具有相同的分子式,不同结构式的现象。 同分异构体:分子式相同而结构式不同的化合物互称同分异构体。 副板书:
设置情景,引入新知
组织学生交流活动结果。再问:根据 刚才的活动,思考、讨论以下两个冋 题。
1•你的乙烷分子结构模型与其小组
内其他同学所搭建的是否完全相同?2•根据你现在的理解,给出同分异构 现象的定义。
学生很快得到结论:
1.通过比较分子结构模型, 发现虽然各个组的乙烷结 构中氢原子不一定完全重 合,但可以通过碳碳单键的 旋转而实现重合;
四、教学策略选择与设计
设计的基本策略:结构模型,多媒体,课件主要的教法:讲授法,提问法,归纳法,多媒体
辅助法主要的学法:观察法,练习法,讨论法
五、教学重点及难点
重点:以正丁烷和异丁烷、乙醇和二甲醚为例,认识由于微观结构不同而导致的同分异构现象 难点:同分异构体(碳链异构)的书写
六、教学过程
教师活动
预设学生活动
要点解析,突出重点
课件展示
总结归纳同分异构体的一些要点
课件展示
比较同位素,同素异形体,同分异构体
随堂练习
1白磷和红磷可以相互转化,它们在氧 气中燃烧后都生成五氧化二磷,这一事实 说明了白磷和红磷互为()
A.同一单质B.同位素
C.同素异形体D.同分异构体
2.(2011年浙江宁波检测)日本地震引 起的核泄漏中放射性物质主要是Cs和
新教材2022年高中化学苏教版必修第1册学案:专题5 第3单元 从微观结构看物质的多样性

第三单元从微观结构看物质的多样性一、同素异形现象1.同素异形现象:同一种元素能够形成几种不同的单质的现象。
2.同素异形体:同一种元素可形成不同单质,这些单质互称为这种元素的同素异形体。
3.常见的同素异形体:(1)碳的同素异形体:金刚石、石墨、足球烯(C60)差异分析碳原子的成键方式和排列方式不同(2)氧的同素异形体:O2和O3。
(3)磷的同素异形体:白磷和红磷。
1.(知识关联)氕、氘、氚形成的氢气单质互称为同素异形体吗?提示:不是。
因为形成的H2结构相同,性质相同。
2.(情境思考)白磷是一种非常活泼的非金属单质,常温下在空气中能自燃。
白磷在高压下隔绝空气加热后急速冷却,可得灰黑色固体——黑磷,其转化过程如下:白磷黑磷,黑磷性质稳定,结构与石墨相似。
黑磷是否能导电?白磷转化为黑磷是物理变化还是化学变化?提示:能;化学变化。
黑磷结构与石墨相似,故性质相似,即能导电。
二、同分异构现象1.同分异构现象和同分异构体:2.实例:(1)正丁烷和异丁烷(2)乙醇和二甲醚1.(知识关联)互为同分异构体的物质相对分子质量一定相同,但相对分子质量相同的物质其分子式一定相同吗?提示:不一定。
如H2SO4与H3PO4的相对分子质量均为98。
2.(情境思考)同分异构体是造成有机物种类繁多的原因之一,是否只有有机物才存在同分异构现象?提示:不是。
如氰酸铵(NH4CNO)与尿素[CO(NH2)2]互为同分异构体。
三、晶体与非晶体1.晶体:2.晶体的结构与性质特点:3.常见的晶体:(1)离子晶体①概念:由阴、阳离子按一定方式有规则地排列形成的晶体。
②性质:熔点较高、硬度较大。
固态时不导电,在熔融状态下或水溶液中能够导电。
③微粒间的作用力:离子键。
(2)分子晶体①概念:由分子构成的物质所形成的晶体。
分子晶体是分子之间依靠分子间作用力按一定规则排列形成的。
②性质:熔、沸点较低、硬度较小,不能导电。
③微粒间的作用力:分子间作用力、氢键。
认识有机化合物++课件2022-2023学年高一下学期化学人教版(2019)必修第二册

的是 C
A. CH3CH2CH2CH3
B. CH3CH(CH3)2
C. CH3C(CH3)3
D. (CH3)2CHCH2CH3
二、同分异构现象和同分异构体
(1) 同分异构现象 化合物具有相同的分子式,但具有不同的结构现象称为同分 异构现象。
(2) 同分异构体 具有同分异构现象的化合物互称为同分异构体。 如:正戊烷、异戊烷、新戊烷互称为同分异构体。
理 三同 分子式相同、分子组成相同、分子量相同 解 两不同 结构不同、性质不同
③从主链上取下两个碳原子作为两个支链(两个 甲基),连接在相同或不同碳原子上。
—— —
C—C—C—C C C
C—C—C C
练习3:某烷烃的分子式为C7H16,其同分异构体有多少种?试写出 分子结构中含有3个甲基(—CH3)的同分异构体的结构简式。
同分异构体书写方法: 主链由长到短→支链由整到散→位置由心到边→排布由对到邻、间
点拨精讲 22’
1. 如何判断有机物之间是否互为同系物?
提示:同系物间的分子结构相似,碳骨架的链接方式相同,官能团的种类
和数目都一样;同系物间的组成上相差一个或若干个CH2原子团。 CH2
2. CH2=CHCH3和H2C—CH2组成相同,哪个与CH2=CH2互为同系物? 分子组成上相差一个或若干个CH2原子团的有机物一定是同系物吗?
同分异构体 相同分子式,不同结构的化合物
有机物 CH3(CH2)3CH3、 C(CH3)4
练习2:在下列各组物质中:
(A)O2和O3; (B)12C和14C; (C)CH3(CH2)2CH3和CH3—CH—CH3
H
H
(D)Cl—C—Cl和Cl—C—H; (E)CH4和CH3(CH2)5CH3
高中化学《有机化合物的同分异构现象》教学案新人教版必修1

陕西省汉中市陕飞二中高一化学《有机化合物的同分异构现象》教学案新人教版必修1《有机化合物的同分异构现象》教学案(学习目标)有机物分孑同分异构现象产生的原因2.学习韦写简单的韦机物同分异构体(学习过程)一.有机物同分异构现象产生的原因【活动与蘇1】茱分.子分子式为C2耳0,写出该分子可鉅具有的结构式.___________________________ 和___________________________H H M HH-C-C-0-H 与H-C-0-C-HI I I IH H H H恿羽直有机物分子申原子的连核方式不同.昱遛威同分异掏现象的煉因之一■・0R77d、l. . P •IE— 1. 亠【活动与探究2】某二氯丁烯的结构简式为:CHC1二CHC1,该分子具有两种不同的平面结构, 请写出这两种不同的结构。
H CI____________________________ 和 ____________________________ 总结2:有机物分子中原子的空间位置不同"是造成同分异构现彖的另一个原因。
顺反 异构体分子在化学性质方而具有很「大的相似性,在生理活性方而往往具有很大 的差异。
【问题解决2】写岀丁烯的所有同分异构体,包括因为空间位置不同而造成的同分异构体。
【活动与探究3】仔细观察下列两个分子,讨论这两个分子是否为同一个分子。
它们是同分 异构体吗?「总结3:有机物分子中,连接有四个不同原子或原子团的碳原子.称为手性碳原子。
凡是 含手性碳原子的有机物,均存在镜像异构体(又称为对映异构体)。
互为镜像异构 体的两种分子具有不同的旋光性,在大部分化学性质方而都是相同的,但是,在 生理活性方而则具有很大的不同。
【问题解决3】下列物质是否具备对应异构体?是否具有旋光性?若有,请写出楔形式。
① CHoCl② CHClo③ CH :C1:H H H HIlliH —€——C ——C ——C-I I I I⑤ OH OH OH OHNH2楔形式OI-C011④HCOOH【课堂小结L构成同分异构现象的原因:①因为分子中原子的连接次序不同造成异构-一-连接方式的异构②因为分子中的原子在不同的空间位置造成的异构一一顺反异构③因为分子中含有手性碳原子,形成了两种互为镜像的异构体——对映异构《有机化合物的同分异构现象》练习题2.某烷婭的相对分子质量为86,请写出其所有同分异构体的结构简式。
苏教版高一化学必修2 从微观结构看物质的多样性(共23张PPT)

I2
【答案】A
I2 Br2 I2 CsCl
Br2 I2 Br2 SiO2
作业
Ⅰ . ①BaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤ 干冰 ⑥碘片 按下列要求回答: (1)熔化时不需要破坏化学键的是________(填序号,下同), 熔化时需要破坏共价键的是________,熔点最高的是 ________,熔点最低的是________。 (2)晶体以分子间作用力结合的是________。 【答案】(1)⑤⑥/②/②/⑤ (2)⑤⑥
C2H6O 分子结构不同
沸点
78 ℃
-23 ℃
性质
物理性质不同,化学性质不同
二、同分异构现象
3.四角度认识同分异构体 (1)从物质看:互为同分异构体的物质只能是化合物。它们之间的转 化属于化学变化,若共存则为混合物。 (2)从分子式看:互为同分异构体的化合物,其分子式相同,相对分 子质量也相同,但相对分子质量相同的化合物分子式不一定相同,如甲酸 (HCOOH)和乙醇(CH3CH2OH)的相对分子质量均为46。 (3)从结构看:互为同分异构体的化合物,空间结构不同。 (4)从性质看:互为同分异构体的化合物,物理性质不同,化学性质 可能相似。
一、同素异形现象
【例1】意大利罗马大学的Fulvio Cacace等人获得了
极具理论研究意义的N4分子。N4分子结构如图所示,下列 说法正确的是( )
【答案】D
A.N4属于一种新型化合物 B.N4转化为N2属于物理变化 C.N4的摩尔质量为56 D.N4与N2互为同素异形体
二、同分异构现象 1.同分异构现象和同分异构体 (1)化合物具有相同的分子式,但具有不同结构的 现象,称为同分异构现象。 (2)分子式相同而结构不同的化合物,互称为同分 异构体。 (3)同分异构现象主要表现在有机化合物中。
湖南省华鑫高中高一化学竞赛辅导 第二十四讲 同分异构体、同系物

例1.已知二甲苯有三种同分异构体, 则四氯苯有 ______ 种同分异构体.分析: 四氯苯→苯环上有两个H原子→H原子有邻、间、对三种位置关系→四氯苯有三种同分异构体练习: 已知二氯丙烷有四种同分异构体, 则六氯丙烷有 ____ 种同分异构体.例2.一氯戊烷中含有两个“—CH3”的结构为 ____ 种.分析: 解答此题时需要一定的技巧, 必须先写出戊烷的三种碳架:显然, 在碳架①中的氯原子不能连在链端, 碳架②中的氯原子必须连链端, 碳架③不符合题意.此题的正确答案有:练习: C11H16的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.解答: 四种结构简式为:例题3. 已知将中的c与d原子交换位置, 可以得到另一种物质 . C4H8的烯烃同分异构体有 ____ 种.分析: 四个C 的C架有两种: , 将双键在C架上移动, 则有三种同分异构体产生:模仿题给信息: 有两种同分异构体, 即为:故 C4H8的同分异构体有四种.练习: 已知络离子[Pt(NH3)2Cl2]2+是平面结构, 具有顺和反两种异构体, 如下图所示:若络合物[Pt(NH3)2(OH)2Cl2] 是八面体结构,即: 试推测其异构体有___ 种.分析: 设 NH3为 a , Cl 为 b , OH 为 c .例题4. 下列有机物与溴(Br2)发生 1 : 1 的加成反应, 加成产物各有多少种.分析: 此题求解依靠迁移教材中与溴水的反应, 不难看出 , 与溴水发生加成反应, 有 1,2、3,4、1,4 三种加成方式.而与溴水发生加成反应有: 1,2、3,4、1,4、1,6 四种加成方式.结论: (1) 加成产物有 3 种, (2) 加成产物有 4 种.练习: 与H2发生 1 : 4 加成反应时, 其产物有 ______ 种.答案: 四种:例题5. C4H4有多种同分异构体,分别具有以下特征, 试写出相应的同分异构体的结构简式.(1)A 为链状结构, 可以由两分子的乙炔加成而得, A 为 ________.(2)B 为平面结构, 与溴水发生 1 : 1 加成反应, 加成方式有两种, 但加成产物只有一种. B 为 __________ .(3)C 为正四面体, 每个C 原子分别与另三个C 原子通过单键相连. 则C为 _________ . 分析: A 为: C 为:B 为:练习: C6H6有两种常见的同分异构体, A 为苯, B 是具有空间立体结构的图形, 写出它们的结构简式.答案: C6H6C8H8有两种同分异构体, A 是具有空间立体结构的立方烷, B 是芳香烃, 写出它们的结构简式.答案: C8H8巩固练习:1.下列芳香烃的一氯取代物的同分异物体数目最多的是()2.已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如下图:则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为()A.2B.3C.4D.63. 有三种不同取代基-X、-Y、-Z,当它们同时取代苯分子中的3个氢原子,且每种取代产物中,只有两个取代基相邻时,取代产物有()A.2种B.4种C.6种D.8种4.某烃的分子式为C10H14,不能使溴水褪色,但可使酸性KMnO4溶液褪色,分子结构中有一个烷基,则此烷基的结构共有A.2种B.3种C.4种D.5种5.通式为C n H2n-6的苯的同系物中,如果只有一个侧链的各同分异构体在浓硫酸和浓硝酸的条件下,生成的主要..一硝基取代物共有8种,则此n值为()A.8B.9C.10D.116. 1,2,3-三苯基环丙烷的3个苯基可以分布在环丙烷环平面的上下,因此有如下2个异构体。
高一化学专题一原子核外电子排布与元素周期律教案

高一新课专题一原子核外电子排布与元素周期律第三单元从微观结构看物质的多样性知能点二同分异构现象【教材分析】通过初中和《化学1》的学习,学生了解了物质的多样性与其组成的多样性有关:种类不同、数目不等的元素原子按照特定的方式相互组合成不同的物质。
本单元以同素异形现象、同分异构现象、不同类型的晶体位列,帮助学生认识物质的多样性与微观结构的关系。
为《化学2》中的有机化合物知识、选修模块《物质结构与性质》、《有机化学基础》的学习打基础。
【学情分析】智力因素:初中和《化学1》,学生已经学习了物质的多样性与其组成的多样性有关:种类不同、数目不等的元素原子按照特定的方式相互组合成不同的物质。
为本节课的学生打下坚实的基础。
非智力因素:高一新学期,上了几节课时间了,上课和作业的情况,再加上本人建立了学生的作业及成绩档案记录,给学生施加了一些压力,现在的学习氛围还不错。
高一学生学习知识的态度很认真、渴望知识,并且会主动提前预习。
教学过程主要采取循循善诱的方法。
并且对高一学生充满希望,只要一直认真学下去,前途无量。
【教学目标】1、C类:了解以同分异构现象为例认识物质的多样性与微观结构。
B类:认识物质的结构决定物质的性质,性质的特点体现了结构的特点。
A类:了解利用结构模型可以帮助研究物质的微观结构,提高空间想象能力。
2、ABC类:培养和激发学生学习运用实验(模型)、查阅资料等多种手段获取信息的兴趣和能力;激发学生实验探究理论知识的兴趣,特别是激发学生勇【教学重点和难点】教学重点以同分异构现象为例认识物质的多样性与微观结构;认识物质的结构决定物质的性质,性质的特点体现了结构的特点。
教学难点利用结构模型可以帮助研究物质的微观结构;培养和激发学生学习运用实验(模型)、查阅资料等多种手段获取信息的兴趣和能力;激发学生实验探究理论知识的兴趣,特别是激发学生勇于认识科学探究的意义。
【教学流程】一、同分异构现象【导课】前面我们刚刚学习物质的组成微粒,及其相互之间是怎样结合的,并且简单介绍了共价化合物的空间构型,接下来请同学们把书拿出来翻到第20页,结合书上给的例子,我们共同学习和研究下物质的同分异构现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
问题1:对比两个模型,找找它们的联系?
共同点: 分子式相同 不同点: 结构不同
同分异构
二、同分异构现象
化合物具有相同的分子式,但具有不 同结构的现象,叫做同分异构现象。
同分异构体
具有同分异构现象的化合物互称 同分异构体。
问题2:同分异构体间性质有无差异?
同分异构体间的物理性质差异
物质 熔点/℃ 沸点/℃ 液态密度/g· cm-3 结论:
专题1 微观结构与物质的多样性 第三单元 从微观结构看物质的多样性
同素异形现象 同分异构现象
石 墨
世界上最大的钻 石 ——库利南一号 最硬的,无色 透明的晶体 灰 黑 色 固 体
深灰色、不透明、 质软、易导电的片 状固体
C60
思考:为什么同种元素组成的不同种单质的性质相差这么大呢? 结构决定性质 C60的结构 金刚石的结构
氧气
臭氧
O2
O3
无色
淡蓝色
无味
鱼腥味
-183
-112.4
0.030
>O2
②氧气与臭氧的分子结构:
观察:1980-1991年“臭氧洞”的变化
拓展视野
磷元素的不同单质比较:
一 、同素异形现象
同素异形体的化学性质基本相同
(1)C+ O2 ==CO2 (2)氧气和臭氧都具有强氧化性,
臭氧的氧化性更强。 (3)4P+ 5 O2 == 2P2O5
石墨的结构
碳纳米管
一、 同素异形现象 同素异形现象:同种元素形成的单质性质 不同的现象
同素异形体:同种元素组成的性质不 同的几种单质。
例如: C元素的同素异形体有:金刚石、石墨、C60, O元素的同素异形体有:O2、O3, P元素的同素异形体有:红磷、白磷
1实例: 氧元素的不同单质 ①氧气与臭氧的物理性质比较: 化学 式 颜色 (气态) 气味 沸点 ℃ 溶解性
成,名誉副镇长不错,那咱还用不用举行个仪式什么的?”“仪式就免了,低调,一定要低调,咱们做领导的一定要多办实事 少来虚的。所以说,办公室也不用准备为,不去坐班浪费资源多可惜,直接给我这个中介所门口挂一个副镇长兼妇女主任办公 室的牌子就OK了。”第008章 女秘书OK是什么意思?妇女主任是什么?镇长大人有点闹不清楚,反正只要是官大不过自己,并 且又是白干活不拿钱,那就OK了。镇长不明白,可他很聪明的直接认成了一个极好的词,为的显示自己也不是那么的没学问, 选择了以点头表示认可。“那么,以后是不是我们就可以直接称呼你为女鬼大人了?”一同跟来的是镇长的宝贝女儿黄月英— —对啦,镇长也姓黄,只不过,一般人都称呼他为镇长大人,时间久了,也没人记得他真正叫什么名字了。“那是肯定的。” 女鬼大人还没说话,她身旁体重约有半吨重的夜叉咧着大嘴哈哈大笑了起来,“姑姑,以后我是喊你女鬼大人,还是继续叫你 姑姑?”陆婉娉连个白眼都懒得抛向夜叉,用脚趾头想也知道,此时夜叉正在张开足能同时塞下五个大个儿双黄鸡蛋的大嘴正 笑的人仰马翻——唉,夜叉这孩子什么都好,就是太缺心眼儿,并且话还挺多,哪都能插上一嘴,三十好几了还嫁不出去,并 且还贼能吃,这可真愁死个人了。“大人说话呢,小孩子一边儿玩去。”“哦„„”看到自己又惹姑姑生气了,夜叉识趣的扁 了扁嘴,如同一只被踩了尾巴的狗一样,却又是一副欲言又止的样子,看确实无有自己插话的空当,只好回柴房去劈柴了。 “副镇长好副镇长好,既然女鬼大人现在也算是公职人员,那么,我可不可以做女鬼大人的秘书?”黄镇长的女儿黄月英笑的 是见牙不见眼,随着笑纹的深化,露出两个深深浅浅的小酒窝。“嗯?”这下轮到女鬼大人吃惊了。要知道,她要这个名誉副 镇长可是经过深思熟虑的,虽然是有职无权,实际上连职也无有。但是,在门口一挂上个副镇长的牌子,做生意的时候那效果 可就大打折扣了,自己这点儿小九九从不外露,这黄哈咯又是打的哪样牌啊?陆婉娉尚未搭话,倒是黄镇长胡子直晃荡的奋力 点了点头,“我看这主意行,必须通过,你在这里给女鬼大人帮点儿小忙,也省得整天在家里窝不住,里里外外的给我找麻烦 了。这样吧,女鬼大人虽然是名誉副镇长,可是个闲职,没钱养活你这个秘书的,所以你在这里帮忙可以,也同样是没工资赚 的哟!”不愧是德高望重的老镇长啊,知音啊!陆婉娉心里感动的是内流满面。真了解民间疾苦,手下多个干活的女鬼大人同 样不介意,但她一直耿耿于怀的也即是工资这个世人皆敏感的问题,无论哪个年代,赚个钱都不容易,谁愿意让人用刀子在自 己身上一刀又一刀的割肉啊!尤其是对
比较同素异形体、同分异构体、同位素三个概念
同素异形体 同分异构体 同位素
相同点
同一种元 素组成
结构不同
分子式相同 质子数相同 的同种元素
分子结构 不同 中子数 不同
不同点 研究对象
单质O2 O3化合物 NhomakorabeaC4H10
原子
1H 2H 3H 1 1 1
白磷
红磷
12 • 有下列各组物质: A、 13 C 与 6 6C
正丁烷 -138.4 -0.5 0.5788
异丁烷 -159.6 -11.7 0.557
C2H6O 分子式
球棍模型
C2H6O
C2H6O
结构式
名称 沸点
乙醇 78 ℃
二甲醚 -23℃
有机物种类繁多的原因
⑴有机物中可以含一个碳原子,也可成千上万个碳原子。 ⑵碳原子之间可有单键、双键、三键,也可有环状结构。 ⑶大量存在同分异构现象。
点燃
点燃
一、同素异形现象
同素异形体之间转化
(1)C(石墨) C(金刚石)
(2) 3O2 ==2O3
放电
[讨论 ]
分子式相同的物质一定是同一种 物质吗?
动手并思考: 制作C4H10可能的结构模型
H H H H H C C C C H H H H H
正丁烷
H H H H C C C H H H H C H H
B、金刚石与石墨 C、乙醇与二甲醚 D、 CH
CH3
3
CH3CHCH2CH3
CH3 -C-CH3 CH3
(1)互为同位素的是________ (2)互为同素异形体的是________ (3)互为同分异构体的是________
水是生命之源,人类在生活和生产活动中都离不开水,生活饮用水水质的优劣与人类健康密切相关。随着社会经济发展、科学 进步和人民生活水平的提高,人们对生活饮用水的水质要求不断提高,饮用水水质检测 /jcxm/102013228.html标准也相应地不断发展和完善。由于生活饮用水水质标准的制定与人们的生活 习惯、文化、经济条件、科学技术发展水平、水资源及其水质现状等多种因素有关,不仅各国之间,而且同一国家的不同地区 之间,对饮用水水质检测的要求都存在着差异。
