生产过程质量控制点监测管理制度
质量控制点、质量监控管理规程

1、目的用于加强对质量控制点的管理,规范公司质量监控管理,使所有的过程始终处于受控状态:对仓库、生产车间、检验现场进行监控,确保公司的质量管理符合法规要求。
2、适用范围适用于公司物料储存、生产过程、质量检验的监控。
3、职责3.1生产部负责质量控制点确认,负责编制作业指导书、工艺流程图等质量控制点的管理文件。
3.2生产部负责对生产人员进行培训,生产车间负责按质量控制点文件的具体规定组织实施。
4、工作程序4.1质量控制点的设置原则4.1.1对于整个产品的性能、可靠性、安全性等方面有直接影响的关键项目。
4.1.2工艺文件有特殊要求,对下道工序的加工有重大影响的项目。
4.2质量控制点人员职责分工参与质量控制点的日常工作人员有:操作者、生产管理人员、检验员其职责分工如下:4.2.1操作者—熟悉掌握操作者技能和本工序质量控制方法;熟悉掌握操作方法,严格按工艺文件进行操作和监控,认真自检,按要求填写各项原始记录;做好设备的日常维护保养;发现工序异常,迅速向生产管理人员报告,必要时上报有关部门采取纠正措施。
4.2.2生产管理人员—对操作者进行质量控制点的培训及现场指导,同时应把工序控制点作为工艺检查重点,督查操作者是否按工艺工序控制点有关规定和制度去执行;发现违章作业立即劝阻,对不听劝阻者及时报告并做好记录。
4.2.3检验员—贯彻实施生产部下达的工序质量文件,对质量控制点进行日常监控及记录,发现异常质量波动的应及时告知生产管理人员,协助操作者找出原因,采取措施,加以解决;必要时下达停工指令,同时上报质量部。
4.3质量控制点要求4.3.1质量监控管理的对象是生产过程中构成质量控制点的要素,即人、设备、物料、工艺方法及环境五个方面处于控制状态,为此分析找出其中主导要素。
4.3.2质量监控管理由质量部和生产部同时进行,以保证质量监控工作的有效性。
4.4现场监控方式4.4.1询问相关人员了解职责;4.4.2现场查看生产现场(物料、标识等)、物料存放情况、卫生清洁情况等;4.4.3查阅文件和记录,相关程序规定及记录填写是否符合要求。
生产过程质量控制、质检制度

生产过程质量控制.质检准则生产过程是产品及其质量的保证和实现过程,对这一过程的质量进行控制,具有重要意义。
生产流程原料→检验→入库→出库→称量→混料(助剂)→挤出→冷却→吹干→切粒→包装→检验→合格→成品→入库1生产准备状态检查生产过程是一个系统工程。
为确保这个系统工程协调.有效地运行,多.快.好.省地生产出产品来,产品在生产之前,组织应对生产的准备状态进行全面.系统的检查,并对检查作业进行有效地控制,保证检查过程的全面性.系统性和有效性。
1.1成立检查组1.1.1检查组的组成最高管理者授权一名主管领导(是管理者代表)组建生产准备状态检查作业组,并担任检查组组长。
产品设计.生产工艺.质量管理.质量检验.理化计量.标准化.生产计划.生产部门.生产现场.设备动力,物资供应等有关部门和单位选派出有经验的专业技术人员和管理人员参加检查作业组。
如合同有规则顾客派代表参加,则按合同规则执行。
为了防止泄密,不允许外组织的人员和无关的人员参加检查活动。
1.1.2检查组作业职责①质量管理部门负责编制检查计划与检查活动的协调作业,并监督检查过程的作业质量;②检查组组长负责组织.领导检查作业,审查检查单,提出检查报告质量;③检查组成员的作业:·根据分工,确定检查项目及检查的方式方法.编制相应的检查单,送给组长审批,批准后实施;·实施检查。
按检查项目和检查的方式方法检查;·对检查结果做出准确.公正.客观的评价。
1.2检查作业流程生产准备状态检查流程:申请检查一审查申请一实施检查一处置。
1.2.1申请检查受检查的部门(单位)根据检查内容与要求进行认真准备,当准备好后,向质量管理部门提出申请检查报告,列出受检查的各项内容。
1.2.2审查申请检查组长组织检查组全体成员对申请检查报告进行审查,如同意申请,则按组内分工,检查组成员对受检查对象确定其检查项目,将其列入检查单,送组长审批。
1.2.3实施检查由于检查的专业性很强,要按分工进行检查,由2~3人为一个小组进行检查,互相协作,互相监督,做到检查科学.公开.公平.公正.准确,按计划按程序进行检查。
生产过程质量控制制度

生产过程质量控制制度生产过程质量控制制度是指企业为确保产品质量稳定、符合标准要求而建立的一套规范化的管理制度。
该制度涵盖了从原材料采购到产品出厂的全过程,旨在通过各种控制措施和方法,确保产品在生产过程中的质量稳定性和一致性,以满足客户的需求和期望。
一、制度目的和适合范围生产过程质量控制制度的目的是确保产品质量的稳定性和一致性,以满足客户的需求和期望。
适合范围包括企业所有生产过程和环节。
二、质量控制组织架构1. 质量管理部门:负责制定和监督执行质量控制制度,负责产品质量的监测和评估。
2. 生产部门:负责具体的生产工艺和操作,执行质量控制制度。
三、质量控制流程1. 原材料采购控制:a. 制定供应商评估标准,对供应商进行评估和审批;b. 采购部门按照标准采购原材料,并对原材料进行检验和入库控制。
2. 生产过程控制:a. 制定生产工艺标准和操作规程,明确各个工序的要求;b. 生产部门按照工艺标准和操作规程进行生产,确保每一个工序的质量;c. 设置生产过程监控点,对关键参数进行实时监测和记录;d. 定期进行生产过程的抽样检验和数据分析,及时发现问题并采取纠正措施。
3. 产品检验控制:a. 制定产品检验标准和方法,明确产品的各项指标和要求;b. 在生产过程中进行抽样检验,确保产品符合标准要求;c. 对成品进行全面检验,确保产品质量的稳定性和一致性。
四、质量控制记录和数据分析1. 建立质量控制记录,包括原材料检验记录、生产过程监测记录、产品检验记录等;2. 对质量控制记录进行定期分析,发现问题和异常,及时采取纠正措施;3. 建立质量控制数据统计和分析系统,对数据进行统计和分析,提供决策支持。
五、不合格品处理和纠正措施1. 对于不合格的原材料,采取退货、索赔或者重新采购等措施;2. 对于生产过程中浮现的问题,及时停产并进行分析,找出问题原因并采取纠正措施;3. 对于不合格产品,进行分类处理,包括修复、报废、退货等。
生产过程质量监控管理制度

生产过程质量监控管理制度
制 定
部门审核
质量部审核
制定时间
审核日期
审核日期
批 准
批准日期
执行日期
分发部门
质量部
1.目的
本标准规定了生产过程质量监控的要求、内容。
2.适用范围
本标准适用于生产现场的质量监控。
3.职责
质量部:负责监督本规定实施;
QA人员:负责按本规定操作。
4.内容
4.1.生产开始前检查:
4.1.7.物料具正常状态标志。
4.1.8.计量用具、仪器、仪表经过校正,校定是在有效期内并符合规定要求。
4.1.9.生产用水符合要求。
4.2.生产过程
4.2.1.生产现场整洁,物料摆放整齐,生产操作规范有序,地面整洁。
4.2.2.物料品名、规格、数量、外观质量等情况应与生产所需相一致。
4.2.3.称量有复核。
4.3.3.设备清洁规程要求对设备进行清洗,其结果符合规定要求。
4.3.4.按洁净区清洁规程要求进行清洁,其结果符合规定要求。
4.3.5.按洁净区周转容器清洁规程要求进行清洁,其结果符合规定要求。
4.1.1.生产场所设施、环境卫生应符合规定要求。
4.1.2.空气净化级别应符合规定要求。
4.1.3.个人卫生、工衣着装应符合规定要求。
4.1.4.有生产指令、岗位SOP和清洁清场合格证。
4.1.5.设备管道、工具、用具、容器应完好洁净,状态标志符合生产要求。
4.1.6.原辅、包装材料品名、规格、数量、外观质量等情况应与生产要求相一致并具合格标记。
4.2.4.生产现场应有批生产操作记录。
4.2.5.生产记录填写符合规定要求。
4.2.6.生产操作过程、操作参数控制符合岗位SOP、生产指令。
生产过程监控管理制度

生产过程监控管理制度
生产过程监控管理制度是企业为保障生产过程的稳定和质量控制而制定的规章制度。
该制度的目的是确保生产过程的顺利进行,监控生产环境和生产流程,防止生产过程中发生事故和质量问题,保证产品的质量和安全,提高生产效率和客户满意度。
1. 生产环境监控:包括对生产场所的温度、湿度、光线等条件进行监控,确保生产环境符合产品的要求。
2. 生产设备监控:对生产设备进行定期检查和维护,确保设备正常运行和安全使用。
3. 生产流程监控:对生产过程中的关键环节进行监控,例如原料的采购、配料、搅拌、加热、冷却等过程,以确保产品的质量和一致性。
4. 产品质量监控:对产品进行质量抽检和测试,确保产品符合国家和企业的标准和要求。
5. 不良品处理:制定不良品处理的流程和方法,对不合格产品进行分类、处理或退回,并记录不良品情况和处理结果。
6. 事故预防和应急措施:制定事故预防措施,对潜在的生产安全隐患进行排查和处理,并建立应急预案,以应对突发事故和故障。
7. 绩效评估和改进:对生产过程的监控和管理进行定期评估,找出存在的问题和不足,并制定改进措施,以提高生产效率和产品质量。
生产过程监控管理制度的实施需要全员参与和执行,包括生产人员、技术人员、质量控制人员等。
企业应定期进行培训和宣传,提高员工的意识和能力,确保制度的有效执行。
生产过程关键质量控制环节(点)管理制度

生产过程关键质量控制环节(点)管理制度一、编制目的为了为加强食品安全管理工作,保证相关制度有效实施,特制订本管理制度。
二、适用范围适用于本企业所有涉及与食品安全及食品管理的生产过程关键质量控制环节(点)控制管理。
三、关键控制环节(点)的确定(一)所有食品1.1关键控制环节(点):原辅料质量,验收控制1.1.1使用的原辅材料为实施生产许可证管理的产品,必须选用获得生产许可证企业生产的产品,并有合格证明。
1.1.2品管部负责制定原材料检验标准和对其进行感官检验的各类检测规程、检测点、检测频率、抽样标准、检测项目和判定依据,使用的检测设备等。
1.1.3包装材料供应商为合格供方。
采购的物品入库前,由经销部门采购人员通知质检部门进行抽样和感官检验,质检部门索取产品质量证明(产品合格证、卫生检验检疫合格证明、检验报告等)进行验证,根据《检验规程》和《检验报告》对原材料做出判定,由品管部门填写《材料入库清单》。
对不合格品进行退货处理。
1.1.4生产用水每年抽样送具有资质的检验机构按生活饮用水标准作一次全项检验;1.1.5仓库根据判定结果办理入库手续,入库过程中,由仓库保管员负责核对并检查到货规格、数量、等级是否与发货单和本公司采购合同一致,有无运输损坏;验证无误后,办理入库手续。
(二)膨化食品2.1关键控制环节(点)1:蒸练(油炸型)。
2.2关键控制环节(点)2:干燥(油炸型)、挤压膨化(直接挤压型)。
2.3关键控制环节(点)3:油炸(油炸型)、烘焙(直接挤压型)。
(三)肉制品(热加工熟肉制品类:酱卤肉制品)3.1关键控制环节(点)1:添加剂使用。
3.2关键控制环节(点)2:热加工温度和时间。
3.3关键控制环节(点)3:产品包装和贮运。
3.4关键控制环节(点)4:灭菌。
(四)炒货食品(烘烤类、油炸类、其他类)4.1关键控制环节(点)1:原料清理控制。
4.2关键控制环节(点)2:蒸煮或浸料时的配方控制。
4.3关键控制环节(点)3:原料、半成品、成品的仓库储存条件控制。
生产过程质量控制点监测管理制度

生产过程质量控制点监测管理制度生产过程质量控制点监测管理制度目的:制定生产过程重要质量控制点监测管理制度,确保产品在各个生产环节质量得到严格控制。
二、适用范围:适用于生产部药品生产的质量监控。
三、责任者:生产部生产人员及其管理人员,QA监督员。
四、正文:为了确保产品的质量,必须对生产过程的质量进行监控,现将生产过程重要质量控制点及其监督管理制度表述如下:1、原辅料使用前应目检其物理外观,核对净重并过筛。
液体原辅料应过滤,除去异物。
过筛后的原辅料应粉碎至规定细度。
2、配料配料前应仔细核对原辅料品名、规格、批号、生产厂家及编号,应与检验单,合格证相符。
处方计算、称量及投料必须复核,操作者及复核者均应记录上签名。
3、制粒制料时,必须按规定将原辅料混合均匀。
注意粘合剂的浓度及筛网的大小,并要控制好湿颗粒的干湿程度。
4、干燥严格控制干燥温度,防止颗粒融熔、变质,并定时记录温度。
干燥过程中应按规定翻料,并记录,要注意干燥程度。
5.整粒与混合整料机的落料漏斗应装有磁铁,除去意外进入颗粒中的金属屑。
混合宜采用V型混合机进行总混,每次总混量为一个批号。
混合机的装量一般不宜超过该机总容积的三分之二。
6.片剂6.1 片剂的压片压片前应试压,并检查片重、硬度、厚度、崩解时限和外观,必要时可根据品种要求,增测含量、溶出均匀度。
符合要求后才能开车,开车后应定时(最长不超过15分钟)抽样检查平均片重。
6.2 片子的包衣在包衣过程中,应注意片子的外观,在包衣后,测定片子的崩解时限。
7.胶囊剂的灌装灌装前就试灌,并检查装量、崩解时限和外观,必要时可根据品种,增测含量,溶出度或均匀度。
符合要求后才能灌装。
灌装后应定时抽样检查平均装量,并进行装量差异检查。
8.包装对包装生产线上的产品品名、批号、有效期(或使用期)、标签、装箱单(合格证)、装箱质量、装箱数量等应检查核对,使与实物相符。
9.清场生产现场在换批号和更换品种、规格时,应按清场管理要求进行清场。
质量控制点管理制度(5篇)

质量控制点管理制度1目的和适用范围为加强对质量控制点的管理,使所要控制的过程始终处于受控状态,以确保稳定地生产合格产品,特制定本制度。
适用于公司对关键过程的质量控制。
2职责3工作程序参与质量控制点日常工作的人员主要有:操作者、质检员、机修员、巡检、其职责分工如下:操作者—熟练掌握操作技能和本工序质量控制方法;明确控制目标,正确测量,认真自检,自做标记并按规定填写原始记录;做好设备的维护保养和点检工作;发现工序异常,迅速向质捡人员报告,请有关部门采取纠正措施。
质检员—按作业指导书对控制点进行重点检查,把检查结果及时报告操作者,并做好记录。
同时监督检查操作者是否遵守工艺____和工序控制要求,并向车间技术人员报告重要信息。
机修员—按规定定期对控制点设备进行检查和维护,督促检查设备点检活动,根据点检信息,及时对设备进行检修和调整,并做好设备维修记录。
巡检员—贯彻实施工艺部门下达的工序质量控制文件,对各类人员进行现场指导,参加控制点的验收和日常检查,负责对异常质量波动的分析和研究纠正措施。
质量控制点管理制度(2)是一个组织内部用来管理和控制质量的体系,旨在确保产品或服务的质量能够达到预期水平。
以下是一个简要的质量控制点管理制度的内容:1. 目标和原则:明确质量控制的目标和原则,例如追求零缺陷、持续改进等。
2. 资源管理:确保有足够的资源用于质量控制,包括人力、设备、物料等。
3. 质量计划:制定质量计划,包括质量目标、控制点、质量检测方法等。
4. 质量控制点设置:确定关键的质量控制点,即产品或服务中需要进行质量检测或控制的节点。
5. 质量控制方法:明确使用的质量控制方法,例如抽样检验、全面检测、统计过程控制等。
6. 质量检测:建立质量检测程序,包括检测方法、检测标准、检测频率等。
7. 非符合品管理:建立非符合品管理程序,包括发现及处理不合格品的方法和责任。
8. 数据分析:对质量数据进行分析,发现潜在问题,并提出改进措施。
公司GMP管理文件---生产过程质量控制点监测管理制度

公司GMP管理文件---生产过程质量控制点监测管理制度一、目的:制定生产过程重要质量控制点监测管理制度,确保产品在各个生产环节质量得到严格控制。
二、适用范围:适用于生产技术部生产过程的质量监控。
三、责任者:生产技术部经理、QA检查员。
四、正文:为了确保产品的质量,必须对生产过程的质量进行监控,生产过程质量控制点及其监督管理制度如下:1最终灭菌小容量注射剂2.1纯化水、注射用水:澄明度必须符合标准2.2安瓿的洗涤及干燥灭菌:在准备室脱去外包装送入粗洗室粗洗,后送入精洗室洗涤,外壁应冲洗,内壁至少用纯化水洗两次,最后经过0.45μm 滤膜滤过的澄明度合格的注射用水洗净,干燥、灭菌、冷却,灭菌后的安瓿应立即使用或清洁存放贮存不得超过2天,洗涤后的瓶子应进行清洁度及澄明度检查。
1.3称量:称量前应核对原辅料品名、批号、生产厂家、规格,应与检验报告单相符。
调换原辅料供应商时应有小样试验合格单或已经过验证的报告;称量时必须有复核人,操作人和复核人均应在原始记录上签名。
1.4配制:配制罐必须标明配制液的品名、规格、批号和配制量,投料时必须有人复核及做记录。
1.5粗滤及精滤:药液经含量、PH值检验合格后方可精滤,盛装容器应封闭,标明药液的品种、规格、批号。
药液配制至灭菌一般应在24小时内完成。
1.6灌封:灌装管道、针头使用前用注射用水洗净并煮沸灭菌,直接与药液接1.7灭菌:双扉式灭菌柜,产品灭菌前,要核对品名、批号、数量,按规定的灭菌标准操作程序操作,灭菌时应及时做好记录,并密切注意温度、压力、时间,如有异常情况应及时处理。
灭菌后进行检漏,检漏的真空度在-8kpa。
1.8灯检:检查员视力在0.9以上,视力每年检查一次,检查后的半成品要注明检查者的姓名,由专人抽查。
不合格品及时分类记录,标明品名、规格、代号、批号,置于盛器内移交专人处理。
1.9印字包装:操作前应校对半成品的名称、规格、批号及数量是否与领用的包装材料一致。
1生产过程关键控制点质量管理及考核制度

1生产过程关键控制点质量管理及考核制度一、生产过程的重要性生产过程是指将原始材料转化为最终产品的一系列操作。
一个高效且良好管理的生产过程能够有效地提高产品的质量,并确保产品能够按时交付。
因此,建立一个科学、规范且有效的生产过程管理是企业不可或缺的一项工作。
二、关键控制点的质量管理1.确定关键控制点:通过对生产过程进行细致的分析,确定哪些环节对产品质量起着决定性的作用。
例如,对于食品行业来说,食品加工过程中的温度、时间、酸碱度等因素都是关键控制点。
2.制定操作规程:为每一个关键控制点编制详细的操作规程,包括工艺参数的设定、操作方法的描述、记录的要求等。
同时,制定好的操作规程应该在生产过程中得到严格的遵守,确保每一个关键控制点都得到有效地控制。
3.监测与控制:在关键控制点的质量管理中,监测与控制是十分重要的一环。
通过实时监测和记录环节的数据,确保操作规程得到严格的遵守。
同时,对于关键控制点的参数进行严格的控制,确保产品质量的稳定性。
4.问题分析与改进:关键控制点的质量管理应该是一个不断改进的过程。
当出现质量问题时,需要进行问题分析,找出问题的根本原因,并采取相应的改进措施,避免类似问题再次发生。
三、考核制度的建立为了确保关键控制点质量管理的有效实施,需要建立一个完善的考核制度。
该制度可以包括以下几个方面:1.考核指标的设定:根据关键控制点的质量要求,制定相应的考核指标。
例如,对于食品行业来说,可以考核关键控制点参数是否达到预定值,产品是否符合卫生标准等。
2.考核方法的选择:根据不同的关键控制点,选择适合的考核方法。
可以采用抽样检验、抽查等方法,对关键控制点的质量进行考核。
3.考核频率的确定:根据企业的实际情况,确定考核的频率。
可以每日、每周或每月进行考核,以确保生产过程的持续改进。
4.考核结果的处理:根据考核结果,及时对不符合要求的情况进行整改措施,并对合格情况进行奖励措施,以激励员工保持良好的质量管理。
生产过程质量控制点监测管理制度

生产过程质量控制点监测管理制度( Monitoring and managementsystem of quality control points in production process Monitoring and management system of quality control points in production process 2007-6-16 0:00:00 China 114 network browsing: 2001 veterinary drug tradeCompany GMP management documentsSubjectMonitoring and management system of quality control points in production processCode:SMP-SC-0160-00A total of 7 pagesFormulateTo examineApprovalDate setAudit dateApproval date Issuing department Offic e Quantity issued effective date Distribution unit Office, production technology department, quality department, material supply department, Engineering Department I. Objective: to formulate the monitoring and managementsystem for important quality control points in the production so as to ensure the strict control of the quality of the process , product s in each production link. Two. Scope of application: in the production process it is applicable to quality of production technology department. contro l Three 、 responsibility: production technology manager, QA inspector. Four, text: In order to ensure the quality of the products, the quality of the production process must be monitored and controlled,the quality control points of the production process and the supervision and management system are as follows:1final sterile small volume injection2.1purified water, water for injection: clarity must meet the standards2.2ampoule washing and drying sterilization: in the ready room off the packaging into the rough rough wash wash room, wash room evacuation into washing wall should be rinsed with purified water, the inner wall of at least two times, finally rinse with water after injection of 0.45 m membrane filtration qualified clarity, drying, sterilizing, cooling, ampoule after sterilization should be used immediately or stored clean storage shall not exceed 2 days, after washing bottles should be clean and clarity check.1.3weighing: before weighing, should check the raw materials, name, batch number, manufacturer, specifications, should be consistent with the inspection report. When changing the raw and auxiliary materials supplier, there should be a sampletest certificate or a verified report; when weighing, there must be a reviewer; the operator and the reviewer should sign on the original record.1.4, preparation: the preparation tank must mark the name, specification, batch number and preparation quantity of the preparation liquid, and the material must be reviewed and recorded when feeding.1.5 coarse filtration and fine filtration: after the content of liquid medicine, pH value of qualified inspection, can be carefully filtered, the containers should be closed,indicating the variety of liquid medicine, specifications, batch number. The preparation of liquid medicine to sterilization should be completed within 24 hours.1.6, potting: filling pipes, needles, before use, with injection water washed and boiling sterilization, directly connected with the solutionThe inert gas and compressed air are purified before use, and their purity and particle size should be in accordance with the regulations, and the filling capacity shall be filled according to the relevant provisions. A small sample of semi-finished timely check clarity, loading, sealing quality, semi-finished container should indicate the product name, specifications, batch number, date, filling and sealing machine number and sequence number, name of the operator.1.7: double leaf type sterilization sterilization cabinet products before sterilization, to check the name, batch number, quantity, according to the standard operation procedure of sterilization, sterilization should be timely record, and pay close attention to temperature, pressure and time, if there is abnormal situation should be promptly dealt with. Leak detection after sterilization, vacuumdegree of leak detection at -8kpa.1.8 lamp inspection: inspector's eyesight is above 0.9,Visual inspection once a year, after the inspection of semi-finished products should indicate the nameof the examiner, by hand spot check. The unqualified products timelyclassification records, indicating the name, specifications, code, batch number, placed in the container transfer special treatment.1.9 printing packing: the name, specification, batch number and quantity of semi-finished products should be checked whether they are in accordance with the packing materials. In the process of printing, packaging, packing should always check the name, batch number, specifications, packaging after the damage and the remaining number and collar number, good practical statistics for packaging materials for the number of material balance check, end evacuation quarantine quarantine, inspection after storage.2oral liquid2.1configuration and filtration2.1.1c onfiguration involves equipment, containers, piping, filter plates, cleaned with hot water before use.2.1.2oral liquid should be completed within 4~5 hours, mainly refers to the continuous operation according to the production plan.2.1.3t he prepared liquid should be filtered to the dilute mixing tank in time.2.2potting2.2.1f illing process involves the filling equipment, containers, bottles, storage tanks, pipes, before use, clean with hot water.2.2.2c ontinuous operation according to filling position operation rules, the filling of oral agent should be completed within 8 hours.2.2.3s terilizationBefore the operator enters the work room, the ultraviolet lamp should be opened to irradiate and sterilize.Oral preparation of liquid medicine in preparation process boil, heat preservation 30 minutes sterilization.3Powder3.1weighing and batching:3.1.1r aw materials or intermediate products before weighing shall be cleaned or removed, and the material name, specification and batch number shall be carefully checked and should be in conformity with the inspection report and certificate.3.1.2prescription calculation, weighing and delivery must be reviewed and the operator and reviewer should sign on the record.3.1.3the raw material of the batch is packed in the container and marked with the name, batch number, specifications, quantity, weighing person and date.3.2mix:3.2.1b efore mixing, check the material name, batch number, quantity, etc., confirm the error, and then proceed to the next step.The amount of 3.2.2 generally does not exceed 2/3 of the total capacity of the aircraft.3.2.3mixes the homogeneousmaterial into a batch and makes upa batch number.3.3packaging process:3.3.1p reparation before packing:3.3.1.1prior to the inspection of the packing area: check whether there are any items in the production area which have nothing to do with the batch production.3.3.1.2should not deal with different batches of products in the same packaging room at the same time.Acceptance of 3.3.1.3 products and packaging materials: checking, checking and verifying the codes, batch numbers, commodity names and quantities of packing materials andproducts in accordance with the batch production record.3.3.1.4batch number and validity check printing: in manual or machine printing batch number, production date, the validity of the process, according to the batch record should carefully check the carton, packing bags, labels, inspectioncertificates printed on compliance with requirements.3.3.2p ackaging operations:3.3.2.1at the start of the examination: first set the batch number, production date, the period of validity of the label and certificate shall be attached to the batch file, and manual printing and packaging materials should also be included in the batch file and sampling.3.3.2.2check the batch production record and check the first packing unit,Have you used any packing material that should be used and if there is any defect in the package?.3.3.2.3check the batch number, date of manufacture andvalidity of the printing is correct, the handwriting is clear.3.3.3p acking process: the packing process should be checked with the outer packing box and the instruction manual, and the packing operation can be carried out without error.3.3.4f ile archiving:- fill in the intermediate control records correctly, withoutomission;- samples of printed packing materials are complete and correct. The final documents must be sent to the quality department.3.3.5 clearance:The production site in batches and replacing varieties, specifications, according to the requirements of clearance clearance management. We should hang signs QA clearance after passing the acceptance.4disinfectant4.1weighing: before weighing, should check the raw materials, name, batch number, manufacturer, specifications, should be consistent with the inspection report. When changing the raw and auxiliary materials supplier, there should be a sample test certificate or a verified report; when weighing, there must be a reviewer; the operator and the reviewer should sign on the original record.4.2, preparation: the preparation tank must mark the name, specification, batch number and preparation quantity of the preparation liquid, and the material must be reviewed and recorded when feeding.4.3filling: filling capacity according to the relevant provisions of filling. A small sample of semi-finished timely check clarity, loading, sealing quality, semi-finishedcontainer should indicate the product name, specifications, batch number, date, filling and sealing machine number and sequence number, name of the operator.4.4printing packing: the name, specification, batch number and quantity of semi-finished products should be checked whether they are in accordance with the packing materials. In the process of printing, packaging, packing should always check the name, batch number, specifications, packaging after the damage and the remaining number and collar number, good practical statistics for packaging materials for the number of material balance check, end evacuation quarantine quarantine, inspection after storage.5the quality control points of each dosage form are attached to the schedule.6 process management:6.1process quality management by the quality department is responsible for the management.The object is to makethe process of quality managementelements of process quality of the production process, namely, equipment, materials, technology and the environment of the five areas were in a state of control, so the analysis to find out the leading factors.The management and control methods are put forward and implemented for the leading factors that affect the quality of process.6.2management content and requirements:6.2.1m anagement content:6.2.1.1decides to manage projects that are quality, cost, quantity, safety, equipment, and people.6.2.1.2determines management objectives and their control points.6.2.1.3determines the way to achieve goals andinstitutionalize them.6.2.1.4determine equipment and inspection equipment.6.2.1.5determines the operation methods, environment, and procedures.6.2.1.6 determine material quality requirements.6.2.1.7 determine methods of measurement, inspection, examination and test, as well as process quality audit and product inspection methods 6.2.1.8 determination, inspection and evaluation methods.6.2.1.9 determines handling methods.6..2.2 management requirements:Quality managementof 6.2.2.1 process is carried out by quality department and relevant departments to ensure the quality ofquality management work.6.2.2.2process quality management activities are often carried out,Plans and report to company leader for approval.6.2.3c heck:6.2.3.1inspection departments are working procedure quality management system, the original records, inspection results and measures.The implementation of 6.2.3.2 inspection measures.The 7 schedule:The key points of quality control of small capacity injection 7.1final sterilizationProcessQuality control pointProject quality control frequencyWater systemPurified water conductivity 1 /2h "China Veterinary Pharmacopoeia" full 1 times a weekWater for injectionElectrical conductivity, pH, chloride, ammoniumsalt, clarity 1 /2h "China Veterinary Pharmacopoeia" full 1 times a weekWash bottleThe original packaging ampouleTest report, cleanlinessTunnel oven1 /2htemperature 1 /2hAfter cleaning the ampouleCleanliness 1 /2hPreparationLiquid medicineBatch classification and preparation, drug content, pH, clarity, color, filtering equipment and inspection (such as bubble etc.) 1 /2hPottingDrying ampoulesCleanlinessLiquid medicineColor and lustre1 /2h1 /2hClarity 1 /2hSealLength and appearance 1 /2hThe second half finished fillingThe liquid volume, Cheng Mingdu 1 /2hSterilizationSterilization cabinetMark, volume, temperature, time, vacuum, record 1 /2h Before and after sterilization of semi-finished products The appearance of cleanliness, marking, storage area1 /2hLight inspectionLight inspection productsCheck clarity 1 /2hEach marker, lamp examination code, storage area 1 /2h PackingIn the packaging productsEach marker, lamp examination code 1 /2hPrintingBatch number, content, writingBoxThe number, specification, label1 /2h1 /2hLabelThe content, quantity, usage 1 /2hPackingThe quantity, packing list, printing content, packing their code 1 /2hThe key points of quality control of 7.2 oral liquid ProcessProject quality control frequency of checksWash the bottle and a rubber plugBottled water clarity meets the requirements.Water filled with water to full control.2 / classWash water clarity to meet the requirements.The temperature of 121 DEG C + 2.30 minutes.The pressure of 0.1 Mpa + 0.02.PreparationPurification of water quality standard.2 / classAt the beginning of the filter filter material: titanium bar.Filter precision filter: 0.45 m microporous filter.Filter filter integrity requirementsThe temperature of 18-26 DEG C.Humidity 30-65%.Differential pressure is not less than 5Pa.The size of the liquid medicine preparation prepared accurately.7.3 powder quality control pointsworking procedureQuality control pointQuality monitoring project frequency Mixing weighing accuracyEach batch of blendUniformityEach batch ofWater contentEach batch ofInside the packagePacking quantityDrug loading capacityAt any time / classSealSealing tightness, appearanceAt any time / class outsourceLabelThe content, quantity, usageEach batch ofIn the bagIn the bag containing the packet numberAt any time / classPackingThe quantity, packing list, printing contentEach boxThe key points of quality control of 7.4 disinfectantworking procedure control pointProject quality control frequency bottle Plastic bottle 1. standard.2. to meet the requirements of cleanliness.2 / classDistribution of liquid positionDrinking water clarityStandard.Standard.2 / classPH value2 / class contentStandard.1 / classFilling roomThe indoor temperature and humidityTemperature 18 ~ 26 degrees, humidity 45 ~ 65%.1 / classPartially Prepared ProductsIn accordance with the internal standard workshop.1 / classLoad differenceIn accordance with the internal standard workshop. Bottle sealing quality2 / classIn accordance with the internal standard workshop.1 / classStrict qualification rateNot less than 96%.2 / classLabel qualityIn accordance with the internal standard workshop.2 / classPacking qualityIn accordance with the internal standard workshop.2 / classPacking qualityIn accordance with the internal standard workshop.2 / class。
生产过程监测与控制管理制度

生产过程监测与掌控管理制度1. 前言为保证企业在生产过程中的质量掌控和安全管理,确保产品的合规和高质量,订立本生产过程监测与掌控管理制度。
本制度适用于全部生产环节,并对生产过程中可能显现的问题进行监测与掌控,以减少质量缺陷和生产事故的发生。
2. 监测与掌控目标2.1 确保生产过程中各环节的合规和符合相关法律法规。
2.2 掌控生产过程中的关键参数,以保证产品的质量稳定。
2.3 及时发现和处理生产过程中的问题,以防止质量缺陷和生产事故的发生。
3. 生产过程监测与掌控的责任部门及岗位3.1 质量管理部门负责生产过程的监测和掌控工作。
3.2 生产部门负责生产过程的具体实施和监督。
3.3 监察部门负责对生产过程的监督和检查,并提出改进建议。
3.4 相关岗位负责依照本制度的要求进行工作。
4. 生产过程监测与掌控流程4.1 监测点的设定4.1.1 依据产品特性和生产工艺,确定生产过程中需要监测的关键环节和参数。
4.1.2 设定合理的监测点,确保能够及时、准确地取得相关数据。
4.1.3 对监测点的设定进行定期评估和更新,以适应生产工艺和质量要求的变动。
4.2 监测方法和工具的选择4.2.1 依据监测点的特点和要求,选择合适的监测方法和工具。
4.2.2 确保监测方法和工具的准确性和可靠性,并定期进行校准和维护。
4.2.3 对监测方法和工具进行记录,以备查证和分析使用。
4.3 数据手记与分析4.3.1 对监测点进行数据手记,确保数据的真实准确。
4.3.2 对手记到的数据进行分析,找出异常情况和潜在问题。
4.3.3 依据分析结果,及时采取措施,修正偏差和问题。
4.4 异常情况和问题的处理4.4.1 对于监测到的异常情况和问题,及时进行记录,并进行初步分析和推断。
4.4.2 依据记录和分析结果,订立相应的矫正和防备措施。
4.4.3 确保矫正和防备措施的执行和效果,并进行整改和改进。
4.5 监测与掌控结果的反馈和总结4.5.1 定期对生产过程的监测与掌控结果进行总结和分析。
监测质量控制管理制度

监测质量控制管理制度一、总则为了提高产品质量、保障用户利益,推动企业可持续发展,制订本管理制度。
二、适用范围本制度适用于公司生产、检验、质量控制等环节。
三、监测质量控制管理组织架构1. 质量监控中心质量监控中心是公司全面管理和质量控制的部门。
由质量监控中心主任负责,下设质检组、质管组等。
主要负责监测生产、检验质量,及时发现问题并解决。
2. 质检组由专业的质检人员组成,监测生产过程,保障产品的合格。
3. 质管组主要负责生产过程的质量控制。
监测原材料、生产设备、工艺流程等。
四、监测质量控制基本原则1. 严格执行相关法律法规,保证产品符合相关标准。
2. 采用先进的检验技术和设备,提高检验效率和准确度。
3. 加强员工素质教育,提高员工的责任感和质量意识。
4. 加强对供应商的质量管理和监控,保证原材料的质量。
五、监测质量控制管理流程1. 生产环节(1)生产计划生产部门根据订单,制定生产计划,包括生产数量、生产时间等。
并将生产计划提供给质量监控中心。
(2)生产过程监控质检组对生产过程进行监控,并在发现问题时及时反馈,同时提出改进方案。
(3)生产结束检验生产结束后,对产品进行检验,确认产品是否合格,符合要求后才可包装和入库。
2. 质量检验(1)原材料检验进货部门对原材料进行检验,确认原材料质量合格后方可入库使用。
(2)半成品检验生产过程中,对半成品进行抽检和检验,确保半成品质量符合要求。
(3)成品检验对最终成品进行检验,确认产品是否合格。
六、监测质量控制管理的技术手段1. 质量监测设备公司应配备先进的质量监测设备和仪器,确保检验工作的准确性。
2. 质量监测技术公司应加强对检验人员的培训,提高其检验技术水平。
3. 质量监测信息化公司应建立质量监测的信息化系统,确保质量数据的准确、及时性。
七、监测质量控制的管理手段1. 建立监测质量控制台账,对生产、检验的质量情况进行记录和分析。
2. 加强对员工的培训,提高员工的专业技能和质量意识。
生产过程关键控制点管理制度

生产过程关键控制点管理制度生产过程关键控制点管理制度1 目的为加强对质量控制点的管理,使所有控制的过程始终处于受控状态,以确保稳定地生产合格产品,特制定本制度。
2、适用范围适用于公司对主导产品实现的关键过程的质量控制。
3 职责3.1品控部负责生产过程关键控制点的管理,编制检验用作业指导书、质量控制点管理文件,并监督操作人员按作业指导书、工艺标准进行作业;3.2 各相关岗位负责编制本岗位作业指导书,本部门领导审批,由质量副总审阅签发;3.3生产车间负责按质量控制点文件的规定具体组织实施,工艺应执行研发中心下发的工艺文件;3.4参与质量控制点日常工作的人员主要有:操作者、质检员、机修员,其职责分工如下:操作者——熟练掌握操作技能和本工序质量控制方法;明确控制目标,正确测量,认真自检,自做标记并按规定填写原始记录;做好设备的维护保养和点检工作;发现工序异常,迅速向品控人员报告,请有关部门采取纠正措施。
质检员——按作业指导书对控制点进行重点检查,把检查结果及时报告操作者,并做好记录。
同时监督检查操作者是否遵守工艺纪律和工序控制要求,并向部门主管报告重要信息。
机修员——按规定定期对控制点设备进行检查和维护,督促检查设备点检活动,根据点检信息,及时对设备进行检修和调整,并做好设备维修记录。
4 工作程序4.1质量控制点的设定原则4.1.1工艺文件有特殊要求,对下道工序的加工、装配有重大影响的项目。
4.1.2内外部质量信息反馈中出现质量问题较多的薄弱环节。
4.2质量关键控制点内容4.2.1原材料检验关键点控制4.2.1.1原材料检验人员对每批次的原辅材料按“原材料验收标准”进行检验,控制方法:按抽样标准抽检,验证证件及验证检测值;4.2.1.2化验室人员对内包材每周抽查一次,控制标准:菌落总数<50个/瓶或盖;大肠菌群不得检出;4.2.2前处理车间关键点控制4.2.2.1生产用水24小时正反冲一次,过程监控人员每天检测一次水硬度及电导率,水硬度≤50mg/L,填写“软化水检验原始记录”;4.2.2.2 发酵奶制作过程要严格按照工艺执行,每锅次投料数量需由称料员复核并签字确认,过程质检抽查并签字;。
生产过程质量控制制度

生产过程质量控制制度生产过程质量控制制度是一套用于确保产品质量稳定和一致性的管理体系,它涵盖了从原材料采购到产品出货的全过程。
该制度的目标是通过标准化的流程和操作规范,最大程度地减少产品缺陷和质量问题,提高产品的可靠性和客户满意度。
一、质量控制组织架构为了有效实施生产过程质量控制制度,需要建立一个专门的质量控制组织架构。
该组织架构应包括质量部门、生产部门和相关部门的合作与协调。
质量部门负责制定和监督质量控制制度的执行,生产部门负责按照制度要求进行生产操作,相关部门提供必要的支持和配合。
二、质量控制流程1. 原材料采购控制:- 设定合格供应商名单,并定期对供应商进行评估和审核。
- 制定原材料采购标准和规范,确保原材料的质量符合要求。
- 对进货原材料进行抽样检验,确保其符合标准要求。
2. 生产过程控制:- 制定生产操作规范,明确每个工序的操作要求和质量控制点。
- 对生产设备进行定期维护和检修,确保其正常运行和准确度。
- 对生产过程中的关键参数进行监控和记录,及时发现并纠正异常情况。
3. 产品检验控制:- 制定产品检验标准和方法,确保产品的质量符合要求。
- 对生产出的产品进行抽样检验,检验项目包括外观、尺寸、性能等。
- 对不合格产品进行分类和处理,确保不合格品不流入市场。
4. 过程改进和持续改进:- 对生产过程中出现的问题进行分析和处理,找出根本原因并采取相应的纠正措施。
- 定期进行质量管理评审,对制度执行情况进行评估和改进。
三、质量控制记录和数据分析为了监控和评估质量控制制度的有效性,需要建立相应的记录和数据分析系统。
1. 建立质量控制记录表,记录每个环节的操作和检验结果,确保数据的真实可靠。
2. 对记录的数据进行统计和分析,发现潜在问题和趋势,及时采取措施进行改进。
3. 建立质量控制指标体系,设定合理的目标和要求,通过数据分析评估绩效和改进效果。
四、员工培训和意识提升为了确保质量控制制度的有效实施,需要对员工进行培训和意识提升。
生产过程质量监控管理规程

1、目的:制定生产过程质量监控管理规程,确保生产全过程严格按工艺规程执行。
2、范围:适用于生产过程质量监控的管理。
3、职责:质量授权人、质量部部长、生产负责人、生产管理人员、QA对本规程的实施负责。
4、内容:4.1 生产过程质量监控是生产质量管理的基础工作,是生产现场工作的重要组成部分,由现场QA按本规程的要求进行工作。
4.2监控依据:相应工艺规程中的质量监控要点,工艺参数。
4.3监控要求:4.3.1现场QA 每班按生产过程质量监控要点及监控频次对每批产品每个工序进行监控检查并记录。
4.3.2生产操作人员负有对产品质量的自我监督责任,并应服从检查和按指令整改。
4.3.3生产工艺员负有指导整改和监督整改的责任。
4.3.4生产过程中经现场QA 检查不符合规定要求或标准时,现场QA应立即指令整改并发“限期指令整改通知单”。
4.3.5发现问题操作人员应立即按指令整改,必要时按《生产过程偏差处理管理规程》处理。
4.4监控内容:4.4.1生产操作前检查4.4.1.1 生产区:干净、整洁,无与本批次生产无关的物料、记录和杂物;有《清场合格证》且在清场有效期内。
4.4.1.2 生产区设备:已清洁,有明显状态标志,并在清洁有效期内。
4.4.1.3 容器、器具:已清洁,有状态标志,并在清洁有效期内。
4.4.1.4 操作人员:工作服洁净整齐、个人卫生符合要求。
4.4.1.5 物料标示清楚,与生产指令一致,有质量部检验合格报告书或合格证。
4.4.1.6 计量器具:有校验合格证,并在使用期内。
4.4.1.7 操作间温湿度、压差符合生产要求。
4.4.2 生产操作检查4.4.2.1 操作过程执行批准的工艺规程及岗位操作规程。
4.4.2.2 对现场样品抽样检查,符合规定标准。
4.4.3 生产结束清场,QA检查清场情况,符合规定要求的发放《清场合格证》。
4.5监控记录4.5.1前处理工序的质量监控按生产班次记录,因各岗位加工的物料不相同,每班的现场QA 记录当班的生产质量情况。
生产过程质量控制制度

生产过程质量控制制度
标题:生产过程质量控制制度
引言概述:生产过程质量控制制度是企业为保证产品质量,提高生产效率而制
定的一套规范和流程。
建立健全的生产过程质量控制制度对于企业的发展至关重要,可以有效降低生产过程中的质量风险,提高产品的合格率和客户满意度。
一、设立质量控制部门
1.1 确定质量控制部门的职责和权责
1.2 配备专业的质量控制人员
1.3 制定质量控制部门的工作流程和标准
二、建立质量控制流程
2.1 制定生产过程质量控制的具体流程和方法
2.2 定期对生产过程进行质量检查和监控
2.3 设立质量异常处理机制,及时处理生产过程中出现的质量问题
三、制定质量标准和指标
3.1 确定产品的质量标准和指标
3.2 制定生产过程中各个环节的质量指标
3.3 定期评估和调整质量标准和指标,确保其符合市场需求和客户要求
四、培训员工
4.1 开展质量控制相关的培训和教育
4.2 提高员工对质量控制的重视和意识
4.3 建立员工质量控制意识的考核机制,激励员工积极参与质量控制工作
五、引入先进技术和设备
5.1 更新生产设备,提高生产效率和质量
5.2 引入先进的质量控制技术和方法
5.3 不断改进和优化生产过程,提高产品质量和企业竞争力
综上所述,建立健全的生产过程质量控制制度是企业发展的基础,只有不断完善和执行这套制度,企业才能在激烈的市场竞争中立于不败之地,赢得客户的信任和认可。
生产过程质量控制制度不仅是企业的管理体系,更是企业的竞争力和发展动力。
生产与质量监控制度

生产与质量监掌控度1. 目的与范围本规章制度的目的是确保公司的生产过程和产品质量符合相关法规、标准和客户需求,以提高生产效率、降低本钱、保障产品质量和满足客户需求。
本制度适用于我公司全部生产线及生产相关部门,并适用于全部员工、合作伙伴和供应商。
2. 质量管理体系2.1 公司将建立完善的质量管理体系,并对其进行日常监控和连续改进。
2.2 质量管理体系包含但不限于以下内容:2.2.1 质量策划•订立质量目标和计划,明确质量要求和目标,确保在生产过程中实现可控的质量水平。
2.2.2 质量掌控•建立完善的质量掌控程序,包含原材料子、生产过程和最终产品的检验,确保产品符合规定的质量标准和客户需求。
•建立质量检验点和质量检验标准,针对紧要环节和关键工序进行全面检验,及时发现和矫正问题,防止不良品流入市场。
2.2.3 质量改进•建立质量改进机制,收集客户反馈和内部看法,对产品和生产过程进行分析和改进,以提高产品质量和生产效率。
•鼓舞员工供应改进建议,并对其进行评估和嘉奖,以促进全员参加质量管理和改进。
2.3 公司将连续开展培训和教育,提高员工的质量意识、技能和责任心,在全员范围内强化质量管理。
3. 生产过程管理3.1 生产计划和排程•依据市场需求和客户订单,订立认真的生产计划和排程,确保生产布置合理、配套齐全。
•每个部门和岗位负责人要依照生产计划和排程,合理布置生产任务,保证产品定时交付。
3.2 设备和工具管理•建立设备和工具管理制度,包含设备台账、巡检和保养记录等,确保设备和工具的正常运行和维护。
•针对关键设备和工具,订立维护计划和备件储备,以防备和应对可能的故障和维护和修理需求。
3.3 原材料子和零部件管理•建立原材料子和零部件供应商评估制度,确保选择优质供应商和合格的原材料子和零部件。
•建立原材料子和零部件进货检验制度,对每批次原材料子和零部件进行检验,确保其符合质量要求。
3.4 生产记录与分析•建立完整的生产记录和数据分析系统,包含生产过程记录、产品质量数据、异常情况记录等。
5-生产过程关键控制点监控制度
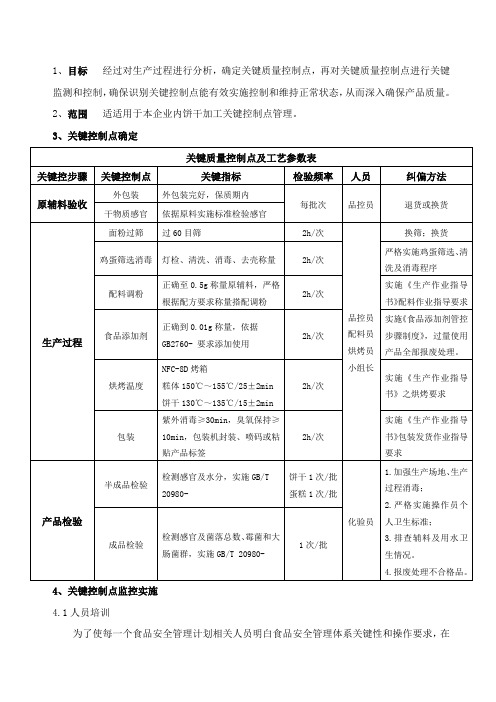
1、目标经过对生产过程进行分析,确定关键质量控制点,再对关键质量控制点进行关键监测和控制,确保识别关键控制点能有效实施控制和维持正常状态,从而深入确保产品质量。
2、范围适适用于本企业内饼干加工关键控制点管理。
3、关键控制点确定
4、关键控制点监控实施
4.1人员培训
为了使每一个食品安全管理计划相关人员明白食品安全管理体系关键性和操作要求,在
实施之前应对各部门人员进行食品安全管理计划中相关控制点培训。
4.2现场操作
实施现场要确保效果,应提供必需资源(如合格原料、测试仪器、SOP、统计)以表现工作内容是符合食品安全管理计划要求,而且现场人员工作应按食品安全管理计划要求展开,并将工作中控制活动作好统计。
4.3监督检验
关键控制点负责操作员生产前和生产过程中认真严谨开展自查,品控部安排现场品控员定时、不定时检验各关键控制点,发觉问题立即纠错,并做好相关统计归档。
4.4纠错处理
在日常监控和体系活动中发觉异常情况,应按纠偏方法程序进行处理。
5、相关文件
《饼干加工工艺步骤图及工艺规程》、《饼干生产作业指导书》。
6、相关统计
《进货查验台账》、《原材验收汇报》、《出厂检验统计》、《出厂检验汇报》、《关键质量控制点(CCP)控制统计》、《烘烤统计》、《食品添加剂发放使用统计》、《车间清洁消毒统计表》、《个人卫生健康晨检统计表》、《生产车间卫生安全检验表》、《成品留样统计》、《设备、设施清洗消毒统计》。
重庆卡顿尔食品
2月1日。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生产过程质量控制点监测管理制度2007-6-16 0:00:00 中国兽药114网信风浏览:2001公司GMP管理文件题目生产过程质量控制点监测管理制度编码:SMP-SC-0160-00共7页制定审核批准制定日期审核日期批准日期颁发部门办公室颁发数量生效日期分发单位办公室、生产技术部、质量部、物资供应部、工程部一、目的:制定生产过程重要质量控制点监测管理制度,确保产品在各个生产环节质量得到严格控制。
二、适用范围:适用于生产技术部生产过程的质量监控。
三、责任者:生产技术部经理、QA检查员。
四、正文:为了确保产品的质量,必须对生产过程的质量进行监控,生产过程质量控制点及其监督管理制度如下:1最终灭菌小容量注射剂2.1纯化水、注射用水:澄明度必须符合标准2.2 安瓿的洗涤及干燥灭菌:在准备室脱去外包装送入粗洗室粗洗,后送入精洗室洗涤,外壁应冲洗,内壁至少用纯化水洗两次,最后经过0.45μm滤膜滤过的澄明度合格的注射用水洗净,干燥、灭菌、冷却,灭菌后的安瓿应立即使用或清洁存放贮存不得超过2天,洗涤后的瓶子应进行清洁度及澄明度检查。
1.3称量:称量前应核对原辅料品名、批号、生产厂家、规格,应与检验报告单相符。
调换原辅料供应商时应有小样试验合格单或已经过验证的报告;称量时必须有复核人,操作人和复核人均应在原始记录上签名。
1.4 配制:配制罐必须标明配制液的品名、规格、批号和配制量,投料时必须有人复核及做记录。
1.5 粗滤及精滤:药液经含量、PH值检验合格后方可精滤,盛装容器应封闭,标明药液的品种、规格、批号。
药液配制至灭菌一般应在24小时内完成。
1.6 灌封:灌装管道、针头使用前用注射用水洗净并煮沸灭菌,直接与药液接触的惰性气体、压缩空气,使用前净化处理,其纯度及所含微粒量应符合规定,灌装量按有关规定灌装。
及时抽取少量半成品检查澄明度、装量、封口等质量状况,半成品盛器内应标明产品名称、规格、批号、日期、灌封机号及顺序号,操作者姓名。
1.7灭菌:双扉式灭菌柜,产品灭菌前,要核对品名、批号、数量,按规定的灭菌标准操作程序操作,灭菌时应及时做好记录,并密切注意温度、压力、时间,如有异常情况应及时处理。
灭菌后进行检漏,检漏的真空度在-8kpa。
1.8 灯检:检查员视力在0.9以上,视力每年检查一次,检查后的半成品要注明检查者的姓名,由专人抽查。
不合格品及时分类记录,标明品名、规格、代号、批号,置于盛器内移交专人处理。
1.9印字包装:操作前应校对半成品的名称、规格、批号及数量是否与领用的包装材料一致。
印字、包装、装箱过程中应随时检查品名、规格、批号,包装结束后统计好包装材料的实用数、损坏及剩余数与领用数做物料平衡检查,结束后送待检区待检,检验合格后入库。
2 口服液2.1配置与过滤2.1.1配置过程中所涉及设备、容器、管道、过滤板框在使用前均用热水清洗干净。
2.1.2口服剂配置药液应在4~5小时内完成,主要是指根据生产计划而进行的连续作业。
2.1.3配置好的药液应及时过滤至稀配罐中。
2.2灌封2.2.1灌封过程当中所涉及的灌装设备、容器、内瓶、储料罐、管道在使用前用热水清洗干净。
2.2.2按灌装岗位操作规程连续操作,口服剂的灌封应在8小时内完成。
2.2.3灭菌操作人员进入工作间之前应开启紫外灯照射灭菌。
口服剂配制药液在配制过程中煮沸保温30分钟灭菌。
3粉散剂3.1称量、配料:3.1.1称量前的原辅料或中间产品,须清洁或除去外包装,必须认真校对物料名称、规格、批号,应与检验报告单、合格证相符。
3.1.2处方计算、称量及投料必须复核,操作者及复核者均应在记录上签名。
3.1.3配好的批次的原辅料装于容器中,并附上标志,注明品名、批号、规格、数量、称量人、日期。
3.2 混合:3.2.1混合前先核对物料的品名、批号、数量等,确认无误后再进行下一步操作。
3.2.2量一般不超过该机总容量的2/3。
3.2.3混合具有均一性的物料为一个批量,编为一个批号。
3.3包装工序:3.3.1包装前的准备:3.3.1.1开始前包装区的检查:检查生产区内有无与该批生产无关的物品。
3.3.1.2在同一包装室内不应同时处理不同批的产品。
3.3.1.3产品和包装材料的接收:对照批生产记录检查、核对包装材料和产品的代号、批号、品名及数量。
3.3.1.4批号及有效期印字的检查:在手工或机器打印批号、生产日期、有效期的过程中,应对照本批记录表认真检查纸箱、内包装袋、标签、检验合格证上印字是否符合要求。
3.3.2包装作业:3.3.2.1开始时的检查:第一张套印上批号、生产日期、有效期的标签以及合格证应附在批文件上,同时说明书等印刷包装材料也应被取样并归入批档案中。
3.3.2.2对照批生产记录检查第一包装单元,是否使用了应该使用的包装材料,包装上是否有缺陷。
3.3.2.3检查批号、生产日期和有效期的印刷是否正确,字迹是否清楚。
3.3.3包装过程:包装过程应将药品与外包装箱、说明书进行核对无误后,方可进行包装作业。
3.3.4文件归档:——中间控制记录填写正确无遗漏;——印刷包装材料样品已齐全正确无误。
批文件最后必须送交质量部。
3.3.5清场:生产现场在换批号和更换品种、规格时,应按清场管理要求进行清场。
QA验收清场合格后应挂标示牌。
4消毒剂4.1称量:称量前应核对原辅料品名、批号、生产厂家、规格,应与检验报告单相符。
调换原辅料供应商时应有小样试验合格单或已经过验证的报告;称量时必须有复核人,操作人和复核人均应在原始记录上签名。
4.2配制:配制罐必须标明配制液的品名、规格、批号和配制量,投料时必须有人复核及做记录。
4.3灌装:灌装量按有关规定灌装。
及时抽取少量半成品检查澄明度、装量、封口等质量状况,半成品盛器内应标明产品名称、规格、批号、日期、灌封机号及顺序号,操作者姓名。
4.4印字包装:操作前应校对半成品的名称、规格、批号及数量是否与领用的包装材料一致。
印字、包装、装箱过程中应随时检查品名、规格、批号,包装结束后统计好包装材料的实用数、损坏及剩余数与领用数做物料平衡检查,结束后送待检区待检,检验合格后入库。
5各剂型质量控制要点见附表。
6工序管理:6.1工序质量管理由公司质量部负责管理。
工序质量管理的对象是使生产过程中构成工序质量的要素,即人、设备、物料、工艺方法及环境等五个方面均处于控制状态,为此分析找出其中主导要素。
对影响工序质量的主导要素,提出管理控制方法并加以实施。
6.2管理内容与要求:6.2.1管理内容:6.2.1.1 决定管理项目即质量、成本、数量、安全、设备和人等。
6.2.1.2 决定管理目标及其控制点。
6.2.1.3 决定达到目标的方法并进行制度化。
6.2.1.4 确定设备、检验器具。
6.2.1.5 确定操作方法、环境及其程序。
6.2.1.6 确定物料的质量要求。
6.2.1.7 确定计量、检验、考核、试验等方法,以及工序质量审核和产品检验方法6.2.1.8 决定检验及评价方法。
6.2.1.9 决定处理方法。
6..2.2管理要求:6.2.2.1工序质量管理由质量部组织有关部门共同进行,以保证质量管理工作的质量。
6.2.2.2工序质量管理工作经常进行活动,计划和方案报公司主管领导批准后实施。
6.2.3检查:6.2.3.1检查各部门有无工序质量管理制度、原始记录、检查结果及措施。
6.2.3.2检查措施实施情况。
7 附表:7.1最终灭菌小容量注射剂质量控制要点工序质量控制点质量控制项目频次制水纯化水电导率1次/2h《中国兽药典》全项1次/周注射用水电导率、pH、氯化物、胺盐、澄明度1次/2h《中国兽药典》全项1次/周洗瓶原包装安瓿检验报告单、清洁度1次/2h隧道烘箱温度1次/2h洗净后安瓿清洁度配制药液批号划分与编制、主药含量、pH、澄明度、色泽、过滤器材的检查(如其泡点等) 1次/2h灌封烘干的安瓿清洁度1次/2h药液色泽1次/2h澄明度1次/2h封口长度、外观1次/2h灌封后半成品药液装量、澄明度1次/2h灭菌灭菌柜标记、装量、温度、时间、记录、真空度1次/2h灭菌前后半成品外观清洁度、标记、存放区1次/2h灯检灯检品抽查澄明度1次/2h每盘标记、灯检者代号、存放区1次/2h在包装品每盘标记、灯检者代号1次/2h印字批号、内容、字迹1次/2h装盒数量、说明书、标签1次/2h标签内容、数量、使用记录1次/2h装箱数量、装箱单、印刷内容、装箱者代号 1次/2h7.2口服液质量控制要点工序质量控制项目检查频次洗瓶、胶塞装瓶水澄明度符合要求。
2次/班装水控制装水要满。
精洗水澄明度符合要求。
温度121±2℃。
时间30分钟。
压力0.1 Mpa±0.02。
配制纯化水水质符合标准。
2次/班滤材初滤:钛棒。
滤材精滤:0.45μm微孔滤器。
滤材滤器完整性符合要求温度18-26℃。
湿度30-65%。
静压差不小于5Pa。
配制药液体积配制量准确。
7.3 粉散剂质量控制要点工序质量控制点质量监控项目频次配料混合称量准确性每批混合均匀度每批水分每批内包分装量药品装量随时/班封口封口紧密度、外观随时/班外包标签内容、数量、使用记录每批中包中包内装的小包数随时/班装箱数量、装箱单、印刷内容每箱7.4消毒剂质量控制要点工序控制点质量控制项目频次瓶塑料瓶1.符合标准。
2.洁净度符合要求。
2次/班配液岗位饮用水澄明度符合标准。
2次/班PH值符合标准。
2次/班含量第一节生产过程中品质控制流程符合标准。
1次/班灌装室室内温湿度温度18~26℃,湿度45~65%。
1次/班半成品符合车间内控标准。
1次/班装量差异符合车间内控标准。
2次/班瓶封口质量符合车间内控标准。
1次/班严密度合格率不小于96%。
2次/班贴签质量符合车间内控标准。
2次/班装盒质量符合车间内控标准。
2次/班装箱质量符合车间内控标准。
2次/班页脚内容11。
