压力蒸汽灭菌器风险评估报告
WF32-0.4卧式矩形压力蒸汽灭菌器风险评估

WF32-0.4卧式矩形压力蒸汽灭菌器风险评估
YXQ-WF32-0.4卧式矩形压力蒸汽灭菌器
风险评估
一、概述:
对公司设备灭菌器风险分析,安装于前处理提取净化车间,用于物料清洁及成品干燥、灭菌操作。
二、评估目的:
对灭菌器可能因在设计、安装、运行、性能等方面可能存在的缺陷项进行风险评估;并由此制定经过验证或确认的风险控制措施。
从而彻底消除或避免降低灭菌器可能存在的缺陷项给产品质量、生产环境、人员健康、公共安全等带来的风险隐患。
三、风险评估
应用失败模式影响分析(FMEA)对风险进行评估
风险的严重程度(S)
风险发生概率(P)
可检测性(D)
风险评价准则:RPN(风险优先系数)计算:RPN = S×P×D
●高风险水平:RPN≥ 9。
此为不可接受风险。
必须尽快采用控制措施,通过提高可检测性及/或降低风险产生的可能性来降低最终风险水平。
验证应首先集中于确认已采用控制措施且持续执行。
●中等风险水平:RPN=6-8。
此风险要求采用控制措施,通过提高可检测性及/或降低风险产生的可能性来降低最终风险水平。
所采用的措施可以是规程或技术措施,但均应经过验证。
●低风险水平:RPN<6。
此风险水平为可接受,无需采用额外的控制措施
五、风险评估
我们对灭菌器可能存在的质量风险分别进行评估。
详细内容见以
下质量风险评估记录。
风险评估记录。
压力蒸汽灭菌效果监测结果分析

压力蒸汽灭菌效果监测结果分析摘要:目的:了解血站压力蒸汽灭菌质量状况,探讨影响灭菌效果的因素,以便有效控制血液污染。
方法:通过现场调查与采样检测方法,连续5年对玉溪市中心血站压力蒸汽灭菌效果进行化学和生物监测。
结果:2011~2015年共采样监测样品1715份,灭菌效果总合格率为99.65%。
3M指示胶带全部达到变色标准。
2例化学指示卡变色不均。
生物指示剂有4例培养有细菌生长。
结论:玉溪市中心血站压力蒸汽灭菌质量总体较好,但针对不足需要常抓不懈,完善灭菌操作规范,切实有效做好监督工作。
关键词:灭菌效果;监测;化学指示剂;生物指示剂压力蒸汽灭菌是最常用,杀菌效果最可靠的灭菌方法之一。
在血站系统有着举足轻重的作用,是预防血液污染的重要措施之一,也是向临床提供安全、可靠、高质量血液的首要环节。
由于影响灭菌效果的因素较多,需要按要求进行定期监测;发现问题,认真分析产生原因,及时纠正整改,以保证灭菌效果安全可靠。
现将玉溪市中心血站2011年~2015年连续监测情况报告如下:1 材料与方法1.1 材料美国3M公司3M压力蒸汽灭菌指示胶带;山东新华医疗器械股份有限公司新华牌压力蒸汽灭菌化学指示卡;美国3MTM压力蒸汽灭菌生物培养指示剂,其指示菌为嗜热脂肪杆菌芽孢(ATCC7953,芽孢含量:5*105~5*106);以上监测用指示剂经国家批准,出厂检验合格,并在效期内使用。
1.2 方法及监测标准1.2.1 3M指示胶带:将指示胶带粘贴于每一待灭菌物品包外,经过灭菌后观察其颜色的改变,以指示是否经过灭菌处理。
1.2.2 化学指示卡:可以指示灭菌温度和持续作用时间,以间接指示灭菌效果,将指示卡放于待灭菌包内,每次灭菌都要使用,每包必放,经灭菌后,取出指示卡,根据颜色及性状的改变判断是否达到灭菌条件。
1.2.3 生物指示剂:是利用嗜热脂肪杆菌芽孢的活菌对灭菌效能进行监测。
根据其微生物的死亡情况判断灭菌是否成功。
将2支生物指示剂管置于待灭菌包中心部位,经过灭菌后将生物指示剂取出,盖朝上垂直于手中,用一夹子夹住菌管下部将管内安瓿夹碎,让培养液流出浸没菌片。
3、压力蒸汽灭菌锅风险评估报告
1. 概述YXQ-LS-100A 型全自动立式压力蒸汽灭菌器是本公司质量部QC 室用于原 辅料、中间产品、成品微生物限度、无菌检查实验的灭菌设备。
本设备主要由外壳、灭菌器桶、灭菌网篮组成,装有泄压装置安全阀、双刻度压力表、微型热敏打印机。
应对该设备的性能及使用过程进行风险评估,确定该设备在使用过程中可能存在的风险点,并针对风险点采取相应的控制措施,然后通过设备确认的方式确定性能标准,以保证检验过程可靠,检验结果真实反映物料本身属性。
2. 范围YXQ-LS-100A 型全自动立式压力蒸汽灭菌器质量风险评估。
3. 风险评估小组及职责 3.1. 风险评估小组成员3.2. 风险评估小组职责4. 风险评估标准小组职务 姓名 所在部门 工作职务 组长 质量部 QC 主管 组员 质量部 QC 组员 质量部 QC 组员 质量部 QA 主管 组员质量部工程部经理部门 职责风险管理 委员会主任负责质量风险评估分小组上报的质量风险评估项目进行全面的分析、评估审核,对建议措施的批准。
组长风险管理提供适当的资源,对风险管理工作负领导责任。
负责组建风险评估小组,风险评估报告的批准。
保证风险管理实施和评定,组织风险评估小组成员对风险评估记录和风险评估报告的审核,监督风险事件采取预防和纠正措施的执行。
组员负责分析所有已知的和可预见的危害信息的收集,并用失败模式影响分析(FMEA )进行YXQ-LS-100A 型全自动立式压力蒸汽灭菌器质量风险评估和风险控制,必要时各组员应进行风险沟通,并对其正确性和有效性负责。
负责制定降低风险预防和纠正措施,风险发生部门负责人负责预防和纠正措施的实施。
风险评估报告的整理,风险评估相应记录的归档。
本次质量风险评估使用失败模式影响分析(FMEA)工具,识别潜在的失败模式,对风险的严重程度、发生可能性和可检测性评分,采用4分制原则进行评估。
4.1.严重程度(S):测定风险的潜在后果,主要针对可能危害产品质量、病患健康及数据完整性的影响。
压力蒸汽灭菌器验证报告
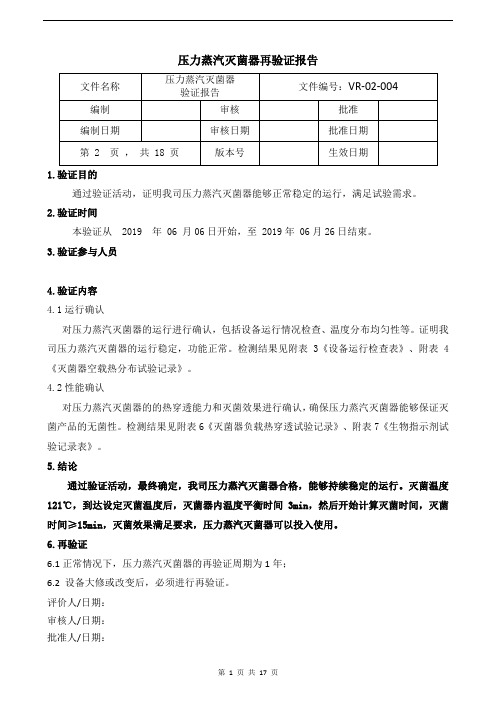
压力蒸汽灭菌器再验证报告1.验证目的通过验证活动,证明我司压力蒸汽灭菌器能够正常稳定的运行,满足试验需求。
2.验证时间本验证从 2019 年 06 月06日开始,至 2019年 06月26日结束。
3.验证参与人员4.验证内容4.1运行确认对压力蒸汽灭菌器的运行进行确认,包括设备运行情况检查、温度分布均匀性等。
证明我司压力蒸汽灭菌器的运行稳定,功能正常。
检测结果见附表3《设备运行检查表》、附表4《灭菌器空载热分布试验记录》。
4.2性能确认对压力蒸汽灭菌器的的热穿透能力和灭菌效果进行确认,确保压力蒸汽灭菌器能够保证灭菌产品的无菌性。
检测结果见附表6《灭菌器负载热穿透试验记录》、附表7《生物指示剂试验记录表》。
5.结论通过验证活动,最终确定,我司压力蒸汽灭菌器合格,能够持续稳定的运行。
灭菌温度121℃,到达设定灭菌温度后,灭菌器内温度平衡时间3min,然后开始计算灭菌时间,灭菌时间≥15min,灭菌效果满足要求,压力蒸汽灭菌器可以投入使用。
6.再验证6.1正常情况下,压力蒸汽灭菌器的再验证周期为1年;6.2 设备大修或改变后,必须进行再验证。
评价人/日期:审核人/日期:批准人/日期:附表1培训记录表培训主办人:附表2校验记录表检查人/日期:复核人/日期:第4页共17页设备运行检查表检查人/日期:复核人/日期:灭菌器空载热分布试验记录(第一次)运行确认评价表灭菌器负载热穿透试验记录(第一次)附表7生物指示剂试验记录表附表8性能确认评价表附表9验证效果评价表。
压力蒸汽灭菌器风险评估报告

人员 操作
人员卫生
洁净区要求洁净度高,人员及工作服带来的污染
中
清洁操作
未严格执行操作规程,因此清洁不彻底,造成污染
中
生产过程
因设备摆放位置的更改,缺乏实际操作而造成清洁或生产操作 不符合规定
中
清洗残留
残留限度设定不合理,不能有效消减残留风险
高
环境 安全
使用安全
使用后,待压力表显示为“零”后才能开门,否则造成事故
中
拆卸、安装
拆卸和安装过程中直接接触药液的部件被污染,不易清洗
中
仪器仪表
重新安装后未校验或校验失败,因此计数不准确
中
公用介质
电:停电时应提前通知,以免造成损失(药品、设备)
中
公共介质
蒸汽:蒸汽不稳时,操作难度加大
中
使用年限
设备已使用过一段时间,设备使用过程中,损坏的几率增加,
易对生产造成中途停止的结果
4
拆卸、安装过程中部件
被污染
2
1整体移动, 不进行拆卸, 避免 损坏设备部件
1
8
低
仪器仪表
校验失败或未校 验
压力表、温度表、真空表计数 不准确或不能代表
4
重新安装后未校验或校
验失败
2
1安装后进行校验
2及时粘贴检定标签
3生产前检查
1
8
低
动力:电
突然停电设备受
损害
停电时没有及时通知,造成损
失(药品、设备)
蒸汽控制不当
蒸汽安全阀损坏未及时发现致 使蒸汽压力过高,发生危险的 可能性高;过低,不能设备正 常运行
4
蒸汽安全阀损坏未及时 发现致使蒸汽压力过 高;
压力蒸汽灭菌锅风险评估报告

压力蒸汽灭菌锅风险评估报告首先,压力蒸汽灭菌锅的高温和高压环境可能导致设备内部的爆炸。
在使用过程中,如果发生锅体不耐压、密封不严或过高的压力等问题,就会增加火灾和爆炸的风险。
为了降低这一风险,应确保设备的质量可靠,定期进行维护和检修,并严格按照操作规程进行操作。
其次,压力蒸汽灭菌锅内部的高温和高压环境也会对操作人员造成烫伤和其他伤害。
在打开锅盖或者接触设备内部时,操作人员容易接触到高温的蒸汽和物体,从而导致烫伤。
此外,高压环境下,设备的突然开门也可能导致物体被喷出,造成伤害。
因此,在使用压力蒸汽灭菌锅时,操作人员应佩戴防护手套、面罩等个人防护装备,同时遵守操作规程,确保安全操作。
此外,压力蒸汽灭菌锅也存在机械故障和设备损坏的风险。
设备在长时间高温和高压的工作环境下,易出现机械故障或损坏,从而影响其正常工作。
为了减少这一风险,应定期检查设备的运行情况,及时发现和修复潜在的机械故障;此外,还应确保设备的质量可靠,采取可行的预防措施,减少设备的损坏。
最后,压力蒸汽灭菌锅的使用也存在操作不当导致杀菌效果不达标的风险。
在使用过程中,如果操作人员不按照规程进行操作,如设置不正确的温度和时间,未进行适当的负载测试等,就容易导致菌落未达到消灭要求,从而影响杀菌效果。
为了减少这一风险,操作人员应接受专业培训,了解设备的正确操作方法,并严格按照规程进行操作。
综上所述,压力蒸汽灭菌锅使用风险评估报告需要考虑设备的爆炸、操作人员的烫伤和伤害、机械故障和设备损坏以及操作不当导致杀菌效果不达标等风险。
只有通过对这些风险进行评估和预防控制,才能确保压力蒸汽灭菌锅的安全使用,为用户提供可靠的灭菌服务。
压力蒸汽消毒器验证报告

压力蒸汽消毒器验证报告目录一、概述二、目的三、安装确认3.1 资料档案3.2 检查原件说明书及维修手册3.3 检查仪器的规格标准3.4 检查安装是否恰当3.5 建立使用日记3.6 维修服务3.7 技术特性四功能性试验4.1 目的4.2 仪表校正4.3 消毒功能测试4.4 计算4.5 结论五、再确认5.1 线路连接5.2 附件5.3 清洁5.4 检查六、评价和建议七、批准一、概述组成细胞的蛋白质分子的功能取决于它的特殊结构,在一定高温条件下受热时,蛋白质间分子内氢键发生断裂影响了分子空间构型的重排,从而导致微生物的死亡。
对这一课题进行的大量研究表明,细菌孢子,尤其是芽孢杆菌和梭状芽孢具有耐热性。
耐热孢子的破坏取决于在湿热条件下孢子的水合作用以及核酸及蛋白质的变性。
因此,蒸汽灭菌中使用饱和蒸汽是至关重要的。
压力蒸汽消毒器是利用压力饱和蒸汽对物品进行迅速而有效的消毒灭菌设备。
适用于医院、药厂或科研部门等单位,对医疗器械、敷料、玻璃器皿、溶液、培养基等进行消毒、灭菌。
验证小组成员:涂泽求、卜振军、杨静、周林彬二、目的为了保证对玻璃器皿、培养基等所进行的消毒灭菌达到规定(F0≥8),消毒器的确认是无菌验证的基础,因此对此仪器进行验证。
三、安装确认3.1 资料档案仪器的名称:手提式压力蒸汽消毒器型号:YX——280B生产厂商:江苏省江阴市医疗设备厂进厂日期:2001年6月公司内部设备编号:1-21-00安放地点:三楼化验室3.2 检查使用说明书、维修保养手册、备件清单等。
检查结果:使用说明书保存完好。
存放处质管部文档室检查人杨静复核人周林彬日期2002 年7月 6 日3.3 检查安放是否恰当,符合要求。
检查结果:本仪器安放在微生物室,符合要求。
检查人杨静复核人周林彬日期2002 年7月6日3.4 已制定使用规程和维修保养制度,建立使用日记和维修记录。
3.5 维修服务:维修服务单位:江苏省江阴市医疗设备厂电话:0510--6286534联系人:杜建龙3.6 安装确认总结论:符合本公司GMP及供应商提议的要求。
压力蒸汽灭菌锅风险评估报告

7.结论:
本次风险评估主要高风险点存在于上述4项内容,分别采取了相应控制措施,使各风险RPN值降低到≤7,保证质量风险在可控范围内。
通过对YXQ-LS-100A型全自动立式压力蒸汽灭菌器质量风险分析,风险点主要发生在文件、人员、设备运行和性能方面,风险管理小组经过对该设备进行前瞻性评估,以及检查风险管理的方式对风险管理过程的评审,认为:
1、风险管理已适当的实施;
2、通过相应的确认、验证活动可以保证质量风险的可控;
3、综合剩余风险是可接受的;
4、确保全部剩余风险处于风险可接受准则的可接受范围内,且受益超过风险。
同意批准进行YXQ-LS-100A型全自动立式压力蒸汽灭菌器确认。
风险管理委员会主任:
日期:。
立式压力蒸汽灭菌器效果验证报告

验证小组人员名单目录序号项目名称页码1目的 (5)2验证类别 (5)3验证时间 (5)4验证依据 (5)5验证内容 (5)6接受标准 (5)7验证的实施步骤 (5)8偏差及异常处理 (9)9验证报告、结果分析和结论 (9)10验证结论批准、会签及日期 (9)11验证证书 (10)摘要公司对立式高压蒸汽灭菌器121℃高压灭菌30分钟的灭菌效果进行了验证,为确认立式压力蒸汽灭菌器的可靠性,确保微生物学检验及环境监测数据的真实可靠。
验证结果如下:当加入未灭菌枯草杆菌黑色变种芽胞菌片的培养肉汤经培养后显混浊,而在115℃灭菌20分钟后的枯草杆菌黑色变种芽胞菌片的培养肉汤经培养后清亮,无混浊,说明枯草杆菌黑色变种芽胞菌全部被灭活。
当未灭菌的嗜热脂肪芽孢杆菌生物指剂经培养后由紫色变为黄色,而在121℃压力蒸汽灭菌20分钟后的仍为紫色时,说明嗜热脂肪芽孢杆菌全部被灭活。
枯草芽孢杆菌、大肠杆菌、沙门菌、铜绿假单孢菌、金黄色葡萄球菌培养在121℃灭菌30分钟后,经培养无菌生长,细菌挑战性试验合格。
1 目的:提供足够的数据和文件依据,确认立式压力蒸汽灭菌器的可靠性,确保微生物学检验及环境监测数据的真实可靠。
2 验证类别:同步验证3 验证时间:2011年12月4 验证依据:《药品生产质量管理规范》(2010年修订);《药品生产验证指南》(2003年修订);《验证管理规定》SMP-10002-035.验证可接受标准6.1 试验条件6.1.1 检测用仪表确认7.1.3 菌培养物制备:分别取枯草芽孢杆菌、大肠埃希菌、沙门菌、铜绿假单孢菌、金黄色葡萄球菌1白金耳于装有9ml营养肉汤培养基的试管中,于30~35℃培养18~24小时后,出现浑浊,说明各种菌均有生长,即得枯草芽孢杆菌、大肠埃希菌、沙门菌、铜绿假单孢菌、金黄色葡萄球菌的培养物,备用。
7.2 取样方法:7.2.1 取样点:立式压力蒸汽灭菌器内上、中、下三部位各取样点(见物品放置图)物品放置图7.2.2 取样频次:每个试验进行三次。
不锈钢立式压力蒸汽灭菌器验证方案及报告

不锈钢立式压力蒸汽灭菌器验证方案及报告一、方案背景咱们得明确一下方案背景。
这款不锈钢立式压力蒸汽灭菌器,是我国医疗行业常用的一种灭菌设备。
它采用高温高压的蒸汽对物品进行灭菌,具有快速、高效、安全等特点。
那么,我们的任务就是验证它的灭菌效果,确保它能在实际应用中达到预期的无菌效果。
二、验证目标咱们得明确验证目标。
这次验证的主要目标是:1.确认不锈钢立式压力蒸汽灭菌器在正常工作条件下,能稳定达到设定的温度和压力。
2.验证灭菌器在不同负载条件下,对物品的灭菌效果。
3.确认灭菌器在连续工作状态下,性能稳定,不影响灭菌效果。
三、验证方法1.温度和压力监测:通过温度和压力传感器,实时监测灭菌器内部温度和压力,确保它们达到设定的标准。
2.生物指示剂法:将生物指示剂放置在待灭菌物品中,通过检测生物指示剂的存活情况,判断灭菌效果。
3.负载试验:在不同负载条件下,对灭菌器进行试验,观察其灭菌效果。
4.连续工作试验:让灭菌器连续工作一定时间,检测其性能是否稳定。
四、验证步骤明确了验证方法,就是具体的验证步骤了:1.准备工作:检查灭菌器是否正常运行,确保温度和压力传感器准确无误。
2.温度和压力监测:在灭菌器运行过程中,实时记录温度和压力数据。
3.生物指示剂法:将生物指示剂放置在待灭菌物品中,进行灭菌处理,然后检测生物指示剂的存活情况。
4.负载试验:分别在不同负载条件下,进行灭菌试验,观察灭菌效果。
5.连续工作试验:让灭菌器连续工作一定时间,检测其性能是否稳定。
五、验证结果与分析完成了验证步骤,就是分析验证结果了:1.温度和压力监测:将实时记录的温度和压力数据与设定值进行比对,判断灭菌器是否稳定运行。
2.生物指示剂法:分析生物指示剂的存活情况,判断灭菌效果。
3.负载试验:对比不同负载条件下的灭菌效果,找出最佳负载范围。
4.连续工作试验:分析灭菌器在连续工作状态下的性能稳定性。
六、结论与建议根据验证结果,给出结论与建议:2.建议:在使用过程中,注意控制负载范围,避免过度负载;定期检查和维护灭菌器,确保其性能稳定。
蒸汽行业安全风险评估

蒸汽行业安全风险评估
蒸汽行业安全风险评估是通过对蒸汽行业的各个环节和相关因素进行综合分析和评估,识别可能存在的安全风险,并制定相应的措施和管理措施,以降低安全风险的发生概率和减小安全事故的影响。
安全风险评估主要包括以下几个方面的内容:
1. 设备安全评估:对蒸汽行业中的各类设备如锅炉、压力容器、管道等进行安全评估,包括设备的设计、制造、安装、维修等方面的安全风险,确保设备的使用安全和可靠性。
2. 工艺安全评估:对蒸汽行业中的各项工艺控制措施进行评估,识别可能存在的工艺安全隐患,包括温度、压力、流量等参数的控制、过程的监测和操作规程的执行等方面的风险。
3. 人员安全评估:对蒸汽行业中的操作人员的技能、知识和素质进行评估,确保其具备相应的安全培训和操作能力,减少人为因素对安全的影响。
4. 环境安全评估:对蒸汽行业的环境因素进行评估,包括排放的废气、废水、废渣等对环境的影响,确保符合相关环保法规和标准。
5. 管理安全评估:评估蒸汽行业的管理体系和管理制度,包括安全管理责任、纪律、安全培训、应急预案等方面的评估,确保管理措施的有效实施和落地。
通过对以上几个方面的综合评估,可以识别蒸汽行业安全风险,并提出相应的改进措施和管理措施,确保蒸汽行业的安全运行。
哈尔滨市医疗机构压力蒸汽灭菌效果检测评价

E B I 一 1 2 5 A — P T 3 型温度压力记 录仪的温度压力探头放 置在灭菌器 内部的排气 口正上方 , 在整个灭菌周期 内 每秒钟记录一个温度和压力的数值。 在灭菌周期结束 后, 将记 录仪从灭菌器 内取 出。待记录仪外壳温度降 至4 0 ℃以下后 ,将温度记录仪探针朝上放入信号转 换器 , 读取数据 。使用 WI N L O G 2 0 0 0 一 P 软件 , 在 电脑 上读取记录仪记 录的数据 , 分析是否达到压力蒸汽灭 菌 器设 定 的温度 和压 力 。 1 . 3 . 2 生物监 测 方 法 用 生物 指示 物 ( 3 M 公 司生 产 ) 置于标准监测包的中心位置制作的一次性使用标准 测试包 , 置于灭菌器排气 口上方或生产厂家建议 的灭 菌器内最难灭菌的部位 。在灭菌周期结束后 , 采用无 菌 操作 法将 生 物指 示物 取 出 , 夹碎 指示 物 中 内含 的培 养基玻璃管 , 送 实验 室培养 , 并做 阳性对照 , 4 8 小时 后 观察 结果 。如果 指示 液颜 色 未变 色 表 明灭菌 合格 , 变黄为未达到灭菌要求 。同时阳性对照管生长正常 , 呈 黄色 嘲 。 1 . 3 - 3 无 菌器 械 监 测 方 法 可 采 取破 坏 性 方 法 取 样 的灭菌医疗器材 , 参照《 中华人民共 和国药典》 中“ 无 菌 检查 法 ” 进行。 对不 能用破 坏性 方 法取样 的 , 应在 环 境 洁净 度 1 0 0 0 0级 下 的局部 1 0 0级 条件 下 , 用浸 有 采 样液的棉拭子涂抹被检物体表面 , 采样取全部表面或 不少于 1 0 0 c m , 剪 去 手 接触 部 位 , 将 棉 拭 子投 入 装 有 采样 液 的试 管 内进行无 菌 检查 。 采用 直接 接种 法分 别 接种至各含硫 乙醇酸盐流体培养 基和改 良马丁培养 基 的试 管 中 , 按 规定 的温度 培养 1 4天 , 观察 并记 录是 否有菌生长 ,结合 阳性对照和阴性对照实验结果 , 判 断 是否 为灭 菌合 格 。 1 . 4 统计 分析 数据 采 用 E x c e l 软 件进 行统 计分 析 。
医院消毒供应中心压力容器风险评估及防范

灭菌质量的监测
通用要求
温度
时间
压力
下排气式
敷料
121℃
30 min 102.9 kPa
器械
121℃
20 min 102.9 kPa
预真空式
器械、敷料 132~134℃ 4 min
205.8 kPa
灭菌前准备
(1)每天设备运行前应进行安全检查,包括灭菌 器压力表处在“零”的位置;记录打印装置处于备 用状态;灭菌器柜门密封圈平整无损坏,柜门安全 锁扣灵活、安全有效;灭菌柜内冷凝水排出口通畅, 柜内壁清洁;电源、水源、蒸汽、压缩空气等运行 条件符合设备要求。
救援现场图片
安全事故案例
2006年8月14日18时16分,中国石油大庆炼化分 公司发生一起压力容器重大事故,经现场核实, 有2台压力容器爆炸,造成3人死亡,2人重伤。
2006年8月22日9时00分,广东明珠药业有限公 司发生一起压力容器严重事故,造成2人重伤。2 名正在作业的职工烫伤(烫伤面积分别为: 60%、 65%)。
安全事故案例
2006年7月30日11时许,温州市鹿城区某厂突发锅 炉爆炸事故,造成5人死亡、4人受伤。事故调查 发现没有制定锅炉安全生产规章制度和操作规程, 安全生产责任制也没有建立健全,也没有对从业 人员进行安全生产培训,锅炉操作工无锅炉操作 证。
2006年5月9日,温州市特种设备检测中心对 该厂的锅炉进行检测,5月17日出具了锅炉内部检 验报告,要求该厂对已超期未校验的安全阀和压 力表进行校验,但该企业却没有及时送检、校验。
压力蒸气灭菌应注意的几个问题
2、灭菌物品要摆放合理 灭菌柜内的物品不应过挤,其总体积预
真空不超过90%亦也不少于10%。下排气不 超过80%亦也不少于5%。灭菌包在柜内要分 层放置,灭菌包一律竖放,包与包之间要有 间隙,最好将灭菌包放在金属筐内。金属物 品包应放在下层,纸塑包装袋应竖放于篮筐 里再放入架子上,摆放要垂直,这样不仅利 于灭菌,还便于搬运贮存。
LDZX-75KBS_立式压力蒸汽灭菌器风险评估

编号: RAP-EC-001LDZX-75KBS 立式压力蒸汽灭菌器风险评估分析(评估小组)起草:年月日评估人员:批准:xxxxxx制药有限公司一、目的LDZX-75KBS立式自动电热压力蒸汽灭菌器用于我公司微生物限度检查时的灭菌处理。
为降低和控制车间生产过程中的微生物限度相关的风险,建立有效的LDZX-75KBS立式自动电热压力蒸汽灭菌器质量控制体系,提高产品质量提供风险分析参考。
二、适用范围LDZX-75KBS立式自动电热压力蒸汽灭菌器的设计,安装,使用,验证过程。
三、定义:风险:是危害发生的可能性及其危害程度的综合体。
风险管理:即系统性的应用管理方针、程序实现对目标任务的风险分析、评价和控制。
风险分析:即运用有用的信息和工具,对危险进行识别、评价。
风险控制:即制定减小风险的计划和对风险减少计划的执行,及执行后结果的评价。
四、风险识别内容4.1、风险评估风险由两方面因素构成,风险评估是基于对危害发生的频次和危害程度以及可控测度三方面考虑而得出的综合结论。
4.1.1风险产生的后果即危害的严重程度(S)严重程度:第1级:可忽略第2级:微小第3级:中等第4级:严重第5级:毁灭性4.1.2风险发生的概率(P)第1级:稀少(发生频次小于每十年一次)第2级:不太可能发生(发生频次为每2年一次)第3级:可能发生(发生频次为每月一次)第4级:很可能发生(发生频次为每周一次)第5级:经常发生(几乎每次都可能发生)4.1.3风险发生时的可预知性(D)第1级:不可能预知第2级:不太可能预知第3级:可能预知第4级:很可能预知第5级:完全可预知4.2风险识别五、风险控制5.1降低风险的计划5.1.1在实施验证准备阶段,对所有相关的文件均进行了一次核查,以确保文件的准确性。
5.1.2对相关的操作人员进行了岗位操作规程的培训,以确保全部验证过程能按文件规定执行。
合理安排工时,避免人员过度疲劳。
5.1.3在设备运行阶段确保仪表、安全阀等均经过校验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
清洗时操作不规范或不符合操作规程
2
1定期培训和考核
1
8
低
11
生产操作
药品混淆
设备污染,交叉污染
4
因设备改变的摆放房间及位置,人员操作时不认真,走错房间
2
1人员定期培训和考核
1
8
低
12
操作不规范
设备污染,交叉污染
4
未严格执行操作规程,因此造成污染
2
1人员定期培训和考核
1
8
低
仅供个人用于学习、研究;不得用于商业用途。
停电时没有及时通知,造成损失(药品、设备)
4
突然停止供电
2
1停电前应及时通知
1
8
低
7
公共介质
蒸汽不稳
操作难度加大;蒸汽压力过低时影响浓缩时间
4
操作难度加大,容易跑料
2
1定期维修保养蒸汽管道
2开机前检查
1
8
低
附件:表1-2风险因素失败模式效果分析表
序号
步骤
子步骤
风险
影响
S
原因
P
控制措施
D
起始RPN
风险
拆卸、安装
过程中部件污染
过程中部件被污染,不易清洗
4
拆卸、安装过程中部件被污染
2
1整体移动,不进行拆卸,避免损坏设备部件
1
8
低
5
仪器仪表
校验失败或未校验
压力表、温度表、真空表计数不准确或不能代表
4
重新安装后未校验或校验失败
2
1安装后进行校验
2及时粘贴检定标签
3生产前检查
1
8
低
6
动力:电
突然停电设备受损害
Pour l 'étude et la recherche uniquement à des fins personnelles; pas à des fins commerciales.
толькодля людей, которые используются для обучения, исследований и не должны использоваться в коммерческих целях.
2
1生产前检查
2定期培训并考核,学习应急方法,状况发生后用最快的速度采取最正确的处理方法
3参数读数时采取班长复核
1
8
低
2
工作压力
压力不当
蒸汽压力过高可能对人员或设备产生危险;过低,影响工作效率或不能设备正常运行
4
蒸汽安全阀损坏未及时发现致使蒸汽压力过高;
2
1生产前检查
2定期培训并考核,学习应急方法,状况发生后用最快的速度采取最正确的处理方法
For personal use only in study and research; not for commercial use
压力蒸汽灭菌器
风险评估报告
共线产品风险分析列表:
风险
内容
因素
影响事项
影响力
设备性能
设备性能
温度范围
超过温度范围,可能会导致设备无法正常运行
中
压力范围
超过压力范围,可能会导致设备无法正常运行
For personal use only in study and research; not for commercial use.
Nur für den persönlichen für Studien, Forschung, zu kommerziellen Zwecken verwendet werden.
水平
8
设备性能
使用年限
设备使用过程中损坏几率增加
易对生产造成中途停止的结果
4
设备使用时间较长
3
1进行调试确认设备能够正常运行
1
12
中
9
人员操作
人员卫生
人员及工作服不达标
污染环境、污染药品4人员及工作服卫生不符合 Nhomakorabea净级别要求
2
1定期培训和考核
2生产前检查
1
8
低
10
清洁操作
清洗不达标
设备污染,交叉污染
4
3参数读数时采取班长复核
1
8
低
3
蒸汽压力
蒸汽控制不当
蒸汽安全阀损坏未及时发现致使蒸汽压力过高,发生危险的可能性高;过低,不能设备正常运行
4
蒸汽安全阀损坏未及时发现致使蒸汽压力过高;
2
1生产前检查
2定期培训并考核,学习应急方法,状况发生后用最快的速度采取最正确的处理方法
3参数读数时采取班长复核
1
8
低
4
中
使用年限
设备已使用过一段时间,设备使用过程中,损坏的几率增加,易对生产造成中途停止的结果
中
人员操作
人员卫生
洁净区要求洁净度高,人员及工作服带来的污染
中
清洁操作
未严格执行操作规程,因此清洁不彻底,造成污染
中
生产过程
因设备摆放位置的更改,缺乏实际操作而造成清洁或生产操作不符合规定
中
清洗残留
残留限度设定不合理,不能有效消减残留风险
高
环境安全
使用安全
使用后,待压力表显示为“零”后才能开门,否则造成事故
中
附件:表1-1风险因素失败模式效果分析表
序号
步骤
子步骤
风险
影响
S
原因
P
控制措施
D
起始RPN
风险
水平
1
设备性能
工作温度
温度不当
工作温度过高,对人员、药液、设备产生危险;工作温度过低使浓缩工作时间增加或设备不能正常运行
4
蒸汽控制不当,不合规定
中
蒸汽压力范围
超过蒸汽压力范围,蒸汽安全阀已失去效用,对操作人员伤害大,超过设备设计压力可能会导致不能正常运行
中
拆卸、安装
拆卸和安装过程中直接接触药液的部件被污染,不易清洗
中
仪器仪表
重新安装后未校验或校验失败,因此计数不准确
中
公用介质
电:停电时应提前通知,以免造成损失(药品、设备)
中
公共介质
蒸汽:蒸汽不稳时,操作难度加大
