周晓燕 异染性脑白质营养不良
异染性脑白质营养不良研究进展

乏症。 ARS A部 分 缺 乏 表 现 为 在 婴 儿 期 就 出 现 的 但 并 不 加 重 的 神 经 或 肌 肉 症状 , 测 为 底 物 结 合 位 点 发 生 推
个 月发 病 , 期 表 现 为 行 走 困难 、 过 伸 、 力 低 下 、 早 膝 智 易 激 惹 、 张 力 降低 、 肌 腱反 射 减 弱 , 期 出 现 废 用 性 肌 萎 后
缩、 肢痉挛性瘫痪 、 身性 强直 阵 挛性癫 痫发 作、 四 全 眼 震、 神经萎 缩、 语等。 视 失 病情 常 进 行 性 发 展 , 般 在 5 一 岁 前 死 亡 。 2 青 少 年 型 : 病 年 龄 从 儿 童 早 期 到 青 少 () 发 年晚期不等 , 起 为共济失调 、 力 低 下、 情 淡 漠 , 初 智 感
异 染 性脑 白质 营养 不 良( tc rmai l k d sr. me ho t u o yt a ce o
障碍和 姿 势异 常 出现较 晚, 误 诊 为精 神 分裂 症 , 易 可
py h ,ML 是 一 种 常 染 色 体 隐 性 遗 传 性 疾 病 , 最 常 D) 是 见 的 溶 酶 体 病 [ 由于 芳 基 硫 酸 酯 酶 A(rl l ts 1 】 。 ays f ae A, ua ARS 或 神 经 鞘 脂 激 活 蛋 白 B( hn oii ci tr A1 s ig l d at ao p p v p oe S P. ,s p s ) 脑 硫 脂 激 活 蛋 白 的 rti B, A B a oi B 即 n n 缺 陷 , 溶 酶 体 内脑 硫 脂 水 解 受 阻 , 沉 积 在 中 枢 神 使 而
病例汇报-异染性脑白质营养不良1例

患者于10年前感冒后出现头痛、头晕,伴有恶心、呕吐,呕吐物为胃 内容物,约4天后出现持物不准、行走不稳,曾就诊于外院,家人诉 诊断为“小脑硬化”,给予改善脑代谢等药物治疗,出院时患者无头痛 、头晕,无恶心、呕吐,无持物不准、行走不稳。出院后逐渐出现注 意力不集中、学习困难、走路不稳、四肢远端肌肉萎缩,未予特殊治 疗。5年前患者出现行走不稳及四肢远端肌肉萎缩加重,伴有认知力 、计算力、反应力下降,曾于外院行“造血干细胞治疗”,症状无明显 改善,逐渐发展至需要借助外物行走,1年前患者出现饮水偶有呛咳 ,后逐渐加重,于2016-07-24因发热、头痛就诊于我院。
肌腱反射、肱三头肌腱反射、膝反射(+++),踝反 射(-),髌阵挛(-),踝阵挛(-),双侧巴氏征阴 性,双侧Hoffmann征(+),颈部无抵抗,脑膜刺激 征阴性。
颅脑MRI+MRA(2016-7-26 本院):双侧额顶颞叶、 中脑、基底节及丘脑区多发异常信号影,脱髓鞘病变,
MRA未见异常。
1.脑白质病变 2.急性上呼吸道感染
PAS染色:未见异常物质沉积; 刚果红染色:未见淀粉样物质沉积。
结论:轻度周围神பைடு நூலகம்病变。
1.异染性脑白质营养不良 2.急性上呼吸道感染
谢谢
遗传代谢氨基酸和酰基肉碱检查未见异常。 尿有机酸检查无异常。 铜、铜蓝蛋白未见异常。 血皮质醇未见异常。 脑脊液检查:白细胞(-),糖氯正常;蛋白定量:2.04g/L。 四肢肌电图:上下肢运动神经病变(波幅降低为主,轴索变 性可能性大)。
左侧腓神经活检:
HE染色、改良Gomori三色染色示:镜下可见7个神经纤维 束,神经束内有髓神经纤维数量轻度减少,约10%;未见 髓鞘消解腔;未见洋葱球样结构,未见血管周围及跨壁炎 细胞浸润;
异染性脑白质营养不良1例
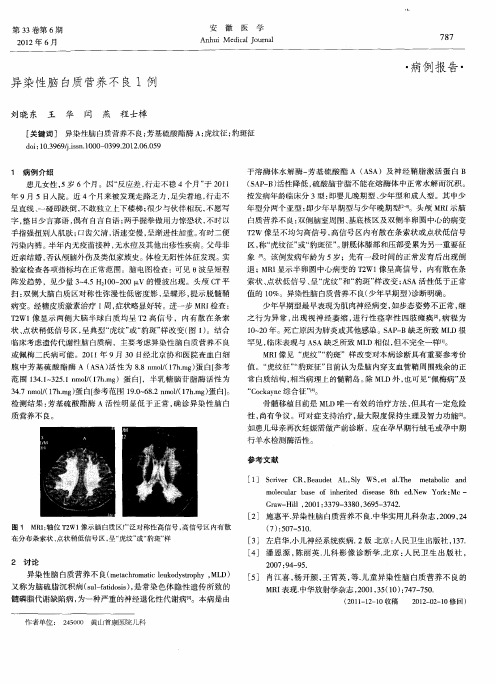
又称为脑硫 脂沉积病 (u—a ds )是 常染色体 隐性遗传所 致的 slft oi , i s 髓磷脂代谢 缺陷病 , 为一种严重 的神经退化性代谢病【 l 】 。本病 是由
作者单位 : 2 5 0 黄山首康 医院儿科 400
[ ] 肖江喜 , 开颜 , 5 杨 王霄英 , 儿童异染性 脑 白质营养不 良的 等.
di1.9 9 .s. 0 — 3 92 1 . . 9 o:0 6  ̄i n1 0 0 9 . 20 0 3 s 0 0 65
1 病 例 介 绍
于溶酶体水解 酶一 芳基 硫酸酯 A ( S A A)及神经鞘 脂激 活蛋 白 B (A — ) S P B 活性降低 , 酸脑苷脂不 能在熔 酶体 中正 常水解 而沉积 。 硫 按发病年龄临床分 3型 : 即婴儿晚期型 、 少年型和成人型 。其 中少 年 型分 两个 亚型 : 即少年早期型与少年晚期型 。头 颅 MR 示脑 I 白质营养不 良: 双侧 脑室周 围、 基底核 区及 双侧半 卵圆中心 的病变
值 。“ 虎纹征 ”豹斑征” “ 目前认为是脑内穿支血管鞘周围残余的正
常 白质结构 , 当病理上的髓鞘 岛。 ML 相 除 D外 , 也可见“ 佩梅病 ” 及
“ oky e 合 征 ”1 C e an 综 [ 4 。
3 . n o (7 . ) 白[ 范围 1.~ 8 mo (7 . ) 47 m l 1 h 蛋 参考 / mg 90 6 . n l 1h 2 / mg 蛋白] 。 检测结 果 : 基硫酸酯 酶 A活性 明显低 于正 常 , 诊异染 性脑 白 芳 确 质营养不 良。
小儿异染性脑白质营养不良预防和措施PPT

演讲人:
目录
1. 什么是小儿异染性脑白质营养不良? 2. 为什么要预防小儿异染性脑白质营养不 良? 3. 何时进行预防措施? 4. 如何实施预防措施? 5. 谁负责预防小儿异染性脑白质营养不良 ?
什么是小儿异染性脑白质营养 不良?
什么是小儿异染性脑白质营养不良?
为什么要预防小儿异染性脑白质营养不良?
降低发病率
通过遗传咨询和产前筛查降低该疾病的发病 率。
特别是对于有家族史的家庭,遗传咨询是பைடு நூலகம் 常重要的预防措施。
为什么要预防小儿异染性脑白质营养不良?
改善生活质量
有效的预防措施能够改善患儿及其家庭的生 活质量。
通过早期干预和治疗,能够减轻症状,提高 生活质量。
定义
小儿异染性脑白质营养不良是一种罕见的遗传性 疾病,主要影响儿童的脑白质,导致神经功能受 损。
该病因脑部白质的变性和营养不良而引发,通常 在婴儿期或幼儿期被诊断。
什么是小儿异染性脑白质营养不良?
症状
患儿可能出现运动协调性差、认知障碍和肌肉无 力等症状。
这些症状的严重程度因个体差异而异,早期识别 和干预至关重要。
遗传咨询师可以帮助家庭理解风险并做出知 情选择。
如何实施预防措施?
健康监测与干预
对高风险儿童进行定期健康监测以及早期干 预。
通过专业的医疗团队进行监测,确保及时发 现和处理问题。
谁负责预防小儿异染性脑白质 营养不良?
谁负责预防小儿异染性脑白质营养不良?
医疗工作者
医生、护士和遗传咨询师等医疗工作者在预防中 扮演重要角色。
对于新生儿进行早期筛查,以便及时发现潜在的 疾病。
新生儿筛查可以帮助在症状出现前进行干预。
小儿异染性脑白质营养不良危害及预防PPT课件

这可能需要长期的物理治疗和康复训练。
小儿异染性脑白质营养不良的危害 社会适应问题
由于认知和运动障碍,患者可能面临社交困 难。
这可能导致情绪问题和良?
如何预防小儿异染性脑白质营养不良?
遗传咨询
对于有家族史的家庭,进行遗传咨询是非常重要 的。
未来的研究方向
长期跟踪研究
进行长期的随访研究,以便更好地了解疾病的发 展及其影响。
这对于优化治疗方案和患者管理至关重要。
谢谢观看
患者可能出现运动协调不良、语言发育延迟、认 知障碍等症状。
症状的严重程度因个体差异而异。
小儿异染性脑白质营养不良的 危害
小儿异染性脑白质营养不良的危害
对智力的影响
该病会导致儿童认知功能受损,影响学习能 力。
许多患者在学业上表现不佳,难以适应正常 的教育环境。
小儿异染性脑白质营养不良的危害 对运动的影响
如何治疗小儿异染性脑白质营 养不良?
如何治疗小儿异染性脑白质营养不良?
多学科合作
治疗需要神经科医生、康复治疗师和心理医 生的团队合作。
这种多学科的综合治疗可以提供全面的支持 。
如何治疗小儿异染性脑白质营养不良? 个性化康复计划
根据每个患者的具体情况制定个性化的康复 计划。
包括物理治疗、职业治疗和言语治疗等。
这可以帮助父母了解潜在风险,并作出知情决策 。
如何预防小儿异染性脑白质营养不良? 早期筛查
在出生后进行早期筛查,可以帮助尽早发现潜在 问题。
及时的干预可能改善预后。
如何预防小儿异染性脑白质营养不良?
健康生活方式
建立健康的生活方式,包括均衡饮食和定期锻炼 ,有助于改善整体健康。
小儿异染性脑白质营养不良科普宣传

谢谢观看
希望未来能够找到更有效的治疗方案。
我们能做什么?
我们能做什么?
公众教育
提高公众对小儿异染性脑白质营养不良的认识, 以便早期识别。
通过社区活动和讲座传播相关知识。
我们能做什么?
支持研究
鼓励捐款和支持相关的研究项目。 研究资金的增加可以加速新治疗方法的开发。
我们能做什么?
关心患者
为患者家庭提供信息和资源,帮助他们应对挑战 。
谁会受到影响?
发病人群
小儿异染性脑白质营养不良主要影响婴幼儿,尤 其是家族中有该疾病病史的儿童。
尽管任何儿童都有可能被影响,但某些种族可能 更高风险。
谁会受到影响?
遗传因素
该疾病的遗传性使得有家族史的儿童更容易发病 。
进行基因检测可以帮助识别携带者。
谁会受到影响?
性别差异
目前的研究表明,男性儿童似乎更容易受到影响 。
小儿异染性脑白质营养不良 科普宣传
演讲人:
目录
1. 什么是小儿异染性脑白质营养不良? 2. 谁会受到影响? 3. 何时发现及诊断? 4. 如何管理与治疗? 5. 我们能做什么?
什么是小儿异染性脑白质营 养不良?
什么小儿异染性脑白质营养不良?
定义
小儿异染性脑白质营养不良是一种遗传性疾病, 主要影响大脑白质的发育和功能。
具体的性别差异机制仍在研究中。
何时发现及诊断?
何时发现及诊断?
发现时间
通常在儿童6个月到2岁之间就能观察到症状。 早期发现对干预和管理至关重要。
何时发现及诊断?
诊断方法
通过临床评估、影像学检查(如MRI)和基因检 测进行确诊。
专业医生的综合评估是关键。
小儿异染性脑白质营养不良的科普知识PPT

该病的症状有哪些?
该病的症状有哪些? 运动症状
常见症状包括肌肉无力、运动协调不良和步 态异常。
一些儿童可能会出现行走延迟或跌倒频繁的 现象。
该病的症状有哪些? 认知症状
认知功能可能受到影响,表现为学习困难和 语言发育迟缓。
部分儿童可能会有注意力缺陷或社交能力不 足。
影像学检查能够提供有关脑部结构的重要信息。
如何进行诊断?
基因检测
基因检测可以确认是否存在相关的基因突变。
这对于确诊和家族遗传咨询非常重要。
如何进行治疗?
如何进行治疗? 对症治疗
目前没有治愈该病的方法,治疗主要是针对 症状。
物理治疗、职业治疗和语言治疗可以帮助改 善患者的生活质量。
如何进行治疗? 支持性治疗
该病通常在婴儿期或幼儿期首次表现出症状,影 响儿童的运动和认知能力。
什么是小儿异染性脑白质营养不良? 病因
该病通常由基因突变引起,这些突变影响脑细胞 的脂质代谢。
最常见的基因突变包括ARSA和PSAP等,这些突变 导致神经髓鞘的形成异常。
什么是小儿异染性脑白质营养不良? 发病机制
病理学上,脑白质的髓鞘化受损,导致神经信号 传导的障碍。
小儿异染性脑白质营养不良
演讲人:
目录
1. 什么是小儿异染性脑白质营养不良? 2. 该病的症状有哪些? 3. 如何进行诊断? 4. 如何进行治疗? 5. 如何预防与管理?
什么是小儿异染性脑白质营 养不良?
什么是小儿异染性脑白质营养不良? 定义
小儿异染性脑白质营养不良是一种罕见的遗传性 神经系统疾病,主要影响脑白质的发育和功能。
如何预防与管理?
定期随访
小儿异染性脑白质营养不良危害及预防PPT

演讲人:
目录
1. 什么是小儿异染性脑白质营养不良? 2. 为什么小儿异染性脑白质营养不良是一 个严重的问题? 3. 何时应该进行诊断? 4. 如何预防小儿异染性脑白质营养不良? 5. 总结与展望
什么是小儿异染性脑白质营 养不良?
什么是小儿异染性脑白质营养不良? 定义
小儿异染性脑白质营养不良是一种遗传性疾病, 主要影响ቤተ መጻሕፍቲ ባይዱ脑的白质,导致神经功能受损。
该疾病通常在婴幼儿期发病,影响孩子的运动、 认知及语言能力。
什么是小儿异染性脑白质营养不良? 病因
这种疾病与特定基因突变有关,影响脂质代谢, 导致脑白质的缺乏和损伤。
常见的基因突变包括:ABCD1基因的突变。
什么是小儿异染性脑白质营养不良? 症状
何时应该进行诊断?
家族史
有家族遗传病史的孩子应进行定期筛查,及早发 现潜在风险。
家族遗传咨询可以帮助家庭了解风险和管理方案 。
如何预防小儿异染性脑白质 营养不良?
如何预防小儿异染性脑白质营养不良? 遗传咨询
有家族病史的父母在怀孕前应进行遗传咨询 ,以了解潜在风险。
这可以帮助父母做出知情的生育选择。
许多患者在成长过程中需要长期的康复和护 理支持。
为什么小儿异染性脑白质营养不良是一个严重的问 题? 社会负担
疾病的长期管理将对家庭及社会医疗资源造 成压力。
这可能导致更多的医疗费用和心理支持需求 。
为什么小儿异染性脑白质营养不良是一个严重的问 题? 教育问题
孩子可能在学校面临学习困难,影响他们的 学业和社交能力。
孩子可能表现出运动协调困难、认知迟缓、视力 或听力障碍等症状。
症状的严重程度因人而异,有些孩子可能只表现 出轻微的症状。
小儿异染性脑白质营养不良预防和措施课件

何时采取预防措施?
孕前咨询
有家族史的家庭在计划怀孕之前应咨询遗传专家 。
提前了解可能的遗传风险可以帮助做出明智的决 策。
何时采取预防措施? 孕期监测
在孕期定期进行超声检查和基因筛查,以确保胎 儿健康。
早期发现异常可以及时进行干预。
何时采取预防措施? 出生后评估
新生儿应在出生后进行全面的健康评估。
及时的评估和干预可以显著改善预后。
谢谢观看
孕妇应保持健康的生活方式,定期进行产前检查 ,以降低胎儿风险。
营养均衡、避免有害物质接触是关键。
如何预防小儿异染性脑白质营养不良? 早期干预
对高风险儿童进行早期评估和干预,可以改善其 发展结果。
包括物理治疗、语言治疗等。
谁应该参与预防工作?
谁应该参与预防工作? 医疗工作者
医生和护士应对相关疾病有充分的认识,并提供 适当的筛查和建议。
遗传咨询
了解该病的遗传特性可以帮助家长进行有效的生 育规划。
通过遗传咨询,潜在的携带者可以做出知情选择 。
如何预防小儿异染性脑白质营 养不良?
如何预防小儿异染性脑白质营养不良? 遗传筛查
实施基因筛查可以帮助识别高风险家庭。
早期识别可以为后续的干预和管理提供依据。
如何预防小儿异染性脑白质营养不良? 孕期保健
小儿异染性脑白质营养不良的预 防与措施
演讲人:
目录
1. 什么是小儿异染性脑白质营养不良? 2. 为什么要进行预防? 3. 如何预防小儿异染性脑白质营养不良? 4. 谁应该参与预防工作? 5. 何时采取预防措施?
什么是小儿异染性脑白质营养 不良?
什么是小儿异染性脑白质营养不良?
定义
小儿异染性脑白质营养不良是一种遗传性神经系 统疾病,主要影响脑白质的发育和功能。
婴儿晚期型异染性脑白质营养不良一例报告
脱落球束导管堵塞术 I ; 例 海绵赛砸赢术4侧
辅助检查 : 车组 病 例腰 穿 脑背 液 常 规 隹化 盐 c 打 1 均正常 血 精 4 6 ~9 5  ̄ o/ :咀 胆 固 醇 6 2 —85 lI m ̄ lL 甘油 酯 l o / 9—2 5『 L 蠊密 度脂 蛋 白胆 同醇 川r 、
多的患者 受益
( 稿 1蝈 2 0 - -3 收 3 031 2 ) 0
u管周 的细 胞 内 拜 性糊 质 l L
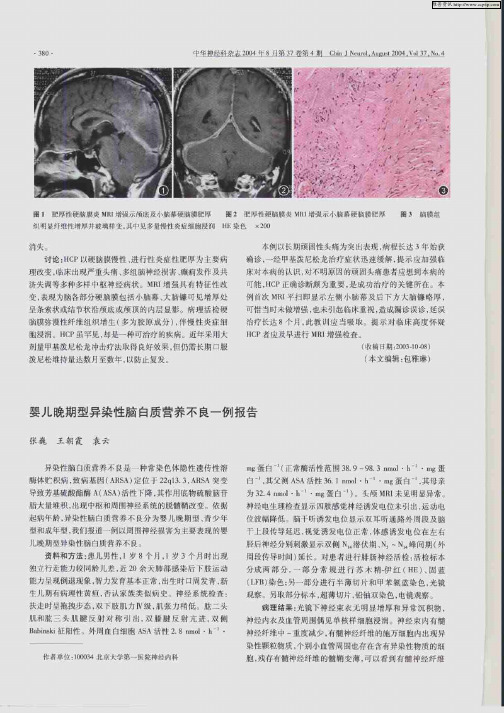
目 2 崽 青肺 腑神经 衙椅 电 境 r m有髓 冲磐 纤维 洋葱 球样 结 构. 嫩 抛的腿Ⅲ 出现 异常蔷 酶排样钻 椅
x6 0 7 0
( 史编辑 半鹏 ) 率
理改在, J 床出现严重头痛、 多组脑神经搦害 . 癫嫡发作及共
济失调等多种多样中枢神经墒状 M [ R 增强具有特征性改
变. 表现 l脯 备部 分硬腌 膜包 括小 肺幂 、 腑罐 可 见增 厚处 为 太
能, C 确诊断颇为重要. H PI E 是成功精疗的关键所在
车
例 首 次 MR 平 扫 即显 示 庄 删 小 眦 群 及 后 下 方 大 脑 镰 略 厚 . I
神经内农及血管周围偶 见单棱样细盱浸润 神经束 内有髓 包
抻经纤维 中 一重度 减少 - 有髋 神经纤 维的施万{ 胞内 出现抖 『 H
槊吐颗粒物质. 十别小 m管周围也存在青有异船性物质的细
作青单位 :0O4北 大学 第 一 哓 I 内科 1 3  ̄ 鳋
胞, 残存有髓神经 维 的髓鞘韭薄 . f 可以看到有髓种经纤维
肌和眩 三 肌 越 反射 对 称 引 出 . 膝 髓 反 射 亢 进 . 删 双 双 B hlk 征 阳性 aisi l 外周血 白细 胞 A A活性 2 8n o h ・ S m l
异染性脑白质营养不良

异染性脑白质营养不良
临床表现
2. 少年型(少数), 成人型(极少) 首发症状: 精神障碍\行为异常&记忆力减退 晚期: 构音障碍\四肢活动不灵\锥体束征\痫性
发作\共济失调\眼肌麻痹&周围神经病 可见视盘苍白萎缩 偶见视网膜樱桃红点
异染性脑白质营养不良
临床表现
3. 辅助检查 尿液芳基硫酸酯酶A明显↓, 活性消失 硫脑苷酯(+)支持本病诊断 CT: 脑白质\脑室旁对称不规则低密度区, 无占
患儿应避免\限制摄入富含维生素A食物Leabharlann 预后异染性脑白质营养不良
预后差 婴幼患儿发病后1~3年因四肢瘫卧床不起 伴严重语言&认知障碍, 可存活数年 成人病例进展较缓慢, 存活时间较长
异染性脑白质营养不良 (Metachromatic Leukodystrophy)
概念
神经鞘脂沉积病 Alzheimer(1910)首先报道 常染色体隐性遗传 发病率0.8~2.5/10万 呈家族性, 国内多散发病例
异染性脑白质营养不良
病因
22号染色体上芳基硫酯酶A(arylsulfatase-A) 基因缺乏→芳基硫酯酶A不足
位效应, 不强化 MRI: T1WI低信号, T2WI高信号
异染性脑白质营养不良
临床诊断标准
1. 婴幼儿进行性运动
障碍\视力减退&精
T2
T1
神异常
2. CT或MRI证实两侧
半球对称性白质病
灶
3. 尿芳基硫酸酯酶A
活性消失
T2
T1
异染性脑白质营养不良
治疗
目前尚无有效疗法 支持&对症治疗为主 基因疗法尚处于探索阶段 维生素A是合成硫苷酯的辅酶
我国异染性脑白质营养不良治疗获突破

在经过1个多⽉的治疗后,患有异染性脑⽩质营养不良的⼼⼼(化名),⽩细胞、红细胞、⾎⼩板均恢复正常,其体内缺乏的芳基硫酸酯酶指数也由⼊院时的每17⼩时13毫克升⾄每17⼩时79毫克(正常值范围为每17⼩时130毫克~325毫克)。
9⽉6⽇,空军总医院宣布,其⾎液科应⽤“半相合⾻髓移植联合间充质⼲细胞输注”⽅法治疗异染性脑⽩质营养不良疾病获得成功。
经检索,采⽤这⼀“双管齐下”的⽅法治疗这种疾病在国内尚属⾸例。
据空军总医院⾎液科主任王恒湘介绍,⼼⼼今年7岁,2009年9⽉出现记忆⼒下降、咀嚼和吞咽⾷物困难、⾔语不清、平地跌跤等症状,今年3⽉被确诊为异染性脑⽩质营养不良。
7⽉,患⼉来到空军总医院就诊时,已出现四肢肌⾁萎缩症状。
该院经过反复论证,决定由患⼉的母亲捐献⾻髓,采⽤“半相合⾻髓移植联合间充质⼲细胞输注”的⽅法进⾏治疗。
王恒湘告诉记者,⾻髓移植的⽬的是重建患⼉的造⾎及免疫功能,让全新的⽩细胞在其体内“⽣根发芽”,从⽽正常分泌出⼈体必需的芳基硫酸酯酶,阻⽌病情恶化;在术后⼀周左右,再将从母亲⾎液中提取的200毫升间充质⼲细胞注⼊患⼉椎管内,⼀周1次,⼀个⽉为⼀疗程,其⽬的是促进神经细胞再⽣,修复患⼉已受损的神经功能。
⽬前,患⼉已接受3次间充质⼲细胞输注治疗,呛咳等症状得到有效缓解。
据介绍,异染性脑⽩质营养不良是⼀类罕见的严重神经退化性代谢病,发病率极低,约为1/16万,为常染⾊体隐形遗传。
由于患者体内缺乏⼀类芳基硫酸酯酶,从⽽引发神经系统⼴泛脱髓鞘,发病时患者可表现为智⼒下降、运动功能障碍,浑⾝肌⾁萎缩、步态不稳等。
如果病情⽆法得到控制,患者最终将因全⾝肌⾁萎缩或出现各类并发症死亡。
⽽此前医学上尚⽆有效的治疗⽅法,并⼀直将该病归为神经内科疾病。
小儿异染性脑白质营养不良护理

如何实施护理 家庭参与
鼓励家属参与护理过程,提升患者的依从性 和积极性。
家庭的支持对患者的康复至关重要。
如何实施护理 跨学科团队合作
护理团队应与医生、治疗师和心理咨询师密 切合作,共同制定和执行护理方案。
多学科合作有助于全面满足患者的需求。
护理的效果评估
应定期对患者进行评估,以调整护理和治疗方案 。
评估包括身体、认知、情感和社交等多方面。
何时进行护理干预
急性发作
在患者出现急性症状或并发症时,应迅速进行护 理干预。
及时的医疗干预可以有效控制病情发展,防止并 发症。
如何实施护理
如何实施护理
个性化护理计划
根据每个患者的具体情况制定个性化的护理 计划。
为什么需要护理
促进康复
通过物理治疗和职业治疗等干预措施,能够 促进患者的功能改善。
早期干预和持续的康复训练能够有效改善运 和认知功能。
何时进行护理干预
何时进行护理干预 早期诊断
在确诊后,应尽早实施护理计划,以便及时干预 。
早期干预有助于减缓病情发展,提高生活质量。
何时进行护理干预 定期评估
症状的严重程度因个体而异,可能在不同年龄段 表现不同。
为什么需要护理
为什么需要护理
病情管理
有效的护理可以帮助管理症状,提升患者的 生活质量。
通过定期评估和个性化的护理计划,能够及 时调整治疗策略。
为什么需要护理
心理支持
患者及其家庭往往面临巨大的心理压力,良 好的护理能提供必要的支持。
心理辅导和家庭支持能够帮助家庭适应这一 疾病。
家属的意见和建议对优化护理方案非常重要。
谢谢观看
异染性脑白质营养不良

异染性脑白质营养不良异染性脑白质营养不良(异染色性白质脑病,异染色性白质萎缩,异染色性白质营养不良,异染性脑白质病)【病因】(一)发病原因异染色性脑白质营养不良属常染色体隐性遗传,突变基因位于第2 2号染色体上。
由芳基硫脂酶A(aryl sulfatase-A)缺乏所引起。
(二)发病机制硫酸脑苷脂分布于神经组织髓鞘、肾小管上皮细胞等细胞膜中。
正常情况下,芳基硫酸脂酶A催化硫酸脑苷脂水解,将半乳糖硫酸脑苷脂分解为半乳糖脑苷脂和硫酸。
此酶缺乏时引起硫酸脑苷脂于体内沉积。
主要的病理改变为中枢神经系统髓鞘脱失,周围神经受累轻微。
病理切片中,以甲苯染色时,可见神经细胞、神经胶质细胞和巨噬细胞中有红黄色的异染物质沉积。
肝、肾组织亦可同时受累。
【症状】根据起病年龄可以区分为晚期婴儿型(1~2岁起病)、少年型(4~1 5岁起病)和成年型(16岁以后起病),以晚期婴儿型最为常见。
典型者其病程可分为以下3期:第1期:1~2岁之间发病,病前婴儿发育正常;起病后病儿逐步出现运动减少、肌张力降低,步态蹒跚,维持姿势困难,不能独立站、坐,甚至抬头困难。
体格检查可见肌张力降低,腱反射降低或消失,视盘苍白,锥体束征阴性。
脑电图正常或有慢波增多。
脑脊液压力正常,可有轻度蛋白质增高。
此期持续数周至数个月。
第2期:病儿进行性智能减退。
语言减少到消失,对周围环境逐步反应减少。
尖叫而卧床不起。
体格检查可见瞳孔光反应迟钝。
视盘苍白萎缩,面无表情,吞咽动作缓慢,四肢肌张力增高。
肢体伸直,腱反射亢进,病理锥体束征阳性,但躯干和颈肌肌张力正常或偏低。
脑脊液压力、细胞正常,蛋白质明显升高。
脑电图出现弥漫性慢波灶。
此期病程可持续一至数年。
第3期:为晚期病症。
病儿对外界极少反应,常有抽搐和肌阵挛发作。
呈现特殊的去皮质强直体位,头后仰,项强直,肌强直,四肢腱反射极难引出,两侧锥体束征阳性。
瞳孔散大而对光反应极差,眼球游动或是有“玩偶”眼征。
吸吮和吞咽严重障碍。
异染性脑白质营养不良1例报告及文献复习

异染性脑白质营养不良1例报告及文献复习戚静;刘坚【摘要】@@ 脑白质营养不良是指中枢神经系统正常髓鞘生长受累所致疾病,该类疾病应只包括那些由遗传决定的脑白质病.异染性脑白质营养不良(metachromatic leukodystrophy,MLD)为脑白质营养不良中的较常见类型.此病又称异染性白质脑病.是一种严重的神经退化性代谢病,系常染色体隐性遗传性疾病,MLD是由于硫酸脑苷脂及其他含硫酸的糖脂不能脱硫酸,而沉积在全身组织的溶酶体中,主要在中枢及周围神经系统中,其次有肾、胆囊、肝等.最终导致神经系统脱髓鞘而形成的进展性、退化性神经系统疾病.MLD是一种并不很少见的遗传代谢性疾病,在临床工作中需加强对此病的认识,本文的报道以期达到此目的,尽可能减少误诊.【期刊名称】《中国神经精神疾病杂志》【年(卷),期】2011(037)012【总页数】2页(P714-714,729)【作者】戚静;刘坚【作者单位】湖北省襄阳市中心医院神经内科,襄阳,441021;湖北省襄阳市中心医院儿科【正文语种】中文【中图分类】R742脑白质营养不良是指中枢神经系统正常髓鞘生长受累所致疾病,该类疾病应只包括那些由遗传决定的脑白质病。
异染性脑白质营养不良(metachromaticleukodystrophy,MLD)为脑白质营养不良中的较常见类型,此病又称异染性白质脑病,是一种严重的神经退化性代谢病,系常染色体隐性遗传性疾病,MLD是由于硫酸脑苷脂及其他含硫酸的糖脂不能脱硫酸,而沉积在全身组织的溶酶体中,主要在中枢及周围神经系统中,其次有肾、胆囊、肝等,最终导致神经系统脱髓鞘而形成的进展性、退化性神经系统疾病。
MLD是一种并不很少见的遗传代谢性疾病,在临床工作中需加强对此病的认识,本文的报道以期达到此目的,尽可能减少误诊。
患者女,3岁。
顺产。
1岁前四肢力量无明显异常,踢物时双腿有力,发育未见异常,但1岁3个月时患者尚不能独立行走,步行不稳,姿势异常,1岁半时仍然如此,当时查体:神清,智力一般,言语不清,步态异常,四肢肌力Ⅴ-级,肌张力低,双下肢腱反射差,未引出病理反射。
异染性脑白质营养不良

异染性脑白质营养不良什么是异染性脑白质营养不良?异染性脑白质营养不良(Pelizaeus-Merzbacher disease, PMD)是一种罕见的遗传性疾病,主要发生在儿童。
该疾病主要影响中枢神经系统,特别是脑白质区域,导致脑白质缺乏正常的隔离物质,从而影响神经元之间的正常信号传递。
PMD的症状有哪些?PMD的症状可以在患病婴儿和幼儿时期就开始表现。
常见的症状包括:•运动障碍:包括肌张力异常、运动失调和肌肉僵硬等。
•发育迟缓:智力和语言发展受到影响,患儿可能出现智力障碍、言语困难等。
•视觉问题:患病儿童可能出现视神经萎缩和眼球运动异常等问题。
PMD的诊断及治疗PMD的诊断通常通过神经影像学检查(如核磁共振成像)和基因检测来确定。
目前尚无治愈PMD的方法,治疗主要是针对症状进行的支持性治疗,包括物理疗法、言语治疗和康复训练等。
病情较重的患者可能需要长期的护理和监护。
对于家庭来说,提供支持和关爱对于帮助患者提高生活质量至关重要。
PMD的遗传与家庭规划PMD是一种遗传性疾病,主要是由X染色体上的缺陷基因引起的。
因此,携带有PMD基因突变的家族在家庭规划和生育方面可能需要一些额外的考虑。
遗传咨询和基因检测可帮助家庭了解风险并做出明智的决策。
结语异染性脑白质营养不良是一种复杂的遗传性疾病,尽管目前尚无明确的治疗方法,但及早诊断和有效管理可以帮助减轻症状,并提高患者的生活质量。
家庭支持和关爱在治疗中起着至关重要的作用,对患者的康复和生活质量具有积极的影响。
希望未来能有更多针对PMD的研究,为患者和家庭提供更多的希望和支持。
异染性脑白质营养不良该怎么办

异染性脑白质营养不良该怎么办
很多的患者出现了异染性脑白质营养不良的现象发生,严重的影响到患者的身体的健康问题出现,因此出现了上述的问题要及时地进行治疗,这样才能够保证患者安全,那么异染性脑白质营养不良该怎么办?那么下面我就为大家来介绍一下这个问题吧。
指导意见:治疗以支持和对症治疗为主,患儿应避免和限制摄入富含维生素A的食物。
异染性脑白质营养不良能治吗回答者:赵俊辉治疗需要结合孩子的病情,孩子目前还很小,建议尽早的采取合理的治疗
异染性脑白质营养不良的治疗方法回答者:赵俊辉根据你的描述,孩子可能存在脑神经的受损,建议可以咨询一下神经组织修复疗法的治疗。
异染性脑白质营养不良的治疗方法回答者:神经损伤专家
脑白质营养不良是芳基硫酸酯酶A的活性缺乏,引起脑硫脂沉积于体内,导致中枢神经系统广泛脱髓鞘,也称脱髓鞘脑病。
治疗不当会受累神经会因缺血过久导致脑萎缩以及更严重的症
发生。
治疗应及早的增强机体免疫功能,提高肌体抗病能力。
营养神经,中西医结合扩张微循环使受损残余神经得到充分的血供,预防病情继续发展。
并采用神经再生之药兴奋激活麻痹和休克的神经恢复其功能并使体内产生抗致病病毒抗体预防迟发神经再
度受损加重病情达失髓鞘达受累神经的再生修复获得早日康复,。
需帮助请发发病时和最近的磁共震为你指导。
以上就是我为大家介绍的这个问题的看法,患者出现了上述的问题,那么应当立即采取相应的治疗的措施进行治疗,这样才能够保证患者的安全,避免因为上述的疾病出现从而影响到患者的健康的情况发生,那么最后祝患者能够早日康复。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
护理措施
骨髓移植: 骨髓移植(BMT)可纠正MLD患者的代谢异常。1985年
Bayever等对一个晚婴型患者进行了BMT,结果发现智力 得到了明显提高。1990年Krivit等报道一个5年前接受B MT的10岁女孩,其神经电生理及脑硫脂代谢均得到了明 显改善。但也有研究表明BMT并未使MLD的症状得到明显 改善,且MRI表明脑白质的损伤是持续加重的。目前多 认为BMT宜应用于晚婴型的症状前或青少年型的早期患 者。
MRI检查:MRI表现为脑室周围及皮质下白质广泛的,对称性的改变,在T1WI为低信号 、T2WI为高信号,通常自双侧额叶向后发展,注入造影剂后,病灶无强化。在症状早期即 有很明显的改变,但无U形纤维及小脑受累。后期可景及小脑,U形纤维,并有脑室扩大和 脑皮质萎缩。
CT扫描可在病灶部位发现低密度影,但不如MRI清晰。单光子发射计算机体层摄影术在 MRI有异常表现前1年即可发现病灶部位脑血流量降低,因此可用于早期诊断。
临床表现
MLD通常按发病年龄分以下三型:晚婴型 、青少年型、成人型。
晚婴型:最常见,病情也最重,患儿出生时 正常,有一段正常生长发育过程,多在12-24个 月发病,早期表现为行走困难、膝过伸、智力 低下、易激惹、肌张力降低、腱反射减弱,后 期出现废用性肌萎缩、四肢痉挛性瘫痪、全身 性强直阵挛性癫痫发作、眼震、视神经萎缩、 失语等。病情常进行性发展,一般在5岁前死亡 。
周围神经、脑组织、肾脏、肝管、 胆囊活检发现异染的,电镜下呈特异性 的人字型和蜂窝状结构物质,可确诊本 病。脑脊液蛋白多数大于1.0g/L,周围 神经传导速度减慢,脑干诱发电位潜伏 期延长,脑电图示弥漫性慢波,均有助 于MLD的诊断。杂合子尽管无临床症状, 但可有神经电生理SAP-B基因突变检测多用 于鉴别携带者及产前诊断,并可鉴别患 者基因型,为基因治疗提供依据。基因 检测联合ARSA活性、SAP-B蛋白测定可以 确保产前诊断。
青少年型:
发病年龄从儿童早期到青少年晚期不等,初起为共 济失调,智力低下、感情淡漠,晚期出现痴呆、部 分性癫痫发作、视神经萎缩、四肢瘫痪等。病情可 缓慢进展,也可迅速发展。年龄较小者周围神经受 累较重,年龄较大者则以学习和行为障碍等脑部症 状为主。
成人型:
多在2l岁后发病,症状与青少年型相似,但病情较 轻,常以精神症状首发,运动障碍和姿势异常出现 较晚,易误诊为精神分裂症,可伴有周围神经受累 ,也可仅有周围神经受累。
治疗:
1.对症支持治疗 支持治疗可最大限度保 持生理及智力功能。若有癫痫发作,可 用抗癫痫药治疗;痉挛时可用肌肉松弛 剂。
2 .积极的物理治疗 目的在于尽量保持 智力、神经肌肉功能及活动能力。
酶替代治疗
治疗:
1971年Porter等人通过在培养基内补充ARSA ,发现MLD患者皮肤成纤维细胞的代谢缺陷得到了纠 正。此后,有多种酶替代治疗方案用于临床。有人 应用牛脑提取的ARSA静脉或鞘内注射治疗MLD患者, 虽使肝脏中ARSA的活性恢复正常,但脑内ARSA活性 及脱髓鞘病变无任何改善。现已证明补充的ARSA不 能通过血脑屏障,有人使用酶降解抑制剂作为酶替 代治疗辅助治疗,旨在抑制ARSA降解,促进残余ARS A的功能,但未见明显效果。
基因治疗:
MLD为单基因遗传病,成功的基因治 疗(GT)将使本病得到根本治疗。近10年 来,国外学者就MLD的GT方法进行了大量 探索,并取得了令人可喜的结果。尽管G T在临床应用之前尚有许多理论和技术性 问题需要解决,但它仍是未来的发展方 向。
感谢下 载
异染性脑白质营养不 良
燕 周晓燕
定义
异染性脑白质营养不良(metachr omatic leukodystrophy,MLD))是一 种常染色体隐性遗传性疾病,为脑白 质营养不良中的较常见类型,此病又 称异染性白质脑病,是一种严重的神 经退化性代谢病,是最常见的溶酶体 病。
病因 由于芳基硫酸酯酶A(arylsulphatase A,ARSA)或神经鞘脂激活蛋白B(sphingolipi d activator protein B,SAP-B,saposin B )即脑硫脂激活蛋白的缺陷,使溶酶体内脑硫 脂水解受阻,而沉积在中枢神经系统的白质 、周围神经及肾、胆囊、肝等内脏组织,引 起脑白质、周围神经脱髓鞘形成的进展性、 退化性神经系统疾病。
诊断:
由于本病临床表现无特异,发病 率低,特别是仅有脑部或周围神经症状 时,易误诊为病毒性脑炎、多发性硬化 症、多发性周围神经病等。因此,如有 以上临床特点,均应考虑到本病的可能 ,及时行生化及影像学检查,必要时行 病理或基因检查。
诊断:
生化检测:尿沉渣发现大量异染颗粒可初步诊断。检测血白细胞及皮肤成纤维细胞 中ARSA活性可确诊本病。
磁共振质子波谱(MRS)表现可以反映MLD脑内异常病理及生化改变,MRS能够在MLD脑组 织结构改变之前发现生化代谢的异常,敏感性较好,对于MLD的早期诊断有积极的意义。ML D此病也可能累及患者的肾、胆囊、肝等,胆囊超声的异常可作为本病辅助的临床诊断,与 其他类型的脑白质营养不良相鉴别。
病理及其他检查:
