最新厦门大学结构化学习题集
结构化学考试题库 含具体答案

结构化学考试题库1第一部分量子力学基础与原子结构一、单项选择题(每小题1分)1.一维势箱解的量子化由来()①人为假定②求解微分方程的结果③由势能函数决定的④由微分方程的边界条件决定的。
答案:④2.下列算符哪个是线性算符()①exp ②▽2③sin④答案:②3.指出下列哪个是合格的波函数(粒子的运动空间为0+)()①sinx②e -x③1/(x-1)④f(x)=e x (0x 1);f(x)=1(x 1)答案:②4.基态氢原子径向分布函数D(r)~r 图表示()①几率随r 的变化②几率密度随r 的变化③单位厚度球壳内电子出现的几率随r 的变化④表示在给定方向角度上,波函数随r 的变化答案:③5.首先提出微观粒子的运动满足测不准原理的科学家是()①薛定谔②狄拉克③海森堡③波恩答案:③6.立方势箱中22810ma hE <时有多少种状态()①11②3③7④2答案:③7.立方势箱在22812ma h E ≤的能量范围内,能级数和状态数为()①5,20②6,6③5,11④6,17答案:③8.下列函数哪个是22dx d 的本征函数()①mxe②sin 2x ③x 2+y 2④(a-x)e -x答案:①9.立方势箱中2287ma h E <时有多少种状态()①11②3③4④2答案:③10.立方势箱中2289ma h E <时有多少种状态()①11②3③4④2答案:③11.已知xe 2是算符x P ˆ的本征函数,相应的本征值为()①ih2②i h 4③4ih ④ i h答案:④12.已知2e 2x 是算符x i ∂∂-的本征函数,相应的本征值为()①-2②-4i③-4ih④-ih/π答案:④13.下列条件不是品优函数必备条件的是()①连续②单值③归一④有限或平方可积答案:③14.下列函数中22dx d ,dx d的共同本征函数是()①coskx②xe-bx③e-ikx④2ikxe-答案:③215.对He +离子而言,实波函数||m nl ψ和复波函数nlm ψ,下列哪个结论不对()①函数表达式相同②E 相同③节面数相同④M 2相同答案:①16.氢原子基态电子几率密度最大的位置在r =()处①0②a 0③∞④2a 0答案:①17.类氢体系m43ψ的简并态有几个()①16②9③7④3答案:①18.对氢原子和类氢离子的量子数l ,下列叙述不正确的是()1l 的取值规定了m 的取值范围2它的取值与体系能量大小有关3它的最大取值由解R 方程决定4它的取值决定了轨道角动量M 的大小答案:②19.对He +离子实波函数py2ψ和复波函数121-ψ,下列结论哪个不对()①Mz 相同②E 相同③M 2相同④节面数相同答案:①20.对氢原子实波函数px2ψ和复波函数211ψ,下列哪个结论不对()①M 2相同②E 相同③节面数相同④Mz 相同答案:④21.He +体系321ψ的径向节面数为()①4②1③2④0答案:④22.Li 2+体系3p ψ的径向节面数为()①4②1③2④0答案:②23.类氢离子体系Ψ310的径向节面数为()①4②1③2④0答案:②24.若l =3,则物理量M z 有多少个取值()①2②3③5④7答案:④25.氢原子的第三激发态是几重简并的()①6②9③12④16答案:④26.由类氢离子薛定谔方程到R ,H ,Ф方程,未采用以下那种手段()①球极坐标变换②变量分离③核固定近似④线性变分法答案:④27.电子自旋是()①具有一种顺时针或逆时针的自转②具有一种类似地球自转的运动③具有一种非空间轨道运动的固有角动量④因实验无法测定,以上说法都不对。
有机化学习题与答案(厦门大学)

有机化学习题与答案(厦门大学)work Information Technology Company.2020YEAR有机化学习题与答案(厦门大学)第一章绪论习题一、根据下列电负性数据:判断下列键中哪个极性最强为什么答案 <请点击>二、(a) F2、HF、BrCl、CH4、CHCl3、CH3OH诸分子中哪些具有极性键?(b) 哪些是极性分子答案 <请点击>三、下列各化合物有无偶极矩?指出其方向。
答案 <请点击>四、根据O和S的电负性差别,H2O和H2S相比,哪个的偶极-偶极吸引力较强,哪个的氢键较强?答案 <请点击>五、写出下列化合物的路易斯电子式。
答案 <请点击>六、把下列化合物由键线式改写成结构简式。
七、下面记录了化合物的元素定量分析和相对分子质量测定的结果,请计算它们的化学式。
(1) C:65.35%,H:5.60%,相对分子质量 110(2) C:70.40%,H:4.21%,相对分子质量 188(3) C:62.60%,H:11.30%,N:12.17%,相对分子质量 230(4) C:54.96%,H:9.93%,N:10.68%,相对分子质量 131(5) C:56.05%,H:3.89%,Cl:27.44%,相对分子质量 128.5(6) C:45.06%,H:8.47%,N:13.16%,Cl:33.35%,相对分子质量 106.5答案 <请点击>八、写出下列化学式的所有的构造异构式。
答案 <请点击>第一章绪论习题(1)1、什么是烃、饱和烃和不饱和烃?点击这里看结果2、什么是烷基?写出常见的烷基及相应的名称。
点击这里看结果3、给下列直链烷烃用系统命名法命名点击这里看结果4、什么是伯、仲、叔、季碳原子,什么是伯、仲、叔氢原子?点击这里看结果5、写出己烷的所有异构体,并用系统命名法命名。
点击这里看结果6、写出符合下列条件的烷烃构造式,并用系统命名法命名:1.只含有伯氢原子的戊烷2.含有一个叔氢原子的戊烷3.只含有伯氢和仲氢原子的已烷4.含有一个叔碳原子的已烷5.含有一个季碳原子的已烷6.只含有一种一氯取代的戊烷7.只有三种一氯取代的戊烷8.有四种一氯取代的戊烷9.只有二种二氯取代的戊烷点击这里看结果7、写出2-甲基丁烷和2,2,4-三甲基戊烷的可能一氯取代物的结构式,并用系统命名法命名。
结构化学考试题库 含具体答案

结构化学考试题库1第一部分量子力学基础与原子结构一、单项选择题(每小题1分)1.一维势箱解的量子化由来()①人为假定②求解微分方程的结果③由势能函数决定的④由微分方程的边界条件决定的。
答案:④2.下列算符哪个是线性算符()①exp ②▽2③sin④答案:②3.指出下列哪个是合格的波函数(粒子的运动空间为0+)()①sinx②e -x③1/(x-1)④f(x)=e x (0x 1);f(x)=1(x 1)答案:②4.基态氢原子径向分布函数D(r)~r 图表示()①几率随r 的变化②几率密度随r 的变化③单位厚度球壳内电子出现的几率随r 的变化④表示在给定方向角度上,波函数随r 的变化答案:③5.首先提出微观粒子的运动满足测不准原理的科学家是()①薛定谔②狄拉克③海森堡③波恩答案:③6.立方势箱中22810ma hE <时有多少种状态()①11②3③7④2答案:③7.立方势箱在22812ma h E ≤的能量范围内,能级数和状态数为()①5,20②6,6③5,11④6,17答案:③8.下列函数哪个是22dx d 的本征函数()①mxe②sin 2x ③x 2+y 2④(a-x)e -x答案:①9.立方势箱中2287ma h E <时有多少种状态()①11②3③4④2答案:③10.立方势箱中2289ma h E <时有多少种状态()①11②3③4④2答案:③11.已知xe 2是算符x P ˆ的本征函数,相应的本征值为()①ih2②i h 4③4ih ④ i h答案:④12.已知2e 2x 是算符x i ∂∂-的本征函数,相应的本征值为()①-2②-4i③-4ih④-ih/π答案:④13.下列条件不是品优函数必备条件的是()①连续②单值③归一④有限或平方可积答案:③14.下列函数中22dx d ,dx d的共同本征函数是()①coskx②xe-bx③e-ikx④2ikxe-答案:③215.对He +离子而言,实波函数||m nl ψ和复波函数nlm ψ,下列哪个结论不对()①函数表达式相同②E 相同③节面数相同④M 2相同答案:①16.氢原子基态电子几率密度最大的位置在r =()处①0②a 0③∞④2a 0答案:①17.类氢体系m43ψ的简并态有几个()①16②9③7④3答案:①18.对氢原子和类氢离子的量子数l ,下列叙述不正确的是()1l 的取值规定了m 的取值范围2它的取值与体系能量大小有关3它的最大取值由解R 方程决定4它的取值决定了轨道角动量M 的大小答案:②19.对He +离子实波函数py2ψ和复波函数121-ψ,下列结论哪个不对()①Mz 相同②E 相同③M 2相同④节面数相同答案:①20.对氢原子实波函数px2ψ和复波函数211ψ,下列哪个结论不对()①M 2相同②E 相同③节面数相同④Mz 相同答案:④21.He +体系321ψ的径向节面数为()①4②1③2④0答案:④22.Li 2+体系3p ψ的径向节面数为()①4②1③2④0答案:②23.类氢离子体系Ψ310的径向节面数为()①4②1③2④0答案:②24.若l =3,则物理量M z 有多少个取值()①2②3③5④7答案:④25.氢原子的第三激发态是几重简并的()①6②9③12④16答案:④26.由类氢离子薛定谔方程到R ,H ,Ф方程,未采用以下那种手段()①球极坐标变换②变量分离③核固定近似④线性变分法答案:④27.电子自旋是()①具有一种顺时针或逆时针的自转②具有一种类似地球自转的运动③具有一种非空间轨道运动的固有角动量④因实验无法测定,以上说法都不对。
《结构化学》(1-5章)习题答案

目录第一章答案----------------------------------------------------------------------------1 第二章答案---------------------------------------------------------------------------26 第三章答案---------------------------------------------------------------------------47 第四章答案---------------------------------------------------------------------------63 第五章答案---------------------------------------------------------------------------711《结构化学》第一章习题答案1001 (D) 1002 E =h ν p =h /λ 1003,mvh p h ==λ 小 1004 电子概率密度 1005 1-241-9--34s kg m 10626.6s kg m 100.1106.626⋅⋅⨯=⋅⋅⨯⨯==-λhp T = m p 22 = 3123410109.92)10626.6(--⨯⨯⨯ J = 2.410×10-17J 1006 T = h ν- h ν0=λhc -0λhcT = (1/2) mv 2 v =)11(20λλ-m hc = 6.03×105 m ·s -11007 (1/2)mv 2= h ν - W 0 = hc /λ - W 0 = 2.06×10-19 J v = 6.73×105 m/s 1008 λ = 1.226×10-9m/10000= 1.226×10-11 m 1009 (B) 1010 A,B 两步都是对的, A 中v 是自由粒子的运动速率, 它不等于实物波的传播速率u , C 中用了λ= v /ν,这就错了。
结构化学章节习题(含答案!)

第一章 量子力学基础一、单选题: 13x lπ为一维势箱的状态其能量是:( a ) 22229164:; :; :; :8888h h h hA B C D ml ml ml ml2、Ψ321的节面有( b )个,其中( b )个球面。
A 、3 B 、2 C 、1 D 、03、立方箱中2246ml h E ≤的能量范围内,能级数和状态数为( b ).A.5,20B.6,6C.5,11D.6,174、下列函数是算符d /dx的本征函数的是:( a );本征值为:( h )。
A 、e 2xB 、cosXC 、loge xD 、sinx 3E 、3F 、-1G 、1H 、2 5、下列算符为线性算符的是:( c )A 、sine xB 、d 2/dx 2 D 、cos2x6、已知一维谐振子的势能表达式为V = kx 2/2,则该体系的定态薛定谔方程应当为( c )。
A [-m 22 2∇+21kx 2]Ψ= E ΨB [m 22 2∇- 21kx 2]Ψ= E Ψ C [-m 22 22dx d +21kx 2]Ψ= E Ψ D [-m 22 -21kx 2]Ψ= E Ψ 7、下列函数中,22dx d ,dxd的共同本征函数是( bc )。
A cos kxB e –kxC e –ikxD e –kx2 8、粒子处于定态意味着:( c )A 、粒子处于概率最大的状态B 、粒子处于势能为0的状态C 、粒子的力学量平均值及概率密度分布都与时间无关系的状态.D 、粒子处于静止状态9、氢原子处于下列各状态 (1)ψ2px (2) ψ3dxz (3) ψ3pz (4) ψ3dz 2 (5)ψ322 ,问哪些状态既是M 2算符的本征函数,又是M z 算符的本征函数?( c )A. (1) (3)B. (2) (4)C. (3) (4) (5)D. (1) (2) (5) 10、+He 离子n=4的状态有( c )(A )4个 (B )8个 (C )16个 (D )20个 11、测不准关系的含义是指( d ) (A) 粒子太小,不能准确测定其坐标; (B)运动不快时,不能准确测定其动量(C) 粒子的坐标的动量都不能准确地测定; (D )不能同时准确地测定粒子的坐标与动量12、若用电子束与中子束分别作衍射实验,得到大小相同的环纹,则说明二者( b ) (A) 动量相同 (B) 动能相同 (C) 质量相同13、 为了写出一个经典力学量对应的量子力学算符,若坐标算符取作坐标本 身,动量算符应是(以一维运动为例) ( a )(A) mv (B) i x ∂∂ (C)222x ∂-∂14、若∫|ψ|2d τ=K ,利用下列哪个常数乘ψ可以使之归一化:( c )(A) K (B) K 2 (C) 1/K15、丁二烯等共轭分子中π电子的离域化可降低体系的能量,这与简单的一维势阱模型是一致的, 因为一维势阱中粒子的能量 ( b )(A) 反比于势阱长度平方 (B) 正比于势阱长度 (C) 正比于量子数16、对于厄米算符, 下面哪种说法是对的 ( b )(A) 厄米算符中必然不包含虚数 (B) 厄米算符的本征值必定是实数(C) 厄米算符的本征函数中必然不包含虚数17、对于算符Ĝ的非本征态Ψ ( c )(A) 不可能测量其本征值g . (B) 不可能测量其平均值<g >.(C) 本征值与平均值均可测量,且二者相等18、将几个非简并的本征函数进行线形组合,结果 ( b )(A) 再不是原算符的本征函数(B) 仍是原算符的本征函数,且本征值不变 (C) 仍是原算符的本征函数,但本征值改变19. 在光电效应实验中,光电子动能与入射光的哪种物理量呈线形关系:( B )A .波长B. 频率C. 振幅20. 在通常情况下,如果两个算符不可对易,意味着相应的两种物理量( A)A .不能同时精确测定B .可以同时精确测定C .只有量纲不同的两种物理量才不能同时精确测定 21. 电子德布罗意波长为(C )A .λ=E /h B. λ=c /ν C. λ=h /p 22. 将几个非简并的本征函数进行线形组合,结果( A ) A .再不是原算符的本征函数B .仍是原算符的本征函数,且本征值不变C .仍是原算符的本征函数,但本征值改变23. 根据能量-时间测不准关系式,粒子在某能级上存在的时间τ越短,该能级的不确定度程度ΔE (B )A .越小 B. 越大 C.与τ无关24. 实物微粒具有波粒二象性, 一个质量为m 速度为v 的粒子的德布罗意波长为:A .h/(mv)B. mv/hC. E/h25. 对于厄米算符, 下面哪种说法是对的 ( B )A .厄米算符中必然不包含虚数B .厄米算符的本征值必定是实数C .厄米算符的本征函数中必然不包含虚数 26. 对于算符Ĝ的非本征态Ψ (A ) A .不可能测得其本征值g. B .不可能测得其平均值<g>.C .本征值与平均值均可测得,且二者相等 27. 下列哪一组算符都是线性算符:( C )A . cos, sinB . x, logC . x d dx d dx,,22二 填空题1、能量为100eV 的自由电子的德布罗依波波长为( 122.5pm )2、函数:①xe ,②2x ,③x sin 中,是算符22dxd 的本征函数的是( 1,3 ),其本征值分别是( 1,—1;)3、Li 原子的哈密顿算符,在( 定核 )近似的基础上是:(()23213212232221223222123332ˆr e r e r e r e r e r e mH +++---∇+∇+∇-= )三 简答题1.计算波长为600nm(红光),550nm(黄光),400nm(蓝光)和200nm(紫光)光子的能量。
厦门大学结构化学第4章答案

第三章所给答案中,IF 5是四方锥构型,所以点群为C 4v ,大家更正一下!第一次作业:4-24.2. 对H 2+体系,根据极值条件: , 以及22112222112222aa ab bb aa ab bbc H c c H c H c S c c S c S ε++=++ 导出 解:参考书本《结构化学》厦大版,P97。
22112222112222aa ab bb aa ab bb c H c c H c H YE c S c c S c S Z++==++ …… (1) 2211122211;E Y Y Z E Y Y Z c Z c Z c c Z c Z c ∂∂∂∂∂∂=-=-∂∂∂∂∂∂ …….(2) 又 ,有:11220;0Y Z Y Z E E c c c c ∂∂∂∂-=-=∂∂∂∂ (3)且12122aa ab Y c H c H c ∂=+∂,12122aa abZ c S c S c ∂=+∂;12222ab bb Y c H c H c ∂=+∂, 12222ab bb Z c S c S c ∂=+∂ …… (4) 将(4)代入(3),可导出:第二次作业:4.3, 4.5, 4.6, 4.134.3、比较O 22+、O 2 、O 2-、O 22- 的键长及磁性,并按顺序排列。
解:比较键长从键级的角度分析,键级: 磁性考虑分子是否存在单电子,存在单电子则为顺磁性,不存在单电子则为反磁性的。
(具体原因可参考分子磁性的研究论文)上述各分子的电子组态:O 22+: O 2: O 2-: O 22-: 所以:12()()0aa aa ab ab c H ES c H ES -+-=12()()0ab ab bb bb c H ES c H ES -+-=10c ε∂=∂20c ε∂=∂10E c ∂=∂20Ec ∂=∂12()()0aa aa ab ab c H ES c H ES -+-=12()()0ab ab bb bbc H ES c H ES -+-=1(*)2b n n =-22242222()()()()s s p p KK σσσπ*2224222222()()()()()s s p p p KK σσσππ**2224322222()()()()()s s p pp KK σσσππ**2224422222()()()()()s s p p p KK σσσππ**4-5 根据N 2+、N 2、N 2- 的电子组态,预测各体系N-N 键长度,并比较它们的稳定性。
厦门大学结构化学答案2

1.9 用测不准原理说明普通光学光栅(间隙约 10-6m)观 察不到 10000V 电压加速的电子衍射。(1 eV = 1.602x10-19 J ) 解:发生电子衍射时,电子动量的不确定度在数量级上 与电子动量是相近的,由测不准原理可知电子位置的不确定 度:
∆ ≈
ℎ ℎ ℎ = = = ∆ ℎ/
显然,光学光栅的宽度要远大于电子的德布罗意波长, 观察不到电子衍射。
1.12 判断下列算符是否是线性厄米算符: (1)d/dx (2)∇2 (3)x1+x2 (4)e x2 解:线性算符的定义为 (φ1 + φ2)= φ1 + φ2 φ
∗
厄米算符的定义为 ∫ φ∗ φ dτ=∫ φ
dτ
线性算符比较好判定,证明是否为厄米算符。 (1) ∫ φ∗ φ d =∫ φ∗ dφ = φ∗ φ | − ∫ φ dφ∗ = φ∗ d φ∗ d
习题 2
1.8 质量0.004kg子弹以500m/s速率运动,原子中的电子以 1000m/s速率运动,试估计它们位置的不确定度,证明子弹有确 定的运动轨道, 可用经典力学处理, 而电子运动需量子力学处理。 解:(注: 因题中为给出速率的不确定度,所以,可以自行 引入此量,可取范围显然在0-100%之间,可以取中间量10%,由此 导出动量的不确定度, 以进一步由测不准原理导出位置的不确定 度的数量级) 若假定速率的不准确度为10%, 对子弹而言:ΔPx=mΔVx=m(10%Vx)=0.2kg·m/s Δx≈h/ΔPx=3.31 × 10−33m 对电子而言:Δx≈h/ΔPx=h/[m(10%Vx)]=7.28 × 10−7m 可以看出,子弹位置的不确定度比子弹小得多,完全可以 忽略,所以子弹可用经典力学处理;而电子位置的不确定度与分 子尺寸(10−10m)相比,根本不能忽略,所以电子运动需要用量子 力学处理。
厦门大学结构化学习题集

结构化学习题集习题1:1.1 某同步加速器,可把质子加速至具有100×109eV的动能,试问此时质子速度多大?1.2 计算波长为600nm(红光),550nm(黄光),400nm(蓝光)和200nm(紫光)光子的能量。
1.3 在黑体辐射中,对一个电热容器加热到不同温度,从一个针孔辐射出不同波长的极大值,试从其推导Planck常数的数值:T/℃1000 1500 2000 2500 3000 3500l max/nm 2181 1600 1240 1035 878 7631.4 计算下列粒子的德布洛意波长(1) 动能为100eV的电子;(2) 动能为10eV的中子;(3) 速度为1000m/s的氢原子.1.5 质量0.004kg子弹以500ms-1速度运动,原子中的电子以1000ms-1速度运动,试估计它们位置的不确定度, 证明子弹有确定的运动轨道, 可用经典力学处理, 而电子运动需量子力学处理。
1.6 用测不准原理说明普通光学光栅(间隙约10-6m)观察不到10000V 电压加速的电子衍射。
1.7 小球的质量为2mg,重心位置可准确到2μm,在确定小球运动速度时,讨论测不准关系有否实际意义?1.8 判断下列算符是否是线性\厄米算符:(1)(2)(3)x1+x2(4)1.9 下列函数是否是的本征函数?若是,求其本征值:(1)exp(ikx)(2)coskx (3)k (4)kx1.10 氢原子1s态本征函数为(a0为玻尔半径),试求1s 态归一化波函数。
1.11 已知一维谐振子的本征函数为其中a n和α都是常数,证明n=0与n=1时两个本征函数正交。
1.12 若是算符的本征函数(B为常数), 试求α值,并求其本征值。
1.13 计算Poisson 方括,1.14 证明Poisson 方括的下列性质:(1)(2)1.15 角动量算符定义为:, ,证明: (1) (2)1.16 在什么条件下?有无定值。
结构化学期考

原子轨道形成的?(请标注出 m 和 n 的值) (3) 试判明下列分子的几何构型、所属点群及中心原子的杂化形式:(a) XeF4, (b)BrF3; (c) SF4 (4)已知 I2 离子在某些离子化合物晶体中可以形成如下图所示的二聚体结构 (I42+) ,试运用前线分子轨道理论分析其离子间的化学键。
1
三. (20%)试运用休克尔分子轨道理论近似确定分子 H3+、H3、H3-的最稳定 构型是三角形还是直线型,请注意必须分别计算出三种分子在各种构型中的能 量并作比较。 四. (20%)已知正常的铜晶体属于面心立方,晶胞参数 a = 361.5 pm,铜原 子量为 64, (1) 试求晶体的密度及晶体中最短的原子间距;
厦门大学《结构化学》课程试卷
____学院____系____年级____专业 主考教师:____试卷类型: (A 卷/B 卷)
一. (16%) (1)对于极性双原子分子 AB,如果分子轨道中的一个电子有 81% 的时间在 A 原子轨道a 上,19%的时间在 B 的原子轨道b 上,若不考虑原子轨 道的重叠,试写出该分子轨道波函数的形式。 ( 2 )下列四个氯化物中,哪个氯的活泼性最差?并说明理由。 (a) C6H5Cl , (b) C2H5Cl, (c) CH2═CH—CH2Cl,(d) C6H5CH2Cl。 (3)在正方形过渡金属配合物中,若四个配位体分别位于 x 轴和 y 轴上,试判 断中心金属原子的价层 d 原子轨道中哪个轨道的能级最高?并说明判断理由。 (4)已知离子化合物 AB 的晶体属于正交底心,每个晶胞有两个 A 原子和两个 B 原子,两个 A 原子的分数坐标分别是(0,0,0)和(1/2,1/2,0),一个 B 原子的分数 坐标是(1/4,1/4,1/2),试推导出另一个 B 原子的分数坐标, 并据此画出其晶胞。 二. (24%) (1)应用 18 电子规则,算出羰基配合物 Mn(C5H5)(CO)x 中 x 的值,并画出它的 结构。 (2)已知 Hg 原子价层电子层排布:5d106s2,试分析 HgCl2 分子的成键情况:
结构化学试题收集

2001年三、填空题(8分)1、一维势箱中的粒子, 已知, 处于基态时在_____1/2_____处几率密度最大。
2、既具有偶极矩, 又具有旋光性的分子必属于______Cn______________分子点群。
3、B5H9分子中除存在正常B-H键外,还存在3c-2e 桥键和5c-6e硼键。
4、若c轴为21螺旋轴,则点(x,y,z)由此21螺旋轴相联系的等效点坐标为(-x,-y, ?+z) 。
5、A3型密堆积可抽象出晶胞,含个球,个结构基元,该晶胞的特征对称元素为。
6、一个配位多面体结构中,共边连接和共面连接会使结构的稳定性。
7、将晶体中可能存在的各种宏观对称元素通过一个点尽可能组合可得到32;晶体的微观对称元素组合可得到230个;他们分属7大;有14种。
8、离子极化现象将使离子键向过渡。
9、1,3,5-己三烯的合环反应,在加热条件下为旋关环。
四、1.S1P2组态的基谱项是: (a) 4P1/2 (b) 4P5/2 (c) 4D1/2 (d) 4D5/22、已知径向分布函数为D(x), 则电子出现在半径r=xnm, 厚度为1 nm的球壳内的几率P为:(a). P=D(X+1)-D(x); (b)P=D(r)dr (c). P=D(X+1) (d).P= D (r)r2sin θdrdθd3.按价电子对互斥理论哪个分子呈四面体形状(a).XeF4 (b). XeO4 (c). ICl4- (d). BrF4-4.平面四方形配位场中d轨道裂分为几个能级? (a).2 (b). 3 (c).4 (d). 55.哪个分子磁性最大?(a).Fe(H2O)63+ (b). Fe(CN)64- (c). Mn(H2O)63+ (d). Co(NH3)3+6、氢的成键型式可包括:(a)金属键 (b). 氢键 (c). 氢分子配键 (d). 离子键7. 下列哪些分子中形成π34 离域键 (a).NO2 (b). O3 (c). H2C=CH=Cl (d). CH2=CH-CH2+8、径向分布函数是指:(a)R2 (b)R2dr (c)r2R2 (d)r2R2dr五、计算题(12分)NH4Cl 为简单立方点阵结构,晶胞中包含1个NH4+和1个Cl-,晶胞参数a = 387 pm。
厦门大学结构化学答案

5.2 从原子轨道 ??s 和 ??Px 的正交性,证明两个 sp 杂化轨道相互正交。
?1= √?? ??+ √1- ?? ???????? ?2= √1- ??- √?? ???? ????证明:h 1h 2d(s 1px )(1spx)d(1 ) s 2d(1) px 2d(1)2s px d( )2s pxd(1 ) (1 ) 0 0 0即 h 1 和 h 2 正交 , 证毕。
5.3 写出下列分子或离子中,中心原子所采用的杂化轨道:分子或离子几何构型 中心原子的杂化轨道CS 2 直线形 sp NO 2+直线形 sp NO 3- 正三角形 sp 2CO 3 -正三角形 sp 2BF 3 正三角形 sp 2CBr 4正四面体 sp 3+ 正四面体 3PF 4sp IF 6+八面体sp 3d 25.6 实验测定水分子的∠ HOH 为 104.5°,试计算 O-H 键与孤对电子杂化轨道中s 、p 轨道的成分。
解:H 2O 分子中 O 原子取不等性 sp3 杂化,两个 OH 键所涉及的 O 原子杂化轨道的夹角 θ满足: α+ βcos θ= 0式中 α、β分别为杂化轨道中 s 、p 轨道所占有的百分数。
又有 β=1-α, 故有:α+ ( 1 - α) cos104.5 =°0得: α= 0.20,β= 1 - α= 0.80即每个 O-H 键中 O 2s成分为 0.20,2p 成分为 0.80;水分子还有两个孤对电子杂化轨道,则每个孤对电子杂化轨道中,2s 轨道成分为:(1.0-2x0.20)/2= 0.302p 轨道成分为: 1.0-0.3= 0.70或(3.0-2x0.8) /2 = 0.70即水分子的孤对电子杂化轨道中s 成分占0.30, p 成分占0.70。
5.12 对于极性分子 AB,如果分子轨道中的一个电子有90%的时间在 A 原子轨道上, 10%的时间在 B 的原子轨道 ?? 上,试描述该分子轨道波函数的形式(此??????处不考虑原子轨道的重叠)解:根据分子轨道理论可设该分子轨道波函数形式为= a??+ b ?? ,该????122φ φ dτ 0轨道满足归一性要求:2 dτ a bA B故 b1a2依题意有: a2 =0.9, b2=0.1,故可知 : a0.9, b0.1所以,波函数= 0.949??0.316??????。
结构化学考试题库 含具体答案

结构化学考试题库1第一部分量子力学基础与原子结构一、单项选择题(每小题1分)1.一维势箱解的量子化由来()①人为假定②求解微分方程的结果③由势能函数决定的④由微分方程的边界条件决定的。
答案:④2.下列算符哪个是线性算符()①exp ②▽2③sin④答案:②3.指出下列哪个是合格的波函数(粒子的运动空间为0+)()①sinx②e -x③1/(x-1)④f(x)=e x (0x 1);f(x)=1(x 1)答案:②4.基态氢原子径向分布函数D(r)~r 图表示()①几率随r 的变化②几率密度随r 的变化③单位厚度球壳内电子出现的几率随r 的变化④表示在给定方向角度上,波函数随r 的变化答案:③5.首先提出微观粒子的运动满足测不准原理的科学家是()①薛定谔②狄拉克③海森堡③波恩答案:③6.立方势箱中22810ma hE <时有多少种状态()①11②3③7④2答案:③7.立方势箱在22812ma h E ≤的能量范围内,能级数和状态数为()①5,20②6,6③5,11④6,17答案:③8.下列函数哪个是22dx d 的本征函数()①mxe②sin 2x ③x 2+y 2④(a-x)e -x答案:①9.立方势箱中2287ma h E <时有多少种状态()①11②3③4④2答案:③10.立方势箱中2289ma h E <时有多少种状态()①11②3③4④2答案:③11.已知xe 2是算符x P ˆ的本征函数,相应的本征值为()①ih2②i h 4③4ih ④ i h答案:④12.已知2e 2x 是算符x i ∂∂-的本征函数,相应的本征值为()①-2②-4i③-4ih④-ih/π答案:④13.下列条件不是品优函数必备条件的是()①连续②单值③归一④有限或平方可积答案:③14.下列函数中22dx d ,dx d的共同本征函数是()①coskx②xe-bx③e-ikx④2ikxe-答案:③215.对He +离子而言,实波函数||m nl ψ和复波函数nlm ψ,下列哪个结论不对()①函数表达式相同②E 相同③节面数相同④M 2相同答案:①16.氢原子基态电子几率密度最大的位置在r =()处①0②a 0③∞④2a 0答案:①17.类氢体系m43ψ的简并态有几个()①16②9③7④3答案:①18.对氢原子和类氢离子的量子数l ,下列叙述不正确的是()1l 的取值规定了m 的取值范围2它的取值与体系能量大小有关3它的最大取值由解R 方程决定4它的取值决定了轨道角动量M 的大小答案:②19.对He +离子实波函数py2ψ和复波函数121-ψ,下列结论哪个不对()①Mz 相同②E 相同③M 2相同④节面数相同答案:①20.对氢原子实波函数px2ψ和复波函数211ψ,下列哪个结论不对()①M 2相同②E 相同③节面数相同④Mz 相同答案:④21.He +体系321ψ的径向节面数为()①4②1③2④0答案:④22.Li 2+体系3p ψ的径向节面数为()①4②1③2④0答案:②23.类氢离子体系Ψ310的径向节面数为()①4②1③2④0答案:②24.若l =3,则物理量M z 有多少个取值()①2②3③5④7答案:④25.氢原子的第三激发态是几重简并的()①6②9③12④16答案:④26.由类氢离子薛定谔方程到R ,H ,Ф方程,未采用以下那种手段()①球极坐标变换②变量分离③核固定近似④线性变分法答案:④27.电子自旋是()①具有一种顺时针或逆时针的自转②具有一种类似地球自转的运动③具有一种非空间轨道运动的固有角动量④因实验无法测定,以上说法都不对。
结构化学习题集

结构化学习题集习题1:某同步加速器,可把质子加速至具有100×109eV的动能,试问此时质子速度多大?计算波长为600nm(红光),550nm(黄光),400nm(蓝光)和200nm(紫光)光子的能量。
在黑体辐射中,对一个电热容器加热到不同温度,从一个针孔辐射出不同波长的极大值,试从其推导Planck常数的数值:T/℃1000 1500 2000 2500 3000 3500l max/nm 2181 1600 1240 1035 878 763计算下列粒子的德布洛意波长(1) 动能为100eV的电子;(2) 动能为10eV的中子;(3) 速度为1000m/s的氢原子.质量0.004kg子弹以500ms-1速度运动,原子中的电子以1000ms-1速度运动,试估计它们位置的不确定度, 证明子弹有确定的运动轨道, 可用经典力学处理, 而电子运动需量子力学处理。
用测不准原理说明普通光学光栅(间隙约10-6m)观察不到10000V电压加速的电子衍射。
小球的质量为2mg,重心位置可准确到2μm,在确定小球运动速度时,讨论测不准关系有否实际意义?判断下列算符是否是线性\厄米算符:(1)(2)(3)x1+x2(4)下列函数是否是的本征函数?若是,求其本征值:(1)exp(ikx)(2)coskx (3)k (4)kx氢原子1s态本征函数为(a0为玻尔半径),试求1s态归一化波函数。
已知一维谐振子的本征函数为其中a n和α都是常数,证明n=0与n=1时两个本征函数正交。
若是算符的本征函数(B为常数), 试求α值,并求其本征值。
计算Poisson 方括,证明Poisson 方括的下列性质:(1)(2)角动量算符定义为:, ,证明: (1) (2)在什么条件下?设体系处于状态中,角动量和M Z有无定值。
若有其值是多少?若无,求其平均值。
已知一维势箱粒子的归一化波函数为n=1, 2, 3 ……(其中l为势箱长度)计算(1)粒子的能量(2)坐标的平均值(3)动量的平均值试比较一维势箱粒子(波函数同上题)基态(n=1)和第一激发态(n=2)在0.4l~0.6l区间内出现的几率。
2020年厦门大学结构化学习题集精品版

结构化学习题集习题1:1.1 某同步加速器,可把质子加速至具有100×109eV的动能,试问此时质子速度多大?1.2 计算波长为600nm(红光),550nm(黄光),400nm(蓝光)和200nm(紫光)光子的能量。
1.3 在黑体辐射中,对一个电热容器加热到不同温度,从一个针孔辐射出不同波长的极大值,试从其推导Planck常数的数值:T/℃1000 1500 2000 2500 3000 3500l max/nm 2181 1600 1240 1035 878 7631.4 计算下列粒子的德布洛意波长(1) 动能为100eV的电子;(2) 动能为10eV的中子;(3) 速度为1000m/s的氢原子.1.5 质量0.004kg子弹以500ms-1速度运动,原子中的电子以1000ms-1速度运动,试估计它们位置的不确定度, 证明子弹有确定的运动轨道, 可用经典力学处理, 而电子运动需量子力学处理。
1.6 用测不准原理说明普通光学光栅(间隙约10-6m)观察不到10000V 电压加速的电子衍射。
1.7 小球的质量为2mg,重心位置可准确到2μm,在确定小球运动速度时,讨论测不准关系有否实际意义?1.8 判断下列算符是否是线性\厄米算符:(2)(3)x1+x2(4)(1)1.9 下列函数是否是的本征函数?若是,求其本征值:(1)exp(ikx)(2)coskx (3)k (4)kx1.10 氢原子1s态本征函数为(a0为玻尔半径),试求1s 态归一化波函数。
1.11 已知一维谐振子的本征函数为其中a n和α都是常数,证明n=0与n=1时两个本征函数正交。
1.12 若是算符的本征函数(B为常数), 试求α值,并求其本征值。
1.13 计算Poisson 方括,1.14 证明Poisson 方括的下列性质:(1)(2)1.15 角动量算符定义为:, ,证明: (1) (2)1.16 在什么条件下?有无定值。
厦门大学结构化学第1章答案

1.6 具有 0.2nm 波长的电子和光子,它们的动量和总能量各是多少? 解:微观粒子具有波粒二象性。对于一切粒子均满足: p
h
故: p
h
6.626 1034 3.31 1024 kg m s 1 10 2 10
31
①对于电子: me 9.11 10
1.9
用测不准原理说明普通光学光栅(间隙约 10-6m)观察不到 10000V 电压加速的电子衍射。 解: 根据不确定度关系,电子位置的不确定度为: ( px = 2meU 的理解?)
h h 6.626 1034 px 2meU 2 9.11 1031 1.602 1019 104 1.226 1011 x
34
J s , c 2.998 108 m s 1 )
代入各类波长,得到相应的光子能量。
E1 3.31 1019 J
E2 3.61 1019 J
E1 4.97 1019 J
E1 9.93 1019 J
1.4 某同步加速器,可把质子加速至具有 100×109eV 的动能,试问此时质子速度多大? 解: m p 1.67265 10
hc
T
hc
W
6.626 1034 2.998 108 4.2 2.0eV 2 107 1.602 1019
⑵ 当动能 T=0 时得到红限波长:
hc 6.626 1034 2.998 108 295.2nm W 4.2 1.602 1019
(这里积分得不到相对应的σ值, 需核实)
4
T
E (T )
结构化学复习题答案

结构化学复习题答案一、选择题1. 下列关于原子轨道的描述中,正确的是:A. s轨道是球形的B. p轨道是哑铃形的C. d轨道是花瓣形的D. f轨道是复杂的多叶形答案:A2. 根据价层电子对互斥理论,中心原子的杂化类型为sp^3d^2的分子几何构型是:A. 正四面体形B. 八面体形C. 正方形平面形D. 三角锥形答案:B3. 氢键是一种:A. 离子键B. 共价键C. 金属键D. 范德华力答案:D二、填空题1. 根据分子轨道理论,双原子分子的电子配置为\(\sigma_{1s}^{2}\sigma_{1s}^{*2}\sigma_{2s}^{2}\sigma_{2s}^{*2}\pi_{2p_{x}}^{2}\pi_{2p_{y}}^{2}\sigma_{2p_{z}}^{2}\),该分子的键级为________。
答案:三2. 原子半径的大小顺序一般为:同周期自左向右逐渐减小,同主族自上而下逐渐增大。
例如,钠(Na)的原子半径大于铝(Al),镁(Mg)的原子半径大于硫(S)。
答案:正确三、简答题1. 描述分子的极性是如何决定的。
答案:分子的极性由构成化学键的原子的电负性差异以及分子的空间构型决定。
如果构成化学键的原子电负性差异较大,形成的键将是极性键。
此外,即使键是极性的,如果分子的空间构型是对称的,如二氧化碳(CO2),分子整体也可能是非极性的。
2. 解释什么是配位数,并给出一个例子。
答案:配位数是指一个中心原子或离子周围直接相连的原子或离子的数量。
例如,在六水合铜(II)离子[Cu(H2O)6]^{2+}中,铜离子的配位数是6,因为它与六个水分子的氧原子直接相连。
四、计算题1. 计算甲烷(CH4)的键能,并估算其在25°C时的分解热。
答案:甲烷的键能可以通过计算C-H键的平均键能(大约为414kJ/mol)乘以4(因为甲烷中有四个C-H键)来估算。
分解热可以通过键能和反应中涉及的熵变来估算,但需要更详细的数据来进行精确计算。
厦门大学结构化学第3章答案

厦门大学结构化学第3章答案厦门大学结构化学第3章答案第3章习题答案总结3.1 寻找下列生活用品中所含的对称元素:剪刀、眼镜、铅笔(削过与未削)、书本、方桌。
解:对称元素:对称面、对称心、对称轴、映转轴。
(面、点、线)(,i,Cn,Sn)① 剪刀:对称轴(C2)、对称面(2个v) ② 眼镜:对称面( v)③铅笔(削过):对称面( 个v)、对称轴(C )④铅笔(未削):对称面( 个v, h)、对称心(i)、对称轴(C , 个C2)、映转轴(S ) ⑤书本:对称面(2个v, h)、对称心(i)、对称轴(C2主轴,2个C2轴) ⑥方桌:对称面(4个v)、对称轴(C4)3.2 CO和CO2都是直线型分子,试写出这两个分子各自的对称元素。
解:CO:对称元素:对称轴(C )、对称面( 个v)CO2(O=C=O)对称元素:对称轴(C , 个C2)、对称面( 个v,h)、对称心(i),映转轴(S )3.3 分别写出顺式和反式丁二稀分子的对称元素。
解:①顺式丁二烯:对称轴(C2),对称面(2个v)②反式丁二稀: 对称轴(C2),对称面( h),对称心(i) C2v C2h3.4 指出下列几何构型所含的对称元素,并确定其所属对称点群:(1)菱形(2) 蝶形(3)三棱柱(4) 四角锥(5) 圆柱体(6) 五棱台厦门大学结构化学第3章答案,试写出C2v点群的乘法表。
3.5 H2O属C2v点群,有4个对称元素:E、C2、v、v点群的乘法表:3.6 BF3为平面三角形分子,属D3h点群,请写出其12个对称元素,并将其分为6类。
解:BF3为平面三角形分子,属D3h点群对称元素:2C3,3C2, h,3 v,2S31215分类: E,C 3 , 3 ,C 2 2 , C 2 ,h,v , v v ,S3C,S3,C, 注:群中的对称元素可按相似变换分类。
相互共轭元素的一个集合构成群的一类。
即:K ( A ) g i ag i 1 ,gi跑遍所有的群元素。
厦门大学结构化学答案11
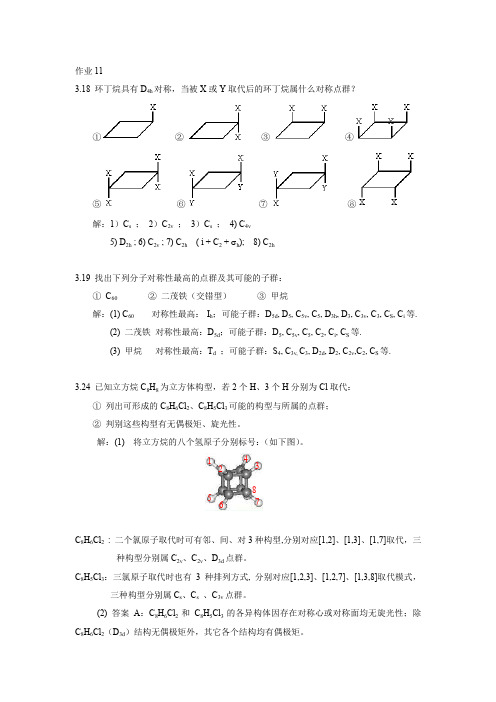
3.18 环丁烷具有D 4h 对称,当被X 或Y 取代后的环丁烷属什么对称点群?① ② ③ ④⑤ ⑥ ⑦ ⑧ 解:1)C s ; 2)C 2v ; 3)C s ; 4) C 4v5) D 2h ; 6) C 2v ; 7) C 2h ( i + C 2 + h ); 8) C 2h3.19 找出下列分子对称性最高的点群及其可能的子群:① C 60 ② 二茂铁(交错型) ③ 甲烷解:(1) C 60 对称性最高: I h ;可能子群:D 5d , D 5, C 5v , C 5, D 3h , D 3, C 3v , C 3, C S , C i 等.(2) 二茂铁 对称性最高:D 5d ;可能子群:D 5, C 5v , C 5, C 2, C i , C S 等.(3) 甲烷 对称性最高:T d ;可能子群:S 4, C 3v, C 3, D 2d , D 2, C 2v ,C 2, C S 等.3.24 已知立方烷C 8H 8为立方体构型,若2个H 、3个H 分别为Cl 取代:① 列出可形成的C 8H 6Cl 2、C 8H 5Cl 3可能的构型与所属的点群;② 判别这些构型有无偶极矩、旋光性。
解:(1) 将立方烷的八个氢原子分别标号:(如下图)。
C 8H 6Cl 2 : 二个氯原子取代时可有邻、间、对3种构型,分别对应[1,2]、[1,3]、[1,7]取代,三种构型分别属C 2v 、C 2v 、D 3d 点群。
C 8H 5Cl 3:三氯原子取代时也有3种排列方式, 分别对应[1,2,3]、[1,2,7]、[1,3,8]取代模式,三种构型分别属C s 、C s 、C 3v 点群。
(2) 答案A :C 8H 6Cl 2和C 8H 5Cl 3的各异构体因存在对称心或对称面均无旋光性;除C 8H 6Cl 2(D 3d )结构无偶极矩外,其它各个结构均有偶极矩。
1 2 34567 8偶极矩旋光性C8H6Cl21,2取代C2v有无1,3取代C2v有无1,7取代D3d无无C8H6Cl31,2,3取代C S有无1,2,5取代C S有无1,3,8取代C3v有无3.26 将分子或离子按下类条件归类:CH3CH3,NO2+, (NH2)2CO, C60,丁二烯,B(OH)3, CH4, 乳酸⑴既有极性又有旋光性⑵既无极性又无旋光性⑶无极性但有旋光性⑷有极性但无旋光性解:(1)有极性及旋光性: 乳酸(2)无极性无旋光性: C60, CH4, B(OH)3,反式丁二烯,NO2+,CH3CH3(3)无极性有旋光性: 乙烷(仅限具D3对称性的非平衡构象!!)(4)有极性无旋光性: (NH2)2CO。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
厦门大学结构化学习题集结构化学习题集习题1:1.1 某同步加速器,可把质子加速至具有100×109eV的动能,试问此时质子速度多大?1.2 计算波长为600nm(红光),550nm(黄光),400nm(蓝光)和200nm(紫光)光子的能量。
1.3 在黑体辐射中,对一个电热容器加热到不同温度,从一个针孔辐射出不同波长的极大值,试从其推导Planck常数的数值:T/℃ 1000 1500 2000 2500 3000 3500l max/nm 2181 1600 1240 1035 878 7631.4 计算下列粒子的德布洛意波长(1) 动能为100eV的电子;(2) 动能为10eV的中子;(3) 速度为1000m/s的氢原子.1.5 质量0.004kg子弹以500ms-1速度运动,原子中的电子以1000ms-1速度运动,试估计它们位置的不确定度, 证明子弹有确定的运动轨道, 可用经典力学处理, 而电子运动需量子力学处理。
1.6 用测不准原理说明普通光学光栅(间隙约10-6m)观察不到10000V 电压加速的电子衍射。
1.7 小球的质量为2mg,重心位置可准确到2μm,在确定小球运动速度时,讨论测不准关系有否实际意义?1.8 判断下列算符是否是线性\厄米算符:(1)(2)(3)x1+x2(4)1.9 下列函数是否是的本征函数?若是,求其本征值:(1)exp(ikx)(2)coskx (3)k (4)kx1.10 氢原子1s态本征函数为(a0为玻尔半径),试求1s 态归一化波函数。
1.11 已知一维谐振子的本征函数为其中a n和α都是常数,证明n=0与n=1时两个本征函数正交。
1.12 若是算符的本征函数 (B为常数), 试求α值,并求其本征值。
1.13 计算 Poisson 方括,1.14 证明Poisson 方括的下列性质:(1)(2)1.15 角动量算符定义为:, ,证明: (1) (2)1.16 在什么条件下?1.17 设体系处于状态中,角动量和M Z有无定值。
若有其值是多少?若无,求其平均值。
1.18 已知一维势箱粒子的归一化波函数为n=1, 2, 3 …… (其中l为势箱长度)计算 (1)粒子的能量 (2)坐标的平均值 (3)动量的平均值1.19 试比较一维势箱粒子(波函数同上题)基态(n=1)和第一激发态(n=2)在0.4l~0.6l区间内出现的几率。
1.20 当粒子处在三维立方势箱中(a=b=c),试求能量最低的前3个能级简并度。
1.21 写出一个被束缚在半径为a的圆周上运动的质量为m的粒子的薛定锷方程,求其解。
1.22 若用一维势箱自由粒子模拟共轭多烯烃中π电子, (a)丁二烯 (b)维生素A (c)胡萝卜素分别为无色、桔黄色、红色,试解释这些化合物的颜色。
1.23 若用二维箱中粒子模型, 将蒽(C14H10)的π电子限制在长700pm, 宽400pm的长方箱中,计算基态跃迁到第一激发态的波长.习题2:2.1 已知氢原子的归一化波函数为(1) 试求其基态能量和第一激发态能量。
(2)计算坐标与动量的平均值。
2.2 试求氢原子由基态跃迁到第一激发态(n=2)时光波的波长。
2.3 试证明氢原子1s轨道的径向分布函数极大值位于。
2.4 计算氢原子在和处的比值。
2.5 已知s和p z轨道角度分布的球谐函数分别为:,,试证明s和p z轨道相互正交。
2.6 试画出类氢离子和3d xy轨道轮廓,并指出其节面数及形状。
2.7 原子的5个d轨道能量本来是简并的,但在外磁场的作用下,产生Zeeman效应(能量分裂),试作图描述这种现象。
2.8 试证明球谐函数Y10、Y21、Y32是方程的本征函数。
2.9 已知氢原子2p z轨道波函数为①计算2p z轨道能量和轨道角动量;②计算电子离核的平均距离;③径向分布函数的极值位置。
2.10已知氢原子2s 轨道波函数为试求其归一化波函数。
2.11 类氢离子的1s轨道为:,试求径向函数极大值离核距离,试问He+与F6+的极大值位置。
2.12 证明类氢离子的电子离核的平均距离为2.13 写出Li2+离子的Schrödinger方程,说明各项的意义,并写出Li2+离子2s态的波函数①计算径向分布函数最大值离核距离;②计算1s电子离核的平均距离;③比较2s与2p态能量高低。
2.14 画出4f轨道的轮廓图, 并指出节面的个数与形状.2.15 写出Be原子的Schrödinger方程,计算其激发态2s12p1的轨道角动量与磁矩。
2.16 根据Slater规则, 说明第37个电子应填充在5s轨道,而不是4d 或4f轨道.2.17 已知N原子的电子组态为1s22s22p3①叙述其电子云分布特点;②写出N的基态光谱项与光谱支项;③写出激发态2p23s1的全部光谱项。
2.18 已知C原子与O原子电子组态分别为1s22s22p2与1s22s22p4,试用推导证明两种电子组态具有相同的光谱项,但具有不同的光谱支项,简要说明原因。
2.19 写出下列原子的基态光谱项与光谱支项:Al、S、K、Ti、Mn。
2.20 写出下列原子激发态的光谱项:C[1s22s22p13p1] Mg[1s22s22p63s13p1] Ti[1s22s22p63s23p63d34s1]2.21 基态Ni原子可能的电子组态为[Ar]3d84s2或[Ar]3d94s1。
由光谱实验测定能量最低的光谱项为3F4,试判断其属于哪种组态。
2.22 根据Slater规则,求Ca原子的第一、二电离能。
2.23 计算Ti原子第一、二电离能。
习题33.1 寻找下列生活用品中所含的对称元素:剪刀、眼镜、铅笔(削过与未削)、书本、方桌。
3.2 CO和CO2都是直线型分子,试写出这两个分子各自的对称元素。
3.3 分别写出顺式和反式丁二稀分子的对称元素。
3.4 指出下列几何构型所含的对称元素,并确定其所属对称点群:(1)菱形 (2) 蝶形 (3)三棱柱 (4) 四角锥 (5) 圆柱体 (6) 五棱台3.5 H 2O属C2v点群,有4个对称元素:E、C2、、,试写出C2v点群的乘法表。
3.6 BF3为平面三角形分子,属D3h点群,请写出其12个对称元素,并将其分为6类。
3.7 二氯乙烯属C 2h点群,有4个对称元素:E、C2、、i,试造出C2h点群的乘法表。
3.8 判断下列分子所属的点群:苯、对二氯苯、间二氯苯、氯苯、萘。
3.9 指出下列分子中的对称元素及其所属点群:SO2(V型)、P4(四面体)、PCl5(三角双锥)、S6(船型)、S8(冠状)、Cl2。
3.10 指出下列有机分子所属的对称点群:①②③④⑤3.11 对下列各点群加入或减少某些元素可得到什么群?① C3+i ② C3+s h③ T+i ④ D3d-i ⑤ D4h-σh3.12 试用对称操作的表示矩阵证明:⑴⑵⑶3.13 判断下列说法是否正确,并说明理由:(1). 凡是八面体配合物一定属于O h点群(2). 异核双原子分子一定没有对称中心(3). 凡是四面体构型分子一定属于T d点群(4). 在分子点群中,对称性最低的是C1,对称性最高的是O h群3.14 CoCl63+是八面体构型的分子,假设两个配位为F原子取代,形成CoCl4F2分子,可能属于什么对称点群?3.15 环丁烷具有D4h对称,当被X或Y取代后的环丁烷属什么对称点群?①②③④⑤⑥⑦⑧3.16 找出下列分子对称性最高的点群及其可能的子群:① C60②二茂铁(交错型)③甲烷3.17 根据偶极矩数据,推测分子立体构型及其点群:① C3O2(μ=0) ② H-O-O-H (μ=6.9×10-30C·m)③ H2N-NH2(μ=6.14×10-30C·m) ④ F2O (μ=0.9×10-30C·m)⑤N≡C-C≡N(μ=0)3.18 已知连接苯环上C-Cl键矩为5.17×10-30C·m,C-CH3键矩为-1.34×10-30C·m,试推算邻位、间位、对位C6H4ClCH3的偶极矩(实验值分别为4.15×10-30、5.49×10-30、6.34×10-30C·m)3.19 请判断下列点群有无偶极矩、旋光性:C i C nvD n D nd T d偶极矩旋光性3.20 指出下列分子所属的点群,并判断其有无偶极矩、旋光性①② IF5③环己烷(船式和椅式)④ SO42-(四面体)⑤(平面)⑥⑦ XeOF4(四方锥)⑧3.21 已知C6H5Cl 和C6H5NO2偶极矩分别为1.55D 和3.95D, 试计算下列化合物的偶极矩:(1) 邻二氯苯 (2) 间二硝基苯 (3) 对硝基氯苯 (4) 间硝基氯苯 (5) 三硝基苯3.22 已知立方烷C8H8为立方体构型,若2个H、3个H分别为Cl取代:①列出可形成的C8H6Cl2、C8H5Cl3可能的构型与所属的点群;②判别这些构型有无偶极矩、旋光性。
3.23 下列分子具有偶极矩,而不属于C nv群的是① H2O2 ② NH3③ CH2Cl2④H2C=CH23.24 下列各组分子或离子中,有极性但无旋光性是① N3-② I3-③ O33.25 由下列分子的偶极矩数据,推测分子的立体构型及所属的点群3.26 将分子或离子按下类条件归类:CH3CH3,NO2+, (NH2)2CO,C60,丁三烯,B(OH)3,CH4,乳酸⑴既有极性又有旋光性⑵既无极性有无旋光性⑶无极性但由旋光性⑷有极性但无旋光性3.27 对D6点群求出各表示的直积,并确定组成它们的不可约表示 A1×A2, A1×B1, B1×B2, E1×E23.28 分子属D2h点群,试写π电子组成的可约表示,并将其化成不可约表示的直和习题44.1 根据极值条件:,以及导出4.2 写出O2、O2-、O22-的键级、键长长短次序及磁性。
4.3 按分子轨道理论说明Cl2的化学键比Cl2+强还是弱?为什么?4.4 画出CN-的分子轨道能级示意图,写出基态的电子组态,计算键级及不成对电子数。
4.5 试用分子轨道理论讨论SO分子的电子结构,说明基态时有几个不成对电子?4.6 下列AB型分子:N2、NO 、O2 、C2、F2、CN、CO哪几个是得电子变为AB-后比原来中性分子能量低,哪几个是失电子变为AB+后比原来中性分子能量低?4.7 OH分子已在星际空间发现1)试按分子轨道理论只用氧原子2p轨道和氢原子的1s轨道叠加,写出其电子组态。
2)在哪个分子轨道中有不成对电子?3)此轨道是由氧和氢的原子轨道叠加形成,还是基本上定域于某个原子上?4)已知OH的第一电离能为13.2eV、HF为16.05eV,它们的差值几乎和O原子与F原子的第一电离能(15.8eV和18.6eV)的差值相同,为什么?4.8 用两种分子轨道记号写出O2的分子轨道。
