药物化学喹诺酮类抗菌药
喹诺酮类抗菌药物

环丙沙星
总结词
环丙沙星是一种广谱抗菌药物,主要用于治 疗呼吸道、胃肠道和泌尿生殖系统感染。
详细描述
环丙沙星对革兰氏阳性菌、革兰氏阴性菌和 厌氧菌等具有抗菌作用,可用于治疗肺炎、 支气管炎、急性呼吸道感染等呼吸道疾病,
以及胃肠道感染和泌尿生殖系统感染。
诺氟沙星
要点一
总结词
诺氟沙星是一种广谱抗菌药物,主要用于治疗胃肠道 感染和泌尿生殖系统感染。
01
研发新的喹诺酮类药物,以满 足临床对感染性疾病的治疗需 求。
02
针对现有喹诺酮类药物的不足 ,进行改进和优化,提高疗效 和安全性。
03
发掘新的喹诺酮类药物的作用 机制和靶点,以拓展其抗菌谱 和抗菌活性。
喹诺酮类药物与其他抗菌药物的联合应用
01
02
03
研究喹诺酮类药物与其他抗菌药物联 合应用的治疗方案,以提高抗菌效果 。
开展喹诺酮类药物合理使用和耐药性 监测的国际合作,共同应对抗菌药物 耐药性的挑战。
06
CATALOGUE
喹诺酮类药物的具体品种介绍
氟罗沙星
总结词
氟罗沙星是一种广谱抗菌药物,主要用于治 疗呼吸道、胃肠道和泌尿生殖系统感染。
详细描述
氟罗沙星对革兰氏阳性菌、革兰氏阴性菌和 厌氧菌等具有抗菌作用,可用于治疗肺炎、 支气管炎、急性呼吸道感染等呼吸道疾病, 以及胃肠道感染和泌尿生殖系统感染。
探索喹诺酮类药物与其他抗菌药物联 合应用时的药物相互作用机制。
针对多重耐药菌株的治疗,研究联合 应用喹诺酮类药物与其他抗菌药物的 治疗方案。
喹诺酮类药物的耐药性研究及防控措施
01
02
03
研究喹诺酮类药物耐药菌株的流行病 学和分子机制,为制定防控策略提供 依据。
药物化学-喹诺酮类抗菌药

氯喹(先导化合物)
Cl N
O
O
N
O
O OH
O O
O
OH
N
OH O
H3C
N
N CH3
N
N CH3
N
N
CH3
萘啶酸1962
吡咯酸
西诺沙星
第二代 喹诺酮类抗菌药物
吡哌酸,1974年上市,7位引入哌嗪基, 使抗革兰氏阴性菌活性增加;耐药性降低, 对萘啶酸和吡咯酸耐药菌株也有抑制作用, 但随着第三代喹诺酮类抗菌药物的出现, 它目前也已被淘汰
6
5
4 3
7 8
1
2
诺氟沙星是第一个上市的氟喹诺酮类药物,基本 上为喹啉羧酸类,其它氟喹诺酮类主要改造部位在 1位、5位或8位,也可以在7位上进行较小的改变。
第四代喹诺酮类药物
第四代喹诺酮类药物在抗菌活性、药动 学性质及半衰期上有明显提高,增加 对厌氧菌的抗菌活性是第四代的重要 特征。代表药物有莫西沙星、加替沙 星等。
喹诺酮类药物能否影响人体DNA复制?
由于哺乳动物细胞中不含螺旋酶
和拓扑异构酶Ⅳ,而是通过其它途径 进行DNA的复制,故喹诺酮类对细菌
的选择性高,而对人体的不良反应少。
细菌的耐药性
细胞膜对药物的通透性降低 细菌DNA螺旋酶结构改变 细菌产生药泵
喹诺酮类药物分类(根据结构)
萘啶(氮杂萘核)羧酸类
H 3C
Pefloxacin 培氟沙星
NH 2 O F N F CH 3 N COOH
HN
Rufloxacin
氟罗沙星 Fleroxacin
司帕沙星 Sparfloxacin
结构特点
O O
F
OH HN N N
喹诺酮类抗菌药物:分类与作用机制

靶向细菌DNA逆转录酶
喹诺酮类抗菌药物的作用机制主要是通过,抑制DNA的复制和细胞增殖。此类药物通常会与细菌DNA 逆转录酶结合,抑制酶的活性,从而影响其复制和转录。这样可以有效地杀灭多种细菌,包括革兰阳 性和革兰阴性细菌。此外,喹诺酮类抗菌药物还可以对细胞壁合成和蛋白质合成产生影响,以及干扰 DNA的拓扑结构,从而进一步增强其抗菌作用。
抑制DNA合成
1. 作用机制:喹诺酮类抗菌药物主要通过抑制革兰氏阳性菌和阴性菌的DNA拓 扑 异 构 酶 ( D N A g y r a s e ) 和 D N A 拓 扑 异 构 酶 I V ( To po i s o m e r a s e I V ) 的 活 性来干扰DNA复制和维持细胞生存。 2. 抑菌谱:喹诺酮类抗菌药物对革兰氏阴性菌(如大肠杆菌、克雷伯菌等)和 一些革兰氏阳性菌(如金黄色葡萄球菌、链球菌等)有很好的抑菌作用,但对革 兰氏阳性球菌(如肺炎球菌、链球菌等)的抑菌活性较低。 3. 应用临床:喹诺酮类抗菌药物的临床应用广泛,包括治疗呼吸道、泌尿道、 肠道和皮肤软组织等感染症,特别适用于治疗耐多种药物的革兰氏阴性菌感染。 但是,由于其在长期使用中可能导致耐药性和副作用的发生,应慎重使用。
谢谢
2023/5/2 |
logo/company
喹诺酮类抗菌药物:分类与作用机制
Quinolone antibiotics: Classification and mechanism of action. 汇报人: 2023/5/2 ·
Contents
喹诺酮类抗菌药物基础知识 第一代喹诺酮类药物 第二代喹诺酮类药物 第三代喹诺酮类药物 喹诺酮类药物作用机制 喹诺酮类药物用途与应用限制
PART 03
第二代喹诺酮类药 物 Second-generation quinolone drugs.
药物化学 第九章 化学治疗药 第一节 喹诺酮类抗菌药

合成十多万个化合物
十多种最常用的喹诺酮类药物
其中一些的抗菌作用完全可与优良的半合成头孢菌 素媲美
F HN
N
O
O
OH
N
一、喹诺酮类抗菌药物的发展概述
Chloroquine
第一代喹诺酮抗菌药物的药效学特征 抗革兰氏阴性菌药物,对革兰氏阳性菌 几乎无作用。其活性中等,体内易被代 谢,作用时间短,中枢毒性较大,易产 生耐药性。
O
R6
COOH
R7 N N
R8
R1
一、喹诺酮类抗菌药物的发展 概述
1962年美国sterling-winthrop药厂研 究人员发现萘啶酸有抗菌作用
揭开喹诺酮类抗菌研究序幕 1974年大日本制药公司合成了吡哌酸,
对尿路感染有良效 1978年发现氟哌酸
一、喹诺酮类抗菌药物的发展 概述
从1962年—1978年
常用喹诺酮类药物
OO
F OH
N
N
N
O
H
左氧沙星
主要学习内容
重点药物
盐酸环丙沙星
构效关系 结构类型及作用机制
Ciprofloxacin Hydrochloride 盐酸环丙沙星(环丙氟哌酸)
化学名
化学名为 1-环丙基-6-氟-1,4-二氢-4-氧代-7-
( 1- 哌 嗪 基 ) -3- 喹 啉 羧 酸 盐 酸 盐 一 水 合 物 ( 1-
Cyclopropyl-6-fluoro-1,4-dihydro-4-oxo-7-
萘啶羧酸类
OO
N
OH
OO OH
NN H
Pyridopyrimidinic acids
嘧啶并吡啶类
N N H
执业西药师药学综合知识辅导:喹诺酮类药物

喹诺酮类是一类新的合成抗菌药,由于其化学结构上都有吡啶酮酸基团,故通常将这类药物称为吡啶酮酸类药物,也称喹诺酮类。
本类药物于1962年进入临床,1978年之后其研究与开发十分迅速,已有多个品种使用于临床,他们的抗菌谱近似,主要作用于革兰阴性菌,对革兰阳性菌作用较弱。
根据用于临床时间先后和抗菌性能,本类药物可分为三代:第一代包括萘啶酸、吡嘧酸等,其中萘啶酸为代表药,由于其抗菌谱窄,血药浓度低,现已不再使用;第二代有吡哌酸,甲氟喹酸等,以吡哌酸为代表药,抗菌谱有所扩大,但只对革兰阴性杆菌有抗菌作用,临床使用较多;第三代有诺氟沙星、氧氟沙星、环丙沙星、依诺沙星等,为广谱抗菌药,临床使用广泛。
近年来,由于本类药物的大量使用,耐药菌株有增长的趋势,表现为最低抑菌浓度增大或完全耐药,本类药物之间存在较密切的交叉耐药性。
喹诺酮类药物在进行动物实验时,发现能损害幼龄动物的软骨,造成负重关节损坏而影响关节活动。
在人类,因不能进行此种实验而未能作出结论,因此不主张使用。
但也有人认为动物实验结果与临床实际不符。
为了对患儿负责,使用本类药物必须慎重,越是年龄小的儿童,越要认真考虑。
正确认识喹诺酮类抗菌药物

正确认识喹诺酮类抗菌药物一、历史回顾喹诺酮类属化学合成的抗菌药物,自从1960年合成第一代喹诺酮类药物萘酸后,于1973年合成了第二代喹诺酮药吡哌酸等,1978年合成了第三代喹诺酮药物。
第三代喹诺酮类药物的共同特点是在化学结构7位上连续哌嗪环,6位处又引入了氟原子,从而大大提高了菌活性,增宽了抗菌谱,疗效显著,同时副作用也小,因第三代喹诺酮类药物结构中均有氟原子,故又称氟喹诺酮类(fluoroquinolones)。
也有人根据喹诺酮类药物的抗菌作用、副作用等将其分为四个阶段:第一阶段是指1962-1969年上市的萘啶酸和吡咯酸,它们对大多数兰氏阴性菌有活性,但对革兰氏阳性菌和绿脓杆菌无活性。
此药口服吸收良好,在体内被代谢和灭活,24小时尿中回收率为50%-90%;而原药和活性代谢物仅占给药量的10%左右。
尽管如此,由于在泌尿道、胆道和肠道中浓度较高,可以治疗这些系统感染。
第二阶段在1970-1977年以吡哌酸和西诺沙星主代表,此类对革兰氏阴性菌有活性,在抗菌谱方面,与第一阶段药物相比,对绿脓杆菌有一定作用,对萘啶酸和吡咯酸有高度耐药的菌株也有活性。
此类药物体内代谢稳定,有尿中24小时回收率近90%,其中原药含量>50%,且组织渗透性好,除治疗泌尿道、胆道和肠道感染外,还用于耳、鼻等部位的感染。
第三阶段在1978-1964年,代表药有诺氟沙星、氧氟沙星、环西沙星、诺美沙星等;抗菌谱扩大为G+菌、G-菌和葡萄糖非酵解菌。
此类药具有良好的组织渗透性,除脑组织和脑脊液外,对各种组织均有良好的分布,所以不仅有广泛的抗菌谱,而且有广泛的适应症。
第四阶段指1986年以后所上市的一些喹诺酮类药物,与前几类相比,他们有抗菌谱方面,有些药对葡萄球菌、肺炎球菌、脆弱类杆菌、支原体、衣原体、军团菌等都有很好的作用;有些药对结核分枝杆菌的活性是第三阶段喹诺酮的3-30倍,与异烟腓和利福平相当。
此类药物由于吸收迅速,分布良好,血药浓度大,半衰期长,生物利用度高,所以临床可应用于泌尿感染、呼吸道感染、消化道感染、皮肤和软组织感染、眼、耳、鼻、喉科、口腔科等感染。
药物化学合成抗菌药

第二节 磺胺类药物及抗菌增效剂
二、抗菌增效剂 其他抗菌增效剂: 丙磺舒
抑制有机酸的排泄,从而提高有机酸药物在血液中的浓度。 与青霉素合用,可降低青霉素的排泄速度,从而增强青 霉素的抗菌作用。
克拉维酸
抑制β-内酰胺酶,与β-内酰胺抗生素合用,可保护其免受 β-内酰胺酶的影响,从而增强抗菌活性。
药物化学合成抗菌药
合成抗菌药分类
喹诺酮类抗菌药:
萘啶羧酸类: 吡啶并嘧啶羧酸类: 喹啉羧酸类:诺氟沙星、盐酸环丙沙星、左氧氟沙 星、司帕沙星、加替沙星。
磺胺类抗菌药:磺胺甲噁唑、磺胺嘧啶 抗菌增效剂:甲氧苄啶
药物化学02 2
第一节 喹诺酮类抗菌药
一、喹诺酮类抗菌药的结构特点
喹诺酮类抗菌药以原核生物 DNA 回旋酶为作用 靶点。目前为仅次于β-内酰胺抗生素的抗菌药 物。 1、萘啶羧酸类: 2、吡啶并嘧啶羧酸类: 3、喹啉羧酸类:诺氟沙星、盐酸环丙沙星、左 氧氟沙星、司帕沙星、加替沙星。
药物化学02
O F N HN CH 3 OCH 3 N COOH
10
第二节 磺胺类药物及抗菌增效剂
一、磺胺类药物 1、磺胺类药物的构效关系
(1)对氨基苯磺酰胺为必需结构。 (2)芳氨基上多数无取代,若有取代基,则必须体内易 分解或还原为游离氨基才有效。 ( 3 )磺酰胺基上 N- 单杂环取代抑菌作用增强, N,N- 双 取代一般失去活性。 (4)苯环改成其他芳环或在苯环上引入其他基团,抑菌 活性降低或丧失。 磺胺类药物的pKa值在6.5~7.0时,抑菌作用最强。
药物化学02Βιβλιοθήκη 16药物化学02 7
第一节 喹诺酮类抗菌药
三、喹诺酮类代表药物
盐酸环丙沙星
药物化学-抗菌药-课程设计
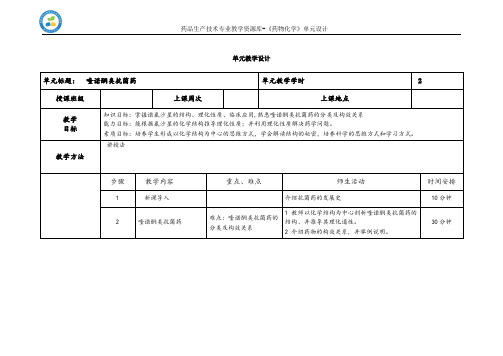
单元教学设计单元标题:喹诺酮类抗菌药单元教学学时 2 授课班级上课周次上课地点教学目标知识目标:掌握诺氟沙星的结构、理化性质、临床应用,熟悉喹诺酮类抗菌药的分类及构效关系能力目标:能根据氟沙星的化学结构推导理化性质;并利用理化性质解决药学问题。
素质目标:培养学生形成以化学结构为中心的思维方式,学会解读结构的秘密,培养科学的思维方式和学习方式。
教学方法讲授法步骤教学内容重点、难点师生活动时间安排1 新课导入介绍抗菌药的发展史10分钟2 喹诺酮类抗菌药难点:喹诺酮类抗菌药的分类及构效关系1教师以化学结构为中心剖析喹诺酮类抗菌药的结构、并推导其理化通性。
2 介绍药物的构效关系,并举例说明。
30分钟教学活动设计2 喹诺酮类抗菌药重点:诺氟沙星的结构、理化性质1教师以化学结构为中心剖析诺氟沙星的结构、并推导其理化性质。
2学生根据老师思路认识诺氟沙星的结构组成、并从结构特征推导其理化性质,深刻理解结构和理化性质的内在联系,培养药个物化学式的思维方式,并提升其对这些重点药物的药物化学知识的应用能力,最终提高其分析问题和解决问题的能力。
30分钟3 案例分析对所学喹诺酮类抗菌药的药物化学知识的应用1教师提供案例2 学生根据案例和所学知识进行分析,并提供解决方案3 教师进行点评总结10分钟5 回顾本次课程的主要内容并强调重点和难点。
布置作业学生作好记录10分钟作业(或考核)作业1、教学单元7作业,详细内容见教学资料。
作业内容及要求以qq形式发送学生,并要求学生上交。
教学材料含含教材、课件、资源(一)教材:马英主编,《药物化学》河南科技出版社,(高职高专规划教材)(二)参考资料:1. 郑虎主编,《药物化学》,人民卫生出版社, 2003。
2. 《药物化学》,李绍顺主编,科学出版社,2009年。
3. 《有机药物化学》原著第二版,郭宗儒主译,化学工业出版社,年。
课后反思。
第九章化学治疗药 第一节 喹诺酮类抗菌药

抗革兰阴性菌
R7
Cl,F,OCH3
降低最小抑菌浓度
22
2. 改善对革兰氏阳性菌的活性
CH3 抗革兰阳性菌
R5 N NH2 F O O OH X8 N R1 N
抗革兰阳性菌
R7
抑制S肺炎球菌的活性 Drug MIC Ciprofloxacin 0.5-2 Sparfloxacin 0.125-0.5 Moxifloxacin 0.01-0.5 Temafloxacin 0.5-1 Trovafloxacin 0.007-0.25
HN N N .HCl.H2O
19
R5 R6
6 5
O
4
Y
COOH
3
B
A N12 R1
4. 2位上引入取代基后,其活性 减弱或消失。
R7 7 X 8 R8
5. 5位取代基中,以氨基的抗菌作用最佳。其 他基团取代时,活性减少。。
20
R5 R6
6 5
O
4
Y
COOH
3
6. 6位不同的取代基对活性的贡献大小 顺序为F>Cl>CN≥NH2≥H,6位引入氟 原子较6位为H的类似物的抗菌活性大30 倍。
N1:有取代基 B环:芳环、杂环(含取代基)
9
常见的喹诺酮类药物
10
二、喹诺酮类药物的作用机制与药效团
• 抑制细菌DNA回旋酶和拓扑异构酶IV
• DNA旋转酶对于细菌的复制、转录和修复起决
定性作用。
• 而拓扑异构酶IV则是在细胞壁的分裂中对细菌
染色体的分裂起关键作用。
11
stabilize
break
抗革兰阳性菌
F
X=C,Cl,F,OCH3 降低最小抑菌浓度
药物化学--喹诺酮类药物-磺胺类药物及抗菌增效剂 ppt课件

20
代表药物
▸ 本品加氢氧化钠溶液溶解,加硫酸铜试液,即生成草绿色沉
淀,用于药典鉴别
▸ 本品显芳香第一胺反应
21
抗菌增效剂
▸ 抗菌增效剂 是一类与某些抗菌药物联合使用时,以特定的
作用机制增强后者抗菌活性的一类物质
▸ 甲氧苄啶单独使用时无临床价值。但与磺胺类抗菌药物合用
时可使后者的抗菌效力提高数十倍,甚至使某些磺胺类药物 由抑菌作用变成杀菌作用
▸ 1位为脂肪烃基或环烃基取代时,抗菌活性及药代动力学较好 ▸ 5位取代基以氨基取代时,抗菌作用增强;5位为甲基,1位引入环丙基时,
活性较好
▸ 6位以氟原子取代时,药物的脂溶性及对细菌细胞壁的穿透力增强 ▸ 7位以哌嗪或哌嗪类似物取代时,抗菌谱广,药代动力学和抗菌活性增强 ▸ 8位以氟原子取代时,体内吸收好,但光敏毒性
后,再加碘试液,生成棕色沉淀,用于药典鉴别
▸ 甲氧苄啶与四环素、青霉素、红霉素及庆大霉素等抗生素或
与黄连素等抗菌药联合使用时同样起到增效作用
22
抗菌增效剂
▸ 简称 TMP ▸ 白色或类白色结晶性粉末,无臭,味苦 ▸ 略溶于三氯甲烷,微溶于乙醇或丙酮,几乎不溶于水,易溶于冰醋酸
23
抗菌增效剂
▸ 含氮杂环:与生物碱沉淀剂发生反应,本品加稀硫酸溶解
9
代表药物
▸ 白色或淡黄色结晶性粉末,无臭,味苦 ▸ 微溶于水,极微溶于乙醇,不溶于乙醚 ▸ 药用品为左旋体;其消旋体氧氟沙星药效为本品的一半
10
代表药物
▸ 两性;药用品常用其盐酸盐或乳
酸盐
▸ 3-羧基-4-酮结构,易与钙、
镁、铝、铁、锌等金属离子反应 生成配合物,从而减少吸收
▸ 叔胺结构:加丙二酸和醋酐溶
喹诺酮类抗菌药物

抗菌普广。尤其对需氧革兰阴性杆菌,包括铜绿假单胞菌在内有强大杀菌作用,对金葡菌及产酶金葡菌也有良好抗菌作用。
体内分布广,组织体液内药物浓度高。
消除半衰期较长,可每日给药1~2次
多数品种有口服及注射剂,使用方便
不良反应较轻,耐受良好
适用于敏感病原菌(金葡菌、铜绿假单胞菌、肠道革兰阴性杆菌、弯曲菌属等)所致泌尿道感染、前列腺炎、淋病、呼吸道感染、胃肠道感染、及骨、关节、软组织感染。
甲氧苄啶(TMP)又称抗菌增效剂
抗菌普广
口服后血药浓度低,不适用于全身感染
细菌不易产生耐药性
主要用于治疗泌尿道感染
硝基呋喃类抗菌药物
呋喃妥因(呋喃坦啶):酸性尿中活性强,主要用于敏感细菌所致的泌尿道感染
呋喃唑酮(痢特灵):肠内浓度高,主要用于细菌性痢疾
呋喃西林:局部外用于伤口、创面、皮肤等感染
03
氟喹诺酮类特点
喹诺酮类作用机制
喹诺酮类药物作用的靶酶为细菌的DNA回旋酶(拓扑异构酶Ⅱ)及解链酶(拓扑异构酶Ⅳ),喹诺酮类药物抑制细菌的回旋酶和解链酶,阻碍细菌DNA合成,导致细菌死亡。哺乳动物真核细胞中不含DNA回旋酶,故喹诺酮类对细菌选择性高,不良反应少。
随着氟喹诺酮类药物广泛应用,临床病原菌对喹诺酮类药物耐药性已迅速增长,以大肠埃希菌、肺炎链球菌、葡萄球菌、淋病萘色球菌和伤害沙门菌耐药性增高最显著。
对呋噻咪、噻嗪类利尿药过敏的患者,对磺胺药也可过敏
04
磺胺类一般仅起抑菌功效,避免与青霉素类药物合用
03
综述:磺胺类为第一类人工合成的防止全身性细菌感染的有效的化疗药物,以后,随着各类抗生素及合成抗菌药的门世,磺胺类药的治疗地位逐渐被取代,但仍有其独特的优点,对某些感染性疾病(如流行性脑脊髓膜炎、鼠疫)具有疗效显著,使用方便,性质稳定、价格低廉等特点。
喹诺酮类药物结构特点与特性、作用机制、特点、分类和抗菌谱

喹诺酮类药物结构特点与特性、作用机制、特点、分类和抗菌谱喹诺酮类药物是化学合成抗菌药,该类药物化学结构、作用机制均不同于其他抗菌药,且具有抗菌谱广、对革兰阴性菌抑制作用强于革兰阳性菌特点,是治疗各种感染性疾病高效且安全一类药物。
喹诺酮类结构特点与特性喹诺酮类是以4-喹诺酮为基本结构的合成类抗菌药,在4-喹诺酮母核N1位、C5位、C6位、C7位、C8位引入不同基团,形成各具特点喹诺酮类药物。
1.抗菌活性C6位引入氟原子同时,C7位引入哌嗪基后,药物与DNA回旋酶亲和力和抗菌活性显著提高,抗菌谱明显扩大,药动学性质显著改善。
N1位引入环丙基后,环丙沙星、司帕沙星、莫西沙星、加替沙星和加雷沙星等药物对革兰阳性菌、衣原体、支原体杀灭作用进一步增强,C6位脱去氟原子且C8位引入二氟甲基的加雷沙星对革兰阴性菌、革兰阳性菌、厌氧菌、支原体、衣原体均具有与莫西沙星类似的良好活性和药动学特征,毒性更低,诞生C6非氟氟喹诺酮类药物。
2.脂溶性C7位引入甲基哌嗪环,可增加氧氟沙星、氟罗沙星和左氧氟沙星药物脂溶性,提高口服生物利用度和对细菌的穿透力。
C8位引入氯原子或氟原子,进一步提高药物口服生物利用度,延长药物消除半衰期,提高药物脂溶性具有扩大抗菌谱和增强抗菌活性效果。
3.光敏反应C8位引入氯原子或氟原子后,在提高疗效同时,增强药物光敏反应,药物包括司帕沙星、氟罗沙星和洛美沙星。
以甲氧基取代C8位氯原子或氟原子时,在提高疗效同时还可降低光敏反应,药物包括莫西沙星和加替沙星。
4.中枢神经系统毒性C7位哌嗪环取代基团与γ-氨基丁酸受体拮抗剂结构相似,可拮抗GABA受体产生中枢神经系统症状。
喹诺酮类药物与茶碱或非甾体类抗炎药合用时易产生中枢毒性。
C6位有疏水性的氟原子使喹诺酮类药物具有一定脂溶性,易于透过血脑屏障。
去掉C6位氟原子的加雷沙星与NSAID合用不诱发惊厥反应,不影响GABA与γ-氨基丁酸A型受体结合,中枢神经系统毒性显著减低。
喹诺酮类、磺胺类及其它合成抗菌药物

17
18
【耐药性】 细菌对磺胺药的耐药性可通过染色体或质粒介导。耐药性 机制是:①对氨基苯甲酸生成过多;②磺胺药对二氢叶酸合成 酶的亲和力降低;③细菌对药物的通透性减弱。④磺胺类药之 间有交叉耐药。 细菌对磺胺药易产生耐药性,尤其在用量不足,时用时停 或疗程过长者更易发生。
19
【药动学】 胃肠易吸收的磺胺药,吸收后分布于全身组织和体液中, 以肝、肾浓度较高,部分与血浆蛋白结合,结合率低者(如磺 胺嘧啶)易透过血脑屏障,在脑脊液中浓度高。磺胺药主要经 肝乙酰化代谢而失效。乙酰化物在尿中溶解度较小,尤其是在 酸性尿中易析出结晶而损害肾。 肠道难吸收的磺胺药主要随粪便排出。 90%以上的磺胺药及其代谢产物主要经肾消除,肾小球滤 过,肾小管的主动转运,N4-乙酰化代谢产物的肾清除率比原形 药物高。pH因影响肾小管的重吸收而影响磺胺类药肾清除率。
3
氟喹诺酮类的特点: ①抗菌谱广,对革兰阴性杆菌作用强; ②体内分布广,特别是在组织液中药物浓度高; ③使用方便,多数为口服制剂,半衰期较长,可以减少服 药次数。 氟喹诺酮类广泛用于临床,对多重耐药革兰阴性杆菌感染 有很好的作用。但近年来细菌对该类药物的耐药性明显升高, 特别是大肠埃希菌的耐药。
4
15
【抗菌作用】 磺胺类药物抗菌谱广, ⑴对革兰阳性菌敏感的有溶血性链球菌、肺炎链球菌, ⑵对革兰阴性菌敏感的有脑膜炎球菌、淋球菌、鼠疫杆菌 和流感杆菌等,对大肠埃希菌、痢疾杆菌、变形杆菌、肺炎杆 菌及沙眼衣原体、放线菌、疟原虫等也有效。 ⑶磺胺甲噁唑对伤寒杆菌,磺胺米隆和磺胺嘧啶银对铜绿 假单胞菌有抑制作用。
21
第三节
其他合成抗菌药物
(一)甲氧苄啶(TMP) 甲氧苄啶抗菌谱与磺胺类相似,抗菌作用较强,但对脑膜 炎球菌作用弱,单用易产生耐药性,临床上主要用作一种磺胺 增效剂或抗菌增效剂。 【抗菌作用】 TMP对金黄色葡萄球菌、链球菌等革兰阳性菌及大肠埃希菌、 奇异变形杆菌、肺炎杆菌、痢疾杆菌、伤寒杆菌等革兰阴性菌 均有抗菌作用,对脑膜炎球菌、淋球菌、产碱杆菌属作用不明 显,对铜绿假单胞菌无效。 TMP抗菌作用比SMZ强20~100倍。
喹诺酮类抗菌药物汇总

过敏反应:部分患者可 能出现皮疹、瘙痒等过 敏反应,严重者可能出 现过敏性休克。
肌腱炎和肌腱断裂:长 期使用喹诺酮类药物可 能导致肌腱炎和肌腱断 裂的风险增加。
神经系统反应:部分患 注意事项:喹诺酮类药
者可能出现头痛、头晕、 物可能影响软骨发育,
失眠等神经系统反应, 因此孕妇和未成年儿童
严重者可能出现癫痫发 应避免使用;此外,与
抗菌谱
喹诺酮类药物主要针对革兰氏 阴性菌,如大肠杆菌、肺炎克 雷伯菌、铜绿假单胞菌等,具
有良好的抗菌活性。
喹诺酮类药物对部分革兰氏 阳性菌也有抗菌作用,如金 黄色葡萄球菌、表皮葡萄球
菌等。
此外,喹诺酮类药物还对支原 体、衣原体、军团菌等非典型 病原体具有一定的抗菌作用。
适应症
下呼吸道感染
喹诺酮类药物常用于治疗社区 获得性肺炎、慢性阻塞性肺疾 病急性加重等下呼吸道感染。
耐药性的监测与控制
监测方法
通过实验室检测细菌对喹诺酮类药物的敏感性,及时发现耐药性。
控制策略
限制喹诺酮类药物的滥用,加强抗菌药物的管理和监管,推广合理用药。
耐药性的影响与挑战
影响
耐药性的产生导致喹诺酮类药物在治 疗细菌感染时的效果降低,甚至失效 。
挑战
耐药性的挑战在于如何有效控制其传 播,同时研发新型抗菌药物以应对耐 药性问题。
04
喹诺酮类药物的临床应用
呼吸系统感染
总结词
喹诺酮类药物在呼吸系统感染中应用广泛,尤其适用于治疗下呼吸道感染,如肺 炎和支气管扩张症等。
详细描述
喹诺酮类药物通过抑制细菌DNA旋转酶,从而影响细菌DNA复制、转录和修复 ,最终导致细菌死亡。对于常见的呼吸系统感染病原体如肺炎链球菌、流感嗜血 杆菌、支原体和衣原体等,喹诺酮类药物具有较好的抗菌活性。
喹诺酮类药物分析

成螯合物。
– 使用注意:不宜与含钙或铁的食物、药物同服 ;长期使用注意钙流失。
• (二)理化性质 • 5.紫外吸收光谱特性
– 分子结构中均有共轭体系,可用紫外分光光度 法进行鉴别和含量测定。
二、鉴别试验
• (一)氟元素反应
–
F-+
茜素氟蓝
+
pH4.3
Ce3+
蓝紫色
• (二)紫外-可见分光光度法
– 鉴别多种喹诺酮类药物
• (三)红外分光光度法
– 标准图谱对照法
二、鉴别试验
• (四)薄层色谱法
– 诺氟沙星的鉴别:取本品与诺氟沙星对照品适量,分别加三氯甲烷-甲醇( 1:1)制成每1ml中含2.5mg的溶液,作为供试品溶液与对照溶液,照薄层色 谱法试验,吸取上述两种溶液各10μl,分别点于同一硅胶G薄层板上,以三 氯甲烷-甲醇-浓氨溶液(15:10:3)为展开剂,展开,晾干,置紫外灯( 365nm)下检视,供试品溶液所显主斑点的位置与荧光应与对照品溶液主斑 点的位置与荧光相同。
• (五)高效液相色谱法
供试液主峰保留时间应与对照品主峰保留时间一致
三、杂质检查
❖ (一)溶液澄清度检查
▪ 控制碱不溶性杂质的限量:喹诺酮类药物在碱中易溶 ,而中间体等杂质不溶。
❖ (二)有关物质检查
▪ 多数喹诺酮类药物均需做有关物质检查。 ▪ 方法:HPLC法 ▪ 举例:1.诺氟沙星中有关物质的检查
一、结构与性质
❖ (一)化学结构
❖ 喹诺酮类药物母核结构:4-喹诺酮-3-羧酸
医学专题抗菌药喹诺酮类摘要

1、N1位取代基对抗菌活性有 很大贡献。
N1 位 取 代 基 如 是 脂 肪 烃 取 代 基时,以乙基或者与乙基体积 相似的乙烯基、氟乙基取代时 抗菌活性最强。
N1位取代基如是脂肪环 烃取代基时,以环丙基 的抗菌活性最强。
N1位取代基也可是芳香 烃取代,苯取代和乙基 取代的作用相似,2, 4-二氟苯基和4-羟基苯 基的取代可扩大抗菌谱, 增强对G+的活性。
6、 甲氧苄啶( TMP) 的作用机理为 A. 抑制二氢叶酸合成酶( ) B. 抑制二氢叶酸还原酶( ) C. 抗代谢作用 ( ) D. 掺入DNA的合成( ) E. 抑制β-内酰胺酶( )
喹诺酮类药物是 DNA回旋酶 (gyrase)和拓扑 异构酶Ⅳ (Topoisomerase Ⅳ) 的抑制剂。
回旋酶
喹诺酮类药物对人体细胞拓扑异构酶影响较小
回旋酶
DNA回旋酶
第二十章 抗菌药 第二节 喹诺酮类抗菌药 三、构效关系
A环时间抗菌作用必须的基本药效结构,3-羧基、4位羰 基氧与DNA螺旋酶和拓扑异构酶Ⅳ作用,是抗菌必须的 活性基团。
第二代代表药物:西诺沙星(Cinoxacin)、吡哌 酸(Pipemidiemidic Acid
1)抗菌谱:对G-起作用,对G+也有效, 较第一代有明 显的优点,对绿脓杆菌有抑菌活性,对萘啶酸和 吡咯酸的耐药菌株有抑制作用。说明两代药物的 交叉耐药作用不同。
诺氟沙星的合成: 用3-氯-4-氟苯胺(1)和乙氧甲烯基丙二酸二乙酯(2)
在120-130℃缩合得缩合物(3)。 (3)在液体石蜡存在下150℃环合,得化合物(4)。 将(4)在DMF中用硫酸二乙酯进行N-乙基化反应,得
化合物(5)。 (5)在2mol/LNaOH下水解生成(6)。 (6)与哌嗪缩合而得诺氟沙星。
中国药科大学药理学第10章合成抗菌药喹诺酮类

1. 喹诺酮类药物 2. 磺胺类药物 3. 其他合成抗菌药
第一节 喹诺酮类药物
一、喹诺酮类( quinolonos ) 概述
含4 - 喹诺酮基本结构。 发展迅速,使用广泛。
第一代:1962年萘啶酸 ( Nalidixic Acid )首先用于临床 ,因抗菌谱窄、 口服吸收差,副作用多,已淘汰。
一、喹诺酮类概述
第四代:氟喹诺酮类
1997年以后出现,如莫西沙星、克 林沙星等。
增强了对G+菌的作用,特别是对厌 氧菌的作用。但对铜绿假单胞菌作 用较差。
常用第三代氟喹诺酮类药物:
诺氟沙星 ( 氟哌酸,Norfloxacin ) 培氟沙星 ( 甲氟哌酸,Perflpxacin ) 依诺沙星 ( 氟啶酸,Enoxacin ) 氧氟沙星 ( 氟嗪酸,Ofloxacin ) 左氧氟沙星 ( 可乐必妥,Levofloxacin ) 环丙沙星 ( 环丙氟哌酸,Ciprofloxacin ) 洛美沙星 ( Lomexacin ) 氟罗沙星 ( 多氟哌酸,Fleroxacin )
菌和铜绿假单胞菌等。
① DNA回旋酶和拓扑异构酶Ⅳ变异。
低度耐药性: 基因突变,DNA回旋
酶A亚基变异,对药物的亲和力降低。
高度耐药性:DNA回旋酶和拓扑
异构酶Ⅳ同时变异。
喹诺酮类—耐药性
② 细胞膜孔蛋白通道减少,对药物 通透性下降。
③ 细菌主动泵出药物。
外排泵表达水平不断提高,是 细菌多重耐药性的主要原因。
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成。21.8.1621.8.1601:34:5801:34:58August 16, 2021
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
DNA的解链与复制 DNA的解链与复制
DNA解链过程 DNA解链过程
超螺旋状态
在DNA复制时,复制叉行进的前方DNA DNA复制时,复制叉行进的前方DNA 分子部分产生超螺旋状态,拓扑异构 分子部分产生超螺旋状态,拓扑异构 酶Ⅳ可松驰超螺旋状态,有利于复制 叉的前进及DNA的合成. 叉的前进及DNA的合成. DNA复制完成后,螺旋酶 DNA复制完成后,螺旋酶又可将DNA分 螺旋酶又可将DNA分 子引入超螺旋,使DNA缠绕,折叠,压 子引入超螺旋,使DNA缠绕,折叠,压 缩以形成染色质储存于菌体内,如果 不压缩卷紧,则DNA链长度远远超过细 不压缩卷紧,则DNA链长度远远超过细 胞壁,根本无法容纳在细胞中.则无 法进行接下来的DNA复制. 法进行接下来的DNA复制.
R5 R6
6 5
O
4
Y
COOH
3
B
A N 12 R1
R7 7 X 8 R8
6位F原子取代最佳,一般不作改变,可 原子取代最佳,一般不作改变, 使药物具有良好的抗革兰氏阳性菌活性, 使药物具有良好的抗革兰氏阳性菌活性, 产生广谱抗菌作用
R5 R6
6 5
O
4
Y
COOH
3
B
A N 12 R1
R7 7 X 8 R8
染色体实际长度 负超螺旋下的长度
DNA螺旋酶 DNA螺旋酶
松散的DNA 松散的DNA
喹诺酮类
高度卷紧的DNA 高度卷紧的DNA
喹诺酮类药物能否影响人体DNA复制? 喹诺酮类药物能否影响人体DNA复制? DNA复制 由于哺乳动物细胞中不含螺旋酶 和拓扑异构酶Ⅳ 和拓扑异构酶Ⅳ,而是通过其它途径 进行DNA的复制,故喹诺酮类对细菌 进行DNA的复制,故喹诺酮类对细菌 的选择性高,而对人体的不良反应少.
喹诺酮类药物的作用机制
抑制G 菌的DNA DNA的螺旋酶 抑制G-菌的DNA的螺旋酶 抑制G+菌的拓扑异构酶Ⅳ 抑制G 菌的拓扑异构酶Ⅳ 拓扑异构酶
DNA是平行的双链结构,细菌的繁 DNA是平行的双链结构,细菌的繁 殖是以解开成单链的DNA链(母链) 殖是以解开成单链的DNA链(母链) 为模版,来合成子链的 DNA的复制过程需要酶的参与,这 DNA的复制过程需要酶的参与,这 些酶比如螺旋酶和拓扑异构酶Ⅳ 些酶比如螺旋酶和拓扑异构酶Ⅳ
开始引入哌嗪基
N N HN N N CH 3 O COOH
吡哌酸
第三代 (氟)喹诺酮类抗菌药物
在第二代基础上,进行6 在第二代基础上,进行6位F取代,加上7位哌 取代,加上7 嗪基,使 嗪基,使药物不仅具有良好的抗革兰氏阴性 菌活性,还具有良好的抗革兰氏阳性菌作用 良好的抗革兰氏阳性菌作用, 菌活性,还具有良好的抗革兰氏阳性菌作用, 故为广谱抗菌药 广谱抗菌药, G+和 故为广谱抗菌药,对G+和G-(包括铜绿假单 孢菌)都有效,对支原体和衣原体及分支杆 菌也有作用.第三代喹诺酮类抗菌药是目前 使用的品种,××沙星. 使用的品种,××沙星. 结构:大部分为喹啉羧酸类结构( 结构:大部分为喹啉羧酸类结构(少数为萘 啶羧酸类),也称为氟喹诺酮类 啶羧酸类),也称为氟喹诺酮类,以诺氟沙星 氟喹诺酮类, (第一个上市)为参照,可以在1位,5位或8 (第一个上市)为参照,可以在1位,5位或8 位进行改造.
5位上-NH2取代抗革兰氏阴性菌活性 位上-NH2取代抗革兰氏阴性菌活性 增强:如司帕沙星; 增强:如司帕沙星; 位上-CH3取代抗革兰氏阳性菌活性 5位上-CH3取代抗革兰氏阳性菌活性 增强:如妥美沙星,替马沙星, 增强:如妥美沙星,替马沙星,格 帕沙星
R5 R6
6 5
O
4
Y
COOH
3
B
A N 12 R1
R7 7 X 8 R8
1位上环丙基取代抗菌活性增强(强于脂肪烃基: 位上环丙基取代抗菌活性增强(强于脂肪烃基: 乙基最佳),若以2.4二氟苯基取代, ),若以2.4二氟苯基取代 乙基最佳),若以2.4二氟苯基取代,还可增加 抗厌氧菌的活性 位上环丙基取代可产生药物的相互作用, 但1位上环丙基取代可产生药物的相互作用,通 过抑制细胞色素P450 从而抑制茶碱类( P450酶 过抑制细胞色素P450酶,从而抑制茶碱类(如咖 啡因) 使血药浓度增加,引起CNS 啡因)在肝脏的代谢 ,使血药浓度增加,引起CNS 过度兴奋等症状 取代基体积越大, 取代基体积越大,可越好地降低药物的最小抑 菌浓度
抗G- (二氢吡啶酮,α位羧基),对G+ 二氢吡啶酮, 位羧基), ),对 几乎无作用;抗菌谱窄,易耐药, 几乎无作用;抗菌谱窄,易耐药,已被淘汰
H3C CH3 N NH CH3
氯喹(先导化合物) 氯喹(先导化合物)
Cl N
O
O
N
O
O OH
O O
O
OH
N
OH O
H3 C
N
N CH3
N
N CH3
N
N
CH3
COOH
COOH
F N N
F N N H3C O N
COOH
CH3
诺氟沙星 Norfloxacin
O F N N H3C O H N CH3 COOH
环丙沙星 Ciprofloxacin
O F H3C HN N F N CH3 HN COOH
氧氟沙星 Ofloxacin
O F N N N CH3 COOH
R5 R6 6 Y
5
O
4
COOH
3
B
A N 12 R1
R7 7 X 8 R8
8位上引入Cl,F,OCH3,可降低最小抑菌 位上引入Cl Cl, 浓度, 原子作用最佳. 浓度,以F原子作用最佳. 位上F原子取代可产生光毒性. 但8位上F原子取代可产生光毒性. 位上引入OCH 8位上引入OCH3还可增加药物抗厌氧菌活 性 变成N原子, 若8位C变成N原子,抗革兰氏阳性菌作用增 还可增加抗厌氧菌活性, 强,还可增加抗厌氧菌活性,生物利用度 提高. 提高.
萘啶酸1962 萘啶酸
吡咯酸
西诺沙星
细菌的耐药性
细胞膜对药物的通透性降低 细菌DNA螺旋酶结构改变 细菌DNA螺旋酶结构改变 细菌产生药泵
第二代 喹诺酮类抗菌药物
吡哌酸,1974年上市,7 吡哌酸,1974年上市,7位引入哌嗪基, 使抗革兰氏阴性菌活性增加;耐药性降低, 抗革兰氏阴性菌活性增加;耐药性降低, 对萘啶酸和吡咯酸耐药菌株也有抑制作用, 但随着第三代喹诺酮类抗菌药物的出现, 它目前也已被淘汰
5 6
4 3
7 8 1
2
诺氟沙星是第一个上市的氟喹诺酮类药物,基本 诺氟沙星是第一个上市的氟喹诺酮类药物, 上为喹啉羧酸类, 上为喹啉羧酸类,其它氟喹诺酮类主要改造部位在 位或8 也可以在7位上进行较小的改变. 1位,5位或8位,也可以在7位上进行较小的改变.
O F N HN N CH3
HN
O
O
Levofloxicin 左氧氟沙星
O F N N N F COOH H3C
Lomefloxacin 洛美沙星
O F N N F H2N COOH
Enoxacin 依诺沙星
O F N N N F H F COOH
H2N
H
HN
F
F
Tosufloxacin
Temafloxacin 替马沙星
曲伐沙星 Trovafloxacin
病原微生物
细菌,真菌,病毒,寄生虫, 细菌,真菌,病毒,寄生虫, 支原体,衣原体,立克次体, 螺旋体,
但后来发现化学治疗药的作用, 但后来发现化学治疗药的作用, 不仅只限于治疗由病原微生物引 起的感染,还用于治疗恶性肿瘤, 起的感染,还用于治疗恶性肿瘤, 糖尿病…… 糖尿病……
化学治疗药的概念
抗菌药
抗菌药(两类) 抗菌药(两类)
抗生素: 抗生素:微生物的代谢产物或在天然 代谢物的基础上半合成,合成(氯霉 素)的天然类似物,总之与天然物质 紧密联系 喹诺酮类抗菌药,抗结核药物,磺胺 喹诺酮类抗菌药,抗结核药物, 类药物及抗菌增效剂:化学全合成药 类药物及抗菌增效剂:
抗菌药的作用机制
第一节 喹诺酮类抗菌药
R5 R6
6 5
O
4
Y
COOH
3
B
A N 12 R1
R7 7 X 8 R8
当1位和8位间形成环状化合物时,会产 位和8位间形成环状化合物时, 生一个手性碳原子,有两个对映异构体, 生一个手性碳原子,有两个对映异构体, 其中以S型异构体活性最强. 其中以S型异构体活性最强. 如氧氟沙星和左氧氟沙星, 如氧氟沙星和左氧氟沙星,以左氧 氟沙星( 型异构体)活性最强. 氟沙星(S型异构体)活性最强.
7位引入哌嗪基可增加药物抗革兰氏阴性 菌的活性 但7位被哌嗪取代可产生对中枢的毒 副作用,即与脑内GABA受体结合,使GABA 副作用,即与脑内GABA受体结合, GABA受体结合 受到拮抗而产生CNS症状(兴奋性增强). CNS症状 受到拮抗而产生CNS症状(兴奋性增强). 改良方法: 改良方法:可通过哌嗪甲基化增大取代基 的空间体积, 的空间体积,7位甲基哌嗪取代的喹诺酮 类药物对CNS毒性降低. CNS毒性降低 类药物对CNS毒性降低. 根据生物电子等排原理, 根据生物电子等排原理,7位也可被其它 复杂的(双)环碱基取代,可增加抗革兰 复杂的( 环碱基取代, 氏阳性菌的活性 位取代基体积增大时, 当7位取代基体积增大时,药物作用的半 衰期延长. 衰期延长.
喹诺酮类药物分类(根据结构) 喹诺酮类药物分类(根据结构)
萘啶(氮杂萘核) 萘啶(氮杂萘核)羧酸类
R3 O COOH
噌啉羧酸类
O O COOH
R2
N
N R1
O
N
N R1
吡啶并嘧啶羧酸类
