氧头孢中间体的溴代反应研究
不同烷基取代苯的溴代和硝化反应的相对速率

一、概述烷基取代苯的溴代和硝化反应是有机化学中的重要反应之一,重要性在于可以合成一系列对取代苯衍生物,这些衍生物在各种领域都有广泛的应用。
研究不同烷基取代苯的溴代和硝化反应的相对速率,有助于了解不同底物结构对反应速率的影响,有利于合成目标产物的选择及优化合成条件。
二、理论1. 溴代反应溴代反应是指苯或其取代物与溴反应,形成卤代取代产物。
苯对溴反应生成溴苯,而烷基取代苯则生成相应的取代产物。
通常情况下,取代基对反应速率的影响与取代基的位置、电子效应、立体效应等有关。
2. 硝化反应硝化反应是指苯或其取代物与硝酸反应,在硝酸的作用下形成硝基取代产物。
与溴代反应类似,不同的烷基取代苯在硝化反应中也会产生不同的硝基取代产物。
三、实验1. 实验目的本实验旨在研究不同烷基取代苯的溴代和硝化反应的相对速率,通过实验数据分析底物结构对反应速率的影响,为合成目标产物提供理论依据。
2. 实验方法(1)制备不同烷基取代苯的实验底物;(2)使用不同溴代试剂和硝化试剂进行反应,并控制反应条件;(3)收集实验数据,包括反应产物的生成量、产率等信息;(4)通过数据分析,得出不同烷基取代苯的溴代和硝化反应的相对速率。
3. 实验结果与分析(1)根据实验数据,不同烷基取代苯的溴代反应速率相对差异较大。
部分烷基取代苯的反应速率较快,而另一些则较慢。
(2)在硝化反应中,也观察到不同烷基取代苯的反应速率存在较大差异,一些底物的反应速率明显快于其他底物。
(3)通过对实验数据的分析,得出不同烷基取代苯的溴代和硝化反应的相对速率存在一定规律,具体规律需要进一步研究探讨。
四、结论与展望1. 结论不同烷基取代苯的溴代和硝化反应的相对速率存在一定差异,这一差异受到底物结构的影响。
通过实验数据的分析可以得出,底物结构对反应速率有明显影响。
2. 展望本实验为初步研究,未来将进一步深入探讨底物结构对反应速率的影响规律,并进行进一步的物理化学机理研究。
对助于提高对于溴代和硝化反应的认识,并为合成目标产物提供更准确的指导。
基于头孢类药物中间体氨基噻肟酸合成研究进展

基于头孢类药物中间体氨基噻肟酸合成研究进展头炮是所有头孢类抗菌药的总称,主要是利用冠头炮菌来进行培养,继而得到纯天然的头炮菌素C作为原材料,通过半合成的方式,对侧链进行改造最终获得的一种抗生素。
随着时代的发展,有关头炮的研究始终没有终止,尤其是氨基噻肟酸的合成,在经过长期探索以后,终于得出了合成的有效方式。
本文在研究的过程中,主要是结合实际情况来分析头孢类药物中间体氨基噻肟酸合成研究的进展,以期为今后开展的相关工作提供宝贵经验。
标签:头炮类药物;氨基噻肟酸;合成头炮属于一种在医学生较为常见的抗生素,根据自身抗菌性能的差异,也会分为不同代,且这一类型的抗生素在市场中还占据着较大份额。
需要注意的是,头炮不能够在饮酒的状态下服用。
目前,头孢类药物中间体氨基噻肟酸的合成方法有很多,大致是可以分为乙酰乙酸甲酯法、乙酰乙酸乙酯法、乙酰乙酸乙酯一锅煮法、4-氯乙酰乙酸乙酯法等,在实际应用的过程中乙酰乙酸乙酯法是现如今我国最为成熟的合成方法。
一、氨基噻肟酸概述氨基噻肟酸,化学名2-甲氧亚胺基-2-(2-氨基噻唑)-4-乙酸;2-(2-氨基-4-噻唑基)-2-甲氧亚胺乙酸或2-氨基噻唑-4-甲基异肟酸。
其自身的熔点可以最高可以达到132℃,当温度达到这一标准时,变回分解成粉末状,为白色结晶体,遇到碱性水溶液时具有不可溶性,在遇到水、乙醇、氯仿等具有微溶特性,是医药中的一种重要中间体,可以用于三代头炮菌素的合成。
由于头炮自身具有较为良好的疗效,而在巨大的国际市场的推动下,我国氨基噻肟酸也得到进一步发展。
就国际市場现状来分析,市场对于这一类型的药物需求量在4.5千吨,而在我国这一方面的生产已经超过了2000吨,并且诚然持续增长,年出口量也已经达到了800吨,一般情况下,该类药物在国内的价格是维持在14~15万/吨,可以创造巨大的经济效益。
因此,在今后发展的过程中,如何采取更为具有经济性价值的药物合成方式,已经成为其今后发展的关键。
同多酸催化下几种含氧芳香烃溴代反应的研究

摘 要 : 分别 以 4 酚类化合物:- 种 2甲基苯酚、 邻苯二酚、 间苯二酚 、 对苯二酚 为反 应物, 首先将反应底物的羟基进行
甲基 或 者 甲氧 基 甲基 保护 , 后将 所 得 到 的产 物 在 醋酸 溶 剂 中 , 溴化 钾 和 过 氧 化 氢 为试 剂 , 然 以 钼酸 铵 为 催 化 嗣 的 条 件 下 , 究 了 在苯 环 骨架 上 引入 了 溴原 子 的 方法 . 研 研究 结果 表 明 , 实验 方 法 操 作 简单 易 行 , 应 时 间较 短 , 物专 一 性 好 , 反 产 后 处 理 简单 , 且 收率 较 高 , 化溴 原 子 对苯 环 的 进攻 位 置 主 要受 到催 化 荆 钼 酸 大 分子 结 构 的控 制 . 物 经 红 外 光 谱 并 活 产 和 核 磁 共振 谱 进 行 了结 构 表 征 , 证实 成 功 合成 了 目标化 合 物.
OH
N N
O OH
罗汉松烷
聚合物
收稿 日期 :0 90—4 20 —81
基金 项 目: 辽宁 省 教 育厅 科 学 技 术研 究 项 目(0 9 2 )辽 宁 省 教 育厅 创 新 团 队项 目(o 8 O ) 2 0 A4 6 ; 2O Tl7 作者 简 介 : 张成 路 (9 6 , 。 宁 盖 州人 , 宁 师范 大 学 教 授 , 士 . 1 6一) 男 辽 辽 博
第 1 期
张 成 路 等 : 同 多酸催 化 下 几 种含 氧 芳 香 烃 溴代 反 应 的研 究
7 9
本 文分别 以邻 甲酚 、 苯二 酚 、 邻 间苯 二酚 、 对苯 二酚为 反应 底物 , 官能 团转 化后 , 同多酸 钼酸 的 经 在 催 化下 , 进行 溴代得 到 了 4种 不 同的溴代产 物 , 反应 方法见 附图 :
氧头孢中间体的溴代反应研究

阴性菌有良好抗菌作用。氟氧头孢 的抗菌谱和其
他第 三代 头 孢 菌 素 相 似 , 革 兰 阳性 菌 的抗 菌 作 对 用 几乎 与拉 氧 头 孢 相 同 , 菌 性 能 与第 四代 头孢 抗
是 使用 量 和金 额 最 大 的一 类 药 物 。其 中头 孢 类抗感 染 药在抗 感 染药 物 中间 占到 5 % 以上 的 比 0
第 2 第 4期 4卷 21 0 2年 4月
化 学 研 究 与 应 用
Ch mia s a c n p l ai n e cl Re e rh a d A pi t c o
V0 . 4. . 12 No 4 Apr 2 2 ., 01
文章 编 号 :04 1 5 (0 2 0 -6 00 1 0 —6 6 2 1 ) 40 5 -3
摘要 : 6A A( . 以 - P 6氨基青霉烷 酸) 为原料 , 过苯 甲酰 化保护 , 的氧化 , 经 硫 二苯 甲酯 保护 , 7位氨 基异构化 , 开
环重排 , 得到异丙 烯基 表唑啉。用 N S 溴素分别尝试进行溴 代 , B, 最终 得到两个溴代 物异构体 , 并经过 核磁共 振氢谱对结构进行 了确证 。 关键词 : 氧头孢 中间体 ; 异丙烯基表唑啉 ; 溴代
,
例。
氧 头孢烯 类 的产 品 目前 只 有拉 氧 头 孢 ( 1 图 )
菌素相近。两者均对 内酰胺酶有较好的稳定性 在我国, 氧头孢烯类药 品的开发至今仍 受到技术
上 瓶 颈 的 限 制 , 期 无 法 生 产 原 料 , 终 依 赖 进 长 始
口 …
和氟氧头孢 ( 2 , 图 ) 均是 由 日 本盐 野义制药株式 会社研 究 开发 。拉 氧 头孢 的抗 菌性 能 与 第 三代 头 孢菌 素相 近 , 抗菌 谱与 头 孢 噻肟 近 似 , 多种 革 兰 对
基于头孢类药物中间体氨基噻肟酸合成研究进展

基于头孢类药物中间体氨基噻肟酸合成研究进展头孢类药物是一类广泛应用于临床的抗生素。
其核心结构为β-内酰胺环,通过对环的不同取代,可以得到不同作用谱和药物性质的头孢类化合物。
其中,氨基噻肟酸是头孢类药物的重要中间体,是合成许多头孢类抗生素的前体。
本文将综述近年来关于氨基噻肟酸的合成研究进展。
氨基噻肟酸的合成路线通常有两种,一种是从天然氨基噻唑出发,经过一系列反应,得到氨基噻肟酸;另一种是从噻唑酮类物质出发,通过环加成、取代和消除等反应,构建β-内酰胺环结构,最终合成氨基噻肟酸。
从天然氨基噻唑出发的合成路线,通常包括以下反应:首先将氨基噻唑和芳香醛类的化合物反应,形成噻唑酮,再通过脱羰基、取代等反应,得到氨基噻肟酸。
其中,脱羰基反应的选择性和收率是影响合成效率的重要因素。
目前,通过在噻唑酮与波美度预处理剂之间,加入一些碱性活性剂和催化剂等,可以提高脱羰基反应的选择性和效率。
另外,在氨基噻肟酸合成过程中,由于中间体具有硫辛酸结构,容易被氧气氧化而产生不良副反应。
研究表明,抗氧化剂的加入可以有效抑制氧化反应,提高中间体产率。
另一种合成路线是从噻唑酮类出发,构建β-内酰胺环结构,最终得到氨基噻肟酸。
这种方法通常采用的反应为环加成反应,即将噻唑酮类化合物与另一种含有亲电基团的化合物反应形成环状结构,再通过消除反应打开环得到氨基噻肟酸。
在环加成反应中,催化剂的选择和反应条件对于反应效率和产率有重要影响。
目前研究中常用的催化剂为铜催化剂、氧化铁催化剂、盐酸等。
此外,环加成反应中还需要解决的问题是反应选择性和反应废物的处理。
针对这些问题,研究者使用了不同的手段,如选择性保护、不对称催化等方法,以提高反应的选择性和收率。
总体来说,随着合成技术的不断发展和研究者对物质反应本质的深入理解,氨基噻肟酸的合成方法得到不断改进和优化。
这些进展为头孢类药物的合成提供了更加高效、经济和绿色的方法。
未来还有许多需要解决的问题和挑战,如更大规模的产业化生产、新型催化剂的研发和反应副产物的处理等。
7α-甲氧基头孢菌素的重要中间体合成路线简析
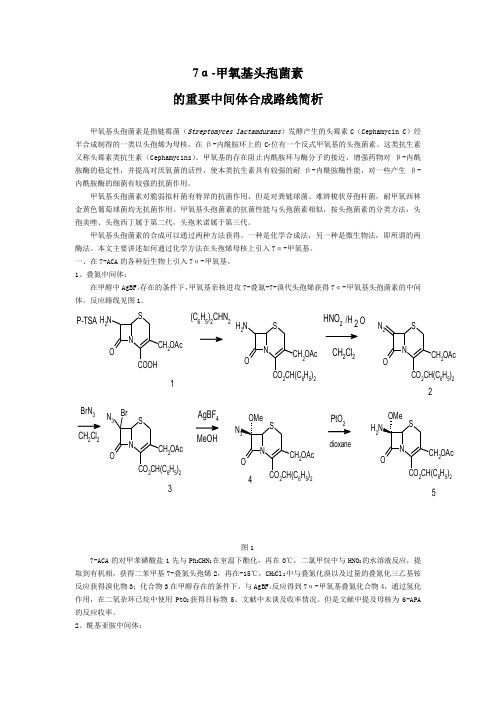
7α-甲氧基头孢菌素 的重要中间体合成路线简析甲氧基头孢菌素是指链霉菌(Streptomyces lactamdurans )发酵产生的头霉素C (Cephamycin C )经半合成制得的一类以头孢烯为母核,在β-内酰胺环上的C 7位有一个反式甲氧基的头孢菌素。
这类抗生素又称头霉素类抗生素(Cephamycins )。
甲氧基的存在阻止内酰胺环与酶分子的接近,增强药物对β-内酰胺酶的稳定性,并提高对厌氧菌的活性,使本类抗生素具有较强的耐β-内酰胺酶性能,对一些产生β-内酰胺酶的细菌有较强的抗菌作用。
甲氧基头孢菌素对脆弱拟杆菌有特异的抗菌作用,但是对粪链球菌、难辨梭状芽孢杆菌,耐甲氧西林金黄色葡萄球菌均无抗菌作用。
甲氧基头孢菌素的抗菌性能与头孢菌素相似,按头孢菌素的分类方法,头孢美唑、头孢西丁属于第二代,头孢米诺属于第三代。
甲氧基头孢菌素的合成可以通过两种方法获得。
一种是化学合成法,另一种是微生物法,即所谓的两酶法。
本文主要讲述如何通过化学方法在头孢烯母核上引入7α-甲氧基。
一、在7-ACA 的各种衍生物上引入7α-甲氧基。
1、叠氮中间体:在甲醇中AgBF 4存在的条件下,甲氧基亲核进攻7-叠氮-7-溴代头孢烯获得7α-甲氧基头孢菌素的中间体。
反应路线见图1。
N SCH 2OAc OCO 2CH(C 6H 5)2N 2N SCH 2OAc ONH 2COOHN SCH 2OAc OCO 2CH(C 6H 5)2N 3Br2OAc 26H 5)22OAc 26H 5)2H 2(C 6H 5)2CHN 2N SCH 2OAc OCO 2CH(C 6H5)2NH2HNO 2CH 2Cl 2BrN 3CH 2Cl 2AgBF 4MeOHPtO 2图17-ACA 的对甲苯磺酸盐1先与Ph 2CHN 2在室温下酯化,再在0℃,二氯甲烷中与HNO 2的水溶液反应,提取到有机相,获得二苯甲基7-叠氮头孢烯2,再在-15℃,CH 2Cl 2中与叠氮化溴以及过量的叠氮化三乙基铵反应获得溴化物3;化合物3在甲醇存在的条件下,与AgBF 4反应得到7α-甲氧基叠氮化合物4,通过氢化作用,在二氧杂环已烷中使用PtO 2获得目标物5。
新法合成头孢他啶中间体溴代异丁酸叔丁酯

107新法合成头孢他啶中间体α-溴代异丁酸叔丁酯田克情1, 杨丽2 赵有贵1 胡亚伟1 申玉双1(1 河北化工医药职业技术学院化学与环境工程系, 河北 石家庄 050026;2 河北远征药业有限公司 河北石家庄 050000)摘 要:以异丁酸和液溴为原料,通过控制反应条件将酰化和α-氢取代两步反应“一锅烩”进行合成了α-溴代异丁酰溴,α-溴代异丁酰溴和叔丁醇反应得到α-溴代异丁酸叔丁酯,通过单因素实验和正交试验的方法确定出酯化反应的最佳工艺条件,即n(酰溴):n(叔丁醇):n(催化剂)=1:1.2:0.5,三聚磷酸钠做催化剂,四氢呋喃做溶剂,反应温度65℃,反应时间4h,产率达95%,化合物结构经1H NMR 进行确证。
关键词:α-溴代异丁酸叔丁酯;“一锅烩”法;正交试验;中试研究中图分类号:O625.53 文献标识码:A 文章编号:1003-5168(2012)22-0107-02头孢他啶又名头孢羟甲噻肟,是一种新型的具有较高安全性、抗绿脓杆菌有效且不引起出血倾向的第三代头孢菌素。
头孢他啶是目前市场上销售量较大的头孢类药物之一,由于头孢他啶的专利保护期已于2001年到期,目前国内约有20多家制药企业获得国家食品药品监督管理局的批准文号,因此,头孢他啶上游产品的需求量日益增多 。
α-溴代异丁酸叔丁酯是合成头孢菌类药物的重要医药中间体[3-5],它是生产头孢他啶的中间体之一。
目前国内生产该中间体的公司较少,多数分布在南方,采用的合成方法多数对环境污染较大,且生产能力较低不能满足国内的需求。
河北省石家庄及环渤海经济圈是全国重要的原料药、医药中间体生产地,经调研发现,目前仅石家庄周边就有多个医药化工公司需要使用大量的α-溴代异丁酸叔丁酯,如河北金通化工有限公司,晋州昌运化工有限公司等。
根据调研结果并受企业委托,对传统的α-溴代异丁酸叔丁酯的生产工艺进行了改进,设计了如Scheme 1所示的合成路线。
Br 2C O HCH 3CH 3CH 3CH 3BrC O CH 3C BrO CH 3C O CH 3C BrC CH 3CH 3CH 3CH 3CH C O O CH 3Scheme 1新法合成α-溴代异丁酸叔丁酯 1 实验部分 1.1 仪器与试剂BRUKERAC-P 500型核磁共振仪;PE-M-1730型红外光谱仪;美国PMG 型质谱仪;异丁酸,溴,红磷为市售化学纯,三聚磷酸钠,叔丁醇,四氢呋喃为市售分析纯,且做无水干燥处理。
一种溴化反应合成头孢活性酯中间体的方法[发明专利]
![一种溴化反应合成头孢活性酯中间体的方法[发明专利]](https://img.taocdn.com/s3/m/cdcdfe222cc58bd63086bd89.png)
专利名称:一种溴化反应合成头孢活性酯中间体的方法专利类型:发明专利
发明人:高令峰,郑庚修,张启龙,孙伟,卢伟阳,付凯,张希诚申请号:CN202010534453.8
申请日:20200612
公开号:CN111592471A
公开日:
20200828
专利内容由知识产权出版社提供
摘要:本发明属于医药化工领域,具体涉及一种溴化反应合成头孢活性酯中间体的方法。
本发明以tert‑butyl()‑2‑((2‑methoxy‑2‑oxoethoxy)imino)‑3‑oxobutanoate为原料,溴素作为溴源,通过使用文丘里泵混合技术,能够有效提高原料与溴素的微观接触,减少一溴代产物与溴素的微观接触,控制局部高浓度溴素引起的多溴化,提高溴化的选择性,一溴代产品的选择性提高到85%以上,副反应少,成本低,产品纯度99.5%以上,能够有效降低多溴代产物的生成,操作更简便,符合绿色化工的要求,适合工业化生产。
申请人:济南大学,山东金城医药化工有限公司
地址:250022 山东省济南市市中区南辛庄西路336号
国籍:CN
代理机构:济南誉丰专利代理事务所(普通合伙企业)
代理人:赵凤
更多信息请下载全文后查看。
青霉素合成新型头孢菌素中间体——GCLE的研究共21页文档

结论
总之,GCLE是非常具有生命力的中间体, 它的出现给青霉素工业盐开辟了新的时代,又 由于它的起始原料是廉价的青霉素, 因此积极开发GCLE是当前抗生素工业的热 点之一,这对我国民族医药工业的发展意义 重大。
66、节制使快乐增加并使享受加强。 ——德 谟克利 特 67、今天应做的事没有做,明天再早也 是耽误 了。— —裴斯 泰洛齐 68、决定一个人的一生,以及整个命运 的,只 是一瞬 之间。 ——歌 德 69、懒人无法享受休息之乐。——拉布 克 70、浪费时间是一桩大罪过。——卢梭
合成GCLE技术
合成GCLE的关键是青霉素扩环和卤化过程, 卤化过程可在扩环过程中进行,也可在闭环后 完成,还可通过还原后的3-环外双键化合物直 接卤化得到。
闭环前卤化
采用硫代亚磺酸酯为亚磺酸捕捉剂,对位于亚 磺酸捕捉体的侧链3-甲基-3-丁烯酸的烯丙位进 行卤化,卤化试剂为电解含有硫酸的饱和 NaCI溶液所产生的Cl2、HOCl、Cl2O等烯型活 性氯化剂,最后用氨水闭环,得到所需的3-氯 甲基-△3—头孢烯酸。
其简易工艺流程如下:
闭环后卤化
由3-去乙酰氧基头孢(7-ADCA)出发直接 丙位溴化,虽易进行,但卤化后将生成的 △ —烯而失去药效,因此必须将△ —烯进一 步氧化成△3—烯,再还原得到3-卤代甲基头 孢。因此,闭环后卤化常用的方法是先将3-甲 基头孢菌素氧化,再通过光溴化得到3-溴甲基 亚砜体,然后经过还原得到目标化合物。但收 率只有55% —61%。当R1基团为苯乙酰氨基 时,也会生成一半的苄基溴化的副产物。
国内研究进展
国内已有以青霉素为起始原料,经氧化、 酯化、开环、氯化、闭环等反应制得GCLE, 其总收率为50%,纯度为97%,其中改进了 氯化和闭环反应。
三溴氧磷溴代反应机理

三溴氧磷溴代反应机理
三溴氧磷溴代反应是一种常见的有机合成反应,其机理涉及多个步骤。
本文将以三溴氧磷溴代反应机理为主题,详细介绍每个步骤的具体过程和反应条件。
三溴氧磷溴代反应是一种通过磷中心离子的溴代反应。
该反应通常在有机合成中用于引入溴原子,形成新的有机溴化合物。
三溴氧磷是一种常用的溴化试剂,它可以与底物发生取代反应,将溴原子引入到有机分子中。
反应的第一步是三溴氧磷与底物(通常是烯烃或芳香化合物)发生加成反应,生成一个中间体。
中间体是一个五元环的离子,其中磷原子与底物中的一个碳原子形成共价键。
接下来的步骤是一个溴离子的迁移过程。
在这个过程中,中间体中的一个溴原子会离开,并与另一个碳原子形成新的共价键。
这个步骤是一个亲核取代反应,其中溴离子作为亲核攻击底物中的一个碳原子。
在反应的最后一步中,离开基会从中间体中离开,形成最终的产物。
这个过程是一个消除反应,其中离开基与中间体中的一个溴原子形成新的共价键,并且中间体中的其他原子重新排列以形成最终的产物。
三溴氧磷溴代反应的机理是一个复杂的过程,涉及多个中间体和过渡态。
为了实现该反应,通常需要适当的反应条件。
反应的温度和溴代试剂的浓度是影响反应速率和产率的重要因素。
溴代反应的底物结构也会影响反应的速率和产物选择性。
例如,烯烃底物通常比芳香化合物更容易发生溴代反应,因为烯烃中的π键更易被破坏。
三溴氧磷溴代反应是一种重要的有机合成反应,可以用于引入溴原子。
通过详细了解其机理和反应条件,我们可以更好地应用该反应,并在有机合成中取得更好的效果。
溴代三嗪生产工艺

溴代三嗪生产工艺
溴代三嗪是一种重要的有机化合物,广泛应用于医药、农药、染料、光敏剂等领域。
其生产工艺包括以下几个步骤:
1. 原料准备:以三氨基嘧啶为原料,通过氧化、硝化、氯化等化学反应制得。
2. 溴代反应:将三氨基嘧啶与溴化钠在适当的溶剂和反应条件下进行反应,得到溴代三嗪。
3. 中间体处理:通过一系列的中间体处理步骤,将溴代三嗪转化为目标产物。
这些步骤包括还原、水解、烷基化等反应。
4. 精制与提纯:通过吸附剂、溶剂萃取、结晶等方法对产物进行精制与提纯,得到高纯度的溴代三嗪。
以上是溴代三嗪的生产工艺流程,其中每个步骤的反应条件、催化剂、溶剂等都需要精确控制,以确保产品质量和产量的稳定。
随着科技的不断进步,溴代三嗪的生产工艺也在不断优化和改进,以适应市场需求和环保要求。
- 1 -。
光催化溴代反应

光催化溴代反应
光催化溴代反应是一种在特定光催化剂的存在下,使溴化物离子与有机物发生取代反应,从而生成溴代产物的有机化学反应。
其中,光催化剂在吸收光能后,电子被激发到高能级,然后通过与溴化物离子的反应产生活性中间体。
这种活性中间体接着与有机物发生取代反应,最终生成溴代产物和其他副产物。
实现光催化溴代反应的过程通常包括选择合适的光催化剂,如能吸收可见光的钛酸钡(BaTiO3)、二氧化钛(TiO2)等。
这些催化剂可以通过各种方式制备成纳米颗粒、薄膜等不同形式,以便提高其活性和表面积。
此外,还需要设计一个连续流反应系统,该系统应包括光光源、反应室以及用于溴代反应的底物。
总之,光催化溴代反应是一种利用光催化剂将溴化物离子与有机物进行溴代反应的化学反应,该反应在化学合成、材料科学等领域具有广泛的应用前景。
三溴氧磷溴代反应机理

三溴氧磷溴代反应机理三溴氧磷溴代反应是有机化学中的一种重要反应,其机理研究对于理解和掌握有机化学的基本原理和反应规律具有重要意义。
本文将以三溴氧磷溴代反应机理为标题,分析其反应过程和机理。
三溴氧磷(PBr3)是一种常见的卤代磷试剂,具有强烈的溴代作用。
在有机合成中,PBr3常常用于将羟基(-OH)转化为卤代基(-Br)。
三溴氧磷溴代反应可以通过两个步骤进行,即亲核进攻和消除反应。
在亲核进攻步骤中,三溴氧磷(PBr3)首先与羟基(-OH)发生反应,形成一个中间体。
这个中间体是一个溴化磷酸酯(RO-PBr2)。
在此反应中,三溴氧磷(PBr3)作为亲核试剂攻击羟基的氧原子,将一个溴原子取代羟基中的氧原子。
这个亲核进攻反应是一个亲核取代反应,反应机理符合斯尼2(S_N2)机理。
消除反应是三溴氧磷溴代反应的第二个步骤。
在这个步骤中,溴化磷酸酯(RO-PBr2)进一步与三溴氧磷(PBr3)发生反应,生成溴代磷酸酯(RO-PBr)和氢溴酸(HBr)。
这个消除反应是一个消除取代反应,反应机理符合斯尼1(S_N1)机理。
总体来说,三溴氧磷溴代反应是一个两步反应,包括亲核进攻和消除反应。
亲核进攻步骤中,三溴氧磷(PBr3)作为亲核试剂攻击羟基的氧原子,形成溴化磷酸酯(RO-PBr2)。
消除反应步骤中,溴化磷酸酯(RO-PBr2)进一步与三溴氧磷(PBr3)发生反应,生成溴代磷酸酯(RO-PBr)和氢溴酸(HBr)。
三溴氧磷溴代反应在有机合成中具有广泛的应用。
它可以将羟基(-OH)转化为卤代基(-Br),从而引入新的官能团。
此外,三溴氧磷溴代反应还可以用于合成其他重要有机化合物,如醚、酮等。
总结起来,三溴氧磷溴代反应是一种重要的有机化学反应,其机理包括亲核进攻和消除反应两个步骤。
在亲核进攻步骤中,三溴氧磷(PBr3)攻击羟基的氧原子,形成溴化磷酸酯(RO-PBr2)。
在消除反应步骤中,溴化磷酸酯(RO-PBr2)进一步与三溴氧磷(PBr3)发生反应,生成溴代磷酸酯(RO-PBr)和氢溴酸(HBr)。
溴代肟醚生产工艺

溴代肟醚生产工艺
溴代肟醚(Bromoalkyl phenyl ether)是一类含有溴和酯基的化合物,常用于有机合成反应中作为中间体。
生产溴代肟醚的工艺可以通过以下步骤实现:
1. 原料准备:首先需要准备相应的苯酚和溴代烷烃(如溴丙烷)作为原料。
这些原料需要经过检验和处理,确保其质量符合要求。
2. 反应步骤:将苯酚和溴代烷烃加入到反应容器中,在适当的条件下进行反应。
通常情况下,反应温度会控制在适宜的范围内(通常为100-150摄氏度),并使用催化剂或其他辅助剂来促进反应的进行。
3. 分离纯化:反应结束后,需要对反应混合物进行分离和纯化。
这可能涉及到蒸馏、萃取、结晶等分离技术,以得到目标产物溴代肟醚的纯品。
4. 产品收集与储存:最后,收集纯净的溴代肟醚产物,并进行适当的储存和包装,以确保其稳定性和安全性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Bromination research of oxacephem intermediate
XIA Xiao.don91,YUAN Hon91,LUO Zhong.meil,YE Jia-linl,CAO Sheng—hual‘,DING Xiao.don92‘ (1.Sichuan Industrial Institute of Antibiotics,China National Pharmaceutical Group Corporation,Chengdu 610052,China;
1HNMR(3001VlHz,CDCl3,艿):1.95(S,3H), 4.42(q,2H,.,=9.46Hz),5.40(d,1 H,J= 3.34Hz),6.09(d,1H,.,=3.35Hz),6.92(8,1H), 7.25.7.98(in,15H,ArH)。 1HNMR(300MHz,CDCl3,6):2.33(S,3H), 4.03(q,2H,.,=9.86Hz),5.39(d。IH,J= 3.34Hz),6.09(d,1H,.,=3.351-I,,),6.97(S,1H), 7.26-7.94(m,15H,ArH)。
2结果与讨论
经过对产物核磁数据和原料核磁数据的对比 分析鉴定,产物结构如图3。
A:异丙烯基表
唑啉3 g(6.6 ret001)搅拌溶于15 mL四氯化碳中,
通氮气保护,加入NBSl.77 g(9.9 rnm01),升温至 35℃,光照条件下,反应2 h,TLC检测已无原料, 有两个主产物点,还有少量杂质点。待冷至室温 后,加入1 g亚硫酸氢钠,搅拌5 rain后,再加人饱 和碳酸氢钠溶液,继续搅拌2h,分液,有机层用 10%氯化钠溶液洗一次,加入无水硫酸钠干燥后 抽滤,减压浓缩得油状物,过柱(洗脱剂,石油醚: 乙酸乙酯=10:1),分离两个主产物。 B:异丙烯基表唑啉3 g(6.6 mmo|)搅拌溶于 10 mL四氯化碳中,通氮气保护,溴素1.58 g(9.9 mm01)溶于5 mL四氯化碳中,缓慢滴加。升温至 35℃,光照条件下,反应l h后TLC检测已无原 料,仍是两个主产物点。板上看基本无其他杂质。 待冷至室温后,加入l g亚硫酸氢钠,搅拌5 rain 后,再加入饱和碳酸氢钠溶液,继续搅拌2 h,分 液,有机层用10%氯化钠溶液洗一次,加入无水硫 酸钠干燥,抽滤。减压浓缩得油状物,过柱(洗脱 剂,石油醚:乙酸乙酯=10:1),分离两个主产物。 经TLC分析,采用NBS和液溴进行溴代分别 得到的两个产物,对应的风值均相同,将R,值对 应相同的产物合并,分别做核磁共振氢谱,数据如
2。Analytical&Testing Center,Sichuan University,Chengdu
610064,China)
Abstract:Starting from
tection
6一APA(6一aminopenicillanic acid),the
isopropenylepioxazoline WU synthesized
下:
图1拉氧头孢
F喀l
0
Imamoxef
FYs\/JL
I
F
r洲 s划、铲 k—N
图2氟氧头孢
Fi&2 Flomoxef
喻
EbN,(CH3)3S iCI
1实验部分
1.1实验试剂与仪器 1.1.1试剂异丙烯基表唑咻:自制;四氯化碳: 成都科龙试剂有限公司;NBS(Ⅳ.溴代丁二酰亚
胺):成都科龙试剂有限公司;液溴:成都科龙试剂 有限公司;亚硫酸氢钠:成都科龙试剂有限公司; 碳酸氢钠:成都科龙试剂有限公司 1.1.2仪器ZF-I型三用紫外分析仪、B0ehi Ro- tavapor R—114型旋转蒸发仪、DF一101S即热式恒温 加热磁力搅拌器、SHZ-D(1lI)型循环水式真空泵、
methyl
70,一methoxy—l--oxaeephemt[J].Tetra伽,1979,20
(28).35I-354.
[3]邢其毅.基础有机化学(第三版)[M].北京:高等教育
出版社。2005:341-342.
(责任编辑罗娟)
万方数据
clization and rearrangement Two brominauxl isomers were obtained with the u∞of NBS and bromine。and their structures were testi— fled by 1H-NMR.
Key
words:oxaceph咖intermediate;isopropenylepioxazoline;bromination 阴性菌有良好抗菌作用。氟氧头孢的抗菌谱和其 他第三代头孢菌素相似,对革兰阳性菌的抗菌作 用几乎与拉氧头孢相同,抗菌性能与第四代头孢 菌素相近。两者均对口-内酰胺酶有较好的稳定性 在我国,氧头孢烯类药品的开发至今仍受到技术 上瓶颈的限制,长期无法生产原料,始终依赖进
througlI
five main steps:pro-
by benzoylationtoxidation of sulfur,protection by diphenylmethyl ester,the iso-merlzation of7・』flllino group,ag well∞decy-
殳一
图3
Fig.3
两个异构物的结构式
The two brominated isomers
NBS和液溴两者与异丙烯基表唑啉的反应产 物并无差异。根据结构鉴定的结果可以看出,所 得到的两个主要产物均不是目标化合物,而是在 异丙烯基的另一个只含有一个氢的碳上进行的自 由基取代反应,得到的两个立体异构体。 理论上推断可能的反应机理是由子烯键和羰 基中间的碳原子形成自由基以后,形成一个共轭 体系,更有利于形成的自由基的稳定。同时烯键 和羰基中间的碳具有手性,形成自由基之后,溴自 由基可以从正反两个方向进攻,最终得到两个立 体异构体。而氯代反应的机理可能不是经过一个 自由基的历程¨J。
(300MI-Iz,CDa3,艿):1.79(s,3i-i),4.92(8,lrl),5.06 (s,IH),5-19(s,li-i),5.34(s,1H),5.35(d,1H,歹= 3.18Hz),&02(d,1H,J=3.23Hz),6.89(s,tH),7.25— 7.88(m,15H,ArH)。 1.2.2异丙烯基表唑啭的溴化
万方数据
第4期
HO
夏小冬等:氧头孢中间体的溴代反应研究
651
我国氧头孢烯类抗生素的发展主要受限于氧 头孢烯母核(719-氨基.3・氯甲基一1-氧代一3・头孢一4-
S
,啦
羧酸二苯甲酯)的合成,它需要一个重要中间
体——异丙烯基表唑啉,通过卤代,水解,闭环3
步反应得到。其中,卤代反应是整个氧头孢中间 体合成的瓶颈。有文献报道可以采用直接通入氯 气的方法进行异丙位的氯代【2】,但是实际操作过 程中发现氯气的量不好控制,而且收率不高。 因此本文试图通过Ⅳ.溴代丁二酰亚胺(NBS) 以及液溴尝试进行改进口J。本实验拟合成路线如
口【¨。
抗感染药物占我国药品市场份额的四分之 一,是使用量和金额最大的一类药物。其中头孢 类抗感染药在抗感染药物中间占到5产品目前只有拉氧头孢(图1) 和氟氧头孢(图2),均是由日本盐野义制药株式 会社研究开发。拉氧头孢的抗菌性能与第三代头 孢菌素相近,抗菌谱与头孢噻肟近似,对多种革兰
第24卷第4期 2012年4月
化学研究与应用
Chemical Research and Application
V01.24.No.4
Apr。,2012
文章编号:1004・1656(2012)04-0650-03
氧头孢中间体的溴代反应研究
夏小冬1,袁 红1,罗忠枚1,叶家林1,曹胜华h,丁小东2。
(1.中国医药集团总公司 四川抗菌素工业研究所,四川成都610052; 2.四川大学分析测试中心,四川成都610064)
收稿日期:2012-01-09;修回日期:2012-03-1l
联系人简介:曹胜华(1960-),男,研究员,主要研究方向:抗生素和抗肿瘤药物的合成与应用研究。E-硼Iil:∞憾IIcngIlua2t瑚@sins.啪;
丁小东(1969・),男,副研究员,主要研究方向:药物的合成及分析方法。E-mail:dingxi@163.00m
摘要:以6-APA(6-氨基青霉烷酸)为原料,经过苯甲酰化保护。硫的氧化,二苯甲酯保护,7位氨基异构化,开 环重排,得到异丙烯基表唑啉。用NBS,溴素分别尝试进行溴代,最终得到馕个溴代物异构体,并经过核磁共 振氢谱对结构进行了确证。 关键词:氧头孢中间体;异丙烯基表唑啉;溴代
中图分类号:0626.2 文献标识码:A
参考文献: [1]周平凡.我国非典型p内酰胺类抗生素的发展现状
[J].河j匕化T,2006.29(8):64-66. [2]Mitsuru Yoshioka,Temji Tauji,Shoichiro reoeontrolled。straighffo州ard
synthesis IJyeo,et a1.Ste— of 3-substituted
万方数据
652
化学研究与应用
F:
第24卷
DLSB.10/30低温冷却液循环泵、ZK-82A型真空干
燥箱、BRUKERACF—300 MHz核磁共振仪 1.2实验方法 1.2.1异丙烯基表唑啉的合成6一APA为原料, 苯甲酰氯作为氨基酰化试剂,双氧水氧化,一锅 煮。经后处理得到苯甲酰青霉素亚砜。由二苯甲 酮腙经氧化后与2位羧基成酯,得到苯甲酰基保 护的青霉素亚砜酯。在三甲基氯硅烷和强碱作用 下,对7位氨基进行异构化,最后使用三苯基膦进 行开环反应,后处理重结晶的到异丙烯基表唑啉。 1111.P:1 14.3-1 16.7。C,核磁共振氢谱数据如下:‘HNIVIR
