【化学】培优 易错 难题铁及其化合物推断题辅导专题训练附详细答案
【化学】化学铁及其化合物推断题的专项培优 易错 难题练习题(含答案)含答案解析

【化学】化学铁及其化合物推断题的专项培优易错难题练习题(含答案)含答案解析一、铁及其化合物1.某盐A是由三种元素组成的化合物,且有一种为常见金属元素,某研究小组按如下流程图探究其组成:请回答:(1)写出组成 A的三种元素符号______。
(2)混合气体B的组成成份______。
(3)写出图中由C转化为E的离子方程式______。
(4)检验E中阳离子的实验方案______。
(5)当A中金属元素以单质形式存在时,在潮湿空气中容易发生电化学腐蚀,写出负极的电极反应式______。
【答案】Fe、O、S SO2和SO3 Fe2O3+6H+=2Fe3++3H2O 取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+ Fe-2eˉ=Fe2+【解析】【分析】由红棕色固体溶于盐酸得到棕黄色溶液,可知C为氧化铁、E为氯化铁溶液,说明A中含有铁元素和氧元素,1.6g氧化铁的物质的量为 1.6g160g/mol=0.01mol;由气体B与足量氯化钡溶液反应生成白色沉淀可知,白色沉淀D为硫酸钡、气体B中含有三氧化硫,由硫原子个数守恒可知,三氧化硫的物质的量为 2.33g233g/mol=0.01mol,气体B的物质的量为0.448 22.4/LL mol=0.02mol,由A是由三种元素组成的化合物可知,A中含有硫元素、气体B为二氧化硫和三氧化硫的混合气体,二氧化硫的物质的量为(0.02—0.01)mol=0.01mol,m (SO3)+m(SO2)+m(Fe2O3)=0.01mol×80g/mol+0.01mol×64g/mol+1.6g=3.04g,说明A 中nFe):n(S):n(O)=1:1:4,则A为FeSO4。
【详解】(1)由分析可知,A为FeSO4,含有的三种元素为Fe、O、S,故答案为:Fe、O、S;(2)由分析可知,三氧化硫的物质的量为 2.33g233g/mol=0.01mol,气体B的物质的量为0.448 22.4/LL mol=0.02mol,由A是由三种元素组成的化合物可知,A中含有硫元素、气体B为二氧化硫和三氧化硫的混合气体,故答案为:SO2和SO3;(3)C为氧化铁、E为氯化铁溶液,氧化铁与盐酸反应生成氯化铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;(3)E为氯化铁溶液,检验铁离子的实验方案为可取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+,故答案为:取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+;(5)铁在潮湿空气中容易发生电化学腐蚀,铁做原电池的负极,失去电子发生氧化反应生成亚铁离子,电极反应式为Fe-2eˉ=Fe 2+,故答案为:Fe-2eˉ=Fe 2+。
培优 易错 难题铁及其化合物推断题辅导专题训练附详细答案

培优易错难题铁及其化合物推断题辅导专题训练附详细答案一、铁及其化合物1.某强酸性溶液 X 中可能含有 Fe2+、Fe3+、Al3+、Ba2+、NH4+、CO32-、NO3-、SO42-、SiO32-中的若干种,现取 X 溶液进行连续实验,实验过程及产物如图所示。
实验过程中有一种气体为红棕色。
根据以上信息,回答下列问题:(1)由强酸性条件即可判断 X 溶液中肯定不存在的离子有_____。
(2)溶液 X 中关于硝酸根离子的判断,正确的是_____(填编号,下同)。
a.一定含有 b.一定不含有 c.可能含有(3)气体 F 的电子式为_____,化合物 I 中含有的化学键类型有_____。
(4)转化①的离子方程式为_____。
转化⑦的离子方程式为_________。
(5)对不能确定是否存在的离子,可以另取 X 溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是_____。
①NaOH 溶液②KSCN 溶液③氯水和 KSCN 的混合溶液④pH 试纸⑤KMnO4溶液【答案】CO32-、SiO32- b 共价键和离子键 3Fe2+ +4H+ +NO3-= 3Fe3++NO↑ +2H2O AlO2-+2H2O+CO2===HCO3-+Al(OH) 3↓②【解析】【分析】某强酸性溶液X中一定含有氢离子,一定不含CO32-、SiO32-,加过量的硝酸钡溶液,产生白色沉淀C是硫酸钡,一定含有SO42-,一定不含Ba2+,产生气体A一定是亚铁离子和硝酸根离子、氢离子发生氧化还原反应得到的NO,所以一定含有Fe2+,一定不含NO3-,NO 遇到氧气转化为气体D为二氧化氮,二氧化氮与水、氧气反应生成溶液E为硝酸溶液,溶液B中加入过量氢氧化钠生成气体F,F为氨气,则原溶液中一定含有NH4+,氨气和硝酸溶液反应生成I为硝酸铵,溶液H中通入过量二氧化碳产生沉淀K和溶液L,沉淀K一定为氢氧化铝,原溶液中一定含有Al3+,L是NaHCO3,溶液B中生成的有铁离子,所以沉淀G是Fe(OH)3,溶于盐酸得到J为氯化铁溶液,但原溶液中不一定含有Fe3+。
【化学】化学 铁及其化合物推断题的专项 培优 易错 难题练习题含答案

【化学】化学铁及其化合物推断题的专项培优易错难题练习题含答案一、铁及其化合物1.将铁、铝的混合物进行如下实验:(1)操作X的名称是________。
(2)气体A是________(填化学式)。
(3)A与Cl2混合光照可能发生爆炸,A在该反应中作________(填“氧化剂”或“还原剂”)。
(4)溶液B中的阴离子除OH-外还有________(填离子符号,下同),溶液D中存在的金属离子为________。
(5)加入足量NaOH溶液时发生反应的离子方程式为___________;加入稀盐酸发生反应的离子方程式为_________。
(6)向溶液D中加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:___________。
【答案】过滤 H2还原剂 AlO2- Fe2+ 2Al+2OH-+2H2O=2AlO2-+3H2↑ Fe+2H+=Fe2++H2↑ 4Fe(OH)2+O2+2H2O=4Fe(OH)3【解析】【分析】金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,溶液B是NaAlO2与NaOH的混合溶液,固体C是Fe,Fe是比较活泼的金属,与HCl发生置换反应产生FeCl2和氢气,因此溶液D为FeCl2,据此分析解答。
【详解】(1)操作X的名称是分离难溶性的固体与可溶性液体混合物的方法,名称是过滤,故答案为:过滤;(2)根据上述分析可知,金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,故答案为:H2;(3)A是H2,H2和Cl2的混合气体光照会发生爆炸,反应生成HCl,在该反应中,氢元素的化合价升高,失去电子,被氧化,所以H2作还原剂,故答案为:还原剂;(4)溶液B是反应产生的NaAlO2与过量的NaOH的混合溶液,所以溶液B中阴离子除OH-外还有AlO2-,铁可以和盐酸反应生成FeCl2和H2,溶液D中含有的金属离子为Fe2+,故答案为:AlO2-;Fe2+;(5)加入足量NaOH溶液时,Al与NaOH溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,加入稀盐酸,Fe与稀盐酸反应生成氢气和氯化亚铁,发生反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为2Al+2OH-+2H2O=2AlO2-+3H2↑;Fe+2H+=Fe2++H2↑;(6)溶液D为FeCl2,向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,其中沉淀转化的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
备战高考化学 铁及其化合物推断题 培优易错试卷练习(含答案)附答案解析

备战高考化学铁及其化合物推断题培优易错试卷练习(含答案)附答案解析一、铁及其化合物1.物质X是某新型净水剂的中间体,它可以看成由AlCl3(在180℃升华)和一种盐A按物质的量之比1:2组成。
在密闭容器中加热X使之完全分解,发生如下转化:请回答下列问题:(1)X的化学式为__。
(2)将E混合晶体溶于水配成溶液,向溶液中加入过量稀NaOH溶液时发生的总反应的离子方程式为__。
(3)高温下,若在密闭容器中长时间煅烧X,产物中还有另外一种气体,请设计实验方案验证之_。
【答案】AlCl3·2FeSO4 Al3++2H++6OH-=AlO2-+4H2O 将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2【解析】【分析】固体氧化物B溶于稀盐酸后得到的溶液C中滴加KSCN溶液,混合液变血红色,说明B中含有Fe3+,则B为Fe2O3,C为FeCl3溶液,无色D气体能使品红褪色,则D为SO2,由元素守恒可知A中含有Fe、S、O元素,A加热分解能生成氧化铁和二氧化硫,则盐A为FeSO4,氧化铁的物质的量为3.2g160g/mol=0.02mol,生成二氧化硫为0.448L22.4L/mol=0.02mol,由Fe、S原子为1:1可知生成SO3为0.02mol,4.27g混合晶体E为AlCl3和SO3,AlCl3的物质的量为4.27g-0.02mol80g/mol133.5g/mol=0.02mol,X的组成为AlCl3∙2FeSO4,以此解答该题。
【详解】(1)根据上述分析,X的化学式为AlCl∙2FeSO4;(2)将E混合晶体溶于水配成溶液,三氧化硫反应生成硫酸,则硫酸与氯化铝的物质的量相等,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为:Al3++2H++6OH-=AlO2-+4H2O;(3)若在高温下长时间煅烧X,生成的三氧化硫再分解生成二氧化硫和氧气,另一种气体分子式是O2,检验氧气的方法为:将气体通入足量NaOH溶液中,收集余气,把一条带火星的本条伸入其中,若复燃,则说明是O2。
化学 铁及其化合物推断题的专项 培优 易错 难题练习题含答案解析

化学 铁及其化合物推断题的专项 培优 易错 难题练习题含答案解析一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
化学铁及其化合物推断题的专项培优 易错 难题练习题附答案解析

化学铁及其化合物推断题的专项培优易错难题练习题附答案解析一、铁及其化合物1.物质X是某新型净水剂的中间体,它可以看成由AlCl3(在180℃升华)和一种盐A按物质的量之比1:2组成。
在密闭容器中加热X使之完全分解,发生如下转化:请回答下列问题:(1)X的化学式为__。
(2)将E混合晶体溶于水配成溶液,向溶液中加入过量稀NaOH溶液时发生的总反应的离子方程式为__。
(3)高温下,若在密闭容器中长时间煅烧X,产物中还有另外一种气体,请设计实验方案验证之_。
【答案】AlCl3·2FeSO4 Al3++2H++6OH-=AlO2-+4H2O 将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2【解析】【分析】固体氧化物B溶于稀盐酸后得到的溶液C中滴加KSCN溶液,混合液变血红色,说明B中含有Fe3+,则B为Fe2O3,C为FeCl3溶液,无色D气体能使品红褪色,则D为SO2,由元素守恒可知A中含有Fe、S、O元素,A加热分解能生成氧化铁和二氧化硫,则盐A为FeSO4,氧化铁的物质的量为3.2g160g/mol=0.02mol,生成二氧化硫为0.448L22.4L/mol=0.02mol,由Fe、S原子为1:1可知生成SO3为0.02mol,4.27g混合晶体E为AlCl3和SO3,AlCl3的物质的量为4.27g-0.02mol80g/mol133.5g/mol=0.02mol,X的组成为AlCl3∙2FeSO4,以此解答该题。
【详解】(1)根据上述分析,X的化学式为AlCl∙2FeSO4;(2)将E混合晶体溶于水配成溶液,三氧化硫反应生成硫酸,则硫酸与氯化铝的物质的量相等,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为:Al3++2H++6OH-=AlO2-+4H2O;(3)若在高温下长时间煅烧X,生成的三氧化硫再分解生成二氧化硫和氧气,另一种气体分子式是O2,检验氧气的方法为:将气体通入足量NaOH溶液中,收集余气,把一条带火星的本条伸入其中,若复燃,则说明是O2。
【化学】培优易错试卷铁及其化合物推断题辅导专题训练附答案解析

【化学】培优易错试卷铁及其化合物推断题辅导专题训练附答案解析一、铁及其化合物1.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:(1)写出下列物质的化学式:B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】Al HCl 杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH- +2H2O=2AlO2-+3H2↑【解析】【分析】金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;判断C为Fe,以此解答该题。
【详解】根据上述分析可知A是Na,B是Al,C为Fe,气体甲是H2,气体乙是Cl2,气体丙是HCl;D是NaOH,E是盐酸,F是FeCl2,G是FeCl3,H是Fe(OH)3。
(1)根据上述分析可知,物质B是Al,丙是HCl;(2)黄绿色气体乙是Cl2,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;(3)FeCl2与NaOH溶液发生反应:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,Fe(OH)2具有还原性,容易被溶解在溶液中的氧气氧化,发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,固体由白色迅速变为灰绿色,最后变为红褐色,因此可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变成红褐色;(4)反应③是Al与NaOH溶液发生反应产生NaAlO2和H2,反应的离子方程式为:2Al+2OH- +2H2O=2AlO2-+3H2↑。
培优 易错 难题铁及其化合物推断题辅导专题训练附答案解析

培优易错难题铁及其化合物推断题辅导专题训练附答案解析一、铁及其化合物1.某固体化合物A,按图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
回答下列问题:(1)物质A是___(填化学式)。
(2)反应②的离子反应方程式为___。
(3)反应④的化学反应方程式为___。
【答案】Fe(OH)3 Fe2O3+6H+=2Fe3++3H2O 4Fe(OH)2+O2+2H2O=4Fe(OH)3【解析】【分析】已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液,据此分析。
【详解】已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液。
(1)依据推断可知A为Fe(OH)3;(2)反应②是盐酸和氧化铁发生的复分解反应,反应的离子反应方程式为Fe2O3+6H+=2Fe3++3H2O;(3)反应④是氢氧化亚铁和氧气水发生反应生成氢氧化铁的也还原反应,反应的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
2.某强酸性溶液 X 中可能含有 Fe2+、Fe3+、Al3+、Ba2+、NH4+、CO32-、NO3-、SO42-、SiO32-中的若干种,现取 X 溶液进行连续实验,实验过程及产物如图所示。
实验过程中有一种气体为红棕色。
根据以上信息,回答下列问题:(1)由强酸性条件即可判断 X 溶液中肯定不存在的离子有_____。
(2)溶液 X 中关于硝酸根离子的判断,正确的是_____(填编号,下同)。
a.一定含有 b.一定不含有 c.可能含有(3)气体 F 的电子式为_____,化合物 I 中含有的化学键类型有_____。
培优 易错 难题铁及其化合物推断题辅导专题训练及答案

培优易错难题铁及其化合物推断题辅导专题训练及答案一、铁及其化合物1.X、Y、Z、W 为四种常见元素,其中 X、Y、Z 为短周期元素。
ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,W原子的最外层电子数小于4且W 的常见化合价有+3、+2,WX3的稀溶液呈黄色,回答下列问题:(1)X在元素周期表的位置________________,其简单阴离子的结构示意图为____________________,用电子式表示X的氢化物的形成过程______________________________。
(2)Z的氧化物在通讯领域用来作_______________。
锗与Z是同一主族元素,它可用来制造半导体晶体管。
研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH溶液反应但在有H2O2存在时可与NaOH溶液反应生成锗酸盐,反应的化学方程式为:_______________________________(3)W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:____________________________________,若灼烧W(OH)2固体得到___________。
【答案】第三周期ⅦA族光导纤维 Ge + 2H2O2 +2NaOH = Na2GeO3 + 3H2O 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Fe2O3【解析】【分析】根据元素的性质及用途等信息分析元素的种类;根据核外电子排布情况确定在元素周期表中的位置;根据物质的性质及反应的现象书写反应方程式,及用相关化学用语表示物质的组成和结构。
【详解】Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,则Z为硅;ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,则X 为氯;Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,则Y为铝;W原子的最外层电子数小于4且W的常见化合价有+3、+2,WX3的稀溶液呈黄色,则W为铁;(1)X为氯元素,在元素周期表的位置为:第三周期ⅦA族;氯离子的结构示意图为:;用电子式表示HCl的形成过程:;(2)Z为硅,二氧化硅在通讯领域用作光导纤维;根据题干信息知锗NaOH溶液在有H2O2存在时反应生成锗酸盐,反应的化学方程式为:Ge + 2H2O2 + 2NaOH = Na2GeO3 + 3H2O;(3)反应现象知该反应为氢氧化亚铁被氧化为氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3,Fe(OH)3不稳定,灼烧分解得到固体Fe2O3。
【化学】培优 易错 难题铁及其化合物推断题辅导专题训练附答案解析
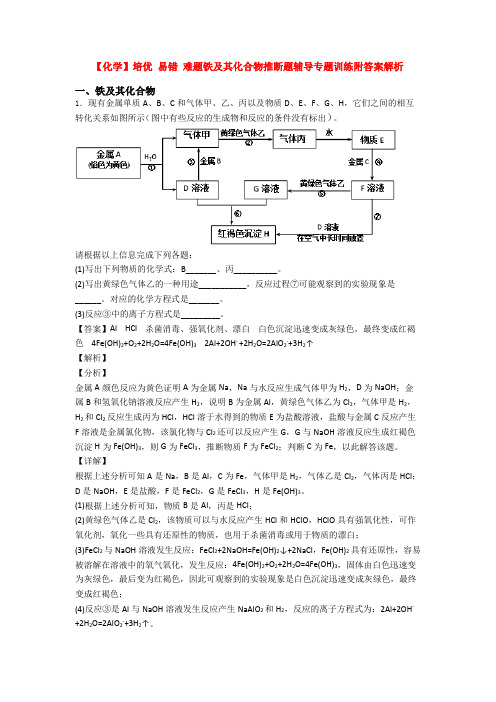
【化学】培优易错难题铁及其化合物推断题辅导专题训练附答案解析一、铁及其化合物1.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:(1)写出下列物质的化学式:B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】Al HCl 杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH- +2H2O=2AlO2-+3H2↑【解析】【分析】金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;判断C为Fe,以此解答该题。
【详解】根据上述分析可知A是Na,B是Al,C为Fe,气体甲是H2,气体乙是Cl2,气体丙是HCl;D是NaOH,E是盐酸,F是FeCl2,G是FeCl3,H是Fe(OH)3。
(1)根据上述分析可知,物质B是Al,丙是HCl;(2)黄绿色气体乙是Cl2,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;(3)FeCl2与NaOH溶液发生反应:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,Fe(OH)2具有还原性,容易被溶解在溶液中的氧气氧化,发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,固体由白色迅速变为灰绿色,最后变为红褐色,因此可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变成红褐色;(4)反应③是Al与NaOH溶液发生反应产生NaAlO2和H2,反应的离子方程式为:2Al+2OH- +2H2O=2AlO2-+3H2↑。
高考化学培优 易错 难题(含解析)之铁及其化合物推断题附详细答案

高考化学培优 易错 难题(含解析)之铁及其化合物推断题附详细答案一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
备战高考化学知识点过关培优 易错 难题训练∶铁及其化合物推断题含详细答案

备战高考化学知识点过关培优易错难题训练∶铁及其化合物推断题含详细答案一、铁及其化合物1.已知A、B、C、D四种物质均含有铁元素,彼此转化关系如下:请回答:(1)反应①称为铝热反应(属于置换反应),写出该反应的化学方程式:__、其中Al作__剂。
(2)反应④的离子方程式为:__。
(3)新配制的C溶液中应加入__,以防止其转化为D。
检验D溶液中阳离子的常用试剂是__(填化学式),实验现象为__。
【答案】2Al+Fe2O3高温2Fe+Al2O3还原剂 2Fe2++H2O2+2H+=2Fe3++2H2O 铁粉(屑) KSCN (或NH4SCN)溶液变红(或呈现血红色)【解析】【分析】氧化铁与铝单质在高温下发生铝热反应,生成A,则A为Fe,铁和水蒸气在高温下反应生成B,B为黑色磁性氧化物,则B为Fe3O4,Fe3O4中铁元素的化合价含有+2、+3价,与盐酸反应生成FeCl3和FeCl2,铁与过量盐酸反应生成FeCl2,则C为FeCl2,FeCl2与双氧水反应生成FeCl3,则D为FeCl3,据此分析解答。
【详解】(1)反应①称为铝热反应(属于置换反应),该反应的化学方程式:2Al+Fe2O3高温2Fe+Al2O3,反应中Al有0价变为+3价,化合价升高,失电子,被氧化,作还原剂;(2)反应④为FeCl2与双氧水反应生成FeCl3,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;(3)C为FeCl2,D为FeCl3,亚铁离子具有还原性,易被氧化,新配制的FeCl2溶液中应加入铁粉(屑),以防止其转化为FeCl3。
检验三价铁离子常用试剂是KSCN(或NH4SCN),三价铁离子遇SCN-变为血红色溶液。
2.A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应。
(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是__________。
【化学】化学铁及其化合物推断题的专项培优 易错 难题练习题(含答案)附答案解析

【化学】化学铁及其化合物推断题的专项培优易错难题练习题(含答案)附答案解析一、铁及其化合物1.将铁、铝的混合物进行如下实验:(1)操作X的名称是________。
(2)气体A是________(填化学式)。
(3)A与Cl2混合光照可能发生爆炸,A在该反应中作________(填“氧化剂”或“还原剂”)。
(4)溶液B中的阴离子除OH-外还有________(填离子符号,下同),溶液D中存在的金属离子为________。
(5)加入足量NaOH溶液时发生反应的离子方程式为___________;加入稀盐酸发生反应的离子方程式为_________。
(6)向溶液D中加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:___________。
【答案】过滤 H2还原剂 AlO2- Fe2+ 2Al+2OH-+2H2O=2AlO2-+3H2↑ Fe+2H+=Fe2++H2↑ 4Fe(OH)2+O2+2H2O=4Fe(OH)3【解析】【分析】金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,溶液B是NaAlO2与NaOH的混合溶液,固体C是Fe,Fe是比较活泼的金属,与HCl发生置换反应产生FeCl2和氢气,因此溶液D为FeCl2,据此分析解答。
【详解】(1)操作X的名称是分离难溶性的固体与可溶性液体混合物的方法,名称是过滤,故答案为:过滤;(2)根据上述分析可知,金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,故答案为:H2;(3)A是H2,H2和Cl2的混合气体光照会发生爆炸,反应生成HCl,在该反应中,氢元素的化合价升高,失去电子,被氧化,所以H2作还原剂,故答案为:还原剂;(4)溶液B是反应产生的NaAlO2与过量的NaOH的混合溶液,所以溶液B中阴离子除OH-外还有AlO2-,铁可以和盐酸反应生成FeCl2和H2,溶液D中含有的金属离子为Fe2+,故答案为:AlO2-;Fe2+;(5)加入足量NaOH溶液时,Al与NaOH溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,加入稀盐酸,Fe与稀盐酸反应生成氢气和氯化亚铁,发生反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为2Al+2OH-+2H2O=2AlO2-+3H2↑;Fe+2H+=Fe2++H2↑;(6)溶液D为FeCl2,向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,其中沉淀转化的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
备战高考化学 铁及其化合物推断题 培优 易错 难题练习(含答案)附答案解析

备战高考化学铁及其化合物推断题培优易错难题练习(含答案)附答案解析一、铁及其化合物1.A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示。
(1)若A为强碱,C、D常被用做食用“碱”。
C→ D反应的离子方程式为 ______________。
(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,则检验D溶液中金属阳离子的试剂为_____________,D→ C反应的离子方程式为___________。
(3)若A为非金属单质,D是空气中的主要温室气体。
D还可以转化为A,写出该反应的化学方程式_________。
【答案】CO32-+ CO2 + H2O = 2HCO3- KSCN溶液 2Fe3++ Fe = 3Fe2+ 2Mg+ CO2点燃2MgO +C【解析】【分析】(1)若A为强碱,C、D常被用做食用“碱”,应为碳酸钠和碳酸氢钠,根据反应流程可知,A 为氢氧化钠,与少量二氧化碳反应生成C为碳酸钠,与足量二氧化碳反应生成D为碳酸氢钠,碳酸钠溶液通入二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水;(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,根据流程可推知A为铁,B为硝酸,过量的铁与稀硝酸反应生成C为硝酸亚铁,少量的铁与稀硝酸反应生成D为硝酸铁,硝酸亚铁与硝酸反应生成硝酸铁,硝酸铁与铁反应生成硝酸亚铁;(3)若A为非金属单质,D是空气中的主要温室气体CO2。
根据流程可知A为碳,碳在氧气不足的条件下燃烧生成C为CO,在氧气充足时燃烧生成D为CO2,CO在氧气中燃烧生成CO2,CO2与C在高温条件下反应生成CO。
【详解】(1)若A为强碱,C、D常被用做食用“碱”,应为碳酸钠和碳酸氢钠,根据反应流程可知,A 为氢氧化钠,与少量二氧化碳反应生成C为碳酸钠,与足量二氧化碳反应生成D为碳酸氢钠,碳酸钠溶液通入二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水,故C→ D反应的离子方程式为CO32-+ CO2 + H2O = 2HCO3-;(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,根据流程可推知A为铁,B为硝酸,过量的铁与稀硝酸反应生成C为硝酸亚铁,少量的铁与稀硝酸反应生成D为硝酸铁,硝酸亚铁与硝酸反应生成硝酸铁,硝酸铁与铁反应生成硝酸亚铁,则检验D溶液中金属阳离子Fe3+的试剂为KSCN溶液,D→ C反应的离子方程式为2Fe3++ Fe = 3Fe2+;(3)若A为非金属单质,D是空气中的主要温室气体CO2。
【化学】化学铁及其化合物推断题的专项培优易错试卷练习题(含答案)附答案

【化学】化学铁及其化合物推断题的专项培优易错试卷练习题(含答案)附答案一、铁及其化合物1.室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。
在合适反应条件下,它们可以按下面框图进行反应;E是无色溶液,F是淡绿色溶液。
B和C反应发出苍白色火焰。
请回答:(1)A是__________,B是__________,C是__________(请填写化学式);(2)反应①的化学方程式______________________________;(3)反应③的离子方程式______________________________;(4)反应④的离子方程式______________________________。
【答案】Fe Cl2 H2 2Fe+3Cl22FeCl3 Fe+2H+=Fe2++H2↑ 2Fe2++Cl2=2Fe3++2Cl-【解析】【分析】室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体,B是氯气,B和C反应发出苍白色火焰,C是氢气,E是氯化氢。
F是淡绿色溶液,F溶液中含有亚铁离子,所以A是铁,F是氯化亚铁,D是氯化铁,据以上分析解答。
【详解】室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体,B是氯气,B和C反应发出苍白色火焰,C是氢气,E是氯化氢。
F是淡绿色溶液,F溶液中含有亚铁离子,所以A是铁,F是氯化亚铁,D是氯化铁,(1)根据以上分析可知A、B、C分别是Fe、Cl2、H2;(2)反应①为铁与氯气反应生成氯化铁,化学方程式为2Fe+3Cl22FeCl3;(3)反应③为铁与盐酸反应生成氯化亚铁和氢气,离子方程式为Fe+2H+=Fe2++H2↑;(4)反应④为氯化亚铁与氯气反应生成氯化铁,离子方程式为2Fe2++Cl2=2Fe3++2Cl-。
2.A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系:其中①②③均为有单质参与的反应。
(1)若A是常见的金属,①③中均有同一种黄绿色气体参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式_________________________。
备战高考化学培优 易错 难题(含解析)之铁及其化合物推断题及详细答案

备战高考化学培优易错难题(含解析)之铁及其化合物推断题及详细答案一、铁及其化合物1.已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G为黄绿色;形成D的元素原子的最外层电子数是次外层的3倍;B的焰色反应呈紫色(透过蓝色钴玻璃);K为红棕色粉末。
其转化关系如图。
请回答:(1)工业上制C用A不用H的原因______________________。
(2)写出C与K反应的化学方程式_________________,该反应的反应物总能量___________(填“大于”或“小于”)生成物总能量。
(3)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,接通电源(短时间)电解E水溶液的化学方程式___________________。
(4)写出E物质的电子式___________________。
(5)J与H反应的离子方程式为________________________。
(6)写出G与熟石灰反应制取漂白粉的化学方程式_______________________。
【答案】氯化铝是共价化合物,熔融状态下不导电 2Al+Fe2O3高温Al2O3+2Fe 大于2KCl+2H2O2KOH+H2↑+Cl2↑ Al3++3AlO2-+6H2O=4Al(OH)3↓2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O【解析】【分析】【详解】形成D的元素的原子最外层电子数是次外层的3倍,原子只能有2个电子层,最外层电子数为6,则D为O2;K为红棕色固体粉末,K为Fe2O3;由于电解A得到C与D,则C与K 生成A的反应为铝热反应,故A为Al2O3,L为Fe,C为Al;黄绿色气体G为Cl2,与C反应得到H为AlCl3;B的焰色反应呈紫色(透过蓝色钴玻璃),B中含有K元素,B在催化剂、加热条件下反应生成氧气,则B为KClO3,E为KCl,电解KCl溶液生成KOH、H2和Cl2,过量的F与氯化铝反应得到J,则I为H2,F为KOH,J为KAlO2;(1)H为AlCl3,氯化铝是共价化合物,熔融状态下不导电,故工业上制Al用氧化铝不用氯化铝,故答案为氯化铝是共价化合物,熔融状态下不导电;(2)C与K反应的化学方程式为:2Al+Fe2O3高温Al2O3+2Fe,该反应为放热反应,故该反应的反应物总能量大于生成物总能量,故答案为2Al+Fe2O3高温Al2O3+2Fe;大于;(3)Fe是目前应用最广泛的金属,用碳棒作阳极,Fe作阴极,接通电源(短时间)电解KCl水溶液的化学方程式为:2KCl+2H2O 电解2KOH+H2↑+Cl2↑,故答案为2KCl+2H2O 电解2KOH+H2↑+Cl2↑;(4)E为KCl,KCl的电子式为,故答案为;(5)J与H反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为Al3++3AlO2-+6H2O=4Al(OH)3↓;(6)G为Cl2,G与熟石灰反应制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
备战高考化学知识点过关培优 易错 难题训练∶铁及其化合物推断题附详细答案

备战高考化学知识点过关培优 易错 难题训练∶铁及其化合物推断题附详细答案一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
备战高考化学铁及其化合物推断题(大题培优 易错 难题)及答案

备战高考化学铁及其化合物推断题(大题培优易错难题)及答案一、铁及其化合物1.A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应。
(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是__________。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是________,反应③的化学方程式是____。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是________。
【答案】2Fe2++Cl2=2Fe3++2Cl-4NH3+5O24NO+6H2O 2C+SiO22CO↑+Si【解析】(1). A是常见的金属单质,D、F是气态单质,反应①为置换反应且在水溶液中进行,由转化关系可知,A为变价金属,F具有强氧化性,则A为Fe,F为Cl2、B为HCl、C为氯化亚铁、D为氢气、E为氯化铁,反应②(在水溶液中进行)的离子方程式是:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;(2). B、C、F都是气态单质,B有毒,则B为氯气,反应②需要放电条件才能发生,为氮气与氧气反应,③反应中有水生成,可以推知C为N2,F为O2,E为NO,A为NH3,反应①为置换反应,A、D相遇有白烟生成,可推知D为HCl,A与D反应产物为氯化铵,电子式为,反应③的化学方程式是:4NH3+5O24NO+6H2O,故答案为:;4NH3+5O24NO+6H2O;(3). A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,反应①为置换反应,考虑是碳与二氧化硅反应生成硅与CO,碳与F反应生成E,CO与F生成E,则F为氧气,通过验证符合图示转化关系,则反应①的化学方程式是2C+SiO22CO↑+Si,故答案为:2C+SiO22CO↑+Si。
备战高考化学 铁及其化合物推断题 培优 易错 难题练习(含答案)含答案

备战高考化学铁及其化合物推断题培优易错难题练习(含答案)含答案一、铁及其化合物1.已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加D溶液,白色沉淀逐渐消失。
(1)则各是什么物质的化学式为:A_______、B_______、C_______、D_______。
(2)现象②中所发生的反应的化学方程式为:__________________________________、______________________________。
(3)现象③中所发生反应的离子方程式为:__________________________________、________________________________。
【答案】BaCl2 FeSO4 AlCl3 NaOH; FeSO4 + 2NaOH=Fe(OH)2↓+ Na2SO4 4Fe(OH)2 + O2+ 2H2O=4Fe(OH)3 Al3+ + 3OH-=Al(OH)3↓ Al(OH)3 + OH-=AlO2- + 2H2O【解析】【分析】①A+B→白色沉淀,加入稀硝酸,沉淀不溶解应,则生成的白色沉淀为BaSO4,②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色,是Fe(OH)2的转化为Fe(OH)3,故A 为BaCl2,B为FeSO4,D为NaOH,则C为AlCl3,氯化铝溶液与NaOH溶液反应生成白色沉淀Al(OH)3,Al(OH)3能溶解在NaOH溶液中,符合③中现象。
【详解】(1)根据以上分析可知A、B、C、D依次为BaCl2、FeSO4、AlCl3、NaOH;(2)现象②先生成白色沉淀,在空气中放置,沉淀由白色转化为红褐色时所发生的反应的化学方程式为:FeSO4 + 2NaOH=Fe(OH)2↓+ Na2SO4,4Fe(OH)2+O2+2H2O=4Fe(OH)3;(3)现象③中所发生反应的离子方程式为:Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【化学】培优易错难题铁及其化合物推断题辅导专题训练附详细答案一、铁及其化合物1.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:(1)写出下列物质的化学式:B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】Al HCl 杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 2Al+2OH- +2H2O=2AlO2-+3H2↑【解析】【分析】金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;判断C为Fe,以此解答该题。
【详解】根据上述分析可知A是Na,B是Al,C为Fe,气体甲是H2,气体乙是Cl2,气体丙是HCl;D是NaOH,E是盐酸,F是FeCl2,G是FeCl3,H是Fe(OH)3。
(1)根据上述分析可知,物质B是Al,丙是HCl;(2)黄绿色气体乙是Cl2,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;(3)FeCl2与NaOH溶液发生反应:FeCl2+2NaOH=Fe(OH)2↓+2NaCl,Fe(OH)2具有还原性,容易被溶解在溶液中的氧气氧化,发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,固体由白色迅速变为灰绿色,最后变为红褐色,因此可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变成红褐色;(4)反应③是Al与NaOH溶液发生反应产生NaAlO2和H2,反应的离子方程式为:2Al+2OH- +2H2O=2AlO2-+3H2↑。
【点睛】本题是无机物推断,物质的颜色及转化关系中特殊反应是物质推断的突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,试题培养了学生的分析能力及逻辑推理能力。
2.下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。
已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。
请回答下列问题:(1)A在B中燃烧的现象是__________________________________________。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是_________________________。
(3)G+J→M的离子方程式是____________________________________。
(4)Y受热分解的化学方程式是______________________________________。
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是 ____________________。
【答案】放出大量的热,产生苍白色火焰 2:1 3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓4Fe(NO3)3Δ2Fe2O3+12NO2↑+3O2↑酸性高锰酸钾溶液【解析】【分析】F是地壳中含量最多的金属元素的单质,则F为Al,转化关系中X电解得到三种物质,为电解电解质与水型,A、B为气态单质,二者为氢气和氯气,二者反应生成D,D为HCl,E 为黑色固体,为氧化物,和HCl反应又生成B气体,A为H2,B为Cl2,E为MnO2,电解X 是电解氯化钠溶液,C为NaOH,与Al反应生成G,G为NaAlO2;M为红褐色沉淀为Fe(OH)3,所以J是含三价铁离子的物质,是H和D反应生成,证明J为FeCl3,H、I为氧化物判断H为Fe2O3,I为红棕色气体为NO2,结合转化关系可知,N为HNO3,Y为Fe(NO3)3,结合物质的性质来解答。
【详解】(1) A为H2,B为Cl2,H2在Cl2中燃烧的现象是:气体安静燃烧,放出大量的热,火焰呈苍白色,并有白雾产生;(2) D+E→B的反应为MnO2+4HCl加热MnCl2+Cl2↑+2H2O,MnO2中Mn元素化合价降低,被还原,HCl 中Cl元素化合价升高,被氧化,4mol盐酸参与反应,发生氧化反应的盐酸为2mol,另外2mol盐酸显酸性,则n(被氧化的物质HCl):n(被还原的物质MnO2)=2:1;(3) G(NaAlO2)+J(FeCl3)→M(Fe(OH)3)的反应是在水溶液中发生的双水解反应,反应离子方程式是:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓;(4)依据分析推断可知Y为Fe(NO3)3,受热分解生成二氧化氮和氧化铁,依据原子守恒配平书写的化学方程式是:4Fe(NO3)3Δ2Fe2O3+12NO2↑+3O2↑;(5)检验硫酸铁溶液中是否存在Fe2+的方法是取少量待测液于试管中,滴加几滴酸性高锰酸钾溶液,若溶液紫色褪去,证明原溶液中含有Fe2+,反之没有Fe2+。
3.已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。
在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
请回答下列问题:(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。
则B的化学式为__。
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是__。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___。
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是___。
【答案】FeCl3 Al(OH)3+OH-=AlO2-+2H2O 2H2S+SO2═3S+2H2O CO32-+CO2+H2O═2HCO3-【解析】【分析】(1)D是生产、生活中用量最大、用途最广的金属单质,则D是铁,A可用于自来水消毒,A为Cl2;(2)若D是氯碱工业的主要产品之一,B有两性,D为NaOH、B为Al(OH)3;(3)C是形成酸雨的主要气体,则A为H2S、D为O2、B为S、C为SO2;(4)若A的焰色反应呈黄色,说明A中含有Na元素,且A、B、C均含有同一种元素据此分析。
【详解】(1)D是生产、生活中用量最大、用途最广的金属单质,则D是铁,A可用于自来水消毒,由转化关系可知,A为Cl2、B为FeCl3、C为FeCl2;(2)若D是氯碱工业的主要产品之一,B有两性,由转化关系可知,A为铝盐、D为NaOH、B为Al(OH)3、C为NaAlO2,反应②为氢氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的离子方程式是:Al(OH)3+OH−=AlO2−+2H2O;(3)若A、C、D都是常见气体,C是形成酸雨的主要气体,则A为H2S、D为O2、B为S、C 为SO2,反应③为硫化氢与二氧化硫反应生成硫和水,反应的化学方程式为:2H2S+SO2═3S+2H2O;(4)若A的焰色反应呈黄色,D为二氧化碳,由转化关系可知,A为NaOH、B为Na2CO3、C 为NaHCO3,反应②为碳酸钠溶液与二氧化碳反应生成碳酸氢钠,反应的的离子方程式是:CO32−+CO2+H2O═2HCO3−。
4.某化学兴趣小组探究氯化铁溶液的某些性质,将一定量氯化铁固体先加入含1molHCl的浓盐酸中,再加水配制成1L溶液A。
(1)若在A溶液中加入一块铜片,一段时间后得溶液B。
写出铜片在FeCl3溶液中反应的离子方程式:___;(2)若在B中加铁粉mg,充分反应后剩余固体ng;过滤,从1L滤液中取出20mL,向其中滴入40mL2mol/LAgNO3溶液时,Cl-恰好完全沉淀。
则溶液A中FeCl3的物质的量浓度是__;(3)若在A溶液中加铁粉至不再溶解,则需铁粉__克。
【答案】2Fe3++Cu= Cu2++2Fe 1mol/L 56g【解析】【分析】【详解】(1)Fe3+有较强氧化性,可将Cu氧化成Cu2+,离子方程式为2Fe3++Cu= Cu2++2Fe;(2)若在B中加铁粉mg,充分反应后剩余固体ng,则此时滤液中溶质只有FeCl2,滴入40mL2mol/LAgNO3溶液时,Cl-恰好完全沉淀,则20mL滤液中n(Cl-)=0.04L×2mol/L=0.08mol,则1L滤液中n(Cl-)=0.08mol×1000mL20mL=4mol,加入了1molHCl,则溶液中n(Cl-)=4mol-1mol=3mol,则n(FeCl3)=1mol,溶液体积为1L,所以溶液A中FeCl3的物质的量浓度是1mol/L;(3)A中加铁粉发生反应2Fe3++Fe=3Fe2+、2H++Fe=Fe2++H2↑,溶液中n(FeCl3)=1mol,n(HCl)=1mol,所以消耗的铁粉物质的量为0.5mol+0.5mol=1mol,质量为56g。
【点睛】解决此类题目要注意寻找守恒关系,不能盲目写反应方程式;第3题要注意HCl也可以与铁粉反应。
5.以下是与氧气性质有关的实验,回答相关问题。
(1)写出铜和氧气反应的化学方程式__。
(2)写出铁丝在氧气中燃烧的化学方程式__,该反应的实验现象为__。
(3)硫燃烧时瓶底盛少量水的作用是__,硫在氧气中燃烧比在空气中燃烧更剧烈的原因是因为___不同。
【答案】2Cu+O22CuO 3Fe+2O2Fe3O4剧烈燃烧,火星四射,放出热量,生成黑色固体吸收生成的二氧化硫气体,防止污染空气氧气浓度【解析】【详解】(1)该实验的原理是:铜粉与氧气反应生成氧化铜;发生反应的化学方程式为2Cu+O22CuO;(2)该铁丝在氧气中燃烧生成了四氧化三铁,该反应的化学方程式是:3Fe+2O2点燃Fe3O4 ;反应的实验现象是:剧烈燃烧,火星四射,生成黑色固体;(3)由于二氧化硫是对大气有污染的气体,做硫在氧气燃烧的实验时瓶底盛放少量水的作用是:吸收二氧化硫防止污染空气;硫在空气中燃烧产生淡蓝色火焰、在氧气中燃烧蓝紫色火焰,氧气中氧气的浓度比空气中氧气的浓度要大。
6.铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:问题1:铁为何称为黑色金属?问题2:CuO在高温下可分解为 Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?(1)对于问题1,同学们上网查找,有两种解释:A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属①你认为正确的说法是__________。
