中美两国药品流通模式比较与分析
我国药品质量管理体系及欧美发达国家药品质量管理体系的异同

我国药品质量管理体系与欧美发达国家药品质量管理体系的异同摘要:通过对我国药品质量管理体系与欧美发达国家药品管理体系的构成及其要素的介绍,比较他们的异同,促进药品生产企业质量管理水平的普遍提高。
说明建立一个全面质量管理体系对保障药品质量的重要性,构建符合新版GMP。
关键词:质量管理体系;新版GMP;1、国外药品质量管理发展历史和现状在五六十年代经过了一系列的国际药害事件后,美国政府发现单以抽查检验为药品质量的保障方式存在较大的不确定性,而药品生产过程控制对保证药品质量发挥着重要的作用。
正是由于对保障药品质量的认识理念从药品生产结果的抽检到药品生产过程的保证之巨大转变,1962年美国食品药品监督管理局(简称FDA)制定实施了全球首版GMP。
FDA工作人员将对国内外的生产企业,进口的各类产品进行跟踪检查,并抽取样品进行检查【1】,另外,FDA对药品上市后的不良反应也非常重视,每年约收到400000份产品不良报告【2】在此之后,欧美各国纷纷建立了各自的药品GMP,1975年WHO也正式向全球公布GMP 规范。
1982年在国内医药产业不断发展的推动下,参照先进国家药品质量保障的经验和理念,。
国际ICH组织分别于2005年11月颁布《Q9药品风险管理》,2008年6月颁布《QlO 药品质量体系》,2008年7月欧盟将《Q9药品风险管理》的内容纳入GMP指南中,2009年4月美国FDA参照ICH发布了《符合制药cGMP法规要求的质量系统》指导性文件,正式将风险管理的理念引人药品质量体系建设中。
国际上,主要发达国家一系列介绍和推广新质量管理理念的指南文件相继颁布实施,标志着药品行业进入了一个质量管理的新纪元【3—6】。
1.1 欧盟1994年以设在法国的欧洲药典委员会秘书处为基础成立了欧洲药品质量管理局(EDQM)。
EDQM主要功能之一是对上市后的仿制药品的监督管理,其主要监督手段是对产品的符合性签证和对通过欧洲各国官方药品检验所(OMCL)之间的欧洲网络系统来对药品的市场监督【7】.另外,上市后药品监督的另一种方法是不良反应监测【8—9】,例如最近在意大利发生了减肥药西布曲明的死亡事件,中止了该品种的上市销售【10】。
中美药品注册审批制度比较研究一种行政法的视角

中美药品注册审批制度比较研究一种行政法的视角一、本文概述药品注册审批制度在全球范围内具有举足轻重的地位,它直接关系到药品的安全性和有效性,影响着公众的健康和生命安全。
中美两国作为世界上最大的药品市场之一,其药品注册审批制度的完善与否,对于全球药品监管具有示范和引领作用。
因此,本文旨在从行政法的视角出发,对中美两国的药品注册审批制度进行深入的比较研究,以期为我国药品监管制度的完善提供有益的借鉴和启示。
本文将简要介绍药品注册审批制度的基本概念、功能及重要性,明确研究背景和目的。
接着,文章将重点对中美两国的药品注册审批制度进行详细的梳理和分析,包括制度框架、审批流程、监管要求、法律责任等方面。
通过对比分析,文章将揭示两国药品注册审批制度的异同点,并探讨其背后的行政法理念和价值取向。
在此基础上,文章将进一步探讨中美药品注册审批制度在实践中面临的挑战和问题,如审批效率、创新激励、公众参与等。
通过深入剖析这些问题,文章将提出针对性的完善建议,以期推动中美两国药品注册审批制度的持续改进和优化。
文章将总结研究成果,强调药品注册审批制度在保障药品安全有效方面的重要作用,并呼吁全球各国加强药品监管合作,共同推动药品注册审批制度的进步和发展。
二、美国药品注册审批制度概述美国的药品注册审批制度,作为其整个医药监管体系的核心组成部分,一直以来都以其严谨、高效和透明而备受全球关注。
美国的药品注册审批制度主要由美国食品与药品监督管理局(Food and Drug Administration,简称FDA)负责执行。
FDA在保障公众健康、确保药品安全有效方面发挥着至关重要的作用。
在美国,药品的注册审批过程被称为新药申请(New Drug Application,简称NDA)。
这一过程的核心在于确保新药在投放市场前,已经通过了严格的安全性、有效性评估。
申请人需要向FDA提交详尽的研究资料,包括药物的临床前研究、临床试验数据、药品的生产工艺和质量控制等信息。
国内外医药电商发展现状与趋势分析

国内外医药电商发展现状与趋势分析随着互联网的快速发展,电子商务已经成为我们生活中的一部分。
而医药电商作为电子商务的一种形式,已经越来越受到人们的关注。
本文将对国内外医药电商的发展现状与趋势进行分析。
一、国内医药电商发展现状目前,国内医药电商领域已经呈现出了良好的发展态势。
据不完全统计,截至2020年底,我国已有超过500家医药电商平台,其中绝大多数是以B2B模式为主。
持续升级的互联网技术和医疗科技以及政策支持,整个行业发展将更加迅速。
1.在线销售渠道逐渐增加随着消费者的需求不断增长,医药电商逐渐成为一个新的销售渠道。
在线药店、第三方电商平台、市场科技公司和医院医药平台等形式的出现,大大地丰富了消费者的购买方式。
此外,医药电商还引入了虚拟医生、智能问诊等技术,大大方便了人们购买药品。
2.电商与医药重合度提高在新零售时代,医药电商正在和医药产业的生态模式越来越重合。
除了继续扩大品类外,企业开始走向产业链上游和下游,积极掌握更多资源和服务内容,包括配送物流、供应链管理、医疗器械等方面的服务。
此外,由于我国医疗资源不足,医药电商还有利于让更多病人享受医疗资源。
3.政策优惠逐步明朗国家政府在近年来对医药电商提供了大量的政策支持,如“互联网+医疗健康”行动计划、跨境电商政策、国家医药电子商务统一平台等。
这些政策为医药电商的发展提供了有力的保障和指引,也为消费者提供了更多优惠的产品和服务选择。
二、国际医药电商发展趋势国际医药电商在我国的发展也值得借鉴。
以下是国际医药电商的发展趋势:1.礼品卡是电商的趋势消费者在礼品卡上花费的金额不断攀升,在过去两年中增长了近40%。
虽然纸质礼品卡在某些情况下仍然是有效的,但是随着礼品卡。
2.虚拟医疗服务的重要性得到提高在国外,像Teladoc这样的在线医疗服务提供者已经越来越流行。
在医生和患者之间建立信任关系的过程中,虚拟医疗服务已经成为一个非常重要的渠道。
由于在线医疗人数不断增长,对手机应用的需求将继续增长,从而促进了电商的发展。
比较中美两国的医疗保健体系。

比较中美两国的医疗保健体系。
比较中美两国的医疗保健体系医疗保健一直是世界各国亟需解决的问题。
在医疗保健领域,中美两国都各自拥有自己的医疗保健体系。
在这篇文章中,我们将深入比较中美两国医疗保健体系的异同点。
一、医疗保健的支付方式中美两国医疗保健的支付方式有很大的区别。
在中国,由于政府始终掌握着医疗保健系统,因此,所有的医疗费用基本上都由政府承担。
这种医疗保健支付方式促进了中国医疗保健服务的扩张。
而在美国,由于市场力量的作用,医疗费用的支付主要是由私人健康保险、社会救助和个人自费支付等方式来完成。
这种医疗支付方式使得美国的医疗保健服务通常较为昂贵。
二、医疗保健服务质量中美两国的医疗保健服务质量也存在很大的区别。
在中国,由于大部分居民都受益于普及基础医疗服务,大部分医生只能提供较为基础的医疗保健服务。
而在美国,社会教育水平普遍较高,因此医疗保健服务质量较高。
美国医生也有更多的医疗资源来提供优质的医疗保健服务。
三、医疗保健服务可及性中美两国的医疗保健服务可及性也存在很大的区别。
在中国,由于人口数量众多,医生资源较为匮乏,因此许多人在医疗保健服务方面面临着困难。
而在美国,由于医疗保健资源相对较为充足,因此人们更容易获得医疗保健服务。
四、医疗保健体系的监管机制中美两国医疗保健体系的监管机制也有所不同。
在中国,医疗体系主要由政府监管,卫生部长负责制定和实施有关全国卫生计划的政策和计划。
而在美国,州政府和联邦政府都有监管权力,美国食品药品监督管理局负责医疗保健产品和服务的监管。
五、医疗保健服务的价格中美两国的医疗保健服务价格有很大的区别。
在中国,由于医疗保健服务主要由政府提供,因此价格通常较为低廉。
而在美国,由于市场经济的作用,医疗保健服务价格通常较高。
此外,美国医疗保险的价格和性质也有所不同,在美国私人医疗保险的价格和福利状况都有所不同。
总之,在中美两国的医疗保健体系之间存在很大的差异。
尽管两者各自有其优缺点,但是两个国家共同的目标就是为人民提供更全面、更高质量的医疗保健服务。
中国、美国及日本三国连锁药店对比图文分析报告

中国、美国及日本三国连锁药店对比图文分析报告(2017.09.22)2011年后我国药店连锁率逐年提升,特别是2015年,药店行业连锁率增加6.3个百分点。
这很大程度上受2013年6月推行的新版GSP的影响。
新版GSP对于药品零售企业的人员配置、硬件设施及信息系统等提出了更为严格的要求,暴露出单体药店存在的一些问题。
新版GSP与旧版GSP部分内容对比一、新版GSP加剧执业药师紧缺现状,单体药店获取医师成本更高2013年新版GSP规定:1、药品零售企业法定代表人或企业负责人应当具备执业药师资格;2、药品零售企业应当按国家有关规定配备执业药师,负责处方审核,指导合理用药。
我国的执业药师严重不足,药店执业药师配置率低。
截止到2015年底,我国注册执业药师共有257,633名,其中在零售药店工作的药师有218,517名。
由此计算得出,药店执业药师的配置率仅为48.77%。
即使全部执业药师均就职于零售药店,如果按照一店一执业药师的方式配置,理论上也只有57.5%的药店符合规定。
在全国执业药师总数有限的情况下,连锁药店更具竞争优势。
目前来看,单体店每家需配备1-2名执业药师,而连锁药店可5-8家店面共用1名执业药师,这大大降低了连锁药店的经营成本。
以2015年全国执业药师平均年薪5.56万元计算,假设连锁药店5家共用1名药师,单体店1家1名药师,则每家连锁药店的平均人力成本比单体店减少4.45万元。
全国药店平均单店营业收入约90万元(以2015年全国药店数量44.8万家和收入规模4045亿元计算),1名药师的薪酬占比为6.2%(5.56万元/90万元),单体店将比连锁店高出4.9个百分点的费用率(4.45万元/90万元)。
面对职业药师紧缺的现状,职业药师的薪酬将可能进一步提高,连锁药店的成本优势更加明显。
国内外药品监管模式对比研究及其借鉴意义

国内外药品监管模式对比研究及其借鉴意义随着全球化的不断深入,药品也成为了一个涉及全球社会利益的重要话题。
药品作为一种特殊的消费品,其安全和有效性都需要严格监管,而药品监管模式的不同也直接影响了药品的质量和使用效果。
本文将探讨国内外药品监管模式的对比研究及其借鉴意义。
一、国内药品监管现状目前,我国药品监管工作主要由国家药监局负责,其职责主要包括批准药品注册和备案、监管药品生产经营、药品信息发布等。
国家药监局是一个行政部门,其主要考虑的是在政策层面上规范药品监管行为和执法。
同时,我国还有药品监督管理部门、药品药材检验机构等一系列专业机构,致力于维护药品的质量和安全。
然而,我国药品监管存在一些缺陷。
首先,监管部门在药品安全事故发生时,一些监管责任人没有及时履行职责,导致了药品安全问题的进一步扩大。
其次,我国药品市场存在复杂的利益关系,监管部门的管理难度较大。
例如,一些药品经销商不合规经营,有些生产企业也因为利益而不合规操作。
这些都给药品监管部门带来了很大的挑战。
二、国外药品监管现状国外药品监管机构与我国类似,主要包括FDA(美国食品药品监督管理局)、EMA(欧洲药物评估局)等。
这些机构不仅有权对药品从生产到销售的全过程进行监管,还会进行药品的临床试验,以确保药品的安全和有效性。
美国FDA甚至对药品的广告宣传活动和市场信息也进行监管,以确保广告信息真实有效、不误导消费者。
相较于我国,国外药品监管更加严格和权威。
例如FDA,其审批药品的时间和流程很长,需要对药品的生产过程、药品成分、安全性和有效性等方面进行全面的检查评估。
这些步骤虽然繁琐,但能够确保药品的高质量和安全性。
此外,国外药品监管机构还会利用先进的技术手段,对药品进行全面监管,以确保消费者的用药安全。
三、对比与借鉴国内外药品监管机构的对比可以得知,国外的药品监管更加严格和高效。
国外监管机构除了对药品生产过程的监管以外,还会对药品从临床试验到销售和宣传的全过程进行监管,以确保消费者的用药安全和合法权益。
中美药品营销渠道比较及启示

商 业 经 济
S AN E JNG I H GY I J
N . 21 o 6.0 0 Toa No3 2 tl .5
【 文章编号】 1 964( 1) —020 0 -032 00 08—2 0 0 6
中美药 品营销渠道 比较 及启示
m dc ebs esq i e nt c nm dm g t s m,n r t dvl m n ein -o e e er s e ein ui s, u knc s u ̄no oe l scs t adpo e ee p et f d c e cmm r dce et i n c o r o i ye i mo o om i e ct o a h
L e fn IK - a g
Ab ta t o o ae i eUS me ia re n , ed v lp n bly o hn ' p ama e t a nepi si a e, s c :N w cmp rd w t t dc lmak t g t eeo me ta it fC ias h r c u cle trr e wek r r hh i h i i s s w oeaee trr e emoea d po ta it i a e,a dme cllgsi sb k ad Co s eigO lpat a i ain i h lsl nep s sa r n rf l swek r n d a o i c i a w r . n i rn U" rc clst t n i r i b i y i ts c d i u o
道方面, 已经形成了低成本、 高效率的渠道网络系统。对 占到了 4%的比例 , 0 从这些数据中, 可以看出美国制药企 于我国许多的制药企业来说 ,如何进一步完善其营销渠 业对新药研发的重视和所取得成果。药品研发是美国制 性发展的根基 ,更是其在全球药品市场竞 道是 当前 面临着 的一 个重要 问题 , 决这一 问题 , 要解 就需 药企业长期 良 要了解分析美国的药品渠道 ,以更好地学习借鉴他人的 争中获胜的关键。 ( 二) 批发商数量少、 盈利能力强 经验 。
中美两国医药供应链拓扑结构比较研究

健全 药 品供应 体 系 . 一方 面众 多 的 医药 商业 企 业 和 医药 方进 行 生 产 加工 和 包 装 。 后 通 过 分 销商 、 另 然 医疗 服 务提 供
供应 链体 系 面临 着新 一轮 的洗牌 . 纷 “ 纷 圈地 ” 强供 应链 部 门最终 流向用 户 . 是 医药供 应链 也具 有其特 殊性 : 加 但 建设 ,希 望利 用 现代 物流 和供 应 链 管理 技 术来 降低 成 本 、 打造 核心 竞争 力 美 国从 2 O世纪 7 O年 代开 始至 今 三十多 年 的 的时 间形 成 了较成 熟 的市 场 经 济 主导 的 医药 供应 链 ( ) 品 的特 殊性 。药 品作 为 一种 特殊 的商 品 , 1药 与其他 商 品相 比有 明显 的特 征 , 生命 的关 联 性 、 及 高质 量性 、 公共
成员, 包括 新药 研 发 部 门 , 原材料 供 应 商 , 制造 商 , 分销 商 ,
技 术 手段 引入 医药 生产 加工 、 流通 销 售 以及 消 费 的各个 环 医 疗服务 提 供部 门( 医院 和诊 所 等 ) 以及最终 消 费者 ( 图 如 节 . 但可 以达 到资 源 配 置 的 合理 化 . 能 有 效 提高 医药 1 。 供应 链 中存 在三种 流 : 不 还 )在 物流 、 信息 流 、 资金流 。 图示 中
一2 1 第 4 0 2年 期
■现 代 管理 科学
■管 理创新
中美两国医药供应链拓扑结构比较研究
●侯 艳红 丛 萌
摘要: 文章 首先 分析 了中 国医药供 应链 拓 扑结 构特征 及 其历 史演 变 , 并对 医药供应 链 中药品 制造 商 、 分销 商 、 零售 商 以及政府和保险机构等节点成员进行 了分析。 其次, 分析美国医药供应链拓扑结构特点以及美国特 色的 PM B 组织。最后 通 过对 比分析 认 为我 国 医药供 应 链 在减 少层 级 、 建立 类似 PM 织 的 中介机 构 , 持 成 员 间合作 关 系方 面加 以改进 , B组 保 可 以降低 整 个供 应链 的成本 , 高供 应链 的运作 效 率和服 务 水平 。 提 关键 词 : 医药供应 链 ; 扑 结构 ; 拓 药品福 利 管理 者
中美仿制药审批监管的比较分析

中美仿制药审评监管的比较分析
15、工艺验证和工艺能力
对比
内容工艺能力(CPk).pptx
工艺验证不再是一时一事,而是贯穿药品研发生产
的全过程,对产品和工艺的认识理解贯穿整个生命
美国
过程,工艺验证的目的不再是仅仅满足批准的质量 标准,而是保证药品的疗效(intended use)
工艺能力(Process Capability),减少批内和批
中国
只有API通过药品审评审批后,使用该API的制剂 才能获得审评
这一程序限制了制剂的审评
结论 借鉴FDA的关联审评,不单独审评API,节约审评资源
中美仿制药审评监管的比较分析
12、辅料的DMF和药典标准
对比
内容
辅料不要求DMF,大多数辅料在USP中收载 美国 辅料只要符合USP便可用于申报ANDA和NDA
确定如Felodipne,Bupropine等
中国
尚未建立类似橙皮书的药品信息 尚未建立RLD的产生路径
结论
尽快参照FDA的橙皮书,建立中国的橙皮书 RLD如何合法购买应有政策和明确流程
中美仿制药审评监管的比较分析
6、BE试验机构及核查
对比
内容
FDA接受任何国家符合GCP的临床试验机构(CRO)的BE试验结果
不利于企业最初的仿制药立项市场分析
中国
中国仿制药申报无论是BE备案还是受理都会公示; 通过受理品种搜索专家软件或申请人之窗可以查
到
企业知道相关品种在研究、在BE、在审评的数量; 避免企业重复申报
结论 申报品种信息公开,这点中国做的比美国好
中美仿制药审评监管的比较分析
8、仿制药收费
对比
美国医药市场及创新模式

美国医药市场及创新模式美国医药市场的特点之一是高度竞争。
美国拥有众多的医药公司,涉及到制药、生物技术、医疗器械等多个领域。
这种竞争激励了企业提高技术创新和产品质量,促进了市场的发展。
同时,竞争也促使企业在价格上保持良性竞争,使医疗资源更加合理地分配。
其次,美国医药市场具有广泛的渠道和消费者选择。
在美国,患者可以通过众多的渠道购买和获取他们所需的医药产品。
除了传统的药店和医院,零售药店、互联网平台等新兴渠道也逐渐涌现。
这种多元化的渠道促使企业提供更多样化的产品以满足不同消费者的需求。
另一个特点是美国医药市场对创新的高度重视。
美国政府和企业积极鼓励创新,投入大量资源用于药物和医疗器械的研发。
美国拥有世界上最多的专利,是众多创新药物和技术的孵化地。
这种重视创新的氛围吸引了全球各地的研究人员和专业人才前往美国发展,进一步推动了创新的进程。
在创新模式方面,美国医药市场采取了多种途径来促进创新。
首先,美国政府通过合理的知识产权保护、税收优惠和补贴等措施,鼓励企业投入研发并推动技术创新。
同时,美国也鼓励企业之间的合作,通过合作研发和技术转让来加快创新的进程。
其次,美国医药市场具有开放的监管环境。
美国食品药品监督管理局(FDA)是负责批准和监管医药产品的机构,其审批流程相对简明,使新药能够更快地进入市场。
这种开放的监管环境提供了一个更为灵活和创新的发展平台。
此外,美国医药市场还鼓励市场竞争,以推动创新。
美国政府通过政府采购、药品定价和医疗保险等手段来维护竞争,促使企业在价格和质量上不断提高。
这种竞争推动了不断的创新和进步。
然而,美国医药市场也存在一些问题。
医疗成本高昂、医药价格上涨和药物供应短缺等都是当前面临的挑战。
这些问题的解决需要政府和企业继续进行和创新,以推动医药市场的可持续发展。
综上所述,美国医药市场具有高度竞争和创新性,其创新模式通过政府支持、开放监管环境和市场竞争等多种途径推动医药行业的发展。
然而,面临的挑战也需要政府和企业共同努力来解决。
中美创新药注册制度的比较研究

三、结论与建议
通过比较中美两国的创新药注册制度,可以发现两国制度各有特点和优势。 中国制度注重行政审批和监管,确保药品的安全性和有效性;美国制度注重数据 审查和评估,对药品的创新性和市场前景有更高的度。为完善我国创新药注册制 度,提出以下建议:
三、结论与建议
1、加强数据管理和监管:加强临床前研究和临床试验数据的真实性、可靠性 和完整性管理,建立完善的数据审查和监管机制。同时,加强生产环节的监管, 确保药品质量和安全性。
内容摘要
首先,中美两国在仿制药注册监管方面存在一些差异。中国仿制药注册监管 体系相对较为完善,包括药品注册审批、药品生产、药品流通等环节。而美国在 仿制药注册监管方面则更加注重药品的安全性和有效性,要求更加严格。
内容摘要
其次,中美两国在仿制药注册监管方面的差异也体现在审批程序、审批标准 等方面。中国仿制药审批程序相对较为繁琐,审批标准也更加注重药品的安全性 和有效性。而美国则在审批程序和审批标准方面更加灵活,注重药品的适应症和 市场需求。
2、审批流程
2、审批流程
美国FDA的药品审批流程包括申请、审评、审批、上市后监测等多个环节。在 审评环节,FDA采用科学、公开、透明的审评标准,对药品的安全性、有效性和 质量进行全面评估。而中国CDE的药品审批流程相对简单,主要包括申请、审评、 审批三个环节,但在审批环节中缺乏明确的审评标准和公开透明的机制。
文献综述
国内外学者针对中美药品注册审批制度进行了一系列研究。这些研究主要集 中在制度框架、审批流程、监管机构等方面。然而,大多数研究仅某一方面的比 较,缺乏对整体框架和最新改革的系统分析。
比较分析
1、申请要求
1、申请要求
中美药品注册审批制度在申请要求方面存在一定差异。美国食品药品监督管 理局(FDA)对药品申请人的资格没有特殊要求,但申请人需提交完备的技术资 料、临床试验报告等相关文件。而中国药品审评中心(CDE)则对申请人资格有 严格的规定,同时要求申请人提交相关证明文件和临床试验报告等资料。
美国药品流通模式分析与启示

美国药品流通模式分析与启示美国药品流通模式分析及其对全球药品流通模式的启示随着全球医疗水平的提高和医药行业的快速发展,药品流通模式成为了各界的焦点。
美国作为全球最大的药品市场,其药品流通模式具有很高的研究价值。
本文将从美国药品流通模式的历史演变、现状及问题出发,探讨其对全球药品流通模式的启示。
美国药品流通模式的发展历程可以追溯到20世纪中期。
自那时以来,美国药品流通行业经历了从分散到集中,从传统药品销售到现代电子商务的转变。
然而,在行业快速发展的同时,也暴露出一些问题,如药品价格居高不下、药品可及性不均等。
本文采用文献综述和案例分析相结合的方法,系统梳理了美国药品流通模式的演变过程、现状及问题。
同时,通过收集和分析公共数据、访谈等方式,对美国药品流通模式进行了深入探讨。
美国药品流通模式的现状是:在药品供应链中,制药企业、批发商、零售药店、医疗机构等多种角色通过市场竞争和协作共同完成药品流通。
虽然行业整体发展迅速,但也存在一些问题。
药品价格普遍偏高,给消费者带来了较大的经济负担。
药品可及性不均等,部分地区药品供应不足,而部分地区则存在药品冗余。
影响美国药品流通模式的因素主要包括政府、市场和社会三个方面。
政府对药品流通的管控主要通过法规和政策实现,市场因素则通过供求关系、竞争状况等影响药品流通模式,社会因素则包括医疗保健需求、公众意见等。
针对美国药品流通模式的问题及其影响因素,本文提出了以下建议:一是加强政府监管,通过完善法规和政策,规范药品流通秩序,降低药品价格;二是发挥市场机制作用,通过市场竞争和协作,提高药品流通效率;三是社会需求,积极回应社会关切,提高药品可及性。
美国药品流通模式对全球药品流通模式具有重要启示。
政府应加大对药品流通行业的监管力度,确保市场秩序规范、公平竞争。
充分发挥市场机制在药品流通中的作用,提高药品流通效率,降低药品价格。
社会需求,提高药品可及性,实现药品资源的合理配置。
随着医药行业的快速发展,药品流通体制的改革已成为各国政府的重点。
国内外中药行业的市场分析及发展对策

医药行业国内我国中药产业规模越来越大,年销售额已从1980年的近10亿元,增长到现在的400多亿元。
据介绍,中药包括中成药、饮片和中药材。
中成药的发展水平在一定程度上代表着中药工业化发展的水平。
现在我国中成药所需用的药材占到全部药材的70%以上。
而在20世纪的70年代,我国中药临床应用还是以饮片为主,成药为辅。
当时,中成药所用原料药材仅占全部药材的20%,全部药材的70%用于加工饮片。
20多年前,我国许多地方几乎是市市有中成药厂,县县办饮片加工场,厂小品种多,生产方式落后。
那时,全国最大的中成药企业是上海市中药一厂,一年的销售额也就1000多万元。
现在,我国年销售额超过一亿元的中成药企业有120多家,年销售额相当于一亿美元以上的中成药企业也有十来家。
大批中成药新兴企业的不断崛起,展现出我国传统中药日益现代化的崭新风貌。
据中国医药保健品商会中药部主任刘张林介绍,我国中药出口在经历了3年的下降之后,去年终于止跌回升。
海关统计资料显示,中药进出口总额与前年同期相比,呈现全面增长。
至去年11月底,我国中药进出口总额为6.04亿美元,同比增长13.7%。
预计全年中药进出口总额可达6.6亿美元。
刘张林说:中药材在我国中药出口中仍占有举足轻重的地位,去年1-11月,中药材出口3.15亿美元,占中药出口的62.9%,同比增长5.4%。
在出口中药材中,鲜蜂王浆(粉)、甘草以及西洋参加工贸易占有较大比重。
中成药与保健品的出口也有较大幅度的增长,至11月底已出口8176万美元,同比增长18.9%,清凉油、片仔癀出口增长幅度较大。
植物提取物的出口在前几年较快增长的基础上,仍保持了10.6%的增长率,出口额为1.04亿美元。
据分析,我国去年中药出口止跌回升主要有四个方面原因:韩国、日本及东南亚地区等中药主市场的经济全面复苏,世界植物药市场对我国中药的需求,我国中药现代化工程与中药国际化的推动,国家对中药出口所给予的优惠政策与支持。
我国对美国市场中药商品贸易出口分析
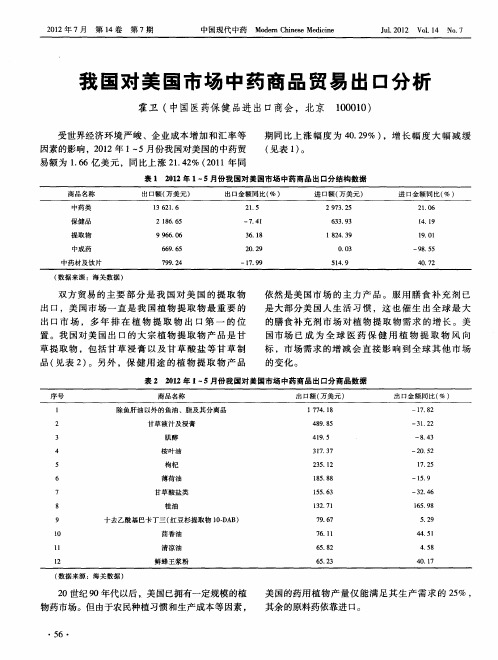
表 3 21 02年 1 —5月 份 我 国 对 美 国市 场 中药 商 品 出 口分 省 市数 据
( 数据来源 :海关数据 )
表 4 0 2年 1 2 1 —5月份我国对美国市场 中药 出口 前1 O家企业排名 ( 出 口额排名 ) 按
主流市 场 。
万美 元 ,同 比增长 3 . 9 ,占全 部企业 对美 国中药 67 %
出 口额 的 4 .8 ;中外 合 资 企 业 为 7 7 1% 5家 ,出 口 5
4 17 4 . 1万美 元 ,同 比增 长 2 6 , 占全 部 企 业 对 美 .%
国 中药 出 口额 的 3.5 ;国有 企业 为 6 99 % 9家 ,出 口 1723 2 .2万美 元 ,同 比增 长 4 .4 , 占全部 企业 对 24 %
l 2 3 4 5 6 7
应 用情 况 ,从使 用 范围看 :( ) 约 有 7 % 的美 国针 1 0 灸 医师在 治疗 中使 用 中草 药 或 中成 药 ,一些 正 骨 医 师 和营养 师 也在 学 习 使用 ;( 常用 的 中草 药 或 剂 2) 型 ;汤 剂 、片剂 、粉 剂 、胶 囊 ;( )中药 在 美 国 主 3 要作 为天 然 健康 食 品销 售 ,而未 真 正 进入 美 国 药 物
基本 属于膳 食 补 充 剂 范 畴 ,主 要 在 有 机食 品专 卖 店
销售 ,而不 是在 药店 销售 。 近年 来 ,F A 加 强 了 天 然 植 物 药 的法 规 管 理 , D
20 03年启 动 了对膳食 补 充剂 实行 G P管 理 ,对 膳食 M 补 充剂 的生 产 和 标 签 制 订 了严 格 的 标 准 。 《 导 原 指
中美药典通则方法对比

中美药典通则对比:
1.定义和范围:中美药典通则方法在定义和范围上有所不同。
例如,美国药典(USP)涵盖了药品、医疗器械、食品补充剂、生物制品等领域的检测方法,而中国药典(ChP)主要针对药品的检测方法。
2.检测项目:中美药典通则方法的检测项目也有所不同。
例如,
USP对某些药品的溶出度、释放度等进行了更详细的规定,而ChP则对药品的含量、有关物质等进行了更严格的要求。
3.检测方法:在具体的检测方法上,中美药典通则方法也存在
差异。
例如,对于同一种药品,USP和ChP可能采用不同的色谱条件、流动相组成、检测波长等。
此外,在溶出度试验中,USP和ChP也可能采用不同的溶出介质、转速等条件。
4.更新频率:中美药典通则方法的更新频率也有所不同。
USP
更新较快,每年都有大量的通则方法进行更新或修订。
而ChP 的更新相对较慢,可能每年只更新一小部分通则方法。
中美药品gmp法规解读汇编

中美药品gmp法规解读汇编
药品 GMP(Good Manufacturing Practice)是指药品生产质量管理规范,是确保药品生产过程中质量和安全的一系列规范和标准。
中美药品 GMP 法规有一些共同之处,也有一些差异,下面我会从多
个角度对中美药品 GMP 法规进行解读。
首先,中美药品 GMP 法规在适用范围上有一些差异。
美国FDA (Food and Drug Administration)的 GMP 法规适用于美国境内和出口到美国的药品生产,而中国的 GMP 法规则适用于中国境内的药
品生产。
在具体的生产要求和标准上,中美药品 GMP 法规也存在一
些差异,比如在原材料采购、生产设备、生产过程控制等方面的要
求可能会有所不同。
其次,中美药品 GMP 法规在监督管理机构和执法力度上也有一
些不同。
美国的 FDA 对药品 GMP 的监督管理非常严格,对违反
GMP 法规的企业会进行严厉的处罚,包括产品召回、罚款甚至停产
等措施。
而中国的药品监管部门也在加强对 GMP 法规的监督管理,
但在执法力度和执行效果上可能还存在一些差距。
另外,中美药品 GMP 法规在更新和修订方面也有一定差异。
美
国的 FDA 经常对 GMP 法规进行修订和更新,以适应新的科技和生产模式,而中国的 GMP 法规也在不断修订和完善,但在更新速度和灵活性上可能还有所欠缺。
总的来说,中美药品 GMP 法规在适用范围、监督管理和更新修订等方面存在一些差异,但都致力于保障药品生产的质量和安全,促进全球药品质量的提升。
希望以上解读能够对您有所帮助。
中美医药产业创新体系对比分析

中美医药产业创新体系对比分析阿丽塔,汪 楠,田 玲(中国医学科学院医学信息研究所,北京 100050)摘要: 目的为完善我国医药产业创新体系,促进我国新药研发提供参考。
方法在阐述了产业创新体系理论的基础上,对比分析了政府、企业、大学和科研院所在中美医药产业创新体系中发挥的不同作用,提出了建立和完善我国医药产业创新体系的建议。
结果与结论我国政府要加大对医药产业的支持力度,企业要加强自主创新,大学和科研院所要深化科研体制改革,建立和完善我国的医药产业创新体系。
关键词: 医药产业;创新体系;新药研发;中美对比中图分类号:R95 文献标识码:A 文章编号:100227777(2009)0120018205The Comparation of Pharmaceutical Industry Innovation System of U nited States and ChinaA Lita,Wang Nan and Tian ling(Chinese Academy of Medical Science,Instit ute of Medical Information, Beijing100005)ABSTRACT: Objective It is reference to imp rove t he innovation system of Chinese p harmaceutical industry and pro mote Chinese research and develop ment of new drugs.Methods The t heory of indust rial innovation system was int roduced,t he f unction of government,factory,university and instit ute in p harmaceutical indust ry innovatio n system of United States and China was compared.R esults and Conclusions Advices were given to make Chinese p harmaceutical indust ry innovation system more perfect. KEY WOR DS: pharmaceutical industry;innovation system;new drug research and development;US.and China 现代医药产业是对国家的经济发展和社会进步具有重要影响的高技术产业,创新药物研究与开发是医药产业技术进步的核心,集中体现了生命科学和生物技术领域前沿的新成就,是新世纪科技和经济国际竞争的战略制高点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中美两国药品流通模式比较与分析摘要:药品流通是指药品从生产企业到消费者手中的全过程。
在我国,有人把现行的药品流通模式比喻为“橄榄球”,即药品从生产企业开始,经过多层代理商、批发商销售到医院和药店,最后才到消费者手中,形成两头尖,中间宽的利益分配格局。
本文中笔者将通过对美国药品流通模式的介绍,对中国目前药品流通中存在的一些问题进行探讨。
关键词:药品流通;PBM;医疗保障一、美国药品流通模式简介美国的药品流通格局中,多种消费渠道的零售成为整个流通模式中的主体,制药企业、批发商、零售商、药品福利管理机构(Pharmacy benefit management,PBM)参与其中,PBM的作用尤为关键。
1.PBM是美国一种专业化医疗费用管理的第三方组织,这种组织参与到医药产品流通的各个环节,如药品购买、分销管理以及药品使用目录管理、处方药报销管理等方面。
其主要职能如下:(1)药品报销目录的管理PBM应用其药品管理基础,制定一份报销目录,该目录可以告知医生在特定的治疗等级下,哪种药品的成本效果最佳和临床有效率最高。
这些目录收录的药品都是根据其医疗费用使用专业经验所选择的,鼓励其成员和药房进行使用的药品。
PBM下设的药学和医学治疗委员会负责评价药品有效性,如果该药品在有效性方面比其他药品有优势性,则仍然可以保留;否则便会变更。
(2)药品购买PBM负责采购和分发药品。
企业的产品能否进入报销目录会大大影响销售量,所以它们会给予可观的折扣,以此增加市场份额。
PBM则利用这一点和采购权,通过与生产企业就药品价格和折扣问题进行磋商,降低医疗产品价格。
(3)处方药报销管理在美国,由于药品销售额中由第三方付费的处方药销售额占94.1%,只有5.19%由消费者自掏腰包支付。
①PBM在药房和保险方之间充当消费协调人的角色,就处方药的报销水平与零售药店进行协商,最终达到一个可以使得保险方满意的标准。
同时,PBM使用先进的自动化程序和信息技术,对药品使用进行事前评价、同时评价和回顾性评价,即在药品使用之前,以及在处方未调配之前、调配之后对高成本的、有潜在滥用可能的药品使用进行监督,对处方合理性、药物相互作用、处方替换等进行评价,以确保药品使用合理。
2.医药分业模式下零售是主渠道美国医药分业(Seperation of dispensing and prescribing)由来已久,医师负责为患者诊断病情,决定如何治疗,药师根据医师处方调配药品,患者一般在药店购药。
在美国,按照消费者购买药品的渠道来看,药品零售领域是主渠道,连锁药店、独立药店、等占了59%的市场份额,而公立医院、非公立医院、诊所、长期监护病房、健康维护组织(HMOs)和家庭病房、诊所等医疗单位占据了27%的市场份额②,除此以外,其他方式如邮购,作为药品流通的一条新兴渠道,也在整个药品流通份额中占据一席之地。
3.大型批发企业垄断经营美国的药品批发企业从20世纪70年代开始,经过30多年的兼并和重组,呈现出寡头垄断的局面,并形成了高度集约化的药品流通局面。
1975年—2000年,其卫生保健产品批发商、分销商的数量已从约200家减少到不足50家。
尤其是被称为“五大巨头“的五家巨型公司则垄断了这个市场近90%的份额,而它们的经营品种几乎覆盖了整个医药领域。
③美国巨型药品批发企业在过去经营的主要行为是大规模从药品生产企业购进药品,储运到自己的仓库内,然后直接将药品按照客户的需要销往各个连锁药店及大型医院。
然而,随着药品零售业的蓬勃发展,药品零售企业开始直接向生产企业购进药品,并利用美国当今发达的第三方物流体系,对药品进行仓储和运输。
这样药品可以从储运中心里,直接按照各零售店的需求安排统一配送,明显节约了经营成本。
针对这样的变革,巨型批发企业着眼于其客户的需要,为其提供了多种便捷的中介服务:(1)库房(包括库房配送业务),即批发商直接承担药品从供应链初始端至终端零售企业的运输服务,可将药品直接进入连锁药店或医院的药品库房。
(2)批发商直接负责向生产企业下达订单和付款,并将货物直接送到大型零售客户手中。
这两种服务既进一步减少了流通中的环节,同时也使批发企业节约了仓储及维护的大量人员和成本。
由此可见,美国的药品流通环节非常简单。
一般来说,药品从生产企业开始,中间只需经过一层批发商、分销商,即可到达零售商或医疗单位,然后就到了消费者手中。
而PBM作为药品费用支付方(Third party payers,包括雇主、保险机构、政府提供的医疗保险)的代理,虽不直接参与药品流通过程,但在资金流和折扣流中对药品使用的影响却十分巨大。
在美国这种第三方付费模式下,药品的使用不是由医师决定,而是由PBM和支付方即保险方共同决定药品能否列入报销范围(Formulary,即保险目录)和报销比例;同时,PBM与制药企业协商药品价格及折扣率,并监督医师处方行为,达到决定药品使用的目的。
由此可得出一些启示,美国由第三方付费而将消费者的利益联合了起来,从而结成一个利益群体,即保险方,参与与PBM、药房、制药企业的谈判,这是就比单独的个人力量强大的多,有了争取消费者自己利益的可能。
而在我国则不存在这样的情况,下面简要对我国药品流通体制特点进行介绍。
二、我国药品流通模式特点1.医疗机构是药品销售的主渠道我国未实行医药分业,医疗机构是药品分销的主渠道。
在全国药品销售额中,医院药品销售额占80%以上,大大高于发达国家的20%的平均水平。
在1992年以后,我国医疗体制改革倡导“建设好国家,吃饭靠自己”,由于我国90%以上的医院是政府兴办的,而各级政府的财力又有限,根本无法维持医院的正常运转。
不得不允许医院通过销售药品获得差价收入进行补偿。
这就是“以药养医”的政策。
在市场经济条件下,药品越来越多,价差越来越大,同类疗效的药品价差可达十几倍。
医院靠“以药养医”,导致医院采用采购和销售价格高的、折扣大的药品。
保证药品的销售收入成为医院的重要收入来源。
我国从2000年开始实行药品分类管理制度,尽管可凭处方到药店购药,但由于长期以来的购药习惯、医院和药店药品种类的差异及医院对处方外流的限制,患者在医院开处方一般只能在医院药房取药,医院在药品销售过程中处于优势地位。
2.批发环节与零售环节的进销差率不合理从理论上讲,进销差率的规定应以使经营企业的流通费用得到补偿并能取得合理的利润为宜。
由于批发企业是批量销售,销量较大,为了使利润分配合理,批发环节的进销差率应小于零售环节。
在我国,由于药品批发环节的进销差率较大,诱发过多的商业流通企业从事药品的批发,影响药品市场的正常秩序,引发了不正当竞争。
截至2005年底,我国医药市场有大约7000家药厂,13000多家医药批发企业,12万多家零售企业④。
3.流通环节上,药品批发企业过多过滥,市场无序竞争非法促销,折让回扣,层层加价,推动药品价格上涨。
这些企业基本上都是按行政区划层层设置的国有药品专营企业,由于其产权制度的缺陷和政策性的保护,使得有的批发企业经营效率较低,却又能享受到地域垄断所带来的应有利润。
由于药品批发、零售企业过多过滥,无序竞争,造成药品流通环节费用增加。
一些药厂、药商相互勾结,在虚高定价和回扣让利上大作促销竞争文章,以取得市场份额。
按原有规定从药厂出厂的药品,经过几级医药公司批发到医院,再零售到病患者手中,流通环节加价达37%,实际还远不止这些。
据调查,现行药品批发环节的层层加价占40%,零售环节加价占30%,而发达国家药品在批发环节的加价一般在10%以下,零售环节加价一般在20%以下⑤。
据调查,目前市场上出现的“平价药店”之所以药价较低,很重要原因就是流通费用低,开展产销直营。
由此可见,流通环节是造成药价虚高的重要领域。
三、我国药品流通模式改革的难点与方向探讨1.我国药品流通模式改革的难点美国的模式令人羡慕,但不同的国情、不同的历史文化背景,医药政策也应有所差别。
我国的药品流通模式改革难点来自于以下几方面:(1)相关利益集团的复杂性。
在我国,除了药品生产企业、经营企业、医疗机构等利益集团以外,招标采购机构、保险机构、政府、医生药师、护士群体都代表各自的利益,医药销售代表在工作过程中为了达到使医生最终用自己药的的,通常要出让折扣、花钱买通主治医师、用药护士、分管用药的主任、药房人员等等,其间各种利益群体存在错综复杂的关系,缺乏有效监管和制约。
要进行某项改革,政府需平衡复杂利益集团的关系,这是改革的难点所在。
(2)建立医疗机构补偿机制是改革的瓶颈。
在我国,医药流通模式改革如果实行医药分业经营等割断药品利益链的手段,医院药品收入将减少,这必将导致医院诊疗价格的提高或医疗服务质量的下降,从而以牺牲广大患者的利益作为最终代价。
为避免这种现象发生,必须建立医疗机构补偿机制。
而目前我国医院已经在偏市场化的道路上走了多年,地方财政受经济发展水平所限,补贴不可能一下增多,这都是难点所在。
(3)民众根深蒂固的就医购药习惯。
习惯最难改变,特别是这种习惯与历史文化传统相联系时则更难改变。
可以设想,如果效仿美国的做法实行医药分业经营,人们的就医意愿将受到极大影响,特别是我国农村人口医疗服务的可获得性将受到更大的影响。
(4)医疗保险发展的进程缓慢,总体水平较低,覆盖面窄。
我国44.8%的城镇人口和79.3%的农村人口没有制度性医疗保障⑥,居民靠自费看病,承受着生理、心理和经济三重负担。
在此情况下,医疗保险支付方就不能像美国那样形成强大的利益群体代表,不能参与进入与企业、药房、医院等的博弈中。
消费者个人利益分散,难以有话语权。
(5)医保手册所列药品目录在我国是由政府制定,选取同等疗效的低价常见药品供医生参考使用。
但其实施没有硬性实施规定和监督实施机制,形同虚设。
在国内,由政府部门制定的医保手册一般只作为医生的用药参考,所以医生在逐利的意识下,一般会选择用价格较高的或已收回扣的同等疗效的药来替代医保手册上所列药品。
2.我国药品流通模式改革方向探讨综合以上对我国药品流通模式改革的难点分析,不难看出对于我国这样一个人口众多的国家,药品流通模式改革只能采取渐进式改革方式,从药品分类管理制度、药师制度的建立、推行和完善开始,逐步规范药品流通环节,改变民众的就医、购药习惯,政府建立医疗机构补偿机制,从根本上解决“以药养医”的问题,逐步完善医疗保障体系,让群众真正得到实惠。
(1)引入类似PBM的药品利益管理机构美国的药品流通模式中PBM环节是我国没有的,这由整个医疗体系结构决定。
医疗服务的专业性特点决定了消费者与医疗服务提供方之间存在信息不对称,如果不改变这种信息不对称,医疗服务(包括药品)价格虚高的问题就无法解决。
而解决信息不对称的最有效办法就是采用代理,由第三方监督医疗服务提供过程,PBM就起到了代理监督作用。
