环境工程原理课后习题答案
环境工程原理课后习题答案2-8章

课
后
答
案
网
ww w
.k
hd
3.4如图所示,有一水平通风管道,某处直径由400mm减缩至200mm。 为了粗略估计管道中的空气流量,在锥形接头两端各装一个U形管 压差计,现测得粗管端的表压为100mm水柱,细管端的表压为40mm 水柱,空气流过锥形管的能量损失可以忽略,管道中空气的密度为 1.2kg/m3,试求管道的空气流量 。
《第二章 质量衡算与能量衡算》
.c om
2.8 某河流的流量为3.0m3/s,有一条流量为0.05m3/s的
课
后
答
质量流量是多少?假设原河水和小溪中不含示踪剂。
案
网
出,溪水中示踪剂的最低浓度是多少?需加入示踪剂的
ww w
1.0mg/L。为了使河水和溪水完全混合后的示踪剂可以检
.k
hd
溪水中加入示踪剂。假设仪器检测示踪剂的浓度下限为
A1 19 19 1.12 19 15 Am 16.9 19 ln 15 A1 19 1.27 A2 15
1 0.002 1 0.00026 0.000176 458 45 3490 2.95 10 3 m 2 K / W
课
后
答
案
网
α1为管外流体 对流传热系数
rm1 3 28.47 mm 30 ln 27 30 43.28mm 60 ln 30 30 73.99mm 90 ln 60
rm 3
课
rm 2
后
答
案
网
解:设铝复合管、石棉、软木的对数平均半径分别为rm1、rm2、rm3
ww w
.k
hd
aw
.c om
(完整word版)环境工程原理第三版课后答案(word文档良心出品)

1.2简要阐述环境工程学的主要任务及其学科体系。
解:环境工程学作为环境学科的一个重要分支,主要任务是利用环境学科以及工程学的方法,研究环境污染控制理论、技术、措施和政策,以改善环境质量,保证人类的身体健康和生存以及社会的可持续发展。
图1-2是环境工程学的学科体系。
1.3去除水中的悬浮物,有哪些可能的方法,它们的技术原理是什么?解:去除水中悬浮物的方法主要有:沉淀、离心分离、气浮、过滤(砂滤等)、过滤(筛网过滤)、反渗透、膜分离、蒸发浓缩等。
上述方法对应的技术原理分别为:重力沉降作用、离心沉降作用、浮力作用、物理阻截作用、物理阻截作用、渗透压、物理截留等、水与污染物的蒸发性差异。
1.4空气中挥发性有机物(VOCs)的去除有哪些可能的技术,它们的技术原理是什么?解:去除空气中挥发性有机物(VOCs)的主要技术有:物理吸收法、化学吸收法、吸附法、催化氧化法、生物法、燃烧法等。
上述方法对应的技术原理分别为:物理吸收、化学吸收、界面吸附作用、氧化还原反应、生物降解作用、燃烧反应。
1.5简述土壤污染可能带来的危害及其作用途径。
解:土壤污染的危害及其作用途径主要有以下几个方面:①通过雨水淋溶作用,可能导致地下水和周围地表水体的污染;②污染土壤通过土壤颗粒物等形式能直接或间接地为人或动物所吸入;③通过植物吸收而进入食物链,对食物链上的生物产生毒害作用等。
1.6环境净化与污染控制技术原理可以分为哪几类?它们的主要作用原理是什么?解:从技术原理上看,环境净化与污染控制技术原理可以分为“隔离技术”、“分离技术”和“转化技术”三大类。
隔离技术是将污染物或者污染介质隔离从而切断污染物向周围环境的扩散,防止污染近一步扩大。
分离技术是利用污染物与污染介质或其它污染物在物理性质或化学性质上的差异使其与介质分离,从而达到污染物去除或回收利用的目的。
转化技术是利用化学或生物反应,使污染物转化成无害物质或易于分离的物质,从而使污染介质得到净化与处理。
中国石油大学环境工程原理课后习题答案

第二章 质量衡算与能量衡算2.1 某室内空气中O 3的浓度是0.08×10-6(体积分数),求:(1)在1.013×105Pa 、25℃下,用μg/m 3表示该浓度; (2)在大气压力为0.83×105Pa 和15℃下,O 3的物质的量浓度为多少?解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol 空气混合物的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×298K/273K=24.45L所以O 3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L )-1=157.05μg/m 3(2)由题,在所给条件下,1mol 空气的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K )=28.82L所以O 3的物质的量浓度为0.08×10-6mol/28.82L =2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa 的条件下,SO 2的平均测量浓度为400μg/m 3,若允许值为0.14×10-6,问是否符合要求?解:由题,在所给条件下,将测量的SO 2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--⨯⨯⨯=⨯⨯=⨯⨯⨯ 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位:质量:1.5kgf·s 2/m= kg密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm2= Pa4.7atm= Pa670mmHg= Pa功率:10马力=kW比热容:2Btu/(lb·℉)= J/(kg·K)3kcal/(kg·℃)= J/(kg·K)流量:2.5L/s= m3/h表面张力:70dyn/cm= N/m5 kgf/m= N/m解:质量:1.5kgf·s2/m=14.709975kg密度:13.6g/cm3=13.6×103kg/ m3压力:35kg/cm2=3.43245×106Pa4.7atm=4.762275×105Pa670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K)3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m3/h表面张力:70dyn/cm=0.07N/m5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t时的密度,lb/ft3;ρ0——温度为t0时的密度,lb/ft3。
环境工程原理第二版课后答案

第I 篇习题解答第一章绪论1。
1简要概述环境学科的发展历史及其学科体系。
解:环境学科是随着环境问题的日趋突出而产生的一门新兴的综合性边缘学科.它经历了20世纪60年代的酝酿阶段,到20世纪70年代初期从零星的环境保护的研究工作与实践逐渐发展成为一门独立的新兴学科.环境学科是一门正在蓬勃发展的科学,其研究范围和内涵不断扩展,所涉及的学科非常广泛,而且各个学科间又互相交叉和渗透,因此目前有关环境学科的分支学科还没有形成统一的划分方法.图1-1是环境学科的分科体系。
图1—1环境学科体系1.2 简要阐述环境工程学的主要任务及其学科体系。
解:环境工程学作为环境学科的一个重要分支,主要任务是利用环境学科以及工程学的方法,研究环境污染控制理论、技术、措施和政策,以改善环境质量,保证人类的身体健康和生存以及社会的可持续发展。
图1—2是环境工程学的学科体系。
图1—2 环境工程学的学科体系环境工程学 环境净化与污染控制技术及原理生态修复与构建技术及原理清洁生产理论及技术原理环境规划管理与环境系统工程环境工程监测与环境质量评价水质净化与水污染控制工程空气净化与大气污染控制工程固体废弃物处理处置与管理物理性污染控制工程 土壤净化与污染控制技术 废物资源化技术环境学科体系环境科学环境工程学环境生态学环境规划与管理1。
3 去除水中的悬浮物,有哪些可能的方法,它们的技术原理是什么?解:去除水中悬浮物的方法主要有:沉淀、离心分离、气浮、过滤(砂滤等)、过滤(筛网过滤)、反渗透、膜分离、蒸发浓缩等。
上述方法对应的技术原理分别为:重力沉降作用、离心沉降作用、浮力作用、物理阻截作用、物理阻截作用、渗透压、物理截留等、水与污染物的蒸发性差异。
1。
4 空气中挥发性有机物(VOCs)的去除有哪些可能的技术,它们的技术原理是什么?解:去除空气中挥发性有机物(VOCs)的主要技术有:物理吸收法、化学吸收法、吸附法、催化氧化法、生物法、燃烧法等.上述方法对应的技术原理分别为:物理吸收、化学吸收、界面吸附作用、氧化还原反应、生物降解作用、燃烧反应。
(完整版)环境工程原理第三版课后答案

1.2简要阐述环境工程学的主要任务及其学科体系。
解:环境工程学作为环境学科的一个重要分支,主要任务是利用环境学科以及工程学的方法,研究环境污染控制理论、技术、措施和政策,以改善环境质量,保证人类的身体健康和生存以及社会的可持续发展。
图1-2是环境工程学的学科体系。
1.3去除水中的悬浮物,有哪些可能的方法,它们的技术原理是什么?解:去除水中悬浮物的方法主要有:沉淀、离心分离、气浮、过滤(砂滤等)、过滤(筛网过滤)、反渗透、膜分离、蒸发浓缩等。
上述方法对应的技术原理分别为:重力沉降作用、离心沉降作用、浮力作用、物理阻截作用、物理阻截作用、渗透压、物理截留等、水与污染物的蒸发性差异。
1.4空气中挥发性有机物(VOCs)的去除有哪些可能的技术,它们的技术原理是什么?解:去除空气中挥发性有机物(VOCs)的主要技术有:物理吸收法、化学吸收法、吸附法、催化氧化法、生物法、燃烧法等。
上述方法对应的技术原理分别为:物理吸收、化学吸收、界面吸附作用、氧化还原反应、生物降解作用、燃烧反应。
1.5简述土壤污染可能带来的危害及其作用途径。
解:土壤污染的危害及其作用途径主要有以下几个方面:①通过雨水淋溶作用,可能导致地下水和周围地表水体的污染;②污染土壤通过土壤颗粒物等形式能直接或间接地为人或动物所吸入;③通过植物吸收而进入食物链,对食物链上的生物产生毒害作用等。
1.6环境净化与污染控制技术原理可以分为哪几类?它们的主要作用原理是什么?解:从技术原理上看,环境净化与污染控制技术原理可以分为“隔离技术”、“分离技术”和“转化技术”三大类。
隔离技术是将污染物或者污染介质隔离从而切断污染物向周围环境的扩散,防止污染近一步扩大。
分离技术是利用污染物与污染介质或其它污染物在物理性质或化学性质上的差异使其与介质分离,从而达到污染物去除或回收利用的目的。
转化技术是利用化学或生物反应,使污染物转化成无害物质或易于分离的物质,从而使污染介质得到净化与处理。
环境工程原理-环境工程原理课后思考题解答5吸附

第五章 吸 附1、固体表面吸附力有哪些,常用的吸附剂有哪些,主要特性是什么,各有什么应用? 答:吸附剂与吸附质间的吸附力有分子引力和化学键引力。
分子引力,吸附力较弱,所以也称范德华吸附。
化学键引力比分子引力大得多。
吸附过程分可逆和不可逆。
常见的吸附剂有活性炭吸附剂、硅胶吸附剂、活性氧化铝、沸石分子筛、有机树脂吸附剂等。
2、吸附平衡是如何定义的,平衡吸附量如何计算?答:吸附平衡是指在一定温度和压力下,吸附剂与吸附质有足够接触时间,吸附量与解吸量相等,载体中吸附质的浓度不再发生变化时,吸附即达到了动态平衡。
3、吸附等温线的物理意义是什么,温度、吸附质分压对吸附是如何影响的?答:气相吸附过程中,操作温度、压力等均有影响,所以吸附平衡关系可以用不同的方法表示,通常用于等温条件下单位质量吸附剂的吸附容量与气相中吸附质分压的关系来表示,即q*=f(p),表示吸附容量与气相中吸附质分压的关系曲线称为吸附等温线。
一般,同一平衡分压下,平衡吸附量随着温度升高而降低。
一定温度下,平衡吸附量随气体压力的升高而增加,所以吸附-解吸循环操作方式通常是低温吸附,高温解吸;高压吸附,低压解吸。
4、Langmuir 方程的基本假设是什么,方程的形式和适用范围,方程式中的常数如何求解? 答:假设:① 吸附剂表面是单分子层吸附;② 被吸附的分子之间没有相互作用力;③ 吸附剂表面是均匀的。
也可写为mm kq q p q p 1*+= 对于一定的吸附剂,其吸附容量是一定的,即q m 一定。
若以p/q*为纵坐标,p 为横坐标作*m 1k q p q kp =+图,可得一直线,该直线斜率为1/q m 。
5、BET 方程的物理意义是什么?答:BET 吸附模型是在Langmuir 方程模型的基础上建立起来的,BET 方程是等温多分子层的吸附模型,其假设条件为:① 吸附剂表面为多分子层吸附,吸附分子在吸附剂上按层次排列;② 被吸附分子间没有相互作用力,每层的吸附服从朗格缪尔吸附模型;③ 第一层的吸附释放的热量为物理吸附热,第二层以上吸附释放的热量为液化热; ④ 总吸附量为各层吸附量的总和。
环境工程原理课后答案

第二章 质量衡算与能量衡算2.1 某室内空气中O 3的浓度是0.08×10-6(体积分数),求:(1)在1.013×105Pa 、25℃下,用μg/m 3表示该浓度; (2)在大气压力为0.83×105Pa 和15℃下,O 3的物质的量浓度为多少?解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol 空气混合物的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×298K/273K=24.45L所以O 3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L )-1=157.05μg/m 3(2)由题,在所给条件下,1mol 空气的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K )=28.82L所以O 3的物质的量浓度为0.08×10-6mol/28.82L =2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa 的条件下,SO 2的平均测量浓度为400μg/m 3,若允许值为0.14×10-6,问是否符合要求?解:由题,在所给条件下,将测量的SO 2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--⨯⨯⨯=⨯⨯=⨯⨯⨯ 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位:质量:1.5kgf·s 2/m= kg密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm2= Pa4.7atm= Pa670mmHg= Pa功率:10马力=kW比热容:2Btu/(lb·℉)= J/(kg·K)3kcal/(kg·℃)= J/(kg·K)流量:2.5L/s= m3/h表面张力:70dyn/cm= N/m5 kgf/m= N/m解:质量:1.5kgf·s2/m=14.709975kg密度:13.6g/cm3=13.6×103kg/ m3压力:35kg/cm2=3.43245×106Pa4.7atm=4.762275×105Pa670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K)3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m3/h表面张力:70dyn/cm=0.07N/m5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t时的密度,lb/ft3;ρ0——温度为t0时的密度,lb/ft3。
环境工程原理-课后习题解答1绪论
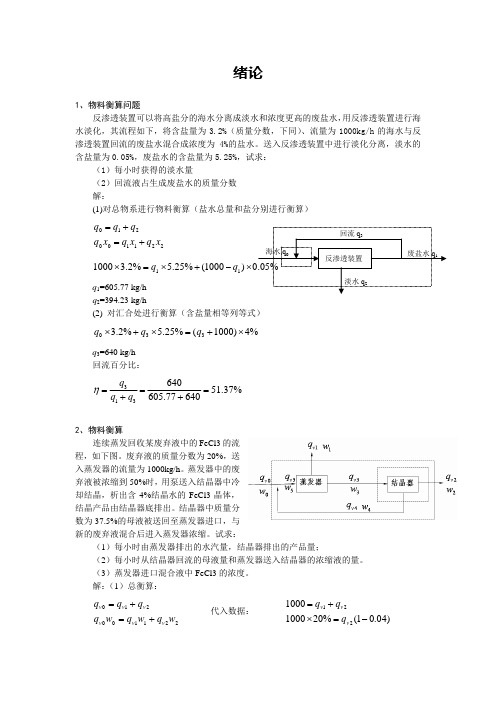
绪论1、物料衡算问题反渗透装置可以将高盐分的海水分离成淡水和浓度更高的废盐水,用反渗透装置进行海水淡化,其流程如下,将含盐量为3.2%(质量分数,下同)、流量为1000kg/h 的海水与反渗透装置回流的废盐水混合成浓度为4%的盐水。
送入反渗透装置中进行淡化分离,淡水的含盐量为0.05%,废盐水的含盐量为5.25%,试求:(1)每小时获得的淡水量(2)回流液占生成废盐水的质量分数解:(1)对总物系进行物料衡算(盐水总量和盐分别进行衡算)221100210x q x q x q q q q +=+=)1000(%25.5%2.3100011⨯-+⨯=⨯q q q 1=605.77 kg/hq 2=394.23 kg/h(2) 对汇合处进行衡算(含盐量相等列等式)%4)1000(%25.5%2.3330⨯+=⨯+⨯q q qq 3=640 kg/h回流百分比:%37.5164077.605640313=+=+=q q q η2、物料衡算连续蒸发回收某废弃液中的FeCl3的流程,如下图。
废弃液的质量分数为20%,送入蒸发器的流量为1000kg/h 。
蒸发器中的废弃液被浓缩到50%时,用泵送入结晶器中冷却结晶,析出含4%结晶水的FeCl3晶体,结晶产品由结晶器底排出。
结晶器中质量分数为37.5%的母液被送回至蒸发器进口,与新的废弃液混合后进入蒸发器浓缩。
试求:(1)每小时由蒸发器排出的水汽量,结晶器排出的产品量;(2)每小时从结晶器回流的母液量和蒸发器送入结晶器的浓缩液的量。
(3)蒸发器进口混合液中FeCl3的浓度。
解:(1)总衡算:221100210w q w q w q q q q v v v v v v +=+= 代入数据: )04.01(%2010001000221-=⨯+=v v v q q q解得:hkg q hkg q v v /3.208/7.79121== (2)以结晶器为物料衡算单位 442233423)1(w q w q w q q q q v v v v v v +-=+= 4343375.096.03.2085.03.208v v v v q q q q +⨯=+= hkg q hkg q v v /5.766/8.97443== (3)%6.275.7661000375.05.7662.01000=+⨯+⨯3、微分热量衡算一污水池内有50m3的污水,温度为15℃,为加速消化过程,需将其加热到35℃。
环境工程原理智慧树知到课后章节答案2023年下西华大学

环境工程原理智慧树知到课后章节答案2023年下西华大学西华大学第一章测试1.本门课程的名称是《环境工程原理》吗?答案:对第二章测试1.将此物理量换算为SI单位:某物质的比定压热容cp=0.24BTU/(lb·℉)=()答案:1.005 kJ/(kg·K)2.将此物理量换算为SI单位:质量1.5kgf·s2/m=()答案:14.7 kg3.将此物理量换算为SI单位:表面张力70dyn/cm =()答案:0.074 N/m4.某室内空气中O3的浓度是0.08×10-6(体积分数),在1.013×105Pa、25℃下,用ug/m3表示该浓度为()ug/m3。
答案:157.055.某一段河流上游流量为36000m3/d,河水中污染物的浓度为3.0mg/L。
有一支流流量为10000 m3/d,其中污染物浓度为30mg/L。
假设完全混合。
求每天有()kg污染物质通过下游某一监测点。
答案:408.026.某河流的流量为3.0m3/s,有一条流量为0.05m3/s的小溪汇入该河流。
为研究河水与小溪水的混合状况,在溪水中加入示踪剂。
假设仪器检测示踪剂的浓度下限为1.0mg/L。
为了使河水和溪水完全混合后的示踪剂可以检出,溪水中示踪剂的最低浓度是( )mg/L,需加入示踪剂的质量流量是( )g/s。
假设原河水和小溪中不含示踪剂。
答案:61;3.057.有一个总功率为1000MW的核反应堆,其中2/3的能量被冷却水带走,不考虑其他能量损失。
冷却水来自于当地的一条河流,河水的流量为100m3/s,水温为20℃。
如果水温只允许上升10℃,冷却水需要()m3/s的流量。
答案:15.948.一加热炉用空气(含O2 0.21, N2 0.79)燃烧天然气(不含O2与N2)。
分析燃烧所得烟道气,其组成的摩尔分数为CO2 0.07,H2O 0.14,O2 0.056,N2 0.734。
环境工程原理习题解答

《环境工程原理》习题解答第三章 流体流动习题3.3污水处理厂中,将污水从调节池提升至沉淀池。
两池水面差最大为10m ,管路摩擦损失为4J/kg 。
流量为34m 3/h 。
求提升水所需要的功率。
设水的温度为25℃。
解:(1)根据流体输送能量方程(3.1.18):∑+++=-++f m m h p gz u We p gz u ρρ222211212121 因2池均为敞口池,且池面很宽广,故p 1=p 2=0,u m1=u m2=0。
根据题意:z 2-z 1=10m ,因此有:∑+-=-f h z z g We )(12=9.8×10+4=102 J/kg “-”号表示流体机械给水做功,即为水泵。
(2)查附录5知:ρ20=998.2 kg/m 3,ρ30=995.7 kg/m 3,则25时水的密度:ρ25=(998.2+995.7)/2=997.0 kg/m 3故提升水所需功率为:N=We×ρQ=102×997.0×34=3.46×106 J/h =961 w (J/s) =0.96 kw习题3.5如图所示,有一直径为1m 的高位水槽,其水面高于地面8m ,水从内径为100mm 的管道中流出,管路出口高于地面2m ,水流经系统的能量损失(不包括出口的能量损失)可按∑h f =6.5u 2计算,式中u 为水在管内的流速,单位为m/s 。
试计算: (1) 若水槽中水位不变,试计算水的流量;(2) 若高位水槽供水中断,随水的出流高位槽液面下降,试计算液面下降1m 所需的时间。
解:(1)按图示选取计算断面,基准面0-0取在地面,则有: p 1=p 2=0,u m1=0,z 1=8m ,z 2 =2m 按单位重量的能量方程(3.1.24)进行计算:∑+++=++f m m h gp z u g p z u ρρ222211212g 12g 1 其中上式中的∑h f =6.5u m22/g 将已知条件代入可得:22225.6022g 1080m m u gu +++=++ 解之得:s m g u m /9.214/122==则出流流量:Q 1=0.785×0.12×2.9=0.0228 m 3/s=82.0 m 3/h(2)设某一时刻水池液位高度为z ,则能量方程可写为:22225.622g 1m m u gu z ++=整理得:14)2(22-=z g u m 经时间dt 后,水流从管内流出的水量为:dQ=0.785×d 2×u m2dt=0.785×0.12×14)2(2-z g =9.3×10-32-z dt此时,水池中的液位下降了dz=dQ/(0.785×D 2)=11.85×10-32-z dt则:dz z dt 24.84-=当z 从8m 降为7m 时所需时间: T=36s 习题3.10题略解:(1)因Q=140m 3/h=0.0389m 3/s则150mm 和100mm 管内的流速为: u 150=2.20m/s ,u 100=4.96m/s 其:Re 150=997×2.2×0.15/(90.3×10-5)=3.64×105 Re 100=997×4.96×0.10/(90.3×10-5)=5.48×105 (2)查莫迪图可得摩阻系数 λ150=0.014, λ100=0.013查P87表3.4.4得局部阻力系数:90度弯头ξw =0.75,底阀ξd =1.5,闸阀ξf =0.17(全开) 入口ξe =0.5,出口ξo =1.0,变径头ξb =0.32(d 2/D 2=0.45) (3) 则所需水泵扬程 gu d L g u d LZ H p 2)(2)(222122211111∑∑∑∑++++∆=ζλζλ =60+{0.014×(60+23)/0.15+(0.5+1.5+2×0.75)} ×2.22/(2×9.81) +{0.013×100/0.1+(3×0.75+0.17+0.32+1)} ×4.962/(2×9.81) =60+3.05+23.08=86.1m (4) 所需水泵理论功率Ne=H p ×Q×ρg=86.1×0.0389×997×9.81=32.8×103 w=32.8 kw (5) 水泵实际功率Ns=Ne/η=32.8/60%=54.7kw (6) 水泵每天所需电费Fd=54.7×24×0.46=603.9≈604元/日习题3.13题略解:(1)全部按长管计算,忽略局部损失,且均按完全湍流计算(2)设A管段流量为Q A,B管段流量为Q B,可列出如下方程组:R MAN L MAN Q A2= (R MBO L MBO +R ON L ON)Q B2Q A+Q B=Q将已知数据代入:6.73×1000×Q A2=(0.784×900+2.03×300)Q B2Q A+Q B=0.12解之得:Q A=0.0368 m3/s=36.8 L/sQ B=0.12-0.0368=0.0832 m3/s=83.2 L/s(3)MN之间的阻力损失为:H MN= R MAN L MAN Q A2=6.73×1000×0.03682=9.11m第四章 热量传递习题4.4某一DN60×3mm 的铝复合管,其导热系数为45W/(m.K),外包一层厚30mm 的石棉后,又包了一层厚为30mm 的软木,石棉和软木的导热系数分别为0.15 W/(m.K)和0.04 W/(m.K)。
环境工程原理课后答案

3.6 水在圆形直管中呈层流流动。
若流量不变,说明在下列情况下,因流动阻力而产生的能量损失的变化情况:(1)管长增加一倍;(2)管径增加一倍。
解:因为对于圆管层流流动的摩擦阻力,有220328dl u r l u p m m f μμ==∆ (1)当管长增加一倍时,流量不变,则阻力损失引起的压降增加1倍(2)当管径增加一倍时,流量不变,则u m,2=u m,1/4d 2=2d 1,2f p ∆=,1f p ∆/16即压降变为原来的十六分之一。
4.10在套管换热器中用冷水将100℃的热水冷却到50℃,热水的质量流量为3500kg/h 。
冷却水在直径为φ180×10mm 的管内流动,温度从20℃升至30℃。
已知基于管外表面的总传热系数为2320 W/(m 2·K )。
若忽略热损失,且近似认为冷水和热水的比热相等,均为4.18 kJ/(kg·K ).试求(1)冷却水的用量;(2)两流体分别为并流和逆流流动时所需要的管长,并加以比较。
解:(1)由热量守恒可得q mc c pc ΔT c =q mh c ph ΔT hq mc =3500kg/h×50℃/10℃=17500kg/h(2)并流时有ΔT 2=80K ,ΔT 1=20K2121802043.2880ln ln 20m T T K K T K T T ∆-∆-∆===∆∆ 由热量守恒可得KAΔT m =q mh c ph ΔT h即KπdLΔT m =q mh c ph ΔT h23500/ 4.18/()50 3.582320/()0.1843.28mh ph h m q c T kg h kJ kg K K L m K d T W m K m Kππ∆⨯⋅⨯===∆⋅⋅⋅⋅ 逆流时有 ΔT 2=70K ,ΔT 1=30K2121703047.2170ln ln 30m T T K K T K T T ∆-∆-∆===∆∆ 同上得23500/ 4.18/()50 3.282320/()0.1847.21mh ph hm q c T kg h kJ kg K K L m K d T W m K m Kππ∆⨯⋅⨯===∆⋅⋅⋅⋅ 比较得逆流所需的管路短,故逆流得传热效率较高。
环境工程原理课后习题(环工班)

环工81301班姓名学号Cm15 X 100mg/L —( 5 + qm2k V 050)m ^/s — 10X 106X 0.25 X m ^/s = 0解之得m = 5.96mg/L2.11有一装满水的储槽,直径 内水面高度z 的关系1m.高3m 。
现由槽底部的小孔向外排水。
小孔的直径为0 5u 0= 0.62 ( 2gz )4cm,测得水流过小孔时的流速 U 0与槽试求放出1m 水所需的时间。
解军:设储槽横截面积为 A ,小孔的面积为 A由题得 所以有 即有Au 0= — dV/dt ,即 U 0= — dz/dt x A/A 2 —dz/dt x( 100/4 ) 2 = 0.62 (2gz)0.5—226.55 X z -0'5 dz= dt= 3m1= Z 0— 1mX(nX 0.25m 2) -1 = 1.73m积分计算得t = 189.8s2.13有一个4X 3m 的太阳能取暖器,太阳光的强度为 3000kJ/ (m ・h ),有50%的太阳能被吸收用来加热流过取暖器的水流。
水的流量为0.8L/min 。
求流过取暖器的水升高的温度。
2.6某一段河流上游流量为36000m/d ,河水中污染物的浓度为 3.0mg/L 。
有一支流流量为 10000 m 3/d ,其中污染物浓度为30mg/Lo 假设完全混合。
(1) 求下游的污染物浓度(2) 求每天有多少kg 污染物质通过下游某一监测点。
解: ( 1)根据质量衡算方程,下游污染物浓度为m 旦一2°/^ 3.0 更00 f 」000%/] 8.87mg/LCV1 CV2 (2)每天通过下游测量点的污染物的质量为m(0/1 CV2) 8.87 (36000 10000) 10 3kg/d 408.02kg/d则由质量衡算,得即36000 100002.7某一湖泊的容积为10X 106m ,上游有一未被污染的河流流入该湖泊,流量为 污水,其中含有可降解污染物, 态时湖中污染物的浓度。
环境工程原理课后习题答案..
第I 篇 习题解答第一章 绪论1 . 1简要概述环境学科的发展历史及其学科体系。
解:环境学科是随着环境问题的日趋突出而产生的一门新兴的综合性边缘学科。
它经历了20世纪60年代的酝酿阶段,到20世纪70年代初期从零星的环境保护的研究工作与实践逐渐发展成为一门独立的新兴学科。
环境学科是一门正在蓬勃发展的科学,其研究范围和内涵不断扩展,所涉及的学科非常广泛,而且各个学科间又互相交叉和渗透,因此目前有关环境学科的分支学科还没有形成统一的划分方法。
图1-1是环境学科的分科体系。
图1-1 环境学科体系1.2 简要阐述环境工程学的主要任务及其学科体系。
解:环境工程学作为环境学科的一个重要分支,主要任务是利用环境学科以及工程学的方法,研究环境污染控制理论、技术、措施和政策,以改善环境质量,保证人类的身体健康和生存以及社会的可持续发展。
图1-2是环境工程学的学科体系。
图1-2 环境工程学的学科体系1.3 去除水中的悬浮物,有哪些可能的方法,它们的技术原理是什么?解:去除水中悬浮物的方法主要有:沉淀、离心分离、气浮、过滤(砂滤等)、过滤(筛网过滤)、反渗透、膜分离、蒸发浓缩等。
上述方法对应的技术原理分别为:重力沉降作用、离心沉降作用、浮力作用、物理阻截作用、物理阻截作用、渗透压、物理截留等、水与污染物的蒸发性差异。
环境工程学环境净化与污染控制技术及原理 生态修复与构建技术及原理清洁生产理论及技术原理 环境规划管理与环境系统工程 环境工程监测与环境质量评价水质净化与水污染控制工程 空气净化与大气污染控制工程 固体废弃物处理处置与管理物理性污染控制工程 土壤净化与污染控制技术 废物资源化技术环境学科体系环境科学环境工程学环境生态学环境规划与管理1.4 空气中挥发性有机物(VOCs)的去除有哪些可能的技术,它们的技术原理是什么?解:去除空气中挥发性有机物(VOCs)的主要技术有:物理吸收法、化学吸收法、吸附法、催化氧化法、生物法、燃烧法等。
环境工程原理课后答案解析

第二章质量衡算与能量衡算2.1 某室内空气中O3的浓度是0.08×10-6(体积分数),求:(1)在1.013×105Pa、25℃下,用μg/m3表示该浓度;(2)在大气压力为0.83×105Pa和15℃下,O3的物质的量浓度为多少?解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol空气混合物的体积为V1=V0·P0T1/ P1T0=22.4L×298K/273K=24.45L所以O3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L)-1=157.05μg/m3(2)由题,在所给条件下,1mol空气的体积为V1=V0·P0T1/ P1T0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K)=28.82L所以O3的物质的量浓度为0.08×10-6mol/28.82L=2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa的条件下,SO2的平均测量浓度为400μg/m3,若允许值为0.14×10-6,问是否符合要求?解:由题,在所给条件下,将测量的SO2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--⨯⨯⨯=⨯⨯=⨯⨯⨯ 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位:质量:1.5kgf ·s 2/m= kg密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm 2= Pa4.7atm= Pa670mmHg= Pa功率:10马力= kW比热容:2Btu/(lb ·℉)= J/(kg ·K )3kcal/(kg ·℃)= J/(kg ·K )流量:2.5L/s= m 3/h表面张力:70dyn/cm= N/m5 kgf/m= N/m解:质量:1.5kgf ·s 2/m=14.709975kg密度:13.6g/cm 3=13.6×103kg/ m 3压力:35kg/cm 2=3.43245×106Pa4.7atm=4.762275×105Pa670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K)3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m3/h表面张力:70dyn/cm=0.07N/m5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t时的密度,lb/ft3;ρ0——温度为t0时的密度,lb/ft3。
环境工程原理课后习题答案2-8章

课
后
答
案
网
ww w
.k
hd
3.4如图所示,有一水平通风管道,某处直径由400mm减缩至200mm。 为了粗略估计管道中的空气流量,在锥形接头两端各装一个U形管 压差计,现测得粗管端的表压为100mm水柱,细管端的表压为40mm 水柱,空气流过锥形管的能量损失可以忽略,管道中空气的密度为 1.2kg/m3,试求管道的空气流量 。
R 21rm1 b1 22 rm 2 b2 23rm3 b3
网
每米管段的冷损失量: Q T 5 105 46.85W / m
21rm1
答
(2)
案
R
3 30 30 2 45 28.47 2 0.04 43.28 2 0.15 73.99 3.189 K / W
aw
.c om
课
(2)管径增加一倍: um变为原来的1/4,μ和l不变,阻力损失变为原来的1/16
后
答
案
(1)管长增加一倍:阻力损失增加一倍
网
ww w
2 8uml 32uml l um p f 2 2 r0 d d 2
.k
hd
aw
3.6水在圆形直管中呈层流流动,若流量不变,说明在下列情况 下,因流动阻力而产生的能量损失的变化情况: (1)管长增加一倍 (2)管径增加一倍。
A1 19 19 1.12 19 15 Am 16.9 19 ln 15 A1 19 1.27 A2 15
1 0.002 1 0.00026 0.000176 458 45 3490 2.95 10 3 m 2 K / W
课
后
答
案
环境工程原理课后答案(2-9章)

第二章质量衡算与能量衡算2.1 某室内空气中O3的浓度是0.08×10-6(体积分数),求:(1)在1.013×105Pa、25℃下,用μg/m3表示该浓度;(2)在大气压力为0.83×105Pa和15℃下,O3的物质的量浓度为多少?解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol空气混合物的体积为V1=V0·P0T1/ P1T0=22.4L×298K/273K=24.45L所以O3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L)-1=157.05μg/m3(2)由题,在所给条件下,1mol空气的体积为V1=V0·P0T1/ P1T0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K)=28.82L所以O3的物质的量浓度为0.08×10-6mol/28.82L=2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa的条件下,SO2的平均测量浓度为400μg/m3,若允许值为0.14×10-6,问是否符合要求?解:由题,在所给条件下,将测量的SO2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--⨯⨯⨯=⨯⨯=⨯⨯⨯ 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位:质量:1.5kgf·s 2/m= kg密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm 2= Pa4.7atm= Pa670mmHg= Pa功率:10马力= kW比热容:2Btu/(lb·℉)= J/(kg·K)3kcal/(kg·℃)= J/(kg·K)流量:2.5L/s= m 3/h表面张力:70dyn/cm= N/m5 kgf/m= N/m解:质量:1.5kgf·s 2/m=14.709975kg密度:13.6g/cm 3=13.6×103kg/ m 3压力:35kg/cm 2=3.43245×106Pa4.7atm=4.762275×105Pa670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K)3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m3/h表面张力:70dyn/cm=0.07N/m5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t时的密度,lb/ft3;ρ0——温度为t时的密度,lb/ft3。
环境工程原理课后答案要点

环境工程原理课后答案要点现象以及污染控制装置的基本原理,为相关的专业课程打下良好的理论基础。
第二章质量衡算与能量衡算2.1 某室内空气中O 3的浓度是0.08×10-6(体积分数),求:(1)在1.013×105Pa 、25℃下,用μg/m 3表示该浓度;(2)在大气压力为0.83×105Pa 和15℃下,O 3的物质的量浓度为多少?解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol 空气混合物的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×298K/273K=24.45L所以O 3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L )-1=157.05μg/m 3(2)由题,在所给条件下,1mol 空气的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K )=28.82L所以O 3的物质的量浓度为0.08×10-6mol/28.82L =2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa 的条件下,SO 2的平均测量浓度为400μg/m 3,若允许值为0.14×10-6,问是否符合要求?解:由题,在所给条件下,将测量的SO 2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--=??= 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位:质量:1.5kgf·s 2/m= kg密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm2= Pa4.7atm= Pa670mmHg= Pa功率:10马力=kW比热容:2Btu/(lb·℉)= J/(kg·K)3kcal/(kg·℃)= J/(kg·K)流量:2.5L/s= m3/h表面张力:70dyn/cm= N/m5 kgf/m= N/m解:质量:1.5kgf·s2/m=14.709975kg密度:13.6g/cm3=13.6×103kg/ m3压力:35kg/cm2=3.43245×106Pa4.7atm=4.762275×105Pa670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K)3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m3/h表面张力:70dyn/cm=0.07N/m5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t时的密度,lb/ft3;ρ0——温度为t0时的密度,lb/ft3。
环境工程原理的课后习题

第二章1. 某一湖泊的容积为10 * 106 m 3 ,上游有一未被污染的河流流入该湖泊,流量为50 m 3/s 。
一工厂以5 m 3/s 的流量向湖泊排放污水,其中含有可降解污染物,浓度为100 mg/L 。
污染物降解反应速率常数为0.25d -1 。
假设污染物在湖中充分混合。
求稳态时湖中污染物的浓度。
解:设稳态时湖中污染物浓度为m ρ,则输出的浓度也为m ρ… 由质量恒算,得120m m q q k v ρ--=……………………… 带入数值为()6510055010100.25864000m m ρρ⨯-+-⨯⨯÷=….解得m ρ=5.96 mg/L …………………………………………………2.一条河流的上游流量为10.0 m 3/s ,氯化物的浓度为20.0 mg/L ;有一条支流汇入,流量为5.0 m 3/s ,氯化物浓度为40.0 mg/L 。
视氯化物为不可降解物质,系统处于稳定状态,试计算汇合点下游河水中氯化物浓度。
假设在该点两股流体完全混合。
解:因为系统处于稳定状态且完全混合,所以112212(2)20.0*10.040.0*5.0=/=26.7/210.0 5.0v v mv v q qq q mg L mg L ρρρ+=+++分(分)故汇合点下游河水中氯化物浓度为26.7mg/L3.有一个总功率为100MW 的核反应堆,其中2/3的能量杯冷却水带走,不考虑其他能量损失。
冷却水来自于当地的一条河流,河水的流量为100m3/s ,水温为20℃。
(1) 如果水温允许上升10℃,冷却水需要多大的流量?(2) 如果加热后的水返回河中,问河水的水温会上升多少摄氏度? 解:输入冷却水的热量为21000666.73Q MW =⨯=(1) 以冷却水为衡算对象,设冷却水的流量为v q ,热量变化率为m p T q c ∆。
根据热量衡算定律,有310 4.18310666.7v q ⨯⨯⨯=,求得315.94/v q m s =(2) 由题,根据热量衡算方程得3310010 4.183666.710T ⨯⨯⨯∆=⨯求得 1.59T K ∆=4.某一段河流上游流量为36000m 3/d ,河水中污染物的浓度为3.0mg/L 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第I 篇 习题解答 第一章 绪论1 . 1简要概述环境学科的发展历史及其学科体系。
解:环境学科是随着环境问题的日趋突出而产生的一门新兴的综合性边缘学科。
它经历了20世纪60年代的酝酿阶段,到20世纪70年代初期从零星的环境保护的研究工作与实践逐渐发展成为一门独立的新兴学科。
环境学科是一门正在蓬勃发展的科学,其研究围和涵不断扩展,所涉及的学科非常广泛,而且各个学科间又互相交叉和渗透,因此目前有关环境学科的分支学科还没有形成统一的划分方法。
图1-1是环境学科的分科体系。
图1-1 环境学科体系1.2 简要阐述环境工程学的主要任务及其学科体系。
解:环境工程学作为环境学科的一个重要分支,主要任务是利用环境学科以及工程学的方法,研究环境污染控制理论、技术、措施和政策,以改善环境质量,保证人类的身体健康和生存以及社会的可持续发展。
图1-2是环境工程学的学科体系。
图1-2 环境工程学的学科体系1.3 去除水中的悬浮物,有哪些可能的方法,它们的技术原理是什么?解:去除水中悬浮物的方法主要有:沉淀、离心分离、气浮、过滤(砂滤等)、过滤(筛网过滤)、反渗透、膜分离、蒸发浓缩等。
上述方法对应的技术原理分别为:重力沉降作用、离心沉降作用、浮力作用、物理阻截作用、物理阻截作用、渗透压、物理截留等、水与污染物的蒸发性差异。
1.4 空气中挥发性有机物(VOCs )的去除有哪些可能的技术,它们的技术原理是什么?解:去除空气中挥发性有机物(VOCs )的主要技术有:物理吸收法、化学吸收法、吸附法、催化氧化法、生物法、燃烧法等。
上述方法对应的技术原理分别为:物理吸收、化学吸收、界面吸附作用、氧化还原反应、生物降解作用、燃烧反应。
1.5 简述土壤污染可能带来的危害及其作用途径。
解:土壤污染的危害及其作用途径主要有以下几个方面:①通过雨水淋溶作用,可能导致地下水和周围地表水体的污染;②污染土壤通过土壤颗粒物等形式能直接或间接地为人或动物所吸入;③通过植物吸收而进入食物链,对食物链上的生物产生毒害作用等。
1.6 环境净化与污染控制技术原理可以分为哪几类?它们的主要作用原理是什么?解:从技术原理上看,环境净化与污染控制技术原理可以分为“隔离技术”、“分离技术”和“转化技术”三大类。
隔离技术环境工程学环境净化与污染控制技术及原理 生态修复与构建技术及原理清洁生产理论及技术原理 环境规划管理与环境系统工程 环境工程监测与环境质量评价水质净化与水污染控制工程 空气净化与大气污染控制工程 固体废弃物处理处置与管理物理性污染控制工程 土壤净化与污染控制技术 废物资源化技术环境学科体系环境科学环境工程学环境生态学环境规划与管理是将污染物或者污染介质隔离从而切断污染物向周围环境的扩散,防止污染近一步扩大。
分离技术是利用污染物与污染介质或其它污染物在物理性质或化学性质上的差异使其与介质分离,从而达到污染物去除或回收利用的目的。
转化技术是利用化学或生物反应,使污染物转化成无害物质或易于分离的物质,从而使污染介质得到净化与处理。
1.7 《环境工程原理》课程的任务是什么?解:该课程的主要任务是系统、深入地阐述环境污染控制工程,即水质净化与水污染控制工程、大气(包括室空气)污染控制工程、固体废物处理处置与管理和资源化工程、物理性污染(热污染、辐射污染、噪声、振动)控制工程、自然资源的合理利用与保护工程、生态修复与构建工程以及其它污染控制工程中涉及到的具有共性的工程学基础、基本过程和现象以及污染控制装置的基本原理,为相关的专业课程打下良好的理论基础。
第二章 质量衡算与能量衡算2.1 某室空气中O 3的浓度是0.08×10-6(体积分数),求: (1)在1.013×105Pa 、25℃下,用μg/m 3表示该浓度;(2)在大气压力为0.83×105Pa 和15℃下,O 3的物质的量浓度为多少? 解:理想气体的体积分数与摩尔分数值相等由题,在所给条件下,1mol 空气混合物的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×298K/273K =24.45L所以O 3浓度可以表示为0.08×10-6mol×48g/mol×(24.45L )-1=157.05μg/m 3(2)由题,在所给条件下,1mol 空气的体积为V 1=V 0·P 0T 1/ P 1T 0=22.4L×1.013×105Pa×288K/(0.83×105Pa×273K)=28.82L所以O 3的物质的量浓度为0.08×10-6mol/28.82L =2.78×10-9mol/L2.2 假设在25℃和1.013×105Pa 的条件下,SO 2的平均测量浓度为400μg/m 3,若允许值为0.14×10-6,问是否符合要求? 解:由题,在所给条件下,将测量的SO 2质量浓度换算成体积分数,即33965108.31429810400100.15101.0131064A A RT pM ρ--⨯⨯⨯=⨯⨯=⨯⨯⨯ 大于允许浓度,故不符合要求2.3 试将下列物理量换算为SI 制单位: 质量:1.5kgf·s 2/m= kg 密度:13.6g/cm 3= kg/ m 3压力:35kgf/cm 2= Pa 4.7atm= Pa 670mmHg= Pa功率:10马力= kW比热容:2Btu/(lb·℉)= J/(kg·K) 3kcal/(kg·℃)= J/(kg·K)流量:2.5L/s= m 3/h 表面力:70dyn/cm= N/m 5 kgf/m= N/m解:质量:1.5kgf·s 2/m=14.709975kg 密度:13.6g/cm 3=13.6×103kg/ m 3压力:35kg/cm 2=3.43245×106Pa 4.7atm=4.762275×105Pa 670mmHg=8.93244×104Pa功率:10马力=7.4569kW比热容:2Btu/(lb·℉)= 8.3736×103J/(kg·K) 3kcal/(kg·℃)=1.25604×104J/(kg·K)流量:2.5L/s=9m 3/h表面力:70dyn/cm=0.07N/m 5 kgf/m=49.03325N/m2.4 密度有时可以表示成温度的线性函数,如ρ=ρ0+At式中:ρ——温度为t 时的密度, lb/ft 3;ρ0——温度为t 0时的密度, lb/ft 3。
t ——温度,℉。
如果此方程在因次上是一致的,在国际单位制中A 的单位必须是什么? 解:由题易得,A 的单位为kg/(m 3·K)2.5 一加热炉用空气(含O 2 0.21, N 2 0.79)燃烧天然气(不含O 2与N 2)。
分析燃烧所得烟道气,其组成的摩尔分数为CO 2 0.07,H 2O 0.14,O 2 0.,N 2 0.734。
求每通入100m 3、30℃的空气能产生多少m 3烟道气?烟道气温度为300℃,炉为常压。
解:假设燃烧过程为稳态。
烟道气中的成分来自天然气和空气。
取加热炉为衡算系统。
以N 2为衡算对象,烟道气中的N 2全部来自空气。
设产生烟道气体积为V 2。
根据质量衡算方程,有0.79×P 1V 1/RT 1=0.734×P 2V 2/RT 2即0.79×100m 3/303K =0.734×V 2/573KV 2=203.54m 32.6某一段河流上游流量为36000m 3/d ,河水中污染物的浓度为3.0mg/L 。
有一支流流量为10000 m 3/d ,其中污染物浓度为30mg/L 。
假设完全混合。
(1)求下游的污染物浓度(2)求每天有多少kg 污染物质通过下游某一监测点。
解:(1)根据质量衡算方程,下游污染物浓度为1122123.0360003010000/8.87/3600010000V V m V V q q mg L mg L q q ρρρ+⨯+⨯===++(2)每天通过下游测量点的污染物的质量为312()8.87(3600010000)10/408.02/m V V q q kg dkg dρ-⨯+=⨯+⨯=2.7某一湖泊的容积为10×106m 3,上游有一未被污染的河流流入该湖泊,流量为50m 3/s 。
一工厂以5 m 3/s 的流量向湖泊排放污水,其中含有可降解污染物,浓度为100mg/L 。
污染物降解反应速率常数为0.25d -1。
假设污染物在湖中充分混合。
求稳态时湖中污染物的浓度。
解:设稳态时湖中污染物浓度为m ρ,则输出的浓度也为m ρ 则由质量衡算,得120m m q q k V ρ--=即5×100mg/L-(5+50)m ρm 3/s -10×106×0.25×m ρm 3/s =0解之得m ρ=5.96mg/L2.8某河流的流量为3.0m 3/s ,有一条流量为0.05m 3/s 的小溪汇入该河流。
为研究河水与小溪水的混合状况,在溪水中加入示踪剂。
假设仪器检测示踪剂的浓度下限为1.0mg/L 。
为了使河水和溪水完全混合后的示踪剂可以检出,溪水中示踪剂的最低浓度是多少?需加入示踪剂的质量流量是多少?假设原河水和小溪中不含示踪剂。
解:设溪水中示踪剂的最低浓度为ρ 则根据质量衡算方程,有0.05ρ=(3+0.05)×1.0解之得ρ=61 mg/L加入示踪剂的质量流量为61×0.05g/s=3.05g/s2.9假设某一城市上方的空气为一长宽均为100 km 、高为1.0 km 的空箱模型。
干净的空气以4 m/s 的流速从一边流入。
假设某种空气污染物以10.0 kg/s 的总排放速率进入空箱,其降解反应速率常数为0.20h -1。
假设完全混合,(1)求稳态情况下的污染物浓度;(2)假设风速突然降低为1m/s ,估计2h 以后污染物的浓度。
解:(1)设稳态下污染物的浓度为ρ 则由质量衡算得10.0kg/s -(0.20/3600)×ρ×100×100×1×109m 3/s -4×100×1×106ρm 3/s =0解之得ρ=1.05× 10-2mg/m 3(2)设空箱的长宽均为L ,高度为h ,质量流量为q m ,风速为u 。
