锂离子电池用层状LiMnO_2基正极材料的研究进展
锂离子电池正极材料的发展现状和研究进展

作者简介:蒋 兵(1981-),男,助理工程师,主要从事有色金属材料的检验和测试工作。
锂离子电池正极材料的发展现状和研究进展蒋 兵(湖南有色金属研究院,湖南长沙 410015)摘 要:介绍了锂离子电池正极材料钴酸锂、镍酸锂、锰酸锂、磷酸铁锂、钒的氧化物以及导电高聚合物正极材料的发展现状和研究进展。
LiCoO 2在今后正极材料发展中仍然有发展潜力,通过微掺杂和包覆都可使钴酸锂的综合性能得到提高,循环性能大大改善。
环保、高能的三元材料和磷酸铁锂为代表的新型正极材料必将成为下一代动力电池材料的首选。
关键词:锂离子电池;正极材料;磷酸铁锂;三元材料中图分类号:T G146126 文献标识码:A 文章编号:1003-5540(2011)01-0039-04自日本Sony 公司于1990年首先推出以碳为负极的锂离子二次电池产品后,因具有工作电压高、容量大、自放电小、循环性能好、使用寿命长、重量轻、体积小等突出优点,目前,其应用已渗透到包括移动电话、笔记本电脑、摄像机、数码相机等众多民用及军事领域。
另外,国内外也在竞相开发电动汽车、航天和储能等方面所需的大容量锂离子电池。
对锂离子电池而言,其主要构成材料包括电解液、隔膜、正负极材料等。
一般来说,在锂离子电池产品组成部分中,正极材料占据着最重要的地位,正极材料的好坏,直接决定了最终锂离子电池产品的性能指标。
本文将对锂离子电池正极材料的发展现状和研究进展进行综述和探讨。
1 正极材料的选择正极材料在性质上一般应满足以下条件:(1)在要求的充放电电位范围,与电解质溶液具有相容性;(2)温和的电极过程动力学;(3)高度可逆性;(4)在全锂化状态下稳定性好。
其结构具有以下特点:(1)层状或隧道结构,以利于锂离子的脱嵌,且在锂离子脱嵌时无结构上的变化,以保证电极具有良好的可逆性能;(2)锂离子在其中的嵌入和脱出量大,电极有较高的容量,并且在锂离子脱嵌时,电极反应的自由能变化不大,以保证电池充放电电压平稳;(3)锂离子在其中应有较大的扩散系数,以使电池有良好的快速充放电性能。
层状锰酸锂和尖晶石锰酸锂

层状锰酸锂和尖晶石锰酸锂
首先,从化学结构上来看,层状锰酸锂是一种层状结构的化合物,其化学式为LiMnO2。
它具有层状结构,其中锰离子和氧离子形成层状排列,锂离子嵌入在层间。
而尖晶石锰酸锂的化学式为LiMn2O4,具有尖晶石结构,其中锰和氧离子以尖晶石结构排列,锂离子位于空隙中。
其次,从电化学性能上来看,层状锰酸锂具有较高的比容量和比能量,但循环稳定性较差,容量衰减严重;而尖晶石锰酸锂具有较好的循环稳定性和热稳定性,但比容量和比能量较低。
因此,在实际应用中,不同的电池系统会根据具体的要求选择合适的正极材料。
此外,从制备工艺和成本角度来看,层状锰酸锂的制备工艺相对简单,成本较低,但在循环寿命和安全性方面存在局限;而尖晶石锰酸锂的制备工艺复杂,成本较高,但在循环寿命和安全性方面具有优势。
总的来说,层状锰酸锂和尖晶石锰酸锂都是锂离子电池中重要的正极材料,它们各自具有优缺点,在不同的应用场景中会有不同
的选择。
在未来的发展中,科研人员也在不断努力改进这些材料,以满足电池在能量密度、循环寿命、安全性等方面的需求。
锂离子电池正极材料层状镍钴锰复合材料LiNi_xCo_yMn_zO_2的研究

收稿日期5作者简介女,6年生,副教授,张家口市,5基金项目河北省科学技术研究与发展计划项目(53);张家口市科学技术研究与发展指令计划(B )锂离子电池正极材料层状镍钴锰复合材料LiNi x Co y Mn z O 2的研究王甫丽王克柏永清刘朴薛红丹河北建筑工程学院数理系摘要层状镍钴锰复合材料LiNi x Co y Mn z O 2具有比商业化锂离子电池正极材料LiCoO 2低廉的成本、更低的毒性、更好的热稳定性,近年来受到广大科研工作者的关注.本文重点介绍了近年来层状镍钴锰复合正极材料合成方法及掺杂、包覆改性方面的研究成果,并简要概括了目前存在的问题及材料未来的研究趋势.关键词锂离子电池;正极材料;层状LiN i x Co y Mn z O 2中图分类号TQ1310引言目前,锂离子电池正极材料主要有钴酸锂、镍酸锂、锰酸锂及磷酸亚铁锂四个系列,钴酸锂仍是市场主流,但是钴资源有限、价格昂贵、钴有毒和安全性能差等缺点限制其今后的大规模应用;镍酸锂的实际容量较钴酸锂高,Ni 的价格较钴便宜,但镍酸锂制备困难,热稳定性差;锰酸锂具有原料丰富、价格低廉、环境友好、热稳定性好的优势,但锰酸锂的容量低,循环性能差;磷酸亚铁锂价格低廉、资源丰富、循环性能良好、热稳定性优、环境友好,但导电性差、密度低.这些材料自身都有明显不足,制约其进一步应用[12].1999年Liu 等[3]首次报道了层状LiNi 1X Y Co X Mn Y O 2(0<X<05,0<y<05)的镍钴锰三元过渡金属复合氧化物,该氧化物为LiCoO 2/LiNiO 2/LiMnO 2共熔体,具有LiCoO 2的良好循环性能、LiNiO 2的高比容量和LiMnO 2的安全性.2001年T.Ohzuku 等[4]首次合成了具有优良性能的层状NaFeO 2结构的LiNi 1/3Co 1/3Mn 1/3O 2,镍钴锰三元复合材料的研究因此受到特别关注[58].层状镍钴锰三元复合材料一定程度综合了LiCoO 2、LiNiO 2、LiMnO 2的优势,弥补了不足,改善了材料性能,降低了成本[6].本文就近年来层状镍钴锰三元复合材料的制法、性能方面的研究状况进行综述,并简要概述了锂离子电池正极材料的发展趋势.1制备方法11固相法固相合成技术是合成金属氧化物常用的方法,将反应物按计量比混合研磨,压片或造粒,然后置于高温炉中在空气或氧气气氛下烧结.固相合成法具有操作简便,易于工业化生产的优点,是目前产业化生产的主要方法.Ren 等[9]以Co 3O 4,MnO 2,Ni(OH )2,LiOH H 2O 为原材料,固相合成了层状N aFeO 2结构LiNi 1/3Co 1/3Mn 1/3O 2.SEM 图显示,产物平均粒径约为1m,呈无规则聚集状,比表面积12146m 2/g.2546V 电压范围,200mA /g 电流密度下充放电结果显示:产物具有187mAh/g 的初始放电容量,循环30次容量损失17%.于凌燕等[10]以H 2C 2O 42H 2O,LiOH H 2O,乙酸镍,乙酸锰为原料,固相法合成了层状第28卷第4期2010年12月河北建筑工程学院学报JOURNAL O F HEBEI INSTITUTE OF ARCHI TECTU RE A ND CIVIL EN GINEERING Vol 28No 4Dec.2010:2010-07-2:19707024:09211409110094NaFeO 2结构Li[Li 067Mn 0583Ni 025]O 2,该材料粒径60100nm,2544V 之间05C(100mA/g)充放电循环试验,可逆比容量在120mAh/g 以上,如将截止电压高达46V,比容量最高可达234mAh/g.固相法缺点在于合成过程中,各组分难以均匀共混,受热不均匀,需反复研磨和烧结,延长了合成时间,造成能量的浪费,生产效率降低;所得产物粒径较大,不均匀,直接影响材料的电化学性能;气氛、温度、时间、原料等因素对制备的正极材料晶体结构和电化学性能有着重要的影响;产物的粒径分布不易控制,均匀性、一致性和重现性较差.12共沉淀法共沉淀法可以使原材料进行分子级接触,是一种优良的合成方法.pH 值、搅拌速率以及配合物试剂种类、浓度的选择决定了最终产物的性能,具有操作复杂,重现性差的特点.共沉淀法在合成特定形貌的正极材料中被广泛应用[6].卢华权等[11]以Ni(NO 3)2,Mn(NO 3)2为原料,以草酸铵为沉淀剂,不同PH 值(40,55,70,85)下所得沉淀分别与LiNO 3研磨,450烧结6h,压片,800煅烧12h,得结晶良好的LiNi 05Mn 05O 2,电化学性能测试证明:PH =70时合成的材料电化学性能更好,01C 倍率下,材料首次放电比容量达到了185mAh/g,循环20次后,放电比容量仍保持在160mAh/g.钟辉等[12]采用沉淀喷雾造粒法造前驱体,于750在空气中煅烧20h 合成Li(Ni 1/3Co 1/3Mn 1/3)O 2正极材料,XRD 、SEM 、粒度分析、电性能测试表明:该材料是NaFeO 2结构,2842V,2845V 充放电首次放电容量分别为1735和1854mAh/g,首次放电效率分别为90%和838%,40次循环后容量保持96%和84%.13溶胶凝胶法溶胶一凝胶法过程螯合物的形成,同样可使各组分进行分子级接触,使产物一次结晶完全.不但可以降低灼烧温度和减少结晶时间,还能得到粒径较小且分布均匀的产品.戴长松等[13]采用溶胶凝胶法制备了锂离子电池正极材料LiNi 05Co 025Mn 025O 2,XRD 、XPS 、SEM 测试表明:层状结构明显,产品结晶粒度均匀;充放电测试表明:在恒流充电模式下,充电截止电压由435V 升至475V,首次放电容量由179mAh/g 升至201mAh/g,50次循环放电后,容量保持率由7495%升至7848%;在先恒流再恒压的充电模式下,首次放电容量为212mAh/g,50次循环放电后,容量保持率升至8771%;EIS 测试表明:随着充电截止电压的增大,该材料的传荷电阻变小.温建武等[14]以Li(NO 3)2H 2O 、Ni(NO 3)24H 2O 、Mn(NO 3)24H 2O 和Mn(CH 3COO)24H 2O 为原料,以目标产物LiNi 1/3Co 1/3Mn 1/3O 2化学计量比配成05mol/L 水溶液,加入丙烯酸水溶液,然后将混合液置于Co60射线(强度5575Gg/min)辐照2h 的凝胶物质,150烘干20h,研磨,500预烧15h,研磨,在不同温度(850,900,950)煅烧10h,得产物.测试结果表明:900样品层状结构最好,电化学性能最佳,首次放电容量达184mA h/g,01C 和2845V,30次循环放电,容量保持874%.14熔融盐法熔融盐法是利用低共熔混合熔融盐做反应物或兼作熔剂,反应则是在固液态间进行,离子扩散速度显著加快,可以有效降低反应温度和时间,改善材料晶体结构和性能,合成出符合计量比以及结晶发育良好的正极材料[15].汤宏伟等[16]利用低共融混合锂盐038LiOH 062LiNO 3与自制前驱体Ni 08Co 02x Al x (OH )2(0X 015)按一定摩尔比混合,经过3个恒温阶段烧结,(2003h,6005h,85015h)的LiNi 08Co 02x Al x O 2(0X 015),XRD 、SEM 、电性能测试表明:材料具有规整的层状NaFeO 2结构,振实密度达297g/cm3,02C 放电倍率和3043V,首次放电容量达1675mAh/g,循环性能良好.复合物的组成对材料电性能的影响复合物中各成分元素含量不同直接影响材料的结构、热稳定性、循环性能及倍率放电能力,另外,钴含量还直接决定材料价格106河北建筑工程学院学报第28卷2.郭瑞等[17]采用共沉淀法合成锂离子电池正极材料LiCo 2x N i 052x Mn 05X O 2(2x=01,02,033,05),对产物进行了XRD 、SEM 、充放电和DSC 测试,以考察不同钴含量2x 对材料的结构、电化学性能和热稳定性的影响,结果表明:随着材料中钴含量2x 的提高,材料的晶格参数和晶胞体积逐渐减小,材料的循环性能和倍率放电能力得到改善,特别当2x=033时,材料有良好的电化学性能:首次放电容量为175mAh/g,30次循环后容量保持率为891%,同时其具有最好的热稳定性.Kim 等[18]研究了Li 过量对于三元材料Li[Lix(Ni z Co 12z Mn z )1x ]O 2的影响.作者发现过量的Li 能有效抑制充放电过程中的体积变化,尽管过量Li 的贡献没有高含量Co 的贡献大.当Co 含量低时,适度过量的Li 能有效抑制阳离子混排,改善材料的循环性能和倍率性能.在28V~45V 的充放电区间内,Li 105(Ni 037Co 023Mn 040)095O 2首次放电容量达到175mAh/g,50次循环后容量保持率为96%,比Li(N i 034Co 022Mn 044)O 2的性能更为优异.国海鹏等[19]采用Co 2+浓度递增的金属离子(Ni 2+,Co 2+,Mn 2+)混合液分次共沉淀制得Ni 1/2Co 1/6Mn 1/3(OH )2前驱体,与LiOH H 2O 研磨混合,空气气氛下450预烧48h,升温至一定温度(700、750、800、850),恒温烧结12h,室温冷却,研磨的产物LiNi 1/2CO 1/6Mn 1/3O 2.电化学性能测试证明800的梯度材料具有最佳电化学性能,2542V,01C 倍率放电50次后,材料的容量仍保持在1712mAh/g.,其中含量较高的Mn 作为材料骨架起到稳定晶体结构的作用,并能大幅度降低成本,Ni 含量占过渡金属的50%,保证了材料具有较高首次比容量.在不加大成本较高的Co 用量的前提下,通过合成具有Co 含量梯度的正极材料,使Co 在材料粒子中的含量由内到外递增,改善材料的充放电性能.戴长松等[13]对其溶胶凝胶法合成的LiNi 05Co 025Mn 025O 2进行XRD 、XPS 表征表明:Co 、Mn 以+3、+4价形式存在,Ni 以+2、+3价存在,且Ni 2+、N i 3+含量比为11,在2848V 扫描范围内,该材料发生Ni 2+/Ni 3+和Co 3+/Co 4+两对电化学反应,Mn 则主要起稳定晶体结构的作用.3复合材料的改性研究为了进一步改善材料性能,研究者们通过掺杂和包覆等手段进行材料改性.31掺杂改性半径接近的元素,适当的掺杂比例和均匀的掺杂能使材料的结构更稳定,改善材料的循环性能和热稳定性.杨平等[20]采用草酸盐前驱体合成Ti 4+、Mg 2+掺杂正极材料Li(NiM l/3Co l /3x Mn l /3)M x O 2(M=T i,Mg).利用XRD 和SEM 对其结构和形貌进行表征,并采用循环伏安、交流阻抗、恒流/恒压充放电测试其电化学性能.结果表明:Ti 4+、Mg 2+掺杂后晶胞体积增大,大倍率充放电时LiNi l /3Co l /3Mn l /3O 2的电化学反应阻抗Rct 降低,其大倍率充放电性能得到改善,Ti 2+掺杂效果更好;当掺杂量x=0025时,材料晶型完整,具有单一的a NaFeO 2层状结构;1C 倍率时Li(Ni l/3Co l/3-0025Mn l/3)Ti 0025O 2的第二循环放电容量为1432mA h/g,2C 时为1280mA h/g,经100次循环后容量分别为1325和1158mA h/g,容量保持率为9253%和9047%.曹千等[21]将Co Ni (Mn+M)=111(M=Cr,Zr )的硝酸盐溶解于适量水中,氮气保护气氛中缓慢滴加25%氨水和氢氧化钠溶液,然后将沉淀过滤、洗涤、干燥、研磨,乙醇浸润和过量7%的氢氧化锂球磨混合,所得前驱体在480煅烧5h 除去有机物,最后在850下二次煅烧12h.通过少量Cr 、Zr 代替复合材料中Mn 实验,产品进行XRD 、SEM 、CV 、EIS 、充放电测试证明:少量Cr 掺杂,不会影响材料层状晶型,层状结构良好;一定范围掺杂可提高材料电化学过程的可逆性,降低材料的电荷传递阻抗,提高材料的充放电容量和循环性能.而Zr 替代Mn 则对材料性能影响不明显.可能原因是:Cr 、Mn 离子半径接近,而Zr 则较大(r C r =055,r Mn =053,r Zr =160).国海鹏等[19]对梯度材料L N 6M 3O 进行了F 掺杂改性,结果表明,在不牺牲容量的情况下,产物的振实密度得以提升,达到,接近商业化L O 3材料包覆改性吴晓彪等[]以过渡金属乙酸盐和氢氧化锂为原料,采用共沉淀方法制备了锂离子电池富锂正极材107第4期王甫丽等锂离子电池正极材料层状镍钴锰复合材料LiN i x Co y Mn z O 2的研究Co i i 1/2Co 1/n 1/2241g cm 1iCo 2.222料Li[Li (02)Mn (054)Ni (013)Co (013)]O 2并对该材料进行表面包碳.X 射线衍射技术(XRD)、扫描电子显微技术(SEM)实验数据表明,该材料具有层状NaFeO 2结构,包碳后材料结构没有变化,表面覆盖上一层纳米级别的颗粒.电化学性能测试结果表明该材料包碳后在01C(1C=180mA/g),20~48V 电位范围内首次放电比容量高达2590mAh/g.包碳后首次放电比容量,倍率性能,循环性能均得到提高;采用电化学阻抗谱(EIS)研究包碳前后该材料的传荷阻抗,结果显示碳包覆材料的传荷阻抗明显减小,电子电导率得到提高,从而提高电化学性能.Kim 等[23]以蔗糖溶液为碳源,加入LiNi 1/3Co 1/3Mn 1/3O 2后在350下处理1h,得到表面包覆有纳米厚度碳层的样品.与不包覆的样品相比,1%残碳的样品有着更优异的循环性能和倍率性能,而3%残碳的样品的表现出相对较差的电化学性能.同时,包覆后的样品的热稳定性均有所提高.4存在的问题和未来研究方向与钴酸锂相比,镍钴锰复合材料性能得到了一定程度改善,但实际使用容量仍低于理论容量,循环稳定性和高电压充电时安全隐患仍存在,粉体的填充性不理想,昂贵的N i 、Co 元素比例较高,合成工艺较为繁复.未来的研究关键在于:优化掺杂、包覆的改性手段,降低钴含量,降低产业化成本,提高材料的振实密度、改善高低温和高截止电压下的循环稳定性能和倍率性能;探索适合产业化生产的方法、工艺;开发合成有特殊形貌的纳米镍钴锰正极材料的方法、工艺,解决纳米电极材料中粒子的团聚问题.参考文献[1]Kisuk K,Yiag S M,et aL Elect rodes with high capacit y for Recha rgeable lithium batteries.Science,2006,311:977[2]廖文明,戴永年,姚耀春等.4种正极材料对锂离子电池性能的影响及其发展趋势.材料导报,2008,22(10):45~49[3]Liu Z L,Yu A S,Lee J Y.Synthesis and Char act er ization of LiNi1X YCoX MnYO 2as the Cathode Materials of Sec ondary Lithium Batter ies.J.P ower Sources,1999,81/82:41619[4]Ohzuku T,Makimur a yer ed lithium insertion mater ial of LiCo 1/3Ni 1/3Mn 1/3O 2for lithium ion batt eries.Chem Lett,2001,30:642[5]谭龙,刘浩文.锂离子电池正极材料LiNi 1/3Co 1/3Mn 1/3O 2的研究进展.化学世界,2010,2:122~126[6]唐爱东,王海燕,黄可龙,等.锂离子电池正极材料层状Li Ni Co Mn O 的研究.化学进展,2007,19(09):1313~1321[7]田华,叶乃清.正极材料LiNi 1/3Co 1/3Mn 1/3O 2的结构性能及制备技术研究.材料导报,2008,22(专辑X).238~241[8]刘智敏.锂离子电池正极材料层状LiNixCo 12xMn x O 2的合成与改性研究.中南大学博士学位论文,2009[9]Ren H B,Wang Y R,Li D C,et a1.Solid State Ionies,2008,178:1969~1974[10]于凌燕,仇卫华,连芳等.锂离子电池正极材料Li[Li 0.167Mn 0583Ni 025]O 2的合成与性能研究.电化学,2008,14(02):135~139[11]卢华权,吴锋,苏岳峰等.草酸盐共沉淀法制备锂离子电池正极材料LiNi 0.5Mn 05O 2及其电化学性能.物理化学学报,2010,26(01):51~56[12]钟辉,许惠.层状Li(Ni 1/3Co 1/3Mn 1/3)O 2正极材料的合成与电化学性能研究.化学学报,2007,64(02):147151[13]戴长松,葛吴,王殿龙等.层状正极材料LiNi 05Co 025M n 025O 2的结构及电化学行为.无机化学学报,2007,23(03):432~438[14]温建武,滕元成,李玉香等.锂离子电池正极材料LiNi 1/3Co 1/3Mn 1/3O 2的合成及性能研究.电子元件与材料,2009,28(12):30~32[15]KIM J H ,Myung ST,Sun Y K.Molten salt synthesis of LiNi 05Mn 15O 4spinel for 5V class cat hode mater ial of li ion secondar y battery.Electr ochim Act a,2004,49:219~227[16]汤宏伟,朱志红,常照荣.熔融盐法合成高密度锂离子电池正极材料LiNi 08Co 02x Al x O 2.稀有金属材料工程,2010,39(02):333~337[]郭瑞,史鹏飞,程新群等钴含量对锂离子电池正极材料L x N 5x M 5x O 的性能影响稀有金属,,33(3)3~35[]KIM M ,KUM G I N,OI T Sy ,S ,f O L +x (N z z M z )x O (z=x=)y S y D y M 108河北建筑工程学院学报第28卷17.iCo 2i 02n 02.20090:71718J A A CH H .nt hesis tr ucture and Electrochemical Character istics o verlithiated i 1i Co 12n 120104and 0001Posit ive Electrodes P repared b pra r ing ethod.J.Elect rochem.Soc,2008,155(01):A82~A89[19]国海鹏.层状锂离子电池正极材料LiNi 1/2Co 1/6Mn 1/3O 2的制备及性能研究.北京化工大学硕士学位论文,2008[20]杨平,张传福,戴曦等.正极材料Li(Ni 1/3Co 1/3X Mn 1/3)M x O 2(M =Ti,M g)的合成及性能.中国有色金属学报,2009,19(01):101~107[21]曹千.锂离子电池正极材料.复旦大学硕士论文,2008[22]吴晓彪,董志鑫,郑建明等.锂离子电池正极材料Li[Li (02)Mn (054)Ni (013)Co (013)]O 2的碳包覆研究.厦门大学学报(自然科学版),2008,增刊:224~227[23]KIM H S,KONG M Z,KIM K,et al.Effect of car bon coating on LiNi 1/3Mn 1/3Co 1/3O 2cathode mater ial for lithium secondary batter ies.J.Power Sour ces,2007,171:917~921Layered Nickel/Cobalt/Manganese ComplexusLiNi x Co y Mn z O 2as Cathode Materials for Lithium Ion BatteryWan g Fu li ,Wa ng Ke ,Ba i Y on gqin g,Liu Pu ,Xu e Hon gda nDepartment of Mat hematics and P hysics,H ebei Institute of Architecture and Civil Engineer ingAbstr act Layered nickel/cobalt/manganese complexus LiNi x Co y Mn z O 2has attr acted mor e and moreattentions from scientists for its excellent properties,such as lower cost,lower toxicity and high er ther mal stability than LiCoO 2as a cathode material.Various synthesis methods,doping and surface modification approaches ar e introduced in detail.T he achievements of this scientific re search area in r ecently years are displayed,and the current main problems and further resear ch trend of the materials are also pointed out.Key words lithium ion batter y;cathode materials;layered structure LiNi x Co y Mn z O 2109第4期王甫丽等锂离子电池正极材料层状镍钴锰复合材料LiN i x Co y Mn z O 2的研究。
锂离子电池正极材料LiMnO_2的掺杂及其电化学性能

锂离子电池正极材料LiMnO 2的掺杂及其电化学性能粟智1,*徐茂文1叶世海2王永龙2(1新疆师范大学生命科学与化学学院,乌鲁木齐830054;2南开大学化学学院,新能源材料化学研究所,天津300071)摘要:采用水热法合成了用于锂离子电池正极材料的LiM x Mn 1-x O 2(M=Mg,Y,Zr)化合物.采用X 射线衍射(XRD)、透射电子显微镜(TEM)、X 射线光电子能谱(XPS)等手段对材料的晶体结构和形貌进行了表征,材料的电化学性能通过恒流充放电和交流阻抗谱(EIS)进行测试,分析了掺杂元素在改善材料性能中的作用.结果表明,掺杂后的LiM x Mn 1-x O 2正极材料循环性能优于未经掺杂的材料.其中以掺杂钇的Li 0.99Mn 0.979Y 0.021O 2正极材料循环性能最佳,在室温下,充放电电流密度为50mA ·g -1时,60次循环后放电容量为226.3mAh ·g -1.关键词:层状LiMnO 2;掺杂;水热合成法;电化学性能中图分类号:O643.3Doping of Layered LiMnO 2as Cathode Materials for Lithium -IonBatteries and Their Electrochemical PropertiesSU Zhi 1,*XU Mao -Wen 1YE Shi -Hai 2WANG Yong -Long 2(1College of Life Science and Chemistry,Xinjiang Normal University,Urumqi 830054,P.R.China ;2Institute of New EnergyMaterial Chemistry,College of Chemistry,Nankai University,Tianjin 300071,P.R.China )Abstract :Hydrothermal methods were used to prepare doped LiM x Mn 1-x O 2(M=Mg,Y,Zr)as cathode materials for lithium -ion batteries.The structure and morphology of the as -prepared cathode materials were characterized by X -ray diffraction (XRD),transmission electron microscopy (TEM)and X -ray photoelectron spectroscopy (XPS).The effects of ion doping on the performance of orthorhombic materials was analyzed in terms of their crystal structure,charge -discharge curves,cycle performance and electrochemical impedance spectroscopy (EIS).Results show that the dopedmaterials had better cycle performance.In particular,the discharge capacity of Li 0.99Mn 0.979Y 0.021O 2remains 226.3mAh·g -1after 60cycles with a current density of 50mA ·g -1at room temperature.Key Words :Layered LiMnO 2;Doping;Hydrothermal synthesis;Electrochemical property[Article]物理化学学报(Wuli Huaxue Xuebao )Acta Phys.-Chim.Sin .,2009,25(6):1232-1238Received:December 26,2008;Revised:March 9,2009;Published on Web:April 13,2009.*Corresponding author.Email:suzhixj@;Tel:+86991-4333246.国家自然科学基金(20773070)和新疆师范大学博士基金(XJNUBS0807)资助鬁Editorial office of Acta Physico -Chimica Sinica层状LiMnO 2具有比容量高、价格低、污染小等优点,符合锂离子电池的高性能、低成本和环境友好的发展趋势,是一种非常有应用前景的锂离子电池正极材料.研究发现,该材料存在的主要问题有[1-5],在充放电过程中LiMnO 2易向类尖晶石结构Li 2Mn 2O 4相转变,导致其容量的迅速衰减;另外,LiMnO 2合成困难,尤其是层状LiMnO 2;还有电极材料中的锰在电解液中的溶解和锂在电极表面的沉积.为解决这些问题,人们从其衰变机理、掺杂离子的选择等方面进行了探索和研究.对LiMnO 2性能改善采用最多的方法是阳离子掺杂,并在改善材料LiMnO 2的循环性能方面已取得了较好的效果[6-13].本文用水热法对LiMnO 2正极材料进行掺杂改性,合成了阳离子掺杂正极材料LiMn 1-x M x O 2(M=Mg,Y,Zr),并对合成材料的微观结构、初始容量、循环稳定性及高倍率放电性能进行了研究.探讨了阳离子掺June1232No.6粟智等:锂离子电池正极材料LiMnO2的掺杂及其电化学性能杂对材料电化学性能的影响机制.1实验部分1.1材料制备实验用试剂均为分析纯,均由天津基准化学试剂有限公司生产.LiMnO2材料的制备:将6mol·L-1的LiOH溶液30mL和自制的Mn2O3(将Mn(CH3COO)2·4H2O在500℃焙烧15h)2g置入高压反应釜中,150℃保温36h.产物随炉冷却,取出后用去离子水洗涤,直至pH值为9左右,于105℃烘箱(DL-101-2BS,天津市中环实验电炉有限公司)中放置12h备用.LiMn0.99M0.01O2(M=Mg,Y,Zr)材料的制备:分别取Mn/M=0.99/0.01(M=Mg,Y,Zr)摩尔比的Mg(NO3)·6H2O(Y(NO3)3·6H2O,Zr(NO3)4·5H2O)加去离子水制成悬浊液后,边搅拌边加入6mol·L-1的LiOH溶液30mL,然后按以上水热法进行掺杂材料的制备.LiMn1-x Y x O2(x=0.02,0.03,0.05)材料的制备:取Mn/Y=0.02,0.03,0.05(摩尔比)的Mn2O3和Y(NO3)·6H2O,加去离子水制成悬浊液后,边搅拌边加入6 mol·L-1的LiOH溶液30mL,然后按以上水热法进行钇掺杂材料的制备.1.2材料表征样品的物相结构通过X射线衍射仪(Rigaku D/ max-2500,日本理学株式会社)测定.采用Cu Kα(λ= 0.15418nm)辐射源,石墨单色检测器,管电压40kV,管电流100mA,衍射角2θ为3°-80°,扫描速率为2(°)·min-1.样品的形貌分析是先将样品放入无水乙醇中,用超声波分散一定时间,取少量分散液滴在有铜网支撑的碳膜上.然后,在加速电压为200kV,真空度高于6.7×10-4Pa的透射电子显微镜(FEI Tecnai 20,美国FEI公司)下进行形貌观察.采用X射线光电子能谱仪(XPS,PHI-5300,美国PE公司)对最终产品进行测试.操作时,用Mg Kα辐射作为激发源(1253.6eV),功率为25W,入射角为45°,扫描方式为全谱扫描.材料的组成采用等离子体发射光谱仪(ICP-AES,IRIS Advantage1000,美国Thermo公司)进行测定,操作时载气的辅助气流量为0.5L·min-1,雾化室压力为152kPa,泵速为110r·min-1,RF(射频)功率为1150W;长波积分5s,短波积分15s. 1.3电化学性能测试将活性物质、乙炔黑、粘结剂聚四氟乙烯(PTFE)按质量比75∶20∶5混合,用无水乙醇作为分散剂将其碾压成片,然后切成直径为8mm的圆片,在烘箱中105℃干燥8h,得到所需的正极极片.电解质溶液使用1mol·L-1的LiPF6/PC(碳酸丙烯酯)(10%,w,下同)+EC(碳酸乙烯酯)(30%)+DEC(二乙基碳酸) (60%)的有机混合溶液.负极使用锂片(新疆有色金属研究所生产,纯度99.99%),在真空手套操作箱(STX-3型,南京科析实验仪器研究所)里组装好模拟电池,将电池静置12h以后,在电池测试系统(Land CT2001A,武汉金诺电子有限公司)上进行充放电和循环性能测试.测试温度为25℃,充放电电表1样品的化学组成Table1Chemical composition of the as-preparedsamples measured by ICP-AESDesign formula ICP-AESLiMnO2Li0.99MnO2LiMn0.99Mg0.01O2Li0.99Mn0.99Mg0.01O2LiMn0.99Zr0.01O2Li0.98Mn0.99Zr0.01O2LiMn0.99Y0.01O2Li1.01Mn0.99Y0.01O2LiMn0.98Y0.02O2Li0.99Mn0.979Y0.021O2LiMn0.95Y0.05O2Li1.02Mn0.952Y0.048O2图1不同掺杂的LiMnO2样品的XRD图Fig.1XRD patterns of doped-o-LiMnO2sampleso:orthorhombic structure1233Acta Phys.-Chim.Sin.,2009Vol.25流密度为50mA·g-1,充放电电压为2.0-4.3V.循环7伏安实验采用电化学工作站(LK2005,天津兰力科化学电子高技术有限公司)进行测试,扫描速率为0.1mV·s-1.运用交流阻抗仪(IM6ex,德国Zahner公司)测定材料的电化学阻抗谱,测定频率范围为10kHz-10mHz,微扰电压为5mV.2结果与讨论2.1材料结构和形貌分析表1列出了用等离子体发射光谱仪(ICP-AES)分析得到合成材料的化学组成.图1为合成材料的XRD谱.表2是利用Retiveld方法对XRD谱图进行精修后,用最小二乘法计算得到合成材料的晶胞参数.从图1中可以看出材料掺杂前后所得到的最终产物均为层状正交结构.从图1中还可以看出,当掺杂离子浓度较低时均可得到纯相掺杂的正交结构LiMnO2材料(o-LiMnO2).从ICP-AES分析结果来看,用水热法可以得到接近按摩尔比设计的目标材料,从表2中发现,除Mg2+外,其它离子掺入后均增大了材料的晶胞体积.这是由于Mg2+的离子半径(0.065nm)与Mn3+离子半径(0.066nm)接近,而Y3+离子半径(0.093nm)和Zr4+(0.080nm)均大于被替代的Mn3+的离子半径.图2为合成材料的TEM图.从图中可以看出,用水热法合成得到材料分布比较均匀,材料尺寸在100-200nm范围,结晶度较好,离子掺杂后并未改变材料的形貌.2.2材料的电化学性能测试采用不同的充放电倍率对掺杂化合物进行电化学循环性能测试,材料的电化学循环寿命见图3.从图3中可以看出,o-LiMnO2正极材料在电化学嵌入/脱出锂过程中,无论掺杂与否,材料的放电容量在循环的初期,是逐步增大的,这与尖晶石结构的LiMn2O4以及单斜层状LiMnO2循环初期容量快速衰减正好相反,在容量达到一定值后趋于稳定.这表2样品经Rietveld精修后的晶胞参数Table2Lattice parameters of the as-preparedsamples after Rietveld refinementSample a/nm b/nm c/nm103V/nm3 Li0.99MnO20.45700.57410.280073.46Li0.99Mn0.99Mg0.01O20.45700.57400.280173.45Li0.98Mn0.99Zr0.01O20.45710.57410.280273.53Li1.01Mn0.99Y0.01O20.45720.57420.280473.61Li0.99Mn0.979Y0.021O20.45700.57440.280573.63Li1.02Mn0.969Y0.031O20.45670.57460.280873.69图2样品的TEM图Fig.2TEM images of the as-prepared samples(a)Li0.99MnO2,(b)Li0.99Mn0.99Mg0.01O2,(c)Li1.01Mn0.99Y0.01O2,(d)Li0.98Mn0.99Zr0.01O 2 1234No.6粟智等:锂离子电池正极材料LiMnO2的掺杂及其电化学性能说明o-LiMnO2在电化学循环过程的初期有一个活化的过程.这种活化的过程是一个向尖晶石相LiMn2O4转化的过程,这种电化学循环过程中形成的尖晶石相不同于直接合成的标准尖晶石相LiMn2O4,这种结构具有更高的稳定性[14].从图中可知,在掺入1%的阳离子后,材料的初始容量均有所增加,但随着掺杂量的增加,材料的放电容量逐渐下降,如掺入2%与3%的钇时,材料的初始放电容量分别为128.3和125.8mAh·g-1,低于掺入1%的钇放电容量134mAh·g-1.对其它掺杂离子结果基本一致.对电极材料来说,材料的容量是由其有效的Mn3+含量决定的.由于Mg2+为低价金属阳离子,当Mg2+离子取代部分Mn3+,导致Mn3+浓度减小,从而引起初始容量的降低,但会在Mn3+离子的价带引入空穴,从而产生有效的Mn3+,这些离子会干扰反铁磁自旋排列,增加层状结构的稳定性[15].对掺入高价态离子,如掺入Zr4+,由于Zr4+的电荷高于Mn3+,并且Zr4+离子半径(0.080nm)大于Mn3+的离子半径(0.066nm),为了保持电荷平衡,将产生Mn2+,而Mn2+离子半径(0.080nm)也大于Mn3+的离子半径,因此在材料中掺入Zr4+高价阳离子后,电极材料的离子分布形式发生了变化,材料中的Mn3+在充放电过程中产生的Jahn-Teller结构畸变得到有效抑制,因而掺入Zr4+后能增强材料的结构稳定性和有利于Li+的嵌脱[16].而对于掺入Y3+后,尽管不能改变本体材料中Mn3+浓度,由于Y3+为非Jahn-Teller效应离子,当Y3+引入晶格后,由于形成结构稳定的YO6八面体,替代因Jahn-Teller畸变效应而扭曲的MnO6八面体,降低了MnO6八面体的扭曲应力,从而减小了材料的结构畸变.同时Y3+的离子半径大于Mn3+的离子半径,使得材料的晶胞体积增大,有利于稳定材料的结构和Li+的嵌脱,增强了材料的电化学循环可逆性,从而引起初始容量的增加.但Y3+又是非活性物质,因此随离子的含量增大,会造成材料的初始容量下降.图4显示了在充放电电流密度为50mA·g-1时,图3样品在不同放电倍率下的电化学循环寿命图Fig.3Cycle performance of the as-prepared samples at various discharge current densitiescharge current:50mA·g-1;potential range:4.3-2.0V(vs Li/Li+)图4样品的第1周(a)和第10周(b)充放电曲线Fig.4The charge-discharge curves of the as-prepared samples in the1st(a)and10th(b)cycles1235Acta Phys.-Chim.Sin.,2009Vol.25材料的第1周和第10周充放电曲线.从曲线可以看出,样品第1周期只在3.0V左右有一个明显的充电平台,但只出现较弱的放电平台,表明存在较大的不可逆容量,而第10周在3.0V和4.0V出现了两个平台,表明材料在电化学过程中已发生了结构变化.图5显示了Li0.99MnO2和Li1.01Mn0.99Y0.01O2两种材料的循环伏安曲线图.由图可知,第1周阳极过程中,锂离子从电极材料o-LiMnO2中脱嵌,在4.0V 左右有一个很宽的氧化峰,说明大多数的锂离子都能够脱嵌出来.而阴极过程中,2.8V左右的还原峰强度较弱,说明第1周锂离子可逆嵌入/脱出的效率相对较低,与材料的充放电行为基本一致.在随后的循环中,在3.0V左右的氧化峰强度逐渐增强,同时2.8V和4.0V的两个还原峰强度也逐渐增强.对于其它离子掺杂后材料的循环伏安曲线所表现的规律也基本相似.但是掺杂1%钇离子后,第1周的不可逆容量明显减小,并且在以后的循环中掺杂材料的氧化还原峰面积大于未掺杂材料,表明掺杂材料的活化速率增大和循环可逆性增强.为了进一步证实掺杂对样品中Li+扩散能力的影响,对合成的材料进行了交流阻抗谱测试.图6为所得到材料经电化学循环10周后的交流阻抗谱图.采用图中所示的等效电路对测定数据进行拟合,结果见表3.表3中的数据说明,对于阳离子来说,由于晶格结合电阻很相近,因此掺杂后对结构的改变是相似的,因而表现在电化学反应阻抗上基本一致.但电荷转移电阻和Warburg阻抗存在着差别,特别是Warburg阻抗差别比较大,这就反映出掺杂离子的不同对锂离子的扩散有着一定的影响.掺杂后由于增大了材料的晶胞体积,从而使锂离子的扩散就要容易得多,反映在电化学容量上,其容量要高.另外,由于掺杂后锂离子扩散速度快,Warburg阻抗小,其电荷转移相对容易些,反映在电化学性能上就是其高倍率充放电能力得到了提高[17].2.3材料的X射线光电子能谱分析为进一步证明材料循环性能的提高是由于掺杂离子增加了材料的结构稳定性,对材料进行了XPS表3样品交流阻抗测试数据拟合结果Table3Fitting results of EIS data for the as-prepared samplesSample106CPE(F)W/ΩLi0.99MnO2 4.34134.16Li0.99Mn0.99Mg0.01O2 2.4641.42Li1.01Mn0.99Y0.01O2 1.9780.51Li0.98Mn0.99Zr0.01O2 3.1496.38R ct/Ω65.6267.3154.8661.31R el/Ω3.133.243.103.21图5样品的循环伏安曲线Fig.5CV curves of the as-prepared samplesscan rate:0.1mV·s-1;voltage range:2.0-4.3V;(a)Li0.99MnO2,(b)Li1.01Mn0.99Y0.01O2图6样品经电化学循环10周后的交流阻抗谱图Fig.6Impedance spectra of the as-prepared samplesafter10cyclesR el represents the electrolyle solution resistance;R ct represents the charge-transfer resistance,CPE represents the constant phase element, and W represents the Warburg impedance.1236No.6粟智等:锂离子电池正极材料LiMnO 2的掺杂及其电化学性能分析.图7为掺杂前后o -LiMnO 2材料中Mn 2p 、Mg 2s 、Y 3d 和Zr 3d 的XPS 谱图,表4列出了用ICP -AES 和XPS 方法对材料组成进行分析的结果.从图7可以看出,元素掺杂后,Mn 2p 1/2和Mn 2p 3/2光电子能谱峰的裂分距离发生了变化.Mn 2O 3和MnOOH [18]的Mn 2p 3/2的结合能为641.60eV,Mn 2p 1/2结合能为653.40eV,裂分距离为11.80eV.而本文中未掺杂时裂分距离为12.03eV,但掺杂Mg 、Y 、Zr 后裂分距离分别为11.89eV,11.93eV 和11.90eV,表明掺杂后Mn 的化学形态发生了变化,并且掺杂低价Mg 2+时,Mn 2p 光电子谱峰总体向高能量方向移动,说明Mn 的氧化状态发生了变化,Mn 的平均价态上升,定性地证明了掺杂低价阳离子可以提高Mn 的价态.另外掺杂Zr 4+时Mn 2p 光电子谱峰总体向低能量方向移动,说明了Mn 的氧化状态也发生了变化,Mn 的平均价态降低,定性地证明了掺杂高价阳离子可以降低Mn 的价态.而测定得到材料中Mg 2s ,Y 3d 以及Zr 3d 结合能与文献得到的值基本一致[19-23].表4数据说明用XPS 测定合成材料的表面组成与用ICP -AES 法测定材料的体相组成基本一致,说明掺杂离子进入了材料的晶格,这与材料XRD 的分析结果一致.3结论在层状LiMnO 2电极材料中,掺杂低价离子Mg 2+后,可以提高锰的平均价态,从而能有效地抑制由于Mn 3+的Jahn -Teller 效应而产生的结构畸变;在层状LiMnO 2中掺杂部分Y 3+后,可以起到降低材料中MnO 6八面体的扭曲应力,减小材料的结构畸变,从而增强材料的电化学循环可逆性,在一定程度上改善了材料的电化学性能;掺入高价离子Zr 4+后,电极材料的离子分布形式发生了变化,电极材料在充放电过程中的结构畸变得到有效抑制,从而减小了由结构变化而引起的容量损失,改善了电极材料的a:by ICP -AES method;b:by XPS method表4材料的化学组成和表面组成Table 4Chemical and surface composition of as -prepared materialsChemical composition a Surface composition b Li 0.99MnO 2Li 1.01MnO 2Li 0.99Mn 0.99Mg 0.01O 2LiMn 0.988Mg 0.012O 2Li 1.01Mn 0.99Y 0.01O 2Li 1.01Mn 0.991Y 0.009O 2Li 0.98Mn 0.99Zr 0.01O 2Li 1.01Mn 0.988Zr 0.012O 2图7样品的XPS 谱图Fig.7XPS spectra of the as -prepared samples(a)Li 0.99MnO 2,(b)Li 0.99Mn 0.99Mg .01O 2,(c)Li 1.01Mn 0.99Y 0.01O 2,(d)Li 0.98Mn 0.99Zr 0.01O 21237Acta Phys.-Chim.Sin.,2009Vol.25电化学循环性能.References1Ammundsen,B.;Desilvestro,J.;Groutso,T.;Hassell,D.;Metson, J.B.;Regan,E.;Steiner,R.;Pickering,P.J.J.Electrochem.Soc., 2000,147(11):40782Huang,Z.F.;Meng,X.;Wang,C.Z.;Sun,Y.;Chen,G.J.Power Sources,2006,158(2):13943Sugiyama,J.;Noritake,T.;Hioki,T.;Itoh,T.;Hosomi,T.;Yamauchi,H.Mater.Sci.Eng.B,2001,84(3):2244Xia,Y.;Zhou,Y.;Yoshio,M.J.Electrochem.Soc.,1997,144: 25935Morales,J.;Sanchez,L.;Tirado,J.L.J.Solid State Electrochem.Acta,1999,45:2556Roberson,A.D.;Armstrong,A.R.;Bruce,P.G.Chem.Mater., 2001,12:23807Landa,A.I.;Chang,C.C.;Kumta,P.N.;Vitos,L.;Abrikoso,I.A.Solid State Ionics,2002,149(3-4):20958Park,S.H.;Lee,Y.S.;Sun,mun.,2003,5(2):1249Li,D.C.;Takahisa,M.T.;Hideyuki,N.C.J.Power Sources, 2004,135:26210Jeong,K.H.;Ha,H.W.;Yun,N.J.;Hong,M.Z.;Kim,K.Electrochim.Acta,2005,50(27):534911Shukla,N.N.;Prasad,R.J.Phys.Chem.Solids,2006,67(8):1731 12Park,C.W.;Mangani,I.R.;Ryu,H.W.;Park,C.J.;Lee,J.S.;Song,S.J.;Moon,J.H.;Kim,J.Phys.Chem.Solids,2007,68:112613Lee,J.;Lee,J.M.;Yoon,S.;Kim,S.O.;Sohn,J.S.;Rhee,K.I.;Sohn,H.J.J.Power Sources,2008,183(1):32514Jang,Y-II;Huang,B.Y.;Wang,H.F.;Sadoway,D.R.;Chiang,Y.M.J.Electrochem.Soc.,1999,146(9):321715Huang,Y.Y.;Zhou,H.H.;Chen,J.T.;Gao,D.S.;Su,G.Y.Acta Phys.-Chim.Sin.,2005,21(7):725[黄友元,周恒辉,陈继涛,高德淑,苏光耀.物理化学学报,2005,21(7):725]16Tang,Z.Y.;Zhang,N.;Lu,X.H.;Huang,Q.H.Acta Phys.-Chim.Sin.,2005,21(1):89[唐致远,张娜,卢星河,黄庆华.物理化学学报,2005,21(1):89]17Shi,M.L.AC impedance spectroscopy principles and applications.Beijing:National Defence Industry Press,2001:21[史美伦.交流阻抗谱原理及应用.北京:国防工业出版社,2001:211]18Tan,B.J.;Klabunde,K.J.;Sherwood,P.M.A.J.Am.Chem.Soc., 1991,113:85519Nefedov,V.I.;Firsonm,M.N.;Shaplygin,I.S.J.Electrom.Spectrosc.Relat.Phenom.,1982,26:6520Vasquez,R.P.;Foote,M.C.;Hunt,B.D.J.Appl.Phys.,1989,66: 486721Ingo,G.M.;Parazzo,E.;Bagnrelli,O.;Zaccnetti,N.Surf.Interface Anal.,1990,16:51522Liu,S.H.;Wang,D.H.;Pan,C.H.Analysis of X-rayphotoelectron spectroscopy,Beijing:Science Press,1988:330[刘世宏,王当憨,潘承璜编著.X射线光电子能谱分析.北京:科学出版社,1988:330]23Sinha,S.;Badrynarayanan,S.;Sinha,A.P.B.J.Less-Common Metals,1987,134:2291238。
锂电池的研究进展

锂电池的研究进展摘要:锂离子电池由于比能量高和使用寿命长,已成为便携式电子产品的主要电源。
尖晶石LiMn2O4正极材料在不同混合溶剂的电解质溶液的电化学性能。
用循环伏安法和交流阻抗技术研究了Li/有机电解液/LiMn2O4电池的电化学行为,综述了锂离子电池正极材料LiMn2O4的制备、结构及其电化学性能。
采用溶胶-凝胶法和旋转涂布工艺,在较低的退火温度(450e)下制备了尖晶石型LiMn2O4薄膜。
关键词:正极材料; 电化学性能 ;薄膜1前言作为锂离子电池电解质溶液的主体成分,溶剂的组成和性质影响和决定着LiMn2O4正极材料的宏观电化学性能。
电解质溶液的电导率大小、电解质溶液在电极表面的氧化电位以及电解质溶液对电极材料活性物质的溶解性都在不同程度上直接影响LiMn2O4电极材料的容量、寿命、自放电性能和倍率充放电性能[。
近年来,寻找合适的电解质溶液组分,以进一步改善和提高LiMn2O4正极材料的电化学性能正在引起人们越来越广泛的关注。
系统地研究溶剂组成对LiMn2O4正极材料电化学性能的影响,探讨影响LiMn2O4正极材料电化学性能电解质溶液因素,进一步明确新型电解质溶液体系的优化目标,将为LiMn2O4正极材料在锂离子电池工业中的广泛应用奠定基础。
本文使用恒电流充放电和粉末微电极的循环伏安方法研究了尖晶石LiMn2O4正极材料在不同混合溶剂体系的电解质溶液中的电化学性能。
结合溶剂组分和电解质溶液的理化特性,详细探讨了影响LiMn2O4正极材料电化学性能的溶剂因素及其影响机制。
锂离子电池正极材料的选择是锂离子电池电化学性能的关键。
作为正极材料的嵌锂化合物是锂离子电池中锂的/存库0,它应满足:(1)在所要求的充放电电范围内,具有与电解质溶液的电化学相容性;(2)温和的电极过程动力学;(3)高度的可逆性;(4)全锂化状态下在空气中的稳定性。
目前研究较多的是层状的LiMO2和尖晶石型LiM2O4(M=Co、Ni、Mn、V等过渡金属离子)。
锂离子电池正极材料的研究及其性能优化

锂离子电池正极材料的研究及其性能优化随着人们对环保意识的不断提高,电动汽车、能源存储以及便携式电子设备等需求愈发增长,锂离子电池作为一种高能量密度、轻量化、环保的电池类型备受瞩目。
而锂离子电池的性能,尤其是其正极材料的性能,是影响整个电池性能的关键因素。
本文将从锂离子电池正极材料的基础结构入手,通过对正极材料的组成元素以及内部作用机制的探究,分析其性能特点,并结合当前的研究进展,探讨锂离子电池正极材料的性能优化方向。
一、锂离子电池正极材料的基础结构锂离子电池是一种以锂离子在电解液中的扩散为工作原理的电池。
正极材料是锂离子电池中最重要的组成部分之一,其主要作用是存储锂离子和提供电子传导。
正极材料的基础结构一般由三个部分组成:金属氧酸化物、导电剂和粘结剂。
其中,金属氧酸化物是正极材料的主要成分,占正极材料的大部分重量,其在电池中起到存储锂离子的作用。
导电剂主要是为了提高正极材料的导电性,增加正极材料对锂离子的传导和储存能力,减小电极极化和电池内阻。
而粘结剂则是为了保证正极材料的结构牢固稳定,能够经受反复的充放电循环。
二、锂离子电池正极材料的组成元素及其作用机制1. 金属氧酸化物目前市场上主要使用的锂离子电池正极材料主要有三种金属氧酸化物:三元材料(如LiCoO2、LiMn2O4等)、锰酸锂材料(如LiMnO2)和钴酸锂材料(如LiFePO4)。
三元材料是较早研究和应用的正极材料之一,其磷酸根结构稳定,特别是在高温下稳定性好,同时其储能能力和功率密度优秀。
但是其中的钴含量高,钴资源稀缺,同时钴价格昂贵,因此其成本较高。
锰酸锂材料具有环保、价格低廉和锂离子传输速度快等优点,同时其钠离子掺杂还可提高其稳定性和循环寿命。
但是锰酸锂材料的能量密度较低,且容量随循环次数的增加而逐渐减小。
钴酸锂材料被认为是一种具有高安全性、优异的循环性能以及适合大电流放电的正极材料。
该材料的选择主要基于其晶体结构的稳定性和高的电子导电率。
锂离子电池正极材料研究

锂离子电池正极材料研究吴怡芳; 白利锋; 王鹏飞; 马小波; 李成山【期刊名称】《《电源技术》》【年(卷),期】2019(043)009【总页数】4页(P1547-1550)【关键词】锂离子电池; 正极; 研究现状【作者】吴怡芳; 白利锋; 王鹏飞; 马小波; 李成山【作者单位】西北有色金属研究院陕西西安710016【正文语种】中文【中图分类】TM91220世纪70年代末80年代初,Murphy D W和Armand M等提出用嵌锂化合物代替二次锂电池中金属负极锂的设想,并称之为“摇椅式”电池[1]。
后来Scrosati B等组装出以LiWO2或 Li6Fe2O3为负极,以 TiS2、WO3、NbS2或V2O5作为正极的实验型摇椅式电池[2-3]。
1987年,Auborn J J和Barberio L 报道了MO2(或WO2)/LiPF6-PC/LiCoO2型摇椅式电池[4]。
但直到1991年,日本SONY公司正式向市场推出以石墨等碳材料作为阳极LiCoO2电池[5],才真正实现了锂离子电池的技术革命。
这种钴酸锂电池具有可逆充放电能力,性能好,比能量高,循环性能和安全性能好等优点,直到现在仍然广泛应用于各种便携式电子装置上。
根据锂离子电池正极材料的不同,主要可以分为层状的LiMO2型(M为过渡金属)正极材料,尖晶石型的LiM2O4正极材料,以及橄榄石型LiMPO4正极材料。
目前,传统的锂离子电池一般都采用石墨作为负极,采用钴酸锂 (LiCoO2)、锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)为正极。
大多数的研究都针对这几类材料及其派生化合物。
此外,还有一些电池在原子级别上是两种或两种以上的正极材料的化合物[6]。
最近几年,一些新型的嵌入型正极材料如硅酸盐(Li2MSiO4)、硼酸盐(LiMBO3)和磷酸盐氟化物(LiMPO4F)也引起了科研人员的极大兴趣。
下面分别对传统正极材料和新一代锂嵌入式正极材料予以概述。
锂离子电池材料探析

锂离子电池材料探析摘要:锂离子电池是高效的能量转化和存储设备。
锂离子电池材料对其性能有着直接的影响。
现阶段,锂离子电池的正极材料主要有层状的钴酸锂(LiCoO2)、氧化镍锂(LiNiO2)、锰酸锂(LiMnO2)和磷酸铁锂(LiFePO4)等;负极材料主要有各种碳材料与一些非碳负极材料,如硅和钛酸锂(Li4Ti5O12);电解液主要为非水系电解液;隔膜主要为聚烯烃隔膜。
锂离子电池不同构成部分的材料,有着一定的发展、应用历程,对其进行探究,具有广泛的应用前景。
关键词:锂离子电池正极负极隔膜电解液材料随着经济的飞速发展,能源供需矛盾日益加剧。
一些能源,如太阳能、地热、风能等,在空间分布上不平衡,导致有效利用难度较大。
为了解决此类问题,能源转化和存储设备的研究受到越来越多的关注。
锂离子电池就是能够实现能源高效转化和存储的设备之一,近年来锂离子电池的研究得到广泛开展。
高功率、高容量的正负极材料是锂离子电池发展的关键,探索低成本、高能量密度的锂离子电池材料,成为了锂离子电池推广应用的必由之路。
1 锂离子电池概述锂离子电池由正极、负极、电解液和隔膜等部分组成。
锂离子电池正极能够为电池提供锂源,主要是含锂化合物[1]。
锂离子电池充电的时候,锂离子会脱离正极材料,并受到内部电场的影响进入电解液,最后通过隔膜进入到负极材料当中。
与此同时,电池的电子将脱离被氧化的正极材料,通过外电路进入负极材料,并发生还原反应,使得电能转化为化学能,进而存储于电池当中。
锂离子电池放电的过程和充电的过程正好相反,从负极脱出的锂离子进入到电解液中,通过隔膜进入正极材料,通过外电路做功,电子把存储在电池中的化学能转化为电能。
现阶段,锂离子电池的正极材料大多为含锂的过渡金属化合物,例如,橄榄石结构的磷酸铁锂、尖晶石型的锰酸锂和层状的钴酸锂等。
锂离子电池的负极材料大多为石墨化碳材料。
锂离子电池的电解液大多为碳酸二乙酯、碳酸二甲酯等的聚合物或有机溶液。
锂离子电池三元正极材料掺杂工艺研究进展

2020年第2期广东化工第47卷总第412期·77·锂离子电池三元正极材料掺杂工艺研究进展高琦,张秋俊,桑李超(广东佳纳能源科技有限公司,广东英德513056)Research Progress on Doping Technology of Ternary Cathode Materials forLithium Ion BatteriesGao Qi,Zhang Qiujun,Sang Lichao(Guangdong Jiana Energy Technology Co.,Ltd.,Yingde513056,China)Abstract:NCM ternary cathode material has the advantages of high voltage,high capacity,long cycle life,good safety performance,no memory effect,and small self-discharge.It is widely used in the markets of small lithium battery and power battery.With the increasing demand for energy density,NCM ternary materials tend to be high in nickel and high voltage,but as the Ni content of ternary materials increases,problems such as cation mixing and phase change during charging and discharging are intensified.And high voltage will also aggravate the structural changes of the material.Doping modification is a simple and effective means to improve the electrochemical performance of the material.In this paper,the improvement of electrochemical performance of NCM ternary cathode material by doping process is reviewed in detail from cation doping,anion doping and anion-cation doping.The future application of doping process is prospected.Keywords:lithium ion battery;ternary cathode material;doping process;electrochemical performance锂离子电池自研发成功开始就成为电化学领域的研究热点。
水热法制备正交结构层状LiMnO2正极材料的研究进展

的研究工作都集 中在对该材料进行体相掺杂和表 面包覆 改 性方 面 , 而 关 于 反 应 前 驱体 对 水 热 法 制 备 该材 料及 性 能影 响 的详 细研究 却 没有 引起 人们 足够 的重 视 。
前 的研 究 主 要 集 中于 L i C o O2 、 L i Ni O2 、 L i Mn Oz 、
赵 红远 , 刘兴泉 h , 张
河 南 省 电 力 公 司 驻 马店 供 电公 司 , 河南 驻马店 4 6 3 5 0 0 )
峥 , 吴
明 , 阙 东阳
( 1 . 电子科技大学微电子与固体电子学院 电子薄膜与集成器 件国家重点 实验室 , 四川 成都 6 1 0 0 5 4 ; 2 . 国家 电网
述 了 由 不 同锰 源 制 备 层 状 UMn 0 正极材料 所存 在的优 缺 点, 对今 后 水 热 法 制 备 层 状 L i Mn ( ) z正 极 材
料 的研 究及 发展 前 景 进 行 了展 望 。 关键词 : 锂 离子 电 池 ; 正极材料 ; 层状 L i Mn O2 ; 水 热 法合 成 中图分类号 : TM 9 1 2 文献标识码 : A 文章编 号 : 1 0 0 8 0 5 1 1 ( 2 0 1 3 ) 0 4 — 0 0 6 6 — 0 5
综 述 专 论
S C I E N C E & T E C H N C I L O G Y 化 I N 工 C 科 H 技 E , M 2 0 I C 1 3 A , L 2 1 I ( N 4 D ) U : 6 S 6 T  ̄ R 7 Y 0
水 热 法 制 备 正 交结 构 层 状 L i Mn O2 正 极 材 料 的研 究 进 展 *
L i O H・ H。 O以及 L i NO 3 为 原料 , 采用 固相 法制 备 出层状 L i Mn 0 2 。该 电极 材 料 的首 次 放 电容 量 为
Nb掺杂改性LiNiO2正极材料的制备及电化学性能研究

材料研究与应用 2024,18(2):207‐214Materials Research and ApplicationEmail :clyjyyy@http ://mra.ijournals.cn Nb 掺杂改性LiNiO 2正极材料的制备及电化学性能研究孟祥聪,刘丽英*(广东工业大学材料与能源学院,广东 广州 510006)摘要: 高镍层状氧化物LiNiO 2具有高理论比容量和相对低廉价格,被认为是下一代锂离子动力电池的正极材料之一。
当LiNiO 2正极材料应用于锂离子电池时,其循环稳定性无法满足要求,需经改性后才能得以应用。
采用固相法合成了Nb 掺杂的层状LiNi 1−x Nb x O 2(x =0.005、0.01、0.015)正极材料,利用X 射线衍射、扫描电子显微镜和X 射线能谱等测试手段,分析了Nb 掺杂量(摩尔百分比)对其晶体结构、微观形貌及元素分布的影响,并通过恒电流间歇滴定和交流阻抗测试研究了其电化学性能。
结果表明,随着Nb 元素掺杂量的提高,LiNi 1−x Nb x O 2材料的晶格晶面间距逐渐扩大,一次颗粒尺寸逐渐减小。
在LiNiO 2材料中引入Nb 5+离子,提高了LiNi 1−x Nb x O 2材料的锂离子扩散系数,并通过稳定晶体结构,抑制了Nb 掺杂材料在充放电过程中的相变,有利于其电化学性能的提升。
当Nb 掺杂量为1%时,LiNi 1−x Nb x O 2材料表现出较好的倍率性能,在10 C 大电流密度下的放电比容量高达134.1 mAh∙g −1;随着Nb 掺杂量的增加,LiNi 1−x Nb x O 2材料循环稳定性同步提升,当Nb 掺杂量为1.5%时,LiNi 1−x Nb x O 2材料经150次循环后的容量保持率为73.3%,远高于未掺杂LiNiO 2样品的36.2%。
表明,Nb 掺杂可改善LiNiO 2正极材料的晶体结构和电化学性能,为其在下一代锂离子动力电池的应用提供了理论依据。
纯电动车用锂离子电池发展现状与研究进展

纯电动车用锂离子电池发展现状与研究进展一、概述随着能源和环境问题的日益突出,纯电动车作为一种清洁、高效的交通工具受到了广泛关注。
锂离子电池作为纯电动车的核心能源储存装置,在电动汽车的发展中起着至关重要的作用。
本文将探讨纯电动车用锂离子电池的发展现状与研究进展。
锂离子电池在电动汽车中的应用经历了三代技术的发展。
第一代是以钴酸锂为正极材料的电池,第二代则是以锰酸锂和磷酸铁锂为正极材料的电池,而第三代则是以三元材料为正极的电池。
随着正负极材料向着更高克容量的方向发展和安全性技术的日渐成熟,更高能量密度的电芯技术正在从实验室走向产业化。
从产学研结合的角度来看,动力电池行业在正负极材料、电池设计和生产工艺等方面取得了许多最新动态和科学研究的前沿成果。
这些成果为锂离子电池在电动汽车中的应用提供了技术支持,同时也为解决电池安全性、寿命和成本等问题提供了新的思路和方法。
市场需求与政策导向也是推动锂离子电池在电动汽车中应用的重要因素。
随着电动汽车市场的不断扩大,对锂离子电池的需求也在不断增加。
同时,政府对电动汽车的补贴和支持政策也为锂离子电池的发展提供了有利条件。
纯电动车用锂离子电池的发展现状与研究进展是一个多方面、多层次的问题。
通过不断的技术创新和产业升级,锂离子电池有望在未来的电动汽车市场中发挥更加重要的作用。
1. 纯电动车与锂离子电池的关联锂离子电池作为电动汽车最重要的动力源,与纯电动车的发展密切相关。
随着科技的进步和创新,锂离子电池技术经历了三代发展:第一代以钴酸锂正极材料为主,第二代包括锰酸锂和磷酸铁锂,而第三代则是三元技术。
这些技术的发展使得锂离子电池在能量密度、安全性和成本等方面不断改进,从而推动了纯电动车的市场化和普及化。
锂离子电池的高能量密度使其成为纯电动车的理想选择。
相比于传统的铅酸电池和镍氢电池,锂离子电池能够存储更多的电能,从而延长了纯电动车的行驶里程。
这使得纯电动车能够满足日常出行需求,减少了对传统燃油车的依赖。
富锂锰基层状锂离子电池正极材料的研究现状

富锂锰基层状锂离子电池正极材料的研究现状张嘉;朱泽华;王海峰【摘要】富锂层状正极材料(LLOs)x Li2MnO3·(1-x)LiMO2(M=Mn,Ni,Co,Fe,Cr,etc)以其超高的充放电容量及较低的成本受到了越来越多的关注.然而,该类正极材料的微观结构和反应机理尚不清楚.与此同时,也存在着一些问题,例如较低的首次库仑效率、较差的倍率性能以及工作电压衰减问题,这些都需要通过研究去克服.着眼于富锂层状正极材料研究现状,讨论了其微观结构、反应机理及电化学性能.【期刊名称】《电源技术》【年(卷),期】2015(039)006【总页数】4页(P1323-1326)【关键词】锂离子电池;富锂层状锰基正极材料;微观结构;反应机理【作者】张嘉;朱泽华;王海峰【作者单位】西南石油大学材料科学与工程学院,四川成都610500;西南石油大学材料科学与工程学院,四川成都610500;中国石油工程设计有限责任公司北京分公司,北京100085【正文语种】中文【中图分类】TM912.9如今,化石能源的消耗、全球气候的变暖以及环境污染这些问题逐渐使得传统化石燃料不能满足全球经济迅速发展的要求,从而对一些新能源资源,例如潮汐能、风能、太阳能、地热能等进行了广泛且深入地研究。
然而,这些能源在时间和空间上并不是稳定存在的,并且要通过适当转换和储存才能被应用[1]。
因此,可充电锂离子电池(LiBs)因其高能量密度、大充放电容量、长循环寿命和良好的安全性已经成为了极具吸引力的能源资源。
锂离子电池的电化学性能很大程度上取决于电解液及反应电极的特性和微观结构,正极材料的性质尤为重要,例如橄榄石结构的LiFePO4,尖晶石结构的LiMn2O4,LiCoO2,LiNi0.8-Co0.15Al0.05O2,LiNi0.33Co0.33Mn0.33O2等材料都已经在锂离子电池中实现了商业化应用[1-2]。
然而,上面提到的正极材料几乎都达到了它们可充电比容量的极限(120~200 mAh/g)[2-6]并且由于Co离子存在毒性、价格昂贵,使它们已经无法满足锂离子电池在能量密度、循环寿命及安全问题方面日益增长的性能及环境要求,所以需要对锂离子电池正极材料进行更多更深入的研究。
锂电池的几种主要正极材料对比分析

锂电池的几种主要正极材料对比分析锂电池的性能主要取决于所用电池内部材料的结构和性能。
介绍一下锂电池主要正极钴酸锂,镍酸锂,锰酸锂,磷酸铁锂和钒的氧化物等。
锂电池的性能主要取决于所用电池内部材料的结构和性能。
这些电池内部材料包括正极材料、负极材料、电解液、隔膜和导电材料等。
其中正、负极材料的选择和质量直接决定锂电池的性能与价格。
因此廉价、高性能的正、负极材料的研究一直是锂电池行业发展的重点。
负极材料一般选用碳材料,目前的发展比较成熟。
而正极材料的开发已经成为制约锂电池性能进一步提高、价格进一步降低的重要因素。
在目前的商业化生产的锂电池中,正极材料的成本大约占整个电池成本的40%左右,正极材料价格的降低直接决定着锂电池价格的降低。
对锂动力电池尤其如此。
比如一块手机用的小型锂电池大约只需要5克左右的正极材料,而驱动一辆电动汽车用的锂动力电池可能需要高达500千克的正极材料。
衡量锂电池正极材料的好坏,大致可以从以下几个方面进行评估:(1)正极材料应有较高的氧化还原电位,从而使电池有较高的输出电压;(2)锂离子能够在正极材料中大量的可逆地嵌入和脱嵌,以使电池有高的容量;(3)在锂离子嵌入/脱嵌过程中,正极材料的结构应尽可能不发生变化或小发生变化,以保证电池良好的循环性能;(4)正极的氧化还原电位在锂离子的嵌入/脱嵌过程中变化应尽可能小,使电池的电压不会发生显著变化,以保证电池平稳地充电和放电;(5)正极材料应有较高的电导率,能使电池大电流地充电和放电;(6)正极不与电解质等发生化学反应;(7)锂离子在电极材料中应有较大的扩散系数,便于电池快速充电和放电;(8)价格便宜,对环境无污染。
锂电池正极材料一般都是锂的氧化物。
研究得比较多的有钴酸锂,镍酸锂,锰酸锂,磷酸铁锂和钒的氧化物等。
导电聚合物正极材料也引起了人们的极大兴趣。
1、钴酸锂在目前商业化的锂电池中基本上选用层状结构的钴酸锂作为正极材料。
其理论容量为274mAh/g,实际容量为140mAh/g左右,也有报道实际容量已达 155mAh/g。
层状富锂锰基正极材料的合成与结构调控方法

层状富锂锰基正极材料的合成与结构调控方法新一代便携式电子产品和电动汽车的发展迫切需要提高电池的能量密度。
当前锂离子电池的能量密度受制于正极材料的比容量。
因此,开发高容量正极材料己成为锂离子电池发展的技术关键。
在目前研究的正极材料中,富锂锰基xLi2MnO3-(1-x)LiMO2(M=Co、Ni、Mn)具有高达250~300mAh.g-1的比容量、较好安全性和低廉的成本,被视为最具发展前景的正极体系。
然而,富锂锰基正极存在若干应用问题,如首周效率偏低、容量衰减较快、倍率性能不佳和循环过程中电压下降等。
针对这些问题,本论文工作从材料合成化学、表面组成和体相结构调控等方面探讨了改善这类化合物电化学性能的途径,期望以此推进富锂锰基材料的实用化进程。
本论文的主要研究内容和结果如下:1、合成方法的比较研究。
本工作采用聚合热解法、机械化学法、共沉淀法三种方法制备了富锂锰基材料0.3Li2MnO3-0.5LiNi0.33Mn0.33CO0.33O2(Li[Li0.2Mn0.54Ni0.13CO0.13]O2),并比较研究了不同反应途径生成产物的结构、形貌以及电化学性能。
实验结果表明,聚合热解法在合成反应中能够始终保持金属离子的均匀分布,所制备的材料具有颗粒尺寸小(100~150nm),结晶度高等特点,可实现较高的比容量(291mAh·g-1),较好的倍率性能(210mAh·g-1,1C),但也存在循环稳定性较差(100周80%的容量保持率)的问题。
机械化学法制备的材料虽比容量较低(260mAh·g-1),但循环稳定性较高(500周83%的容量保持率),且制备过程中绿色无污染,适合大规模应用。
传统的共沉淀法虽可制备出较高振实密度的球形材料,但步骤复杂,且控制条件苛刻,不利于材料改性的研究。
据此,我们选用过程可控、重现性好、适合掺杂改性的聚合热解法进行了后续研究。
2、材料表面的表面包覆改性。
linio2正极材料晶格结构

linio2正极材料晶格结构引言:作为一种重要的锂离子电池正极材料,linio2具有很高的能量密度和较长的循环寿命,因此备受研究者的关注。
linio2的晶格结构对其电化学性能起着重要的影响。
本文将重点介绍linio2的晶格结构及其对材料性能的影响。
一、linio2的晶格结构linio2的晶格结构属于正交晶系,空间群为Pnma。
其晶格参数为a = 5.03 Å,b = 8.96 Å,c = 2.95 Å。
晶胞中包含两个Li原子、一个In原子和两个O原子。
二、晶格结构的影响linio2的晶格结构对其电化学性能具有重要影响。
首先,晶格结构影响着锂离子在linio2中的扩散性能。
由于正交晶系的特点,linio2晶体中锂离子在a、b和c三个方向的扩散速率是不同的,其中b方向的扩散速率最快。
其次,晶格结构还会影响linio2的电子传导性能。
由于晶格结构中存在不同的原子间距和键长,电子在晶格中的迁移受到限制,从而影响了材料的导电性能。
三、晶格缺陷及其影响linio2晶格中可能存在一些缺陷,如杂质原子、晶格畸变等。
这些缺陷对材料的电化学性能有着重要的影响。
首先,杂质原子的存在会导致晶格结构的畸变,从而影响锂离子在晶体中的扩散速率。
其次,晶格缺陷还会影响linio2的电子传导性能,限制了电子在材料中的迁移。
四、晶格结构优化策略为了改善linio2的电化学性能,研究者们提出了一些晶格结构优化策略。
一种常见的策略是通过合适的掺杂来改变晶格结构,以提高锂离子的扩散速率和电子的传导性能。
例如,通过掺入一些具有较大离子半径的杂质原子,可以改变晶格参数,缩短锂离子的扩散路径,从而提高材料的电化学性能。
另外,通过调控晶格畸变也可以改善linio2的性能。
通过合理设计合成条件,控制晶格畸变的程度,可以优化材料的电子传导性能。
结论:linio2的晶格结构对其电化学性能具有重要影响。
晶格参数和晶格缺陷会影响锂离子的扩散速率和电子的传导性能。
锂离子电池正极材料富锂锰基固溶体的研究进展

富 锂 锰 基 固 溶 体 正 极 材 料 可 用 通 式 xLi[Li1/3Mn2/3]O2·(1–x)LiMO2 来表达, 其中 M 为过渡金属,
0≤x≤1, 结构类似于 LiCoO2, 具有很高的放电比容 量, 是目前所用正极材料实际容量的 2 倍左右; 由于 材料中使用了大量的 Mn 元素, 与 LiCoO2 和三元材 料 Li[Ni1/3Mn1/3Co1/3]O2 相比, 不仅价格低, 而且安全 性 好 、 对 环 境 友 好 . 因 此 , xLi[Li1/3Mn2/3]O2·(1–x)LiMO2 材料被众多学者视为下一代锂离子电池正极 材料的理想之选.
另一方面, 有关研究的结果表明, Li2MnO3 可与 LiMnO2, LiCrO2 等层状材料形成稳定的富锂锰基固 溶体, 从而改善这类活性层状材料在循环过程中的
英文引用格式: Du K, Hu G R. Review of manganese-based solid solution xLi[Li1/3Mn2/3]O2·(1–x)LiMO2 (in Chinese). Chin Sci Bull (Chin Ver), 2012, 57:
层状结构正极材料的发展历程之暴脾气镍酸锂(LNO)
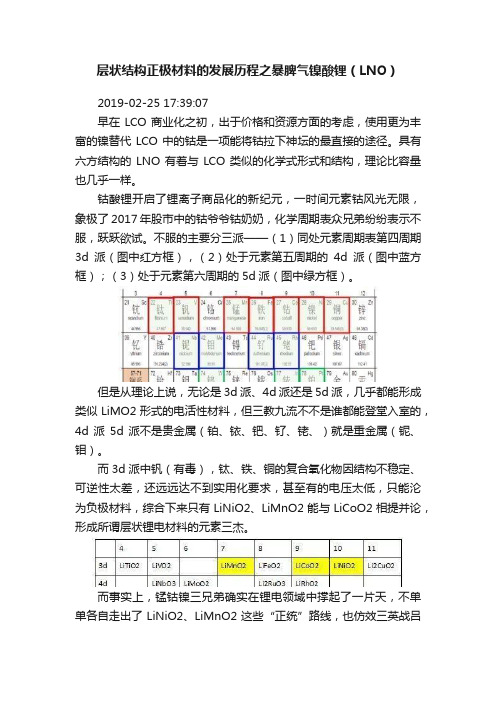
层状结构正极材料的发展历程之暴脾气镍酸锂(LNO)2019-02-25 17:39:07早在LCO商业化之初,出于价格和资源方面的考虑,使用更为丰富的镍替代LCO中的钴是一项能将钴拉下神坛的最直接的途径。
具有六方结构的LNO有着与LCO类似的化学式形式和结构,理论比容量也几乎一样。
钴酸锂开启了锂离子商品化的新纪元,一时间元素钴风光无限,象极了2017年股市中的钴爷爷钴奶奶,化学周期表众兄弟纷纷表示不服,跃跃欲试。
不服的主要分三派——(1)同处元素周期表第四周期3d派(图中红方框),(2)处于元素第五周期的4d派(图中蓝方框);(3)处于元素第六周期的5d派(图中绿方框)。
但是从理论上说,无论是3d派、4d派还是5d派,几乎都能形成类似LiMO2形式的电活性材料,但三教九流不不是谁都能登堂入室的,4d派5d派不是贵金属(铂、铱、钯、钌、铑、)就是重金属(铌、钼)。
而3d派中钒(有毒),钛、铁、铜的复合氧化物因结构不稳定、可逆性太差,还远远达不到实用化要求,甚至有的电压太低,只能沦为负极材料,综合下来只有LiNiO2、LiMnO2能与LiCoO2相提并论,形成所谓层状锂电材料的元素三杰。
而事实上,锰钴镍三兄弟确实在锂电领域中撑起了一片天,不单单各自走出了LiNiO2、LiMnO2这些“正统”路线,也仿效三英战吕布,合力打出了LiNixCoyMnyO2 (其中x+y+z=1)多种套路,根据x:y:z的比例分别有111型、523型、811型等,在锂电领域大有登峰造极之势,此情况暂且不表,先聊聊层状镍酸锂LiNiO2(可简称LNO)。
其实,早在LCO商业化之初,出于价格和资源方面的考虑,使用更为丰富的镍替代LCO中的钴是一项能将钴拉下神坛的最直接的途径。
具有六方结构(R`3m)的LNO有着与LCO类似的化学式形式和结构,理论比容量也几乎一样(275mAh/g)。
“类似”、“几乎”这些字眼也意味着两者还是有所不同,材料科学中常常讲“结构决定性质”,而又是谁在决定着结构呢?理解这个问题要进一步深入到原子层面上,特别是原子的最外围的活跃电子和活跃轨道。
锂离子电池层状正极

锂离子电池层状正极
锂离子电池的层状正极是指电池中的正极材料具有层状结构的特性。
在锂离子电池中,正极通常由锂离子化合物构成,其中包含锂离子的嵌入和释放。
这些层状正极材料对于电池的性能和工作原理至关重要。
层状正极材料的典型例子是锂钴氧化物(LiCoO2)、锂镍锰氧化物(LiNiMnCoO2,常简称为NMC)、锂铁磷酸盐(LiFePO4)等。
这些材料在充放电过程中,锂离子在正极材料的晶格结构中嵌入和释放,从而实现电池的充电和放电过程。
层状正极材料具有稳定的晶体结构,可以容纳和释放锂离子,同时保持电池的稳定性和长周期性能。
不同的正极材料具有不同的特性,比如锂钴氧化物具有高能量密度但不够稳定,而锂铁磷酸盐则相对安全、稳定但能量密度较低。
在锂离子电池的设计和制造中,正极材料的选择和优化对电池性能和安全性至关重要。
层状正极材料的研究和开发是提高锂离子电池能量密度、循环寿命和安全性的重要方向之一。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第33卷第9期硅酸盐学报Vol.33,No.9 2005年9月J OURNAL OF T H E CHIN ESE CERAMIC SOCIET Y September,2005综合评述 锂离子电池用层状LiMnO2基正极材料的研究进展刘静静,仇卫华,赵海雷,李 涛(北京科技大学材料科学与工程学院无机非金属材料系,北京 100083)摘 要:层状LiMnO2材料因其结构不稳定、循环性能差,因而需对其进行掺杂改性。
层状锰系衍生物具有比容量高、循环性能稳定等优点,已成为锂离子电池新的发展方向。
介绍了目前对LiMnO2的掺杂改性研究,对多元层状锰基固溶体正极材料作了重点阐述。
总结了近年来关于多元层状锰基正极材料的研究发展,介绍了其晶体结构、电化学性能、合成与制备技术,以及进一步的改性研究。
如果多元层状固溶体材料的高倍率放电性能得到进一步的提高,则其必将成为新的一代锂离子电池正极的首选材料。
关键词:锂离子电池;正极材料;层状锰酸锂;多元掺杂锰基固溶体中图分类号:TM912.9 文献标识码:A 文章编号:04545648(2005)09112706RESEARCH PR OGRESS ON LAYERE D LiMnO22BASE D CATH ODE MATERIALSFOR L ITHIUM2ION BATTERIESL IU J ing j ing,Q IU Wei hua,Z HA O Hailei,L I Tao(Department of Inorganic Nonmetal Materials,School of Material Science and Engineering,University of Science and Technology Beijing,Beijing 100083,China)Abstract:Research of the effects of doping modification on layered LiMnO2material has been carried out because of its unstable structure and poor retention yered LiMnO2has a higher retention capacity and stable cycle performance,and it has become a promising material in the recent development of the next2generation positive electrode materials for lithium2ion batter2 ies.Research of doping modification of layered LiMnO22based cathode materials,especially multi2element doping manganese base solid solution,is reviewed.The progress in recent years in research of multi2doped layered manganese2based positive electrode materials,such as its crystal structure,synthesis methods,and electrochemical properties,as well as the research of f urther modifications,are summarized.The exploration of simple synthesis methods and improvement of these materials will accelerate its application for lithium2ion batteries in the near f uture.If the discharge capability of multi2element doped layered solid solution materials is f urther enhanced,LiMnO2will be the first choice for a positive electrode material in the development of lithium ion batteries.K ey w ords:lithium2ion battery;cathode material;layered lithium manganate;multi2doped manganese based solid solutions 锂离子电池因其具有质量轻,工作电压高,安全稳定,循环性能好,工作温度范围宽等特点,在移动收稿日期:20041112。
修改稿收到日期:20050518。
第一作者:刘静静(1982~),女,硕士研究生。
通讯作者:仇卫华(1950~),女,副教授。
电话、笔记本电脑、摄像机等微电子产品领域取得了广泛的应用,这是正在积极开发的一种大容量电池,R eceived d ate:20041112.Approved d ate:20050518.First author:L IU Jingjing(1982—),female,graduate student for master degree.E m ail:qingkite@Correspondent author:QIU Weihua(1950—),female,associate pro2fessor.E m ail:qiuwh@也将成为电动汽车的候选电源。
嵌锂化合物正极材料作为二次锂离子电池的重要组成部分,其性能和成本对电池的进一步商业化起着关键性的作用。
目前已商业化的正极材料LiCoO2仍然存在耐过充能力差,高倍率性能不佳,钴的价格高且污染环境等问题;而LiNiO2制备条件苛刻,热稳定性差,使其商业化进程受到阻碍。
LiMn2O4尖晶石的高温循环性差,且高温容量衰减很快,但由于锰价格低廉、绿色无污染等优点,许多研究仍在进行对其掺杂改性及高温性能的研究[1,2]。
层状LiMnO2具有无毒、高容量、成本低等优点,被认为是最具有发展潜力的正极材料。
1996年Bruce等用离子交换法制备出单斜相LiMnO2以来,层状锰系正极材料已引起人们广泛关注[3]。
层状LiMnO2中的氧离子为立方密堆积排列,锰离子位于第一和第二氧层的八面体位,在第一和第三氧层中间,Li+也占据八面体位。
Li+和Mn3+可以彼此占据对方的位置。
单斜结构LiMnO2具有与LiMnO2相同的阳离子排列方式(αNaFeO2结构)。
层状LiMnO2作为锂离子电池正极材料,理论容量高达285(mA・h)/g,接近LiMn2O4尖晶石理论容量的2倍,但其循环性能很差。
除了电解液分解外,其中主要原因就是在循环过程中Mn3+向内层(锂层)迁移,产生J ahn Teller畸变效应,结构改变为一种相对稳定的类似尖晶石的结构,从而带来可逆容量的迅速衰减[4]。
1 LiMnO2掺杂的改性研究为了制备稳定层状结构的LiMnO2,使其在充放电循环中不向尖晶石结构转变,可以在Mn—O层上引入其它过渡金属,如钴、铝等,与锰形成复合金属氧化物,一种金属用于稳定层状结构,另一种则参与氧化还原反应。
目前有很多关于层状LiMnO2掺杂改性的研究,在一定程度上改善了其结构稳定性。
为了提高其可逆容量,可以在制备过程中优化锂锰比,增加可逆锂离子交换量;还可以向锂层引入其它较大体积的碱金属离子,如Na+,K+等,一方面作为支撑柱以稳定层板,减小塌陷,另一方面能够使更多的Li+参与嵌入/脱嵌过程,从而提高材料的可逆容量。
锂引入LiMnO2后取代部分Mn,形成(Li)3a(Li x Mn1-x)3b O2,提高了锰的平均氧化态,有利于保持晶体结构的稳定性。
J ang等[5]通过掺杂A1来稳定LiMnO2层状结构,其最佳工艺条件是:温度为950℃,氧分压为10-8M Pa,A1的最大掺杂摩尔分数为5%~7%。
由于Al3+离子比Mn3+小,为非J ahn Teller离子,用AlO6八面体取代MnO6八面体,不产生畸变,有利于稳定层状LiMnO2结构;并且可以提高锂的插入电势和能量密度,提高电导率,优化材料性能。
Grincourt等[6~8]最先指出掺杂Cr3+的LiMnO2电化学性能明显提高,且降低容量衰减率。
Cr3+的离子半径与Mn3+的极为相近,掺杂Cr3+使Mn—O 键长缩短,Mn3+稳定在八面体位置,从而抑制了Mn3+向内层Li+层扩散,Cr3+在锂离子脱嵌过程中一直位于(Mn,Cr)O2层,从而抑制层状结构向尖晶石相的畸变。
Co3+掺入后占据Mn3+的八面体位置,能稳定层状结构,改善材料性能,Co的含量越高,则在循环中衰变为尖晶石相的速度越慢,但容量也随之下降[9,10]。
Armst rong等[9]利用离子交换法制备了Li(Mn1-y Co y)O2,在LiMnO2中,当Mn3+占据50%的过渡金属位置时,就会发生J ahn Teller效应,而在Li(Mn1-y Co y)O2中,当Mn3+占据70%的金属位置时仍然没有发生J ahn Teller效应。
说明Co3+的掺入在离子交换合成中起到稳定结构的作用。
Ni在LiMn1-x Ni x O2中以二价态存在,可以提高Mn的平均价态,起到稳定结构的作用[11~14]。
其中,LiNi0.5Mn0.5O2被认为是最有可能替代LiCoO2应用于商业生产的一种优异材料[15]。
它的工作电压、容量、循环性能、安全性和材料的成本经济性与LiCoO2相比有一定的优势,弥补了LiNiO2和LiMnO2的不足,有着很好的发展前景。
缺点是合成方法多为液相合成,不利于商业生产,传统的固相合成不易得到单一的纯相组成。
其次,它的低电导率使其比容量下降。
Kang等[16]在Li(Ni0.5Mn0.5)O2中引入了Mg,Al,Co,Ni,Ti等离子,测试结果表明:除了Mg外,其它离子的掺入可增加10%~30%的放电容量,并改善了材料的循环性能。
Li等[17]用简单的固相合成法制备了LiNi0.5Mn0.5-x Ti x O2,但发现:随着Ti的掺入,阳离子混排严重,且初始充放电容量呈下降趋势。
钴的掺杂可以提高其电导率并且提高了材料的热稳定性。
研究发现:钴的掺入量越大,材料的层状结构越好,稳定了结构,不可逆容量有所降低,材料的电子导电性也得到提高,循环性能稳定[18,19]。
