2018学年高中化学学业水平测试检测:第三章专题七 几种重要的金属化合物 学业水平过关 含答案
2018届高三化学学业水平考试试卷

揭阳市2018—2018学年度高中三年级学业水平考试理科综合化学试卷本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
满分300分。
考试时间150分钟。
注意事项:1.本次考试选择题用答题卡作答,非选择题用答题卷作答。
答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和考生号、试室号、座位号填写在答题卷上。
用黑色字迹的钢笔或签字笔在答题卡上填写自己的姓名和考生号,用2B型铅笔把答题卡上考生号、科目对应的信息点涂黑。
2.选择题每小题选出答案后,用2B型铅笔把答题卡上对应题目选项的答案信息点涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。
不按以上要求作答的答案无效。
4.考生必须保持答题卡整洁,考试结束后,将答题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Al 27Si 28 S 32 Cl 35.5 Ca 40 Fe 56 Cu 64第Ⅰ卷7.化学与社会、生产、生活密切相关,下列说法正确的是A.二氧化硫可广泛用于食品的漂白B.从海水提取物质都必须通过化学反应才能实现C.葡萄糖可用于补钙药物的合成D.“地沟油”禁止食用,也不能用来制肥皂8.设N A为阿伏伽德罗常数的值,下列说法正确的是A.14g乙烯和丙烯的混合物中总原子数为3N A个B.2mol/L的硫酸溶液中含有的H+离子数为4N AC.1mol 氯气与足量的铁反应后转移的电子数为3N AD.密闭容器中1molN2与3molH2在铂催化下充分反应,产物的分子数为2N A9.分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,由这些酸和醇重新组合可形成的酯共有A.6种 B.9种C.12种 D.16种11.以葡萄糖为燃料的微生物燃料电池结构示意图如右,关于该电池的叙述不正确的是A.微生物促进了反应中电子的转移B.连接a的电极为负极C.放电过程中,质子(H+)从负极区向正极区迁移D.电池的负极反应为:C6H12O6+6H2O-24e-=6CO2+24H+12.短周期主族元素X、Y、Z、W的原子序数依次增大。
2018-2019年化学高中学业水平测试课件:第三章专题七考点2铝的化合物

解析:Al2O3 虽然难溶于水,但是 2Al(OH)3==△===Al2O3 +3H2O,Al2O3 和 Al(OH)3 中 Al 的化合价相同,所以 Al2O3 是 Al(OH)3 对应的氧化物;金属氧化物与碱性氧化物是两个 不同的概念,二者没有必然的联系;Al2O3 是两性氧化物, Al2O3 与强酸、强碱反应,与弱酸、弱碱不反应。
用氨水与 AlCl3 溶液反应制 Al(OH)3。 4.用硫酸铝钾净水是因为它产生带电荷的 Al3+,沉
淀悬浮水中泥沙。(×) [分析] 原因是在水中生成 Al(OH)3 胶体,该胶体可
以和悬浮在水中的泥沙形成不溶物沉降下来。
►单项选择题Ⅰ 1.下列说法正确的是( ) A.Al2O3 难溶于水,不跟水反应,所以它不是 Al(OH)3 对应的氧化物 B.因为 Al2O3 是金属氧化物,所以它是碱性氧化物 C.Al2O3 能跟所有的酸碱溶液反应 D.Al2O3 能跟强的酸碱溶液反应
铝和氧化铝均能溶于酸和强碱。
答案:D
5.(2015 年 6 月·广东学考)既能与酸又能与碱反应是
两性化合物的特征。下列物质属于两性化合物的是( )
A.Al
B.Na2CO3
C.Al(OH)3
D.(NH4)2SO4
解析:Al 是单质,A 错误;Na2CO3 不是两性化合物, B 错误;Al(OH)3 既能与酸反应又能与碱反应,均生成盐
第三章 金属及其化合物
专题七 几种重要的金属化合物 考点 铝的化合物
一、氧化铝 1.物理性质:难溶的白色固体,熔点很高。 2.化学性质。 Al2O3 是两性氧化物,与强酸或强碱溶液都能反应生 成盐和水。
(1)与强酸的反应:Al2O3+6H+===2Al3++3H2O。 (2)与强碱的反应:Al2O3+2OH-===2AlO- 2 +H2O。 3.用途。 (1)冶炼金属铝的原料; (2)良好的耐火材料。
最新高中学业水平测试·化学 第三章第2节几种重要的金属化合物用途广泛的金属材料

第三章金属及其化合物第2节几种重要的金属化合物用途广泛的金属材料一、单项选择题Ⅰ(每小题1分。
在每小题列出的四个选项中,只有一项最符合题意)1.下列物质的俗名与其化学式不相对应的是()A.小苏打——Na2CO3·10 H2OB.生石膏——CaSO4·2H2OC.苛性钠——NaOHD.胆矾——CuSO4·5H2O答案:A2.小明同学用洁净的铂丝蘸取某无色溶液,在无色火焰上灼烧,火焰呈黄色,通过该实验现象,下列四位同学对该溶液中存在的金属离子的判断正确的是()答案:D3.为了避免青铜器生成铜绿,下列说法中不正确的是()A.将青铜器密封在玻璃容器中B.将青铜器保存在干燥的环境中C.将青铜器保存在潮湿的空气中D.在青铜器的表面覆盖一层防渗的高分子膜答案:C4.不锈钢通常不与酸、碱、盐反应,是因为加入了() A.Ni和Cr B.Ni和AuC.Cr和Au D.Cr和Pt答案:A5.下列说法正确的是()A.金属氧化物只能与酸反应生成盐B.金属氧化物都能与水反应生成碱C.氧化铝既能与盐酸反应又能与氨水反应D.氧化铝是冶炼金属铝的原料答案:D6.下列氧化物中,既能溶于强酸,又能溶于强碱的是() A.Fe2O3B.Ag2OC.CuO D.Al2O3答案:D7.明矾可以净水是因为()A.明矾在水中能电离出SO2-4B.明矾中含有多种阳离子C.明矾溶于水后可以生成Al(OH)3胶体D.明矾可以与碱反应生成Al(OH)3沉淀答案:C8.有关铝及其化合物的说法错误的是()A.铁易生锈,而铝在空气中较稳定,所以铁比铝活泼B.铝能在空气中稳定存在是因为其表面覆盖着一层保护膜C.氧化铝是一种难熔物质,是一种较好的耐火材料D.氢氧化铝能中和胃酸,可用于制胃药答案:A9.下列氧化物的颜色相同的一组是()①FeO②Fe2O3③Fe3O4④CuOA.①②③B.①②④C.②③④D.①③④答案:D10.联合国卫生组织经过考察和研究,认为我国使用的铁锅是有益于人体健康的理想炊具,并向全世界推广,其主要原因是() A.价格便宜,不易生锈B.铁锅只含有铁元素C.烹调的食物中留有人体需要的铁元素D.传热慢,保温性能好答案:C11.下列铁的单质或化合物中,铁元素一般只表现氧化性的是()A.Fe B.FeCl2C.Fe3O4D.FeCl3答案:D12.下列熔合物属于合金的是()①Al与Cu②Fe与C③K与Na④Al与SiA.①②③④B.①③C.②④D.①④答案:A13.在某些食品包装盒内常有一小包灰黑色粉末;将该粉末溶于盐酸,取上层清液,滴加几滴氯水后,再滴加KSCN溶液,出现红色。
2018年化学学业水平测试试题(含答案)

2018年化学学业水平测试试题(含答案)化学试卷可能用到的相对原子质量:H 1.C 12.O 16.Na 23.Al 27.Cl 35.5一、单项选择题1.下列关于O的叙述正确的是:A。
质量数为8B。
质子数为8C。
中子数为16D。
电子数为162.对元素周期表和元素周期律的发现有突出贡献的科学家是:A。
XXXB。
XXXC。
门捷列夫D。
XXX3.下列物质属于化合物的是:A。
XXXB。
O2C。
Br2D。
Ar4.下列物质中氧元素的化合价正确的是:A。
H2O中氧元素的化合价为-1B。
O2中氧元素的化合价为-2C。
NaOH中氧元素的化合价为-1D。
Na2O中氧元素的化合价为-25.下列物质属于电解质的是:A。
CuB。
N2C。
KNO3D。
C2H5OH6.S是元素周期表中第16号元素,下列正确表示S的原子结构示意图的是:7.关于CuSO4溶液和Fe(OH)3胶体描述正确的是:A。
两者都能产生XXX现象B。
两者都不能产生XXX现象C。
CuSO4溶液能产生丁达尔现象,Fe(OH)3胶体不能产生丁达尔现象D。
CuSO4溶液不能产生丁达尔现象,Fe(OH)3胶体能产生丁达尔现象8.观察右图,量筒中液体的体积读数是:9.下列物质中化学键属于离子键的是:A。
H2B。
N2C。
NaClD。
O210.分类是研究和研究化学的一种重要方法,下列分类合理的是:A。
K2CO3和K2O都属于盐B。
KOH和Na2CO3都属于碱C。
H2SO4和HNO3都属于酸D。
Na2O和Na2SiO3都属于氧化物11.下列试剂能够用来鉴别KNO3溶液和KCl溶液的是:A。
AgNO3溶液B。
稀盐酸C。
BaCl2溶液D。
NaOH溶液12.下列物质中酸性氧化物的是:A。
CO2B。
SO2C。
H2OD。
Na2O13.下列化学式中,反映了分子中含有双键的是:A。
H2OB。
O2XXXD。
CH2=CH214.下列物质中,能够使酚酞指示剂变色的是:A。
NaOH溶液B。
HCl溶液C。
2018年江苏省普通高中学业水平测试(必修科目)化学试题及答案

2018年江苏省普通高中学业水平测试(必修科目)试卷化学本卷可能用到的相对原子质量:H 1 C 12N 14O 16Na 23Mg 24Al 27S 32Cl 35.5Ca 40Fe 56Ba 137一、单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分)。
1。
水(H2O)是生命之源。
下列物质的化学式可用“H2O”表示的是()A。
水晶B。
可燃冰 C. 干冰D。
冰2。
下列过程包含化学变化的是()A。
碘的升华B。
粮食酿酒 C. 氧气液化 D. 积雪融化3。
60,27Co在农业上常用于辐射育种。
该原子的质子数是()A。
27 B. 33 C. 60 D. 874. 炼铁过程中存在反应:CaO+SiO2错误!CaSiO3.该反应属于()A. 化合反应B. 分解反应C。
置换反应D。
复分解反应5。
下列化学用语表示正确的是()A。
苯的结构简式:C6H6B。
NaCl的电子式:Na+[∶Cl,∶]-C。
Mg2+的结构示意图:D。
氯化钙的电离方程式:CaCl2===Ca2++Cl错误!排空气集气法6. 下列气体可用右图所示方法收集的是()A。
H2 B。
Cl2 C. NO2 D. CO27。
下列物质属于离子化合物的是()A. HCl B。
K2O C。
CO D. N28. 4NH3+5O24NO+6H2O是硝酸工业中的一个反应。
下列关于该反应的说法正确的是()A。
增大反应物浓度能减慢反应速率 B. 降低温度能加快反应速率C. 使用催化剂能加快反应速率D. NH3与O2能100%转化为产物9。
下列物质的俗名与化学式对应正确的是()A。
食盐——NaCl B. 铁红—-Fe3O4C. 明矾-—Al2(SO4)3D. 烧碱-—Ca(OH)210. 在含有大量OH-、Ba2+、Cl-的溶液中,还可能大量共存的离子是()A. H+B。
Ag+C。
NO错误!D。
SO错误!11。
K2FeO4是一种高效水处理剂。
2019-2020学年广东高中学业水平测试化学必修部分 第3章 专题7 几种重要的金属化合物

专题七几种重要的金属化合物1.钠的氧化物比较1.(2019·6月广东学考)焙制糕点时,常用到小苏打。
小苏打的化学式为() A.NaNO3B.Na2CO3C.Na2SO4D.NaHCO3D[NaHCO3受热易分解,俗称小苏打。
]2.(2019·6月广东学考)物质俗名与化学式相匹配的一组是()A.纯碱——Na2CO3B.烧碱——NaHCO3C.生石灰——Ca(OH)2D.胆矾——FeSO4A[B项,烧碱是NaOH;C项,生石灰是CaO;D项,胆矾是CuSO4·5H2O。
] 3.(2017·广东学业水平考试)物质俗名与对应化学式相匹配的一组是() A.烧碱——Na2CO3B.纯碱——NaHCO3C.熟石灰——Ca(OH)2D.小苏打——NaOHC[烧碱为NaOH;纯碱为Na2CO3;小苏打为NaHCO3。
]4.(2019·1月广东学考)一种传递密信的方法如下:用毛笔蘸取酚酞溶液在白纸上写字,晾干后字迹消失。
在纸面上喷涂某种溶液。
可以使字迹重新显现出来。
则该溶液是()A.盐酸B.苏打水C.氯水D.食盐水答案:B5.(多选)(2017·1月广东学考)物质的用途与物质的化学性质有关的是() A.用醋酸除去水垢B.干冰用作冷冻剂C.活性炭用作除味剂D.制作馒头时加入小苏打AD[A中是醋酸与水垢中碳酸钙、氢氧化镁等发生化学反应,体现用途与化学性质有关;B中干冰气化吸收大量热可作冷冻剂,没有发生化学变化,是利用物理性质;C中活性炭吸附是利用物理性质;D中小苏打受热时分解放出CO2气体,使馒头松软,体现用途与化学性质有关。
]6.(多选)(2018·1月广东学考)下列物质在空气中久置后发生的变化属于化学变化的是()A.浓硫酸体积增大B.淡黄色的Na2O2变白C.浅绿色的FeSO4·7H2O变黄D.盛有NaOH溶液的试剂瓶口出现白色固体答案:BCD7.(2019·1月广东学考)物质的标准名称、俗名和化学式三者相一致的是() A.乙酸、醋酸、C2H6OB.碳酸钠、烧碱、Na2CO3C.碳酸氢钠、小苏打、NaHCO3D.氢氧化钙、生石灰、CaO答案:C8.(2019·1月广东学考)中国科学家研发的新一代“蛟龙”潜水器,向7 000米深海发起冲击。
2018届高考化学一轮复习考情分析检测第3章金属及其化合物3.3铁及其重要化合物
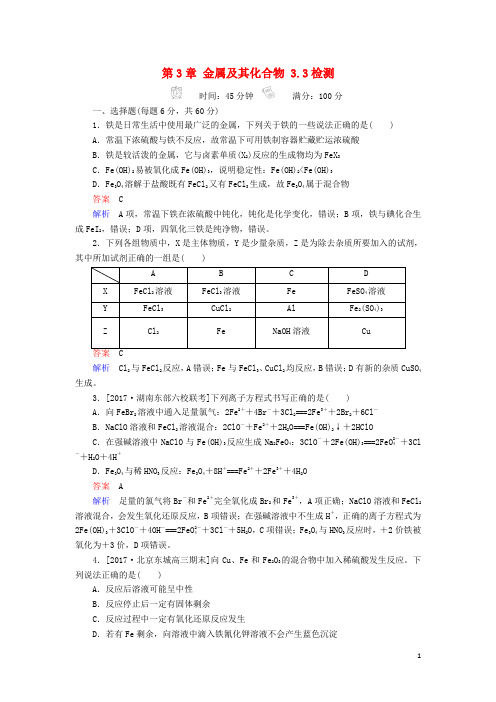
第3章金属及其化合物 3.3检测时间:45分钟满分:100分一、选择题(每题6分,共60分)1.铁是日常生活中使用最广泛的金属,下列关于铁的一些说法正确的是( )A.常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏贮运浓硫酸B.铁是较活泼的金属,它与卤素单质(X2)反应的生成物均为FeX3C.Fe(OH)2易被氧化成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3D.Fe3O4溶解于盐酸既有FeCl2又有FeCl3生成,故Fe3O4属于混合物答案 C解析A项,常温下铁在浓硫酸中钝化,钝化是化学变化,错误;B项,铁与碘化合生成FeI2,错误;D项,四氧化三铁是纯净物,错误。
2.下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是( )解析Cl2与FeCl2反应,A错误;Fe与FeCl3、CuCl2均反应,B错误;D有新的杂质CuSO4生成。
3.[2017·湖南东部六校联考]下列离子方程式书写正确的是( )A.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-B.NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O===Fe(OH)2↓+2HClOC.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3===2FeO2-4+3Cl +-+H2O+4HD.Fe3O4与稀HNO3反应:Fe3O4+8H+===Fe2++2Fe3++4H2O答案 A解析足量的氯气将Br-和Fe2+完全氧化成Br2和Fe3+,A项正确;NaClO溶液和FeCl2溶液混合,会发生氧化还原反应,B项错误;在强碱溶液中不生成H+,正确的离子方程式为2Fe(OH)3+3ClO-+4OH-===2FeO2-4+3Cl-+5H2O,C项错误;Fe3O4与HNO3反应时,+2价铁被氧化为+3价,D项错误。
2018版高中化学第三章金属及其化合物第2节几种重要的金属化合物课时2铝的重要化合物学案新人教版必修

课时2铝的重要化合物1.掌握铝的重要化合物的主要性质及应用。
(重点)2.了解铝的化合物相互转化的关系及图像。
(难点)3.了解两性氧化物和两性氢氧化物的概念。
氧化铝[基础·初探]1.物理性质色态溶解性熔点硬度白色固体难溶于水很高晶体时很大2.化学性质Al2O3是两性氧化物,与酸或强碱都能反应生成盐和水。
3.用途(1)冶炼金属铝的原料。
(2)良好的耐火材料。
【特别提醒】三类氧化物的比较类型概念实例碱性氧化物(都是金能与酸反应生成盐和水的Na2O+2HCl===2NaCl+H2O;属氧化物) 氧化物MgO+H2SO4=== MgSO4+H2O既能与酸反应生成盐和水,Al2O3+6HCl===2AlCl3+3H2O;A l2O3+2NaOH===2NaAlO2+H2O两性氧化物又能与碱反应生成盐和水的氧化物酸性氧化物(主要是能与碱反应生成盐和水的CO2+2NaOH=== Na2CO3+H2O;非金属氧化物) 氧化物SO3+2KOH=== K2SO4+H2O 说明:金属氧化物可以是碱性氧化物(如Na2O)、两性氧化物(如Al2O3),也可以是酸性氧化物(如Mn2O7)。
[题组·冲关]1.下列有关氧化物的叙述,正确的是()A.金属氧化物都是碱性氧化物1B.酸性氧化物在常温、常压下都是气态C.酸性氧化物都是非金属氧化物D.碱性氧化物都是金属氧化物【解析】Na2O2是金属氧化物,但不是碱性氧化物;P2O5、SiO2都是酸性氧化物,但是固态物质;Mn2O7是金属氧化物,但是酸性氧化物。
【答案】 D2.下列说法正确的是()A.Al2O3难溶于水,不跟水反应,所以它不是Al(OH)3对应的氧化物B.因为Al2O3是金属氧化物,所以Al2O3是碱性氧化物C.Al2O3能跟所有的酸、碱溶液反应D.MgO中的杂质Al2O3可以用NaOH溶液除去【解析】Al2O3虽难溶于水,但却是Al(OH)3对应的氧化物,可以根据Al2O3与Al(OH)3中Al的化合价相同判断;金属氧化物多数是碱性氧化物,但有些高价态的氧化物如Mn2O7却是酸性氧化物,Al2O3为两性氧化物;Al2O3与强碱溶液反应,但MgO与强碱不反应。
2018年7月普通高中学业水平考试化学试卷(含参考答案)

第1 页共8 页云南省2018年7月普通高中学业水平考试化学试卷[考生注意考生注意]]:本试卷分为必修模块卷和选修模块卷。
必修模块卷为全体考生必做。
选修模块卷含选修1《化学与生活》、选修5《有机化学基础》,由考生任选其中一个模块作答。
必须在答题卡上指定位置按规定要求作答,答在试卷上一律无效。
相对原子质量:H —1 C —12 O —16 Na —23 Al —27 S —32 Fe —56 Cu —64 必修模块卷(必修《化学1》必修《化学2》)选择题(共48分)一、选择题(本题包括24小时,每小题2分,共48分。
每小题只有一个选项符合题意)1.我国古代的四大发明对人类的发展作出了巨大的贡献,其中之一的“黑火药”是由硝酸钾、木炭粉、硫黄粉按一定比例混合而成,则“黑火药”的名称是由其中的颜色而来。
A .硝酸钾B .木炭粉C .硫黄粉D .无法判断2. 下列物质中,既属于钾盐又属于碳酸盐的是A .KNO 3B .Na 2CO 3C .Na 2SO 4D .K 2CO 33. 下列图示的三种实验操作名称从左到右依次是A .过滤、蒸发、分液B .过滤、蒸馏、分液C .蒸馏、过滤、分液D .分液、蒸馏、过滤4. 下列物质中不属于...天然高分子化合物的是A .蔗糖B .蛋白质C .纤维素D .淀粉5. 下列化学用语,表达正确的是A .甲烷的球棍模型:B .S 2—的结构示意图:C .CO 2的结构式:D .145C 核素中的质量数为8 6. 对铁及其化合物的叙述不正确...的是A .可用KSCN 溶液检验Fe 3+B .Fe(OH)2能在空气中稳定存在C .Fe 能从CuSO 4溶液中置换出Cu D .Fe 2O 3与Al 可发生铝热反应7. 当光束通过下列分散系时,能观察到丁达尔效应的是A .NaOH 溶液B .硫酸C .NaCl D .Fe(OH)3胶体8. 环境保护十分重要,“绿水青山就是金山银山”。
2018版高中化学第三章金属及其化合物学业分层测评14钠的重要化合物新人教版必修1

学业分层测评(十四) 钠的重要化合物(建议用时:45分钟)[学业达标]1.关于Na2O和Na2O2的叙述正确的是( )A.都能与水反应生成NaOHB.都是碱性氧化物C.都是白色固体D.氧化钠比过氧化钠稳定【解析】Na2O2为淡黄色固体,不属于碱性氧化物,但比Na2O稳定。
【答案】 A2.下列叙述中正确的是( )A.过氧化钠是淡黄色固体,久置于空气中变成白色的氢氧化钠固体B.过氧化钠中阴阳离子比例为1∶2C.用过氧化钠漂白织物、麦秆等日久又逐渐变成黄色D.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物【解析】过氧化钠久置于空气中变成白色碳酸钠固体,A错误;过氧化钠漂白是由于它的氧化性将有色物质永久漂白,C错误;碱性氧化物与酸反应生成盐和水,Na2O2与酸反应生成盐、水和氧气,不是碱性氧化物,属于过氧化物,D错误。
【答案】 B3.如图装置,试管b中盛有水,气球a中盛有干燥的Na2O2颗粒。
U形管中注有浅红色的水。
将气球用橡皮筋紧缚在试管口。
实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )A.U形管内红水褪色B.试管内溶液变红C.气球a被吹大 D.U形管水位:d<c【解析】由于发生反应:2Na2O2+2H2O===4NaOH+O2↑,产生O2使气球膨胀,该反应放出大量热量,使广口瓶中空气受热膨胀而出现U形管中水位d>c。
【答案】 C4.等物质的量的Na2CO3和NaHCO3分别与足量的同浓度的盐酸溶液充分反应,其中( ) A.Na2CO3放出的CO2多B.NaHCO3放出的CO2多C .Na 2CO 3放出CO 2的速度快D .NaHCO 3放出CO 2的速度快【解析】 NaHCO 3与HCl 反应时,HCO -3直接与H +发生反应生成CO 2气体;Na 2CO 3与HCl反应时:CO 2-3+H +===HCO -3,然后HCO -3+H +===CO 2↑+H 2O ,故NaHCO 3与盐酸反应放出CO 2的速度快。
2018版高中化学 第三章 金属及其化合物 学业分层测评17 用途广泛的金属材料 新人教版必修1

学业分层测评(十七) 用途广泛的金属材料(建议用时:45分钟)[学业达标]1.在生活、生产中,目前用量最大、用途最广的合金是( )A.钛合金B.铜C.钢D.硬铝【解析】在生产、生活中,目前用量最大、用途最广的合金是钢。
【答案】 C2.合金有许多特点,如NaK合金为液体,而Na和K的单质均为固体。
据此,试推测:生铁、纯铁、碳三种物质中,熔点最低的是( )A.纯铁B.生铁C.碳D.无法确定【解析】合金的熔点低于组成它的各成分。
【答案】 B3.用铜锌合金制成的黄铜制品常被误认为是黄金,下列方法中不能区分其真伪的是( )A.观察外观B.放入盐酸中C.测定密度D.高温灼烧【解析】铜锌合金制成的黄铜放入盐酸中,质量减轻,可以观察到合金溶解并且有气泡冒出,而黄金不溶于盐酸中;黄金密度大,测定密度可以鉴别;高温灼烧,黄金没有变化,而铜锌合金外观上有变化。
【答案】 A4.“嫦娥”探月,标志着中国的航空铝材处于世界领先行列。
下面关于铝合金的说法中,错误的是( )A.铝合金是一种混合物,它比纯铝的熔点低B.高温铝液易被氧化,铝合金应在熔剂层覆盖下熔炼C.镁铝合金耐腐蚀,但能被烧碱腐蚀D.镁铝合金在冷的浓H2SO4中钝化【解析】Mg在冷的浓H2SO4中不钝化。
【答案】 D5.下表中金属难与表中其他金属形成二元合金的是( )C.Zn、W D.Cu、Ag【解析】合金是在熔化状态下形成的一种熔合物。
熔点之间相差过大不易形成熔合物。
Zn熔点较低,419.5 ℃时,其他金属还未熔化;其他金属熔化时,它已气化。
W熔点过高,同样不易与表中其他金属形成合金。
【答案】 C6.有人要用金属材料做一个匾额的边框挂在墙上,从美观、经济、轻便的角度考虑,最好选用( )A.钢铁B.铝合金C.银合金D.金【解析】铝合金既经济又轻便,也很美观,是符合要求的材料。
【答案】 B7.汞合金是目前使用较多的补牙材料。
英国《新科学家》杂志发表了一篇文章,对汞合金补牙材料的安全性提出了质疑。
人教版高中化学必修1第三章《金属及其化合物》检测题(含答案)

《金属及其化合物》检测题一、单选题1.如图是铝的几种重要化合物之间的转化关系,下列表述不正确...的是()A.若加入的A是NaHCO3溶液,则生成沉淀的离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑,溶液的pH增大B.若加入的B是NaHCO3溶液,则生成沉淀的离子方程式为:Al(OH)4-+ HCO3-=Al(OH)3↓+CO32-+H2O,溶液的pH减小C.向AlCl3溶液中加入一定质量的Al(OH)3固体,一段时间后过滤,将所得固体洗涤干燥,称量,固体质量将增加D.若加入的A是氨水、NaOH溶液或CH3COONa溶液等;或加入的B是NH4HCO3溶液、NH4Cl溶液或通入SO2、CO2气体等,均可析出Al(OH)3沉淀2.将表面已完全钝化的铝条插入下列溶液中,不会发生反应的是()A.硫酸铜B.氢氧化钠C.稀硝酸D.稀盐酸3.下列关于某些氧化物的说法正确的是()A.NO2、Na2O2都能与水发生氧化还原反应B.NO、CO2均可用向上排空气法收集C.CO2、SO2可用澄清石灰水鉴别D.CO2、SO3都可由相应单质在O2中燃烧生成4.下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( ) ①金属钠投入到FeCl3溶液中②过量NaOH溶液和明矾溶液混合③少量Ca(OH)2投入过量NaHCO3溶液中④足量Na2O2投入FeCl2溶液中A.只有①④B.只有③C.只有②③D.只有①③④5.下列关于铝及其化合物的叙述中,不正确的是()A.铝是地壳中含量最多的金属元素B.红宝石、刚玉的主要成分是Al2O 3C .铝热反应可以用于冶炼金属D .氢氧化铝可以用作耐火材料6.下列化学用语或表述正确的是( ) A .14 C 的中子数为8 B .纯碱化学式:NaHCO 3 C .次氯酸的结构式:H-Cl-OD .NH 4Cl 的电子式7.对于反应:2Na 2O 2+2 CO 2===2Na 2CO 3+O 2,下列说法中正确的是( ) A .Na 2O 2是氧化剂,CO 2是还原剂 B .Na 2O 2既是氧化剂,又是还原剂C .生成1mol O 2时,电子转移的数目为4N A 个D .每有44 g CO 2与足量Na 2O 2反应,产生气体的体积为22.4L 8.在给定条件下,下列选项所示的物质间转化均能实现的是A .2CO Δ323NaCl(aq)NaHCO (s)Na CO (s)→→ B . MgCl 2·6H 2O (s )HCl∆−−→MgCl 2 Mg(s) C . SiSiO 2H 2SiO 3 D . NH 3(g)NO(g)HNO 3(g)9.下列物质的使用不涉及化学变化的是( )A .明矾作净水剂B .液氯作制冷剂C .溶洞的形成D .生石灰作干燥剂 10.常温下,下列溶液能用铝制容器盛装的是( ) A .稀硫酸B .浓硝酸C .盐酸D .氢氧化钠的溶液11.金属铝不能用来A .存储酸性溶液B .冶炼难熔金属C .制电线电缆D .制航天材料12.下列判断正确的是( )①足量金属Na 与标准状况下 反应时一定转移2 mol 电子 ②金属与氧气反应时都生成最高价金属氧化物 ③金属钠与 反应生成NaOH ,金属铜也能与 反应生成 ④ 与足量 反应时,每生成 转移电子的数目为 ⑤ 遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色 ⑥向饱和烧碱溶液中加入 ,充分反应后,溶液中+不变A .①②③B .②③⑤C .②④⑥D .④13.下列物质中不能由铁跟非金属单质直接结合而成的是 A .四氧化三铁 B .硫化亚铁C .氯化铁D .氯化亚铁二、实验题14.烧碱、纯碱等都是重要的化工原料。
2017-2018学年高中化学学业水平测试检测:第三章专题七 几种重要的金属化合物 学业水平过关 Word版含答案

第三章金属及其化合物专题七几种重要的金属化合物一、单项选择题(每小题1分,在每小题列出的四个选项中,只有一项符合题目要求。
)1.下列金属氧化物常用作耐火材料的是( )A.Fe2O3B.Cu2OC.CaO D.Al2O3解析:耐火材料熔点要高,MgO和Al2O3熔点都很高。
答案:D2.(2015·广州学考模拟)证明溶液中是否有Fe2+,其操作正确的顺序是( )(导学号 58540126)①加少许酸化的KMnO4溶液②加少许氯水③滴加少许KSCN溶液A.①②B.②③C.①②③D.③②解析:滴加少许KSCN溶液先证明无三价铁离子,再滴氯水,二价铁被氧化为三价铁,Fe3+遇KSCN变红。
答案:D3.下列关于Na2CO3和NaHCO3的说法中,不正确的是( )(导学号 58540127)A.均溶于水B.均为白色固体C.受热均易分解D.其水溶液均能使酚酞溶液变红解析:碳酸钠受热不易分解。
答案:C4.制造焊锡时,把铅加入锡中的重要原因是( )A.增加强度B.降低熔点C.增加硬度D.增强抗腐蚀能力解析:形成合金,可降低熔点,更容易完成点焊。
答案:B5.下列物质中,可用于治疗胃酸过多的是( )A.碳酸钠B.氢氧化铝C.氧化钙D.氢氧化钙解析:用于治疗胃酸过多的物质若具有碱性,则碱性不能过强,过强会伤害胃黏膜,在常见的物质中,可选择碳酸氢钠和氢氧化铝粉末。
6.下列离子方程式书写正确的是( )(导学号 58540128)A .铝与氢氧化钠溶液反应:Al +2OH -===AlO -2+H 2↑B .碳酸氢钠溶液与氢氧化钠溶液混合:HCO -3+OH -===CO 2↑+H 2OC .向稀盐酸中缓慢滴加几滴碳酸钠溶液:CO 2-3+2H +===CO 2↑+H 2OD .铜片投入氯化铁溶液中:FeCl 3+Cu===FeCl 2+CuCl 2解析:A 项铝与氢氧化钠溶液的反应有水参与;B 项碳酸氢钠与氢氧化钠反应生成的碳酸钠而不是二氧化碳;D 项不是离子方程式且未配平。
2018-2019年化学高中学业水平测试课件:第三章专题七考点3铁的化合物

B 错误;NaOH 溶液,属于混合物,C 错误;水蒸气仍然
是水,属于纯净物,D 正确。
答案:D
3.(2017 年 1 月·广东学考)下列过程包含有化学变化 的是( )
A.空气液化 B.滴水穿石 C.钢铁冶炼 D.活字印刷 解析:冶炼金属一般是将其化合物变成金属单质, 有新物质生成,属于化学变化。 答案:C
现象
白色沉淀迅速变为灰绿色, 最终变为红褐色
三、铁盐和亚铁盐 1.Fe3+的检验方法。 溶液― KS―C→N溶液呈红色―→Fe3+,溶液―加―N―aO―H→红
溶液 褐色沉淀―→Fe3+。
2.Fe2+的检验方法。 溶 液 ―KS―C→N 溶 液 颜 色 无 变 化 ―氯―水→ 溶 液 变 成 红 色
4.(2014 年 6 月·广东学考)关于铁及其化合物的叙述 正确的是( )
A.铁是一种较活泼的金属 B.Fe2O3 在常温下可以导电 C.Fe2O3 溶于水生成 Fe(OH)3 D.在常温下铁丝容易与水反应放出 H2
解析:金属能导电,但金属的化合物通常情况下不能 导电,只有溶于水或熔融状态才能导电,B 项错误;Fe2O3 不溶于水,也不能与水发生反应,C 项错误;铁在高温条 件下与水蒸气反应能产生氢气,D 项错误。
答案:ACD
1.(2018 年 1 月·广东学考·单选Ⅱ)铁块在 O2 中加热 一段时间后增重了 20 g,说明此过程中至少( )
A.消耗了 20 g O2 B.生成 20 g FeO C.生成 20 g Fe3O4 D.生成 20 g Fe2O3 解析:根据质量守恒定律,铁与氧气反应,铁在 O2 加热增加的是氧气的质量。 答案:A
(FeS2) 发 生 的 反 应 : FeS2 + H2O===Q + S + H2S ↑ ( 已 配 平),则物质 Q 2
2018版高中化学 第三章 金属及其化合物 学业分层测评15 铝的重要化合物 新人教版必修1

学业分层测评(十五) 铝的重要化合物(建议用时:45分钟)[学业达标]1.化学在生产和日常生活中有着重要的应用,下列说法不正确的是( )A.Al2O3用作耐火材料B.Na2O2常用于潜水艇或呼吸面具的供氧剂C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化D.Al(OH)3既溶于NaOH溶液、氨水,又能溶于盐酸【解析】Al(OH)3不溶于氨水等弱碱溶液。
【答案】 D2.下列离子方程式不正确的是( )A.氧化铝与盐酸反应:Al2O3+6H+===2Al3++3H2OB.氢氧化铝与NaOH溶液反应:Al(OH)3+OH-===AlO-2+2H2OC.向AlCl3溶液中滴加氨水:Al3++3OH-===Al(OH)3↓D.向AlCl3溶液中加入过量NaOH溶液:Al3++4OH-===AlO-2+2H2O【答案】 C3.氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的( )A.酸性B.碱性C.两性D.氧化性【解析】氢氧化铝中和胃酸,故利用的是氢氧化铝的碱性。
【答案】 B4.除去MgO中的Al2O3可选用的试剂是( )A.NaOH溶液B.硝酸C.浓硫酸D.稀盐酸【解析】Al2O3为两性氧化物,可溶于NaOH溶液中,而MgO不溶解,过滤即可得到MgO。
【答案】 A5.下列变化不可能通过一步实验直接完成的是( )A.Al(OH)3―→Al2O3B.Al2O3―→Al(OH)3C.Al―→AlO-2 D. Al3+―→Al(OH)3【解析】2Al(OH)3Δ,Al2O3+3H2O;2Al+2NaOH+2H2O===2NaAlO2+3H2↑;Al3++3NH3·H2O===Al(OH)3↓+3NH+4。
【答案】 B6.以Al2O3为原料制取氢氧化铝,最好的方法是( )A.将Al2O3溶于水B.将Al2O3先溶于盐酸中,之后滴加氢氧化钠溶液C.将Al2O3先溶于盐酸中,之后滴加氨水D.将Al2O3先溶于NaOH溶液中,之后滴加盐酸【解析】Al2O3不溶于水,A不能制得Al(OH)3,B、C、D中方法均能制得Al(OH)3,但B中加NaOH、D中加盐酸的量不好控制,过量后均能使Al(OH)3溶解,而C中氨水不能使Al(OH)3溶解,是制取Al(OH)3的最好方法。
2017-2018学年高中化学学业水平测试检测:第三章专题六 金属的化学性质及金属材料 学业水平过关 含答案

第三章金属及其化合物专题六金属的化学性质及金属材料一、单项选择题Ⅰ(每小题1分,在每小题列出的四个选项中,只有一项符合题目要求。
)1.下列金属中熔点最低的是( )A.Fe B.Na C.Sn D.Hg解析:常温下,各选项中只有D中汞是液态,说明汞的熔点最低。
答案:D2.下列性质不属于金属具有的共同性质的是( )A.导电性 B.酸性 C.延展性 D.导热性解析:金属不可能电离出H+,不具有酸性。
答案:B3.把下列金属分别投入0.1 mol/L盐酸中,能发生反应且反应最剧烈的是( ) A.Fe B.Na C.Mg D.Cu解析:金属活动性顺序中Na排在其他金属之前。
答案:B4.元素在自然界里分布并不均匀,如智利富藏铜矿,澳大利亚多铁矿,山东的黄金储量居我国首位,但从整个的地壳含量的多少分析,最丰富的金属元素是( ) A.Fe B.Si C.O D.Al解析:地壳中含量最丰富的前四种元素是O、Si、Al、Fe,其中含量最丰富的金属元素是Al。
答案:D5.(2014年6月·广东学考)将4种金属分别加入到4支装有稀盐酸的试管中,记录的现象如下表所示,正确的是( )答案:B6.钠长时间放置在空气中,最后的产物主要成分是( )A.Na2O B.NaOHC.Na2CO3D.Na2CO3·10H2O解析:本题考查钠在空气中发生的反应。
Na放置在空气中与氧气反应:4Na+O2===2Na2O,Na2O+H2O===2NaOH,2NaOH+CO2===Na2CO3+H2O,Na2CO3与水生成Na2CO3·10H2O,Na2CO3·10H2O 在空气中风化得Na2CO3。
答案:C7.钠与水反应的现象与钠的下列性质无关的是( )A.钠的熔点低B.钠的密度小C.钠的硬度小D.钠的还原性很强解析:钠的熔点低可由钠与水反应时能熔成闪亮的小球来证明;钠的密度小可由钠浮出水面上证明;钠的硬度小可在切割钠时证明,与其在水中反应的现象无关;小球四处游动,剧烈反应,有“嘶嘶”声,证明钠的还原性很强。
【推荐精选】2018年秋高中化学 第三章 金属及其化合物 3.2.2 几种重要的金属化合物随堂检测 新人教版必修1

几种重要的金属化合物随堂检测1.下列各组反应中能得到Al(OH)3的是( )A.Al 2O 3加到热水中B.向NaAlO 2溶液中加入过量盐酸C.将Na 投入NaAlO 2溶液中D.在AlCl 3溶液中加几滴NaOH 溶液2、有下列四组物质,如果把某组物质中的后者逐滴加到前者中至过量,将出现“先产生白色沉淀,后白色沉淀溶解”的现象,则这组物质是( )A.稀硫酸、氯化钡溶液B.氯化铝溶液、氨水C.氯化钠溶液、硝酸银溶液D.氯化铝溶液、氢氧化钠溶液3.铝、氧化铝、氢氧化铝和可溶性铝盐分别与过量强碱溶液反应,其生成物有一定的规律。
下列说法正确的是( )A.都有H 2O 生成B.都有H 2生成C.都有2AlO -生成D.都有Al 3+生成4.有MgCl 2、Al 2(SO 4)3的混合溶液,向其中不断加入NaOH 溶液,得到的沉淀量与加入的NaOH 溶液的关系如图所示。
则溶液中c(Cl -)与c(24SO -)之比为( )A.1∶1B.2∶3C.3∶2D.2∶15.只用试管和胶头滴管,不用其他试剂无法区分的一组溶液是[已知3+223Al +3AlO +6H O=4Al(OH)↓-]( )A.KOH 溶液和AlCl 3溶液B.Na2CO3溶液和盐酸C.NaHCO3溶液和NaOH溶液D.盐酸和NaAlO2溶液6.(双选)下列各组离子一定能大量共存的是( )A.含有大量Fe3+的溶液中:NH4+、Na+、CI-、OH-B.在强碱溶液中:Na+、K+、AlO2-、CO32-C.在pH=1的溶液中:NH4+、Al3+、SO42-、NO3-D.在pH=1的溶液中:K+、Fe2+、Cl-、CO32-7、相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )A.Al B.Al(OH)3 C.AlCl3 D.Al2O38.(1)用氯化铝溶液与氢氧化钠溶液反应时,当Al3+的物质的量与OH-的物质的量之比(以下均填物质的量之比)为________时,Al(OH)3沉淀量最多;________时,Al(OH)3恰好全部溶解。
2018版高中化学 第三章 金属及其化合物 学业分层测评16 铁的重要化合物 新人教版必修1

学业分层测评(十六) 铁的重要化合物(建议用时:45分钟)[学业达标]1.在含有1 mol FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀得到的固体物质是( )A.Fe B.FeOC.Fe(OH)3D.Fe2O3【解析】钠与水反应生成NaOH,NaOH与FeSO4溶液反应生成Fe(OH)2,Fe(OH)2灼烧时被氧化,最后得到的固体物质是Fe2O3。
【答案】 D2.下列关于铁及其化合物的说法中正确的是( )A.Fe3O4是一种红棕色粉末,俗称磁性氧化铁B.铁与水蒸气在加热条件下的反应产物为Fe2O3和H2C.除去FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤D.Fe3+与KSCN反应产生红色沉淀【解析】A项,Fe3O4为黑色晶体;B项,Fe与H2O(g)反应生成Fe3O4;D项,Fe3+与SCN -反应生成红色液体。
【答案】 C3.苹果汁是人们喜欢的饮料。
由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。
若榨汁时加入维生素C,可有效防止这种现象发生。
这说明维生素C具有( )A.氧化性B.还原性C.碱性D.酸性【解析】现榨的苹果汁在空气中会由淡绿色变为棕黄色,是因为溶液中的Fe2+被空气中的氧气氧化生成Fe3+,加入维生素C可有效防止这种现象发生,说明维生素C首先被空气中的O2氧化,而使溶液中的Fe2+不发生反应,因此维生素C具有较强的还原性。
【答案】 B4.下列离子方程式书写正确的是( )A.铁与FeCl3溶液反应:Fe+Fe3+===2Fe2+B.Fe与稀盐酸反应:2Fe+6H+===2Fe3++3H2↑C.FeCl2溶液与Cl2反应:Fe2++Cl2===Fe3++2Cl-D.Fe(OH)3与盐酸反应:Fe(OH)3+3H+===Fe3++3H2O【答案】 D5.向某溶液中加入含Fe2+的溶液后,无明显变化。
当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是( )A.该溶液中一定含有SCN-B.氧化性:Fe3+>Cl2C.Fe2+与SCN-不能形成红色物质D.Fe2+被氧化为Fe3+【解析】溶液中的Fe2+与加入的新制氯水发生反应:2Fe2++Cl2===2Fe3++2Cl-,氧化性:Fe3+<Cl2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章金属及其化合物
专题七几种重要的金属化合物
一、单项选择题(每小题1分,在每小题列出的四个选项中,只有一项符合题目要求。
)
1.下列金属氧化物常用作耐火材料的是( )
A.Fe
2O
3
B.Cu
2
O
C.CaO D.Al
2O
3
解析:耐火材料熔点要高,MgO和Al
2O
3
熔点都很高。
答案:D
2.(2015·广州学考模拟)证明溶液中是否有Fe2+,其操作正确的顺序是( )(导学号 58540126)
①加少许酸化的KMnO
4
溶液②加少许氯水③滴加少许KSCN溶液A.①②B.②③
C.①②③D.③②
解析:滴加少许KSCN溶液先证明无三价铁离子,再滴氯水,二价铁被氧化为三价铁,Fe3+遇KSCN变红。
答案:D
3.下列关于Na
2CO
3
和NaHCO
3
的说法中,不正确的是( )(导学号
58540127)
A.均溶于水
B.均为白色固体
C.受热均易分解
D.其水溶液均能使酚酞溶液变红
解析:碳酸钠受热不易分解。
答案:C
4.制造焊锡时,把铅加入锡中的重要原因是( ) A.增加强度B.降低熔点
C.增加硬度D.增强抗腐蚀能力
解析:形成合金,可降低熔点,更容易完成点焊。
答案:B
5.下列物质中,可用于治疗胃酸过多的是( )
A.碳酸钠B.氢氧化铝
C.氧化钙D.氢氧化钙
解析:用于治疗胃酸过多的物质若具有碱性,则碱性不能过强,过强会伤害胃黏膜,在常见的物质中,可选择碳酸氢钠和氢氧化铝粉末。
答案:B
6.下列离子方程式书写正确的是( )(导学号 58540128)
A.铝与氢氧化钠溶液反应:Al+2OH-===AlO-
2+H
2
↑
B.碳酸氢钠溶液与氢氧化钠溶液混合:HCO-
3+OH-===CO
2
↑+H
2
O
C.向稀盐酸中缓慢滴加几滴碳酸钠溶液:CO2-
3+2H+===CO
2
↑+H
2
O
D.铜片投入氯化铁溶液中:FeCl
3+Cu===FeCl
2
+CuCl
2
解析:A项铝与氢氧化钠溶液的反应有水参与;B项碳酸氢钠与氢氧化钠反应生成的碳酸钠而不是二氧化碳;D项不是离子方程式且未配平。
答案:C
7.自然界中最常见的钠的化合物是( )
A.NaCl B.Na
2
O
C.Na
2O
2
D.NaOH
答案:A
8.化学式与俗名相符的是( )
A.烧碱Na
2CO
3
B.胆矾CuSO
4
〃5H
2
O
C.苏打NaHCO
3
D.纯碱NaOH
解析:烧碱是NaOH,纯碱、苏打是Na
2CO
3
,小苏打是NaHCO
3。
答案:B
9.下列变化不可能通过一步实验直接完成的是( )
A.Al(OH)
3―→Al
2
O
3
B.Al
2
O
3
―→Al(OH)
3
C.Al―→AlO-
2D.Al3+―→Al(OH)
3
解析:A、C、D项反应的化学方程式依次为2Al(OH)
3=====
△
Al
2
O
3
+3H
2
O,2Al。
