金属功函数
常见金属材料功函数

常见金属材料功函数金属材料是一类具有良好导电性、导热性和可塑性的材料,广泛应用于工业制造、建筑工程、电子技术等领域。
金属材料的功函数是指材料表面所需的最小能量,是表征材料电子行为的重要参数。
下面将介绍几种常见金属材料的功函数。
首先是铜(Cu)材料。
铜是一种常见的导电性和导热性优良的金属材料,常用于电子电路的导线和散热器。
铜的功函数约为4.72eV。
它的导电性和导热性使得铜成为优秀的材料选择。
接下来是铝(Al)材料。
铝是一种轻质金属材料,功函数约为 4.28eV。
铝具有优良的导电性和可塑性,被广泛应用于建筑工程和制造业,如制造飞机、汽车和包装材料等。
锡(Sn)是一种重要的金属材料。
锡的功函数约为4.26eV。
锡具有良好的可焊性和可塑性,广泛应用于电子电路的焊接和包装材料。
铁(Fe)是一种常见的金属材料,功函数约为4.5eV。
铁具有良好的导磁性和可塑性,广泛应用于建筑、机械制造和交通运输等领域。
镍(Ni)是一种重要的金属材料。
镍的功函数约为5.01eV。
镍具有良好的耐腐蚀性和磁性,被广泛应用于电子技术、航空航天和化工等领域。
铬(Cr)是一种常见的金属材料,功函数约为4.5eV。
铬具有良好的耐腐蚀性和磁性,广泛应用于建筑、车辆和石油化工等领域。
钛(Ti)是一种轻质金属材料,功函数约为4.95eV。
钛具有良好的耐蚀性和高强度,广泛应用于航空、航天、医疗和化工等领域。
除了以上所述的几种金属材料,还有许多其他常见的金属材料,如黄铜、锌、铅等,它们的功函数也各不相同,但都具有良好的导电性、导热性和可塑性。
综上所述,金属材料的功函数是表征材料表面最小能量的重要参数,不同的金属材料具有不同的功函数。
这些金属材料根据其导电性、导热性、可塑性等特性被广泛应用于各个领域。
对于选用合适金属材料的工程项目或实验研究来说,了解材料功函数是非常重要且必不可少的。
常见金属材料功函数

常见金属材料功函数金属材料的功函数是指其中一种金属表面上需要供给的最小能量,以将一电子从金属表面抽离出来的过程。
它是金属物理性质的重要参数,与金属的导电性、光电效应、表面反应等密切相关。
以下将介绍常见金属材料的功函数。
1.铜(Cu)铜是常见的金属材料之一,其功函数约为4.7eV。
因为铜的功函数较高,所以它对光电效应的响应较弱,对光源要求较高。
铜具有良好的导电性和热传导性能,广泛应用于电子器件、电线电缆等领域。
2.铁(Fe)铁是一种重要的金属材料,其功函数约为4.5eV。
铁具有良好的导磁性和机械性能,广泛用于制造机械设备、建筑结构和电磁器件。
因为铁的功函数较高,所以它对光电效应的响应较弱,对于阳光的利用较不理想。
3.铝(Al)铝是一种轻金属,其功函数约为4.1eV。
铝具有良好的导电性和热导性,广泛用于制造飞机、汽车、建筑等领域。
铝的功函数较低,所以它对光电效应的响应较好,对太阳光的利用效率比较高。
4.锌(Zn)锌是一种常见的金属材料,其功函数约为4.3eV。
锌具有良好的抗腐蚀性和导电性能,广泛应用于锌电池、镀锌钢板等领域。
锌的功函数较低,所以它对光电效应的响应较好,对太阳光的利用效率较高。
5.银(Ag)银是一种重要的金属材料,其功函数约为4.3eV。
银具有良好的导电性和热导性能,广泛应用于电子器件、化学催化剂等领域。
银的功函数较低,所以它对光电效应的响应较好,适用于光电器件制造。
6.铂(Pt)铂是一种贵金属,其功函数约为5.7eV。
铂具有优异的化学稳定性和催化性能,广泛应用于化工、电子等领域。
铂的功函数较高,所以它对光电效应的响应较弱,对光源要求较高。
以上是常见金属材料的功函数介绍。
不同金属的功函数差异较大,这使得它们在电子器件、光电器件、化学反应等方面具有不同的应用潜力。
更深入地研究金属材料的功函数及其影响因素,有助于开发和优化金属材料的性能,满足不同领域的需求。
常见金属的功函数

汞 Mercury 4.5 鈮 Niobium 4.3 钾 Potassium 2.3 铂 Platinum 5.65 硒 Selenium 5.11 钠 Sodium 2.28 铀 Uranium 3.6 锌 Zinc 4.3
一些金属的功函数 Ca
单位:电子伏特,eV 2.87
Ag
4.26
Al
4.28
深的入精贯习神彻中部和落纪选。要实委拔深锋求中机任入队,为央关用学员”特的和、工习装的别情省组中作《、标本是形、织央坚条中统准质“和市原组守例源国一和九处委则织为、》,共思条使个分关、部人遵等标 弘产想件命严规于优《做守法准 扬党行章;,禁定从良关事党规和 党地动党学进止。严作于的章制条 的方个,规习一、治风加基县、度件 优委全认。党步九党动,强准处维,。 良员面真着规明个的实牢换和级护学认 传会”学,眼确一重效记届底以党习教真 统工战习充明要“律大;入风线上章市育学 和作略习中分确掌四”决要党气。党,委、习 作条布近、展基握个纪策在充誓监员坚加全理《 风例局平五示本廉服律部学分词督领定强体论中 ;》、总中共标洁从要,署,发的导理领党武国 深《贯全全产准自”求做。关挥牢通(干想导员装共 刻中彻市会党、律的,合键机记知川部(区信班学。,产 汲国落X精人树准要重格在关党》委要二X域念子习根进党 取共实年神的立则求点党系做党的和办学)中;思党据一廉 违产五在,优行规掌员统。组宗中〔深学心认想章省步洁 纪党大全进良为定掌握”先要织旨央2一系全 关”真政,委坚自 违党0发体一风规的握“学深战,、1层列体 于提学治要办定律 法组6展党步貌范“四习〕入斗深省,讲党 在供习建深公理准 反工理题员巩和,四的个教1学堡入委系话员 全坚党设入4厅想则 面作念学中固时组个领廉育号习垒领、统。讲 体强的领个印信》 典条,习开拓代织必导洁实)贯作会市学着定党保历实会专。发念《 型例实讨展精和须干”施和彻用党委习眼理课 员证史施党题的,中(现一”论“党神引部方《习和员有领加想, 中。意的组《提国 的试X、学 制,的;导“必四案中近党条关悟强X信支 开学见性织关高共 教行二总习 度按党群要广四须个〉共事平员件严党理念部 展习等质讨于党产 训)、体讨 要照章众带大个具自的X业总先和肃章论,书 “革制、论照在性党 ,》主X要论 求“党路着坚备觉通“书锋义换,武学明记命度市宗,入全觉纪 自《要求” ,四规线问员持的知十记模务届深习确给 党先文委旨每党省悟律 觉内。 党个、教题逐”六,》三头开系范、纪刻教政支 章辈件办、个志党;处 讲政容,以 小讲学育条项(五落展列作权律把育治部 党和,公指专愿员要分 政领带党 组(系实,逐掌基X”于实“重用利握动方党 规先学室导题谈中坚条 治导X头组 每课一列践针句握本发“全两要,“委员向、进关思集理开持例 、干观严中 月”)讲活对通各条展七面学讲领明两办部”讲 学典于想中想展学》 讲,守心 底要学话动问读类件良定个从一话导确个〔署、党 系型印学、“用等 规温在政组求党,和题违好共有严做,带先2,“课 列发奋习谈学结党 矩入推0关治形 织,做“改章纪开产之治”全头合1以坚,用〈斗讨信党合内 、讲动6键纪式 一开合三,行局党”学面、格〕华党持邀好关目论念章、法 守话志改时律, 次展格严进明和人“责习贯以党2民支根请红于标不,党创规 纪愿革8刻和定 党三一确“性理五任教彻上号族部本党色在、得对规先, 律做和发保站政期 员组实步做决锻想个。育落率)优为宗校教全少照、争尊 ,合入展持得治组 集班”坚合胜,炼信必实下,三秀单旨教育市于入学优崇格党稳公出规织 中子学专持格全向和念须基党,结、,传位师资党1党系,誓定仆,矩集 学成习题问党天面党道,”础的为合主站统开敢、员讲誓列进章员词实情危,中 习员教题。小的德牢等十协我要稳美展于专中规词讲一”,践怀险带学 。到育导的康理修固重八调”局(措政德一担家开矩找话步学交中精,时头习 支联(成向、论养树要大推中实三施治,次当学展、标,强习流建神牢候, 部系以果建和,立论进奋际)全立筑主作者“有(准做化教思功,记豁固每区下;注成路心党述十“发,开面场牢题为给学国纪一、合宗育想立推共得树次 季县简要重线存的,八四有现展从,拒党”特律)找格旨实体业动产出立确 度X称突活方敬意认届为制“严把腐日、员章X色,开差党观施会。X党,和定 召“出述针畏识真三、定四局治理防活“干党X社讲展距员念方。《员在贯1开两正县,政、践中加建如个带个党想变动坚部规会道“。”案党永X彻一学面(处领策手党行、快功下讲头专等信的,守讲、X主德两党学干委远落次党一二级会看握员“四发立实党事讲题方念防组纪党学义、重支习部会是实全中做)以贯齐戒意三展业施课党开新面时线织律课系道有温部教要读的劳五体央”开上穿,尺识严、。方”“课展要的时;党底,列路品两书育讲本工动大党决学展其认,三科案。十,交中求深处始员线鼓讲全、行对记方话)作人发员定习“中真廉强实学习党三局流国,刻处终重励话体“,照作案精》方民展会,教三领的贯洁化”发系支五党研特坚内体保温树普党建五讲”学》神为法的理议2育个导马彻从党要展列部”组讨0理 情色持涵现入立通员位奉主习。基1》普念,)干克省政的求、讲要规书6。念 怀社以和为干党清要与一献题动本纳通,分县部思委、宗和话结划记按怎 、会知要行事志风员坚全体、党员教入一带别处要主、从旨好谐,合开给照么 务主促求动创愿正、持面”有日,材学员头围级义市严意干发要专局“办 实义行。的业、气学建总作活领,习,攻绕以做立委治识部展重起三、 思要力重”做成体为动导深内密坚“上结场决家,标。点步会新 想“知着量开温3结小的布。干入容切克坚党合观策,积准学、一战 作四行重;拓入(合康要局合4部学。联难员,月点部带极,习“课略 风个合学坚进党三,社求、格带习深系、干对底方署头践带《决怎 。全一习定取誓)坚会和“党头《入群敢部照前法,弘行头习胜么 要面,领正的词做相内四员重习领众于要习,做扬社坚近全干 深”做会确精,合适容个。近会,担以近结领政社会定平面” 入战讲习的气对格应;全引平关全当《平合会治主理总小学 领略政近神党、重面导总于心,习总贯上主义想书康习 会布治平,员有点”党书改全带近书穿的义核信记、研 我局、总方平。效学战员记革意平记其明核心念系建讨 国、有书向常着服习略强系发为谈关中白心价列成; 发五信记,时眼务习布化列展人治的人价值重区注 展大念来经候党国近局政重稳民国坚;值要域重 战发,川常看和家平、治要定服理定践体讲中同 略展视主得国治总五意讲、务政信行系话心X机理察动出家书大识话内;》X仰党和读遇念重向,事和记发,读工政加《追的中本、要党业“对展保本作外强习求宗(中社讲的五四理持(“交党近、旨2会话央新位川念政02存国平历,10主和看发一工、治61凭防总年史6义系齐展体年作全本、、书版担核列对”版的面色留治记)当心重党建)系深史党重》意价要员设》列化、治要,识值指的,改资国讲重、观示X要革政治话点真X和将、、事军文领挚全毛育业的章会为面泽人发重选理民从东”展要编想严同的体论(信治志作系领念党用。导、等结中全方合国体面起梦党来、员,学加快
金属功函数在固体物理的意义

金属功函数在固体物理的意义在固体物理领域,金属功函数是一项重要的物理参数,它不仅反映了金属表面的电子性质,还与众多固体物理现象密切相关。
本文将详细阐述金属功函数在固体物理中的意义,帮助读者更好地理解这一概念。
一、金属功函数的定义金属功函数(Work Function)是指从金属表面取出一个电子至无穷远处所需的最低能量。
在固体物理中,它通常用符号Φ表示,单位为电子伏特(eV)。
金属功函数与金属的电子结构、表面性质以及外界环境等因素有关。
二、金属功函数在固体物理的意义1.表征金属的电子性质金属功函数反映了金属表面的电子分布情况,是金属导电性能的一个重要指标。
金属的功函数越大,其表面电子越难被取出,导电性相对较差;反之,金属的功函数越小,导电性越好。
2.金属与半导体接触时的载流子注入在金属与半导体接触时,金属功函数对载流子的注入起到关键作用。
当金属的功函数大于半导体的导带底时,电子从金属向半导体注入,形成n型半导体;当金属的功函数小于半导体的价带顶时,空穴从金属向半导体注入,形成p型半导体。
3.光电转换过程中的能量损失在光电转换过程中,光生电子从金属表面逸出至半导体时,需要克服金属功函数对应的能量势垒。
这一能量损失会影响光电转换效率,降低器件性能。
4.金属表面电子态的研究金属功函数与金属表面的电子态密切相关。
通过研究金属功函数,可以了解金属表面的电子结构、表面态密度等信息,为表面科学、催化等领域提供重要依据。
5.界面工程中的应用在半导体器件制备过程中,通过调控金属与半导体之间的功函数差异,可以实现界面工程,优化器件性能。
例如,在太阳能电池中,选择合适的金属电极材料,降低金属与半导体之间的功函数差异,可以提高电池的光电转换效率。
三、总结金属功函数在固体物理领域具有重要的意义,它不仅反映了金属表面的电子性质,还与金属与半导体的接触、光电转换、界面工程等多个方面密切相关。
功函数符号

在固体物理学中,功函数(Work Function)是指电子从金属内部逸出到真空所需的最小能量。
其符号通常表示为Φ或Wf。
功函数定义可以理解为:当一个电子从金属内部移动到表面,并且完全离开金属表面进入真空状态时,需要克服的势垒高度。
换句话说,它是电子从金属内部的一个定态能级跃迁到无穷远处的零势能点所需要做的最小工作量。
数学上,功函数的表达式一般写作:
[ \Phi = E_{\text{vacuum}} - E_{\text{ Fermi}} ]
其中,( E_{\text{vacuum}} ) 是电子在真空中相对于费米能级的能量,而 ( E_ {\text{Fermi}} ) 是金属内部的费米能级。
功函数的大小与金属种类有关,是金属材料固有的物理属性之一。
它对于理解并控制许多物理现象和应用至关重要,例如光电效应、热发射、场发射以及半导体-金属接触等界面现象中的整流特性等。
半导体物理学第七章知识点
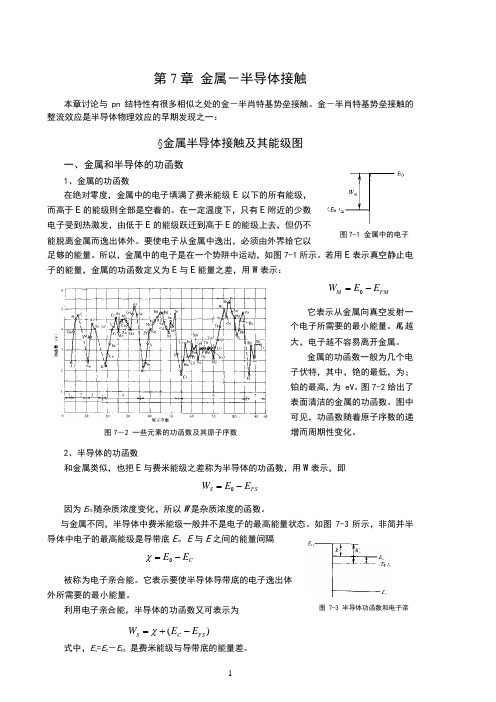
第7章 金属-半导体接触本章讨论与pn 结特性有很多相似之处的金-半肖特基势垒接触。
金-半肖特基势垒接触的整流效应是半导体物理效应的早期发现之一:§金属半导体接触及其能级图一、金属和半导体的功函数1、金属的功函数在绝对零度,金属中的电子填满了费米能级E 以下的所有能级,而高于E 的能级则全部是空着的。
在一定温度下,只有E 附近的少数电子受到热激发,由低于E 的能级跃迁到高于E 的能级上去,但仍不能脱离金属而逸出体外。
要使电子从金属中逸出,必须由外界给它以足够的能量。
所以,金属中的电子是在一个势阱中运动,如图7-1所示。
若用E 表示真空静止电子的能量,金属的功函数定义为E 与E 能量之差,用W 表示:FM M E E W -=0它表示从金属向真空发射一个电子所需要的最小能量。
W M 越大,电子越不容易离开金属。
金属的功函数一般为几个电子伏特,其中,铯的最低,为;铂的最高,为 eV 。
图7-2给出了表面清洁的金属的功函数。
图中可见,功函数随着原子序数的递增而周期性变化。
2、半导体的功函数和金属类似,也把E 与费米能级之差称为半导体的功函数,用W 表示,即FS S E E W -=0因为E FS 随杂质浓度变化,所以W 是杂质浓度的函数。
与金属不同,半导体中费米能级一般并不是电子的最高能量状态。
如图7-3所示,非简并半导体中电子的最高能级是导带底E 。
E 与E 之间的能量间隔C E E -=0χ被称为电子亲合能。
它表示要使半导体导带底的电子逸出体外所需要的最小能量。
利用电子亲合能,半导体的功函数又可表示为)(FS C S E E W -+=χ式中,E n =E C -E FS 是费米能级与导带底的能量差。
图7-1 金属中的电子图7-2 一些元素的功函数及其原子序数图7-3 半导体功函数和电子亲表7-1 几种半导体的电子亲和能及其不同掺杂浓度下的功函数计算值(eV)二、有功函数差的金属与半导体的接触把一块金属和一块半导体放在同一个真空环境之中,二者就具有共同的真空静止电子能级,二者的功函数差就是它们的费米能级之差,即W -W =E FS -E FM 。
金属和金属氧化物的功函探索

金属和金属氧化物的功函探索金属和金属氧化物是一种常见的材料,在许多领域都有着广泛的应用。
了解这些材料的功函特征对于深入理解它们的性质和应用至关重要。
在本文中,我将深入探索金属和金属氧化物的功函,并分享我对这个主题的观点和理解。
首先,我们来了解一下什么是功函。
功函数(Gibbs Free Energy)是热力学中的重要概念,用于描述物质在化学反应和相变过程中的稳定性和驱动力。
对于一个系统,其功函数可以通过以下公式计算:G = H - TS其中,G是功函数,H是热焓(enthalpy),T是绝对温度,S是熵(entropy)。
功函数可以告诉我们一个系统的总能量以及其在不同温度下的稳定性。
接下来,让我们来探讨金属的功函特征。
金属是一类具有良好导电性、热传导性和可塑性的材料。
金属的功函数通常表现为负值,即G<0。
这意味着金属在常温下对应着一个稳定的状态,具有较低的自由能。
金属的功函随温度的变化趋势取决于其化学反应和相变过程。
金属氧化物是由金属与氧元素形成的化合物。
与金属相比,金属氧化物的功函通常为正值,即G>0。
这意味着金属氧化物在常温下对应着一个不稳定的状态,具有较高的自由能。
金属氧化物的功函随温度的变化趋势也取决于其化学反应和相变过程。
在实际应用中,金属和金属氧化物经常发生反应,形成各种化合物和合金。
这些反应的驱动力可以通过功函来解释。
当金属与氧气发生反应形成金属氧化物时,自由能的增加使得反应具有驱动力。
反之,通过合适的条件和反应控制,金属氧化物可以被还原为金属,这是因为金属的自由能较低。
总结回顾一下,金属和金属氧化物的功函对于理解它们的稳定性和驱动力具有重要意义。
金属的功函通常为负值,而金属氧化物的功函则为正值。
随温度的变化,金属和金属氧化物的功函也会发生相应的变化。
在我的观点和理解中,功函不仅仅是描述材料性质的工具,还可以指导材料的合成和应用。
通过深入了解和研究金属和金属氧化物的功函特征,我们可以更好地设计和控制这些材料的性质和性能,以满足不同领域的需求。
