高考化学易错题专题训练-化学反应的速率与限度练习题及答案解析
精选高考化学易错题专题复习化学反应的速率与限度附详细答案

精选高考化学易错题专题复习化学反应的速率与限度附详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
根据图中数据,完成下列问题:(1)该反应的化学方程____;(2)反应开始至2min,气体Z的平均反应速率为_____;(3)达到平衡后,下列说法不正确的是_____。
A.X、Y、Z的浓度之比是1:2:3B.X的消耗速率和Y的生成速率相等C.Z的浓度保持不变【答案】3X+2Y3Z 0.125mol/ ( L min) B【解析】【分析】【详解】(1)根据图知,随着反应的进行X、Y的物质的量减少,而Z的物质的量增大,所以X和Y 是反应物、Z是生成物,10min时反应达到平衡状态,则参加反应的△n (X) = (1.00-0.25)mol=0.75mol、△n(Y)=(1.00-0.50) mol=0.50mol、△n ( Z)=(0.75-0) mol=0.75mol,同一可逆反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.75mol: 050mol:0.75mol=3:2:3所以该反应方程式:3X+2Y3Z;(2) 0-2min内Z的平均反应速率v=ct=0.50mol2L2min=0.125mol/ ( L min),故答案为:0.125mol/ ( L min);(3) A.相同容器中,X、Y、Z的浓度之比等于其物质的量之比=0.25mol:0.50mol:0.75mol=1:2:3,故A正确;B.该反应中X、Y的计量数之比为3:2,当X的消耗速率与Y的生成速率之比为3:2时该反应达到平衡状态,所以当X的消耗速率和Y的生成速率相等时该反应没有达到平衡状态,故B错误;C.当Z的浓度保持不变时,正逆反应速率相等,可逆反应达到平衡状态,故C正确;故选B。
高考化学易错题专题训练-化学反应的速率与限度练习题附答案

高考化学易错题专题训练-化学反应的速率与限度练习题附答案一、化学反应的速率与限度练习题(含详细答案解析)1.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH 2COONH4(s)2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);A.2v生(NH3)=v耗(CO2)B.密闭容器中氨气的物质的量不变C.容器中CO2与NH3的物质的量之比保持不变D.密闭容器中总压强保持不变E.形成6个N-H键的同时有2个C=O键断裂(2)能使该反应的反应速率增大的是___(填选项);A.及时分离出CO2气体B.适当升高温度C.加入少量NH2COONH4(s)D.选择高效催化剂(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【答案】AC BD 大于【解析】【分析】(1)根据化学平衡状态的特征解答;(2)增大浓度或升高温度或加催化剂可加快反应速率来解答;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,结合化学键分析解答。
【详解】(1)A.平衡时应有v生(NH3)=2v耗(CO2),所以2v生(NH3)=v耗(CO2)时,反应没有达到平衡状态,故A错误;B.密闭容器中氨气的物质的量不变,说明正、逆反应速率相等,可以判定反应达到平衡状态,故B正确;C.只要反应发生,容器中CO2与NH3的物质的量之比就是2:1,始终保持不变,不能判定反应是否达平衡状态,故C错误;D.密闭容器中总压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故D正确;E.形成6个N-H键等效于2个C=O键形成的同时有2个C=O键断裂,正、逆反应速率相等,达平衡状态,故E正确;故答案为AC;(2)A.及时分离出CO2气体,生成物浓度减小,反应速率减小,故A错误;B.适当升高温度,反应速率加快,故B正确;C.加入少量NH2COONH4(s),固体物质量变但浓度不变,故C错误;D.选择高效催化剂,反应速率加快,故D正确;故答案为:BD;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,即反应中断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量。
高考化学复习化学反应的速率与限度专项易错题含答案

高考化学复习化学反应的速率与限度专项易错题含答案一、化学反应的速率与限度练习题(含详细答案解析)1.某温度下在2L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。
(1)该反应的化学方程式是________________________(2)若A、B、C均为气体,10min后反应达到平衡,①此时体系的压强是开始时的________倍。
②在该条件达到平衡时反应物的转化率为________%(计算结果保留1位小数)(3)关于该反应的说法正确的是_________。
a.到达10min时停止反应b.在到达10min之前C气体的消耗速率大于它的生成速率c.在10min时B气体的正反应速率等于逆反应速率【答案】2C A+3B 97或1.29或1.3 66.7% b、c【解析】【分析】(1)由图可知,C是反应物,物质的量分别减少2mol,A、B生成物,物质的量增加1mol、3mol,物质的量变化比等于系数比;(2)①体系的压强比等于物质的量比;②转化率=变化量÷初始量×100%;(3)根据化学平衡的定义判断;【详解】(1)由图可知,C是反应物,物质的量减少2mol,A、B生成物,物质的量分别增加1mol 、3mol,物质的量变化比等于系数比,所以该反应的化学方程式为:2C A+3B;(2)①体系的压强比等于物质的量比,反应前气体总物质的量是7mol、反应后气体总物质的量是9mol,所以此时体系的压强是开始时的97倍;②转化率=变化量÷初始量×100%=2÷3×100%=66.7%;(3)a.根据图象,到达10min时反应达到平衡状态,正逆反应速率相等但不为0,反应没有停止,故a错误;b.在到达10min之前,C的物质的量减少,所以 C气体的消耗速率大于它的生成速率,故b 正确;c.在10min时反应达到平衡状态,所以B气体的正反应速率等于逆反应速率,故c正确;选bc。
高考化学易错题专题复习-化学反应的速率与限度练习题含答案
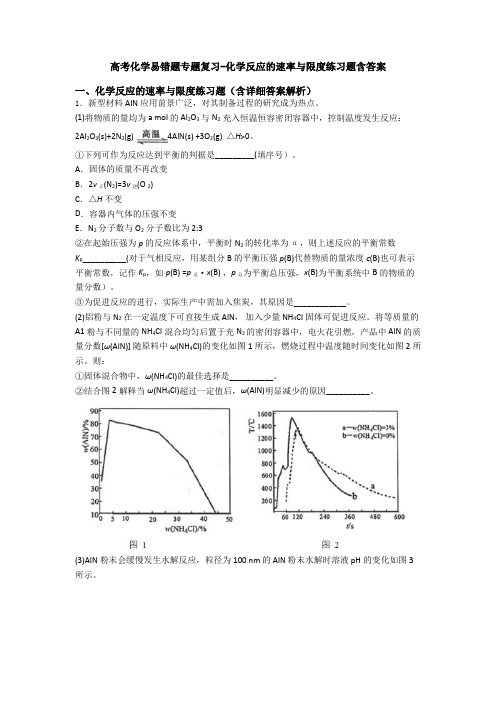
高考化学易错题专题复习-化学反应的速率与限度练习题含答案一、化学反应的速率与限度练习题(含详细答案解析)1.新型材料 AIN 应用前景广泛,对其制备过程的研究成为热点。
(1)将物质的量均为a mol 的 Al2O3与N2充入恒温恒容密闭容器中,控制温度发生反应:2Al2O3(s)+2N2(g) 4AlN(s) +3O2(g) △H>0。
①下列可作为反应达到平衡的判据是_________(填序号)。
A.固体的质量不再改变B.2v正(N2)=3v逆(O 2)C.△H不变D.容器内气体的压强不变E.N2分子数与 O2分子数比为 2:3②在起始压强为p的反应体系中,平衡时 N2的转化率为α,则上述反应的平衡常数K p__________(对于气相反应,用某组分 B 的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作K p,如p(B) =p总·x(B) ,p总为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
③为促进反应的进行,实际生产中需加入焦炭,其原因是____________。
(2)铝粉与 N2在一定温度下可直接生成 AlN,加入少量 NH4Cl 固体可促进反应。
将等质量的A1粉与不同量的 NH4Cl混合均匀后置于充 N2的密闭容器中,电火花引燃,产品中 AlN的质量分数[ω(AlN)] 随原料中ω(NH4Cl)的变化如图1所示,燃烧过程中温度随时间变化如图2所示。
则:①固体混合物中,ω(NH4Cl)的最佳选择是__________。
②结合图2解释当ω(NH4Cl)超过一定值后,ω(AlN)明显减少的原因__________。
(3)AIN粉末会缓慢发生水解反应,粒径为100 nm 的 AlN 粉末水解时溶液 pH的变化如图3 所示。
①AlN 粉末水解的化学方程式是______________。
②相同条件下,请在图3中画出粒径为40 nm 的AlN粉末水解的变化曲线____________。
备战高考化学复习化学反应的速率与限度专项易错题附答案解析
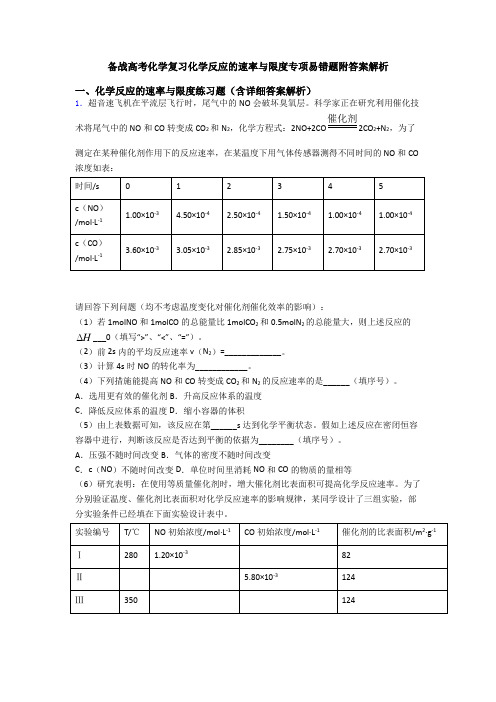
备战高考化学复习化学反应的速率与限度专项易错题附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。
科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式:2NO+2CO 催化剂2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO 浓度如表:请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):(1)若1molNO和1molCO的总能量比1molCO2和0.5molN2的总能量大,则上述反应的H___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)计算4s时NO的转化率为____________。
(4)下列措施能提高NO和CO转变成CO2和N2的反应速率的是______(填序号)。
A.选用更有效的催化剂B.升高反应体系的温度C.降低反应体系的温度D.缩小容器的体积(5)由上表数据可知,该反应在第______s达到化学平衡状态。
假如上述反应在密闭恒容容器中进行,判断该反应是否达到平衡的依据为________(填序号)。
A.压强不随时间改变B.气体的密度不随时间改变C.c(NO)不随时间改变D.单位时间里消耗NO和CO的物质的量相等(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。
为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在上表格中填入剩余的实验条件数据_____、_____、______、______、______。
②请在给出的坐标图中,画出上表中的Ⅰ、Ⅱ两个实验条件下混合气体中NO 浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________。
【答案】< 1.875⨯10-4mol ·L -1·s -1 90% ABD 4 AC 5.80⨯10-3 280 1.20⨯10-31.20⨯10-3 5.80⨯10-3【解析】【分析】反应热的正负可根据反应物和生成物的总能量的大小比较;能提高反应速率的因素主要有增大浓度、使用催化剂、升高温度、增大表面积、构成原电池等,压强能否改变反应速率要看是否改变了浓度;反应是否达到平衡可以从速率(正逆反应速率是否相等)、量(是否保持不变)、压强、气体平均密度,气体平均摩尔质量、颜色等方面判断;验证多个因素对化学反应速率的影响规律,要控制变量做对比实验,每组对比实验只能有一个变量。
精选高考化学易错题专题复习化学反应的速率与限度附答案解析

精选高考化学易错题专题复习化学反应的速率与限度附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:t/s050150250350n(NH3)00.240.360.400.400~50s内的平均反应速率v(N2)=_________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。
N N≡的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1mol NH3过程中___(填“吸收”或“放出”)的能量为____,反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)为加快反应速率,可以采取的措施是_______a.降低温度b.增大压强c.恒容时充入He气d.恒压时充入He气e.及时分离NH3【答案】3X+Y⇌2Z 1.2×10−3mol/(L·s) 放出 46kJ 18.4 b【解析】【分析】(1)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;(2)根据=ct∆∆计算;(3)形成化学键放出能量,断裂化合价吸收能量;(4)根据影响反应速率的因素分析;【详解】(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为3X+Y⇌2Z;(2)0~50s内,NH3物质的量变化为0.24mol,根据方程式可知,N2物质的量变化为0.12mol,(Z)=ct∆∆=0.12mol=2L50s⨯1.2×10−3mol/(L·s);(3)断裂1mol N N≡吸收946kJ的能量,断裂1mol H-H键吸能量436kJ,形成1mo N-H 键放出能量391kJ,根据方程式3H2+N2⇌2NH3,生成2mol氨气,断键吸收的能量是946kJ+ 436kJ×3=2254 kJ,成键放出的能量是391kJ×6=2346 kJ,则生成1mol NH3过程中放出的能量为2346 kJ-2254 kJ2=46kJ;反应达到(2)中的平衡状态时生成0.4mol氨气,所以放出的能量是46kJ×0.4=18.4kJ;(4) a.降低温度,反应速率减慢,故不选a;b.增大压强,体积减小浓度增大,反应速率加快,故选b;c.恒容时充入He气,反应物浓度不变,反应速率不变,故不选c;d.恒压时充入He气,容器体积增大,反应物浓度减小,反应速率减慢,故不选d;e.及时分离NH3,浓度减小,反应速率减慢,故不选e。
高考化学易错题精选-化学反应的速率与限度练习题及答案解析

高考化学易错题精选-化学反应的速率与限度练习题及答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH 2COONH4(s)2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___(填选项);A.2v生(NH3)=v耗(CO2)B.密闭容器中氨气的物质的量不变C.容器中CO2与NH3的物质的量之比保持不变D.密闭容器中总压强保持不变E.形成6个N-H键的同时有2个C=O键断裂(2)能使该反应的反应速率增大的是___(填选项);A.及时分离出CO2气体B.适当升高温度C.加入少量NH2COONH4(s)D.选择高效催化剂(3)如图所示,上述反应中断开反应物中化学键吸收的能量___形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【答案】AC BD 大于【解析】【分析】(1)根据化学平衡状态的特征解答;(2)增大浓度或升高温度或加催化剂可加快反应速率来解答;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,结合化学键分析解答。
【详解】(1)A.平衡时应有v生(NH3)=2v耗(CO2),所以2v生(NH3)=v耗(CO2)时,反应没有达到平衡状态,故A错误;B.密闭容器中氨气的物质的量不变,说明正、逆反应速率相等,可以判定反应达到平衡状态,故B正确;C.只要反应发生,容器中CO2与NH3的物质的量之比就是2:1,始终保持不变,不能判定反应是否达平衡状态,故C错误;D.密闭容器中总压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故D正确;E.形成6个N-H键等效于2个C=O键形成的同时有2个C=O键断裂,正、逆反应速率相等,达平衡状态,故E正确;故答案为AC;(2)A.及时分离出CO2气体,生成物浓度减小,反应速率减小,故A错误;B.适当升高温度,反应速率加快,故B正确;C.加入少量NH2COONH4(s),固体物质量变但浓度不变,故C错误;D.选择高效催化剂,反应速率加快,故D正确;故答案为:BD;(3)由图可知反应物的总能量低于生成物的总能量,所以反应是吸热反应,即反应中断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量。
精选高考化学易错题专题复习化学反应的速率与限度附答案解析

精选高考化学易错题专题复习化学反应的速率与限度附答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.某温度下在2L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。
(1)该反应的化学方程式是________________________(2)若A、B、C均为气体,10min后反应达到平衡,①此时体系的压强是开始时的________倍。
②在该条件达到平衡时反应物的转化率为________%(计算结果保留1位小数)(3)关于该反应的说法正确的是_________。
a.到达10min时停止反应b.在到达10min之前C气体的消耗速率大于它的生成速率c.在10min时B气体的正反应速率等于逆反应速率【答案】2C A+3B 97或1.29或1.3 66.7% b、c【解析】【分析】(1)由图可知,C是反应物,物质的量分别减少2mol,A、B生成物,物质的量增加1mol、3mol,物质的量变化比等于系数比;(2)①体系的压强比等于物质的量比;②转化率=变化量÷初始量×100%;(3)根据化学平衡的定义判断;【详解】(1)由图可知,C是反应物,物质的量减少2mol,A、B生成物,物质的量分别增加1mol 、3mol,物质的量变化比等于系数比,所以该反应的化学方程式为:2C A+3B;(2)①体系的压强比等于物质的量比,反应前气体总物质的量是7mol、反应后气体总物质的量是9mol,所以此时体系的压强是开始时的97倍;②转化率=变化量÷初始量×100%=2÷3×100%=66.7%;(3)a.根据图象,到达10min时反应达到平衡状态,正逆反应速率相等但不为0,反应没有停止,故a错误;b.在到达10min之前,C的物质的量减少,所以 C气体的消耗速率大于它的生成速率,故b 正确;c.在10min时反应达到平衡状态,所以B气体的正反应速率等于逆反应速率,故c正确;选bc。
高考化学化学反应的速率与限度(大题培优易错难题)

高考化学化学反应的速率与限度(大题培优易错难题)高考化学化学反应的速率与限度(大题培优易错难题)一、化学反应的速率与限度练习题(含详细答案解析)1.某实验小组为确定过氧化氢分解的最佳催化条件,用如图实验装置进行实验,反应物用量和反应停止的时间数据如下:分析表中数据回答下列问题:MnO2时间0.1g0.3g0.8gH2O210mL1.5%223s67s56s10mL3.0%308s109s98s10mL4.5%395s149s116s(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而________。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________,理由是__________________________________。
(4)为加快过氧化氢的分解速率,除了使用MnO2作催化剂和改变过氧化氢的质量分数之外,还可以采取的加快反应速率的措施有_____。
(回答任意两个合理的措施)【答案】加快 0.3 不正确 H2O2的浓度扩大二倍(从1.5%→3.0%),但反应所需时间比其二倍小的多升高温度;粉碎二氧化锰,增大其表面积。
【解析】【分析】由题可知,该实验研究浓度和催化剂对反应速率的影响,通过表中数据可分析得出浓度和催化剂对反应速率的影响规律,因为该实验不是直接测出反应速率,而是测出反应停止的时间,要考虑反应物增多对反应时间的影响。
【详解】(1)由表格中的数据可知:相同浓度的H2O2,加入的MnO2越多,反应所用的时间越短,即分解速率越快。
(2)用0.1 g催化剂的反应速率明显小于用0.3 g和0.8 g催化剂的反应速率;用0.8 g催化剂和用0.3 g催化剂的反应速率及反应时间相差不多,但用0.3 g催化剂节约药品。
高考化学复习化学反应的速率与限度专项易错题附详细答案

高考化学复习化学反应的速率与限度专项易错题附详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:t/s050150250350n(NH3)00.240.360.400.400~50s内的平均反应速率v(N2)=_________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。
N N≡的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1mol NH3过程中___(填“吸收”或“放出”)的能量为____,反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)为加快反应速率,可以采取的措施是_______a.降低温度b.增大压强c.恒容时充入He气d.恒压时充入He气e.及时分离NH3【答案】3X+Y⇌2Z 1.2×10−3mol/(L·s) 放出 46kJ 18.4 b【解析】【分析】(1)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;(2)根据=ct∆∆计算;(3)形成化学键放出能量,断裂化合价吸收能量;(4)根据影响反应速率的因素分析;【详解】(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为3X+Y⇌2Z;(2)0~50s内,NH3物质的量变化为0.24mol,根据方程式可知,N2物质的量变化为0.12mol,(Z)=ct∆∆=0.12mol=2L50s⨯1.2×10−3mol/(L·s);(3)断裂1mol N N≡吸收946kJ的能量,断裂1mol H-H键吸能量436kJ,形成1mo N-H 键放出能量391kJ,根据方程式3H2+N2⇌2NH3,生成2mol氨气,断键吸收的能量是946kJ+ 436kJ×3=2254 kJ,成键放出的能量是391kJ×6=2346 kJ,则生成1mol NH3过程中放出的能量为2346 kJ-2254 kJ2=46kJ;反应达到(2)中的平衡状态时生成0.4mol氨气,所以放出的能量是46kJ×0.4=18.4kJ;(4) a.降低温度,反应速率减慢,故不选a;b.增大压强,体积减小浓度增大,反应速率加快,故选b;c.恒容时充入He气,反应物浓度不变,反应速率不变,故不选c;d.恒压时充入He气,容器体积增大,反应物浓度减小,反应速率减慢,故不选d;e.及时分离NH3,浓度减小,反应速率减慢,故不选e。
高考化学易错题专题训练-化学反应的速率与限度练习题附详细答案

高考化学易错题专题训练-化学反应的速率与限度练习题附详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。
一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):实验序号A溶液B溶液①20 mL 0.1 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液②20 mL 0.2 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液(1)该反应的离子方程式___________________________。
(已知H2C2O4是二元弱酸)(2)该实验探究的是_____________因素对化学反应速率的影响。
相同时间内针筒中所得CO2的体积大小关系是_________________<_____________(填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50mL)(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________来比较化学反应速率。
(一条即可)(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:①__________________________;②__________________________。
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 浓度①② 0.0056 KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间该反应放热产物Mn2+是反应的催化剂【解析】【详解】(1)高锰酸钾溶液具有强氧化性,把草酸氧化成CO2,根据化合价升降法进行配平,其离子反应方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;(2)对比表格数据可知,草酸的浓度不一样,因此是探究浓度对化学反应速率的影响,浓度越大,反应速率越快,则①<②;(3)根据反应方程式并结合CO2的体积,求出消耗的n(KMnO4)= 2×10-5mol,剩余n(KMnO4)=(30×10-3×0.01-2×10-5)mol=2.8×10-4mol,c(KMnO4)=2.8×10-4mol÷50×10-3L=0.0056mol·L-1;(4)除通过测定一定时间内CO2的体积来比较反应速率,还可以通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(5)t1~t2时间内速率变快的主要原因可能是:①此反应是放热反应,温度升高,虽然反应物的浓度降低,但温度起决定作用;②可能产生的Mn2+是反应的催化剂,加快反应速率。
高考化学复习化学反应的速率与限度专项易错题含答案解析

高考化学复习化学反应的速率与限度专项易错题含答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.现代工业的发展导致CO 2的大量排放,对环境造成的影响日益严重,通过各国科技工作者的努力,已经开发出许多将CO 2回收利用的技术,其中催化转化法最具应用价值。
回答下列问题:(1)在催化转化法回收利用CO 2的过程中,可能涉及以下化学反应:①CO 2(g)+2H 2O(1)垐?噲?CH 3OH(1)+32O 2(g) △H =+727kJ·mol -1 △G =+703kJ·mol -1 ②CO 2(g)+2H 2O(1)垐?噲?CH 4(g)+2O 2(g) △H =+890kJ ·mol -1 △G =+818kJ ·mol -1 ③CO 2(g)+3H 2(g)垐?噲?CH 3OH(1)+H 2O(1) △H =-131kJ·mol -1 △G =-9.35kJ·mol -1 ④CO 2(g)+4H 2(g)垐?噲?CH 4(g)+2H 2O(1) △H =-253kJ ·mol -1 △G =-130kJ ·mol -1从化学平衡的角度来看,上述化学反应中反应进行程度最小的是____,反应进行程度最大的是_____。
(2)反应CO 2(g)+4H 2(g)=CH 4(g) +2H 2O(g)称为Sabatier 反应,可用于载人航空航天工业。
我国化学工作者对该反应的催化剂及催化效率进行了深入的研究。
①在载人航天器中利用Sabatier 反应实现回收CO 2再生O 2,其反应过程如图所示,这种方法再生O 2的最大缺点是需要不断补充_________(填化学式)。
②在1.5 MPa ,气体流速为20 mL ·min -l 时研究温度对催化剂催化性能的影响,得到CO 2的转化率(%)如下:分析上表数据可知:_____(填化学式)的催化性能更好。
高考化学易错题专题复习-化学反应的速率与限度练习题附详细答案

高考化学易错题专题复习-化学反应的速率与限度练习题附详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.化学反应速率与限度与生产、生活密切相关(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):时间(min)12345氢气体积(mL)(标准状况)100240688810860①反应速率最大的时间段是____________(填0~1、1~2、2~3、3~4、4~5)min,原因是____________。
②在2~3min时间段以盐酸的浓度变化来表示的反应速率为____________。
(设溶液体积不变)(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列____________以减慢反应速率。
(填写代号)A.冰块B.HNO3溶液C.CuSO4溶液(3)C同学为了探究Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
可通过观察___________________________现象,定性比较得出结论。
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________,【答案】2~3 因该反应放热,随着反应,溶液温度升高,故反应速率加快 0.2mol·L-1·min-1 A 反应产生气泡的快慢控制阴离子相同,排除阴离子的干扰【解析】【分析】(1)单位时间内生成氢气的体积越大反应速率越快;锌与盐酸反应放热;②2~3min生成氢气的体积是448mL(标准状况),物质的量是0.448L0.02mol 22.4L/mol,消耗盐酸的物质的量0.4mol;(2)根据影响反应速率的因素分析;(3)双氧水分解有气泡产生;根据控制变量法,探究Fe3+和Cu2+对H2O2分解,控制阴离子相同;【详解】(1)根据表格数据,2 min~3min收集的氢气最多,反应速率最大的时间段是2~3min;锌与盐酸反应放热,随着反应,溶液温度升高,故反应速率加快;②2~3min生成氢气的体积是448mL(标准状况),物质的量是0.448L0.02mol 22.4L/mol=,消耗盐酸的物质的量0.04mol,0.04mol0.2L1minv÷==0.2mol·L-1·min-1;(2)A.加入冰块,温度降低,反应速率减慢,故选A;B.加入HNO3溶液,硝酸与锌反应不能生成氢气,故不选B;C.加入CuSO4溶液,锌置换出铜,构成原电池,反应速率加快,故不选C;(3)双氧水分解有气泡产生,可通过观察反应产生气泡的快慢,定性比较催化效果;根据控制变量法,探究Fe3+和Cu2+对H2O2分解,控制阴离子相同,排除阴离子的干扰,所以FeCl3改为Fe2(SO4)3更为合理。
高考化学易错题精选-化学反应的速率与限度练习题含答案解析

高考化学易错题精选-化学反应的速率与限度练习题含答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.某温度下在2L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。
(1)该反应的化学方程式是________________________(2)若A、B、C均为气体,10min后反应达到平衡,①此时体系的压强是开始时的________倍。
②在该条件达到平衡时反应物的转化率为________%(计算结果保留1位小数)(3)关于该反应的说法正确的是_________。
a.到达10min时停止反应b.在到达10min之前C气体的消耗速率大于它的生成速率c.在10min时B气体的正反应速率等于逆反应速率【答案】2C A+3B 97或1.29或1.3 66.7% b、c【解析】【分析】(1)由图可知,C是反应物,物质的量分别减少2mol,A、B生成物,物质的量增加1mol、3mol,物质的量变化比等于系数比;(2)①体系的压强比等于物质的量比;②转化率=变化量÷初始量×100%;(3)根据化学平衡的定义判断;【详解】(1)由图可知,C是反应物,物质的量减少2mol,A、B生成物,物质的量分别增加1mol 、3mol,物质的量变化比等于系数比,所以该反应的化学方程式为:2C A+3B;(2)①体系的压强比等于物质的量比,反应前气体总物质的量是7mol、反应后气体总物质的量是9mol,所以此时体系的压强是开始时的97倍;②转化率=变化量÷初始量×100%=2÷3×100%=66.7%;(3)a.根据图象,到达10min时反应达到平衡状态,正逆反应速率相等但不为0,反应没有停止,故a错误;b.在到达10min之前,C的物质的量减少,所以 C气体的消耗速率大于它的生成速率,故b 正确;c.在10min时反应达到平衡状态,所以B气体的正反应速率等于逆反应速率,故c正确;选bc。
高考化学化学反应的速率与限度(大题培优 易错 难题)附详细答案

高考化学化学反应的速率与限度(大题培优易错难题)附详细答案一、化学反应的速率与限度练习题(含详细答案解析)1.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:(1)写出该反应的化学方程式_________________________。
(2)计算反应开始到10s,用X表示的反应速率是___________。
(3)下列叙述中能说明上述反应达到平衡状态的是_________。
a.当X与Y的反应速率之比为1:1b.混合气体中X的浓度保持不变c.X、Y、Z的浓度之比为1:1:2(4)为使该反应的反应速率增大,可采取的措施是_______。
a.适当降低温度b.扩大容器的体积c.充入一定量Z【答案】X+Y垐?噲?2Z 0.0395mol·L-1·s-1 b c【解析】【分析】由图表可知,随反应进行X、Y的物质的量减小,Z的物质的量增大,所以X、Y是反应物,Z是生产物,l0s后X、Y、Z的物质的量为定值,不为0,即10s达到平衡状态,反应是可逆反应,且△n(X):△n(Y):△n(Z)=(1.20-0.41)mol:(1.00-0.21)mol:1.58mol=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比,故反应化学方程式为X(g)+Y(g)⇌2Z(g),然后结合v=ctVV及平衡的特征“等、定”及速率之比等于化学计量数之比来解答。
【详解】(1)由上述分析可知,该反应的化学方程式为X(g)+Y(g)⇌2Z(g);(2)反应开始到10s,用X表示的反应速率是1.20mol0.41mol210Ls=0.0395mol•(L•s)-1;(3)a.随着反应的进行,X与Y的反应速率之比始终为1:1,则不能判断是平衡状态,故a 错误;b.混合气体中X的浓度保持不变,符合平衡特征“定”,为平衡状态,故b正确;c.X、Y、Z的浓度之比为1:1:2,与起始量、转化率有关,不能判断是平衡状态,故c错误;故答案为b;(4)a.适当降低温度,反应速率减小,故a错误;b.扩大容器的体积,浓度减小,反应速率减小,故b错误;c.充入一定量Z,浓度增大,反应速率加快,故c选;故答案为c。
高考化学复习化学反应的速率与限度专项易错题附答案

高考化学复习化学反应的速率与限度专项易错题附答案一、化学反应的速率与限度练习题(含详细答案解析)1.某实验小组为确定过氧化氢分解的最佳催化条件,用如图实验装置进行实验,反应物用量和反应停止的时间数据如下:分析表中数据回答下列问题:MnO2时间0.1g0.3g0.8gH2O210mL1.5%223s67s56s10mL3.0%308s109s98s10mL4.5%395s149s116s(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而________。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________,理由是__________________________________。
(4)为加快过氧化氢的分解速率,除了使用MnO2作催化剂和改变过氧化氢的质量分数之外,还可以采取的加快反应速率的措施有_____。
(回答任意两个合理的措施)【答案】加快 0.3 不正确 H2O2的浓度扩大二倍(从1.5%→3.0%),但反应所需时间比其二倍小的多升高温度;粉碎二氧化锰,增大其表面积。
【解析】【分析】由题可知,该实验研究浓度和催化剂对反应速率的影响,通过表中数据可分析得出浓度和催化剂对反应速率的影响规律,因为该实验不是直接测出反应速率,而是测出反应停止的时间,要考虑反应物增多对反应时间的影响。
【详解】(1)由表格中的数据可知:相同浓度的H2O2,加入的MnO2越多,反应所用的时间越短,即分解速率越快。
(2)用0.1 g催化剂的反应速率明显小于用0.3 g和0.8 g催化剂的反应速率;用0.8 g催化剂和用0.3 g催化剂的反应速率及反应时间相差不多,但用0.3 g催化剂节约药品。
(3)从表中数据可知,相同体积3.0%的双氧水中的溶质含量是1.5%的双氧水中溶质含量的二倍,但反应的时间却比其反应时间的二倍小得多,由反应速率计算公式可得出,此实验条件下双氧水的浓度越大分解速率越快,由此得出上述结论不正确;(4)加快反应速率的措施常见的有:增加反应物浓度、适当升高温度、增加反应物表面积(接触面积)、使用催化剂等。
精选高考化学易错题专题复习化学反应的速率与限度含答案

精选高考化学易错题专题复习化学反应的速率与限度含答案一、化学反应的速率与限度练习题(含详细答案解析)1.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。
一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):实验序号A溶液B溶液①20 mL 0.1 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液②20 mL 0.2 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液(1)该反应的离子方程式___________________________。
(已知H2C2O4是二元弱酸)(2)该实验探究的是_____________因素对化学反应速率的影响。
相同时间内针筒中所得CO2的体积大小关系是_________________<_____________(填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50mL)(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________来比较化学反应速率。
(一条即可)(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:①__________________________;②__________________________。
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 浓度①② 0.0056 KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间该反应放热产物Mn2+是反应的催化剂【解析】【详解】(1)高锰酸钾溶液具有强氧化性,把草酸氧化成CO2,根据化合价升降法进行配平,其离子反应方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;(2)对比表格数据可知,草酸的浓度不一样,因此是探究浓度对化学反应速率的影响,浓度越大,反应速率越快,则①<②;(3)根据反应方程式并结合CO2的体积,求出消耗的n(KMnO4)= 2×10-5mol,剩余n(KMnO4)=(30×10-3×0.01-2×10-5)mol=2.8×10-4mol,c(KMnO4)=2.8×10-4mol÷50×10-3L=0.0056mol·L-1;(4)除通过测定一定时间内CO2的体积来比较反应速率,还可以通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(5)t1~t2时间内速率变快的主要原因可能是:①此反应是放热反应,温度升高,虽然反应物的浓度降低,但温度起决定作用;②可能产生的Mn2+是反应的催化剂,加快反应速率。
高考化学知识点过关培优 易错 难题训练∶化学反应的速率与限度附答案

高考化学知识点过关培优易错难题训练∶化学反应的速率与限度附答案一、化学反应的速率与限度练习题(含详细答案解析)1.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:t℃70080083010001200K0.60.9 1.0 1.7 2.6回答下列问题:(1)该反应化学平衡常数的表达式:K=___;(2)该反应为___(填“吸热”或“放热”)反应;(3)下列说法中能说明该反应达平衡状态的是___;A.容器中压强不变B.混合气体中c(CO)不变C.混合气体的密度不变D.c(CO)=c(CO2)E.化学平衡常数K不变F.单位时间内生成CO的分子数与生成H2O的分子数相等(4)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为___。
【答案】()()()()222CO H OCO Hc cc c吸热 BE 830℃【解析】【分析】(1)化学平衡常数等于生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;(2)随温度升高,平衡常数增大,说明升高温度平衡正向移动;(3)根据平衡标志判断;(4)某温度下, c(CO2)×c(H2)=c(CO)×c(H2O),即K=()() ()()222CO H OCO Hc cc c= 1;【详解】(1)根据平衡常数的定义,该反应化学平衡常数的表达式K=()() ()()222 CO H OCO H c cc c(2)随温度升高,平衡常数增大,说明升高温度平衡正向移动,所以正反应为吸热反应;(3)A. CO2(g)+H2(g)CO(g)+H2O(g)反应前后气体系数和相等,容器中压强是恒量,压强不变,不一定平衡,故不选A;B. 根据化学平衡定义,浓度不变一定平衡,所以混合气体中c(CO)不变一定达到平衡状态,故选B;C. 反应前后气体质量不变、容器体积不变,根据=m Vρ,混合气体的密度是恒量,混合气体的密度不变,反应不一定平衡,故不选C;D. 反应达到平衡时,浓度不再改变,c(CO)=c(CO2)不能判断浓度是否改变,所以反应不一定平衡,故不选D;E. 正反应吸热,温度是变量,平衡常数只与温度有关,化学平衡常数K不变,说明温度不变,反应一定达到平衡状态,故选E;F.单位时间内生成CO的分子数与生成H2O的分子数相等,不能判断正逆反应速率是否相等,反应不一定平衡,故不选F;(4)某温度下, c(CO2)×c(H2)=c(CO)×c(H2O),即K =()()()()222CO H OCO Hc cc c=1,根据表格数据,此时的温度为830℃。
高考化学复习化学反应的速率与限度专项易错题及答案
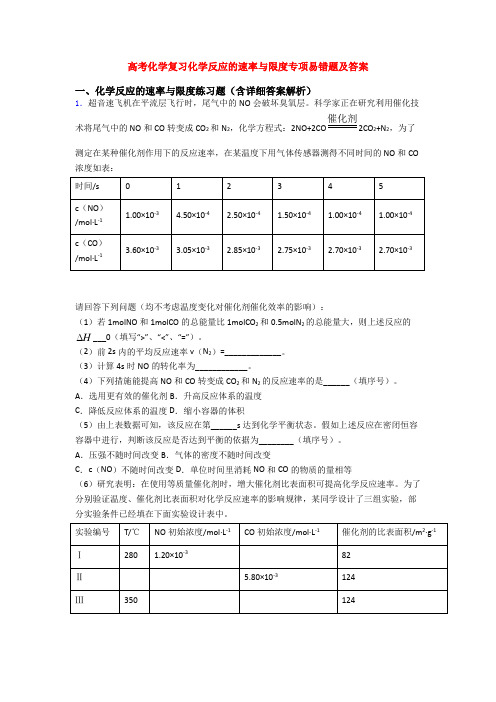
高考化学复习化学反应的速率与限度专项易错题及答案一、化学反应的速率与限度练习题(含详细答案解析)1.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。
科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式:2NO+2CO 催化剂2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO 浓度如表:请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):(1)若1molNO和1molCO的总能量比1molCO2和0.5molN2的总能量大,则上述反应的H___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)计算4s时NO的转化率为____________。
(4)下列措施能提高NO和CO转变成CO2和N2的反应速率的是______(填序号)。
A.选用更有效的催化剂B.升高反应体系的温度C.降低反应体系的温度D.缩小容器的体积(5)由上表数据可知,该反应在第______s达到化学平衡状态。
假如上述反应在密闭恒容容器中进行,判断该反应是否达到平衡的依据为________(填序号)。
A.压强不随时间改变B.气体的密度不随时间改变C.c(NO)不随时间改变D.单位时间里消耗NO和CO的物质的量相等(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。
为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在上表格中填入剩余的实验条件数据_____、_____、______、______、______。
②请在给出的坐标图中,画出上表中的Ⅰ、Ⅱ两个实验条件下混合气体中NO 浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________。
【答案】< 1.875⨯10-4mol ·L -1·s -1 90% ABD 4 AC 5.80⨯10-3 280 1.20⨯10-31.20⨯10-3 5.80⨯10-3【解析】 【分析】反应热的正负可根据反应物和生成物的总能量的大小比较;能提高反应速率的因素主要有增大浓度、使用催化剂、升高温度、增大表面积、构成原电池等,压强能否改变反应速率要看是否改变了浓度;反应是否达到平衡可以从速率(正逆反应速率是否相等)、量(是否保持不变)、压强、气体平均密度,气体平均摩尔质量、颜色等方面判断;验证多个因素对化学反应速率的影响规律,要控制变量做对比实验,每组对比实验只能有一个变量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学易错题专题训练-化学反应的速率与限度练习题及答案解析一、化学反应的速率与限度练习题(含详细答案解析)1.化学反应速率与限度与生产、生活密切相关(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):时间(min)12345氢气体积(mL)(标准状况)100240688810860①反应速率最大的时间段是____________(填0~1、1~2、2~3、3~4、4~5)min,原因是____________。
②在2~3min时间段以盐酸的浓度变化来表示的反应速率为____________。
(设溶液体积不变)(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列____________以减慢反应速率。
(填写代号)A.冰块B.HNO3溶液C.CuSO4溶液(3)C同学为了探究Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
可通过观察___________________________现象,定性比较得出结论。
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________,【答案】2~3 因该反应放热,随着反应,溶液温度升高,故反应速率加快 0.2mol·L-1·min-1 A 反应产生气泡的快慢控制阴离子相同,排除阴离子的干扰【解析】【分析】(1)单位时间内生成氢气的体积越大反应速率越快;锌与盐酸反应放热;②2~3min生成氢气的体积是448mL(标准状况),物质的量是0.448L0.02mol 22.4L/mol,消耗盐酸的物质的量0.4mol;(2)根据影响反应速率的因素分析;(3)双氧水分解有气泡产生;根据控制变量法,探究Fe3+和Cu2+对H2O2分解,控制阴离子相同;【详解】(1)根据表格数据,2 min~3min收集的氢气最多,反应速率最大的时间段是2~3min;锌与盐酸反应放热,随着反应,溶液温度升高,故反应速率加快;②2~3min生成氢气的体积是448mL(标准状况),物质的量是0.448L0.02mol 22.4L/mol=,消耗盐酸的物质的量0.04mol,0.04mol0.2L1minv÷==0.2mol·L-1·min-1;(2)A.加入冰块,温度降低,反应速率减慢,故选A;B.加入HNO3溶液,硝酸与锌反应不能生成氢气,故不选B;C.加入CuSO4溶液,锌置换出铜,构成原电池,反应速率加快,故不选C;(3)双氧水分解有气泡产生,可通过观察反应产生气泡的快慢,定性比较催化效果;根据控制变量法,探究Fe3+和Cu2+对H2O2分解,控制阴离子相同,排除阴离子的干扰,所以FeCl3改为Fe2(SO4)3更为合理。
【点睛】本题主要考查化学反应速率的影响因素,明确影响反应速率的因素是解题关键,注意控制变量法在探究影响化学反应速率因素实验中的应用,理解原电池原理对化学反应速率的影响。
2.某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:t/s050150250350n(NH3)00.240.360.400.400~50s内的平均反应速率v(N2)=_________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。
N N≡的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1mol NH3过程中___(填“吸收”或“放出”)的能量为____,反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)为加快反应速率,可以采取的措施是_______a.降低温度b.增大压强c.恒容时充入He气d.恒压时充入He气e.及时分离NH3【答案】3X+Y⇌2Z 1.2×10−3mol/(L·s) 放出 46kJ 18.4 b【解析】【分析】(1)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;(2)根据=ct∆∆计算;(3)形成化学键放出能量,断裂化合价吸收能量;(4)根据影响反应速率的因素分析;【详解】(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为3X+Y⇌2Z;(2)0~50s内,NH3物质的量变化为0.24mol,根据方程式可知,N2物质的量变化为0.12mol,(Z)=ct∆∆=0.12mol=2L50s⨯1.2×10−3mol/(L·s);(3)断裂1mol N N≡吸收946kJ的能量,断裂1mol H-H键吸能量436kJ,形成1mo N-H 键放出能量391kJ,根据方程式3H2+N2⇌2NH3,生成2mol氨气,断键吸收的能量是946kJ+ 436kJ×3=2254 kJ,成键放出的能量是391kJ×6=2346 kJ,则生成1mol NH3过程中放出的能量为2346 kJ-2254 kJ2=46kJ;反应达到(2)中的平衡状态时生成0.4mol氨气,所以放出的能量是46kJ×0.4=18.4kJ;(4) a.降低温度,反应速率减慢,故不选a;b.增大压强,体积减小浓度增大,反应速率加快,故选b;c.恒容时充入He气,反应物浓度不变,反应速率不变,故不选c;d.恒压时充入He气,容器体积增大,反应物浓度减小,反应速率减慢,故不选d;e.及时分离NH3,浓度减小,反应速率减慢,故不选e。
【点睛】本题考查化学平衡图象分析,根据键能计算反应热,影响化学反应速率的因素,注意压强对反应速率的影响是通过改变浓度实现的,若改变了压强而浓度不变,则反应速率不变。
3.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。
一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):实验序号A溶液B溶液①20 mL 0.1 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液②20 mL 0.2 mol·L-1H2C2O4溶液30 mL 0.01 mol·L-1KMnO4溶液(1)该反应的离子方程式___________________________。
(已知H2C2O4是二元弱酸)(2)该实验探究的是_____________因素对化学反应速率的影响。
相同时间内针筒中所得CO2的体积大小关系是_________________<_____________(填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50mL)(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________来比较化学反应速率。
(一条即可)(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:①__________________________;②__________________________。
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 浓度①② 0.0056 KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间该反应放热产物Mn2+是反应的催化剂【解析】【详解】(1)高锰酸钾溶液具有强氧化性,把草酸氧化成CO2,根据化合价升降法进行配平,其离子反应方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;(2)对比表格数据可知,草酸的浓度不一样,因此是探究浓度对化学反应速率的影响,浓度越大,反应速率越快,则①<②;(3)根据反应方程式并结合CO2的体积,求出消耗的n(KMnO4)= 2×10-5mol,剩余n(KMnO4)=(30×10-3×0.01-2×10-5)mol=2.8×10-4mol,c(KMnO4)=2.8×10-4mol÷50×10-3L=0.0056mol·L-1;(4)除通过测定一定时间内CO2的体积来比较反应速率,还可以通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率;(5)t1~t2时间内速率变快的主要原因可能是:①此反应是放热反应,温度升高,虽然反应物的浓度降低,但温度起决定作用;②可能产生的Mn2+是反应的催化剂,加快反应速率。
4.在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:时间/s012345n(NO)/mol0.0200.0100.0080.0070.0070.007(1)写出该反应的平衡常数表达式:K=________,已知:K(300℃)>K(350℃),该反应是________反应(填“放热”或“吸热”)。
(2)下图中表示NO2的变化的曲线是___,用O2的浓度变化表示从0~2s内该反应的平均速率v=__________。
(3)能说明该反应已经达到平衡状态的是(______)。
a.v(NO2)=2v(O2) b.容器内压强保持不变c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是(______)。
a.及时分离出NO2气体b.适当升高温度c.增大O2的浓度d.选择高效的催化剂【答案】c2(NO2)/c2(NO)c(O2)放热 b 1.5×10-3mol·L-1·s-1 bc c【解析】【分析】【详解】(1) 2NO(g)+O2(g)2NO2(g)反应的平衡常数K=c2(NO2)/[c2(NO)·c(O2)],因为升温平衡向吸热反应方向进行,已知:K(300℃)>K(350℃),温度越高平衡常数越小,升温平衡逆向进行,则该正反应为放热反应。
