合成氨生产常用的原料有哪些
合成氨工艺简介

合成氨工艺简介工艺危险特点:1 高温、高压使可燃气体爆炸极限扩宽,气体物料一旦过氧(亦称透氧),极易在设备和管道内发生爆炸。
2 高温、高压气体物料从设备管线泄露时会迅速膨胀与空气混合形成爆炸性混合物,遇到明火或因郜流速物料与裂(喷)口处摩擦产生静电火花引起着火和空间爆炸。
3 气体压缩机等转动设备在高温下运行会使润滑油挥发裂解,在附近管道内造成积炭,可导致积炭燃烧和爆炸。
4 高温、高压可加速设备金属材料发生蠕变、改变金相组织,还会加剧氢气、氮气对钢材的氢蚀和渗氮,加剧设备的疲劳腐蚀,使其机械强度减弱,引发物理爆炸。
5 液氨大规模事故性泄露会形成低温云团引起大范围人群中毒,遇明火还会发生空间爆炸。
合成氨指由氮和氢在高温高压和催化剂存在下直接合成氨,为一种基本无机化工流程。
现代化学工业中,氨是化肥工业和基本有机化工的主要原料。
工艺流程1 原料气制备(制备H2、CO、N2的粗原料气)1-1煤气化煤气化是用气化剂对煤或焦炭等固体燃料进行热加工,使其转变为可燃性气体的过程,简称造气。
气化剂主要是水蒸气、空气(或氧气)及它们的混合气体。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;空气煤气:以空气为气化剂制取的煤气,主要成分为N2和CO2。
合成氨生产中也称之为吹风气。
水煤气:以水蒸气为气化剂制得的煤气,主要成分H2和CO。
混合煤气:以空气和适量水蒸气为气化剂。
半水煤气:以适量空气和水蒸气做气化剂,所得气体组成符合([H2]+[CO])/[N2]=3.1~3.2的混合煤气,即合成氨的原料气。
1-1-1 以空气为气化剂-空气煤气,其主要成分为空气和二氧化碳C + O2 = CO2C + 1/2O2 = COC + CO2 = 2COCO + 1/2O2 = 2CO21-1-2 以水蒸气为气化剂-水煤气,其主要成分为氢气和一氧化碳。
C + H2O = CO + H2C + 2H2O = CO2 + 2H2CO + H2O = CO2 + H2C + 2H2 = CH41-1-3 间歇式生产半水煤气1-1-3-1固定床煤气发生炉右图为间歇式固定床煤气发生炉燃料层分区示意图。
合成氨的工艺流程

合成氨的工艺流程1. 空气分离:首先,空气中的氮气和氧气需要被分离。
这可以通过空气压缩和冷却,然后用分子筛或液化分离技术将氮气和氧气分离出来。
2. 氮气制备:通过空气分离得到的氮气需要被进一步提纯。
这可以通过低温分馏或其他技术将氮气提纯到适当的纯度。
3. 氢气制备:氢气可以通过天然气蒸汽重整反应或者电解水得到。
4. 催化剂制备:制备出合成氨反应所需的催化剂,通常是以铁为主要成分的铁钼镍催化剂。
5. 合成氨反应:将氮气和氢气在高压高温的条件下通过催化剂进行反应,生成合成氨。
6. 分离纯化:将合成氨经过冷却和减压,然后通过吸收剂、冷却和压缩等工艺步骤来分离纯化合成氨。
7. 储存和运输:将合成氨储存于合适的储罐中,并通过管道或其他运输方式将其运输到需要的地点。
以上就是合成氨的工艺流程,通过这个工艺流程可以高效地制备出高纯度的合成氨,供给各种化工生产需要。
合成氨的工艺流程是一个复杂而精细的过程,其中的每一步都需要严格控制,以确保产出的合成氨的纯度和质量能够满足工业需求。
在合成氨的工艺中,采用了一系列先进的化工技术和设备,以下将进一步细说合成氨的工艺流程过程。
8. 催化剂再生:在合成氨反应中使用的催化剂需要不断地被再生。
随着反应进行,催化剂表面会积聚一定量的杂质物质,从而影响催化剂的活性和选择性。
因此,通过热气流或蒸汽来清洁催化剂表面,以恢复催化剂的活性和选择性。
9. 热力学控制:合成氨的反应是放热反应,因此需保持适宜的温度。
以确保反应不至于过热,影响产品的选择性及催化剂的稳定性。
使用适当的冷却系统来维持反应温度,是非常关键的。
10. 蒸汽重整制氢:氢气是合成氨反应的一种重要原料。
而氢气通常是通过天然气蒸汽重整反应得到的。
在这个过程中,通过加热天然气并与水蒸气反应,生成氢气和二氧化碳。
11. 压缩系统:由于合成氨反应需要高压,所以需要使用高效的压缩系统,来将氮气和氢气压缩至合适的反应压力。
一般情况下,合成氨反应的压力约为100至200大气压。
工业合成氨资料讲解

1. 合成氨工业(1)简要流程(2)原料气的制取N2:将空气液化、蒸发分离出N2或将空气中的O2与碳作用生成CO2,除去CO2后得N2。
H2:用水和燃料(煤、焦炭、石油、天然气)在高温下制取。
用煤和水制H2的主要反应为:(3)制得的H2、N2需净化、除杂质,再用压缩机制高压。
(4)氨的合成:在适宜条件下,在合成塔中进行。
(5)氨的分离:经冷凝使氨液化,将氨分离出来,提高原料的利用率,并将没有完全反应的N2和H2循坏送入合成塔,使之充分利用。
2.合成氨条件的选择(1)合成氨反应的特点:合成氨反应是一个放热的、气体总体积缩小的可逆反应:(2)合成氨生产的要求:合成氨工业要求:○1反应要有较大的反应速率;○2要最大限度的提高平衡混合物中氨气的含量。
(3)合成氨条件选择的依据:运用化学反应速率和化学平衡原理的有关知识,同时考虑合成氨生产中的动力、材料、设备等因素来选择合成氨的适宜生产条件。
反应条件对化学反应速率的影响对平衡混合物中NH3的含量的影响合成氨条件的选择增大压强有利于增大化学反应速率有利于提高平衡混合物中NH3的产量压强增大,有利于氨的合成,但需要的动力大,对材料、设备等的要求高,因此,工业上一般采用20MPa—50MPa的压强升高温度有利于增大化学反应速率不利于提高平衡混合物中NH3的产量温度升高,化学反应速率增大,但不利于提高平衡混合物中NH3的含量,因此合成氨时温度要适宜,工业上一般采用500℃左右的温度(因该温度时,催化剂的活性最强)使用催化剂有利于增大化学反应速率没有影响催化剂的使用不能使平衡发生移动,但能缩短反应达到平衡的时间,工业上一般选用铁触媒作催化剂,使反应在尽可能低的温度下进行。
○1温度:500℃左右○2压强:20MPa—50MPa ○3催化剂:铁触媒除此之外,还应及时将生成的氨分离出来,并不断地补充原料气,以有利合成氨反应。
(6)合成氨生产示意图3.解化学平衡题的几种思维方式(1)平衡模式思维法(三段思维法)化学平衡计算中,依据化学方程式列出“起始”“变化”“平衡”时三段各物质的量(或体积、或浓度),然后根据已知条件建立代数式等式而进行解题的一种方法。
合成氨生产工艺
合成氨生产工艺合成氨生产原理:氨是一种重要的化工原料,特别是生产化肥的原料,它是由氢和氮合成。
合成氨工业是氮肥工业的基础。
为了生产氨,一般均以各种燃料为原料。
首先,制成含H2和CO等组分的煤气,然后,采用各种净化方法,除去气体中的灰尘、H2S、有机硫化物、CO、CO2等有害杂质,以获得符合氨合成要求的洁净的1:3的氮氢混合气,最后,氮氢混合气经过压缩至15Mpa以上,借助催化剂合成氨。
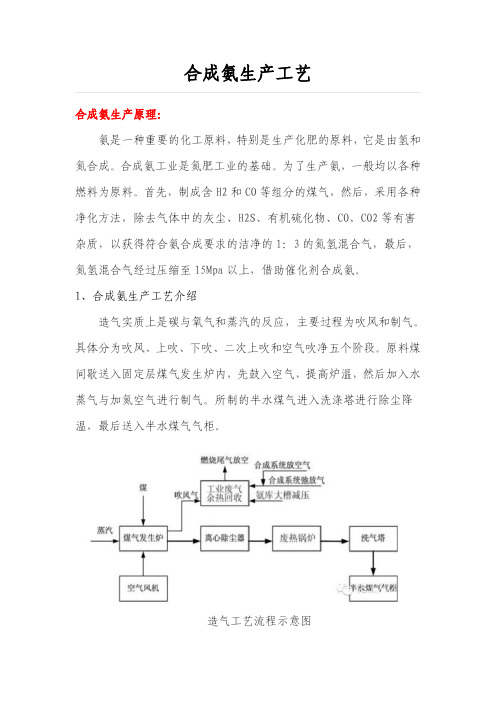
1、合成氨生产工艺介绍造气实质上是碳与氧气和蒸汽的反应,主要过程为吹风和制气。
具体分为吹风、上吹、下吹、二次上吹和空气吹净五个阶段。
原料煤间歇送入固定层煤气发生炉内,先鼓入空气,提高炉温,然后加入水蒸气与加氮空气进行制气。
所制的半水煤气进入洗涤塔进行除尘降温,最后送入半水煤气气柜。
造气工艺流程示意图2、脱硫工段煤中的硫在造气过程中大多以H2S的形式进入气相,它不仅会腐蚀工艺管道和设备,而且会使变换催化剂和合成催化剂中毒,因此脱硫工段的主要目的就是利用DDS脱硫剂脱出气体中的硫。
气柜中的半水煤气经过静电除焦、罗茨风机增压冷却降温后进入半水煤气脱硫塔,脱除硫化氢后经过二次除焦、清洗降温送往压缩机一段入口。
脱硫液再生后循环使用。
脱硫工艺流程图3、变换工段变换工段的主要任务是将半水煤气中的CO在催化剂的作用下与水蒸气发生放热反应,生成CO2和H2。
河南中科化工有限责任公司采用的是中变串低变工艺流程。
经过两段压缩后的半水煤气进入饱和塔升温增湿,并补充蒸汽后,经水分离器、预腐蚀器、热交换器升温后进入中变炉回收热量并降温后,进入低变炉,反应后的工艺气体经回收热量和冷却降温后作为变换气送往压缩机三段入口。
变换工艺流程图4、变换气脱硫与脱碳经变换后,气体中的有机硫转化为H2S,需要进行二次脱硫,使气体中的硫含量在25mg/m3。
脱碳的主要任务是将变换气中的CO2脱除,对气体进行净化,河南中科化工有限责任公司采用变压吸附脱碳工艺。
来自变换工段压力约为1.3MPa左右的变换气,进入水分离器,分离出来的水排到地沟。
合成氨生产常用的原料有哪些

1合成氨生产常用的原料有哪些?原料:(包括提供H2的原料和燃料)固体原料:焦碳、煤气体原料:天然气、重油、焦炉气等液体原料:石脑油、重油、原油等常用的原料有:焦碳、煤、天然气、重油2合成氨生产分哪几个基本工序?三个基本工艺步骤是什么/(1)造气:即制备含有氢、氮的原料气(2)净化:不论采用何种原料和何种方法造气,原料气中都含有对合成氨反应过程有害的各种杂质,必须采取适当的方法除去这些杂质。
(3)压缩和合成:将合格的氮、氢混合气压压缩到高压,在铁催化剂的存在下合成氨。
3写出天燃气蒸汽转化法生产合成气的主要反应方程式、工艺条件和工艺流程图,说明天然气蒸汽转化法为何要进行二段转化操作?(1)主反应式:CH4 + H2O(g) = CO + 3H2 206.3KJ/mol (1)CO + H2O(g) = CO2 + H2 -41.2KJ/mol (2)副反应式:CH4 = 2H2 + C2CO = CO2 + CCO + H2 = H2O + C(2)工艺条件:压力3~4 MPa;一段转化反应温度800℃;二段转化反应温度1000℃;水碳比S=3~4;空间速度(根据炉型、分段情况、催化剂的不同以及反应的不同时期来确定)(4)书上18页第一段4干法脱硫与湿法脱硫各有甚么优缺点?干法:优点:既能脱除有机硫,又能脱除无机硫;出口气含S<1×10-6(无加氢)、S<2×10-8(有加氢)。
缺点:脱硫剂再生困难,只可用于脱微量硫。
湿法:优点:液态脱硫剂易于输送,可以再生,能回收硫磺,可用于脱除大量无机硫。
5改良ADA法脱硫由哪几个基本反应过程构成?原理:分为四步:①用pH=8.5~9.2的稀碱溶液吸收H2SNa2CO3 + H2S == NaHS + NaHCO3②硫氢化物被氧化为S2NaHS + 4NaVO3 + H2O == Na2V4O9 + 4NaOH + 2S偏钒酸钠焦性偏钒酸钠(有还原性)以上两步为脱硫,在脱硫塔中进行。
合成氨生产原料的选择

合成氨工业
• 基本无机化工之一。氨是化肥工业 和基本有机化工的主要原料。从氨 可加工成硝酸,现代化学工业中, 常将硝酸生产归属于合成氨工业范 畴。合成氨工业在20世纪初期形成 ,开始用氨作火炸药工业的原料, 为战争服务;第一次世界大战结束后 ,转向为农业、工业服务。随着科学 技术的发展,对氨的需要量日益增 长。50年代后氨的原料构成发生重 大变化,近30年来合成氨工业发展 很快。
原料气净化比较
• 在合成氨工业中,经变换和脱碳工艺处理,合成氨原料气 中仍含有对氨合成催化剂有毒的CO和CO2气体,必须进一 步处理将其降低至10 mL/m3左右,以保护氨合成催化剂 。目前合成氨厂脱除微量CO、CO2的工艺方法较多,主要 有醋酸铜氨液洗涤法(铜洗法)、低压甲烷化法、甲醇甲烷 化法(双甲工艺)、醇化工艺、非等压醇烷化净化工艺等 。
原料气制备方法比较
氨的合成,首先必须制备合格的氢、氨原料气。 • 氮气可取之于空气或将空气液化分离而得氮气 ;或使空气通过燃料层燃烧,将生成的CO和CO2 除去而制得。 • 氢气一般常用含有烃类的各种燃料,即通过用 焦炭、无烟煤、天然气、重油等为原料与水蒸气 作用的方法来制取。
合成氨的生产原料
•
1.2 合成氨贸易量及利用 每年全球合成氨贸易量约占总产量的12%以上 。2008年约为1870万吨,比2007年下降2.4% 中国的商品液氨很少,主要用于生产肥料, 非肥料需求不到10%,用于浓硝酸、己内酰胺 、丙烯腈等。
1.3 合成氨装置大中小并存,规模趋于合理 引进合成氨装置经扩能改造,单套日产能力提 高20%-50%,年产45万t/a。 新建天然气、煤原料的大型合成装置单套能力 达到50万t/a; 中小规模装置逐步调整改造达到8-18-30万t/a 。企业数量由1500多家,减少至435家。
合成氨工艺

合成氨工艺————————————————————————————————作者:————————————————————————————————日期:合成氨工艺流程(1)原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2OH→2+CO2 =-41.2kJ/mol 0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
②脱硫脱碳过程各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,第一道工序是脱硫,用以保护转化催化剂,以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。
工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法(Selexol)等。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。
合成氨生产原料确定张杰

提高炉温的主要手段是提高入炉空气量。入炉空气量是 由吹风速度和吹风时间来决定的。在氧化层中,碳的燃烧速 度很快,属于扩散控制。所以提高吹风速度,有利于碳的燃 烧反应,还可缩短二氧化碳与灼热碳层的接触时间,以减少 一氧化碳的生成量,从而减少了热损失,增加了炉内的蓄热 量。在入炉空气量一定的情况下,提高吹风速度,还可以延 长制气时间,有利于提高煤气发生炉的生产能力。但吹风速 度过大,将导致吹出物量增加,燃料损失加大,严重时,出 现风洞甚至吹翻,造成气化条件恶化。
精选课件
4.固体燃料气化法生产合成氨工艺流程图
精选课件
(二)烃类蒸汽转化法
该法是在催化剂存在下与水蒸汽反应转化制气。
1.烃类蒸汽转化法基本反应原理
主要发生下述反应:
CH4+H2O→CO+H2 CO+H2O→CO2+H2 CnH2n+nH2O→nCO+(2n+l)H2 反应在800-820℃下进行。从上述反应可知,也有部分氢气来 自水蒸汽。
合成氨生产原料的确定
小组成员:骆骁 张杰华 包二 刘灿 刘江霞
精选课件
一、 合成氨生产条件的比较
目前,合成氨的生产方法主要有固体燃料 气化法(煤或焦炭的气化),烃类蒸汽转化法 (天然气,石脑油),重油部分氧化法。由于 合成氨原料气中的氮气容易取得,所以原料气 的制备主要是制取氢气,而CO在变换过程能 产生同体积的氢气,因此把原料气中的CO和 H2看作有效气体成分。
精选课件
(5)重油预热温度
重油预热温度也是重要的气化条件。提高重油 预热温度有利于气化炉热平衡,可减少气化炉的氧 气消耗,并有利于重油的雾化。但若预热温度过高, 会造成重油中轻馏分气化,产生大量油蒸气,会使 泵抽空,中断输送,造成断火事故。同时重油中馏 分会产生裂解,导致析碳而堵塞管道,对生产不利。 一般重油预热温度在150—260℃之间。
合成氨的概述

未来发展趋势预测
绿色低碳发展
随着环保意识的提高,未来合成氨产业将更加注重绿色低碳发展 ,推动清洁能源和可再生能源的应用。
技术创新加速
技术创新将成为合成氨产业发展的重要驱动力,推动产业不断升 级和转型。
国际化合作加强
随着全球化进程的加速,国内外合成氨企业之间的合作将进一步 加强,推动产业协同发展。
06
控制策略
为了实现精确的温度和压力控制,可以采用先进的控制策略,如PID控制、模糊控制和神 经网络控制等。这些控制策略可以根据实时监测数据进行实时调整,提高合成氨生产的稳 定性和效率。
04
生产过程中环境影响 及治理措施
废气排放及处理
废气来源
合成氨生产过程中产生的废气主 要包括氨气、氮气、氢气等。
废气处理
THANK YOU
作用
合成氨是农业生产中重要的氮肥 来源,也是工业领域的重要原料 ,用于生产各种含氮化学品,如 硝酸、尿素等。
化学反应方程式
原料与产品
原料
合成氨的主要原料是氮气和氢气。氮气来自空气,氢气则通 常通过天然气、石脑油、重油等烃类原料与水蒸气在高温下 进行催化反应制得。
产品
合成氨的产品主要是液氨和氨水。液氨是将氨气冷却至其液 化温度以下得到的液体,而氨水则是将氨气溶于水得到的溶 液。这些产品广泛应用于农业、化工、医药等领域。
针对不同类型的废气,采取相应 的处理措施,如氨气可采用水洗 、酸洗等方法进行处理,氮气和 氢气则可通过燃烧或回收等方式
进行处理。
排放控制
加强废气排放的监测和控制,确 保废气排放符合国家和地方的环
保标准。
废水治理技术
废水来源
合成氨生产过程中产生的废水主要包括冷却水、洗涤水、 工艺废水等。
简述合成氨的主要生产步骤

合成氨的主要生产步骤合成氨是一种重要的化工原料,广泛应用于肥料、塑料、药品等行业。
合成氨的主要生产步骤包括天然气净化、蒸汽重整、合成气制备、合成氨催化反应和分离纯化等环节。
本文将对这些步骤进行详细介绍。
1. 天然气净化合成氨的原料之一是天然气,其中含有杂质如硫化物、二氧化碳等,需要通过净化工艺去除。
天然气净化的主要步骤包括除硫、脱水和除碳。
1.1 除硫天然气中的硫化物会对催化剂产生毒害作用,因此需要将其去除。
常用的方法是利用吸收剂吸收硫化物,并通过再生使其重新可用。
1.2 脱水天然气中的水分会影响后续反应过程,因此需要进行脱水处理。
常用的方法是通过冷却和吸附剂吸附去除水分。
1.3 除碳天然气中的二氧化碳会影响合成气的质量,因此需要进行除碳处理。
常用的方法是利用碱液吸收二氧化碳,再通过热解使其重新可用。
2. 蒸汽重整蒸汽重整是将天然气中的甲烷转化为合成气的重要步骤。
该过程主要包括甲烷蒸汽重整和水蒸气变换反应两个步骤。
2.1 甲烷蒸汽重整甲烷蒸汽重整是将天然气中的甲烷与水蒸气在催化剂的作用下进行反应,生成一氧化碳和氢气。
常用的催化剂有镍基催化剂和铬基催化剂。
2.2 水蒸气变换反应水蒸气变换反应是将一氧化碳与水蒸气在催化剂的作用下进行反应,生成二氧化碳和合成氢。
常用的催化剂有铁铬催化剂和铁锆催化剂。
3. 合成气制备合成气制备是将蒸汽重整产生的合成气进行纯化和调节,以满足后续合成氨反应的要求。
合成气主要由一氧化碳、二氧化碳和氢气组成,其中一氧化碳和氢气的比例需要调节。
4. 合成氨催化反应合成氨催化反应是将合成气在合成氨催化剂的作用下进行反应,生成合成氨。
该反应通常在高压和高温条件下进行,常见的催化剂有铁基催化剂和铑基催化剂。
5. 分离纯化合成氨催化反应产生的合成氨还需经过分离纯化步骤,以获得高纯度的合成氨。
常用的分离纯化方法包括压缩、冷凝、吸附和蒸馏等。
5.1 压缩将产生的合成氨进行压缩,以提高其密度和浓度。
合成氨生产主要分几个工序

1.合成氨生产主要分几个工序?各部分任务如何?答:1)原料气制备即制备含有氢、氮的原料气。
用煤、原油、或天然气作原料,制备含氮、氢气的原料气。
(将煤和天然气等原料制成含氢和氮的粗原料气。
一般焦炭、无烟煤等固体燃料通常采用气化的方法制取合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
渣油可采用非催化部分氧化的方法获得合成气。
)2)净化因为无论用何种方法造气,原料气中都含有对合成氨反应过程有害的各种杂质,必须采取适当的方法除去这些杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
(1)脱硫过程无论以焦炭还是天然气为原料获得的原料气中,都含有一氧化碳、二氧化碳、硫化物等不利于合成反应的成分,需要在进入合成塔之前除去。
其中硫化物对蒸气转化都是有害的,故在原料气进入界区后,首先进行脱硫。
氧化锌脱硫就是H2S气体在固体ZnO上进行反应,生成H2O进入气相,ZnS则沉积在ZnO固体表面上。
脱无机硫温度约200℃。
(2)一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2O→H2+CO2 ,ΔH=-41.2kJ/mol 由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
(3)脱碳过程粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。
根据吸收剂性能的不同,可分为两大类。
合成氨工艺简介解读

• (2)、固定层间歇法制半水煤气各工艺循环的作用 • 吹风:以空气为气化剂,空气自下而上通过燃料层,目的是通过C与 O2的化学反应,放出热量,并贮存于燃料层中,为制气阶段提供热量。 • 回收:吹风后期,空气自下而上,通过燃料层,氧气燃烧后,回收氮 气到气柜,控制H2/N2比。 • 上吹制气:以蒸汽(或配少量空气)为气化剂,自下而上通过燃料层, 燃料中的C与水蒸汽反应,生成半水煤气。这个过程加入空气并不单 纯为了提高温度,主要是为了配入适量N2,以满足原料气H2/N2比要 求,即所谓“上吹加氮”。 • 下吹制气:上吹制气后,蒸汽改变进入燃料层的方向,自上而下通过 燃料层生产水煤气,以保持气化层的位置和温度稳定在一定区域内。 • 二次上吹:下吹制气后,蒸汽改变方向,自下而上通过燃料层,即生 产水煤气,又能排净炉底残留的半水煤气,为空气通过燃料层创造安 全条件。 • 空气吹净:空气自下而上通过燃料层,生产空气煤气,将原来炉上部 残留的水煤气一并送入气柜。
3、流程图
一入
压缩一段来气体 油分离器 活性炭滤油器
二出 一入 二出
三入 一出
二出 二入 一出
二入
饱和热水塔
一出 二入
一入
热交预腐蚀器
二入
电炉
一入
淬冷 器
一出
二出
变换炉
三出
热水换热器 变换气去变脱
变换气冷却 分离器
软水换热器
四、变换气脱硫
• 1、生产原理 • 将变换气中的硫化物(H2S)用碱液法气液相逆向接触 吸收,达到净化变换气的目的。净化后的变换气硫化物含 量在20mg/m3以下,吸收后碱液经氧化再生(催化剂作用 下),析出单质硫,碱液得到再生,循环使用,硫泡沫送 去硫回收岗位处理。 • 吸收反应:Na2CO3 + H2S = NaHS + NaHCO3 • COS + 2Na2CO3 + H2O =Na2CO2S + 2NaHCO3 • Na2CO3 + CO2 + H2O = NaHCO3 • 再生反应:NaHS + 1/2O2 = NaOH+S↓ • NaHCO3 + NaOH = Na2CO3 + H2O • 2Na2CO2S + O 2 = Na2CO3 + 2S↓
工业合成氨的方法

工业合成氨的方法
工业合成氨主要有哈伯-博斯曼法和奥让-吕克法两种方法。
1. 哈伯-博斯曼法:也称为直接合成法。
该方法通过在高温高压下将氮气和氢气反应生成氨气。
反应以铁为催化剂,常温下反应速度较慢,需要加热至400-500摄氏度,压力高达100-200atm。
该方法是工业上最常用的氨合成方法,能够大量生产氨气。
2. 奥让-吕克法:也称为间接合成法。
该方法先将天然气(主要是甲烷)转化为一氧化碳和氢气,然后通过费舍尔-通纳合成反应将一氧化碳和氢气合成为甲醇。
最后,将甲醇通过催化剂进行裂解,生成氢气和一氧化碳,再与氮气进行合成反应得到氨气。
这种方法相对复杂,但可以通过更加便宜的原料制备氨气。
这两种方法都能够实现大规模的工业合成氨气。
在实际应用中,根据不同的条件和资源的可获得性,选择合适的方法进行氨气的合成。
以煤为原料合成氨的工艺

以煤为原料合成氨1概述氨(Ammonia,旧称阿莫尼亚)是重要的无机化工产品之一,在国民经济中占有重要地位。
农业上使用的氮肥,除氨水外,诸如尿素、硝酸铵、磷酸铵、氯化铵以及各种含氮复合肥都是以氨为原料生产的。
合成氨是大宗化工产品之一,世界每年合成氨产量已达到1亿吨以上,其中约有80%的氨用来生产化学肥料,20%作为其它化工产品的原料。
合成氨指由氮和氢在高温高压和催化剂存在下直接合成的氨。
别名氨气,分子式为NH3,英文名:synthetic ammonia。
世界上的氨除少量从焦炉气中回收外,绝大部分是合成的氨。
合成氨主要用于制造氮肥和复合肥料。
氨作为工业原料和氨化饲料,用量约占世界产量的12%。
硝酸、各种含氮的无机盐及有机中间体、磺胺药、聚氨酯、聚酰胺纤维和丁腈橡胶等都需直接以氨为原料生产。
液氨常用作制冷剂。
铵根离子:NH4+;其中氮的化学价为+ 3 ;NH3是氨气。
1.1发现和历史1.1.1怎样固氮——问题浮出水面氨(Amonia),分子式NH3,1754 年由英国化学家普里斯特利(J.Joseph Priestley)加热氯化铵和石灰石时发现。
1784 年,法国化学家贝托雷(C.L.Berthollet)确定了氨是由氮和氢组成的。
从那以后很长一段时间,氨的主要来源是氮化物,而氮化物的主要来源是自然界中的硝石矿产。
19 世纪以来,人类步入了现代化的历程。
随着农业的发展,氮肥的需求量在不断提高;同时随着工业的突飞猛进,炸药的需求量也在迅速增长。
1809 年,在智利发现了一个很大的硝酸钠矿产地;但是面对人类不断膨胀的需求,自然界的生物和矿产资源毕竟有限。
然而全世界无论何处,大气的五分之四都是氮,如果有人能学会大规模地、廉价地把单质的氮转化为化合物的形式,那么,氮是取之不尽、用之不竭的。
因此将空气中丰富的氮固定下来并转化为可被利用的形式,成为一项受到众多科学家注目和关切的重大课题,而合成氨,作为固氮的一种重要形式,也变成了19 至20 世纪化学家们所面临的突出问题之一。
合成氨相关知识

合成氨生产合成氨的主要原料有天然气、石脑油、重质油和煤(或焦炭)等。
①天然气制氨。
天然气先经脱硫,然后通过二次转化,再分别经过一氧化碳变换、二氧化碳脱除等工序,得到的氮氢混合气,其中尚含有一氧化碳和二氧化碳约0.1%~0.3%(体积),经甲烷化作用除去后,制得氢氮摩尔比为3的纯净气,经压缩机压缩而进入氨合成回路,制得产品氨。
以石脑油为原料的合成氨生产流程与此流程相似。
②重质油制氨。
重质油包括各种深度加工所得的渣油,可用部分氧化法制得合成氨原料气,生产过程比天然气蒸气转化法简单,但需要有空气分离装置。
空气分离装置制得的氧用于重质油气化,氮作为氨合成原料外,液态氮还用作脱除一氧化碳、甲烷及氩的洗涤剂。
③煤(焦炭)制氨。
随着石油化工和天然气化工的发展,以煤(焦炭)为原料制取氨的方式在世界上已很少采用。
用途氨主要用于制造氮肥和复合肥料,氨作为工业原料和氨化饲料,用量约占世界产量的12%。
硝酸、各种含氮的无机盐及有机中间体、磺胺药、聚氨酯、聚酰胺纤维和丁腈橡胶等都需直接以氨为原料。
液氨常用作制冷剂。
合成氨的工艺流程1原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;2净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2O→H2+CO2=-41.2kJ/mol0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
合成氨原料气

合成氨原料气合成氨是一种重要的化工原料,广泛应用于农业、化肥生产和工业领域。
合成氨的原料气是合成氨过程中至关重要的一环,直接影响合成氨的产量和质量。
本文将围绕合成氨原料气展开讨论,探讨其来源、成分和影响因素。
合成氨原料气的主要成分是氮气和氢气。
氮气主要来自空气,而氢气则通常采用天然气蒸汽重整或煤气化等方法生产。
氮气和氢气按一定比例混合后,经过催化剂的作用,反应生成合成氨。
因此,保证原料气中氮气和氢气的纯度和比例是合成氨生产的关键。
合成氨原料气的品质也受到其他杂质的影响。
例如,原料气中的氧气、水蒸气、二氧化碳等杂质会影响催化剂的活性,降低合成氨的产率。
因此,在生产过程中需要通过各种方法去除这些杂质,确保原料气的纯净度。
原料气的温度和压力也会影响合成氨的产率和质量。
在反应中,适当的温度和压力能够提高反应速率,增加产量,但过高或过低的温度和压力会导致反应失控或产物质量下降。
因此,控制原料气的温度和压力是合成氨生产中需要重点关注的问题。
合成氨原料气的来源也值得关注。
传统的合成氨生产通常采用化石燃料为原料生产氢气,但这种生产方式会产生大量二氧化碳等温室气体,对环境造成严重影响。
因此,近年来越来越多的合成氨生产商开始使用清洁能源,如风能、太阳能等替代传统原料气,以减少对环境的影响。
合成氨原料气是合成氨生产中至关重要的一环,其成分、纯度、温度、压力和来源都会直接影响合成氨的产量和质量。
生产商需要密切关注原料气的质量和来源,采取有效措施确保原料气的纯净度和稳定性,以提高合成氨的生产效率和产品质量,同时减少对环境的影响。
希望通过本文的讨论,读者能更加深入了解合成氨原料气的重要性和影响因素,为相关领域的研究和生产提供参考。
【优】合成氨生产原料的比较最全PPT资料

要用于制取化工原料。
3.以煤为原料制取氢气
一是煤的焦化(或称高温干馏),二是煤的 气化。焦化是指煤在隔绝空气条件下,在90 -1000℃制取焦碳副产品为焦炉煤气。焦炉 煤气组成中含氢气55-60%(体积)甲烷2327%、一氧化碳6-8%等。每吨煤可得煤气 30气的原料 。
❖ 煤的气化是指煤在高温常压或加压下,与气化剂反
应转化成气体产物。气化剂为水蒸汽或氧所(空
气),气体产物中含有氢有等组份,其含量随不同
气化方法而异。我国有大批中小型合成氢厂,均以
煤为原料,气化后制得含氢煤气作为合成氨的原料。 这是一种具有我国特点的制取氢源方法。采用OGI 固定床式气化炉,可间歇操作生产制得水煤气。该 装置 小,操作容易,其气体产物组成主要是氢及
合成氨生产原料的分析比较
❖ 化工0803班 第八组
一.合成氨的原料
天然气 ❖合成1氨.成以本仍重然低油于煤头为合成原氨成料本。 部分氧化法制取氢气 重油原料包括有常压、减压渣油及石油深度加工后 气化剂为水蒸汽或氧所(空气),气体产物中含有氢有等组份,其含量随不同气化方法而异。
❖ 重油原料包括有常压、减压渣油及石油深度加工后的燃料油,重油与水蒸汽及氧气反应制得含氢 气体产物。
双甲工艺流程图
水蒸汽转化制氢的工艺。我国在该领域进行了大量 我国有大批中小型合成氢厂,均以煤为原料,气化后制得含氢煤气作为合成氨的原料。
部分重油燃烧提供转化吸热反应所需热量及一定的反应温度。
有成效的研究工作,并建有大批工业生产装置。我 以重油为原料部分氧化法制取氢气
如果煤用现行价格(503元/吨)不变,天然气 年(含 年)前每年涨价8%。
年天然气制氨成本估计1749. 合成气精制新工艺是有利于氮肥企业节能降耗,增产增收,更是造福于社会的优秀技术。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1合成氨生产常用的原料有哪些?原料:(包括提供H2的原料和燃料)固体原料:焦碳、煤气体原料:天然气、重油、焦炉气等液体原料:石脑油、重油、原油等常用的原料有:焦碳、煤、天然气、重油2合成氨生产分哪几个基本工序?三个基本工艺步骤是什么/(1)造气:即制备含有氢、氮的原料气(2)净化:不论采用何种原料和何种方法造气,原料气中都含有对合成氨反应过程有害的各种杂质,必须采取适当的方法除去这些杂质。
(3)压缩和合成:将合格的氮、氢混合气压压缩到高压,在铁催化剂的存在下合成氨。
3写出天燃气蒸汽转化法生产合成气的主要反应方程式、工艺条件和工艺流程图,说明天然气蒸汽转化法为何要进行二段转化操作?(1)主反应式:CH4 + H2O(g) = CO + 3H2 206.3KJ/mol (1)CO + H2O(g) = CO2 + H2 -41.2KJ/mol (2)副反应式:CH4 = 2H2 + C2CO = CO2 + CCO + H2 = H2O + C(2)工艺条件:压力3~4 MPa;一段转化反应温度800℃;二段转化反应温度1000℃;水碳比S=3~4;空间速度(根据炉型、分段情况、催化剂的不同以及反应的不同时期来确定)(4)书上18页第一段4干法脱硫与湿法脱硫各有甚么优缺点?干法:优点:既能脱除有机硫,又能脱除无机硫;出口气含S<1×10-6(无加氢)、S<2×10-8(有加氢)。
缺点:脱硫剂再生困难,只可用于脱微量硫。
湿法:优点:液态脱硫剂易于输送,可以再生,能回收硫磺,可用于脱除大量无机硫。
5改良ADA法脱硫由哪几个基本反应过程构成?原理:分为四步:①用pH=8.5~9.2的稀碱溶液吸收H2SNa2CO3 + H2S == NaHS + NaHCO3②硫氢化物被氧化为S2NaHS + 4NaVO3 + H2O == Na2V4O9 + 4NaOH + 2S偏钒酸钠焦性偏钒酸钠(有还原性)以上两步为脱硫,在脱硫塔中进行。
③氧化剂(偏钒酸钠)再生Na2V4O9 + 2ADA(O) + 2NaOH +H2O == 4NaVO3 + 2ADA(H)④ADA再生2ADA(H还原态) + O2 == 2ADA(O氧化态) + 2H2O以上两步为再生,在再生塔中进行。
ADA(O):蒽醌二磺酸钠6采用低温交换的目的7写出苯菲尔法脱除CO2吸收和再生主要反应,为什么要加入二乙醇胺?脱碳:K2CO3 + CO2 + H2O == 2KHCO3钾碱再生:2KHCO3 == K2CO3 + H2O + CO2吸收反应(脱碳):KH2AsO3 + CO2 + H2O == KHCO3 + H3AsO3K2CO3 + CO2 + H2O == 2KHCO3 80~90℃钾碱再生:2KHCO3 == K2CO3 + H2O + CO2 105~110因为在K2CO3溶液中加入少量二乙醇胺,可大大加快CO2的吸收速度,降低CO2的分压,同时还可除去原料气中的H2S等酸性组分。
8什么是平衡氨含量,影响平衡氨含量的因素有哪些?有何影响?在一定温度和压强下,所生成的氨的含量,叫做平衡氨含量。
影响因素:(1)温度、压强,(2)理论计算出当xNH3为最大值时r=H2/N2=3;实践证明在高压下,最大氨含量时的r =2.9~3.0(3)惰性气体组分xi(甲烷、氩气):应在高压低温下进行9影响氨合成反应速度的因素有哪些?有何影响?(1)温度:为放热的可逆反应,存在一个最适宜温度(反应速率最快)(Tm<Te)(2)压力:压力P增大,反应速率也增大,所以要求在高压下进行合成。
(3)氢氮比:仍要求H2:N2略低于3。
反应机理为氮的活性吸附所控制。
(4)惰性气体:增加惰性气体组分的含量,总反应速率下降。
(5)空间速度:中压法:20000~30000 h-1;低压法:10000 h-1(轴向冷激式合成塔,可充分利用反应热,降低功耗,延长催化剂的使用寿命)10氨合成的工艺影响因素有哪些?如何选择确定氨合成的工艺条件?因素:压力、温度、空间速度、合成气体的初始组成、惰性气体含量、初始氨含量合成氨的工艺条件:中小型厂(中压法):操作压力30MPa,425~490℃,氢氮比=2.8~2.9,空间速度24000 h-1,出口气氨含量为14~18%。
循环气中惰性气体含量控制在16~20%,氨含量控制在3.2~3.8%。
大型厂(低压法):操作压力15MPa,410~490℃,氢氮比=2.8~2.9,空间速度9000 h-1,出口气氨含量12%,循环气中惰性气体含量控制在8~15%,氨含量控制在2~3.2%。
11氨合成塔的结构有何特点?合成塔由内件和外筒所组成:外筒:承受高压(30MPa),不承受高温(40℃),采取层板包扎式。
内件:承受高温(500℃),不承受高压(1~2MPa),易受氢腐蚀。
内件包括:催化剂筐:催化剂床层+并流套管(冷管)+气体分配盒热交换器:列管式热交换器。
电加热器(在中心管内):催化剂的升温还原,催化剂使用后期活性降低时维持反应的热平衡(即补充热量)并流三套管合成塔内件和单管并流合成塔内件各有何优缺点?并流三套管优点具有操作稳定、适应性强、结构普可靠,缺点结构复杂,冷管与分气盒占据较多的空间,催化剂还原时床层下部受冷管传热的影响升温困难,还原不易彻底。
单管并流合成塔的优点是使结构简化,提高了塔的容积系数。
凯洛格立式轴向四段冷激式氨合成塔的优缺点?第57页最上面1硫酸生产的主要原料有哪些?目前用什么原料生产硫酸的产量较大?(1)硫酸生产用原料:硫铁矿、硫磺、硫酸盐(石膏)、含SO2烟气(有色金属冶炼副产物)及含H2S 废气。
(2)石油、天然气开采中的副产物硫磺。
2写出硫铁矿的焙烧反应,提高焙烧反应的速率的途径有哪些?4FeS2 + 11O2 == 8SO2+ 2Fe2O3 , △H=-3411KJ/mol途径:(1)提高反应温度:850~950℃,>950℃烧渣熔融结块,熔化在矿石表面,阻滞了氧气的渗透。
(2)减小矿石粒度:粒度小较好,但过细时(如硫精矿,0.07~0.15mm,为浮选法得到),易于粘连,限制了气流速度,炉气的含尘量也增大。
(3)增加空气与矿粒的相对运动:可采取流化状态反应以减小气体的扩散阻力,故使用沸腾炉燃烧硫铁矿。
(4)提高入炉空气含氧量:可增大氧气的扩散速度,但不经济,一般不允许炉气中O2过剩系数过大。
3沸腾焙烧炉由哪几部分构成,其作用是什么?沸腾炉的结构:风室、空气分布板、沸腾层、沸腾层上部燃烧空间。
作用:扩大部分的作用:细粒大部分顺炉壁流回到沸腾区风帽的作用:高速气流吹松炉料而不至于沉积到气体分布板上。
4二氧化硫炉气净化的目的是什么?除去这些杂质的方法是什么?目的:会带入转化系统会降低二氧化硫的转化率,腐蚀系统的设备和管道。
因此,必须对炉气进行进一步的净化。
方法:酸雾的清除5试述文泡冷电酸洗净化流程?炉气→文氏管→复挡除沫器→泡沫塔→复挡除沫器→冷凝器或增湿塔→电除雾器→净化器→去干燥工序写出二氧化硫催化氧化的反应,此反应有什么特点?如何提高二氧化硫的平衡转化率?SO2 + ½O2 == SO3 ,△rHm(25℃)=-98.89kJ/mol为放热的可逆反应T降低,P升高,都能使平衡转化率增大6何谓最适宜温度,它与气体组成有什么关系?最适宜温度是:当达到一定温度时,反应最完全,产率最高T升高,正反应速率增大,逆反应速率也增大,但平衡向左移动,所以必然会有一个最适宜的反应温度Tm,在此温度下反应,总反应速率最大。
7写出二氧化硫催化氧化反应,此反应有什么特点?如何提高二氧化硫平衡转化率?SO2 + ½ O2 == SO3 ,△rHm(25℃)=-98.89kJ/mol特点:为放热的可逆反应,T降低,P升高,都能使平衡转化率增大,8转化过程的工艺条件是如何确定的?(1)最适宜反应温度:尽量使反应按照最适宜温度线进行,采取的方法:在催化剂活性温度范围内操作;尽可能接近最适宜温度进行反应;采取分段操作。
2)SO2的起始浓度根据充分利用原料、减少尾气污染和生产总成本最低的原则,要求:含煤硫铁矿为原料的一转一吸流程中,炉气中SO2控制在<7%;硫磺制酸时,SO2控制在8~9%;硫铁矿为原料的二转二吸流程中SO2控制在9~10%(3)最终转化率根据最低生产成本(降低催化剂用量)和提高S利用率及减轻污染(高转化率)的原则:对于中间换热、一次转化的流程(一转一吸流程)选取最终转化率为97.5~98%;对于两转两吸流程的最终转化率可达99.5%。
9转化器为什么分段操作,中间冷却有哪几种方式,其优缺点是什么?冷却方式:间接换热式和冷激式两种优缺点①反应速度快,最终转化率高(最后一段转化时O2高);②可采取高SO2炉气(最后一段转化时先除去了SO3);③减轻尾气污染(尾气中SO2达到排放标准);④换热面积大(增加的中间吸收再去转化时又需加热);⑤动力消耗大(气流阻力大)。
10硫酸生产为何选择98.3%的硫酸来吸收三氧化硫?当吸收酸<98.3%时,吸收慢,且易生成酸雾;当吸收酸>98.3%时,P(SO3)较大,吸收率低;当吸收酸=98.3%时,P(H2O)最低,形成的酸雾最少。
所以98.3%浓硫酸为最佳吸收剂。
1画出隔膜法氯碱生产的基本工艺过程示意图?第98页图2什么是理论分解电压?什么是槽电压?槽电压由哪几部分构成?理论分解电压:为了使物质能在两电极上连续不断析出时外界所加的最小电压,其理论计算值称理论分解电压,它等于阳极与阴极电极电位之差。
槽电压:电解槽两电极上所加的电压称为槽电压。
槽电压包括:理论分解电压E、过电位E0、电流通过电解液的电压降△EL和通过电极、导线、接点等的压降△ER3什么是电压效率,什么事电流效率?它们与电能效率的关系是什么?电压效率:ηE:ηE = E (理分) /E(槽) ,隔膜法ηE = 60%电流效率ηI :隔膜法ηI = 96%关系:电能效率η:η = ηE×ηI ,隔膜法η < 60%4为什么离子膜法电解的阴极液中NaCl含量低,根据离子膜选择透过性示意图分析。
5导致离子膜性能下降的主要因素有哪些?离子膜长期处于NaOH低浓度下运行,还会使膜膨胀、严重起泡、分离直至永久性破坏。
6离子膜电解槽的主要阴阳极材料有哪些?阳极为金属阳极(DSA),阴极为铁板、不锈钢板、镍板等。
7试论述电解工艺条件的选择?(1)饱和食盐水质量:影响到离子膜的使用寿命、槽电压及电流效率,如含Ca2+ 、Mg2+ ,通过膜孔时易堵塞,所以控制c(Ca2+) +c( Mg2+ ) <2×10-8mol/L 。
