微生物检测原始记录文本
微生物限度检查原始记录

菌落数
阴性对照g),□(个/ml)□(cfu/g)】
平皿号
各稀释倍数
各稀释倍数
10-1
10-2
10-3
阴性对照
10-1
阴性对照
1
2
平均菌落数
菌数
□(个/g)□(个/ml)□(cfu/g)
结论:
□符合规定□不符合规定
备注:
表单编号:QR-QD-099,版本:A0
复检者:检验者:
微生物限度检查原始记录
检品名称
检验编号
批号
检验日期
检验依据
紫外消毒时间:时分至时分
请检部门
一、细菌数:(30℃~35℃)
营养琼脂培养基批号:
生化培养箱:
二、霉菌和酵母菌数:(23℃~28℃)
玫瑰红钠琼脂培养基批号:
生化培养箱:
平皿号
稀释倍数
1
2
3
4
5
1ml菌数总和
平均
菌落数
阴性对照
1
2
3
4
5
1ml菌数总和
日期:日期:
微生物检测原始记录

室温:湿度:
样品名称
规格
检验类别
出厂检验
抽样基数
抽样方式
抽样数量
检测依据
GB/T4789.2-2010
接种时间
使用主要仪器
恒温培养箱
培养基名称
平板计数琼脂培养基
报告时间
样号
36+1℃培养24~48h
稀释度
报告数cfu/ml(g)
1:10
1:100
1:1000
空白
1
接种量ml
1
1
1
1
0.1
0.01
分析号
1
2
3
4
5
6
7
8
9
1
初发酵产酸、气
复发酵产酸、气
BGLB分离培养
2
初发酵产酸、气复发酵产酸、气BGL Nhomakorabea分离培养
检测结果
检验结论
备注:月桂基硫酸盐胰蛋白胨发酵阳性管转种培养实验:1.复发酵:+/+表示产酸、产气为阳性;-/-表示不产酸、不产气为阴性;+/-表示产酸、不产气。接种量在1ml以上者,用双料发酵管;1ml以下者,用单料发酵管。
检验员:审核人:审核时间:
大肠菌群检测原始记录
室温:湿度:
样品名称
规格
检验类别
出厂检验
抽样基数
抽样方式
抽样数量
检测依据
GB/T4789.3-2010
接种时间
使用主要仪器
恒温培养箱
报告时间
样号
培养温度、时间
培养基名称
结果判定报告数(MPN)/100ml(g)
36±1℃24h±2
微生物检验原始记录范本
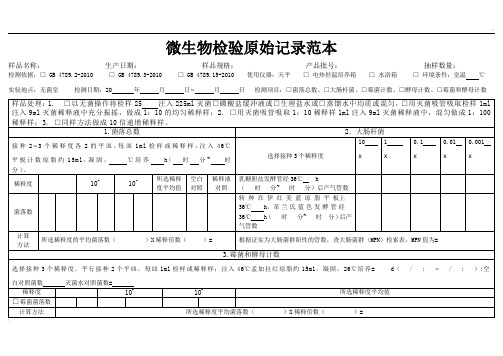
样品名称:生产日期:样品规格:产品批号:抽样数量:
检测依据:□ GB4789.2-2010□GB 4789.3-2010□GB 4789.15-2010使用仪器:天平□ 电热恒温培养箱 □ 水浴箱 □ 环境条件:室温℃
实验地点:无菌室检测日期:20年月日~月日检测项目:□菌落总数、□大肠杆菌、□霉菌计数、□酵母计数、□霉菌和酵母计数
稀释度
10-
ቤተ መጻሕፍቲ ባይዱ10-
所选稀释度平均值
□霉菌菌落数
计算方法
所选稀释度平均菌落数()X稀释倍数( )=
□霉菌菌落数
计算方法
所选稀释度平均菌落数()X稀释倍数( )=
检验菌落总数大肠菌群霉菌 酵母
结果:cfu/MPN/100计数cfu/计数cfu/
检测者: 审核者:
1.菌落总数
2.大肠杆菌
接种2~3个稀释度各2的平皿,每皿1ml检样或稀释样,注入46℃平板计数琼脂约15ml,凝固,℃培养h(时分~时分)。
选择接种3个稀释度
10
x
1
x
0.1x
0.01x
0.001x
稀释度
10-
10-
所选稀释度平均值
空白对照
稀释液对照
乳糖胆盐发酵管经36℃h
(时 分~时分)后产气管数
菌落数
转 种 在 伊 红 美 蓝 琼 脂 平 板上36℃h,革兰氏蓝色发酵管经36℃h(时分~时 分)后产气管数
计算 方法
所选稀释度的平均菌落数( )X稀释倍数( )=
根据证实为大肠菌群阳性的管数,查大肠菌群(MPN)检索表,MPN值为=
3.霉菌和酵母计数
选择接种3个稀释度,平行接种2个平皿,每皿1ml检样或稀释样;注入46℃孟加拉红琼脂约15ml,凝固,26℃培养=d( / :~/ : );空白对照菌数灭菌水对照菌数=
公共场所空气微生物检验原始记录

公共场所空气微生物检验原始记录日期:XXXX年XX月XX日地点:XXXX公共场所(如:商场/学校/医院等)检验目的:本次检验旨在对XXXX公共场所的空气中微生物进行检测,以评估其空气质量和卫生状况。
检验方法:1.采样器选择:使用一次性采样器进行操作,以避免交叉感染和污染。
2.采样时间:每次采样时间为15分钟,分为两个时间段,分别为上午XX时XX分至上午XX时XX分和下午XX时XX分至下午XX时XX分。
3.采样位置:根据公共场所的不同区域,选取代表性的区域进行采样。
包括但不限于入口处、办公区、卫生间、通道等区域。
4. 采样方法:将采样器放置在距离地面1.5米的位置,打开采样器电源并调整合适的流量(通常为1.0L/min),进行采样。
5.采样器编号:每个采样位置的采样器都标有唯一的编号,以避免混淆。
检验结果:上午采样结果:位置1(入口处):XXXCFU/m^3位置2(办公区):XXXCFU/m^3位置3(卫生间):XXXCFU/m^3位置4(通道):XXXCFU/m^3下午采样结果:位置1(入口处):XXXCFU/m^3位置2(办公区):XXXCFU/m^3位置3(卫生间):XXXCFU/m^3位置4(通道):XXXCFU/m^3结论与建议:1.根据检测结果,XXXX公共场所的空气中微生物的总数超出了标准范围,表明空气质量较差。
2.位置X(如:卫生间)的微生物数目明显高于其他位置,建议加强该区域的清洁和消毒工作。
3.建议在公共场所增加通风设施,以提高空气流通和减少微生物滋生的可能性。
4.对于公共场所,尤其是人员流通频繁的区域,定期进行微生物检测,并根据检测结果进行相应的清洁和卫生措施。
注意事项:1.检验前,确保采样器的清洁和消毒,以避免外部污染对结果的影响。
2.检验时,避免对采样器进行过度触摸,以防手部细菌污染采样器。
检验人员签名:____________________。
消毒医疗器材微生物检验原始记录精选全文
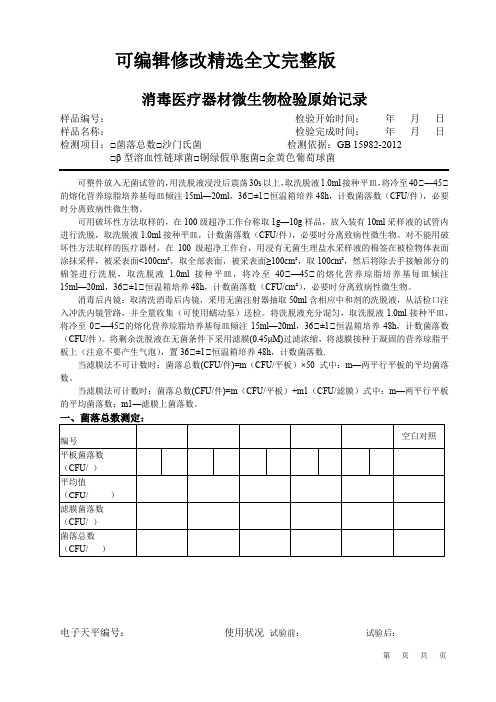
可编辑修改精选全文完整版消毒医疗器材微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:□菌落总数□沙门氏菌检测依据:GB 15982-2012□β型溶血性链球菌□铜绿假单胞菌□金黄色葡萄球菌可整件放入无菌试管的,用洗脱液浸没后震荡30s以上,取洗脱液1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件),必要时分离致病性微生物。
可用破坏性方法取样的,在100级超净工作台称取1g—10g样品,放入装有10ml采样液的试管内进行洗脱,取洗脱液1.0ml接种平皿,计数菌落数(CFU/件),必要时分离致病性微生物。
对不能用破坏性方法取样的医疗器材,在100级超净工作台,用浸有无菌生理盐水采样液的棉签在被检物体表面涂抹采样,被采表面<100cm²,取全部表面,被采表面≥100cm²,取100cm²,然后将除去手接触部分的棉签进行洗脱,取洗脱液 1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/cm²),必要时分离致病性微生物。
消毒后内镜:取清洗消毒后内镜,采用无菌注射器抽取50ml含相应中和剂的洗脱液,从活检口注入冲洗内镜管路,并全量收集(可使用蠕动泵)送检。
将洗脱液充分混匀,取洗脱液1.0ml接种平皿,将冷至0℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件)。
将剩余洗脱液在无菌条件下采用滤膜(0.45μM)过滤浓缩,将滤膜接种于凝固的营养琼脂平板上(注意不要产生气泡),置36℃±1℃恒温箱培养48h,计数菌落数.当滤膜法不可计数时:菌落总数(CFU/件)=m(CFU/平板)×50式中:m—两平行平板的平均菌落数。
微生物检测原始记录

菌落总数与大肠菌群检验原始记录
共页第页
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时 --- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:温馨提示:最好仔细阅读后才下载使用,万分感谢!。
微生物检验原始记录

微生物检验原始记录日期:20XX年X月X日实验人员:XXX实验目的:1.研究不同物质对微生物生长的影响;2.测定微生物在不同条件下的生长速率;3.探究微生物在不同温度下的生长变化。
实验材料:1.维生素B1溶液(10g/L);2.蔗糖溶液(10g/L);3.葡萄糖溶液(10g/L);4.酪蛋白溶液(10g/L);5.红藻提取物溶液(10g/L);6.无菌琼脂培养基;7.无菌平板;8.无菌试管。
实验步骤:1.制备无菌培养基1)加热琼脂培养基至溶解;2)将溶解的琼脂培养基加入试管内;3)用无菌胶头滴管将培养基均匀地分注于无菌平板上;4)将平板培养基放置于室温下,待其凝固。
2.将维生素B1溶液、蔗糖溶液、葡萄糖溶液、酪蛋白溶液和红藻提取物溶液分别加入无菌试管中,每种物质各占10个试管。
3.将每个试管中的液体用无菌胶头滴管均匀地分注于不同编号的无菌平板上。
4.打开消毒柜门,将作用于琼脂培养基的紫外灯打开并进行照射,确保平板完全消毒。
5.在实验室的洁净工作台上,用无菌移液器将各个试验组织的接触培养基的无菌操作。
6.将分配彼此间较远、避免相互干扰的生长时间的培养基标上编号,放入恒温箱中。
7.将标注为控制组的培养基放置于室温下,其余的培养基分别放置在不同温度的恒温箱(30℃、37℃、4℃)中,进行培养。
8.在培养基上观察微生物生长情况,并记录观察结果。
实验结果:在维生素B1溶液的培养基中,观察到微生物在两天后有较好的生长情况,在第四天生长速率达到最高峰。
在蔗糖溶液的培养基中,微生物在一天后开始生长,并在第二天迅速增加,但随后生长速率略有下降。
在葡萄糖溶液的培养基中,微生物在一天后开始生长,但生长速率较缓慢,在第三天达到峰值。
在酪蛋白溶液的培养基中,微生物在一天后开始生长,并在第二天显著增加,但在第三天数量趋于稳定。
在红藻提取物溶液的培养基中,微生物在两天后开始生长,生长速率相对较慢,但在第五天达到最高峰值。
在不同温度下的培养基中,观察到微生物在30℃的恒温箱中生长速率最快,37℃次之,而在4℃的恒温箱中微生物生长速率非常缓慢。
微生物限度检验原始记录模板
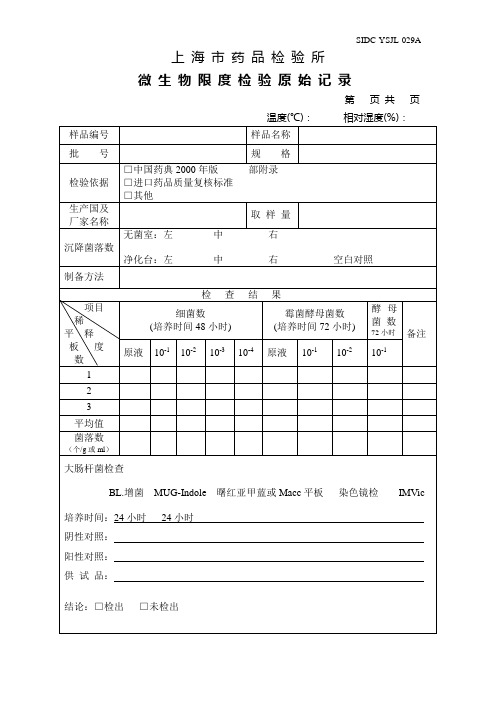
阳性对照:
供试品:
结论:□检出□未检出
沙门氏菌检查
肉汤增菌四硫磺酸钠亮绿胆盐硫乳或Macc平板三糖铁琼脂斜面
培养时间:24小时24小时24小时
阴性对照:
阳性对照:
供试品:
结论:□检出□未检出
金黄色葡萄球菌检查
亚碲酸钠肉汤增菌卵黄高盐或甘露醇高盐平板染色镜检血浆凝固酶试验
培养时间:24小时24小时
阴性对照:
阳性对照:
供试品:
结论:□检出□未检出
铜绿假单胞菌检查
BL增菌溴化十六烷基三甲铵平板染色镜检氧化酶试验绿脓菌素试验
培养时间:24小时24小时
阴性对照:
阳性对照:
供试品:
结论:□检出□未检出
活螨:□检出□未检出
其他检验方法:
结论
□(均)符合规定 □(均)不符合规定
检验者:校对者:审核者:
日期:日期:日期:
制备方法
检查结果
项目
稀
平释
板度
数
细菌数
(培养时间48小时)
霉菌酵母菌数
(培养时间72小时)
酵母菌数
72小时
备注
原液
10-1
10-2
10-3
10-4
原液
10-1
10-2
10-1
1
2
3
平均值
菌落数
(个/g或ml)
大肠杆菌检查
BL.增菌MUG-Indole曙红亚甲蓝或Macc平板染色镜检IMVic
培养时间:24小时24小时
上海市药品检验所
微生物限度检验原始记录
第 页 共 页
温度(℃): ቤተ መጻሕፍቲ ባይዱ对湿度(%):
药品微生物限度检验原始记录

委托检验协议书
(甲方)委托方:阳江市人民医院
(乙方)受委托方:阳江市检测检验中心
由于甲方有部分制剂检验项目尚未能检验,为了保证制剂质量和临床用药安全,甲方特委托乙方对甲方生产的制剂进行以下项目检验:
1.中药制剂成品的薄层色谱法鉴别检查;
2.中药制剂成品的微生物限度检测;
乙方对每批送检品的检验完成周期为10个工作日,每批检品数量为4瓶,并参照国家发改委和财政部[2003]213号收费标准收取药品检验费用(具体价格见附件1),乙方出具的检验报告书仅对甲方送检的样品负责,双方按照委托合同条款执行,时间从2016年9月1日起至2018年9月1日止。
此合同一式二份,双方各执一份。
(甲方)委托方:阳江市人民医院(乙方)受委托方:阳江市检测检验中心负责人:负责人:
年月日年月日。
微生物检测原始记录

微生物检测原始记录XXXX检测有限公司菌落总数与大肠菌群检验原始记录共页第页样品名样品编号仪器设仪器设备检验依检验环境温度:一、菌落总数cfu/ml(g) 培养基名称:培养温度:培养时间:年月日时--- 年月日时稀释倍数空白∕稀释液对照原液10-1 10-2 10-3 10-4平板1平板2平均值检测结果:二、大肠菌群MPN/100ml(g)培养基名称:培养温度:培养时间:年月日时--- 年月日时LST发酵1m l×30.1m l×30.01m l×3初发酵结果复发酵试验检测结果主检:年月日校核:年月日XXXX检测有限公司菌落总数和大肠菌群检测原始记录共页第页样品名称样品编号仪器设备名称仪器设备编号检验环境温度:湿度:检验依据GB4789.2-2010GB4789.3-2010一、菌落总数cfu/ml(g) 培养基名称:培养温度:36±1℃培养时间:年月日时--- 年月日时样品数稀释倍数样1样2样3样4样5平板1 平板2 平板1 平板2 平板1 平板2 平板1 平板2 平板1 平板2原液10-110-210-310-4空白对照检验结果二、大肠菌群cfu/ml(g) 培养基名称:培养温度:36±1℃培养时间:年月日时--- 年月日时样品数稀释倍数样1样2样3样4样5平板1 平板2 平板1 平板2 平板1 平板2 平板1 平板2 平板1 平板2原液10-1 10-2 10-3 10-4空白对照验证试验检验结果主检:年月日校核:年月日XXXX检测有限公司水质微生物检验原始记录共页第页样品名称样品编号设备名称检验环境温度:湿度:检验依据一、菌落总数cfu/ml(g) 培养温度:36±1℃稀释倍数原液10-1 10-2 10-3 10-4 10-5 平板1平板2平均值检测结果:二、总大肠菌群MPN/100ml(g)培养温度:36±1℃培养时间:LST培养基10m l×1m l×0.1m l×0.01m l×发酵结果验证试验伊红美蓝琼脂平板革兰氏染色乳糖复发酵检测结果三、大肠埃希氏菌MPN/100ml(g)验证试验自总大肠菌群乳糖发酵试样中的阳性管中取一滴转接种与EC培养基中置44.5℃培养24小时观察伊红美蓝琼脂平板四、耐热大肠菌群MPN/100ml(g)验证试验将总大肠菌群多管发酵法初发酵或产气的管中用无菌金属接种环将试液接种到EC-MUG管中置44.5℃培养24小时观察培养后的EC-MUG管在暗处用波长366nm功率为6W的紫外光灯照射主检:年月日校核:年月日XXXX检测有限公司乳酸菌与大肠菌群检测记录共页第页样品名称样品编号仪器设备名称检验环境温度:湿度:检验依据一、乳酸菌cfu/ml(g) 培养温度:36±1℃培养时间:稀释倍数 原液 10-310-410-510-610-7平板1 平板2平均值检测结果:二、大肠菌群 MPN/100ml (g )培养温度: 培养时间: 年 月 日 时 --- 年 月 日 时LST 发酵 1m l ×3 0.1m l ×3 0.01m l ×3 发酵结果 验证试验 伊红美蓝琼脂平板 革兰氏染色乳糖复发酵检测结果主检:年月日校核:年月日XXXX检测有限公司致病菌检验原始记录共页第页样品样品编仪器仪器设检验温度:湿度:致病菌培养温度:培养时间:年月日时--- 年月日时金黄色葡萄球菌(定性检验)检验依据:25g样品+225ml7.5%氯化钠肉汤,均质将上述培养物,分别划线接种到Baird-Parker和血平板涂片染色观察溶血血浆凝固酶试验实验现象检测结果前增菌增菌分离沙门氏菌检验依据:25g样品+225mlBPW,均质将上述培养物,分别取1ml转接种于10mlTTB与10mlSC内,进行前增菌再次将上述培养物,分别划线接种于BS琼脂平板XLD琼脂平板生化试验实验现象检测结果志贺氏菌检验依据:25g样品+225mlGN增菌液将上述培养物分别划线接种于HE平板和EMB平板划线接种TSI,葡萄糖半固体生化试验实验现象检测结果溶血性链球菌检验依据:25g样品+225ml生理盐水,吸取5ml接种于50ml葡萄糖肉汤曾菌,划线接种于血平板涂片染色观察溶血血浆凝固酶试验实验现象检测结果主检:年月日校核:年月日XXXX检测有限公司霉菌和酵母菌检验原始记录页第页样品名样品编仪器设仪器设检验依检验环温度:培养基培养温度:28±1℃培养时间:年月日时--- 年月日时:观察培养培养温观察时观察结果第1天第2天第3天第4天第5天观察结菌落计数:培养温度:28±1℃培养时间:年月日时--- 年月日时稀释空白∕稀释液对照原液10-1 10-2 10-3 10-4 平板1平板2平均检测主检:年月日校核:年月日XXXX检测有限公司商业无菌检验原始记录页第页样品名称样品编号仪器名称检验环境温度:湿度:仪器编号检验依据1、保温试验:将完整试样一份置于36±1℃培养箱保温十天,每天观察胖听、泄漏现象。
微生物检测原始记录

XXXX检测有限公司
令狐采学
菌落总数与大肠菌群检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
菌落总数和大肠菌群检测原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
致病菌检验原始记录共页第页
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
共页第页
培养温度:28±1℃培养时间:年月日时年月日
时:
菌落计数:
培养温度:28±1℃培养时间:年月日时年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
微生物检测原始记录模版

菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。
28微生物限度检测原始记录
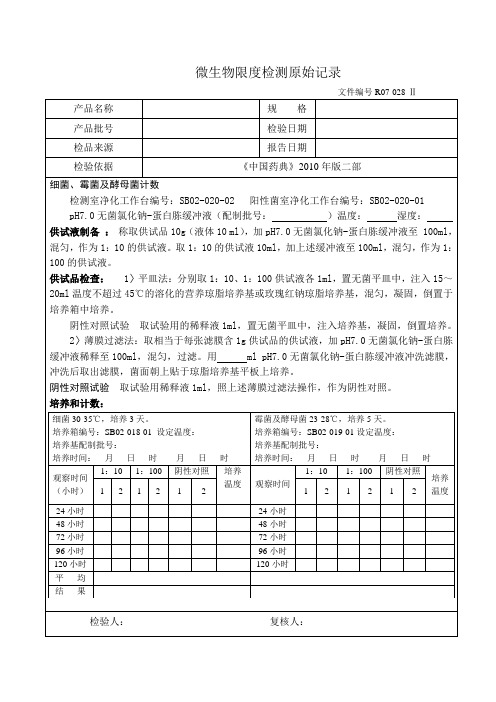
检验人:复核人:
微生物限度检测原始记录
文件编号R07-028-Ⅱ
产品名称
规格
产品批号
检验日期
试验方法
培养箱编号
培养温度
培养
时间
结果
供试品
培养
温度
观察时间
1:10
1:100
阴性对照
培养
温度
1
2
1
2
1
2
1
2
1
2
1
2
24小时
24小时
48小时
48小时
72小时
72小时
96小时
96小时
120小时
120小时
平均
结果
检验人:复核人:
微生物限度检测原始记录
文件编号R07-028-Ⅱ
产品名称
规格
产品批号
检验日期
控制菌检查:大肠埃希菌
大肠埃希菌批号:营养肉汤培养基配制批号:
阳性对照试验阳性对照试验方法同供试品的检查,对照菌加菌量为10-100cfu。
阴性对照试验取稀释液10ml照控制菌检查法检查。
试验方法
培养箱编号
培养温度
培养时间
结果
供试品
阳性对照
阴性对照
营养肉汤
编号:SB02-018-01
TTB
编号:SB02-018-01
DHL
编号:SB02-018-01
MacC
编号:SB02-018-01
细菌30-35℃,培养3天。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XXXX检测有限公司
菌落总数与大肠菌群检验原始记录
共页第页主检:
菌落总数和大肠菌群检测原始记录
共页第页
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
水质微生物检验原始记录
共页第页
主检:年月日校核:年月日
XXXX检测有限公司
乳酸菌与大肠菌群检测记录
共页第页主检:
XXXX检测有限公司
致病菌检验原始记录
共页第页
XXXX 检测有限公司 主检:
年 月 日 校核:
主检: 年 月 日 校核: 年 月 日
XXXX 检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
商业无菌检验原始记录
共页第页
XXXX检测有限公司
主检日期校核日期。
