微生物检验记录表
微生物检验记录表
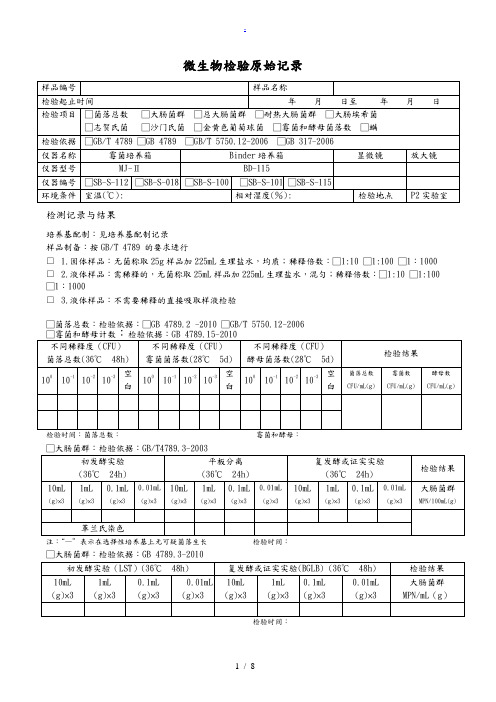
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物检验原始记录表
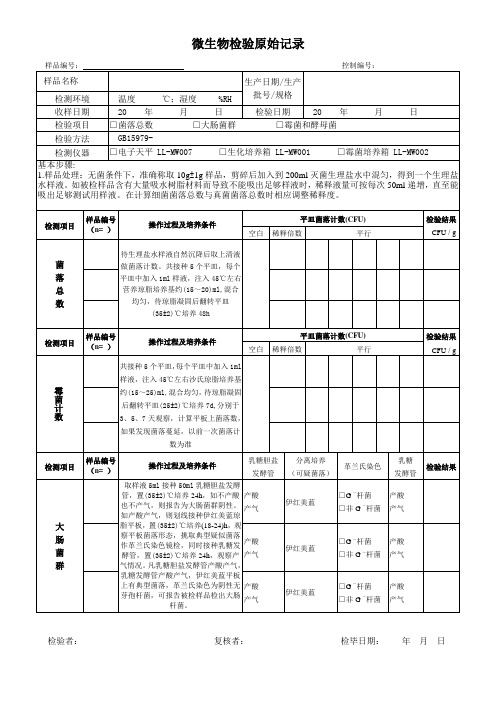
生产日期/生产批号/规格
检测环境
温度 ℃;湿度 %RH
收样日期
20 年 月 日
检验日期
20 年 月 日
检验项目
□菌落总数 □大肠菌群 □霉菌和酵母菌
检验方法
GB15979-
检测仪器
□电子天平LL-MW007□生化培养箱LL-MW001□霉菌培养箱LL-MW002
基本步骤:
1.样品处理:无菌条件下,准确称取10g±1g样品,剪碎后加入到200ml灭菌生理盐水中混匀,得到一个生理盐水样液。如被检样品含有大量吸水树脂材料而导致不能吸出足够样液时,稀释液量可按每次50ml递增,直至能吸出足够测试用样液。在计算细菌菌落总数与真菌菌落总数时相应调整稀释度。
检测项目
样品编号(n=)
操作过程及培养条件乳Fra bibliotek胆盐发酵管
分离培养
(可疑菌落)
革兰氏染色
乳糖
发酵管
检验结果
大
肠
菌
群
取样液5ml接种50ml乳糖胆盐发酵管,置(35±2)℃培养24h,如不产酸也不产气,则报告为大肠菌群阴性。如产酸产气,则划线接种伊红美蓝琼脂平板,置(35±2)℃培养(18-24)h,观察平板菌落形态,挑取典型疑似菌落作革兰氏染色镜检,同时接种乳糖发酵管,置(35±2)℃培养24h,观察产气情况。凡乳糖胆盐发酵管产酸产气,乳糖发酵管产酸产气,伊红美蓝平板上有典型菌落,革兰氏染色为阴性无芽孢杆菌,可报告被检样品检出大肠杆菌。
样品编号(n=)
操作过程及培养条件
平皿菌落计数(CFU)
检验结果
CFU/g
空白
稀释倍数
平行
霉菌计数
共接种5个平皿,每个平皿中加入1ml样液,注入45℃左右沙氏琼脂培养基约(15~25)ml,混合均匀,待琼脂凝固后翻转平皿(25±2)℃培养7d,分别于3、5、7天观察,计算平板上菌落数,如果发现菌落蔓延,以前一次菌落计数为准
微生物检验记录表

微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物检验记录簿表格
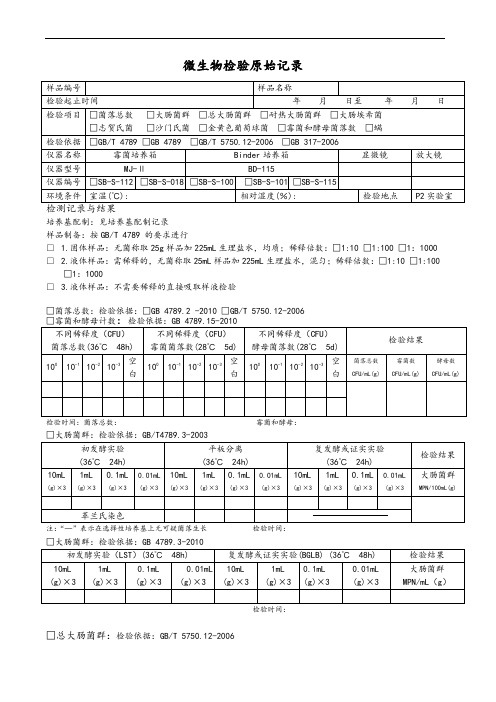
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物限度检查记录版
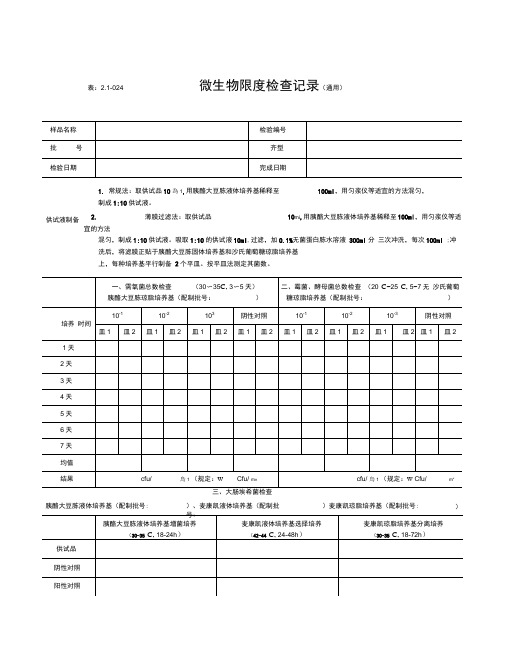
表:2.1-024微生物限度检查记录(通用)1. 常规法:取供试品10為1,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
2. 薄膜过滤法:取供试品10mi ,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
吸取1:10的供试液10ml ,过滤,加0.1%无菌蛋白胨水溶液 300ml 分 三次冲洗,每次100ml ;冲洗后,将滤膜正贴于胰酪大豆胨固体培养基和沙氏葡萄糖琼脂培养基 上,每种培养基平行制备 2个平皿。
按平皿法测定其菌数。
胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批)麦康凯琼脂培养基(配制批号: )供试液制备微生物限度检查记录、需氧菌总数检查30〜353〜5)、霉菌、酵母菌总数检查20C〜25C,5〜7天)三糖铁琼脂斜面穿刺接种 (18〜24h )三、控制菌检查 (30-35 C )检验者:表:2.1-024号:结论本品经按《中国药典》2015年版“非无菌产品微生物限度检查法”进行检验,结果审核者:微生物限度检查记录(丸剂)供试液制备供试液。
胰酪大豆胨增菌 (18〜24h )RV 沙门选择培养木糖赖氨酸脱氧胆酸分离培养(18〜48h )胰酪大豆胨液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)四、沙门菌检查 (30 °C 〜35C ) 胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:五、耐胆盐革兰阴性菌检杳胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:审核者:检验者: 表:2.1-024阴性对照阳性对照三、大肠埃希菌检查)、麦康凯液体培养基(配制批结果□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出/g)四、沙门菌检查(30°C〜35C)胰酪大豆东液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:、表: 2.1-024 微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)审核者:检验者:表:2.1-024 微生物限度检查记录(30〜353〜5天)、霉菌、酵母菌总数检查20C〜25C, 5〜7天)1、 口服液体药用聚酯瓶:取数个试瓶,加入1/2标示容量的氯化钠注射液,将盖旋紧,振摇1分钟,即得供试液。
微生物检验原始记录
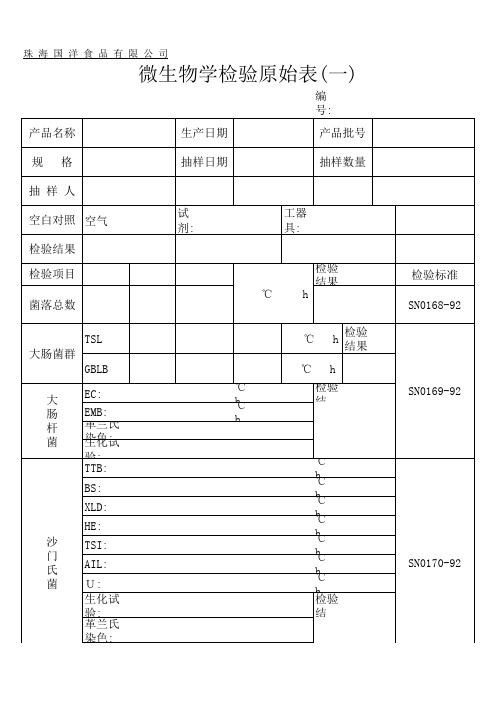
染色:
TCBS: 无盐胰
胨水: 副 30g/L: 溶 NaCl三 性 糖革铁兰琼氏 弧 染色: 菌 70g/L:
100g/L: 生化试
验: TCBS:
T1N1: 氧酶试
验:
霍 TSI:
乱 弧
KIA:
菌 AGS:
T1N0:
T1N3: 生化试 验:
寄生虫
℃ h
℃ h℃ h
粘丝试 验:
℃ h℃ h
编 号: ℃ h ℃ h ℃ h 检验 结
℃ h℃ h℃ h℃ h
检验 结
℃ h℃ h
℃ h℃ h℃ h检验 结
检验 结
SN0172-92 SN0173-92 SNT1022-2001 93/140/EEC
检验日期: 检 验 员:
验讫 日审 核:
报告 日 复 核:
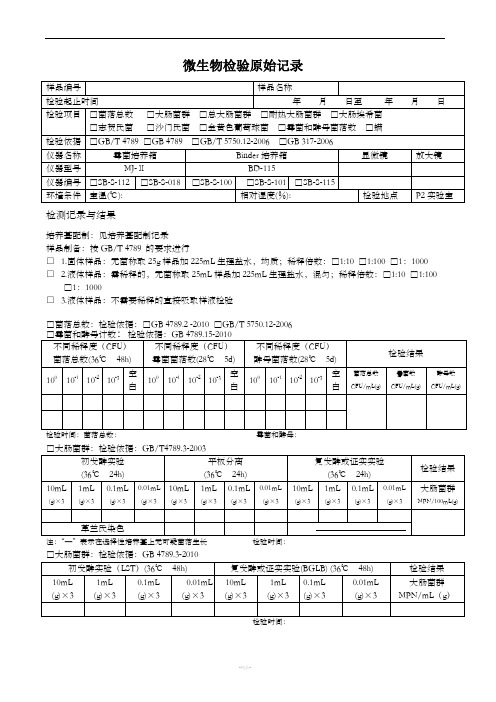
珠海国洋食品有限公司
微生物学检验原始表(一)
编 号:
产品名称
生产日期
产品批号
规格
抽样日期
抽样数量
抽样人 空白对照 空气 检验结果 检验项目 菌落总数
试
工器剂:具:来自检验结果℃
h
TSL 大肠菌群
GBLB
大 EC: 肠 EMB: 杆 革兰氏 菌 染生色化:试
验: TTB:
BS:
XLD:
HE: 沙 TSI: 门 氏 AIL: 菌 U:
生化试 验: 革兰氏 染色:
℃
h
检验 结果
℃h
℃
检验
h℃
结
h
℃ h℃ h℃ h℃ h℃ h℃ h℃ h检验 结
检验标准 SN0168-92 SN0169-92
SN0170-92
血清学 试验:
微生物检验记录表

微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789的要求进行
□1.固体样品:无菌称取25g样品加225mL生理盐水,均质:稀释倍数:口1:10 01:100 口1: 1000 □2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀:稀释倍数:口1:10 01:100□ 1: 1000
□3.液体样品:不需要稀释的直接吸取样液检验
口大肠菌群:检验依据:GB/T4789. 3-2003
口大肠菌群:检验依据:GB 4789. 3-2010
口总大肠菌群:检验依据:GB/T 5750. 12-2006
口大肠埃希氏菌:检验依据:GB/T 5750. 12-2006
口致病菌口沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据:DGB 4789. 4-2010 DGB 4789. 5-2012 OGB 4789. 10-2010
GB 317. 4-. 10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(辅料)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
食品企业微生物检验原始记录表

7.5氯化钠肉汤:
鉴别
分离
B-P平板:
血平板:
B-P平板:
血平板:
B-P平板:
血平板:
B-P平板:
血平板:
B-P平板:
血平板:
确证
试验
染色镜检:
血浆凝固酶:
染色镜检:
血浆凝固酶:
染色镜检:
血浆凝固酶:
染色镜检:
血浆凝固酶:
染色镜检:
血浆凝固酶:
原始检验记录人:
自凝性:
菌体抗原(O)鉴定:
鞭毛抗原(H)鉴定:
自凝性:
菌体抗原(O)鉴定:
鞭毛抗原(H)鉴定:
自凝性:
菌体抗原(O)鉴定:
鞭毛抗原(H)鉴定:
金黄色
葡
萄
球
菌cfu/g
增菌
胰胨大豆肉汤:
7.5氯化钠肉汤:
胰胨大豆肉汤:
7.5氯化钠肉汤:
胰胨大豆肉汤:
7.5氯化钠肉汤:
胰胨大豆肉汤:
7.5氯化钠肉汤:
包装完好、干净,符合香港食环署供港要求。
符合要求()
色泽
具有产品应有的色泽。
符合要求()
滋味、气味
具有产品应有的滋味和气味,无异味。
符合要求()
状态
具有产品庆有的状态,无正常视力可见外来异物。
符合要求()
菌
落
总
数cfu/g
取样
数量
样品1
样品2
样品3
样品4
样品5
稀释度
10-1
10-2
10-1
10-2
10-1
10-2
10-1
10-2
10-1
微生物检验记录表
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000
□ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
□总大肠菌群:检验依据:GB/T 5750.12-2006
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
微生物限度检验记录(辅料)。
微生物限度检查记录表格

10^
10-4
阴性对照
10-1
10-2
阴性对照
1
2
平均
结果
cfu/g(规定:wcfu/g)
cfu/g(规定:wcfu/g)
大肠埃希菌检杳口培养条件:30〜35C18〜24h
胆盐乳糖培养基
(批号:)
MUG培养基
(批号:)
靛基质
(批号:)
EMB培养基
(批号:)
镜检、 生化试验
5h
24h
5h
24h
供试品
阴性对照
阳性对照
结果
□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出)
大肠菌群检查口培养条件:30〜35C
乳糖胆盐发酵培养基(18〜
24h)
EMB培养基(18〜24h)
(批号:)
乳糖发酵培养基(24〜
48h)
供
试
品
10-1
10-2
10-3
阴性对照
阳性对照
结果
个/g(规定:v个/
活螨检杳□
检杳方法
□直接法
□漂浮法□分离法
结果
□检出活螨
□未检出活螨
(规定不得检出)
结论
□符合规定
□不符合规定
(2
供试液制备
取供试品g,加入pH7.0无菌氯化钠-蛋白胨缓冲液至ml,混匀。
□研钵法□振摇法
细困、霉困和酵母困计数口
平皿
号
细菌数(30〜35°C3天)
营养琼脂培养基(批号:)
霉菌和酵母菌数(23〜28C5天) 玫瑰红钠琼脂培养基(批号:)
24h
供试品
阴性对照
阳性对照
结果
微生物限度检查记录

取样点
稀释度
碟号1
碟号2
平均
菌落数
总菌落数
报告
菌落数
空白
培养基
名称
标准规定
结论
供试液
玫
瑰
红
钠
培
养
基
不
得
过
25个/25cm2
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
检验人复核人
微生物检查记录(验证)(附页)
表-ZL00124
大肠杆菌检查培养温度(36℃±1℃)始温℃末温℃
细菌菌落数测定培养温度(30℃~35℃)始温℃末温℃
培养时间月日时分至月日时分
取样点
稀释度
碟号1
碟号2
平均
菌落数
总菌落数
报告
菌落数
空白
培养基
名称
标准规定
结论
供试液
营
养
琼
脂
培
养
基
不
得
过
100个
/25cm2
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
供试液
阴性对照
表-ZL00123霉菌菌落数测定培养温度(25℃~28℃)始温℃末温℃
取样点
BL
MUG
I
EMB
(Macc)
革兰氏染色
Lac
IMViC
结果
标准
规定
结论
供试液
不
得
检
微生物检测记录表

平皿号 平皿 1 平皿 2 平皿 3 平皿 4 平皿 5 平均数 结果数 检验结果判定应≤100cfu/g
7 真菌菌落检测
细菌菌落总数
沙氏琼脂培养基批号:
恒温培养箱编号:
设备校准状态:
琼脂凝固后翻转平皿置 25℃±2℃培养 7 天,分别于 3、5、7 天观察,计算平板上菌落数,如果发现菌落 蔓延,以前一次的菌落计数为准。
板 35℃±2℃,培养 24h
5 结果报告:报告结果为阴性结果填写“未检出”,结果未阳性填写“阳性”,检验结果均为“未检出”判定
合格
大肠菌群
绿脓杆菌
金黄色葡球菌
溶血性链球菌
A/0
6 细菌菌落检测
营养琼脂培养基批号:
恒温培养箱编号:
设备校准状态:
待琼脂凝固后翻转平皿置 35℃。培养成 48 小时后,计算平板上的菌落数。
SCDLP 培养基批号: 血琼脂批号:
恒温培养箱编号:
设备校准状态:
SCDLP 培养基 35℃±2℃, 培 养 24h ,血 琼脂 平 板 35℃±2℃,培养 24h 4 溶血性链球菌
葡萄肉汤培养基批号: 血琼脂批号:
恒温培养箱编号:
设备校准状态:
葡萄肉汤培养基 35℃±
2℃,培养 24h,血琼脂平
样品品名称 生产批号 检验依据
1 大肠菌群 乳糖胆盐发酵培养基批号: 35℃±2℃,培养 24h
微生物检测记录表
型号规格 取样数量 报告日期
恒温培养箱编号:
设备校准状态:
2 绿脓杆菌
SCDLP 培养基批号:
恒温培养箱编号:
十六烷三甲基溴化铵琼脂批号:
设备校准状态:
SCDLP 培养基 35℃±2℃, 培养 24h,十六烷三甲基 溴化铵琼脂 35℃±2℃, 培养 24h 3 金黄色葡萄球菌
微生物检验记录表Word版

微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物检验记录1

编号:RSB26-02药品微生物限度检查实验记录ml①匀浆仪挡min ②研钵法③保温振摇法④薄膜过滤法2、水溶性供试品:取供试品g或ml 加入乳化剂(g或ml)3、抑菌性供试品处理方法:取供试品g或ml 加入PH7.0无菌氯化钠-蛋白胨缓冲液ml方法:①培养基稀释法②离心沉淀法③薄膜过滤法④中和法细菌数:30~35℃48h 霉菌(酵母菌)总数:23~28℃72h大肠埃希菌检查35~37℃24h 沙门菌检查活螨检查检验员:复核员:微生物限度检查操作记录复核人:检验人:编号:RSB26-02 药品微生物限度检查实验记录①匀浆仪挡min ②研钵法③保温振摇法④薄膜过滤法2、水溶性供试品:取供试品g或ml 加入乳化剂(g或ml)3、抑菌性供试品处理方法:取供试品g或ml 加入0.9%无菌氯化钠-蛋白胨缓冲溶液ml方法:①培养基稀释法②离心沉淀法③薄膜过滤法④中和法细菌数:30~35℃48h 霉菌(酵母菌)总数:23~28℃72h大肠杆菌检查35~37℃24h 沙门菌检查活螨检查供试品瓶或盒直接检查法集螨法结果编号:RSB27-01无菌检查记录表检品编号: 室温: 湿度:供试液制备:1、常规法供试品瓶(支)无菌0.9%氯钠溶液ml2、非水溶液性供试品供试品瓶(支)加入乳化剂(g或ml)检查法:1、直接法2、薄膜法药液浓度冲洗液用量ml结论:本品按中国药典2005版二部XL.H无菌检查法,结果规定复核者:检验者:编号:RSB26-03 药品微生物限度检查实验记录供试液制备:1、常规法:取供试品g或ml 加入0.9%无菌氯化钠-蛋白胨缓冲液至ml①匀浆仪挡min ②研钵法③保温振摇法④薄膜过滤法2、水溶性供试品:取供试品g或ml 加入乳化剂(g或ml)3、抑菌性供试品处理方法:取供试品g或ml 加入0.9%无菌氯化钠-蛋白胨缓冲液至ml方法:①培养基稀释法②离心沉淀法③薄膜过滤法④中和法细菌数:30~35℃48h 霉菌(酵母菌)总数:23~28℃72h大肠杆菌检查35~37℃24h 沙门菌检查活螨检查供试品瓶或盒直接检查法集螨法结果检验员:复核员:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
