缓冲液的配制以及常用数据
常见缓冲液配制方法

常见缓冲液配制方法
一、介绍
缓冲液是常见的生物或化学反应的催化剂,主要用于维持反应物的酸
碱度在一定的范围内,有利于提高反应效率。
缓冲液有许多种,其配制方
法也多种多样。
下面将介绍常见缓冲液的配制方法,包括常用缓冲液的配
制方法,复合缓冲液的配制方法,以及常见的国际标准缓冲液的配制方法。
二、常用缓冲液的配制方法
1、磷酸缓冲液的配制
磷酸缓冲液是常用的酸性缓冲液,可以根据需要使用不同浓度的磷酸
来配制。
比如,将0.2mol/L的磷酸钠和0.2mol/L的磷酸氢钠混合,可以
得到一种磷酸缓冲液,其碱度为pH7.0。
同样,如果需要制备一种低碱度
的磷酸缓冲液,可以将3mol/L的磷酸钠和3mol/L的磷酸氢钠混合,以得
到其pH值为2.12的缓冲液。
2、碳酸缓冲液配制
碳酸缓冲液是常用的酸性缓冲液,可以根据需要使用不同浓度的碳酸
氢钠来配制。
比如,将0.2mol/L碳酸氢钠和0.2mol/L碳酸钠混合,可以
得到一种碳酸缓冲液,其碱度为pH7.0。
同样,如果需要制备一种低碱度
的碳酸缓冲液,可以将3mol/L碳酸氢钠和3mol/L碳酸钠混合,以得到其pH值为2.12的缓冲液。
3、氨水缓冲液配制
氨水缓冲液是常用的碱性缓冲液。
最全常用缓冲液配方及缓冲范围

最全常用缓冲液配方及缓冲范围缓冲液是一种能够维持溶液pH值相对稳定的溶液。
它可以减少酸碱反应的影响,使物质在酸碱环境中保持稳定。
在生命科学实验室和工业生产中,常用的缓冲液有许多种。
下面是最常用的一些缓冲液配方及其缓冲范围。
1. Phosphate缓冲液:Phosphate缓冲液通常由磷酸二氢盐和磷酸氢二盐组成。
它的pH范围为2.1-7.4,在生物化学和细胞生物学实验中得到广泛应用。
配方1:-0.1M磷酸二氢盐,pH2.0-2.8-0.2M磷酸氢二盐,pH5.8-7.4配方2:-0.1M磷酸二氢盐,pH2.1-3.1-0.2M磷酸氢二盐,pH5.6-7.42. Tris缓冲液:Tris缓冲液由三羟甲基氨基甲烷(Tris)和其酸盐组成。
它的pH范围为7-9,在分子生物学和生化实验中广泛使用。
配方:- 1 M Tris HCl,pH 7.4-9.0- 1 M Tris base,pH 7.0-9.23.MES缓冲液:MES缓冲液是一种针对中性pH值(5.5-6.7)的缓冲液,常用于细胞生物学和酶活性实验。
配方:-0.1MMES,pH5.5-6.74.HEPES缓冲液:HEPES缓冲液是一种适用于细胞培养和酶活性实验的缓冲液,其pH 范围为6.8-8.2配方:-0.1MHEPES,pH6.8-8.25.CAPS缓冲液:CAPS缓冲液是一种适用于生化实验的缓冲液,其pH范围为9.7-11.1配方:-0.1MCAPS,pH9.7-11.1这些是最常用的缓冲液配方及其缓冲范围,可以根据实验的需要选择合适的缓冲液。
需要注意的是,在配制缓冲液时应使用高纯度的化学品,并根据实验要求精确控制缓冲液的pH值。
此外,在实验过程中应注意缓冲液的保存和稳定性,以确保实验结果的准确性。
缓冲液的配制以及常用数据

缓冲液的配制以及常用数据附录10 常用缓冲溶液的配制(一)磷酸缓冲液母液:A:0.2mol/L Na2HPO4溶液;Na2HPO4·2H2O 35.61g,或Na2HPO4·7H2O 53.65g,或Na2HPO4·12H2O 71.64g,用蒸馏水溶至1 000mL。
B:0.2mol/L NaH2PO4溶液;NaH2PO4·H2O 27.6g或NaH2PO4·2H2O 31.2g, 用蒸馏水溶至1 000mL。
(二)Tris缓冲液母液:A:0.2 mol/L三羟甲基氨基甲烷(Tris)(24.2g溶至1 000 mL)。
B:0.2 mol/L HClA:50 mL + B:x mL,稀释至200 mL。
(三)醋酸盐缓冲液A:0.2 mol/L醋酸液(11.55 mL稀释至1 000 mL)。
B:0.2 mol/L醋酸钠溶液(16.4 g C2H2O2Na或27.2 g C2H2O2Na·3H2O 溶至1 000 mL)。
(四)柠檬酸—磷酸缓冲液母液:A:0.1 mol/L柠檬酸溶液(19.21 g溶至1 000 mL)B:0.2 mol/L磷酸氢二钠溶液(53.65 g Na2HPO4·7H2O 或71.7 g Na2HPO4·12H2O溶至1 000 mL)使用时可以每升中加入1 g酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
(六)甘氨酸—盐酸缓冲液(0.05mol/L)甘氨酸相对分子量为75.07,0.2mol/L甘氨酸溶液含15.01g/L。
(七) 甘氨酸—氢氧化钠缓冲液(0.05mol/L)甘氨酸相对分子量为75.07,0.2mol/L甘氨酸溶液含15.01g/L。
(八) 硼砂—氢氧化钠缓冲溶液贮备液A:0.05mol/L硼砂(19.05 g Na2B4O7·10H2O配成1000mL)贮备液B:0.2mol/L氢氧化钠。
各种缓冲液的配制方法
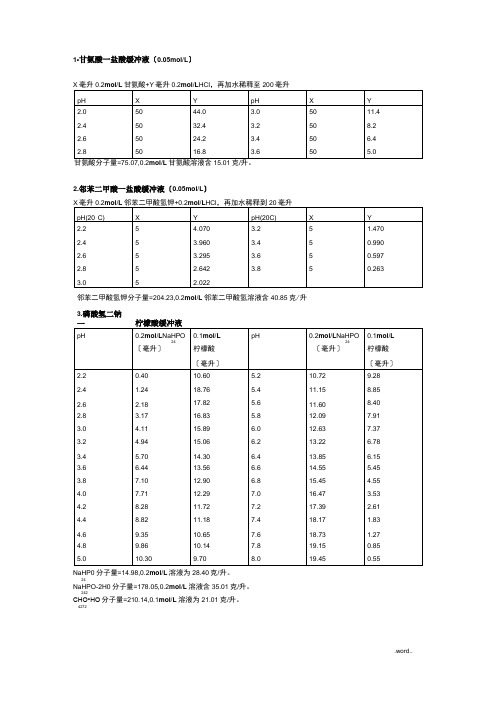
1•甘氨酸一盐酸缓冲液〔0.05mol/L〕=75.07,0.2mol/L15.01/ 2.邻苯二甲酸一盐酸缓冲液〔0.05mol/L〕NaHP0分子量=14.98,0.2mol/L溶液为28.40克/升。
24NaHPO-2H0分子量=178.05,0.2mol/L溶液含35.01克/升。
242CHO•HO分子量=210.14,0.1mol/L溶液为21.01克/升。
42721pH50%柠檬酸CHO•H0:分子量210.14,0.1mol/L溶液为21.01克/升。
6872柠檬酸钠NaCHO•2H0:分子量294.12,0.1mol/L溶液为29.41克/毫升。
36572NaAc•3H0=136.09,0.2mol/L27.22/227.磷酸盐缓冲液NaHPO•2H0分子量=178.05,0.2mol/L溶液为85.61克/升。
242NaHPO•2HO分子量=358.22,0.2mol/L溶液为71.64克/升。
242NaHPO•2HO分子量=156.03,0.2mol/L溶液为31.21克/升。
242NaHPO•2HO分子量=178.05,1/15M溶液为11.876克/升。
242KHPO分子量=136.09,1/15M溶液为9.078克/升。
248•磷酸二氢钾一氢氧化钠缓冲液〔0.05M〕巴比妥钠盐分子量=206.18;0.04M溶液为8.25/10.Tris一盐酸缓冲液〔0.05M,259〕三羟甲基氨基甲烷〔Tris〕HOCH2CH2OHCHOCH2NH2分子量=121.14;0.1M溶液为12.114克/升°Tris溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
硼砂NaBO•HO,分子量=381.43;0.05M溶液〔=0.2M硼酸根〕含19.07克/升。
2472硼酸HBO,分子量=61.84,0.2M溶液为12.37克/升。
23硼砂易失去结晶水,必须在带塞的瓶中保存。
硼砂NaBO•10HO,分子量=381.43;0.05M溶液〔=0.2M硼酸根〕含19.07克/升。
常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液:取5mol/L醋酸溶液,加乙醇60ml和水20ml,用10mol/L 氢氧化铵溶液调节pH值至,用水稀释至1000ml;三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至;三羟甲基氨基甲烷缓冲液:取氯化钙0.294g,加L三羟甲基氨基甲烷溶液40ml 使溶解,用1mol/L盐酸溶液调节pH值至,加水稀释至100ml;三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至;乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液,再用水稀释至250ml;巴比妥缓冲液:取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至,滤过;巴比妥缓冲液:取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml;巴比妥-氯化钠缓冲液:取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中;然后用L盐酸溶液调节pH 值至,再用水稀释至500ml;甲酸钠缓冲液:取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至~;邻苯二甲酸盐缓冲液:取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液必要时用稀盐酸调节pH值至,加水稀释至1000ml,混匀;枸橼酸盐缓冲液:取枸橼酸4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml;枸橼酸盐缓冲液:取%枸橼酸水溶液,用50%氢氧化钠溶液调节pH值至;枸橼酸-磷酸氢二钠缓冲液:甲液:取枸橼酸21g或无水枸橼酸19.2g,加水使溶解成1000ml,置冰箱内保存;乙液:取磷酸氢二钠71.63g,加水使溶解成1000ml;取上述甲液与乙液混合,摇匀;氨-氯化铵缓冲液:取氯化铵 1.07g,加水使溶解成100ml,再加稀氨溶液1→30调节pH值至;氨-氯化铵缓冲液:取氯化铵5.4g,加水20ml溶解后,加浓氯溶液35ml,再加水稀释至100ml;硼砂-氯化钙缓冲液:取硼砂0.572g与氯化钙2.94g,加水约800ml溶解后,用1mol/L盐酸溶液约调节pH值至,加水稀释至1000ml;硼砂-碳酸钠缓冲液~:取无水碳酸钠5.30g,加水使溶解成1000ml;另取硼砂1.91g,加水使溶解成100ml;临用前取碳酸钠溶液973ml与硼砂溶液27ml,混匀;硼酸-氯化钾缓冲液:取硼酸3.09g,加L氯化钾溶液500ml使溶解,再加L 氢氧化钠溶液210ml;醋酸盐缓冲液:取醋酸铵25g,加水25ml溶解后,加7mol/L盐酸溶液38ml,用2mol/L盐酸溶液或5mol/L氨溶液准确调节pH值至电位法指示,用水稀释至100ml,即得;醋酸-锂盐缓冲液:取冰醋酸50ml,加水800ml混合后,用氢氧化锂调节pH 值至,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml;醋酸-醋酸钠缓冲液:取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠18g,加冰醋酸,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至,再加水稀释至100ml;醋酸-醋酸钠缓冲液:取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml;醋酸-醋酸钾缓冲液:取醋酸钾14g,加冰醋酸,再加水稀释至1000ml;醋酸-醋酸铵缓冲液:取醋酸铵7.7g,加水50ml溶解后,加冰醋酸6ml与适量的水使成100ml;醋酸-醋酸铵缓冲液:取醋酸铵100g,加水300ml使溶解,加冰醋酸7ml,摇匀;磷酸-三乙胺缓冲液:取磷酸约4ml与三乙胺约7ml,加50%甲醇稀释至1000ml,用磷酸调节pH值至;磷酸盐缓冲液:取磷酸二氢钠38.0g,与磷酸氢二钠5.04g,加水使成1000ml,即得;磷酸盐缓冲液:甲液:取磷酸,加水至1000ml,摇匀;乙液:取磷酸氢二钠71.63g,加水使溶解成1000ml;取上述甲液与乙液混合,摇匀;磷酸盐缓冲液:取磷酸二氢钾100g,加水800ml,用盐酸调节pH至,用水稀释至1000ml;磷酸盐缓冲液:取L磷酸二氢钠溶液一定量,用氢氧化钠试液调节pH值至;磷酸盐缓冲液:取磷酸二氢钾8.34g与磷酸氢二钾0.87g,加水使溶解成1000ml;磷酸盐缓冲液:取磷酸二氢钾0.68g,加L氢氧化钠溶液,用水稀释至100ml;磷酸盐缓冲液:取磷酸二氢钠1.74g、磷酸氢二钠2.7g与氯化钠1.7g,加水使溶解成400ml;磷酸盐缓冲液含胰酶:取磷酸二氢钾6.8g,加水500ml使溶解,用L氢氧化钠溶液调节pH值至;另取胰酶10g,加水适量使溶解,将两液混合后,加水稀释至1000ml;磷酸盐缓冲液:取L磷酸二氢钾溶液250ml,加L氢氧化钠溶液118ml,用水稀释至1000ml,摇匀;磷酸盐缓冲液:取磷酸二氢钾0.68g,加L氢氧化钠溶液,用水稀释至100ml;磷酸盐缓冲液:取L磷酸二氢钾溶液50ml与L氢氧化钠溶液35ml,加新沸过的冷水稀释至200ml,摇匀;磷酸盐缓冲液:取磷酸氢二钠1.9734g与磷酸二氢钾0.2245g,加水使溶解成1000ml,调节pH值至;磷酸盐缓冲液:取磷酸二氢钾 1.36g,加L氢氧化钠溶液79ml,用水稀释至200ml;磷酸盐缓冲液:取磷酸二氢钾27.22g,加水使溶解成1000ml,取50ml,加L氢氧化钠溶液,再加水稀释至200ml;磷酸盐缓冲液:甲液:取磷酸氢二钠35.9g,加水溶解,并稀释至500ml;乙液:取磷酸二氢钠2.76g,加水溶解,并稀释至100ml;取上述甲液与乙液混合,摇匀;磷酸盐缓冲液~:取磷酸氢二钾 5.59g与磷酸二氢钾0.41g,加水使溶解成1000ml,即得;1.甘氨酸-盐酸缓冲液0.05M:X ml 0.2M甘氨酸 +Y ml 0.2M盐酸再加水稀释至200ml甘氨酸分子量= 0.2M甘氨酸溶液含15.01g/L2.邻苯二甲酸-盐酸缓冲液0.05M:X ml 0.2M邻苯二甲酸氢钾 +Y ml 0.2M盐酸再加水稀释至20ml0.2M邻苯二甲酸氢钾溶液含40.85g/L3.磷酸氢二钠-柠檬酸缓冲液:X ml 0.2M Na2HPO4+Yml 0.1M柠檬酸Na2HPO4分子量= 0.2M溶液含28.40g/LNa2HPO4·2H2O分子量= 0.2M溶液含35.61g/LC6H8O7·H2O分子量= 0.1M溶液含21.01g/L4.柠檬酸-氢氧化钠-盐酸缓冲液先不配使用时可以每升中加入1g酚,若最后pH有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存;5.柠檬酸-柠檬酸钠缓冲液0.1MC6H8O7·H2O分子量= 0.1M溶液含21.01g/L;Na3C6H5O7·2H2O分子量=溶液含29.41g/L6.乙酸-乙酸钠缓冲液0.2MNaAc三水分子量= 0.2M溶液为27.22g/L 7.磷酸盐缓冲液1磷酸氢二钠-磷酸二氢钠缓冲液0.2M X ml 0.2M Na2HPO4/ml +Y ml 0.2M NaH2PO4/mlNa2HPO4·2H2O分子量= 0.2M溶液含35.61g/LNa2HPO4·12H2O分子量= 0.2M溶液含71.64g/LNaH2PO4·H2O分子量= 0.2M溶液含27.6g/LNaH2PO4·2H2O分子量= 0.2M溶液含31.21g/L2 磷酸氢二钠-磷酸二氢钾缓冲液1/15M X ml 1/15M Na2HPO4/ml +Y ml 1/15MKH2PO4/mlNa2HPO4·2H2O分子量= 1/15M溶液含35.61g/L;KH2PO4分子量= 1/15M溶液含9.078g/L8.磷酸二氢钾-氢氧化钠缓冲液0.05M X ml 0.2M KH2PO4+Y ml 0.2M NaOH 再加水稀释至20ml9.巴比妥钠-盐酸缓冲液18℃100 ml 0.04M 巴比妥钠/ml +0.2M 盐酸/ml巴比妥钠分子量= 0.04M 溶液为8.25g/L盐酸缓冲液50ml 0.1M 三羟甲基氨基甲烷Tris 溶液于X ml 0.1M 盐酸混匀后,加水稀释至100ml三羟甲基氨基甲烷Tris 分子量= 0.1M 溶液为12.114g/L; Tris 溶液可以从空气中吸收二氧化碳,使用时注意将瓶盖严; 11.硼酸-硼砂缓冲液0.2M 硼酸根硼砂Na 2B4O 7·10H 2O 分子量= 0.05M=0.2M 硼酸根溶液为19.07g/L 硼砂易失去结晶水,必须在带塞的瓶中保存 硼酸H 3BO 3分子量= 0.2M 溶液为12.37g/L12.甘氨酸-氢氧化钠缓冲液0.05M X ml 0.2M 甘氨酸 +Y ml 0.2M 氢氧化钠 再加水稀释至200ml甘氨酸分子量= 0.2M 甘氨酸溶液含15.01g/L13.硼砂-氢氧化钠缓冲液0.05M 硼酸根X ml 0.05M 硼砂 +Y ml 0.2M 氢氧化钠 再加水稀释至200ml硼砂Na 2B 4O 7·10H 2O 分子量= 0.05M=0.2M 硼酸根溶液为19.07g/L 14.碳酸钠-碳酸氢钠缓冲液0.1M Ca 2+,Mg 2+存在时不得使用Na 2CO 3·10H 2O 分子量= 0.1M 溶液为28.62g/L NaHCO 3分子量= 0.1M 溶液为8.40g/L。
常用缓冲液的配制方法

常用缓冲液的配制方法1.甘氨酸-盐酸缓冲液(0.05M)X ml 0.2M甘氨酸 +Y ml 0.2M盐酸再加水稀释至200mlpH X/ml Y/ml pH X/ml Y/ml2.2 50 44.03.0 50 11.42.4 50 32.43.2 50 8.22.6 50 24.23.4 50 6.42.8 50 16.83.6 50 5.0甘氨酸分子量=75.07 0.2M甘氨酸溶液含15.01g/L2.邻苯二甲酸-盐酸缓冲液(0.05M)X ml 0.2M邻苯二甲酸氢钾+Y ml 0.2M盐酸再加水稀释至200mlpH X Y pH X Y2.2 5 4.6703.2 5 1.4702.4 53.960 3.4 5 0.9902.6 53.295 3.6 5 0.5972.8 5 2.6423.8 5 0.2633.0 5 2.032邻苯二甲酸氢钾分子量=2.4.23 0.2M邻苯二甲酸氢钾溶液含40.85g/L3.磷酸氢二钠-柠檬酸缓冲液pH 0.2M Na2HPO4/ml 0.1M柠檬酸/ml pH 0.2M Na2HPO4/ml 0.1M柠檬酸/ml2.2 0.40 19.6 5.2 10.72 9.282.4 1.24 18.76 5.4 11.15 8.852.6 2.18 17.82 5.6 11.60 8.402.83.17 16.83 5.8 12.09 7.913.04.11 15.896.0 12.637.373.24.94 15.066.2 13.22 6.783.4 5.70 14.30 6.4 13.85 6.153.6 6.44 13.56 6.6 14.555.453.8 7.10 12.90 6.8 15.454.554.0 7.71 12.29 7.0 16.47 3.534.2 8.28 11.72 7.2 17.39 2.614.4 8.82 11.18 7.4 18.17 1.834.6 9.35 10.65 7.6 18.73 1.274.8 9.86 10.14 7.8 19.15 0.855.0 10.30 9.70 8.0 19.45 0.55Na2HPO4分子量=141.98 0.2M溶液含28.40g/LNa2HPO4·2H2O分子量=178.05 0.2M溶液含35.61g/LC6H8O7·H2O分子量=210.14 0.1M溶液含21.01g/L4.柠檬酸-氢氧化钠-盐酸缓冲液pH 钠离子浓度/M 柠檬酸C6H8O7·H2O/g 氢氧化钠NaOH/g 浓盐酸HCl/ml 终体积/L2.2 0.20 210 84 160 103.1 0.20 210 83 116 103.3 0.20 210 83 106 104.3 0.20 210 83 45 105.3 0.35 245 144 68 105.8 0.45 285 186 105 106.5 0.38 266 156 126 10使用时可以每升中加入1g酚,若最后pH有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
实验常用试剂缓冲液的配制方法

实验常用试剂缓冲液的配制方法
一、常用试剂和试剂配置
1、氯仿。
将1L 99.7%纯度的氯仿加入水中,调节pH值至7.4,溶解
即可得到0.5mol/L的氯仿溶液。
2、二氧化碳水。
将100mL弱碳酸氢氧化钠溶液(NaHCO3,0.5mol/L)加入1L水中,经过气泡交换,可制得CO2水。
3、磷酸盐缓冲液。
将200mL磷酸盐溶液(K2HPO4,0.5mol/L)加入800mL水中,调节pH值至7.2,搅拌均匀,即可得到0.2mol/L磷酸盐缓
冲液。
4、EDTA标准溶液。
将25.0g EDTA·4Na(C10H14N2O8Na2)加入
1000mL水中,热溶解,调节pH值至7.0,搅拌均匀,得到0.2mol/LEDTA
标准溶液。
5、肌酐标准溶液。
将10.0g肌酐(C10H13N3O8)=14.2H2O)加入
1000mL的水中,搅拌,调节pH值至7.4,搅拌均匀,即可得到0.1mol/L
的肌酐标准溶液。
二、缓冲液的配置
1、弱酸缓冲液。
将3.0mL 0.2mol/L磷酸钠溶液(Na2HPO4)加入到
97mL 0.2mol/L磷酸钙溶液(Ca(H2PO4)2)中,搅拌均匀,即可得到
0.2mol/L的弱酸缓冲液。
2、弱碱缓冲液。
将3.0mL 0.2mol/L磷酸氢氧化钠溶液(NaH2PO4)
加入到97mL 0.2mol/L碳酸氢钙溶液(Ca(HCO3)2)中,搅拌均匀,即可
得到0.2mol/L的弱碱缓冲液。
3、弱盐缓冲液。
常用的45种缓冲溶液的配制

常用的45种缓冲溶液的配制1.乙醇-醋酸铵缓冲液(pH3.7)取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L 氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml,即得。
2.三羟甲基氨基甲烷缓冲液(pH8.0)取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0,即得。
3.三羟甲基氨基甲烷缓冲液(pH8.1)取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml,即得。
4.三羟甲基氨基甲烷缓冲液(pH9.0)取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g、氯化钠5.8g、乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0,即得。
5.乌洛托品缓冲液取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml,即得。
6.巴比妥缓冲液(pH7.4)取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过,即得。
7.巴比妥缓冲液(pH8.6)取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml,即得。
8.巴比妥-氯化钠缓冲液(pH7.8)取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g 加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml,即得。
9.甲酸钠缓冲液(pH3.3)取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30,即得。
10.邻苯二甲酸盐缓冲液(pH5.6)取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀,即得。
各种缓冲液的配制方法

各种缓冲液的配制方法缓冲液(Buffer)在生物化学和分子生物学实验中起到了至关重要的作用,它可以维持溶液的稳定性,调节pH值,同时还提供所需的离子环境。
这是一个关于不同类型缓冲液的配制方法的综合指南。
1. Tris缓冲液Tris缓冲液是实验室中最常用的缓冲液之一、以下是Tris缓冲液的配制方法:- 配制0.1 M Tris缓冲液(pH 7.4):a. 在100 mL去离子水中加入12.11 g Tris(Tris(hydroxymethyl)aminomethane)粉末。
b.用盖住容器的滤纸纸带覆盖容器,并将其放在磁力搅拌器上。
c.用盖住容器的锡纸覆盖容器,加热至溶解。
搅拌以加速溶解过程。
d.继续搅拌,使其冷却至室温。
e.使用0.1MHCl或0.1MNaOH调节pH值至7.4,直到所需的pH值稳定。
f.用去离子水稀释至总体积100mL。
2.PBS缓冲液PBS缓冲液是生物学实验中常用的缓冲液之一、以下是PBS缓冲液的配制方法:-配制10×PBS缓冲液:a.在1L去离子水中加入80gNaCl,2gKCl,14.4gNa2HPO4,2.4gKH2PO4b.使用10MNaOH或10MHCl调节pH值至7.4c.用去离子水稀释至总体积1L。
-配制1×PBS缓冲液:a.取10×PBS缓冲液100mL,用去离子水稀释至总体积1L。
3.TAE缓冲液TAE缓冲液常用于琼脂糖凝胶电泳。
以下是TAE缓冲液的配制方法:-配制50×TAE缓冲液:a. 在1 L去离子水中加入242 g Tris base,57.1 mL 0.5 M EDTA,100 mL冰醋酸。
b.用10MNaOH或10MHCl调节pH值至8.3c.用去离子水稀释至总体积1L。
-配制1×TAE缓冲液:a.取50×TAE缓冲液20mL,用去离子水稀释至总体积1L。
4. Tris-HCl缓冲液Tris-HCl缓冲液常用于DNA或RNA的酶切反应。
各种缓冲液的配制方法_

各种缓冲液的配制方法_
一、磷酸缓冲液的配制方法
1.准备:蒸馏水或纯净水、磷酸二铵,滴定级别不低于AR级;
2.计算配制用量:根据实验要求,计算出所需磷酸二铵的总量,用m1表示(单位:克);
3.将磷酸二铵加入蒸馏水或纯净水中,用称取出适量的磷酸二铵,用m2表示(单位:克),加入搅拌槽中,充分搅拌均匀,然后加入剩余的磷酸二铵(m3=m1-m2,单位:克),继续搅拌;
4.检查温度:温度应大于室温;
5.检查pH值:用pH计测量溶液的pH值,调整到与实验要求相符的值;
6.搅拌均匀,过滤,储存,可使用或直接投放使用;
二、碳酸缓冲液的配制方法
1.准备:蒸馏水或纯净水、碳酸氢钠,滴定级别不低于AR级;
2.计算配制用量:根据实验要求,计算出所需碳酸氢钠的总量,用m1表示(单位:克);
3.将碳酸氢钠加入蒸馏水或纯净水中,用称取出适量的碳酸氢钠,用m2表示(单位:克),加入搅拌槽中,充分搅拌均匀,然后加入剩余的碳酸氢钠(m3=m1-m2,单位:克),继续搅拌;
4.检查温度:温度应大于室温;
5.检查pH值:用pH计测量溶液的pH值。
各种缓冲液的配制方法

各种缓冲液的配制方法缓冲液是一种用于调节溶液酸碱度(pH值)的溶液,它可以稳定溶液的pH值,满足实验的需要。
不同实验需要使用不同pH值的缓冲液,因此配制方法也会有所不同。
下面将介绍常见的几种缓冲液的配制方法。
1.磷酸盐缓冲液:磷酸盐缓冲液是最常用的一种缓冲液,在生物化学和分子生物学实验中广泛应用。
配制方法:-0.2M磷酸盐酸(pH2.5):用稀磷酸(H3PO4)溶液调节酸度至所需pH值。
-0.2M磷酸盐盐(pH2.5):用0.2M磷酸钠(Na2HPO4)溶液调节碱度至所需pH值。
-混合上述两种液体,按体积比例混合即可配制所需pH值的磷酸盐缓冲液。
2.乙酸缓冲液:乙酸缓冲液常用于酶催化反应的研究和生物制剂的稳定。
配制方法:-0.1M乙酸酸(pH3.6):用浓烧碱(CH3COOH)溶液调节酸度至所需pH值。
-0.1M乙酸盐(pH3.6):用0.1M乙酸钠(CH3COONa)溶液调节碱度至所需pH值。
-混合上述两种液体,按体积比例混合即可配制所需pH值的乙酸缓冲液。
3.碳酸氢盐缓冲液:碳酸氢盐缓冲液常用于生命科学实验中。
配制方法:-0.1M碳酸酸(pH6.0):用稀碳酸(H2CO3)溶液调节酸度至所需pH 值。
-0.1M碳酸盐(pH6.0):用0.1M碳酸氢钠(NaHCO3)溶液调节碱度至所需pH值。
-混合上述两种液体,按体积比例混合即可配制所需pH值的碳酸氢盐缓冲液。
4. Tris缓冲液:Tris缓冲液是一种多用途的缓冲液,在生物化学和分子生物学研究中广泛应用。
配制方法:- 0.1 M Tris酸(pH 8.0):用三羟甲基氨基甲烷(Tris)溶液调节酸度至所需pH值。
- 0.1 M Tris盐(pH 8.0):用0.1 M Tris盐溶液调节碱度至所需pH值。
- 混合上述两种液体,按体积比例混合即可配制所需pH值的Tris缓冲液。
配制缓冲液时需要准备所需浓度的酸液和盐液,然后根据所需pH值逐渐调整酸度和碱度至目标值。
各种缓冲液配制方法

各种缓冲液配制方法不同缓冲液的缓冲范围pH缓冲液是化学实验室中常用的一种试剂,可以帮助维持溶液的酸碱度。
下面介绍三种常用缓冲液的配制方法和缓冲范围。
一、甘氨酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L甘氨酸和Y毫升0.2 mol/L 盐酸,加入适量的水稀释至200毫升。
缓冲范围:pH值在2.2至3.6之间,X和Y的取值见上表。
二、邻苯二甲酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L邻苯二甲酸氢钾和Y毫升0.2 mol/L盐酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至3.8之间,X和Y的取值见上表。
三、磷酸氢二钠-柠檬酸缓冲液配制方法:根据上表中的数据,取相应的0.2 mol/L和0.1 mol/L的Na2HPO4和柠檬酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至8.0之间,具体取值见上表。
以上缓冲液的配制方法和缓冲范围可根据实验需要进行调整和改变。
在实验过程中,正确选择缓冲液可以提高实验的成功率和准确性。
以下是已经修改好的文章:柠檬酸的浓度可以用毫升表示,其浓度数据如下:9.28 mL8.85 mL8.40 mL7.91 mL7.37 mL6.78 mL6.15 mL5.45 mL4.55 mL3.53 mL2.61 mL1.83 mL1.27 mL0.85 mL0.55 mL对于Na2HPO4,其分子量为141.98,0.2 mol/L的溶液需要28.40 g/L。
而Na2HPO4·2H2O的分子量为178.05,0.2 mol/L的溶液需要35.61 g/L。
最后,Na2HPO4·12H2O的分子量为358.22,0.2 mol/L的溶液需要71.64 g/L。
对于C6H8O7·H2O,其分子量为210.14,0.1 mol/L的溶液需要21.01 g/L。
以下是柠檬酸-氢氧化钠-盐酸缓冲液的相关数据:pH: 2.2.3.1.3.3.4.3.5.3.5.8.6.5钠离子浓度(mol/L): 0.20.0.20.0.20.0.20.0.35.0.45.0.38柠檬酸(g) 氢氧化钠(g) 盐酸(mL)C6H8O7·H2O NaOH 97% HCl (浓)210 210 210210 245 285266 84 8383 144 186156 160 116106 45 68105 126最终体积(L):10使用时可以每升中加入1克酚。
标准缓冲液的配制及常用数据.

标准缓冲液的配制及常用数据一、标准缓冲液pH值与温度对照表二、常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X邻苯二甲酸氢钾分子量= 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升Na2HPO4分子量= 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4-2H2O分子量= 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量= 210.14,0.1 mol/L溶液为21.01克/升。
4① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5柠檬酸C 6H 8O 7·H 2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )Na 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液(1Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·2H 2O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
242KH 2PO4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )9巴比妥钠盐分子量=206.18;0.04M 溶液为8.25克/升 10.Tris –盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100毫升。
实验常用试剂缓冲液的配制方法

实验常用试剂缓冲液的配制方法实验室中经常使用各种试剂和缓冲液进行实验。
下面我将介绍一些常用试剂和缓冲液的配制方法。
1.磷酸盐缓冲液磷酸盐缓冲液一般有三种类型的配方:PBS(磷酸盐缓冲盐溶液)、PBST(含Tween-20的磷酸盐缓冲盐溶液)和TBS(三氯甲烷缓冲盐溶液)。
配制PBS缓冲液:-加入适量的8.0g/L氯化钠和0.2g/L磷酸氢二钠到1L去离子水中。
-调整pH值至7.4,采用10M氢氧化钠(NaOH)或者盐酸(HCl)。
-用去离子水稀释至1xPBS。
配制PBST缓冲液:-配制1xPBS。
- 加入0.1%(v/v)Tween-20。
-混合均匀。
配制TBS缓冲液:-加入2.42g/L三氯甲烷到1L去离子水中。
-加入20g/L三甲基氯化胺到溶液中。
-调整pH值至8.0,采用盐酸(HCl)。
-用去离子水稀释至1xTBS。
2.毛细管电泳缓冲液毛细管电泳缓冲液的配制方法取决于电泳类型,一般包括凝胶和毛细管电泳。
配制凝胶电泳缓冲液:-加入8g/L琼脂糖和0.4g/L硼酸到1L去离子水中。
-用热板搅拌器加热,搅拌至溶解。
-冷却至室温后,调整pH值至8.3,采用盐酸(HCl)或氢氧化钠(NaOH)。
-用去离子水稀释至所需浓度。
配制毛细管电泳缓冲液:-加入10mM氢氧化钠(NaOH)和1mM二硼酸氢钠到500mL去离子水中。
-调整pH值至9.2,采用盐酸(HCl)。
-加入1mM十二烷基硫酸钠。
-用去离子水稀释至所需浓度。
3.蛋白质含量测定蛋白质含量测定一般采用BCA法、Lowry法或Bradford法。
BCA法配制试剂:-在15mL玻璃试管中加入BCA试剂(提取液A)。
-加入0.1M硫酸(提取液B)。
-混合提取液A和提取液B,即得到试剂。
Lowry法配制试剂:-加入白蛋白标准品和Na2CO3/NaOH缓冲液(A液)到250mL锥形瓶中。
-混合硫酸/磷酸/酒精试剂(B液)。
-将A液倒入B液中混合,待用。
Bradford法配制试剂:-加入试剂A到450mL去离子水中。
实验室常用试剂缓冲液的配制方法

实验室常用试剂缓冲液的配制方法实验室中常常需要使用各种试剂和缓冲液,以下是一些常用试剂和缓冲液的配制方法及其用途。
1.NaCl溶液配制:NaCl作为实验室常用的盐类试剂,可用于生化、分子生物学等多个实验室操作中。
常用浓度为0.9%(w/v)的生理盐水。
配制方法如下:称取对应质量的NaCl加入蒸馏水中,搅拌溶解,用蒸馏水调整至最终体积。
2.血红蛋白溶液配制:血红蛋白溶液可用于实验室的一些生化、免疫学等实验。
常用方法如下:从新鲜血液中分离出血红蛋白,加入适量的生理盐水或缓冲液,控制pH值为7.4-7.6,并用密闭容器保存。
3. Tris-HCl缓冲液配制:Tris-HCl缓冲液在生物化学实验中广泛应用于DNA/RNA电泳、蛋白质电泳等实验。
常用方法如下:按需求称取Tris固体加入一定量的去离子水中,搅拌溶解,用强碱(比如氢氧化钠)或强酸(比如盐酸)调整pH值至所需范围。
1. Tris缓冲液配制:Tris缓冲液常用于酶反应、凝胶电泳等实验中,配制方法如下:称取适量的Tris固体加入适量的去离子水中,搅拌溶解,用浓盐酸或盐酸调节pH值至所需范围,并用去离子水稀释至最终体积。
2.PBS缓冲液配制:PBS缓冲液在生物学实验中用于细胞培养、免疫染色等操作中。
配制方法如下:称取适量的NaCl、KCl、Na2HPO4、KH2PO4固体加入适量的去离子水中,搅拌溶解,并用去离子水稀释至最终体积,调整pH值至所需范围。
3. Tris-Borate-EDTA(TBE)缓冲液配制:TBE缓冲液常用于核酸凝胶电泳中,配制方法如下:称取适量的Tris固体加入适量的去离子水中,搅拌溶解,用浓盐酸或盐酸调节pH值至所需范围,然后加入Boric acid和EDTA固体,继续搅拌溶解,并用去离子水稀释至最终体积。
以上仅是一些常见的试剂和缓冲液的配制方法,实验室中还会使用到很多其他试剂和缓冲液。
在配制试剂和缓冲液时,需要注意选择合适的纯度的试剂、使用无菌器具和操作台,并遵循相应的实验操作规范和安全要求。
常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液(pH3、7):取5mol/L醋酸溶液15、0ml,加乙醇60ml与水20ml,用10mol/L氢氧化铵溶液调节pH值至3、7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8、0):取三羟甲基氨基甲烷12、14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8、0。
三羟甲基氨基甲烷缓冲液(pH8、1):取氯化钙0、294g,加0、2mol/L三羟甲基氨基甲烷溶液40ml 使溶解,用1mol/L盐酸溶液调节pH值至8、1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9、0):取三羟甲基氨基甲烷6、06g,加盐酸赖氨酸3、65g,氯化钠5、8g,乙二胺四醋酸二钠0、37g,再加水溶解使成1000ml,调节pH值至9、0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4、2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7、4):取巴比妥钠4、42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH 值至7、4,滤过。
巴比妥缓冲液(pH8、6):取巴比妥5、52g与巴比妥钠30、9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7、8):取巴比妥钠5、05g,加氯化钠3、7g及水适量使溶解,另取明胶0、5g加水适量,加热溶解后并入上述溶液中。
然后用0、2mol/L盐酸溶液调节pH值至7、8,再用水稀释至500ml。
甲酸钠缓冲液(pH3、3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中与,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3、25~3、30。
邻苯二甲酸盐缓冲液(pH5、6):取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5、6,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸4、2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
常用pH缓冲液配置方法及注意事项
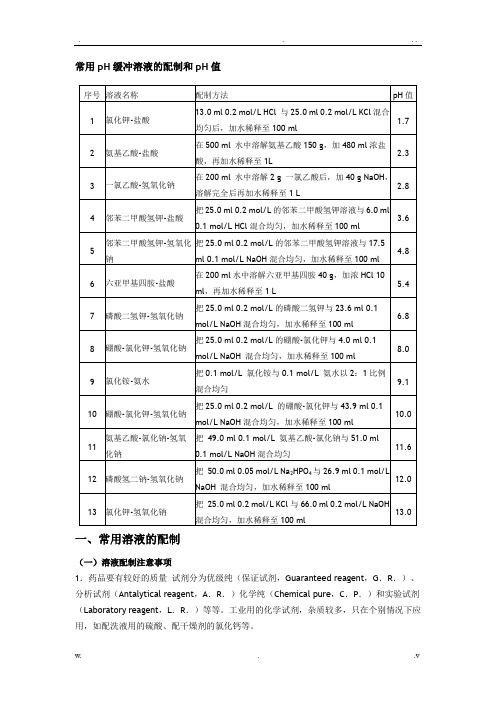
常用pH缓冲溶液的配制和pH值一、常用溶液的配制(一)溶液配制注意事项1.药品要有较好的质量试剂分为优级纯(保证试剂,Guaranteed reagent,G.R.)、分析试剂(Antalytical reagent,A.R.)化学纯(Chemical pure,C.P.)和实验试剂(Laboratory reagent,L.R.)等等。
工业用的化学试剂,杂质较多,只在个别情况下应用,如配洗液用的硫酸、配干燥剂的氯化钙等。
2.药品称量要精确。
3.配制试剂用水应用新鲜的去离子水或双蒸馏水,比电阻值在50万欧姆以上,pH在5.5~7.0之间才可应用,在组织培养等特殊用途时应注意此项要求,配制一般化验用溶液只要求用双蒸馏水或去离子水。
4.配好后的溶液,应立即除菌处理(如高压灭菌、抽滤或加抑菌物质),以防杂菌生长。
(二)0.067(1/15)Mol/L磷酸缓冲液1.1/15Mol/L磷酸二氢钾溶液的配制:称取磷酸二氢钾(KH2PO4,A.R.)9.08g,用蒸馏水溶解后,倾入1000ml容量瓶内,再稀释至刻度(1000ml)。
2.1/15Mol/L磷酸二氢钠溶液的配制:称取无水磷酸氢二钠(Na2HPO4,A.R.)9.47g(或者Na2HPO4·2H2O 11.87g)用蒸馏水溶解后,放入1000ml容量瓶内,再加蒸馏水稀释至刻度(1000ml)。
3.按附表的比例,配制成不同pH值的缓冲溶液。
(三)0.15Mol/L PB液Na2HPO4·2H2O分子量=175.05 0.15Mol/L溶液含26.7g/L。
Na2HPO4·12H2O分子量=358.22 0.15Mol/L溶液含53.7g/L。
NaH2PO4·H2O分子量=138.00 0.15Mol/L溶液含20.7g/L。
NaH2PO4·2H2O分子量=156.03 0.15Mol/L溶液含23.4g/L。
常用标准缓冲溶液的配制

常用标准缓冲溶液在化学分析、仪器分析、生物化学等领域有广泛的应用。
它们通常用于标定传感器、校准仪器、测定物质特性等。
下面将详细介绍如何配制常用标准缓冲溶液。
一、磷酸盐标准缓冲溶液磷酸盐标准缓冲溶液通常用于pH测量。
具体配制方法如下:1. 称取约2克磷酸二氢钾,用纯水溶解。
2. 加入约700ml纯水。
3. 用氢氧化钠溶液调整溶液pH至7.0。
可以使用0.1N氢氧化钠溶液进行调pH。
4. 稀释至总容量为1000ml,这样就得到了磷酸盐标准缓冲溶液。
二、乙酸-乙酸钠缓冲液乙酸-乙酸钠缓冲液常用于PH计的校准。
其配制方法如下:1. 称取无水乙酸钠(28.85g)及乙酸(3mL,约27ml)溶于约500mL纯水中。
2. 用盐酸(1+1)溶液调整溶液pH至3.6~3.8。
3. 稀释至总容量约700mL。
三、纳氏试剂缓冲溶液纳氏试剂是一种常用的显色剂,常用于水质分析等工作中。
缓冲溶液的配制如下:1. 称取三乙醇胺9~15g,加少量纯水溶解,再加入氢氧化钠溶液至pH值约10,即得基本缓冲液。
2. 称取酒石酸钾钠20g及碘化钾2g溶于纯水,稀释至基本缓冲液总容量约50ml,然后慢慢加入碘化汞钾溶液(4%w/v)4~5滴,即得纳氏试剂缓冲溶液。
四、磺基水杨酸标准缓冲溶液磺基水杨酸标准缓冲溶液常用于电位滴定分析,其配制方法如下:1. 称取24克磺基水杨酸,加入约600毫升蒸馏水,完全溶解。
2. 用氢氧化钠溶液调整溶液pH至5.4,使其符合滴定分析要求。
可以使用0.1N氢氧化钠溶液进行调pH。
3. 稀释至总容量约1000ml,这样就得到了磺基水杨酸标准缓冲溶液。
需要注意的是,在配制标准缓冲溶液时,必须严格遵守实验室安全规范,包括正确处理化学药品、避免交叉污染、避免蒸发皿破裂等。
同时,也应注意保护实验环境的卫生和安全,如保持实验台整洁、避免有毒废料的排放等。
此外,对于不同类型和浓度的标准缓冲溶液,可能需要不同的配制步骤和注意事项。
常用缓冲液的配制方法

常用缓冲液的配制方法
一、缓冲液的概念
缓冲液(buffer solution)是一种能够保持溶液的pH值在一定范围
内的溶液,在赋予它特定pH值的同时,缓冲液也具有起到稳定溶液pH的
作用。
比如,在温度或其它参数发生变化的情况下,缓冲液能够促使溶液
的pH值趋于稳定,从而使细胞、酶和其它反应活性的物质的环境稳定。
1、配制pH=6.8的phosphate buffer solution (PBS)
(1)取50ml无菌的水放在一个容量为200ml的玻璃包装容器中;
(2)取5.0gNa2HPO4和1.44gKH2PO4,加入到容器中,搅拌均匀,
直到被完全溶解;
(3)用无菌的水将总量补充到200ml,并搓揉盖部分以保证其中没
有空气;
(4)将缓冲液放到25℃恒温量瓶中,调节pH值到6.8,通常可用
1NNaOH或1NHCl来调节;
(5)滴入5μl 10N NaOH,然后使用pH仪测量,调整pH值到6.8,
并用无菌的水将容量补充到200ml;
(6)将缓冲液置于4℃冷藏或20℃分装,以便日后使用。
2、配制pH=4.5的Citrate buffer solution (CBS)
(1)取50ml无菌的水放在一个容量为200ml的玻璃包装容器中;
(2)取2.7gNa2H2C2O4和2.7gNaHC2O4,加入到容器中,搅拌均匀,直到被完全溶解;
(3)用无菌的水将总量补充到200ml,并搓揉盖部分以保证其中没有空气;。
常用缓冲液配置

实验室常用缓冲液配置方案1)1 M Tris-HCl (pH7.4, 7.6, 8.0)组份浓度:1 M Tris-HCl配制量:1 L配制方法:1. 称量121.1 g Tris置于1 L烧杯中。
2. 加入约800 ml的去离子水,充分搅拌溶解。
4. 将溶液定容至1 L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH值随温度的变化差异很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
2)10×TE Buffer (pH7.4, 7.6, 8.0)组份浓度:100 mM Tris-HCl, 10 mM EDTA配制量:1 L配制方法:2. 向烧杯中加入约800 ml的去离子水,均匀混合。
3. 将溶液定容至1 L后,高温高压灭菌。
4. 室温保存。
3)1.5 M Tris-HCl (pH8.8)组份浓度:1.5 M Tris-HCl配制量:1 L配制方法:1. 称量181.7 g Tris置于1 L烧杯中。
2. 加入约800 ml的去离子水,充分搅拌溶解。
3. 用浓盐酸调节pH值至8.8。
4. 将溶液定容至1 L。
5. 高温高压灭菌后,室温保存。
注意:应使溶液冷却至室温后再调定pH值,因为Tris溶液的pH值随温度的变化差异很大,温度每升高1℃,溶液的pH值大约降低0.03个单位。
4)3 M 醋酸钠(pH5.2)组份浓度:3M 醋酸钠配制量:100ml配制方法:1.称量40.8g NaAc·3H2O置于100-200ml烧杯中,加入月40ml的去离子水搅拌溶解2.加入冰醋酸调节pH值至5.23.加去离子水将溶液定容至100ml4高温高压灭菌后,室温保存。
5)PBS Buffer组份浓度:137 mM NaCl, 2.7 mM KCl, 10 mM Na2HPO4, 2 mM KH2PO4配制量:1 L配制方法:2. 向烧杯中加入约800 ml的去离子水,充分搅拌溶解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附录10 常用缓冲溶液的配制(一)磷酸缓冲液母液:A:0.2mol/L Na2HPO4溶液;Na2HPO4·2H2O 35.61g,或Na2HPO4·7H2O 53.65g,或Na2HPO4·12H2O 71.64g,用蒸馏水溶至1 000mL。
B:0.2mol/L NaH2PO4溶液;NaH2PO4·H2O 27.6g或NaH2PO4·2H2O 31.2g, 用蒸馏水溶至1 000mL。
(二)Tris缓冲液母液:A:0.2 mol/L三羟甲基氨基甲烷(Tris)(24.2g溶至1 000 mL)。
B:0.2 mol/L HClA:50 mL + B:x mL,稀释至200 mL。
(三)醋酸盐缓冲液A:0.2 mol/L醋酸液(11.55 mL稀释至1 000 mL)。
B:0.2 mol/L醋酸钠溶液(16.4 g C2H2O2Na或27.2 g C2H2O2Na·3H2O 溶至1 000 mL)。
(四)柠檬酸—磷酸缓冲液母液:A:0.1 mol/L柠檬酸溶液(19.21 g溶至1 000 mL)B:0.2 mol/L磷酸氢二钠溶液(53.65 g Na2HPO4·7H2O 或71.7 g Na2HPO4·12H2O溶至1 000 mL)使用时可以每升中加入1 g酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
(六)甘氨酸—盐酸缓冲液(0.05mol/L)甘氨酸相对分子量为75.07,0.2mol/L甘氨酸溶液含15.01g/L。
(七) 甘氨酸—氢氧化钠缓冲液(0.05mol/L)甘氨酸相对分子量为75.07,0.2mol/L甘氨酸溶液含15.01g/L。
(八) 硼砂—氢氧化钠缓冲溶液贮备液A:0.05mol/L硼砂(19.05 g Na2B4O7·10H2O配成1000mL)贮备液B:0.2mol/L氢氧化钠。
A:50 ml+B:xml,稀释至200ml。
(九)硼酸—硼砂缓冲液A液(0.05mol/L硼砂):Na2B4O7·10H2O分子量为381.43,0.05mol/L溶液为19.07g/L。
B液(0.2mol/L硼酸):H3BO3分子量为61.84,0.2mol/L的溶液为12.37g/L。
硼砂易失去结晶水,必须在带塞的瓶中保存。
(十)巴比妥钠—盐酸缓冲液(18 oA液(0.04mol/L巴比妥钠)巴比妥钠相对分子质量为206.18,0.04mol/L溶液为8.25g/L. B液(0.2mol/L HCl)。
\附录1 硫酸铵饱和度常用表(一)调整硫酸铵溶液饱和度计算表(25℃)硫酸铵终浓度,饱和度∕%在25℃时,硫酸铵溶液由初浓度调到终浓度时,每升溶液所加固体硫酸铵的克数。
(二)调整硫酸铵溶液饱和度计算表(0℃)硫酸铵终浓度,饱和度∕%*在0℃时,硫酸铵溶液由初浓度调到终浓度时,每100ml溶液所加固体硫酸铵的克数。
附录2 实验中常用酸、碱的比重和浓度的关系名称化学式分子量比重质量分数/%(W / W)物质的量浓度(粗略)/mol·L-1配1L 1mol·L-1溶液所需量/mL盐酸HCl 36.47 1.19 37.2 12.0 841.18 35.4 11.81.10 20.0 6.0硫酸H2SO498.09 1.84 95.6 18.0 281.18 24.8 3.0硝酸HNO363.02 1.42 70.98 16.0 631.40 65.3 14.51.20 32.36 6.1冰醋酸CH3COOH 60.05 1.05 99.5 17.4 59 醋酸CH3COOH 1.075 80.0 14.3 69.93 磷酸H3PO498.06 1.71 85.0 15 67 氨水NH4OH 35.05 0.90 15 670.904 27.0 14.3 700.91 25.0 13.40.96 10.0 5.6氢氧化钠NaOH 40.0 1.5 50.0 19 53 溶液附录3 常用固态酸、碱、盐的物质的量浓度配制参考表名称化学式Mr物质的量浓度/mol·L-1配1L 1mol/L溶液所需量/ g·L-1草酸H2C2O4·2H2O 126.08 1.0 63.04 柠檬酸H3C6H5O7·H2O 210.14 0.1 7.00 氢氧化钾KOH 56.10 5.0 280.50 氢氧化钠NaOH 40.00 1.0 40.00 碳酸钠Na2CO3 106.00 0.5 53.00 磷酸氢二钠Na2HPO4·12H2O 358.20 1.0 358.20 磷酸二氢钾KH2PO4 136.10 1/15 9.08 重铬酸钾K2Cr2O7 294.20 1/60 4.9035 碘化钾KI 166.00 0.5 83.00 高锰酸钾KMnO4158.00 0.05 3.16 乙酸钠NaC2H3O2 82.04 1.0 82.04 硫代硫酸钠Na2S2O3·5H2O 248.20 0.1 24.82名称化学式分子量Mp(℃) BP(℃) 溶解性质性质甲醇CH3OH 32.04 -97.8 64.7 溶于水、乙醇、乙醚、苯等有毒乙醇C2H5OH 46.07 -114.10 78.50 与水及许多有机溶剂混溶易燃丙醇CH3CH2CH2OH 60.09 -127.0 97.20 与水、乙醇、乙醚等混溶对眼有刺激作用异丙醇(CH3)2CHOH 60.09 -88.5 82.5 与水、乙醇、乙氯仿等混溶,不溶于盐溶液易燃丁醇CH3CH2CH2CH2OH 74.12 -90.0 117~118与乙醇、乙醚等多种有机溶剂混溶蒸汽有刺激性戊醇CH3(CH2) 4OH 88.15 -79.0 137.5 与乙醇、乙醚混溶有刺激作用特丁醇(CH3)2COH 74.12 25.6 82.41 溶于水、与乙醇、乙醚混溶丙酮CH3COCH358.08 -94.0 56.5 与水、乙醇、氯仿、乙醚及多种油类混溶挥发性强,易燃,有麻醉性乙醚C2H5OC2H574.12 -116.3 34.6 微溶于水,易溶于浓盐酸与苯氯仿、石油醚及脂肪溶剂易挥发,易燃有麻醉性氯仿CHCL3119.39 -63.5固化61~62易溶于水,能与多种有机溶及油类混溶剂易挥发乙酸乙酯CH3COOC2H588.1 -83.0 77.0溶于水,与乙醇、氯仿、丙酮乙醚混溶易挥发,易燃烧苯C6H678.115.5固化80.1易溶于水,与乙醇、乙醚、氯仿等有机溶剂及油混溶极易燃,有毒甲苯CH3C6H592.13-95固化110.6微溶于水,能与多种有机溶剂混溶易燃,高浓度有麻醉作用二甲苯C6H4(CH3)2106.16 137~140不溶于水,与无水乙醇、乙醚等多种有机溶剂混溶易燃,高浓度有麻醉作用酚C6H5OH 94.11 40.85 182.0 能溶于水,易溶于乙醇、乙醚氯仿、甘油、油。
不溶于石油醚有毒,有腐蚀性浓度有麻醉作用已烷CH3(CH2)4CH386.17 -95~100固化69.0不溶于水,与乙醇、氯仿、乙醚混溶易挥发,易燃,高浓度有麻醉作用环乙烷C2(CH2)4 C284.16 6.47 80.7 不溶于水,与乙醇、乙醚、丙酮苯等混溶易燃,刺激皮肤,高浓度可用于麻醉甲酰胺CH3NO 45.04 2.55 210.5 溶于水,与甲醇、乙醇、丙酮、乙酸、已二醇、甘油等混溶,微溶于、苯、乙醚对皮肤有刺激作用四氯化碳CCl4153.84-23固化76.7易溶于水,能与乙醇、苯、氯仿、乙醚、二硫化碳、石油醚、油等混溶不燃烧,可用于灭火,有毒二硫化碳CS2 76.14 -116.6 46.5难溶于水,与无水甲醇、乙醇、乙醚、苯、氯仿、油类等混溶有毒,有恶臭,极易燃石油醚35.8 不溶于水,能与多种有机溶剂混溶有挥发性,极易燃吡啶C5N5N 79.10-42固化115~116能与水、乙醇、乙醚、石油醚混溶易燃,有刺激作用乙腈C2H3N 41.05 -45 81.6 与水、甲醇、乙酸、甲酯、乙酯、丙酮乙醚等混溶有毒,遇火燃烧附录4 常用有机溶剂及其主要性质附录5 常用酸、碱指示剂中文名英文名变色pH范围酸性色碱性色浓度/ % 溶剂100mL指示剂需0.1mol·L-1NaOH的量/ml间甲酚紫m-Cresol purple 1.2 ~ 2.8 红黄0.04 稀碱 1.05 麝香草酚蓝Thymol blue 1.2 ~ 2.8 红黄0.04 稀碱0.86 溴酚蓝Bromphenol blue 3.0 ~ 4.6 黄紫0.04 稀碱0.6 甲基橙Methyl orange 3.1 ~ 4.4 红黄0.02 水—溴甲酚绿Bromcresol green 3.8 ~ 5.4 黄蓝0.04 稀碱0.58 甲基红Methyl red 4.4 ~ 6.2 红黄0.1 50%乙醇—氯酚红Chlorphenol red 4.8 ~ 6.4 黄红0.04 稀碱0.94 溴酚红Bromphenol red 5.2 ~ 6.8 黄红0.04 稀碱0.78 溴甲酚紫Bromcresolpurple5.2 ~6.8 黄紫0.04 稀碱0.74 溴麝香草酚蓝Bromotymol blue 6.0 ~7.6 黄蓝0.04 稀碱0.64 酚红Phenol red 6.4 ~8.2 黄红0.02 稀碱 1.13 中性红Neutral red 6.8 ~ 8.0 红黄0.01 50%乙醇—甲酚红Cresol red 7.2 ~ 8.8 黄紫红0.04 稀碱 1.05 间甲酚紫m-Cresol purple 7.4 ~9.0 黄紫0.04 稀碱 1.05 麝香草酚蓝Thymol blue 8.0 ~ 9.6 黄蓝0.04 稀碱0.86 酚酞Phenolphthalein 8.2 ~ 10.0 无色紫0.1 96%乙醇—麝香草酚肽Thymolphthalein 9.3 ~ 10.5 无色紫0.1 50%乙醇—茜素黄R Alizarin yellow R 10.0 ~ 12.1 淡黄棕红0.1 50%乙醇—金莲橙O Tropaeolin O 11.1 ~ 12.7 黄红棕0.1 水—附录6 植物组织培养常用培养基矿质盐类MS ER HE SH B5N6大量元素/(mg/L)NH4NO31650 1200 463 KNO31900 1900 2500 2500 2830 CaCl2·2H2O 440 440 75 200 150 166 MgSO4·7H2O 370 370 250 400 250 185 KH2PO4170 340 400 (NH4)2SO4134 NaNO3600NaH2PO4·H2O 125 345 150 KCl 750微量元素/(mg/L)KI 0.83 0.01 1.0 0.75 0.8 H3BO3 6.2 0.63 1.0 5.0 3.0 1.6 MnSO4·4H2O 22.3 2.23 0.1 10 10 4.4 ZnSO4·7H2O 10.6 1.0 1.0 2.0 1.5 Zn(鳌合的)15Na2MoO4·2H2O 0.25 0.025 0.1 0.25CuSO4·5H2O 0.025 0.0025 0.03 0.2 0.04CoCl2·6H2O 0.025 0.0025 0.1 0.025 AlCl30.03NiCl2·6H2O 0.03FeCl3·6H2O 1.0Na2-EDTA 37.3 37.3 20 37.3 37.3 FeSO4·7H2O 27.8 27.8 15 27.8 27.8 蔗糖/g 30 40 20 30 20 50 pH 5.7 5.8 5.8 5.8 5.5 5.8附录7 标准计量单位(一)中华人民共和国法定计量单位(部分内容)(1986-7-1起实施)表1 国际单位制的基本单位量的名称单位名称单位符号长度米m质量千克(公斤) kg时间秒S电流安(培) A 热力学温度开(尔文) K物质的量摩(尔) Mol发光强度坎(德拉) cd表2 用基本单位表示的国际制导出单位量的名称单位名称单位符号面积平方米m2体积立方米m3速度米每秒m/s密度千克每立方米kg/m3 (物质的量)浓度摩尔每立方米,摩尔每升mol/m3,mol/L 光亮度坎德拉每平方米cd/m2表3 国际单位中具有专门名称的导出单位量的名称单位名称单位符号关系式频率赫[兹] Hz s-1力,重力牛[顿] N Kg·m/s2压力,压强,应力帕[斯卡] Pa N/m2能[量],功,热量焦[耳] J N·m功率,辐[射能]通量瓦[特] W J/s电位,电压,电动势伏[特] V W/A 电阻欧[姆] ΏV/A电导西[门子] S A/V光通量流[明] lm cd·sr[光]照度勒[克斯] lx lm/m2表4 国家选定的非国际单位制单位量的名称单位名称单位符号关系式时间分min 1 min=60s[小]时h 1h=60 min=3600s天(日) d 1d=24h=86400s 体积升L,(l)1L=1dm3=10-3m3表5 常用国际制词冠表示的因数词冠名称中文代号国际代号106兆(mega)兆M103千(kilo)千k102百(hecto)百h101十(deca)十da10-1分(deci)分 d10-2厘(centi)厘 c10-3毫(milli)毫m10-6微(micro)微μ10-9纳诺(nano)纳[诺] n10-12皮可(pico)皮[可] p10-15飞母托(femto)飞[母托] f(二)常见非法定计量单位与法定课题单位的换算类别换算英里(mile) 1 mile=1609.344m英尺(ft) 1 ft=0.3048m=12in英寸(in)1in=0.0254m=2.54cm埃(A)1A=10-10m=0.1nm达因(dyn)1dyn=10-5N=1g·cm/s2巴(bar)1bar=105Pa毫巴(mbar)1mbar=100Pa毫米水柱(mmH2O)1mmH2O=9.80665Pa毫米汞柱(mmHg)1mmHg=133.322Pa尔格(erg)1erg=10-7J卡(cal)1cal=4.1868J 附录8 常见的植物生长调节物质及其主要性质名称化学式相对分子质量溶解性质吲哚乙酸(IAA) C10H9O2N 175.19 溶于醇、醚、丙酮,在碱性溶液中稳定,遇热酸后失去活性吲哚丁酸(IBA) C12H13NO3 203.24 溶于醇、丙酮、醚、不溶于水、氯仿a----萘乙酸(NAA) C12H10O2 186.20 易溶于热水,微溶于冷水,溶于丙酮、醚、乙酸、苯2,4-二氯苯氧乙酸(2,4 — D) C8H6C12O3 221.04难溶于水、溶于醇、丙酮、乙醚等有机溶剂赤霉素(GA3) C10H22O6 346.4 难溶于水,不溶于石油醚、苯、氯仿而溶于醇类、丙酮、冰醋酸4-碘苯氧乙酸(PIPA)(增产灵)C8H7O3I 278微溶于冷水,易溶于热水,乙醇、氯仿、乙醚、苯对氯苯氧乙酸(PCPA)(防落素)C8H7O3Cl 186.5溶于乙醇、丙酮和醋酸等有机溶剂和热水激动素(KT) C10H9N5O 215.21 易溶于稀盐酸、稀氢氧化钠,微溶于冷水、乙醇、甲醇6-苄基腺嘌呤(6BA) C12H11N5 225.25 溶于稀碱、稀酸,不溶于乙醇脱落酸(ABA) C15H20O4 264.3 溶于碱性溶液如NaHCO3、三氯甲烷、丙酮、乙醇2-氯乙基膦酸(CEPA)(乙烯利)ClCH2PO(OH)2 144.5 易溶于水、乙醇、乙醚2,3,5-三碘苯甲酸(TIBA) C7H3O2I3 500.92 微溶于不,微溶于醇,易溶于冰醋酸、二乙醇胺青鲜素(MH) C4H4O2N2 112.09 难溶于水,微溶于醇,易溶于冰醋酸、二乙醇胺缩节安(助壮素)(Pix) C7H16NCl 149.5 可溶于水矮壮素(CCC) C5H13NCl12 158.07 易溶于水,溶于乙醇、丙酮,不溶于苯、二甲苯、乙醚B9 C6H12N2O3 160.0 易溶于水、甲醇、丙酮,不溶于二甲苯PP333(多效唑)C15H20CIN3O 293.5 易溶于、甲醇、丙酮三十烷醇(TAL)CH3(CH2)28CH2OH 438.38 不溶于水,难溶于冷甲醇、乙醇,可溶于热苯、丙酮、乙醇、氯仿28H48O6480 溶于甲醇、乙醇等附录9 植物激素与生长调节剂在农业生产中的应用作用药剂名称施用对象方法及效果促进插枝生根NAA 黄杨、松、葡萄、梨500~1000MG/KG,粉剂沾根法IBA 苹果、李、池柏、桑、茶、甘薯20~200mg/L,慢速浸泡法500~5000mg/L,快速浸泡法促进开花NAA 菠萝15~20mg/L,从株心灌乙烯利菠萝400~1000mg/L,喷施或灌心增加雌花乙烯利黄瓜、南瓜100~250mg/L,一~四叶期喷施增加雄花GA3 黄瓜50~150 mg /L,二~四叶期喷施促进结实2,4—D 番茄、茄子10~30 mg /L,局部喷施GA3 杂交水稻不育系40~80 mg /L,始穗期至齐穗期喷施葡萄10~20 mg /L,花期喷施NAA 西瓜1000 mg /L,混入羊毛脂软膏涂沫TIBA 大豆125 mg /L,花期喷施疏花疏果、促进脱落NAA 鸭梨、苹果40 mg /L,局部喷施乙烯利梨240~480 mg /L,花期喷施苹果250 mg /L,盛花前喷施保花保果、防止脱落NAA 棉花10 mg /L,盛花期喷施苹果40~60 mg/L,落果初期喷施GA3 棉花10~50 mg/L,盛花期喷施葡萄200 mg/L,花后10d喷施B9 苹果1000~200 mg/L,采果前60d喷施2,4-D 柑橘50~60,11~12番茄10~25 mg/L,初花期、盛花期浸花朵茄子30 mg/L,浸花处理防落素茄子喷花促进营养生长GA3 芹菜、苋、芜荽50~100 mg/L,采前10~15d 增加产量菠菜、莴苣、四季豆10~30 mg/L,喷苗茶100 mg/L,芽叶刚伸展时花生25~100 mg/L,喷苗增产灵水稻30 mg/L,盛花期喷施花生10~20 mg/L,盛大花期喷施PP333 早稻300 mg/L,秧苗期施BR 芹菜、萝卜、番茄、小麦、水稻、玉米0.01~0.0001 mg/L,浸种或苗期喷施植株矮化CCC 小麦3000 mg/L,拔节期喷施增加产量棉花20~50 mg/L,现蕾期、初花期喷施PP333 大豆250 mg/L,分枝至初花期喷施油菜100~150 mg/L,三叶期喷施烯效唑小麦50 mg/L,分蘖期、拔节期喷施促进果实成熟乙烯利香蕉750~1000 mg/L,采前喷果1000 mg/L,采后浸果一下番茄500~2000 mg/L,采前喷果1000~4000 mg/L,采后浸果一下柿子500 mg/L,采后浸果0.5~1min 促进橡胶分泌乳汁乙烯利橡胶树8%溶液涂树干割线下打破休眠,促进萌发GA3 马铃薯块茎0.5 mg/L,浸泡10min杏种子300~800 mg/L,浸种1.5h人参种子100 mg/L,浸泡24h沙藏催芽党参种子50 mg/L,浸种6h莴苣种子100 mg/L,2~4h菠菜种子0.5 mg/L浸种24h延长休眠、抑制发芽青鲜素(MH)洋葱、大蒜2500 mg/L,2~3片叶已枯马铃薯块茎涂、喷施于中间的青绿色叶面萝卜、芜菁2500~5000 mg/L,采收前4~14d喷施萘乙酸甲酯(MENA)马铃薯块茎1000 mg/L,粘土粉剂混合贮藏附录11 维生素及其主要性质。
