实验十三.苯乙酮的制备
苯乙酮的制备(精)
苯乙酮的沸点文献值为202.0℃,熔点为20.5℃, 折光率l.5372。
图1、带滴 液漏斗和 气体吸收 装置的反 应装置
乳胶管联结 气体吸收
NaOH水 溶 液
苯乙酮的制备
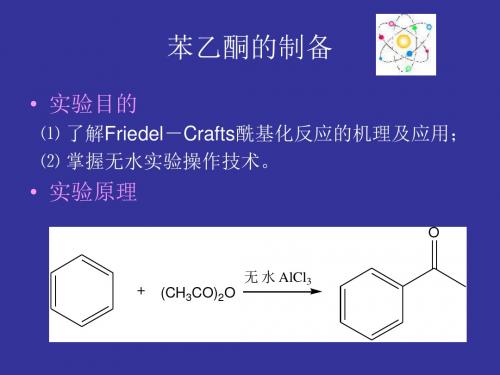
• 实验目的
⑴ 了解Friedel-Crafts酰基化反应的机理及应用; ⑵ 掌握无水实验操作技术。• Fra bibliotek验原理O
+
无 水 AlCl3 (CH3CO)2O
操作步骤
迅速称取25g经研碎的无水AlCl3(放入三颈瓶中)+ 30 mL 经金属钠干燥过的苯,启动搅拌,由滴液漏斗滴加重新 蒸馏过的醋酸酐6mL(约6.5g,0.06mol)和无水苯10mL的 混合溶液(约20min滴完)。反应立即开始,伴随有反应混 合液发热及氯化氢急剧产生。控制滴加速度,勿使反应过 于激烈。滴加完后,在水浴(或电热套)上回流0.5h, 至无氯化氢气体逸出为止(此时三氯化铝溶完)。
将三颈瓶冷却,在搅拌下慢慢滴加100 mL冷却的稀盐酸。 当瓶内固体物质完全溶解后,分出苯层。水层每次用 15mL苯萃取两次。合并苯层,依次用5%的氢氯化钠溶 液、水各20mL洗涤,然后用无水硫酸钠(镁)干燥。
将干燥后的粗产物过滤,蒸去苯以后(温度升到140 ℃左右,停止加热) ,将粗产物转移到50mL的蒸馏
思考题
1、水和潮气对本实验有何影响?在仪器的装 置和操作中应注意哪些事项?为什么要迅速称 取研磨三氯化铝? 2、反应完成后为什么要加入冷却的稀盐酸? 3、指出如何由傅—克反应制备下列化合构:(1) 二苯甲烷;(2)苄基苯基酮;(3)对硝基二苯酮。
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,也叫丙酮苯,是一种有机化合物,化学式为C6H5COCH3,具有强烈的香气和刺激性。
因其广泛应用于工业和医药领域,因此对其制备方法进行深入研究,具有很高的实用价值。
本文对苯乙酮的制备研究进行探讨,介绍其常用的制备方法以及反应机理。
1.酸催化法该方法是通过酸性催化剂催化苯与丙酮反应生成苯乙酮。
常用的酸性催化剂有硫酸、磷酸、五氧化二磷等。
反应机理:酸性催化剂可以将丙酮中的α-氢离子去除,形成羰基负离子,然后与苯发生亲核加成反应,最终得到苯乙酮。
2.氧化偶联法该方法是通过将苯和丙酮溶于碱性氧化剂中进行氧化反应,生成苯甲基酮,然后再将其经过酸催化偶联反应,得到苯乙酮。
二、苯乙酮的反应机理苯乙酮是一种α-酮,其含有酮基和苯环,可以经过多种反应。
1.酮的加成反应苯乙酮的酮基可以发生羰基加成反应。
例如,苯乙酮与氨在氧化铜的催化下发生反应,生成咪唑类物质。
反应机理:氧化铜催化下,苯乙酮中的羰基吸引了氨中的一个氢离子,生成一种带负电荷的羰基中间体,接着,中间体进一步与氨发生亲核加成反应,得到产物。
2.催化加氢反应反应机理:在铂等贵金属催化剂作用下,氢气分子可以在铂催化剂表面吸附,然后分解成氢原子,接着,氢原子在催化剂表面反应,生成苯乙醇。
3.酮的羟醛化反应苯乙酮可以经过羟醛化反应变成苯乙醛。
例如,苯乙酮经过氢气和催化剂的作用下,可以生成苯乙醛。
反应机理:在催化剂的作用下,苯乙酮中的羰基吸引氢离子,然后经过析出水产生α,β-不饱和醛。
最后,α,β-不饱和醛在氢气的作用下,被还原成为苯乙醛。
苯乙酮广泛应用于工业和医药领域,如:1.工业领域苯乙酮作为有机合成材料,广泛应用于合成香料、染料、药物、树脂、柔性泡沫材料等领域。
2.医药领域总之,苯乙酮的制备方法和反应机理的研究,具有很高的实用价值,在生产和科研领域都有广泛的应用和重要的作用。
苯乙酮的制备研究

苯乙酮的制备研究
苯乙酮,化学式为C6H5C(CH3)2CO,也被称为二甲基苯乙酮,是一种有机化合物。
它是一种具有水稳定性的有机溶剂,常用于有机合成和溶液聚合反应中。
苯乙酮的制备方法多样,可以通过多种途径合成。
其中最常见的方法是通过酰化反应制备。
一种常用的制备方法是通过对甲苯与COCl2(氯化亚碳)的反应制备。
具体反应步骤为:
将甲苯与COCl2反应生成叔丁基苯甲酮。
反应条件为在常温下进行,并加入催化剂,如三乙基胺(TEA)。
C6H5CH3 + COCl2 -> C6H5C(CH3)Cl + HCl
然后,将生成的叔丁基苯甲酮与盐酸反应,生成相应的盐酸酯。
通过水解反应,将盐酸酯转化为苯乙酮。
另一种制备苯乙酮的方法是通过碱性条件下的酸酐和苯乙酮水解反应。
具体步骤如下:
将酸酐与盐酸中和,生成稳定的酸盐。
然后,加入苯乙酮和氢氧化钠(NaOH)溶液,进行水解反应。
这种方法相对简单,但产率较低。
另外一种制备苯乙酮的方法是通过酰化反应。
准备好苯基甲酸和酸性催化剂,如三氧化硼(B2O3)或四甲基硅酸(TMSA)。
苯乙酮的制备研究方法有多种,可以选择适合自己实验条件和目的的方法。
每种方法都有其优缺点,需要根据具体情况进行选择。
苯乙酮实验报告

苯乙酮实验报告苯乙酮实验报告引言:实验是科学研究的基础,通过实验可以验证理论,探索未知。
本次实验旨在合成苯乙酮,并通过实验观察和数据分析来了解其性质和特点。
苯乙酮是一种常见的有机化合物,具有广泛的应用领域,对于了解它的合成和性质具有重要意义。
实验目的:1. 合成苯乙酮;2. 观察苯乙酮的物理性质;3. 探究苯乙酮的化学性质。
实验步骤:1. 实验前准备:准备所需实验器材和试剂,包括苯乙酮合成所需的原料和催化剂,以及实验室常用的实验器材。
2. 合成苯乙酮:将苯酚和乙酸以一定的比例混合,加入适量的催化剂,并在一定的条件下进行反应。
反应结束后,通过适当的提取和纯化步骤,得到苯乙酮产物。
3. 观察苯乙酮的物理性质:对合成得到的苯乙酮进行外观观察、溶解性测试、熔点测定等实验,以了解苯乙酮的外观、溶解性和熔点等物理性质。
4. 探究苯乙酮的化学性质:对苯乙酮进行一系列的化学反应实验,如氧化反应、还原反应、酸碱中和反应等,以了解苯乙酮的化学性质和反应特点。
实验结果与讨论:1. 合成苯乙酮:在实验条件下,成功合成了苯乙酮。
合成产物的收率为X%。
2. 苯乙酮的物理性质:苯乙酮为无色液体,具有特殊的香气。
它在常温下易溶于有机溶剂,如醇类、醚类等,但不溶于水。
苯乙酮的熔点为XX℃。
3. 苯乙酮的化学性质:苯乙酮具有较强的氧化性,在氧化剂的作用下可以发生氧化反应,生成相应的酮酸或酮醇。
同时,苯乙酮也可以发生还原反应,还原为相应的醇。
此外,苯乙酮还可以与酸或碱发生中和反应,生成相应的盐类。
结论:通过本次实验,我们成功合成了苯乙酮,并对其物理性质和化学性质进行了观察和分析。
苯乙酮是一种常见的有机化合物,具有广泛的应用领域。
对于进一步研究其性质和应用具有重要意义。
本实验的成功也验证了实验是科学研究的重要手段,通过实验可以获得真实可靠的数据,为理论研究提供有力支持。
同时,实验也提醒我们在实验过程中要严格遵守安全操作规范,保证实验的顺利进行。
苯乙酮的制备实验报告

苯乙酮的制备实验报告
目录
1. 实验目的
1.1 原料准备
1.2 实验步骤
1.2.1 反应体系
1.2.2 反应条件
1.2.3 操作步骤
1.2.4 产物提取
1.3 实验结果分析
实验目的
本实验旨在通过苯乙酮的制备实验,让学生掌握重要的有机合成技术,提高其对化学反应机理的理解能力。
原料准备
- 苯
- 乙酰氯
- NaOH
- 水
- 氯仿
实验步骤
反应体系
在反应釜中,加入适量苯和乙酰氯,同时控制好反应温度。
反应条件
控制反应的温度在适宜范围内,观察反应进程,及时调整反应条件。
操作步骤
1. 将苯加入反应釜中;
2. 加入适量的乙酰氯;
3. 控制反应温度并搅拌均匀反应体系;
4. 加入NaOH溶液进行中和反应;
5. 分离产物层并进行提取。
产物提取
通过对反应产物进行适当的提取步骤,得到苯乙酮等目标产物。
实验结果分析
通过对实验过程、反应条件和产物的分析,总结实验结果,对实验过
程中的问题进行讨论,并提出改进措施,以提高实验的准确性和效率。
苯乙酮的制备

苯乙酮的制备
一、实验目的
学习用Friedel-Crafts酰基化反应制备芳酮的原理和操作方法; 掌握无水操作及防潮气体吸收回流装置的安装和使用。
二、实验原理
F-K反应:芳香烃在无水三氯化铝等催化剂存在下。同酰氯或酸酐作用, 在苯环上引入酰基的反应。 当苯环上有一个酰基取代后,因它是间位定位基,使苯环的活性降低,不 会生成多元取代物的混合物。用酸酐做酰基化试剂时,因有一部分三氯化铝 与酸酐作用和能与芳酮生成配合物,所以1mol的酸酐需要3mol的三氯化铝, 实际上还要过量10~20%。 此反应为放热反应,常有一个诱导期,操作时要注意温度变化,不可盲目 快加。
有机基础实验:正溴丁烷的制备
五、注意事项
1. 严防倒吸!(会爆炸)
2. 滴加过程要控制反应速度,注意诱导期
3. 反应液倒入盐酸溶液中,一定要慢、搅拌、通风橱进行操作 4. 有机层干燥后所有使用的仪器要干燥
5. 前馏分和正馏分均有毒,注意密封,回收。
六、实验结果
状态、颜色、气味、沸程、实际产量、理论产量、产率等
有机基础实验:正溴丁烷的制备
三、试剂与原料
反 应 瓶
25.0g三氯化铝 20mL 苯
恒压 滴液 漏斗
8.0mL乙酸酐 10mL 苯
其它:浓盐酸,水,石 油醚,5%碳酸氢钠,无 水Байду номын сангаас酸镁,无水氯化钙
有机基础实验:正溴丁烷的制备
四、实验装置
拉直或用夹子固定,切 忌漏斗完全浸入水中, 可使漏斗倾斜,露出至 少1/2, 防止倒吸!!!
杯中(慢、搅拌、在通风橱进行,可戴护目镜),固体完全溶
解后冷至室温,转移至分液漏斗,分出有机层,水层用石油醚 萃取两次(每次15mL)。合并有机层,依次用5%氢氧化钠溶 液、水各20mL洗涤。 3. 有机层用无水硫酸镁干燥。 4. 简单蒸馏装置,回收前馏分,收集198~202oC的馏分(注意放 水或换空气冷凝管)
苯乙酮的制备

苯⼄酮的制备【实验⽬的】1、学习利⽤Friedel—Crafts酰基化反应制备芳⾹酮的原理和⽅法。
2、学习⽆⽔操作。
【实验原理】Friedel—Crafts酰基化反应是制备芳⾹酮的最重要和最常⽤的⽅法之⼀,可⽤FeCl3,SnCl4,BF3,ZnCl3,AlCl3等Lewis 酸作催化剂,催化性能以⽆⽔AlCl3和⽆⽔AlBr3为最佳。
本实验采⽤⽆⽔AlCl3作催化剂,⽤苯和⼄酐反应制苯⼄酮。
反应⽅程式为:+(CH3CO)2O⽆⽔AlCl3COCH3+CH3COOH【实验装置】图1 图2【仪器和药品】1、仪器:25mL三颈烧瓶、恒压滴液漏⽃、25mL圆底烧瓶、直形冷凝管、接液管、三⾓烧瓶、铁圈、⼩烧杯、分液漏⽃、漏⽃、⼲燥管、电炉、。
2、药品:⽆⽔苯、⼄酐、⽆⽔AlCl3、浓盐酸、碎冰、10%的氢氧化钠溶液、⽔、⽆⽔氯化钙、⽆⽔硫酸镁。
【实验步骤】(上)6.5.0g(0.048moL)⽆⽔AlCl3 加⼊25mL三颈烧瓶中,8mL(约7g,0.09moL)⽆⽔苯如图1所⽰,⼲燥管中装⽆⽔氯化钙。
2mL(约2.15g,0.02moL)⼄酐(从滴液漏⽃缓慢加⼊)⾄⽆氯化氢⽓体逸出停⽌实验。
⼩磁⼦、沸⽯【实验步骤】(下)往装有反应混合物的三颈瓶中倒⼊9mL浓盐酸和18mL冰⽔的混合物(在通风橱中进⾏),将反应混合物倒⼊分液漏⽃中(若三颈瓶中有固体不溶物,加适量浓盐酸溶解)。
分液混合物分液上层:有机层下层:⽔层加⼊2×4mL苯分液有机层合并有机层依次⽤8mL10%的氢氧化钠溶液、8mL⽔洗涤,⽤⽆⽔硫酸镁⼲燥。
然后在⽔浴上蒸馏回收苯。
【实验注意事项】1、本实验要求⽆⽔系统,实验过程中应尽量避免体系敞⼝在空⽓中。
2、滴加⼄酐时应控制速度,使反应平稳进⾏;反应过程中严格控制好反应温度。
3、苯有毒,是致癌物质之⼀,不要接触⽪肤或吸⼊蒸⽓。
4、注意反应终点和反应混合物处理时⼀定在通风橱内进⾏。
5、⽆⽔三氯化铝的质量是本实验成败的关键,以⽩⾊粉末打开盖冒⼤量的烟,⽆结块现象为好。
十,苯乙酮的制备

十、苯乙酮的制备一、实验目的1. 学习并掌握傅-克酰基化反应的基本原理。
2. 掌握无水操作及机械搅拌的使用方法二、反应式C OCH 33+ (CH 3CO)2+ CH 3COOH三、主要物料及其物理常数四、主要试剂用量及规格醋酸酐 7.5g(7ml ,0.072mol),无水苯 30ml(0.34mol),无水三氯化铝 20g. 浓盐酸,苯,5%氢氧化钠溶液,无水氯化钙。
五、操作步骤1. 安装带搅拌、滴液漏斗、回流、干燥及气体吸收的反应装置2. 加料:迅速称取20g 无水AlCl 3放入250ml 三口瓶中,再加入30ml 无水苯。
3. 自滴液漏斗慢慢滴加7ml 乙酸酐,边加边摇,约15min 加完。
沸水浴上回流20min ,直到无氯化氢气体放出。
4. 将反应物冷至室温,搅拌下加入100ml 配制好的1:1盐酸溶液。
5. 当固体溶解完后,分液,用10ml 苯萃取两次,合并有机层。
6. 依次用50ml 等体积的5%NaOH 和水洗涤有机层无水CaCl 2干燥。
7. 干燥后的产物分批加入50ml 的圆底烧瓶中,水浴或电热套小火加热蒸去苯。
8. 升高温度至140℃,稍冷后改空冷管,收集194-198℃的馏分。
9. 称重、计算产率。
注意事项:1.所用仪器和试剂必须干燥,称取和加入AlCl3时应快速。
2.注意正确安装氯化氢气体吸收装置,防止倒吸。
3.乙酸酐的滴加速度要慢。
4.蒸馏时,尽可能用小瓶,以减少损失。
思考与讨论1.本装置为何要干燥,加料要迅速?2.反应完成后,为何要加入浓盐酸和在冰水中冰解(加入1:1的浓盐酸和水)?。
苯乙酮的制备研究

苯乙酮的制备研究作者:殷福东姜福元来源:《消费导刊》2019年第14期摘要:本文将苯和乙酐或者乙酰氯反应,用三氯化铝作为反应的催化剂可以制得苯乙酮。
关键词:催化剂苯乙酮一、苯乙酮的制备方法将苯和乙酐或者乙酰氯反应,用三氯化铝作为反应的催化剂可以制得苯乙酮。
而在工业上常通过乙苯空气氧化法来制备苯乙酮。
除此之外,在催化氧化乙苯来制备苯乙烯时,苯乙酮可以作为副产物生成。
工业生产出来的苯乙酮中通常含有酸性物质,水和苯酚等杂质,可以用硫酸干燥然后减压分馏来精制以除去这些杂质,或者是在干燥和无光照条件下,在熔融状态时分步结晶精制,在低温时也可以用戊烷来精制。
接下来将介绍一些制备苯乙酮时常用的方法。
(一)工业上制备苯乙酮时一般直接用乙苯在常压下空气氧化。
但这种方法污染比较严重且转化率不高,不但如此,分离和提纯生成的副产物使反应的成本上升。
(二)将苯和乙酸、乙酐或者乙酰氯反应,以三氯化铝作为反应的催化剂可以制得苯乙酮。
苯与乙酸酐酰化法这种方法对环境有污染且产率较低,而且生成的副产物中有醋酸会腐蚀设备。
(三)分解苯甲酸法在一定条件下苯甲酸可以发生分解反应生成水、二氧化碳以及苯乙酮。
这样生成的副产物容易分离且成本较低,缺点是转化率低并且对反应条件要求高,而且还容易形成其他的产物,因此工业生产一般不采用这种方法。
(四)苯乙醇氧化制苯乙酮在高温高压条件下通过苯乙醇制备苯乙酮,但苯乙醇成本较高,并不适用于工业生产。
(五)高温高压下苯乙烯催化氧化法在高溫高压下使用催化剂以及氧化剂氧化苯乙烯可以制备苯乙酮,但苯乙烯同苯乙醇类似,在作为原料使用时价格昂贵不适用于大规模应用。
(六)乙苯多相氧化法这种方法是在氧化剂以及催化剂都具备的条件下对乙苯选择性氧化来制备苯乙酮,近几年的探索重点集中在化学催化这一方面。
二、苯乙酮的生产前景苯乙酮可以作为医药、香料、染料生产领域中的原料,由氧化乙苯而制得苯乙酮,对于饱和碳氢键选择氧化、石油化工下游产品的研究开发以及精细化工的发展有着非常重要的意义。
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮是一种重要的化学原料,被广泛应用于医药、染料、香料、香精、树脂等领域。
其制备方法有多种,包括从苯乙烯、苯甲醛或苯乙酸等原料合成。
本文将探讨苯乙酮的制备研究,介绍不同方法的原理和优缺点,以期为相关领域的科研工作者提供参考。
一、苯乙酮的制备方法1. 从苯乙烯合成将苯乙烯和氧气在催化剂的存在下氧化反应,生成苯乙酮。
催化剂通常采用铜、铬、钴等金属氧化物,也可选择氧化硫酸亚铁等化合物。
该方法操作简便,但设备投资较大。
2. 从苯甲醛还原合成利用还原剂将苯甲醛还原得到苯乙醇,再经过氧化反应得到苯乙酮。
还原剂可选用金属钠、金属铝等。
该方法将苯甲醛作为原料,可利用多种合成途径制备苯乙酮。
首先将苯乙酸和氯化亚砜在氢氧化钠的存在下反应生成苯乙醛,然后再进行氧化反应制备苯乙酮。
该方法所需原料易得,操作简便,适合工业生产。
优点:原料易得,反应途径简单。
缺点:设备投资大,氧化反应选择催化剂需要谨慎,对环境要求高。
优点:利用多种还原剂可制备苯乙酮,适用性广。
缺点:苯甲醛原料价格较高,还原剂对环境有一定的影响。
3. 从苯乙酸酐羧化合成的优缺点优点:原料易得,操作简便,适合工业化生产。
缺点:反应条件要求严格,氯化亚砜等原料对人体有一定的毒性。
三、苯乙酮制备研究的发展趋势1. 利用生物技术随着生物技术的发展,利用酶、微生物等生物催化剂合成苯乙酮成为研究热点。
通过优化酶的反应条件和酶的特异性,可以提高合成效率,并减少对环境的污染。
2. 绿色合成方法在苯乙酮的合成过程中,绿色合成方法备受关注。
包括采用水为溶剂、利用可降解催化剂、减少废弃物产生等方法,致力于实现对环境友好的苯乙酮合成过程。
3. 新型催化剂研究新型催化剂对苯乙酮的合成具有重要作用,包括贵金属、过渡金属、离子液体等催化剂的研究。
这些催化剂不仅可以提高合成效率,还可以减少催化剂的使用量,降低成本。
(完整版)实验十三.苯乙酮的制备

实验十三: 苯乙酮的制备一、实验目的1、学习傅-克酰基化制备芳酮的原理和方法;2、初步掌握无水操作、吸收、搅拌、回流、滴加等基本操作。
二、实验原理Friedel-Crafts 酰基化反应是制备芳酮的重要方法之一,酰氯、酸酐是常用的酰基化试剂,无水FeCl 3,BF 3,ZnCl 2和AlCl 3等路易斯酸作催化剂,分子内的酰基化反应还可以用多聚磷酸(PPA )作催化剂,酰基化反应常用过量的芳烃、二硫化碳、硝基苯、二氯甲烷等作为反应的溶剂。
用苯和乙酐制备苯乙酮的反应方程式如下:(CH 3CO)2O3CH 3COOH++COCH 3具体过程:CH O CH 3O O ++33Cl 3δCH 3COOAlCl 2CH 3OAlCl 3红色溶液+CH 3COOAlCl 2CH 3OAlCl 3H 2OCOCH 3Al(OH)Cl +HCl2CH 3COOH +Al(OH)Cl 2Al(OH)Cl 2Al + 3Cl + H 2O三、实验药品及其物理常数四、主要仪器和材料升降台 木板 隔热垫 电炉 水浴锅 机械搅拌器 四氟搅拌套塞(19#) 玻璃搅拌 三口烧瓶(100mL、19#×3)恒压滴液漏斗(14#×2)大小头(口14#+塞19#)空心塞(14#) 球形冷凝管(19#)直形干燥管(19#×2)分液漏斗圆底烧瓶(100 mL、19#)蒸馏头(19#)螺帽接头(19#)温度计(300℃) 直形冷凝管(19#)空气冷凝管(19#)真空接引管(19#)锥形瓶(50 mL、19#)量筒(100 mL)三角漏斗冰五、实验装置⑴搅拌、滴加、回流、尾气吸收装置⑵萃取、洗涤装置⑶常压蒸馏回收低沸物装置⑷减压蒸馏提纯高沸物装置六、操作步骤【操作要点及注意事项】⑴搭装置:保持反应体系无水是实验成败之关键,所有仪器一定要烘干(除三角漏斗和烧杯)。
仪器的选用,搭配顺序,各仪器高度位置的控制要合理。
苯乙酮的制备方案

苯乙酮的制备一、工作目标1.学习实验室中利用Friedel-Crafts酰基化法制备苯乙酮的原理与方法。
2.掌握带有机械搅拌和气体吸收的加热回流装置的操作方法。
3.掌握带干燥管和吸收有害气体的回流装置使用4.掌握终点监控的方法原理5.掌握有机液体的干燥及高沸点化合物的蒸馏6.掌握使用分液漏斗洗涤和分离液体有机物的操作技术二、工作内容1.解读方案,并确定初步方案2.列出准备单(仪器、试剂以及相关溶液的配制)3.进行试验1)带干燥管和吸收有害气体回流装置的搭建2)物料的投放3)水浴回流装置的搭建4)反应一段时间,进行反应终点的监控5)粗产物的干燥(有机液体的分离与干燥)6)粗产物的蒸馏提纯7)空气冷凝的装置的搭建4.对馏出物进行称重5.结束工作(装置的拆除、清洗、归还)6.数据的处理与总结7.计算产率并撰写报告三、工作进程与安排四、苯乙酮合成准备单1.试剂:2.仪器:五、 苯乙酮的合成原理芳酮一般通过辅克反应来制备,该反应在无水三氯化铝存在下由酰氯或酸酐与芳烃反应得到高产率的芳酮。
本实验以乙酸酐为酰化试剂,与苯发生乙酰化反应制备苯乙酮,其中苯既是反应物,又作为反应溶剂,可用下列反应式表示:+CH 3COCCH 3O O无水 AlCl 3CCH 3O+ CH 3COOH具体反应过程:CH 3C O O CCH 3O+ AlCl 3CH 3C O O CCH 3O AlCl 3AlCl 3(红色溶液)CCH 3O AlCl 3+ H 2O CCH 3O+ Al(OH)Cl 2 + HCl白(放热)CH 3COO AlCl 2 + H 2O Al(OH)Cl 2 + CH 3COOH (放热) Al(OH)Cl 2 + HCl AlCl 3 + H 2O 六、苯乙酮合成工作步骤1. 在250mL 三口烧瓶中,分别安装搅拌器,滴液漏斗及球形冷凝管。
在冷凝管上端装上氯化钙[1]干燥管,并连接气体吸收装置[2],用水做吸收液。
有机化学-实验 苯乙酮的制备

O
CH3 C
+
O
CH3 C
O
AlCl3
O C CH3 + CH3COOH
催化剂用量大原因:
(1)产物醋酸根消耗AlCl3 (2)产物苯乙酮与等摩尔的AlCl3形成稳定的配合物。
实验装置与操作关பைடு நூலகம்点
实验装置
搅拌干燥回流装置
蒸馏装置
实验装置与操作关键点
操作关键点
1. 加料迅速准确,防止试剂吸湿。 2. 控制好乙酐的滴加速度,从而控制反应,必要时可用
冷水冷却烧瓶。 3. 水浴加热至不在有HCl气体产生(石蕊试纸检验)。 4. 配合物水解反应中若仍有沉淀析出,可补加HCl。 5. 萃取前后分液时注意区分产物苯乙酮与水所在的相。 6. 精馏时确保仪器干燥。
实验讨论
1. 你认为影响苯乙酮产率的关键因素有哪些? 2. 反应完成后为何要加入浓HCl和冰水的混合物分解产物? 2. 精馏苯乙酮时为何选择空气冷凝管?
有机化学实验
苯乙酮的制备
江苏大学化学化工学院
Contents
1 实验目的
2
实验原理
3
实验装置与操作关键点
4
实验讨论
实验目的
1. 掌握F-C酰基化反应制备芳酮的原理和方法。 2. 巩固回流、萃取、蒸馏等基本操作,掌握防潮回流及有毒 气体的处理方法。
实验原理
F-C酰基化反应--芳烃在催化剂存在下与酰基化试剂 作用,芳环上的氢原子被酰基取代。 F-C酰基化反应是 制备芳酮的重要方法。
That’s all
苯乙酮的制备

口瓶微溶于水,易溶于许多有机溶剂 冰解,待溶解后,再用分液漏斗分离(取哪一层?) 反应的终点可根据氯化氢气体不再逸出来判断。 冰解,待溶解后,再用分液漏斗分离(取哪一层?)
分液振荡时应及时放气,并静置分层,放出下层,取上层(为什么)
吸收的反应装置。 酸酐作酰基化试剂,则需要更多的无水AlCl3。
同时,可防止碱式铝盐产生沉淀析出,影响产品质量。 傅-克酰基化反应的基本原理 改用空气冷凝管蒸馏,收集195~202℃馏分,即得产品,秤量,计算产率.
② 加料:迅速称取13g无水AlCl 放入100ml三 ④反应液冷却,倒入装有18mL浓盐酸35g碎冰的烧杯中
什么是傅克(Friedel-Crafts)反应?为什么傅克酰基化反应所用的Lewis 酸如AlCl3比傅克烷基化反应中的用量大?
气体放出。 蒸馏时,尽可能用小瓶,以减少损失。
主要物料及其物理常数 改用空气冷凝管蒸馏,收集195~202℃馏分,即得产品,秤量,计算产率. 由于分解络合物的反应是放热的,故用冰水予以降温。 同时,可防止碱式铝盐产生沉淀析出,影响产品质量。
③ 自恒压漏斗慢慢滴加4ml乙酸酐,边加边摇, 因为远离水面,则有相当部分的氯化氢气体不被吸收而逸出,造成空气污染;
蒸馏时,尽可能用小瓶,以减少损失。
答:粗产品苯乙酮制备完毕后,用冰和浓盐酸来处理反应的粗产物,以破坏酰基氧与AlCl3形成的络合物,析出产物苯乙酮。
约15min加完。水浴上搅拌,直到无氯化氢 改用空气冷凝管蒸馏,收集195~202℃馏分,即得产品,秤量,计算产率.
一、实验目的
• 学习并掌握傅-克酰基化反应 的基本原理。
【精品】苯乙酮的制备

【精品】苯乙酮的制备
苯乙酮是一种重要的化学品,广泛应用于香精、药品、农药等行业中。
本文将介绍几
种制备苯乙酮的方法。
1. 酮化反应法
酮化反应法是苯乙酮制备的重要方法之一,反应条件简单,易于控制,适用于大规模
工业生产。
酮化反应一般用苯和乙酸为原料,催化剂为硫酸或磷酸。
反应物质比例要求苯
和乙酸之间的摩尔比为1:1.5-2。
反应温度为150℃左右,反应时间为4-5小时。
反应产物经过蒸馏分离,得到纯苯乙酮。
不同生产厂家的分离方法略有不同,但大多
采用水蒸汽蒸馏法进行分离。
将反应物加入至反应釜,升温至160℃-175℃,经过蒸馏分离,得到苯乙酮和副产物乙酸酯。
经过多级分离、净化,最终得到纯苯乙酮。
总之,以上几种方法都适用于苯乙酮的制备。
其中,酮化反应法应用最为广泛,适用
于大规模工业制备;氧化反应法适用于小规模实验室制备;而醇解反应法则原料价格低廉,能够实现大规模工业生产,成本低。
苯乙酮的制备

答:加酸的目的是使苯乙酮析出,其反应如下:
O
_CCH 3. AlCl 3 H+ ,H2O
O
_CCH 3 + AlCl 3
• 六. 注意事项
• 1.仪器必须是干燥的否则影响反应顺利进行,而且反应容器要与空气 隔绝,装置中凡是和空气相通的部位,应装置干燥管
• 2.反应混合物与水混合时,一定要注意安全,会放出大量的氯化氢气 体。
• 3.注意不要将产品洒落,苯和苯乙酮都是有毒的,而且味道比较大。
• 4.无水三氯化铝的质量是实验成败的关键之一,研细、称量及投料均 需迅速,避免长时间暴露在空气中(可在带塞的锥形瓶中称量。
三、主要物料及其物理常数
化合物 分子 熔点 沸点 密度
溶解性
量
(℃11 5.5
醋酸酐 102.09 -73.1
苯乙酮 120.15 20.5
80.1 0.8786 139.55 1.0820 202 1.5318
不溶 微溶 不溶
四、实验操作步骤
• 1.实验装置图:
• 2.实验步骤:
• ⑴制备:
• 安装好仪器在干燥的三口烧瓶中加入13g无水三氯化铝和 16ml苯在搅拌下逐滴加入4ml乙酸酐,控制加入速度,使 烧瓶刚刚感到发热为准。然后对三口烧瓶进行水浴加热, 保持反应容器微沸,直至没有氯化氢放出为止。
• ⑵精制:
• 将反应混合物冷却到室温,在搅拌下倒入盛有18ml浓盐 酸和35g碎冰的烧杯中,溶解完成后。
五、实验结果
1. 计算产率(理论产量以醋酸酐为准计算
2.也可用减压蒸馏苯乙酮在不同压力下的沸点列表如下:
压力
4
5
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮是一种常见的芳香族酮类化合物,具有广泛的用途,如用于药物合成、杀虫剂合成以及香料和染料合成等。
因此,苯乙酮的制备研究一直受到广泛的关注和探讨。
传统的苯乙酮制备方法主要有两种,一种是通过酰化反应制备,另一种是通过芳环化反应制备。
酰化反应是一种将酸酐或酸与醇或季铵盐反应生成酯键的重要反应。
苯乙酮的制备可以通过苯甲酸与乙酸酐在硫酸催化下进行酰化反应而得到。
反应方程式为:C6H5COOH + (CH3CO)2O → C6H5COCH2COCCH3 + H2O该反应通常在恒温下进行,但需要不断搅拌以提高反应速度。
反应结束后,反应物混合物经蒸馏分离,得到苯乙酮。
芳环化反应是另一种制备苯乙酮的常用方法。
该方法是以苯及其衍生物为反应底物,在适当的催化剂存在下,发生芳香族分子间的亲核加成与失活后的芳香族碳自由基取代反应,形成由芳环与羰基化合物构成的新环。
在这种方法中,苯和丙酮在碘化铝(AlI3)的存在下进行反应,生成苯乙酮。
反应方程式为:该反应需要在干燥条件下进行,并且需要适当控制反应中反应的温度和时间以确保反应物充分转化。
除了传统的制备方法之外,还有一些新型的制备苯乙酮的方法。
近年来,高斯应用量子化学计算的方法,提出一种通过醛/酮转移氢化或不确定介质反应,从苯甲醛以及乙酮派生物中制备苯乙酮的方法。
因为这种方法无需使用有机溶剂,反应的催化剂也可以是较为廉价的金属催化剂。
总的来说,苯乙酮的制备方法主要包括酰化反应、芳环化反应以及其他新型方法。
随着科技的发展和人们对环保和资源的理解,新型方法会逐渐替代传统方法,开发更加绿色、环保的方法,提高制备效率和降低成本,以更好地满足市场需求。
苯乙酮的制备

【实验目的】1、学习利用Friedel—Crafts酰基化反应制备芳香酮的原理和方法。
2、学习无水操作。
【实验原理】Friedel—Crafts酰基化反应是制备芳香酮的最重要和最常用的方法之一,可用FeCl3,SnCl4,BF3,ZnCl3,AlCl3等Lewis酸作催化剂,催化性能以无水AlCl3和无水AlBr3为最佳。
本实验采用无水AlCl3作催化剂,用苯和乙酐反应制苯乙酮。
反应方程式为:+(CH3CO)2O无水AlCl3COCH3+CH3COOH【实验装置】图1 图2【仪器和药品】1、仪器:25mL三颈烧瓶、恒压滴液漏斗、25mL圆底烧瓶、直形冷凝管、接液管、三角烧瓶、铁圈、小烧杯、分液漏斗、漏斗、干燥管、电炉、。
2、药品:无水苯、乙酐、无水AlCl3、浓盐酸、碎冰、10%的氢氧化钠溶液、水、无水氯化钙、无水硫酸镁。
【实验步骤】(上)6.5.0g(0.048moL)无水AlCl3 加入25mL三颈烧瓶中,8mL(约7g,0.09moL)无水苯如图1所示,干燥管中装无水氯化钙。
2mL(约2.15g,0.02moL)乙酐(从滴液漏斗缓慢加入)至无氯化氢气体逸出停止实验。
小磁子、沸石【实验步骤】(下)往装有反应混合物的三颈瓶中倒入9mL浓盐酸和18mL冰水的混合物(在通风橱中进行),将反应混合物倒入分液漏斗中(若三颈瓶中有固体不溶物,加适量浓盐酸溶解)。
分液混合物分液上层:有机层下层:水层加入2×4mL苯分液有机层合并有机层依次用8mL10%的氢氧化钠溶液、8mL水洗涤,用无水硫酸镁干燥。
然后在水浴上蒸馏回收苯。
【实验注意事项】1、本实验要求无水系统,实验过程中应尽量避免体系敞口在空气中。
2、滴加乙酐时应控制速度,使反应平稳进行;反应过程中严格控制好反应温度。
3、苯有毒,是致癌物质之一,不要接触皮肤或吸入蒸气。
4、注意反应终点和反应混合物处理时一定在通风橱内进行。
5、无水三氯化铝的质量是本实验成败的关键,以白色粉末打开盖冒大量的烟,无结块现象为好。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验十三: 苯乙酮的制备
一、实验目的
1、学习傅-克酰基化制备芳酮的原理和方法;
2、初步掌握无水操作、吸收、搅拌、回流、滴加等基本操作。
二、实验原理
Friedel-Crafts 酰基化反应是制备芳酮的重要方法之一,酰氯、酸酐是常用的酰基化试剂,无水FeCl 3,BF 3,ZnCl 2和AlCl 3等路易斯酸作催化剂,分子内的酰基化反应还可以用多聚磷酸(PPA )作催化剂,酰基化反应常用过量的芳烃、二硫化碳、硝基苯、二氯甲烷等作为反应的溶剂。
用苯和乙酐制备苯乙酮的反应方程式如下:
(CH 3CO)2O
3
CH 3
COOH
++COCH 3
具体过程:
CH O CH 3
O O ++
3
3
Cl 3δ
CH 3COOAlCl 2CH 3O
AlCl 3
红色溶液
+
CH 3COOAlCl 2CH 3
O
AlCl 3H 2O
COCH 3
Al(OH)Cl +HCl
2CH 3COOH +Al(OH)Cl 2
Al(OH)Cl 2
Al + 3Cl + H 2O
三、实验药品及其物理常数
四、主要仪器和材料
升降台 木板 隔热垫 电炉 水浴锅 机械搅拌器 四氟搅拌套塞(19#) 玻璃搅拌 三口烧瓶(100 mL 、19#×3) 恒压滴液漏斗(14#×2) 大小头(口14#+塞19#) 空心塞(14#) 球形冷凝管(19#) 直形干燥
管(19#×2)分液漏斗圆底烧瓶(100 mL、19#)蒸馏头(19#)螺帽接头(19#)温度计(300℃) 直形冷凝管(19#)空气冷凝管(19#)真空接引管(19#)锥形瓶(50 mL、19#)量筒(100 mL)三角漏斗冰
五、实验装置
⑴搅拌、滴加、回流、尾气吸收装置⑵萃取、洗涤装置
⑶常压蒸馏回收低沸物装置⑷减压蒸馏提纯高沸物装置
六、操作步骤
【操作要点及注意事项】
⑴搭装置:保持反应体系无水是实验成败之关键,所有仪器一定要烘干(除三角漏斗和烧杯)。
仪器的选用,搭配顺序,各仪器高度位置的控制要合理。
搅拌器转动要灵活。
⑵检验气密性:搅拌套塞既要保证搅拌棒转动灵活又不能漏气,可在玻棒上抹一点硅油脂。
尾气吸收装置中三角漏斗的高度要固定。
⑶加料:所有药品以及取用药品的量筒等仪器都要干燥。
AlCl3要研碎,但易吸水,所以加料速度要快,若大部分变黄则表明已水解,不可用。
⑷搅拌滴加:用同一干燥的量筒先取乙酐再取苯倒入干燥的滴液漏斗中,常温下滴加。
乙酸酐的滴加速度要慢,滴得太快温度不易控制。
⑸搅拌回流:可选择水浴或电热套加热回流,但水浴时要防止水蒸汽通过接口处进入反应体系,尤其是搅拌器套塞要密封,尽量将水浴锅盖盖上。
注意温度的控制、回流气圈的高度。
回流时间的控制(至无HCl气体产生)。
⑹搅拌水解:用酸水解前就要降温,降温时要防止尾气管倒吸碱液。
水解至固体物全部溶解。
⑺分液:注意上下层的取舍。
⑻萃取:萃取剂为苯,分两次进行,振荡要充分,但要防止冲料,分液漏斗更不能漏,注意减轻环境的污染。
所有苯层合并。
⑼洗涤:去除酸性杂质,最后水层尽量分净,苯层倒入干燥的100 mL锥形瓶中干燥。
⑽干燥:干燥剂选择的依据,干燥剂的类型,干燥剂的颗粒大小,干燥剂的用量,液体有机物干燥的时间,干燥的判断标准,干燥后的处理,干燥剂不能倒入蒸馏烧瓶。
⑾常压蒸馏:回收苯,用19 # 仪器,所有仪器要干燥,应该水浴加热,如用电炉要防苯蒸气接触明火。
蒸馏结束后将残留液转入25 mL梨形烧瓶中。
⑿减压蒸馏:用14 #仪器,所有仪器要干燥,接口处要涂硅油脂。
注意操作规程(先抽真空,再加热,结束时,先降温再放空,最后关泵)。
如用常压蒸馏提纯,冷凝管要选用空气冷凝管。
七、实验结果
1、产品性状:;
2、馏分:℃-℃、Pa;
3、理论产量:;
4、实际产量:;
5、产率:;
八、实验讨论
1、实验过程中,颜色是如何变化的?试用化学方程式表示。
2、在烷基化和酰基化反应中,AlCl3的用量有何不同?为什么?本实验为什么要用过量的苯和AlCl3?
3、反应完成后为什么要加入浓盐酸和冰水的混合物来分解产物?
4、为什么硝基苯可作为反应的溶剂?芳环上有OH、NH2等基团存在时对反应不利,甚至不发生反应,为什么?
九、实验体会
谈谈实验的成败、得失。
