大学有机方程式总结(完美)
有机化学方程式最全总结

有机反应方程式总结(一)烷烃1.甲烷与氯气在光照条件下反应生成氯仿:2.烷烃燃烧通式:(二)烯烃1.乙烯的制取:2.乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应:3.乙烯与溴的四氯化碳溶液反应:4.乙烯的催化加氢:5.乙烯的加聚反应:6. 1,3-丁二烯与溴(1:1)的反应:1,4加成:1,2加成:7.丙烯加聚:8. 2-甲基-1,3-丁二烯加聚:9.丙烯与氯气加热条件下反应(α-H的取代):(三)炔烃1.乙炔的制取:2.乙炔与足量溴的四氯化碳溶液反应:3.乙炔制聚氯乙烯:(四)芳香烃1.甲苯与酸性KMnO4溶液反应:2.苯的催化加氢:3.苯与液溴催化反应:4.苯的硝化反应:5.苯的磺化反应:6.甲苯与浓硝酸、浓硫酸的混合酸加热时获得三硝基甲苯:(五)、卤代烃1.溴乙烷在氢氧化钠水溶液中加热反应:2.溴乙烷在氢氧化钠醇溶液中加热反应:3. 2-甲基-2-溴丁烷消去溴化氢:4. 溴乙烷制备丙酸:(六)、醇类1.乙醇与钠反应:2.乙醇的催化氧化:3.乙醇制乙烯:4.乙醇制乙醚:5.乙醇和浓的氢溴酸加热反应制溴乙烷:(七)、酚类1.苯酚与氢氧化钠溶液反应:2.苯酚钠与CO2反应:3.苯酚与溴水反应:4.制备酚醛树脂:(八)、醛类1.乙醛的催化加氢:2.乙醛的催化氧化:3.乙醛与银氨溶液反应:4.乙醛与新制氢氧化铜反应:5.乙醛与HCN溶液反应:(九)、羧酸1.乙酸与乙醇发生酯化反应:2.乙酸与氨气加热条件下发生反应:3.乙酸发生还原反应生成乙醇:4.乙酸与氯气催化剂条件下反应(α-H被取代):5.两分子乳酸脱去两分子水:(十)、酯类1.乙酸乙酯与H2O混合加入稀硫酸水解:2.乙酸乙酯碱性水解:3.油脂的皂化反应(以硬脂酸甘油酯为例) :(十一)、高分子化合物1.苯乙烯合成聚苯乙烯:2.异戊二烯合成聚异戊二烯(天然橡胶):3.甲基丙烯酸甲酯合成聚甲基丙烯酸甲酯(有机玻璃):4.己二酸与己二胺脱水缩合合成纤维聚酰胺-66(尼龙-66):5.乳酸合成聚乳酸6.两分子乳酸成环。
有机化学方程式(70个)

有机化学基础反应方程式汇总1. 甲烷(烷烃通式:C n H 2n +2)甲烷的制取:CH 3CaO △2CO 3+CH 4↑(1)氧化反应甲烷的燃烧:CH 4+2O 2 点燃CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应CH 4+Cl 光照3Cl(一氯甲烷)+HClCH 3Cl+Cl 光照2Cl 2(二氯甲烷)+HClCH 2Cl 2+Cl 光照3(三氯甲烷)+HCl (CHCl 3又叫氯仿)CHCl 3+Cl 光照4(四氯化碳)+HCl(3)分解反应甲烷分解:CH 高温22. 乙烯(烯烃通式:C n H 2n )乙烯的制取:CH 3CH 2浓硫酸170℃2=CH 2↑+H 2O(消去反应)(1)氧化反应乙烯的燃烧:CH 2=CH 2+3O 点燃2+2H 2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:CH 2=CH 2+Br 2Br —CH 2Br与氢气加成:CH 2=CH 2+H 2催化剂CH 3CH 3 与氯化氢加成:CH 2=CH 2+HCl 催化剂CH 3CH 2Cl 与水加成:CH 2=CH 2+H 2O催化剂CH 3CH 2OH(3)聚合反应 乙烯加聚,生成聚乙烯:n CH 2=CH 2催化剂 [CH 2—CH 2 ] n 适当拓展:CH 3CH =CH 2+Cl 3׀ Cl CH -׀ ClCH 2 CH 3CH =CH 2+H 2催化剂CH 3CH 2CH 3 CH 3CH =CH 2+HCl 催化剂CH 3CH 2CH 2Cl 或CH 3׀ ClCHCH 3 CH 3CH =CH 2+H 2O 催化剂CH 3CH 2CH 2OH 或CH 3׀ OHCHCH 3 n CH 2=CH -CH 3催化剂 [CH 2—׀ CH 3CH ] n (聚丙烯) 3. 乙炔(炔烃通式:C n H 2n-2)乙炔的制取:CaC 2+2H 2 CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 点燃2+2H 2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
大学有机化学方程式汇总

大学有机化学方程式汇总
有机化学是研究碳化合物及其衍生物的化学性质和反应机理的学科。
在大学有机化学课程中,学生需要掌握各种有机反应的方程式。
本文档汇总了一些常见的有机化学反应方程式,供大家参考和研究。
烷烃的燃烧反应
烷烃是一类只含有碳和氢的有机化合物。
它们在氧气存在下可以发生燃烧反应,生成二氧化碳和水。
例如,甲烷的燃烧反应方程式如下:
CH4 + 2O2 -> CO2 + 2H2O
烷烃的卤代反应
烷烃可以与卤素(如氯、溴、碘)发生卤代反应,生成相应的烷基卤化物。
例如,甲烷与氯气发生卤代反应的方程式如下:
CH4 + Cl2 -> CH3Cl + HCl
醇的脱水反应
醇是含有羟基(OH)的有机化合物。
它们可以通过脱水反应,去除一个或多个水分子,生成烯烃或烷烃。
例如,环戊醇的脱水反应方程式如下:
C5H11OH -> C5H10 + H2O
烯烃的加成反应
烯烃是含有碳碳双键的有机化合物。
它们可以发生加成反应,
通过加入其他物质,形成新的化学键。
例如,乙烯与氢气发生加成反应生成乙烷的方程式如下:
C2H4 + H2 -> C2H6
酮的氧化反应
酮是含有羰基(C=O)的有机化合物。
它们可以发生氧化反应,其中羰基上的氧原子被还原,生成醇。
例如,乙酮的氧化反应方程式如下:
CH3COCH3 + [O] -> CH3COCH2OH
以上是一些大学有机化学中常见的反应方程式。
希望本文档对
您的学习有所帮助。
大学有机化学方程式总结

大学有机化学方程式总结
1. 碳氢化合物的烷烃类反应
1.1 卤代烃和氢化钠的反应
碳氢化合物(卤代烃)与氢化钠反应生成相应的烷烃,并释放出相应的卤化钠。
反应方程式如下:
R-X + NaH -> R-H + NaX
1.2 卤代烃和氢化亚铜的反应
碳氢化合物(卤代烃)与氢化亚铜反应生成相应的烷烃,并释放出相应的卤化铜。
反应方程式如下:
R-X + 2Cu2O + 2Cu -> R-H + 3Cu2X2
2. 醇类的酯化反应
2.1 醇与羧酸的酯化反应
醇与羧酸反应生成相应的酯,并释放出相应的水。
反应方程式如下:
R-OH + R'-COOH -> R'-COOR + H2O
2.2 醇与酸酐的酯化反应
醇与酸酐反应生成相应的酯,并释放出相应的酸。
反应方程式如下:
R-OH + R'-COO-CO-R'' -> R'-COOR + R''-COOH
3. 烯烃的加成反应
3.1 烯烃与卤素的加成反应
烯烃与卤素反应生成相应的二卤代烃。
反应方程式如下:
R-CH=CH2 + X2 -> R-CH2-CHX-CH2-X
3.2 烯烃与负氧化剂的加成反应
烯烃与负氧化剂反应生成相应的环氧化合物。
反应方程式如下:
R-CH=CH2 + [O] -> R-CH2-CH2-O-CH2-CH2-R
以上是一些大学有机化学方程式的总结,希望对您有帮助。
参考文献:
1. 有机化学方程式实验室手册,XX大学化学系,20XX年。
大学有机方程式总结_有机反应总结

化学竞赛有机方程式总结烷烃的化学反应:⒈卤代(F 2,I 2不可作卤化剂)CH 4+Cl 2−→−γh CH 3Cl+CH 2Cl 2+CHCl 3+CCl 4+HCl CH 3CH 2CH 3+Cl 2 −−−→−︒)25(h C γCH 3CHClCH 3(57%)+CH 3CH 2CH 2Cl(43%) ⒉氧化(略)烯烃的化学反应:⒈加卤素:CH 3CH=CH 2+Br 2−−→−4CCl CH 3CHBr -CH 2Br⒉加氢卤酸:CH 3CH=CH 2+HBr →CH 3CHBr -CH 3 符合马氏规则⒊与无机酸:CH 3CH=CH 2+H 2SO 4→CH 3CH(OSO 3H)-CH 3CH 3CH=CH 2+HOCl →CH 3CH(OH)-CH 2Cl⒋与水加成:CH 3CH=CH 2−−→−42SO H CH 3CH(OSO 3H)-CH 3−−→−O H 2CH 3CH(OH)CH 3 ⒌与硼烷加成:CH 3CH=CH 2−−→−62H B (CH 3CH 2CH 2)3B −−−→−)O(OH H -2CH 3CH 2CH 2OH顺式加成,反马氏取向生成1︒醇 ⒍过氧化物存在下,反马氏取向:CH 3CH=CH 2+HBr →−−−→−过氧化物CH 3CH 2CH 3Br HCl 、 HI 无此反应⒎催化加氢成烷烃:用Pt,Pd,Ni 等⒏高锰酸钾氧化:碱性:CH 3CH=CH 2+KMnO 4−−→−-OH CH 3CH(OH)CH 2OH+MnO 2+KOH酸性:CH 3CH=CH 2+KMnO 4−−→−∆+/H CH 3COOH+CO 2↑⒐臭氧化: R O RRC=CHR ′−→−3OC CHR ′→ 可根据产物推断反应物结构R O -O 故多用于双键位置判定′COOH′CHO′CH 2OH⒑催化氧化:CH 2=CH 2+O 2−−−→︒C 300-CH 2-CH 2 OCH 2=CH 2+O 2−−−−→−22CuCl~PdCl CH 3CHO 多用于工业生产 ⒒α-取代反应: 氯代:CH 2=CHCH 3−−−−→−︒C600-/400Cl 2CH 2=CH -CH 2Cl 溴代:CH 2=CHCH 3−−→−NBS CH 2=CH -CH 2Br ⒓重排:(CH 3)3CCH=CH 2−−→−HCl (CH 3)2CClCH(CH 3)2(主)+(CH 3)3CCHClCH 3(次) 这一重排是由于分步加成和第一步中,由H +对双键的加成生成碳正离子,其稳定性3︒>2︒>1︒,故在可能的情况下,它将以重排的方式趋于更稳定的状态。
完美版)大学有机化学方程式总结

完美版)大学有机化学方程式总结有机化学是研究碳化合物的科学领域,是大学化学课程中的重要一砖。
本文将对有机化学方程式进行总结,以便帮助学生更好地掌握这门学科。
烃类方程式烷烃:烷烃是一类只含有碳和氢的有机化合物,通式为CnH2n+2.例如,甲烷的方程式为CH4.烯烃:烯烃是一类含有碳-碳双键的有机化合物,通式为CnH2n。
例如,乙烯的方程式为C2H4.炔烃:炔烃是一类含有碳-碳三键的有机化合物,通式为CnH2n-2.例如,乙炔的方程式为C2H2.功能团方程式烃基:选择一个合适的烃基,取代有机分子的一个或多个氢原子。
例如,苄基(CH2C6H5)。
羟基:羟基是一个氧原子和一个氢原子组成的功能团,通式为-OH。
例如,乙醇的方程式为CH3CH2OH。
羰基:羰基是一个碳氧双键的功能团,通式为-C=O。
例如,乙醛的方程式为CH3CHO。
胺基:胺基是一个氮原子和若干个氢原子组成的功能团,通式为-NH2.例如,甲胺的方程式为CH3NH2.脱水反应脱水反应是一种使有机分子失去水分子的化学反应。
常见的脱水反应方程式为:R-OH -。
R + H2O其中,R代表一个烃基,例如CH3.反应机制取代反应:取代反应是一种将一个原子或一个基团替换为另一个原子或基团的反应。
常见的取代反应有氯代烃的取代反应。
加成反应:加成反应是一种两个或多个分子结合生成一个新分子的反应。
常见的加成反应有烯烃的加成反应。
消除反应:消除反应是一种分子内或分子间发生氢、卤素或其他官能团相互消除形成双键或三键的反应。
常见的消除反应有炔烃的消除反应。
以上是对大学有机化学方程式的简要总结,希望能够为学生们的学习提供帮助。
要深入了解有机化学,还需进一步学习和实践。
有机化学常用反应方程式汇总

光照光照光照光照 高温CaO△ 催化剂 加热、加压催化剂 △催化剂有机化学方程式汇总1. CH 4 + Cl 2CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 2OH 10. CH 2 = CH 2—CH 2Br 11. CH 2 = CH 2312. nCH 2 = CH 13. nCH 22] n 14. 2CH 2CHO 15. CH ≡CH + Br 2 CHBr = CHBr 16. CHBr = CHBr+ Br 2CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl 18. nCH 2 = CH [ CH 2-CH ] n Cl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)2 +H 2O H+H 2ONaOHH 2O醇△催化剂 △浓硫酸 170℃浓硫酸140℃△ 催化剂 △24.+ 3H 2-NO 2O 26. 3CH ≡CH →27. CH 3CH 2Br + H 2O CH 3CH 2OH + HBr28. CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr29. CH 3CH 2Br+ NaOH CH 2 = CH 2 + NaBr +H 2O30. 2CH 3CH 2OH+2Na 2CH 3CH 2ONa + H 2↑31. 2CH 3CH 2OH+O 2 2CH 3CHO + 2H 2O32. CH 3CH 2OH CH2 = CH 2↑+ H 2O 33.C 2H 5OH+C 2H 5OH C 2H 5OC 2H 5+H 2O 2O 2O O 3O + 2O+CO 33738. CH 339. 2CH 340. CH 34+2Ag ↓+3NH 3+H 2O41CH 3CHO+2Cu(OH)2CH 3COOH+Cu 2O ↓+2H 2O42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑ 43.2CH 3COOH+Na 2CO 3 2CH 3COONa+H 2O+CO 2↑浓硫酸△催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2O O OC —CO OCH2-CH244. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O46. 2CH3COOH + Cu(OH)2 (CH3COO)2Cu + 2H2O47.CH3COOH+CH3CH2OH CH3COOCH2CH3 +H2O48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COOH→ [ OCH2CH2C ] n +H2O50. C6H12O6 (s)+ 6O2 (g)6CO2 (g)+ 6H2O(l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2OC6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11+ H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n+ nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n+ nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2 C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH257. C17H35COO-CH2 CH2-OH C17H35COO-CH +3NaOH3C17H35COONa+ CH-OHC17H35COO-CH2 CH2-OH58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光HClClCHClClCH+−→−+2223光2.3.4.5.6.7.8.222Br CH CH CH CH +=-=9.10.11.12. 13.14.15.16.17.OH NH Ag CHO CHOH HOCH 2342)(2)(+ O H NH Ag COONH CHOH HOCH 2344232)(++↓+−→−∆18.19.20.21.高中有机化学知识点总结 1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解 (5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
(完整版)大学有机化学反应方程式总结(较全).doc
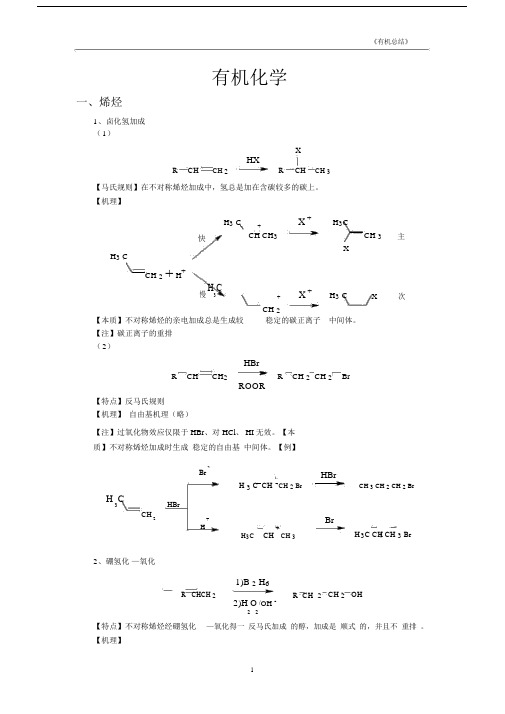
有机化学一、烯烃1、卤化氢加成 ( 1)XHXRCHCH 2R CHCH 3【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】H 3 C+X +H 3CCH 3主快CH CH 3XH 3 CCH 2+ H +慢H 3C+X +H 3 CX次CH 2 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子 中间体。
【注】碳正离子的重排( 2)HBrR CHCH 2 R CH 2 CH 2 BrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于 HBr 、对 HCl 、 HI 无效。
【本质】不对称烯烃加成时生成 稳定的自由基 中间体。
【例】BrH 3 C CH CH 2 BrH 3CHBrCH2+H+H 3CCH CH 3HBrCH 3 CH 2 CH 2 BrBrH 3C CH CH 3 Br2、硼氢化 —氧化1)B 2 H 6R CHCH 2R CH 2 CH 2 OH2)H O /OH -2 2【特点】不对称烯烃经硼氢化 —氧化得一 反马氏加成 的醇,加成是 顺式 的,并且不 重排 。
【机理】H 3CH 3CH 3CCHCH 2CHCH 3CHCH 3HBH 2HBH 2HBH 2H 3CCH 3CH=CH 2-CH 2CH 2CH 3O OH-CH CH 2(CH 3 CH 2 CH 2 )3BH 3 CH 2CH 2C BO OHHBH 2CH 2CH 2CH 3CH 2CH 2CH 3CH 2 CH 2 CH 3+-H 3 CH 2 CH 2 C BOHOH 3CH 2CH 2 C -OCH 2CH 2CH 3B-CH CH CH3OOHHO O22CH 2CH 2CH 3HOO -B(OCH 2CH 2CH 3)3BOCH 2 CH 2CH 3OCH 2CH 2CH 3B(OCH 2 CH 2 CH 3 )3+3NaOH 3NaOH3HOCH 2CH2CH33+Na 3BO3【例】1)BH 3OH H2)H 2O 2/OH -CH3HCH33、 X 2 加成BrBr 2 /CCl 4CCCC Br【机理】Br BrBrBr -Br+C +C BrCCC CC CBrBr H 2OBr +BrC+C C-HCC C+2【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
(完整版)有机化学方程式汇总

有机化学反应方程式汇总1. 甲烷与氯气CH 4+Cl 2CH 3Cl+HCl CH 3Cl+Cl 2CH 2Cl 2+HClCH 2Cl 2+Cl 2CHCl 3+HCl CHCl 3+Cl 2CCl 4+HCl (分步取代)2. 甲烷的燃烧3. 烷烃的燃烧通式4. 甲烷的热分解 CH 4−−→−高温C+2H 25. 烷烃的热分解6. 乙烯实验室制法 CH 3CH 2OH H 2O + CH 2=CH 2 ↑(浓硫酸:催化剂,脱水剂)7. 乙烯的燃烧8. 乙烯通入溴水中9. 乙烯和氢气加成10. 乙烯和HCl 的反应 11. 乙烯水化制乙醇 12. 乙烯催化氧化制备乙醛13. 乙烯的加聚反应 14. 制取聚丙烯 CH 4 + 2O CO 2 + 2H 2O燃烧C n H 2n+2 + O n CO 2 + (n + 1)H 2O 3n+1 2燃烧△C 4H C 2H 4+C 2H 6△C 4H CH 4 + C 3H 6CH 2=CH 2 + 3O 2 2CO 2 + 2H 2O点燃2CH 2=CH 2 + O 2CH 3CHO催化剂加热加压CH 3CH=CH 2 + H CH 3CH 2CH 3催化剂CH 2=CH 2 + Br 2 CH 2BrCH 2BrCH 2=CH 2 + HCl CH3CH 2Cl 催化剂CH 2=CH 2 + H 2O CH 3CH 2OH催化剂―CH 2―CH 2―nn CH 2=CH 2催化剂―CH 2――nn CH 2=CH ―CH 催化剂15. 1,3-丁二烯的加成反应 1,2加成1,4加成完全加成16. 1,3-丁二烯的加成反应 17. 乙炔的制取 CaC 2+2H 2O →C 2H 2↑+Ca(OH)218. 乙炔的燃烧19. 乙炔通入溴水中20. 乙炔与氢气的加成反应21. 乙炔水化制备乙醛22. 聚氯乙烯的制备23. 苯的燃烧 24. 苯与液溴反应(FeBr 3作催化剂)25. 苯的硝化反应Cl+ Cl 2催化剂+ Cl 2催化剂Cl+ 2Cl 2催化剂Cl ClCl―CH 2―C=CH ―CH 2―nn CH 2=C ―CH=CH 2催化剂CH 3CH 32 C 2H 2 + 5 O 4 CO 2 + 2 H 2O (l) + 2600 kJ点燃1, 2 - 二溴乙烷HC CH +Br BrC C Br Br H H 1, 1 , 2 , 2 - 四溴乙烷+Br BrC C Br BrH H C C Br Br H Br Br H 催化剂HC CH+H 2H 2C CH 2CH ≡CH + HCl CH 2=CHCl 催化剂氯乙烯CH ≡CH + H 2O乙醛3C C OH 催化剂聚氯乙烯H 2C CHCln -CH 2-CH --Cln 点燃+ 15 O 12 CO 2 + 6 H 2O2+ Br 溴苯NO 226. 苯的磺化反应27. 苯与氢气加成生成环己烷28. 苯与氯气的加成反应29. 苯的同系物被高锰酸钾酸性溶液氧化30.甲苯和氯气的取代反应31. 甲苯的硝化反应32. 甲苯和氢气的加成反应33. 溴乙烷水解 CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr34. 溴乙烷消去反应 CH 3CH 2Br +NaOH CH 2=CH 2↑ + NaBr + H 2O35. 乙醇与钠反应 2CH 3CH 2OH + 2Na 2CH 3CH 2ONa + H 2↑36. 乙醇催化氧化 2CH 3CH 2OH + O 2 2CH 3CHO + 2H 2O37. 乙醇的燃烧 CH 3CH 2OH +3O 2→2CO 2 + 3H 2OH 2O,△ Cu △醇 △HO SO 3+△+ H 2O3H 苯磺酸催化剂2△ClCl Cl ClClCl + 3 Cl 2光照C H KMnO 4 (H +)CH 3HO NO 2+ 3浓硫酸+ 3 H 2OCH 3NO 2NO 2O 2N2,4,6-三硝基甲苯 (TNT)+ 3 H CH 3CH 3CH 3CH 3Cl+ Cl + HClFeCH 3ClCH 3+ Cl + HClFe38. 乙醇与浓氢溴酸的反应 CH 3CH 2OH +HBr →CH 3CH 2Br + H 2O39. 乙醇脱水(分子内、分子间) CH 3CH 2OH CH 2=CH 2 ↑+H 2O (消去反应)2CH 3CH 2OH CH 3CH 2—O —CH 2CH 3+ H 2O (取代反应)40. 苯酚的电离方程式 41. 苯酚与NaOH 溶液反应42. 苯酚与金属钠反应 43. 苯酚和碳酸钠溶液反应44. 苯酚钠和盐酸反应 45. 苯酚钠溶液中通入CO 2气体46. 苯酚和浓溴水反应(苯酚的定性检验和定量测定方法)47. 苯酚的硝化反应48. 苯酚与FeCl 3溶液49. 苯酚的加成反应浓H 2SO 4 140℃OH电离O -+ H+OH + NaOHONa + H 2OOH 2 + 2Na ONa 2 + H OH + Na 2CO ONa + NaHCO 3+ HCl OH + NaClONa + CO 2 + H 2OH + NaHCO 3ONa OH+ 3 HNO + 3 H 2OOHNO 2O 2NNO 2浓硫酸苦味酸OHFeCl 3溶液紫色,易溶于水的物质OHOH+ 3 H 2Ni环己醇OH+ 3 Br OHBr BrBr+ 3 HBr50. 苯酚的缩聚反应n + n + n H 2O2OHH C OH n51.苯酚的酯化反应52. 乙醛的加成反应(还原反应) 53. 乙醛的氧化反应—燃烧反应54. 乙醛的催化氧化反应 55. 乙醛与银氨溶液的反应 ③ CH 3CHO + 2 [Ag(NH 3)2]+3COO - + NH 4+3 + H 2O56. 乙醛与Cu(OH)2悬浊液反应57. 乙醛的制备方法乙醇氧化法乙烯氧化法乙炔水化法58. 醛的加成反应(还原反应)59. 醛的催化氧化反应OH+ CH 3COOH + H 2OOOCCH3乙酸酐CH 3CHO + H 23CH 2OH 2CH 3CHO + 5O 4CO 2 + 4H 2O点燃2 CH 3CHO + O 3COOH① Ag + + NH 3·H 2O AgOH + NH 4+② AgOH + 2 NH ·H 2O [Ag(NH3)2]+ + OH - + 2 H 2O2 CH 3CH 2OH + O 3CHO + 2 H 2O + H 23CHOHC CH 2 + O 22 CH 3CHO 加热 加压H 2C CH 2催化剂2R―CHO + O 2―COOHR ―CHO + H 2―CH 2OHCH 3CHO + 2 Cu(OH)23COOH + Cu 2O + 2 H 2OCu 2+ + 2 OH - Cu(OH)260. 醛与银氨溶液的反应 61. 醛与Cu(OH)2悬浊液反应 62. 甲醛的银镜反应 63. 甲醛与Cu(OH)2悬浊液反应 64. 乙酸与氢氧化铜悬浊液 2CH 3COOH + Cu(OH)2 = (CH 3COO)2Cu + 2H 2O65. 乙酸乙酯制取(用饱和碳酸钠溶液收集)CH 3COOH + CH 3CH 2OHCH 3COOC 2H 5 + H 2O66. 乙二酸和乙二醇反应C ―OH ∣C ―OH OOHO ―CH 2∣HO ―CH 2+ + 2H 2O 浓硫酸C C O CH 2CH 2O O OnHOOC ―COOH + nHOCH 2―CH 2OH + 2nH 2O ―C ―C ―OCH 2―CH 2O ―O On浓硫酸67. 乙醇和硝酸酯化CH 3CH 2OH + HNO 3 CH 3CH 2ONO 2 + H 2O浓硫酸68. 乙酸乙酯的水解CH 3COOC 2H 5 + H 2O CH 3COOH + CH 3CH 2OH 稀硫酸CH 3COOC 2H 5 + NaOH ==== CH 3COONa + CH 3CH 2OH69. 甲酸钠与银氨溶液反应HCOONa +2Ag(NH 3)2OH NH 4OCOONa +2Ag ↓+3NH 3↑+H2O浓硫酸△R ―CHO + 2Cu(OH)2 R ―COOH + Cu 2O ↓ + 2H 2OR ―CHO + 2Ag(NH 3)2OH R ―COONH 4 + 2Ag ↓ + 3NH 3 + H 2O HCHO + 4 Cu(OH)2 CO 2 + 2 Cu 2O + 5 H 2O HCHO + 4 [Ag(NH 3)2]+ + 4 OH - (NH 4)2CO 3 + 4 Ag + 6 NH 3 + 2 H 2O70.甲酸钠与新制氢氧化铜反应HCOONa+2Cu(OH)2+ NaOH Na2CO3+Cu2O↓+3H2O71.葡萄糖的银镜反应CH2OH(CHOH)4CHO+2Ag(NH3)2OHCH2OH(CHOH)4COONH4+2Ag↓+3NH3↑+H2O72.葡萄糖与新制氢氧化铜反应CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O 73. 蔗糖水解C12H22O11 + H2O 催化剂C 6H 12O6 + C6H12O6蔗糖葡萄糖果糖74. 麦芽糖水解C12H22O11 + H2O 催化剂2C6H12O6麦芽糖葡萄糖75. 淀粉水解(C6H10O5)n + nH2O 催化剂nC6H12O6淀粉葡萄糖76. 纤维素水解(C6H10O5)n + nH2O 催化剂nC6H12O6纤维素葡萄糖77. 工业制取肥皂(皂化反应)C17H35COO―CH2∣C17H35COO―CH∣C17H35COO―CH2+ 3NaOH 3 C17H35COONa +HO―CH2∣HO―CH∣HO―CH278.油酸甘油酯硬化79.工业制造乙苯 + CH2=CH280.制造硝酸纤维的反应81.甲苯与高锰酸钾酸性溶液反应5 +6KMnO4+9H2SO4→ 5 +3K2SO4+ 6MnSO4+ 14H2O82.甘油制取炸药83.甲醛与苯酚反应制取酚醛树脂代表物之间的转化关系:CH3CH3CH2=CH2 CH=CH CH2=CHCl CH3CH 2OHCH 2BrCH2BrCH2OHCH2OHCHOCHOCOOHCOOH[ CH2—CH ]nClCH3CHO CH3COOHCH3COOC2H5CH3CH2BrO=CO=CCH2CH2OO。
有机化学方程式总结

有机部分化学方程式小结1.甲烷的主要化学性质(1)氧化反应 CH4(g)+2O2(g)−−→−点燃 CO2(g)+2H2O(l)(2)取代反应2.乙烯的主要化学性质(1)氧化反应: C2H4+3O2 2CO2+2H2O(2)加成反应乙烯还可以和氢气、氯化氢、水等发生加成反应。
CH2=CH2+ H2CH3CH3CH2=CH2+HCl CH3CH2Cl(一氯乙烷)CH2=CH2+H2O CH3CH2OH(乙醇)(3)聚合反应:3.乙炔的主要化学性质(1)乙炔的实验室制取(2)加成反应(氯乙烯)(聚氯乙烯)(1)4.苯的主要化学性质(2)氧化反应 2C6H6+15O2−−→−点燃 12CO2+6H2O(3) 取代反应+ Br 2−−→−3FeBr + HBr苯与硝酸(用HO-NO2表示)发生取代反应, 生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。
+ HO-NO 2浓硫酸 △+ H 2O( TNT 三硝基甲苯)(4) 加成反应用镍做催化剂, 苯与氢发生加成反应, 生成环己烷。
+ 3H 2 −−→−催化剂5.苯酚的主要化学性质 (1)苯酚的弱酸性(2)苯酚的取代反应(鉴别苯酚)(鉴别苯酚: 滴加FeCl3溶液, 溶液呈紫色) 6.卤代烃的主要化学性质 (1)取代反应 (2)消去反应7、乙醇的重要化学性质NO 2(1)乙醇与金属钠的反应: 2CH3CH2OH+2Na 2CH3CH2ONa+H2↑(2)乙醇的氧化反应①乙醇的燃烧 CH3CH2OH+3O2−−→−点燃 2CO2+3H2O②乙醇的催化氧化反 2CH3CH2OH+O2−−→−AgCu或2CH3CHO+2H2O③乙醇在常温下的氧化反应CH3CH2OH−−−−−−−−→−或酸性重铬酸钾溶液酸性4KMnOCH3COOH(3)乙醇的消去反应:(4)乙醇的取代反应:8、乙醛的重要化学性质(1)氧化反应银镜反应: 配银氨溶液: AgNO3 + NH3·H2O == AgOH↓ + NH4NO3AgOH + 2NH3·H2O == Ag(NH3)2OH + 2H2O甲醛的银镜反应 HCHO + 4Ag(NH3)2OH 2H2O + 4Ag↓+6NH3+(NH4)2CO3(2)还原反应9、乙酸的重要化学性质(1)乙酸的酸性①乙酸能使紫色石蕊试液变红②乙酸能与碳酸盐反应, 生成二氧化碳气体利用乙酸的酸性, 可以用乙酸来除去水垢(主要成分是CaCO3):2CH3COOH+CaCO3(CH3COO)2Ca+H2O+CO2↑乙酸还可以与碳酸钠反应, 也能生成二氧化碳气体:2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑上述两个反应都可以证明乙酸的酸性比碳酸的酸性强。
有机化学方程式(70个)

有机化学基础反应方程式汇总1. 甲烷(烷烃通式:CnH2n+2)甲烷的制取:CaO △(1)氧化反应甲烷的燃烧:点燃甲烷不成使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应 光照一氯甲烷)+HCl 光照二氯甲烷)+HCl 光照三氯甲烷)+HCl (CHCl3又叫氯仿) 光照四氯化碳)+HCl(3)分解反应甲烷分解:高温2. 乙烯(烯烃通式:CnH2n)乙烯的制取:浓硫酸170℃=CH2↑+H2O(消去反应) (1)氧化反应乙烯的燃烧:CH2=点燃乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:CH2=—CH2Br与氢气加成:CH2=CH2+H2催化剂CH3CH3 与氯化氢加成:CH2=CH2+HCl 催化剂CH3CH2Cl 与水加成:CH2=CH2+H2O催化剂CH3CH2OH(3)聚合反应 乙烯加聚,生成聚乙烯:n CH2=CH2催化剂 [CH2—CH2 ] n 适当拓展:CH3CH =׀ Cl CH -׀ ClCH2 CH3CH =CH2+H2催化剂CH3CH2CH3 CH3CH =CH2+HCl 催化剂CH3CH2CH2Cl 或CH3׀ ClCHCH3 CH3CH =CH2+H2O 催化剂CH3CH2CH2OH 或CH3׀ OHCHCH3 nCH2=CH -CH3催化剂 [CH2—׀ CH3CH ] n(聚丙烯) 3. 乙炔(炔烃通式:CnH2n-2)乙炔的制取: CH↑+Ca(OH)2(1)氧化反应乙炔的燃烧:点燃乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:CHBr =CHBr CHBr =—CHBr2 与氢气加成:HC≡CH+H2催化剂H2C =CH2与氯化氢加成:HC≡CH+HCl催化剂CH2=CHCl (3)聚合反应图2 乙烯的制取图1 甲烷的制取图3 乙炔的制取氯乙烯加聚,得到聚氯乙烯:nCH2=CHCl催化剂[CH2—׀ Cl CH ] n 乙炔加聚,得到聚乙炔:n HC≡CH催化剂 [CH =CH ] n 4. 1,3-丁二烯 与溴完全加成:CH2=CH -CH =CH2Br -CHBr -CHBr -CH2Br 与溴1,2-加成:CH2=CH -CH =CH2Br -CHBr -CH =CH2 与溴1,4-加成:CH2=CH -CH =CH2Br -CH =CH -CH2Br 5. 苯苯的同系物通式:CnH2n-6(1)氧化反应苯的燃烧:2+15O2点燃苯不克不及使溴水和酸性高锰酸钾溶液褪色。
大学有机化学方程式

1.加硫酸--烯烃的间接水合法制醇:
2.加水--烯烃的直接水合法制醇:
3.加卤素:
4.溴鎓离子机理:
5.加次卤酸(X2/H2O or HXO):
6.自由基加成反应(HBr 特有)
在过氧化物存在下与溴化氢反应得反马氏规则的加成产物:氢加到含氢较少的碳原子上氯化氢和碘化氢没有过氧化物效应,加成取向仍符合马氏规则。
HI吸热不易反应
7.硼氢化反应:
烷基硼烷在碱性条件下用过氧化氢处理转变成醇,反应后氢加在含氢较少的烯碳原子上,用来制备伯醇:
硼氢化反应得顺式加成产物,立体选择性很高,是一个立体专一性的反应。
8.高锰酸钾氧化:
9.臭氧化还原反应:
若无锌粉的存在该条件下醛会被继续还原成羧酸
10.环氧化反应:
烯烃被过氧酸氧化生成环氧化合物,该反应立体化学上是顺式反应
11.α-氢的反应
在高温或光照下,α-氢易被卤素取代,发生自由基取代反应
12.NBS:N-溴代丁二酰亚胺,常见的烯丙位溴代试剂。
(完整版)有机化学反应方程式汇总

浓硫酸△ 有机物类别官能团 主要化学性质 烷烃——取代反应:CH 4+Cl 2CH 3Cl +HCl烯烃碳碳双键加成反应: CH 2=CH 2+HBr催化剂 △CH 3-CH 2Br ,(还可与Br 2、H 2O 、H 2在一定条件下发生加成反应)加聚反应:nCH 2=CH 2催化剂-[CH 2-CH 2氧化反应:使酸性KMnO 4溶液褪色(同时生成CO 2)炔烃碳碳三键同烯烃 芳香烃苯——取代反应: FeBr 3加成反应:苯的 同系物——取代反应:氧化反应:使酸性KMnO 4溶液褪色(与苯环相连的C 上有H 时统一被氧化为苯甲酸)卤代烃 —X取代反应:CH 3CH 2Br+NaOHH 2OCH 3CH 2OH+NaBr消去反应:CH 3CH 2Br+NaOH CH 2=CH 2↑+NaBr+H 2O 醇—OH与活泼金属反应:2CH 3CH 2OH+2Na 2CH 3CH 2ONa+H 2↑取代反应:CH 3CH 2OH+HBr△CH 3CH 2Br+H 2O 消去反应:CH 3CH 2OH浓硫酸 170℃CH 2=CH 2↑+H 2O氧化反应:2CH 3CH 2OH+O 2催化剂 △2CH 3CHO+2H 2O醛—CHO还原反应(加成反应):CH 3CHO+H 2催化剂 △CH 3CH 2OH氧化反应:2CH 3CHO+O 2催化剂 △2CH 3COOHCH 3CHO+2Ag(NH 3)2OH△CH 3COONH 4+2A g ↓+3NH 3+H 2OCH 3CHO+2C u (O H )2 +NaOH△CH 3COONa+Cu 2O ↓+3H 2O羧酸 —COOH 酸的通性:如CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑酯化反应:CH 3COOH+ CH 3CH 2OH 浓H 2SO 4CH 3COOCH 2CH 3+H 2O 酯—COO —水解反应:CH 3COOCH 2CH 3+H 2OCH 3COOH+ CH 3CH 2OH酚弱酸性:取代反应: 光照+HNO 3—NO 2 +H 2O浓硫酸 △OHOH + NaOH ONa + H 2O OH+3Br 2OHBrBrBr+3HBr↓ 乙醇+HBr+Br 2 Br —CH 3 +3HNO 3 CH 3NO 2O 2N NO 2+3H 2O +3H 2Ni反应试剂有机物类别或官能团反应类型反应方程式举例X2氯气、液溴CH4+Cl2CH3Cl+HCl浓溴水苯酚取代反应溴水或溴的四氯化碳溶液“C=C”或“C≡C”加成反应H2C=CH2 + Br2 BrH2C-CH2BrHX “C=C”或“C≡C”加成反应H2C=CH2+HBr催化剂△H3C-CH2Br醇取代反应CH3CH2OH+HBr△CH3CH2Br+H2OH2O “C=C”或“C≡C”加成反应H2C=CH2+H2O催化剂△H3C-CH2OH酯水解反应CH3COOCH3+H2O催化剂△CH3COOH+CH3OHNa 醇、苯酚、—COOH置换反应2CH3CH2OH+ 2Na 2CH3CH2ONa+H2↑NaOH 苯酚、—COOH中和反应HCOOH+NaOH HCOONa+H2O酯水解反应CH3COOCH3+ NaOH CH3COONa+CH3OH卤代烃取代反应CH3CH2Br+NaOH△CH3CH2OH+NaBr消去反应CH3CH2Br+NaOH CH2= CH2↑+NaBr+H2ONa2CO3苯酚、—COOH复分解反应NaHCO3—COOH 复分解反应HCOOH+NaHCO3==HCOONa+CO2↑+H2OH2“C=C”或“C≡C”加成反应H2C=CH2+H2催化剂△H3C-CH3苯环加成反应羰基、醛基加成反应(还原反应)CH3CHO +H2催化剂△CH3CH2OH银氨溶液、新制Cu(OH)2醛、葡萄糖氧化反应略O2醛、醇氧化反应2CH3CHO+O2催化剂△2CH3COOH 大多数有机物氧化反应大多数有机物可燃烧生成CO2和H2O酸性KMnO4溶液醛、醇、酚、“C=C”、“C≡C”苯的同系物氧化反应略乙醇OH+3Br2OHBrBrBr+3HBr↓光照取代反应烷烃、苯环+3H2Ni。
有机化学方程式总结

有机化学方程式总结有机化学是一门研究有机化合物的组成、结构、性质和变化的科学。
在有机化学的学习中,掌握各种有机化合物的化学反应方程式是非常重要的一部分。
下面是对一些常见有机化学反应方程式的总结:1、烷烃的取代反应CH4 + Cl2 → CH3Cl + HCl2、烯烃的加成反应CH2=CH2 + H2 → CH3CH33、炔烃的加成反应CH≡CH + 2H2 → CH3CH34、醇的氧化反应2CH3CH2OH + O2 → 2CH3CHO + 2H2O5、酮的氧化反应2RCOCH3 + O2 → 2RCOCHO + 2H2O6、羧酸的酯化反应CH3COOH + CH3CH2OH → CH3COOCH2CH3 + H2O7、酯的水解反应CH3COOCH2CH3 + H2O → CH3COOH + CH3CH2OH8、醛的还原反应R-CHO + H2 → R-CH2OH9、酮的还原反应R-CO-R' + H2 → R-CH2-R' + H2O10、酰胺的水解反应NH2CO-R + H2O → NH3 + R-COOH以上仅是一些常见的有机化学反应方程式,但它们是学习有机化学的基础。
通过理解和记忆这些反应方程式,可以更好地理解有机化学的原理和应用。
对于一些复杂的有机化学反应,需要更加深入的学习和理解。
真空泄污系统自控系统是一种高效、环保的自动化设备,专门设计用于处理和减少废物排放。
此系统利用真空技术,自动抽取和处理废气、废液等污染物,达到国家环保排放标准。
真空泵:用于产生负压,从污染源抽取污染物。
传感器:检测污染物的种类和浓度,以便控制系统能够做出相应的调整。
控制系统:根据污染物的种类和浓度,自动调整真空泵的工作状态和净化设备的运行。
净化设备:对抽取的污染物进行过滤、吸附、化学反应等处理,降低或消除污染。
排放系统:经过处理的污染物被安全地排放到大气中。
自动检测:系统自动检测污染物的种类和浓度,实时调整处理策略。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
完美基本有机反应:烷烃的化学反应:⒈卤代(F 2,I 2不可作卤化剂)CH 4+Cl 2−→−γh CH 3Cl+CH 2Cl 2+CHCl 3+CCl 4+HCl CH 3CH 2CH 3+Cl 2 −−−→−︒)25(h C γCH 3CHClCH 3(57%)+CH 3CH 2CH 2Cl(43%)⒉硝化,磺化,氧化(略) 烯烃的化学反应:⒈加卤素:CH 3CH=CH 2+Br 2−−→−4CCl CH 3CHBr -CH 2Br⒉加氢卤酸:CH 3CH=CH 2+HBr →CH 3CHBr -CH 3 有区域选择,符合马氏规则 ⒊与无机酸:CH 3CH=CH 2+H 2SO 4→CH 3CH(OSO 3H)-CH 3 CH 3CH=CH 2+HOCl →CH 3CH(OH)-CH 2Cl⒋与水加成:CH 3CH=CH 2−−→−42SO H CH 3CH(OSO 3H)-CH 3−−→−OH 2CH 3CH(OH)CH 3⒌与硼烷加成:CH 3CH=CH 2−−→−62H B (CH 3CH 2CH 2)3B −−−→−)O(OH H -2CH 3CH 2CH 2OH 顺式加成,反马氏取向生成1︒醇⒍过氧化物存在下,反马氏取向:CH 3CH=CH 2+HBr →−−−→−过氧化物CH 3CH 2CH 3Br HCl 无此反应⒎催化加氢成烷烃:用Pt,Pd,Ni 等 ⒏高锰酸钾氧化:酸性:CH 3CH=CH 2+KMnO 4−−→−-OH CH 3CH(OH)CH 2OH+MnO 2+KOH 碱性:CH 3CH=CH 2+KMnO 4−−→−∆+/H CH 3COOH+CO 2↑ ⒐臭氧化: R ORRC=CHR’−→−3OC CHR’→ 可根据产物推断反应物结构R O -O 故多用于双键位置判定−−−→−O璈O H 222RCOR+R’COOH−−→−O H -Zn 2RCOR+R’CHO−−→−4LiAlH RRCHOH+R’CH 2OH⒑催化氧化:CH 2=CH 2+O 2−−−−→−︒C300-Ag/200CH 2-CH 2 OCH 2=CH 2+O 2−−−−→−22CuCl ~PdCl CH 3CHO 多用于工业生产 ⒒α-取代反应:氯代:CH 2=CHCH 3−−−−→−︒C 600-/400Cl 2CH 2=CH -CH 2Cl 溴代:CH 2=CHCH 3−−→−NBSCH 2=CH -CH 2Br 两个反应均为自由基取代反应,NBS 即N-溴代琥珀酰亚胺⒓重排:(CH 3)3CCH=CH 2−−→−HCl(CH 3)2CClCH(CH 3)2(主)+(CH 3)3CCHClCH 3(次) 这一重排是由于分步加成和第一步中,由H +对双键的加成生成碳正离子,其稳定性3︒>2︒>1︒,故在可能的情况下,它将以重排的方式趋于更稳定的状态。
⒔聚合反应:含二聚和多聚(略) 共轭双烯的反应: ⒈1,2-加成和1,4-加成:CH=CH -CH=CH −→−2BrBrCH 2CH=CHCH 2Br+BrCH 2-CHBr -CH=CH 21,4-产物 1,2-产物 不同反应条件下主要产物不同室温以上或极性溶剂: CH=CH -CH=CH+Br 2→BrCH 2CH=CHCH 2Br (1,4)0℃以下或非极性溶剂CH=CH -CH=CH+Br 2→BrCH 2-CHBr -CH=CH 2 (1,2) ⒉与等摩尔的H 2加成:CH=CH -CH=CH −−−→−+Na EfOH CH 3CH=CHCH 3 (1,4) CH=CH -CH=CH −−→−/PdH 2CH 3CH 2CH=CH 2 (1,2) ⒊双烯加成(Diels-Alder 反应): 合成六元环的良好反应 炔烃的反应:⒈加氢①催化加氢:CH 3C ≡CH −−→−/PdH 2CH 3CH 2CH 3 ②部分加氢:CH 3C ≡CCH 3−−−−→−-PdBaSO H 42/ CH 3CH=CHCH 3(顺式)CH 3C ≡CCH 3−−−→−-)(3l NH Na CH 3CH=CHCH 3(反式) ⒉亲电加成:① 加卤素:CH 3C ≡CH −−→−2)(Br A CH 3CBr=CHBr −−→−)(2B Br CH 3CBr 2-CHBr 2 反应B 远难于A ,故可停留在第一步产物阶段②双键优先于叁键加成: CH 2=CH -CH 2-C ≡CH −→−2BrBrCH 2-CHBr -CH 2C ≡CH③加氢卤酸:CH 3C ≡CH+HBr →(A)CH 3CBr=CH 2+HBr →(B)CH 3CBr 2CH 3 反应亦可停留在A 阶段 ⒊与亲核试剂加成:①与水加成:CH 3C ≡CH+H 2O −−→−4HgSO [CH 3C(OH)=CH 2]−−→−重排CH 3COCH 3 中间步骤称为烯醇式重排②加HCN :CH ≡CH+HCN −−−−−→−-ClNH Cl Cu 422CH 2=CH -CN 产物为制取聚丙烯腈的原料③与其他亲核试剂的加成:CH ≡CH+ROH →CH 2=CH -ORCH ≡CH+NH 3→CH 2=CH -NH 2 CH ≡CH+CH 3COOH →CH 2=CH -OOCCH 3 ⒋作为酸的反应:① 与碱金属反应:CH 3C ≡CH+Na[NH 3(l)]→CH 3C ≡C -Na② 与重金属(盐)反应:CH 3C ≡CH +Ag/NH 3-H 2O →CH 3C ≡C -Ag ↓ CH 3C ≡CH+Cu/NH 3-H 2O →CH 3C ≡C -Cu ↓ ⒌氧化反应:①高锰酸钾氧化:RC ≡CR’+KMnO 4/H +→RCOOH+R’COOH②臭氧化:RC ≡CR’−−−−−→−B A OH ./CCl O .243RCOOH+R’COOH⒍聚合反应:① 线型低聚:2CH ≡CH →Cu 2Cl 2-NH 4Cl/H +→CH 2=CH -C ≡CH 产物是制取丁二烯和氯丁二烯的原料② 环型低聚:3CH ≡CH −−−→−︒-C500400 ⒎制备高级炔:CH 3C ≡CNa+CH 3CH 2CH 2Br →CH 3C ≡C -CH 2CH 2CH 3 卤代烷的反应:⒈亲核取代反应:RX+NaOH-H2O→ROHRX+NH3→RNH2RX+R’ONa→ROR’RX+NaCN→RCNRX+H2S→RSHRX+NaC≡CR’→RC≡CR’RX+CH3COONa→CH3COORRX+NaI-丙酮→RI+NaX↓(X:Cl,Br)RX+AgNO3-C2H5OH→RNO3+AgX↓后一个反应常用于RX的鉴别⒉消除反应:CH3CH2CHClCH3+KOH-ROH→CH3CH=CHCH3(主要)+ CH3CH2CH=CH2遵守查依采夫规则主要生成含取代基较多的双键产物⒊生成金属有机化合物:RCl+MgEt2O→RMgCl RCl+Li→RLi⒋被还原:RCl+LiAlH4,THF→RHRCl+Zn/HCl→RHRCl+Pt/H2→RH⒌卤素置换:RCl(Br)+NaI-丙酮→RI+NaCl醇的性质:⒈醇的酸性:与活泼金属反应CH3CH2OH+Na→CH3CH2ONa+H2↑酸性ROH(3︒<2︒<1︒<CH3OH)<HOH<RCOOH碱性RO-(3︒>2︒>1︒>CH3O-)>OH->RCOO-⒉成酯反应:①与硫酸成酯:CH3OH+H2SO4→(CH3O)2SO2+H2O产物(CH3O)2SO2是常用的甲基化试剂②与硝酸成酯:−+H CH2ONO2CHONO2CH2ONO2CH2OHCHOHCH2OH+HNO3−→产物称硝酸甘油可作为炸药或用于医药−+H CH3COOCH2CH3③与有机酸成酯:CH3CH2OH+CH3COOH−→⒊卤代反应:①与氢卤酸反应:ROH+HX→RX+H2O产物亦可视为氢卤酸的酯HX:HI>HBr>HClCH3CH2OH+HCl/ZnCl2→CH3CH2Cl+H2O试剂HCl/ZnCl2称Lucas试剂,用于鉴别醇的级别ROH反应活性:烯醇式~3︒>2︒>1︒②重排反应:(CH3)3C-CH2OH+HCl→(CH3)2CClCH2CH3③与卤化磷反应:ROX+PX3→RX+H3PO4 (PBr3.PCl3)−P RIROH+I2−→⒋消除反应:与硫酸共热CH 3CH 2CHOHCH 3−−−→−∆/SO H 42CH 3CH=CHCH 3(主要)+CH 3CH 2CH=CH 2 ROH 的反应活性:3︒>2︒>1︒(CH 3)3C -OH −−−−→−︒C/87SO H 42(CH 3)2C=CH 2CH 3CH 2CHOHCH 3−−−−−→−︒C/100SO 60%H 42CH 3CH=CHCH 3 CH 3CH 2CH 2CH 2OH −−−−−→−︒C/140SO 75%H 42CH 3CH 2CH=CH 2 ⒌氧化反应:① CrO 3-H 2SO 4氧化:RCHOH −−−−→−423SOH -CrO RCH=OROH 2︒ROH 氧化成酮 3︒ROH 不易氧化② HIO 4氧化:RRCOH -CHOHR’ −−→−4IOH RRC=O+R’CH=O ⒍醇制法①烯烃的硼氢化:CH 3CH=CH 2−−−−−−→−B A -2262OH -O .H H .B CH 3CH 2CH 2OH ③ 格氏试剂法:是合成指定结构的醇的最好方法RCH=O+CH 3CH 2MgBr →RCHOMgBrCH 2CH 3+H 2O(H +)→RCHOHCH 2CH 3 ④ 羰基化合物还原法:RCH=O →RCH 2OH 羰基化合物还可以是 醛 酮 酯 酰卤 羧酸 还原剂可以是LiAlH 4 √ √ √ √ √ NaBH 4 √ √ × √ × H 2/Ni √ √ √ √ × 羰基化合物的反应: 亲核加成反应:⒈NaHSO 3加成:RCH=O+NaHSO 3→RCHOH -SO 3Na ↓ 产物为结晶状,反应物不同结晶不同,可用于鉴别⒉HCN 加成:RCH=O+HCN/OH -→RCHOHCN +H 2O/H +→RCHOH -COOH ⒊格氏试剂加成:RCH=O+R’MgX →RCHOHR’ 使用不同的羰基化合物可分别得到1︒,2︒,3︒醇⒋胺的加成:RCH=O+NH 2R’→RCHOHNHR’→RCH=NR’产物可水解(H 2O-H +)复原,故可用于保护羰基,亦可经还原制取1︒,2︒胺 ⒌胲(羟胺)的加成:RCH=O+NH 2-OH →RCH=N -OH(肟)产物可发生重排,工业上用于尼龙-6单体生产 =O → =N -OH → =O ⒍肼的加成:RCH=O+H 2N -NH 2→RCH=NH 2(腙)⒎醇的加成:RCH=O+CH 3OH −−−−−→←OH HCl 2/)(无水RCH< −−−−→←OH OH CH 23/RCH< 生成半缩醛(酮)及缩醛(酮),可用于羰基保护⒏炔的加成:RCH=O+ CH ≡CH/Na-NH 3(l)→RCHOH -C ≡CH ⒐Wittig 加成:RCH=O+Ph 3P=CHR’→RCH=CHR’ ⒑Michael 加成:CH 2=CHCH=O+HCN →[CH 2CNCH=CH -O -H]→CH 2CNCH 2CH=O 羰基α-H 引起的反应: ⒈羰醛缩合反应:2RCH 2CH=O −−→−-OH RCH 2CHOH -CHRCH=O −−→−-OH 2RCH 2CH=CRCH=O 接长碳链的重要反应,用途广泛① Claisen-Sehmidt 反应:芳醛和含α-H 的醛缩合-CH=O+CH 3CH=O/OH -→ -CH=CHCH=O ② Perkin 反应:芳醛和酸酐缩合-CH=O+(CH 3CO)2O/AcONa → -CH=CHCOOH ③ Tollen’s 反应,可以制取一个有趣的化合物 3H 2C=O+CH 3CH=O →⒉碘仿反应:RCOCH 3+I 2-NaOH →[RCOCI 3]→RCOOH+CHI 3凡含有RCO -结构,或经氧化后可生成此结构的化合物均可发生此反应,它既可用于该结构的鉴定,也可在合成过程中作切断碳链用. 醛酮的氧化还原反应:⒈氧化反应:①银镜反应:RCH=O+2[Ag(NH 3)2]++2OH -→2Ag ↓+RCOO -NH 4++3NH 3+HOHTollen 也称反应,适用于醛,但α-羟基酮有时也给出正反应,类似的反应还有与新制氢氧化铜的反应。
