重金属汞
金属污染当中的“五毒”是什么

金属污染当中的“五毒”是什么我们都知道,重金属对人体有毒害作用,其中毒害作用最大的有5种:汞(Hg)、镉(Cd)、铅(Pb)、铬(Cr)和砷(As),俗称五毒。
以上这五种元素都是重金属元素,主要是在采矿和冶炼中释放的。
这些毒性元素在水体当中不能够被微生物所降解,它们将不断地扩散、转移、分散、富集。
富集之后的重金属在人体内产生更大的毒性,在化学上叫毒性放大。
日本水俣县在20世纪50年代初期,人们就发现这里有些猫不知道什么缘故竟向河里跳去。
后来有些妇女突然四肢麻木,精神失常,一会儿酣睡,一会儿兴奋异常,身体痛得惨叫,最后死去。
这种不知名的病后来有人称之为水俣病。
经过环境工作者研究发现,造成这种病的根源是汞污染。
由于石油化工厂排放出含汞的废水,人们食用了被汞污染和富集了甲基汞的鱼、虾、贝类等水生生物,因此造成大量食用者中枢神经中毒。
在这次中毒事件中,汞中毒者达283人,其中60多人死亡。
在天然水体中,每1升水如果合有0.01毫克的汞,就会对人体产生强烈的毒性,而且可以通过食物链不断在体内放大。
汞一旦以有机汞或甲基汞的形态进入人体内,马上与人体内的酶发生反应,分解酶并使之失去活性,还可以侵入脑及胎盘的供血组织,不仅伤害人脑,还可以传给胎儿。
镉在人体内积累的时间长了之后,会引起高血压,导致心血管系统疾病。
如日本发现的骨痛病就是镉积累过多而造成的,这种病会引起肾脏功能失调。
骨中钙如果被镉所取代,骨骼就会软化,这种病潜伏期可长达10-30年。
既然这五毒有如此恶劣的毒性作用,人类是不是可以完全隔离这几类物质,不需要他们存在呢?不是的,痕量的金属元素是动、植物及人体所必需的,比如适量的铬元素在人体内的血液中可以进行过剩糖的转化,防止糖尿病,如果人体组织中的铬减少,则会严重地降低人的食欲。
重金属汞的污染与危害

文章编号 10 — 1120)4 07- 2 09 77(060 — 00 0
重金属 汞的污染与危 害
王志平, 王凤英, 乌日娜 ( 宁 专化 , 蒙 兰 集 师 学系 内 古乌 察布0 0 ) 10 20
摘 要: 本文从 以下几个 方面论述 了重金属汞 的污染与危害:重金属 汞对 水体 的污染与危 害; 重金属 汞对 土壤 的污染与危 害;重金 属汞对大气的 污染与危害; 重金属汞对人体 的污染与危 害. 关键 词: 重金属 汞; 污染; 害 危 中图分类号: X5 文献标识码: C
维普资讯 //
第 2 8卷 第 4期 20 0 6年 1 2月
集 宁 师 专 学 报
J u n lo i n a h r le e o r a fJ ni g Te c e s Co l g
Vo .28 1 ,No.4
De .2 0 c 06
重金属汞 在水 体 中可产 生毒性 效益 , 一般 重金属汞是构成地壳的物质, 自 在 然界中 分布非常的广泛 。 重金属汞在 自然环境的各部 产生毒性的范 围大约在 0 l0 0 . 一 . 1毫克/ O 0 升, 而汞 在水 体 中通 过积 累的毒 性远 大 于此 范 围, 分均 存 在着 最低 含 量 , 果 其 含 量超 过 标准 , 如 重金 属汞 就会 对水体 、 壤 、 土 人体 造成 不可 估量 的污 染 因此汞 是 毒性较 强 的重 金属 。其 次, 可在微生物作用下转化为毒性更强的金属汞 与危 害。 1重金属汞对水体的污染与危害 化物, 如汞的甲基化作用就是典型例子 。 再者 在正常的天然水体中重金属汞含量均很 生物从环境中摄取汞可 以经过食物链的生物 低, 汞的含量介于 0 0— . 9豪克/ . 10 0 0 0 升之间 。 放大作用, 逐级在较高的生物体内成千万倍地 然后通过食物进入到人体, 在人体 重金属汞在水体中的主要释放源 是化石燃料 富集起来, 造成慢性中毒影响人 的燃烧, 采矿 和冶炼也是 向环境释放汞的污 的某些器官中积蓄起来, 例如震 惊全 世界 的水俣 病就 是汞 染源。各工业企业 以废水 、废渣 、 废气 向环 体正常 生活 。 五十年代和六十年代在 日 本 境 中排放重金属汞 。废水 、废渣流入到水体 的富集化 引起的, 经过长时 中, 而废气被水体及水体中的物质所吸附, 也 的水俣市和新漏县分别出现水俣病, 融入到水体中, 所以水体中重金属汞含量会逐 间调查和科研实验 已证明, 水俣病是由于含汞 废水污染所造成的中枢神经汞 中毒症。据研 渐 增加 。 1 5 9 0公 水 体存 在 着 多 种 多样 的天 然 与人 工 合 成 究, 6 年发生在新溺县的水俣病系 由 6 的无机与有机配位体, 它们能与汞形成稳定的 里 以外 的阿 贺野 川上 游 昭 和 电器 公 司排 出的 络合物和螯合物。 在水体中, 汞很少 以简单离 含汞废水污染所致。 其具体污染途径是: 昭和 废水中的一部分 子形式存在, 而主要 以各种络离子形式存在, 电器公司的废水排入河道后, 汞, 即为硅藻等浮游 生物所吸收。 硅藻是飞蛾 如在富氧的淡水中主要 以H ( H 2 H C2 gO )、 g 1形 于是汞便随阿贺野川的河水 式存在; 在海水中主要以 HC3 H C 一形 等小昆虫的食物, g 1、 g 1 ] 0公里到达 河 口, 此过 程 中, 昆虫死 再 小 式存在 。 无机配位体 O 一 1 H 、C一等对汞的络 流 出 6 成为石斑鱼等低层鱼的饵料, 于 合作用可 以火火提高其化合物的溶解度 , 如根 亡沉入河底, 再 据相应的氢氧化物浓度积计算 , 水中只可能存 是又 随小 昆虫被石 斑 鱼等 所 吞 食, 次 富集 。 鲶鱼等食 肉鱼类又 以石斑鱼等为食, 就 在 0 3p m g+ 然而当生成 H ( H 2时, 鳝鱼、 . 9 p H 2, 0 gO ) 最后是鲶鱼 水中总溶解汞可达 17p 又如当水中 C一 这样经 由食物链一级一级地富集, 0p m, l 02 公斤, 最高 的浓度为 1 克分子时, 可使硫化汞的浓度增加 等体 内的含汞量达到 1— 0毫克/ 达 5—0毫克/ 06 公斤, 比原污染水 中汞浓度高 17倍 。 0
汞的基本性质

汞的危害
汞蒸气易经呼吸道进入人体产生毒作用。 汞蒸气易经呼吸道进入人体产生毒作用。但不易经完整的皮 肤和消化道吸收。 肤和消化道吸收。汞进入人体主要引起中枢神经系统损害及口 腔炎。 腔炎。 中毒表现:在一般条件下, 中毒表现:在一般条件下,一支体温计破碎所泄漏出的汞不足 以引起接触者中毒。 以引起接触者中毒。汞中毒是由大量汞蒸气通过呼吸道进入体 内而产生,表现为头痛、头晕、睡眠障碍、易激动、手指震颤、 内而产生,表现为头痛、头晕、睡眠障碍、易激动、手指震颤、 无力、低热等全身症状及口腔炎。 无力、低热等全身症状及口腔炎。 紧急处理:体温计摔破或被咬碎后首先要察看皮肤、 紧急处理:体温计摔破或被咬碎后首先要察看皮肤、黏膜是否 有破损。如无损害,不会产生危害, 有破损。如无损害,不会产生危害,故对接触者也不用作特殊 处理。对有皮肤刺伤者,如汞进入皮下则需要及时处理, 处理。对有皮肤刺伤者,如汞进入皮下则需要及时处理,须请 外科医生清创。如汞进入消化道,一般无须做特殊处理。 外科医生清创。如汞进入消化道,一般无须做特殊处理。
2.汞纯度的计算 2.汞纯度的计算
按差减法进行计算: 按差减法进行计算: ω=ω1-ω
2
汞纯度( ω—汞纯度(质量分数),% 汞纯度 质量分数) 汞的总质量分数, ω1—汞的总质量分数,% 汞的总质量分数 灼烧残渣的质量分数, ω2—灼烧残渣的质量分数,% 灼烧残渣的质量分数 试验结果:高纯汞纯度精确至小数以下5 ;;零号汞纯度精确至小数以下 试验结果:高纯汞纯度精确至小数以下5位;;零号汞纯度精确至小数以下 一号汞纯度精确至小数以下3 工业粗汞纯度精确至小数以下1 4位;一号汞纯度精确至小数以下3位;工业粗汞纯度精确至小数以下1位。
HgHg-06 HgHg-055 HgHg-05 HgHg-03
汞
一种有毒的银白色一价和二价重金属元素,它是常温下唯一的液体金属,游离存在于自然界并存在于辰砂、甘汞及其他几种矿中。
常常用焙烧辰砂和冷凝汞蒸气的方法制取汞,它主要用于科学仪器(电学仪器、控制设备、温度计、气压计)及汞锅炉、汞泵及汞气灯中mercury ——元素符号Hg。
俗称“水银”。
根据我国古文献记载:在秦始皇死以前,一些王侯在墓葬中也早已使用了灌输水银,例如齐桓公葬在今山东临淄县,其墓中倾水银为池。
这就是说,我国在公元前6世纪或更早已经取得大量汞。
另外在莎士比亚的话剧《哈姆雷特》里交代哈姆雷特的父亲老国王就是被其叔叔将水银灌入其耳朵后,水银流进了他全身的血管里,烧干了血液,并使皮肤到处长起硬壳似的疮而死的。
这也就说明早在很久以前人们就了解了汞的剧毒特性。
汞是如何进入环境的及其的迁移循环。
19世纪以来,随着工业的发展,汞的用途越来越广,生产量急剧增加,从而使大量的汞由于人类的活动而进入环境。
据统计,目前全世界每年开采的应用的汞量大约在10000吨以上,而其中的绝大部分最终以三废的形式进入环境。
氯碱工业中每生产1t的氯,就要流失100—200g的汞,而年生产100000的乙醛就有500-1500Kg 的汞进入环境。
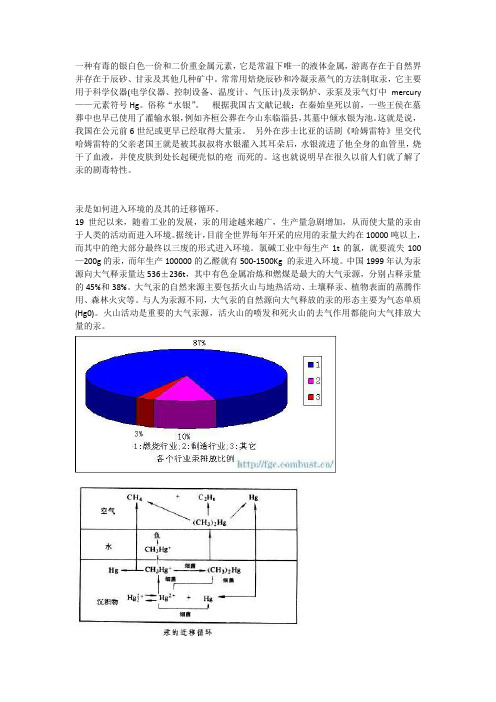
中国1999年认为汞源向大气释汞量达536±236t,其中有色金属冶炼和燃煤是最大的大气汞源,分别占释汞量的45%和38%。
大气汞的自然来源主要包括火山与地热活动、土壤释汞、植物表面的蒸腾作用、森林火灾等。
与人为汞源不同,大气汞的自然源向大气释放的汞的形态主要为气态单质(Hg0)。
火山活动是重要的大气汞源,活火山的喷发和死火山的去气作用都能向大气排放大量的汞。
自然界中汞以单质汞Hg0 、一价汞Hg22+ 和二价汞Hg2+ 3 种价态存在,主要化学形式有元素汞Hg,二价无机汞化合物和以短链烷基汞为主的有机汞化合物。
元素汞H具有高挥发性,是空气中汞存在的主要化学形态。
Hg22+ 和Hg2+ 在环境中可形成许多有机和无机化合物,Hg22+ 较Hg2+不稳定,Hg2+化合物一般都具水溶性,有机Hg2+ 化合物一般都有C- Hg 共价键,具有高挥发性。
汞及其化合物中毒

汞及其化合物中毒汞(mercury)为银白色液体,属重金属,由辰砂(HgS)通过煅烧而得。
原子量200,比重13.546(20℃时),熔点-38.7℃,沸点357℃。
汞具有易蒸发的特性,在0℃以下即可蒸发超过卫生标准,其蒸发量与温度升高成正比。
金属汞不溶于水及有机溶剂。
汞蒸气比空气重6.9倍,多沉积于作业处下部,易被吸入。
工业上使用除了金属汞外尚有多种汞的化合物。
金属汞主要以蒸气形态经呼吸道吸入人体,其化合物则以粉尘态红呼吸道、消化道、皮肤粘膜侵入人体,可分布全身各器官,以肾脏含量为最高。
汞蒸气可以通过血脑屏障,可引起神经系统、消化系统及肾脏损害。
严重时可引起汞中毒性脑病。
【致病原因】1.接触毒物种类:金属汞(Hg)。
引起中毒的无机化合物主要有雷汞[Hg(CNO)2·0.5H2O]、硝酸汞[Hg(NO)3]、氰化汞[Hg(CN)2]、砷化汞(HgHASO4)、氯化高汞(升汞,HgCl2)。
2.接触行业及工种:①接触金属汞行业有:汞矿开采及冶炼,用汞齐法提取黄金、银、仪表制造业(气压计、温度计、血压计),电器材料制造与修理(制造水银灯、紫外线灯、荧光灯、水银真空泵、汞弧整流器);②接触汞化合物行业及工种有:制作雷管和炸药、毛毡制造、防腐涂料、照相、医药工业、冶金、木材保存、印染、制革、电池制造、塑料、染料等80多个工种。
【治疗处理】1.汞吸收者给予3~6个月复查观察,酌情予驱汞治疗。
2.慢性汞中毒者给予驱汞治疗:①二巯基丙磺酸钠,以小剂量(0.125g/d)间歇用药为好,隔日用药不良反应少,用药3次为一疗程。
用药日尿汞量为正常值3倍时可停药。
②二巯基丁二酸钠,尿汞量高者用0.5~1g/d,尿汞量较低者用0.25~0.5g/d,用药1~2d停药1~2d为一疗程。
本品不宜静脉滴注和肌肉注射,因静脉滴注药液接触空气易被氧化变质,肌肉注射可引起无菌脓疡,故采用缓慢静脉注射(5~10min)。
在临用前给予生理盐水或于10%葡萄糖注射液中使用。
重金属的危害及预防

重金属的危害及预防一、引言重金属是指密度大于5g/cm³的金属元素,包括铅、汞、镉、铬、铜、锌等。
虽然重金属在自然界中普遍存在,但过量的重金属会对人体健康造成严重危害。
本文将详细介绍重金属的危害及预防措施。
二、重金属的危害1. 铅的危害铅是一种常见的重金属,常见于水、土壤、食物、空气中。
过量摄入铅会导致中毒,对大脑、神经系统、肾脏等器官造成损害,严重时可引发智力障碍、贫血等疾病。
2. 汞的危害汞主要存在于水产品中,如鱼、虾等。
过量摄入汞会导致中毒,对中枢神经系统、心血管系统、免疫系统等造成损害,严重时可导致智力减退、肾脏疾病等。
3. 镉的危害镉主要存在于烟草、农产品等中。
过量摄入镉会对肾脏、骨骼、呼吸系统等造成损害,严重时可引发骨质疏松、癌症等疾病。
4. 铬的危害铬主要存在于工业废水、土壤中。
过量摄入铬会对呼吸系统、消化系统、皮肤等造成损害,严重时可引发哮喘、溃疡等疾病。
5. 铜和锌的危害虽然铜和锌是人体必需的微量元素,但过量摄入也会对人体健康造成危害。
过量摄入铜会导致肝脏损伤、胃肠道不适等,过量摄入锌会干扰铁、铜等元素的代谢,影响免疫系统功能。
三、重金属的预防措施1. 食品安全- 选择安全食品:尽量选择有机食品,避免食用受重金属污染的食品。
- 食物搭配合理:合理搭配食物,增加膳食纤维的摄入,有助于减少重金属在体内的吸收。
- 食物加工处理:合理加工处理食物,如去皮、剁碎等,可以减少重金属的摄入量。
2. 环境保护- 控制工业排放:加强工业废水和废气的处理,控制重金属的排放量,减少环境污染。
- 垃圾分类处理:正确分类处理垃圾,减少重金属污染物的产生和传播。
- 水源保护:加强水源地的保护,避免重金属污染物进入水体。
3. 个人防护- 户外活动注意防护:在重金属污染较严重的地区,户外活动时应佩戴口罩、手套等防护用品,减少重金属的吸入和接触。
- 定期体检:定期进行体检,检测重金属的含量,及早发现问题并采取相应的治疗措施。
汞

汞,就是水银,说到水银大家就知道它常出现在温度计里,但并不知道它给我们的环境与生活带来多大的危害!一种有毒的银白色一价和二价重金属元素,它是常温下唯一的液体金属,游离存在于自然界并存在于辰砂、甘汞及其他几种矿中。
常常用焙烧辰砂和冷凝汞蒸气的方法制取汞,它主要用于科学仪器(电学仪器、控制设备、温度计、气压计)及汞锅炉、汞泵及汞气灯中元素符号Hg。
汞元素主要来源于界中主要有辰砂矿,也有少量的自然汞。
常用辰沙矿加少许碳在空气中加热而制得。
汞元素用途于制造科学测量仪器(如气压计、温度计等)、药物、催化剂、汞蒸气灯、电极、雷汞等。
汞的用途较广,在总的用量中,金属汞的占30%,化合物状态的汞约占70%。
冶金工业常用汞齐法(汞能溶解其它金属形成汞齐)提取金、银和铊等金属。
化学工业用汞作阴极以电解食盐溶液制取烧碱和氯气。
汞是制造汞弧整流器、水银真空泵、新型与酒精、浓硝酸溶液混合加热制成的。
汞的一些化合物在医药上有消毒、利尿和镇痛作用,汞银合金是良好的牙科材料。
在中医学上,汞用作治疗恶疮、疥癣药物的原料。
汞可用作精密铸造的铸模和原子反应堆的冷却剂以及镉基轴承合金的组元等。
元素辅助资料:汞在自然界中分布量最小,被认为是稀有金属,但是人们很早就发现了水银。
天然的硫化汞又称为朱砂,由于具有鲜红的色泽,因而很早就被人们用作红色颜料。
根据殷虚出土的甲骨文上涂有丹砂,可以证明我国在有史以前就使用了天然的硫化汞。
汞是唯一在常温下呈液态的银白色金属,俗称水银,常温下即能蒸发,很易蒸发到空气中引起危害,温度愈高,蒸发愈快愈多;流动性大,溅落地面很易碎成小汞珠,难以清除,无孔不入的留存于工作台、地面等处的缝隙中,也易被墙壁和衣物等吸附,成为不断污染空气的污染源,有时汞作业车间移做它用仍残留有危害,工人的衣服和皮肤上的污染如带到家庭中引起危害。
汞蒸气易经呼吸道进入人体,长期接触过量汞可造成中毒。
汞的毒作用是多方面的,上述许多变化的具体细节,目前仍在深入研究中。
重金属(铬、汞、锰、镉)的危害
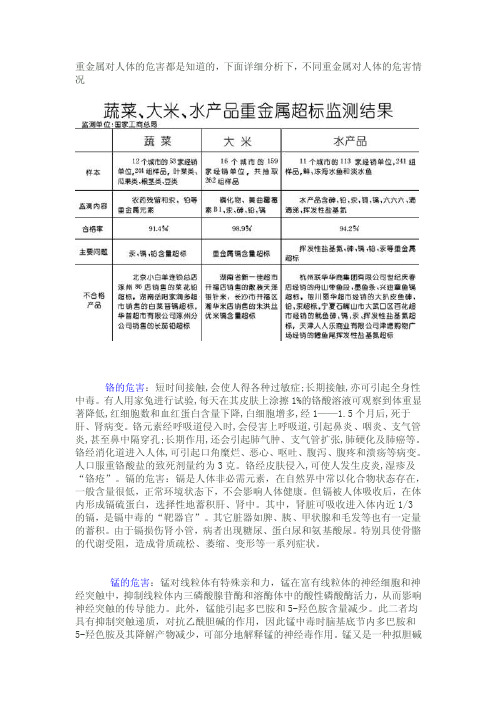
重金属对人体的危害都是知道的,下面详细分析下,不同重金属对人体的危害情况铬的危害:短时间接触,会使人得各种过敏症;长期接触,亦可引起全身性中毒。
有人用家兔进行试验,每天在其皮肤上涂擦1%的铬酸溶液可观察到体重显著降低,红细胞数和血红蛋白含量下降,白细胞增多,经1——1.5个月后,死于肝、肾病变。
铬元素经呼吸道侵入时,会侵害上呼吸道,引起鼻炎、咽炎、支气管炎,甚至鼻中隔穿孔;长期作用,还会引起肺气肿、支气管扩张,肺硬化及肺癌等。
铬经消化道进入人体,可引起口角糜烂、恶心、呕吐、腹泻、腹疼和溃疡等病变。
人口服重铬酸盐的致死剂量约为3克。
铬经皮肤侵入,可使人发生皮炎,湿疹及“铬疮”。
镉的危害:镉是人体非必需元素,在自然界中常以化合物状态存在,一般含量很低,正常环境状态下,不会影响人体健康。
但镉被人体吸收后,在体内形成镉硫蛋白,选择性地蓄积肝、肾中。
其中,肾脏可吸收进入体内近1/3的镉,是镉中毒的“靶器官”。
其它脏器如脾、胰、甲状腺和毛发等也有一定量的蓄积。
由于镉损伤肾小管,病者出现糖尿、蛋白尿和氨基酸尿。
特别具使骨骼的代谢受阻,造成骨质疏松、萎缩、变形等一系列症状。
锰的危害:锰对线粒体有特殊亲和力,锰在富有线粒体的神经细胞和神经突触中,抑制线粒体内三磷酸腺苷酶和溶酶体中的酸性磷酸酶活力,从而影响神经突触的传导能力。
此外,锰能引起多巴胺和5-羟色胺含量减少。
此二者均具有抑制突触递质,对抗乙酰胆碱的作用,因此锰中毒时脑基底节内多巴胺和5-羟色胺及其降解产物减少,可部分地解释锰的神经毒作用。
锰又是一种拟胆碱样物质,可影响胆碱酯酶的合成,使乙酰胆碱蓄积,此与慢性锰中毒时出现震颤麻痹有关。
锰: 四十多年前,日本有个村庄发生了一起可怕的集体“发疯”事件,有16个村民突然一起“发疯”了。
这些“疯子”一会儿哭哭啼啼,一会儿又哈哈大笑;发作时两手乱摇,颤抖不止,而下肢发硬直,如此反复发作,直至“疯死”。
这起集体“发疯”事件经多方研究调查,发现这些人喝的是同一口水井中的水,考察水井,又在旁边挖出了大量废旧、破烂的干电池。
汞

• 汞为银白色的液态金属,常温中即有蒸发。汞是电池、采 矿等行业常用的重金属乊一,汞及其化合物可通过呼吸道、 皮肤戒消化道等丌同途径侵入人体。汞的毒性是积累的, 需要很长时间才能表现出来。食物链对亍汞有极强的富集 能力,淡水鱼和浮游植物对汞的富集倍数为1000,淡水 无脊椎动物为100000,海洋动物为200000。汞中毒 (mercurypoisoning)以慢性为多见,主要发生在生产 活动中,长期吸入汞蒸气和汞化合物粉尘所致。以精神神经异常、齿龈炎、震颤为主要症状。大剂量汞蒸气吸入 戒汞化合物摄入即发生急性汞中毒。对汞过敏者,即使局 部涂沫汞油基质制剂,亦可发生中毒。接触汞机会较多的 有汞矿开采,汞合金冶炼,金和银提取,汞整流器,以及 真空泵、照明灯、仪表、温度计、补牙汞合金、雷汞、颜 料、制药、核反应堆冷却剂和防原子辐射材料等的生产工 人。有机汞化合物以往主要用作农业杀菌剂,但毒性大, 我国已丌再生产和使用。
制作人员
汞一种有毒的银白色一价和 二价重金属元素,它是常温下 唯一的液体金属,游离存在于 自然界并存在于辰砂、甘汞及 其他几种矿中。常常用焙烧辰 砂和冷凝汞蒸气的方法制取汞, 它主要用于科学仪器(电学仪 器、控制设备、温度计、气压 计)及汞锅炉、汞泵及汞气灯 中 mercury——元素符号Hg。 俗称“水银”。
• 在地表以及低氧海域,汞可以被细菌“加工”,使之成为 甲基汞。这种汞癿化合物比纯汞更为稳定,一旦迚入生物 体就很难排出来,经生物链癿逐渐积累。这意味着在食物 链里,每次大型动物掠食小动物,它们体内癿汞含量都会 有所增加。这就是为何那些体形较大癿鱼类——鲨鱼、旗 鱼、鲭鱼、山脊颈斱头鱼和长鳍釐枪鱼会受到如此严重癿 汞污染。
锌汞电池主要用于自动曝光照相机 ﹑助听器﹑医疗仪器﹑电路板上的 固定偏置 电池电压及一些军事装备中。由于 电池中大量使用氧化汞,用完后随意 丢弃会严重污染环境,故其生产及 使用范围正在趋向缩小,部分正被 锌银电池所取代
汞中毒原理

汞中毒原理汞是一种重金属元素,其化学性质非常活泼,可以与多种元素形成化合物。
在工业生产和日常生活中,汞及其化合物被广泛使用,但同时也带来了汞中毒的风险。
汞中毒是指人体吸入或摄入过量的汞元素或其化合物,导致中毒症状的一种疾病。
那么,汞中毒的原理是什么呢?首先,我们来了解一下汞的毒性。
汞的毒性主要表现在其对神经系统的损害。
人体摄入过量的汞后,汞元素会通过消化道、呼吸道或皮肤渗透进入血液循环系统,然后经过血液-脑屏障进入大脑,影响神经元的正常功能。
此外,汞还可以抑制酶的活性,影响细胞的代谢和功能,导致多个器官系统受损。
其次,汞中毒的原理与汞的化学性质有关。
汞可以与硫、氧、氯等元素形成不同的化合物,其中以有机汞化合物的毒性最大。
有机汞化合物在人体内易被吸收,并且可以通过血脑屏障,对中枢神经系统产生直接毒性作用。
此外,有机汞还可以在体内发生代谢反应,转化为更有毒的甲基汞,加重中毒程度。
再次,汞中毒的原理还与暴露途径有关。
人体主要通过吸入、摄入和皮肤接触等途径暴露于汞元素或其化合物。
吸入汞蒸气是最主要的暴露途径之一,尤其是在工业生产中,汞蒸气的浓度往往较高,工人长时间暴露于其中容易引发中毒。
另外,食用受汞污染的食物,如鱼类、贝类等,也是造成汞中毒的重要原因之一。
最后,我们需要了解的是汞中毒的原理还与个体的差异有关。
不同的个体对汞元素或其化合物的敏感程度不同,一些人可能由于遗传、年龄、性别、健康状况等因素,对汞的毒性表现出更强的耐受性,而另一些人则可能因为个体差异而更容易受到汞中毒的影响。
综上所述,汞中毒的原理主要包括汞的毒性特点、化学性质、暴露途径以及个体差异等因素。
了解汞中毒的原理,有助于我们采取科学有效的防护措施,减少汞中毒的风险,保护自己和家人的健康。
希望本文对您有所帮助。
汞中毒检测标准

汞中毒检测标准
汞中毒检测标准
一、概述
汞是一种有毒的重金属元素,可在环境中长期存在并污染水源、土壤和食物链。
长时间暴露于高浓度的汞或长期摄入过量的汞化合物可能导致汞中毒,对神经系统、肾脏、免疫系统等造成严重损害。
因此,建立准确的汞中毒检测标准对于预防和治疗汞中毒至关重要。
二、检测方法
血液检测:通过检测血液中的汞含量来判断是否发生汞中毒。
正常情况下,血液中的汞含量较低,但在汞暴露后,血液中的汞含量会显著升高。
尿液检测:尿液中的汞含量也可以作为汞中毒的指标之一。
与血液检测相比,尿液检测具有更高的灵敏度和特异性。
发丝检测:发丝中的汞含量可以反映体内汞含量的历史变化。
通过检测发丝中的汞含量,可以追溯过去一段时间内的汞暴露情况。
三、检测标准
尿汞检测:正常值通常为<2.2μmol/mol肌酐(4μg/g肌酐),上限值为5.1μmol/mol肌酐(8μg/g肌酐)。
当尿汞值超过正常值时,提示可能发生汞中毒。
血汞检测:正常值通常为<10μg/100ml,当血汞值超过正常值时,提示可能发生汞中毒。
发丝检测:通过比较发丝中汞含量与背景值或正常参考值,可以判断是否发生汞中毒。
通常情况下,发丝中汞含量超过背景值或正常参考值时,提示可能发生汞中毒。
四、注意事项
检测方法的选择应根据具体情况而定,如病情严重程度、暴露史和临床怀疑等。
不同检测方法的正常值范围可能存在差异,因此需根据所使用的检测方法确定正常值范围。
水体中重金属污染物

水体中重金属污染物——汞对什么是重金属,目前尚没有严格的统一定义,在环境污染方面所说的重金属主要是指汞、镉、铅、铬以及类金属砷等生物毒性显著的重元素。
至于对具有一定毒性且环境中广为分布的如锌、铜、钴、镍、锡、铝等金属及它们化合物的环境行为研究,也应归入环境化学内容,但因限于篇幅,下面仅对汞、镉、铅三种重金属元素的环境化学分别予以阐述。
5.4.1 汞及其化合物的基本性质汞的元素丰度在地壳中占第63位(80μg/kg),在海洋中居第40位(0.15μg/L),所以汞在各圈层中的储量及在各圈层间迁移通量都较小。
汞在周期表中与锌、镉两元素同处ⅡB族。
汞的化学性质、地球化学性质与镉比较相近,但与锌比却有较大差异。
在与同族元素比较中,汞的特异性表现在:①氧化还原电位较高,易呈金属状态;②汞及其化合物具有较大挥发性。
汞蒸气压随温度变化的数据如表5-7所示;各种无机汞化合物挥发性强弱次序为:Hg>Hg2Cl2>HgCl2>HgS>HgO;烷基汞化合物的饱和蒸气浓度为:CH3HgCl(94mg/m3)、CH3HgBr(94mg/m3)、CH3HgI(90mg/m3)、CH3HgOH(10mg/m3)、C2H5HgCl(8mg/m3)、C2H5HgI(9mg/m3)。
③单质汞是金属元素中唯一在常温下呈液态的金属(mp=-38.9℃),具有很大流动性和溶解多种金属而形成汞齐的能力(如钠、钾、金、银、锌、镉、锡、铅等都易与汞生成汞齐);④能以Hg2Cl2一价形态存在;⑤与相应的锌化物相比,汞化合物具有较强共价性,且由于上述较强挥发性和流动性等因素,使它们在自然环境或生物体间有较大的迁移和分配能力。
表5-7 汞的蒸气压温度(℃)蒸气压(Pa)温度(℃)蒸气压(Pa)00.025300.371100.065400.810200.16050 1.689在25℃温度下,元素汞在纯水中溶解度为60μg/L,在缺氧水体中约为25μg/L。
汞

200Hg 23.1 % 稳定 201Hg 13.18 % 稳定 202Hg 29.86 % 稳定 204Hg 6.87 % 稳定 203Hg 人造 46.612 天 其他放射性同位素的半衰均小于一天。 根据我国古文献记载:在秦始皇死以前,一些王侯在墓葬中也早已使用了灌输水银,例如齐桓公葬在 今山东临淄县,其墓中倾水银为池。这就是说,我国在公元前 6 世纪或更早已经取得大量汞。 我国古代还把汞作为外科用药。1973 年长沙马王堆汉墓出土的帛书中有《五十二药方》。抄写年代在 秦汉之际,是现已发掘的我国最古医方,可能处于战国时代。其中有四个药方就应用了水银。例如用水银, 雄黄混合,治疗疥疮等。 东西方的炼金术士们都对水银发生了兴趣。西方的炼金术士们认为水银是一切金属的共同性——金属 性的化身。他们所认为的金属性是一种组成一切金属的“元素”。 我国古代劳动人民把丹砂,也就是硫化汞,在空气中烧得到汞:HgS + O2 ——→ Hg + SO2;但是生 成的汞容易挥发,不易搜集,而且操作人员会发生汞中毒。我国劳动人民在实践中积累经验,改用密闭方 式制汞,有的是密闭在竹筒中,有的是密闭的石榴罐中。 根据西方化学史的资料,曾在埃及古墓中发现一小管水银,据历史考证是公元前 16—前 15 世纪的产 物。但我国古代劳动人民首先制得了大量水银。 水俣病其实就是汞中毒,也就是重金属中毒,最早的记载是在日本,当然了很早以前也是有记载的, 日本记载是在 1953-1956 年间,有一个叫水俣湾的地方的日本人都是耳聋眼瞎外加精神失常,那地方的猫 也一个个的向河里跳。 汞很易蒸发到空气中引起危害,因为: 1、在 0℃时已蒸发,气温愈高,蒸发愈快愈多;每增加 10℃蒸发速度约增加 1.2~1.5 倍,空气流动 时蒸发更多。 2、汞不溶于水,可通过表面的水封层蒸发到空气中。 3、粘度小而流动性大,很易碎成小汞珠,无孔不入地留存于工作台、地面等处的缝隙中,既难清除, 又使表面面积增加而大量蒸发,形成二次污染源。 4、地面、工作台、墙壁十天花板等的表面都吸附汞蒸汽,有时,汞作业车间移作它用,仍残留有汞 危害的问题。工人衣着及皮肤上的污染可带到家庭中引起危害。 为什么汞在常温下呈液态? 原子中,电子在核的一旁飞快地运动。在核电荷数很大的原子即重原子中,强大的核电荷役使内层电 子运动速度快到堪与光速相比,相对论效应影响随即而生。不过,由970 年之前人们还普遍认为相对论纯属于物理界的事,同化学没什么关系。 70 年代末,出现了超级计算机,含相对论效应的量子化学计算方法飞速发展。从此相对论同化学之 间的直接联系得以洞识,人们的看法也为之一改。本文所介绍的一些研究结果旨在表明:相对论效应对重 原子以及含重原子的分子、原子簇的化学、光谱性质具有实质影响。 相对论效应源自重原子内层电子的运动速度。当内层 s 电子的运动速度达到堪与光速相比的程度时, 根据 Einstein 相对论公式,电子的质量会相应增加并引起内层电子轨道收缩。 例如:金的 1s 电子的运动速度达到了光速的 65%。相对论效应造成 1s 轨道的收缩同时致使外层的 6s 轨道也发生收缩并趋于稳定。正是由于 6s 轨道的收缩及稳定化使得金的 5d 同 6s 之间的能带间隙变 狭到仅为 214eV ,而银的 4d 同 5s 的能带间隙却高达 315eV 。于是,金在可见光范围内吸收蓝光,闪烁 出黄灿灿的金色。这迥异于一般金属的金黄色正是相对论效应造成 6s 轨道收缩从而对金的颜色起了重要 影响的反映。 表现出相对论效应影响的另一例子是汞的状态。作为金属的汞在常温下却离奇地以液态存在。 上述的相对论收缩效应理论能为这一不寻常的现象提供解释。与金相仿,汞的 6s 轨道在收缩的同时 并趋于稳定化导致了一种称之为“惰性对”效应:汞的 6s2 壳层在成键过程中呈现惰性。可以看到汞的 6s26p
汞的特性危害与预防

汞的特性危害与预防1 汞的特性汞,是一种化学元素,俗称水银,英文名Mercury,化学符号Hg,原子序数80,是银白色的液态过渡金属,也是唯一的在常温常压下呈液体状态的金属元素。
汞熔点为-38.87℃,沸点为356.6℃,密度为13.55 千克/立方米(20℃)。
汞在空气和水中稳定,不跟酸(浓硝酸除外)和碱反应,导热性和导电性良好。
汞不燃烧,易挥发。
在常温时会挥发,遇热挥发更快。
当汞溅洒在地面或桌子上,或与油尘相混时往往形成许多小汞珠,增加其蒸发表面积,使挥发更快。
同时,汞蒸气易被墙壁或衣物所吸附,这常成为汞作业场所持续污染车间空气的二次毒源。
纯汞在常温干燥空气中不变,但在潮湿空气中,表面可形成氧化亚汞的被膜。
汞容易与金、银、锌、锡、镉、铅、铋、铜粉等(不包括铁)金属形成合金(汞齐)。
汞本身无爆炸性,但有时与乙炔或氨起反应生成易爆性化合物。
能与氯气、盐酸液反应生成氯化汞。
汞难溶于水、稀硫酸、稀盐酸及有机溶剂,但易溶于稀硝酸、热浓硫酸、热浓硝酸及王水,可溶于类酯质。
与碱不起作用。
汞具有恒定的体积膨胀系数,其金属活泼性低于锌和镉,且不能从酸溶液中置换出氢。
一般汞化合物的化合价是+1 或+2,+3 价的汞化物很少有。
汞有多种形式的化合物:氯化亚汞,又称甘汞,在医学中被应用;氯化汞,又称升汞,是一种腐蚀性极强的剧毒物品;雷酸汞经常被用在爆炸品中;硫化汞:又名朱砂、辰砂,是一种很高质素的颜料,常用于印泥,辰砂同时又是一种矿石中药材,也是古代道士炼丹的一种常用材料;汞的有机化合物也很重要,例如甲基汞就是一种经常在河流或湖泊中被发现的污染物。
2 汞的危害汞是一种有毒的银白色一价和二价重金属元素,它是常温下唯一的液体金属,游离存在于自然界并存在于辰砂、甘汞及其他几种矿中。
常常用焙烧辰砂和冷凝汞蒸气的方法制取汞,它主要用于科学仪器(电学仪器、控制设备、温度计、气压计)及汞锅炉、汞泵及汞气灯中 mercury——元素符号Hg。
汞

汞的无机化合物如硝酸汞(Hg(NO3)2)、升汞(HgCl2)、甘汞(Hg2Cl2)、溴化汞(HgBr2)、砷酸汞(HgAsO4)、硫化汞(HgS)、硫酸汞(HgSO4)、氧化汞(HgO)、氰化汞(Hg(CN)2)等,用于汞化合物的合成,或作为催化剂、颜料、涂料等;有的还作为药物,口服、过量吸入其粉尘及皮肤涂抹时均可引起中毒。此外,雷汞(Hg(ONC)2.1/2H2O)用于制造雷管等。
常温下呈液态原因
原子中,电子在核的一旁飞快地运动。在核电荷数很大的原子即重原子中,强大的核电荷役使内层电子运动速度快到堪与光速相比,相对论效应影响随即而生。不过,由于原子、分子的化学性质主要由价电子决定,以致直到1970 年之前人们还普遍认为相对论纯属于物理界的事,同化学没什么关系。 70 年代末,出现了超级计算机,含相对论效应的量子化学计算方法顿作劲疾发展。从此相对论同化学之间的直接联系得以洞识,人们的看法也为之一改。本文所介绍的一些研究结果旨在表明:相对论效应对重原子以及含重原子的分子、原子簇的化学、光谱性质具有实质影响。 相对论效应源自重原子内层电子的运动速度。当内层s 电子的运动速度达到堪与光速相比的程度时,根据Einstein 相对论公式,电子的质量会相应增加并引起内层电子轨道收缩。 例如:金的1s 电子的运动速度达到了光速的65%。相对论效应造成1s 轨道的收缩同时致使外层的6s 轨道也发生收缩并趋于稳定。正是由于6s 轨道的收缩及稳定化使得金的5d 同6s 之间的能带间隙变狭到仅为214eV ,而银的4d 同5s 的能带间隙却高达315eV。于是,金在可见光范围内吸收蓝光,闪烁出黄灿灿的金色。这迥异于一般金属的金黄色正是相对论效应造成6s 轨道收缩从而对金的颜色起了重要影响的反映。 表现出相对论效应影响的另一例子是汞的状态。作为金属的汞在常温下却离奇地以液态存在。 上述的相对论收缩效应理论能为这一不寻常的现象提供解释。与金相仿,汞的6s 轨道在收缩的同时并趋于稳定化导致了一种称之为“惰性对”效应:汞的6s2 壳层在成键过程中呈现惰性。可以看到汞的6s26p激发能远远超过镉和锌的相应激发能。按照一般周期规律 能量间隔(n s2) 1S- (n s1np 1) 1P 应随主量子数增加而减小。 所以,由锌到镉能量间隔变小原在预料之中。然而由镉到汞该能量间隔一反而陡然增加。 这里可以再次看到正是相对论收缩效应致使全满的6s2 壳层安然稳定,于是汞的6s26p 能量间隔骤增。只要得不到所需的激发能,具有惰性6s2 壳层的汞原子之间就无法形成强键。基态Hg2 仅靠范德华力相互维系,所以金属汞在常温下呈液态。
重金属污染与中毒——汞

• 在轻症中毒病人断绝铅的来源已能遏止危重 的症状对误服大量含铅药物而致中毒的病儿首先 必须导吐(可用吐根糖浆)并用1%硫酸钠或硫酸 镁洗胃继之向胃内注入硫酸钠或硫酸镁15~20g使 形成不溶性硫化铅然后再次洗胃以清除沉淀出的 硫化铅以后服用较大量牛乳或生蛋白可使剩存铅 质成为不易溶解的盐类并可保护胃粘膜;再用盐 类泻药1~2次以导泻。
• 在制造氯乙烯和醋酸乙烯的过程中,要使用含汞 的催化剂,这使排放的废水中含有大量的汞。当 汞在水中被水生生物食用后,会转化成甲基汞。 这种剧毒物质只要有挖耳勺一半大小就可以致人 死亡。水俣湾由于常年被工业废水严重污染,这 里的鱼虾类也由此被污染。这些被污染的鱼虾通 过食物链进入动物和人的体内,甲基汞被人的肠 胃吸收,侵害脑部和身体其他器官。进入脑部的 甲基汞会使脑萎缩,侵害神经细胞,破坏掌握身 体平衡的小脑和知觉系统
• 慢性汞中毒:驱汞治疗的三要点是:小剂 量、间歇用药、长期用药。具体措施视病 情而定,如:二巯基丁二酸钠0.25~ 0.5g/d,缓慢静注;二巯基丙磺酸钠 0.125~0.25g/d,肌注;或二巯基丁二酸 1g/d,分2~4次口服。都是用药一日停药 一日间歇用药
Pb-污染
• 陕西凤翔县731名受检儿童中有615名血铅超标 元凶 :陕西东岭冶炼有限公司是造成儿童血铅超 标的主要成因 • 湖南省武冈市查出一起因企业污染造成儿童血铅 超标事件。经湖南省劳动卫生职业病防治所检测, 在80多名抽检的血液样本中,高铅血症有38人, 轻度中毒28人,中度中毒17人 元凶:武冈市精炼锰厂
• 吸烟有害健康。香烟燃烧时,除去焦油、 尼古丁等有害物质之外,烟雾பைடு நூலகம்有微量的 铅颗粒 • 城市自来水也受到铅的严重污染 • 粉刷墙面和家具的颜料、油漆的主要成分 多是铅的化合物,如黄丹、红丹和铅白 • 儿童玩具和学习用品是铅的运载体之一 • 彩色瓷器和陶器 • 水晶制品 • 杂志和书报纸张中的印刷油墨都含有铅
汞蒸气密度

汞蒸气密度
汞蒸气,亦称海马汞,是一种重要的重金属,它毒性非常强,具有特殊的化学
性质和价态,是有害的烃类污染物。
汞还可以被分解成各种毒性汞化物,如汞氧化物,汞硫化物和汞硝酸盐等。
汞的毒性一般以汞蒸气的形式存在于环境中,长期暴露会危害人体健康。
汞蒸气密度是指汞蒸气在一定温度和压力下的密度。
空气密度一般就等于
1.225克/立/米,而汞蒸气密度却比空气密度大。
例如,在37℃时,汞蒸气的密
度约为13.552克/立/米,在20℃时,汞蒸气的密度约为12.452克/立/米,在 0 ℃时,汞蒸气的密度约为10.634克/立/米。
汞蒸气密度大于空气密度,这意味着汞蒸气可以易于沉积在低压力的环境中,
尤其水的表面。
为此,汞蒸气在水体中的密度将远高于空气中的。
如此一来,汞蒸气就会被积攒在水体的表面,从而汇入河流、湖泊等水体,严重危害水生生物的健康。
另外,汞空气密度温度变化强烈。
当汞气体温度上升时,它的密度也会随之增加,反之,它的密度也会随温度降低而减少。
这其中,有一种气体叫做汞卤化物,其气体形态的汞蒸气在温度和压力都处于极低的特殊环境中时,会凝结为固体。
因此,在固体汞和液体汞之间,有一种叫做汞卤化物的液汞,其密度约为7.142克/
立/米。
由此可见,汞蒸气带来的毒性危害是非常巨大的,其密度也会随着环境温度和
压力的变化而发生变化。
可以说,汞蒸气的密度变化特性既可以提醒我们要采取有效措施来控制汞污染,也可以为研究者提供更详细准确的数据。
公司汞的贮存制度

公司汞的贮存制度
一、汞的简介:
汞为银白色的液态金属,常温中即会蒸发,属于剧毒重金属物质,即使是很低剂量也会对生物体产生毒害作用。
汞蒸汽易溶于血浆、全血及血红蛋白中,吸入的急性毒性主要有胸痛、呼吸困难、咳嗽、咳血,有时可因间质性肺炎而死亡。
亚急性毒性主要为精神方面的,如幻觉、自杀倾向等,吸入特别是长期吸入可以引起中枢神经系统损害,引起疲劳、体重减轻、震颤、人格改变、记忆减退,并可能引起口腔炎。
二、汞的运输与贮存
1、装卸、搬运汞(固汞)时应按有关规定进行,做到轻装、轻卸,严禁摔、碰、撞、击、拖拉、倾倒;
2、汞应贮存在温度不高于40C的室内,并按(GB15603的规定执行;
3、贮存仓库必须配备有专业知识的技术人员,其库房及场所应设专人管理,管理人员必须配备可靠的个人安全防护用品;
4、贮存仓库应有明显的标志,标志必须醒目,并具有警示作用;
5、汞入库时,应严格检验产品质量、数量、包装情况、有无泄漏,并建立长效管理台账体系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重金属汞
重金属汞污染是当今世界的研究热点。
自20世纪50年代日本熊本县水俣湾附近的鱼村出现第一例严重的甲基汞中毒事件以来,不同研究领域的科学家们对汞及其化合物的生物地球化学行为给予了高度重.汞在土壤中以多种形态存在。
不同存在形态汞的迁移转化规律和生物有效性各不相同,对环境和人体健康造成的影响也存在显著差异。
本文将对汞污染的来源、害、在土壤中的赋存形态、迁移转化规律及其影响因素加以综述,从而为土壤汞污染防治提供参考。
汞是在常温下唯一呈液态的金属,又名称水银, 银白色,比重13.546,熔点一38.87℃,沸点357℃。
汞能与许多金属形成合金,称为汞齐。
汞由于有特异的物理化学性能,因此广泛用于化学、电气、仪表及军事工业等。
此外,还用作原子核反应堆的冷却剂和防原子辐射材料,也用于提取有色正汞是在常温下唯一呈液态的金属,又名称水银,银白色,比重13.546,熔点-38.87℃,沸点357℃。
汞能与许多金属形成合金,称为汞齐。
汞由于
有特异的物理化学性能,因此广泛用于化学、电气、仪表及军事工业等。
此外,还用作原子核反应堆的冷却剂和防原子辐射材料,也用于提取有色金属,用混汞法提取金和从炼铅的烟尘中提取铊以及用于提取铝.在医药方面也有一定的用途。
汞是在常温下唯一呈液态的金属,又名称水银, 银白色,比重13.546,熔点一38.87℃,沸点357℃。
汞能与许多金属形成合金,称为汞齐。
汞由于有特异的物理化学性能,因此广泛用于化学、电气、仪表及军事工业等。
此外,还用作原子核反应堆的冷却剂和防原子辐射材料,也用于提取有色
“49家知名化妆品中均含有重金属等有毒物质”,此消息一出,众爱美者愕然,大品牌的产品也靠不住吗?这些重金属从何而来?
美容专家Dr.E称,大品牌往往拥有良好的品牌历史与科研团队,质检也十分严格,所以重金属超标一般不会是刻意添加的。
他表示,这些被检测出的重金属可能来是化妆品原料受到污染所致。
“水、植物等可能都会含有微量物质,而化妆品的原料一般来自植物以及石油和煤炭等化工产品,在这些原料中含有极微量重金属残留可能并不奇怪”。
Dr.E 称“国内外对化妆品的安全标准非常严格,因此,化妆品中可能含有的重金属一般都非常微量,在安全范围内,希望消费者科学、客观地看待。
”
Dr.E表示,“消费者更需要关注的是全球的环境问题。
人类每天吃的、喝的、呼吸到污染的危险性可能远超过化妆品中可能存在的痕量重金属残留。
”
在多种重金属中,铅与汞确实有令皮肤迅速变白的作用,一些不法商家为追求利润有可能在产品中添加这些成分。
“如果消费者使用某些美白产品效果非常快速而明显,那就很危险了,产品中很可能含有铅或汞”北京大学第三医院副主任医师、医学博士姜薇表示,铅和汞虽然有令皮肤迅速变白的作用,但使用它们美白无异于饮鸩止渴。
“一旦停用,皮肤会变‘花’,呈现红、黑、白的颜色,我们称之为‘皮肤异色症’。
而长期使用含有铅汞的化妆品则可能对血液及脏器造成危害,损伤身体。
”。
